Влияние цитофлавина на клинические и вегетативно-психологические проявления гипертонической болезни
Статьи
Опубликовано в журнале:
«Терапевтический архив » № 5, 2016
Л.А. Белова1, В.В. Машин1, О.Ю. Колотик-Каменева2, Н.В. Белова3, Анжело Скудери4, Пьер Луиджи Антигнани5
1 ФГБОУ ВПО «Ульяновский государственный университет» Минздрава России, Ульяновск, Россия;
2 УЗ «Центральная клиническая медико-санитарная часть», Ульяновск, Россия;
3 ФГБНУ «Научный центр неврологии», Москва, Россия;
4 Университетская клиника Santa Luanda, Сорокаба, Бразилия;
5 Сосудистый центр больницы «Nuova Villa Claudia», Рим, Италия
Резюме
Цель исследования. Изучение влияния включения препарата цитофлавин в схему лечения пациентов с различными стадиями гипертонической болезни.
Материалы и методы. Проанализированы результаты лечения 140 пациентов с гипертонической болезнью - ГБ (53 с I стадией, 50 со II стадией и 37 с III стадией артериальной гипертонии). В зависимости от схемы терапии больных разделили на 2 группы: 74 пациента основной группы получали комплексную терапию, состоящую из антигипертензивной терапии и препарата цитофлавин внутривенно капельно однократно по 10 мл в 200 мл 5% раствора глюкозы 10 дней, затем 60 дней по 2 таблетки 2 раза в день, общий курс 70 дней; 66 больных группы сравнения получали только антигипертензивную терапию. Для получения референсных показателей обследовали 30 практически здоровых лиц (группа контроля). Все больные обследованы стандартными клинико-лабораторными методами, проведена оценка жалоб пациентов и их неврологического статуса с помощью соответствующих опросников в динамике - до и после лечения.
Результаты. Установлено, что включение в схему терапии цитофлавина уменьшает выраженность тревожных, депрессивных, диссомнических и когнитивных расстройств, улучшает качество жизни у пациентов с I стадией ГБ и уменьшает выраженность астенических и вегетативных нарушений при всех стадиях заболевания.
Заключение. Выявленная эффективность и безопасность препарата позволяют рекомендовать его включение в схемы комплексной терапии ГБ I-III стадий.
Ключевые слова: гипертоническая болезнь, цитофлавин, астения, качество жизни, депрессия, тревога, нарушение сна.
Effect of cytoflavin on the clinical and autonomic-psychological manifestations of hypertensive disease
L.A. Belova1, V.V. Mashin1, O.YU. Kolotik-Kameneva2, N.V. Belova3, Angelo Scuderi4, Pier Luigi Antignani5
1 Ulyanovsk State University, Ministry of Health of Russia, Ulyanovsk, Russia;
2 Central Clinical Medical Sanitary Unit, Ulyanovsk, Russia;
3 Neurology Research Center, Moscow, Russia;
4 University Hospital Santa Lucinda, Sorocaba, Brasil;
5 Vascular Center, Nuova Villa Claudia, Rome, Italy.
Aim. To evaluate the impact of incorporating cytoflavin in a treatment regimen for patients with different stages of hypertensive disease (HD).
Subjects and methods. The results of treatment were analyzed in 140 patients with HD (53 with Stage I, 50 with Stage II, and 37 with Stage III). According to the treatment regimen, the patients were divided into 2 groups. A study group (n=74) received combination treatment involving antihypertensive therapy and cytoflavin intravenously dropwisely in a single dose of 200 ml of 5% glucose solution for 10 days, then 2 tablets twice daily for 60 days, with a total cycle time being 70 days. A comparison group (n=66) had antihypertensive therapy only. Thirty apparently healthy individuals (a control group) were examined to have reference values. All the patients were examined using conventional clinical and laboratory studies. The patients' complaints and neurological status were assessed using respective questionnaires over time - before and after treatment.
Results. The incorporation of cytoflavin in a treatment regimen was ascertained to reduce the degree of anxiety, depressive, dissomnic, and cognitive disorders, improves quality of life in patients with Stage I HD, and lowers the degree of asthenic and autonomic disorders in all disease stages.
Conclusion. The found efficacy and safety of the drug may recommend its incorporation in combination therapy regimens for Stages I-III HD.
Keywords: hypertensive disease, cytoflavin, asthenia, quality of life, depression, anxiety, sleep disorder.
АГ - артериальная гипертония
АД - артериальное давление
ГБ - гипертоническая болезнь
ГС - группа сравнения
КЖ - качество жизни
ОА - общая астения
ОГ - основная группа
Пак - пониженная активность
ПсА - психическая астения
СМ - снижения мотивации
ФА - физическая астения Гипертоническая болезнь (ГБ) - наиболее распространенное сердечно-сосудистое заболевание среди трудоспособного населения, обусловливающее наибольшие смертность и инвалидность [1, 2]. Становление и прогрессирование ГБ характеризуется ранним и закономерным поражением органов-мишеней, в первую очередь сердца и сосудистой системы головного мозга в виде гипертонической ангиопатии [2-4]. По результатам эпидемиологического исследования распространенности различных форм сосудистой патологии среди лиц трудоспособного возраста 40-59 лет в открытой популяции Ульяновска (2011-2013 гг.), повышенное артериальное давление (АД) явилось причиной развития различных форм цереброваскулярной патологии в 46,7% случаев. При этом 82,2% от всех выявленных случаев составили хронические формы нарушения мозгового кровообращения, что свидетельствует о значительном потенциале для лечения и профилактики прогрессирования цереброваскулярных расстройств в данной возрастной группе [5].
Наиболее значимыми клиническими проявлениями гипертонической ангиопатии являются нейропсихологические, вегетативные и психоэмоциональные расстройства, что ведет к снижению профессиональной и социальной деятельности, а также ухудшению качества жизни (КЖ) больных ГБ и требует обязательной коррекции [6- 10]. С учетом того что основной причиной данных изменений является гипоксия головного мозга с нарушением энергообразования, последующей метаболической дисфункцией нейронов и гипоксическим повреждением лимбико-ретикулярного комплекса, назначение больным ГБ препаратов, обладающих антиоксидантной активностью и нормализующих энергообмен, является патогенетически обоснованным [11]. Один из таких препаратов - цитофлавин (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург), эффективность которого при острых и хронических нарушениях мозгового кровообращения доказана в многоцентровых плацебо-контролируемых исследованиях [12]. Цитофлавин представляет собой композицию янтарной кислоты, рибоксина, рибофлавина и никотинамида. Препарат положительно влияет на процессы энергообразования в клетке, снижая выраженность окислительного стресса, подавляя избыточный выброс возбуждающих нейротрансмиттеров в условиях ишемии [13, 14].
Целью исследования явилось изучение влияния включения препарата цитофлавин в схему лечения пациентов с различными стадиями ГБ.
Материалы и методы
Проведен анализ результатов терапии 140 больных ГБ I-III стадии, получивших лечение в неврологическом отделении ГУЗ «Центральная клиническая медико-санитарная часть» Ульяновска. В проспективное когортное исследование включены 38 (27,1%) мужчин и 102 (72,7%) женщины в возрасте от 47 до 73 лет (средний возраст больных 62,1+10,7 года).
Диагноз, степень и стадия ГБ верифицированы в соответствии с рекомендациями ВНОК от 2013 г. [15]. Длительность артериальной гипертонии (АГ) у всех пациентов составила более 5 лет (7,3+4,8 года). У 53 (37,9%) пациентов выявлена АГ I степени, у 50 (35,71%) пациентов - АГ II и у 37 (26,4%) пациентов - АГ III.
Критериями включения являлись ГБ I, II, III стадии, критериями исключения - психические, эндокринные, гематологические, онкологические, аутоиммунные, инфекционные заболевания; церебральный инсульт в остром или восстановительном периоде до 1 года, органическое заболевание головного мозга, перенесенная черепно-мозговая травма; декомпенсация сердечной недостаточности, вторичная (симптоматическая) АГ, нарушение ритма и проводимости сердца; беременность, лактация, транзиторная ишемическая атака или гипертонический криз на момент включения в исследование; прием антиоксидантных или ноотропных препаратов в течение последних 3 мес.
Все обследуемые с ГБ I-III стадии рандомизированы методом конвертов на 2 группы с учетом стратификации. Основную группу (ОГ) составили 74 пациента (27 с ГБ I стадии, 27 с ГБ II стадии, 20 с ГБ III стадии), которые получали комплексную терапию, включающую антигипертензивные средства и цитофлавин по схеме: внутривенно капельно однократно по 10 мл в разведении на 200 мл 5% раствора глюкозы 10 дней, затем 60 дней по 2 таблетки 2 раза в день, общий курс препарата 70 дней. В группе сравнения (ГС) 66 пациентов (24 с ГБ I стадии, 24 с ГБ II стадии, 18 с ГБ III стадии) получали только антигипертензивную терапию. У всех больных до начала наблюдения имелись целевые уровни АД. Для получения референсных данных обследованы 30 практически здоровых лиц (группа контроля), сопоставимых по полу и возрасту.
Все больные обследованы стандартными клинико-лабораторными и инструментальными методами в динамике: перед началом лечения и через 70 дней (после окончания курса цитофлавина).
Состояние вегетативно-психологического статуса исследовали с помощью шкалы вегетативной субъективной и объективной оценки, монреальской шкалы когнитивной оценки (МОСА), шкалы тревожности Спилбергера-Ханина; шкалы депрессии CES-D (Center for Epidemiological Studies Depression Scale) [16], субъективной шкалы оценки астении MFI-20 (Multidimensional Fatigue Inventory) с исследованием показателей общей астении (ОА), физической астении (ФА), пониженной активности (ПАк), снижения мотивации (СМ), психической астении (ПсА) [17]; анкеты оценки субъективных характеристик качества сна [18, 19].
Оценивали показатели связанного со здоровьем КЖ по опроснику SF-36 из 8 шкал: шкалы физическая активность (PF), ролевое функционирование, обусловленное физическим состоянием (RP), физическая боль (BP), общее восприятие здоровья (GH), физическое благополучие (PCS); шкалы жизненная активность (VT), социальное функционирование (SF), ролевое функционирование, обусловленное эмоциональным состоянием (RE), психическое здоровье (MH) - психическое благополучие (MCS). Показатели каждой шкалы варьируют от 0 до 100 баллов, где 100 баллов соответствует полному здоровью.
Исследование проведено в рамках Государственного задания Минобрнауки России и по разрешению локального этического комитета ГОУ ВПО «Ульяновский государственный университет».
Статистическую обработку данных исследования проводили с помощью программ Statistica 8.0 с вычислением уровня значимости (р). В зависимости от типа распределения использовали непараметрические методы (критерий U Манна-Уитни, критерий Вилкоксона, корреляционный анализ Спирмена), метод сравнения процентов. Результаты представлены в виде медианы с 25-м и 75-м перцентилями. Статистически значимыми считали различия при вероятности ошибки первого рода меньше 5% (p<0,05).
Результаты
При первичном осмотре большинство пациентов ОГ 68 (91,9%) и ГС 63 (95,4%) предъявляли жалобы на головную боль, проявлявшуюся или усиливающуюся преимущественно при работе в наклонном положении, во время или после ночного сна, при кашле и натуживании. Интенсивность ее уменьшалась во второй половине дня, после умеренной физической нагрузки, после приема кофе или кофеинсодержащих напитков. При наблюдении выявлена достоверная положительная динамика: уменьшение количества жалоб в ОГ на 45,6% (с 68 до 31 случая; p<0,0001), в то время как в ГС положительная динамика отмечалась только у пациентов с ГБ I стадии - на 12,5% (с 24 до 21 случая; р<0,001).
Второй по частоте являлась жалоба на головокружение системного и несистемного характера, усиливающееся при перемене положения тела, поворотах головы, работе в наклонном положении, повышении АД. После лечения уменьшение частоты данного признака отмечено только у пациентов, получивших цитофлавин (ОГ), - на 81,1% (с 74 до 14 случаев; p<0,03).
Кроме того, при первичном осмотре все пациенты предъявляли жалобы на раздражительность 69 (93,2%) в ОГ и 61 (92,4%) в ГС, повышенную утомляемость - 72 (97,3%) и 62 (93,9%), снижение концентрации внимания - 61 (82,4%) и 52 (78,8%), нарушение сна - 59 (79,7%) и 55 (83,3%), слезливость - 22 (29,7%) и 17 (25,8%), снижение памяти - (28 37,8%) и 23 (34,8%). В динамике наблюдения выявлено, что среди пациентов, получивших в схеме лечения цитофлавин, частота предъявления жалоб на раздражительность снизилась на 63,7% (с 69 до 25 случаев; р<0,03), а жалобы на повышенную утомляемость, предъявляемые пациентами ОГ с ГБ II-III стадии, уменьшились на 51% (с 47 до 23 случаев; р<0,02). В ГС динамики не наблюдалось.
При объективном осмотре до начала лечения у всех пациентов выявлены симптомы, характерные для церебральной венозной дисциркуляции [18]: отечность лица и век в утренние часы - у 59 (79,7%) пациентов в ОГ и 53 (80,3%) в ГС, ощущение «засыпанности глаз песком» в утренние часы у 64 (86,5%) и 59(89,4%) соответственно, невозможность спать на низкой подушке у 34 (45,9%) и 28(42,4%) соответственно, дискомфорт при ношении поясов и блуз с высоким воротником у 22 (29,7%) и 15 (22,7%) соответственно. В динамике наблюдения у пациентов, получивших цитофлавин, отмечено достоверное уменьшение интенсивности жалоб на пастозность лица - на 57,6% (с 59 до 25 случаев; p<0,02), симптома «песка в глазах» - на 79,7% (с 64 до 13 случаев; p<0,001) и симптома «высокой подушки» - на 67,6% (с 34 до 14 случаев; p<0,05). В ГС подобной динамики не наблюдалось.
Таким образом, отмечена выраженная положительная динамика состояния пациентов, получивших в схеме лечения цитофлавин, что проявлялось в уменьшении частоты жалоб на головную боль (на 45,6%), головокружение (на 81,1%), раздражительность (на 63,7%), пастозность век в утренние часы (на 57,6%), симптом «песка в глазах» (на 67,6%) и симптом «высокой подушки» (на 67,6%). В ГС положительная динамика отмечена только у пациентов с ГБ I стадии при головных болях - уменьшение количества жалоб на 12,5%.
Анализ динамики вегетативных нарушений (периодическое побледнение или покраснение пальцев и кистей рук, повышенная потливость, лабильность пульса и АД, чувство «замирания» сердца, ощущение сердцебиения или затруднения дыхания при волнении или в душном помещении, плохая переносимость холода или жары; кроме того, больные предъявляли жалобы на склонность к запорам, «вздутию» живота в отсутствие органической патологии) выявил положительную тенденцию у всех пациентов на фоне терапии независимо от стадии ГБ, по обеим шкалам, однако у больных, получивших в схеме лечения цитофлавин, она более выражена (табл. 1).
Так, по субъективной шкале оценки у пациентов с I стадией улучшение отмечено на 51,3%, с ГБ II стадии - на 57,6%, с ГБ III стадии - на 53,5%, в то время как в ГС эти показатели составили 19,3, 7,5 и 20,3% соответственно. Сходная картина получена при анализе данных объективной шкалы вегетативного статуса: в ОГ улучшение при ГБ I стадии достигнуто на 62,1%, с ГБ II стадии - на 54,2% и с ГБ III стадии - на 61,2%, в то время как в ГС эти показатели составили 19,8, 16,2 и 11,7% соответственно.
Анализ показателей психоэмоциональной сферы (табл. 2) выявил у всех пациентов с ГБ когнитивные расстройства в виде нарушения оптико-пространственной деятельности, а также памяти, внимания, абстрактного мышления. После лечения достоверная положительная динамика отмечена у пациентов с ГБ I стадии, получивших цитофлавин, - на 14,1% (с 22,4 до 26,1 балла; p<0,03).
Уровень тревоги по шкале Спилбергера у всех больных до начала лечения расценен как средний, после терапии достоверное улучшение выявлено только у пациентов с ГБ I стадии: на 13,8% (снижение с 38,5 до 33,2 балла) по ситуационной и на 13,3% (снижение с 38,2 до 33,1 балла) по личностной тревожности (p<0,05). Пациенты чувствовали себя бодрее, спокойнее, не переживали из-за незначимых событий, отмечали меньшую усталость к концу дня, были менее скованными и напряженными при общении с окружающими. В ГС подобной динамики не выявлено (p>0,05).
При анализе данных по шкале CES-D отмечено наличие признаков легкой депрессии у больных с ГБ I и II стадий в обеих группах с нарастанием до умеренной степени у пациентов с ГБ III стадии. После лечения уменьшение выраженности показателя зафиксировано только у больных ГБ I стадии - на 24,9% (с 19,7 до 14,8 балла; р<0,05). Пациенты отмечали снижение плаксивости, чувства тоски, не испытывали подавленности, недружелюбия окружающих, старались сконцентрироваться на выполнении повседневной работы. В ГС показатели остались на прежнем уровне.
Таблица 1. Динамика показателей вегетативного статуса в зависимости от схемы терапии, баллы
| Показатель |
ОГ |
ГС |
| ГБ I (n=27) |
ГБ II (n=27) |
ГБ III (n=20) |
ГБ I (n=24) |
ГБ II (n=24) |
ГБ III (n=18) |
| Субъективная шкала: |
| до лечения |
26,1 (21; 32) |
32,1 (27; 36) |
34,6 (28; 38) |
25,9 (22; 30) |
29,4 (27; 34) |
35 (30; 36) |
| после лечения |
12,7 (10; 15)* |
13,6 (12; 16)* |
16,1(14; 19)* |
20,9 (15; 24) |
27,2 (23; 31) |
27,9 (23; 31) |
| Объективная шкала: |
| после лечения |
21,4 (20; 24) |
22,5 (20; 24) |
28,4 (23; 32) |
21,7 (19; 23) |
24.0 (22; 25) |
29,1 (24; 31) |
| после лечения |
8,1 (5; 10)* |
10,3 (7; 11)* |
11,0 (7; 12)* |
17,4 (15; 20) |
20.1 (18; 22) |
25,7 (23; 27) |
Примечание. Здесь и в табл. 2, 3: * - p<0,05 - статистически значимые различия при сравнении в динамике.
Таблица 2. Динамика состояния психоэмоциональной сферы пациентов в зависимости от схемы терапии, баллы
| Показатель |
Шкала МОСА |
Шкала Спилбергера |
Шкала CES-D |
Шкала качества сна |
| группа |
ГБ |
СТ |
ЛТ |
| До лечения |
| ОГ |
I |
22,4 (21; 25) |
38,5 (34; 42,5) |
38,2 (37; 43) |
19,7 (14; 21) |
18,9 (16,2; 20,5) |
| II |
22,9 (21; 25) |
40,2 (36; 43) |
40,6 (36; 43) |
21,6 (16; 23) |
18,1 (16; 21) |
| III |
22,6 (21,5; 25) |
40,9 (35; 44) |
41,2 (35; 44) |
26,1 (18,5; 27) |
18,0 (16,2; 21) |
| ГС |
I |
22,3 (20,5; 25) |
37,4 (34; 42) |
38,8 (38; 43) |
19,9 (15; 22,5) |
18,3 (16,1; 20,5) |
| II |
22,8 (21; 24,5) |
40,3 (35; 43) |
40,0 (37; 42) |
21,1 (16; 22) |
18,3 (16,4; 21) |
| III |
22,7 (21; 25) |
39,9 (34; 42) |
40,4 (35 ;42) |
26,6 (18,5; 25,5) |
18,0 (16,5; 21,5) |
| После лечения |
| ОГ |
I |
26,1 (24; 28)* |
33,2 (32; 39)* |
33,1 (32; 39,5)* |
14,8 (12; 19)* |
22,4 (18; 24)* |
| II |
25,5 (22; 26) |
37,4 (34,5; 41) |
36,6 (44; 41) |
18,0 (15; 22) |
19,0 (17,3; 22) |
| III |
25,7 (22; 26) |
38,9 (35; 41,5) |
39,1 (37; 42) |
23,2 (16; 25) |
18,4 (16; 20) |
| ГС |
I |
23,4 (21; 25) |
36,1 (34; 43) |
36,4 (33,5; 43) |
18,9 (15; 21) |
18,2 (15,1; 20,5) |
| II |
23,2 (22; 25,5) |
38,7 (35,5; 42) |
38,2 (33; 44) |
18,6 (14,5; 22) |
18,3 (15; 21) |
| III |
21,9 (20,5; 24) |
39,0 (35; 42) |
39,5 (34; 43) |
26,1 (16; 24) |
18,1 (15; 21) |
Примечание. СТ - ситуативная тревожность; ЛТ - личностная тревожность.
Таблица 3. Динамика показателей астении в зависимости от схемы терапии (по шкале MFI-20, баллы)
| Показатель |
ОГ |
ГС |
| ГБ I |
ГБ II |
ГБ III |
ГБ I |
ГБ II |
ГБ III |
| До лечения |
| общая астения |
12,5 (9; 15) |
13,1 (10; 16) |
13,8 (10; 16) |
12,6 (9; 15) |
13,0 (10; 17) |
13,8 (10; 15) |
| физическая астения |
11,7 (8; 14) |
12,0 (10; 15) |
13,4 (10; 15) |
11,4 (8; 15) |
12,1 (9; 15) |
13,2 (10; 15) |
| пониженная активность |
11,2 (9; 13) |
11,5 (8; 14) |
12,4 (9; 15) |
11,0 (8; 13) |
11,4 (8; 13) |
12,1 (9; 14) |
| снижение мотивации |
9,7 (5; 14) |
10,3 (7; 14) |
10,7 (6; 13) |
10,1 (7; 13) |
10,0 (7; 14) |
10,9 (6; 14) |
| психическая астения |
10,0 (7; 14) |
9,5 (5; 14) |
10,3 (6; 14) |
10,1 (6; 13) |
9,6 (6; 13) |
10,8 (7; 13) |
| общая оценка |
55,1 (52; 59) |
56,4 (50; 59) |
60,6 (54; 63) |
50,2 (47; 54) |
56,1 (53; 58) |
60,8 (54; 63) |
| После лечения: |
| общая астения |
9,1 (6; 12)* |
9,7 (6; 13)* |
10,4 (7; 14)* |
9,5 (6; 12)* |
9,8 (5; 13)* |
11,3 (8; 13)* |
| физическая астения |
9,0 (6; 13)* |
9,3 (6; 12)* |
10,3 (6; 14)* |
9,1 (6; 12)* |
9,4 (5; 13)* |
10,0 (7; 13)* |
| пониженная активность |
6,8 (3; 10)* |
7,1 (5; 9)* |
11,0 (7; 13)* |
7,6 (4; 11)* |
8,1 (4; 12)* |
10,2 (7; 14) |
| снижение мотивации |
6,9 (3; 9)* |
7,2 (4; 10)* |
7,3 (4; 10)* |
7,6 (4; 10)* |
8,3 (5; 12) |
9,0 (6; 12) |
| психическая астения |
5,3 (3; 7)* |
6,5 (3; 8)* |
6,7 (3; 9)* |
8,0 (5; 11)* |
8,4 (4; 11) |
9,1 (6; 12) |
| общая оценка |
37,1 (31; 42)* |
39,8 (34; 42)* |
45,7 (40; 48)* |
41,8 (37; 44)* |
44,0 (40; 47)*# |
49,6 (44; 2)*# |
Примечание.
# - р<0,05 - статистически значимые различия при сравнении между ОГ и ГС.
До начала лечения все пациенты предъявляли жалобы на выраженные нарушения сна: кошмарные сновидения, ощущение неудовлетворенности ночным сном и снижение бодрости по утрам, дневную сонливость. После лечения положительная динамика показателя зафиксирована только у больных ГБ I стадии - на 15,6% (с 18,9 до 22,4 балла; p<0,01). Ранее отмечено, что для ГБ на ранних стадиях заболевания характерно выявление гиперактивности вегетативной нервной системы с признаками астенического синдрома [14]. При анализе данных по шкале MFI-20 (табл. 3) выявлено наличие признаков астении уже на I стадии ГБ в обеих группах с нарастанием до степени выраженных нарушений к III стадии по показателям ОА, ФА, ПАк. Пациенты не ощущали себя здоровыми и активными, испытывали трудности при выполнении своей работы или других дел, постоянно чувствовали себя усталыми, не могли сконцентрироваться на выполняемой работе. При этом показатели СМ, ПсА находились в норме во всех стадиях заболевания. У больных сохранялось желание деятельности, было множество планов.
После лечения у всех пациентов ОГ отмечена статистически значимая положительная динамика всех составляющих со снижением показателей на 32,7% (с 55,1 до 37,1 балла) при ГБ I стадии, на 29,4% (с 56,4 до 39,8 балла) при ГБ II стадии и на 24,6% (с 60,6 до 45,7 балла) при ГБ III стадии (р<0,01). Пациенты становились более активными, организованными, отмечали снижение усталости и повышение фона настроения, концентрации внимания. В ГС положительная динамика оказалась менее выраженной - на 16,7, 21,6 и 18,4% соответственно (р<0,03).
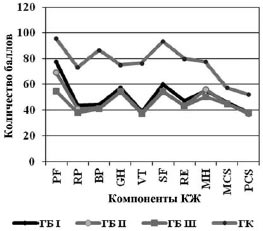
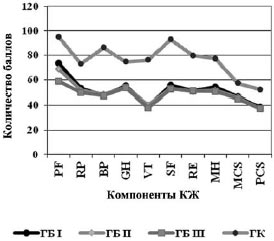
Анализ данных, характеризующих КЖ у пациентов до начала лечения (рис. 1), выявил снижение всех показателей независимо от стадии заболевания сопоставимое в обеих группах (р<0,01).
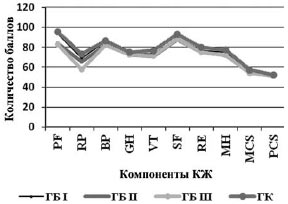
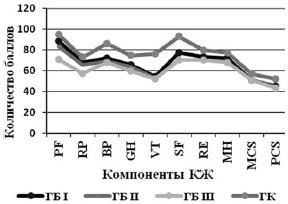
После лечения (рис. 2) показатели КЖ при всех стадиях ГБ у пациентов, получивших цитофлавин, улучшились, в то время как в ГС улучшение выявлено только по показателям эмоционального состояния (RE), психического здоровья (MH), психического (MCS) и физического (PCS) благополучия - при всех стадиях (р<0,01), по показателям общего восприятия здоровья (GH), физического состояния (RP) и активности (PF) - при I и II стадиях ГБ (р<0,04).
Рис. 1. КЖ у больных с ГБ в ОГ (а) и ГС (б).
 |
|
 |
| a |
|
б |
Рис. 2. Динамика показателей КЖ у больных с ГБ в ОГ (а) и ГС (б).
 |
|
 |
| a |
|
б |
При включении цитофлавина в схемы лечения больных ГБ не выявлено нежелательных явлений, лечение было проведено в полном объеме у всех больных.
Обсуждение
Выявлено, что включение цитофлавина в комплексную терапию ГБ курсом 70 дней (однократно, внутривенно, 10 мл в 200 мл 5% раствора глюкозы 10 дней, затем 60 дней по 2 таблетки 2 раза в день) сопровождается достоверным уменьшением частоты жалоб на головную боль (на 45,6%) и головокружение (на 81,1%) при всех стадиях АГ. Данные изменения могут свидетельствовать об эффективности терапии препаратом цитофлавин в отношении церебральной гемодинамики на всех структурно-функциональных уровнях сосудистой системы головного мозга, особенно венозной гемодинамики, что показано в проведенных ранее исследованиях [11, 13, 14]. У всех больных, получивших в схеме лечения цитофлавин, независимо от стадии заболевания, установлено уменьшение частоты и выраженности вегетативных и астенических расстройств, что может служить подтверждением влияния цитофлавина на процессы метаболизма с участием компонентов препарата в цикле трикарбоновых кислот с восстановлением синтеза АТФ и переводом анаэробного механизма окисления в аэробный.
Положительное влияние комплексной терапии с применением препарата цитофлавин на качество сна (улучшение показателя на 15,6%), уровень тревожно-депрессивных (на 24,9%), когнитивных расстройств (на 14,1%) и астении (на 32,7%) на I стадии ГБ свидетельствует о сложности данных процессов и возможности их восстановления с помощью энергокоррекции на ранних стадиях заболевания.
Традиционно одним из критериев эффективности терапии является динамика показателей КЖ. В нашем исследовании у всех больных ГБ, получавших цитофлавин, установлено улучшение показателей КЖ до уровня контрольных значений по всем шкалам.
Таким образом, комплексная терапия с включением цитофлавина курсом 70 дней позволяет предотвратить прогрессирование церебральных расстройств и, следовательно, ускорить выздоровление и сохранить КЖ и социальный статус больных с ГБ.
Заключение
Включение цитофлавина в схему терапии пациентов с ГБ, особенно при I стадии, уменьшает выраженность тревожности (на 13,8% по ситуационной тревожности и 13,3% по личностной тревожности), депрессивных (на 24,9%) и когнитивных (на 14,1%) расстройств, улучшает КЖ и уменьшает астенические (на 32,7%) и вегетативные нарушения при всех стадиях заболевания.
Выявленная эффективность и безопасность препарата позволяют рекомендовать его включение в схемы комплексной терапии ГБ I-III стадии.
Представленные результаты получены в рамках выполнения Ульяновским государственным университетом государственного задания Минобрнауки России.
Конфликт интересов отсутствует.
Литература - Рузов В.И., Гимаев Р.Х., Разин В.А., Лукьяненко О.В., Сапожников А.Н., Шарангин С.А. Структурно-функциональное состояние миокарда и показатели сигнал-усредненной электрокардиограммы у больных гипертонической болезнью. Кардиоваскулярная терапия и профилактика. 2014;4(6): 21-26.
- Silambarasan T, Manivannan J, Priya MK, Suganya N, Chatterjee S, Raja B. Sinapic Acid prevents hypertension and cardiovascular remodeling in pharmacological model of nitric oxide inhibited rats. PLoS One. 2014;9(12):e115682. doi:10.1371/journal.pone.0115682.
- Белова Л.А., Машин В.В., Никитин Ю.М., Белова Н.В., Ниязова Р.М., Рыкер С.А. Дисфункция эндотелия и состояние структурно-функциональных уровней сосудистой системы головного мозга при гипертонической энцефалопатии. Неврологический вестник. 2012;1(44):3-9.
- Zhou M, Mao L, Wang Y, Wang Q, Yang Z, Li S, Li L. Morphologic Changes of Cerebral Veins in Hypertensive Rats: Venous Collagenosis Is Associated with Hypertension. J Stroke Cerebrovasc Dis. 2014;pii:S1052-3057(14)00499-6. doi:10.1016/j.jstrokecerebrovasdis.2014.09.038.
- Белова Л.А., Машин В.В., Сапрыгина Л.В., Кравченко М.А., Гнедовская Е.В., Ощепкова Е.В., Варакин Ю.Я., Суслина З.А. Структура цереброваскулярной патологии в открытой популяции работоспособного населения г. Ульяновска. Анналы клинической и экспериментальной неврологии. 2014;8(4): 4-8.
- Суслина З.А., Фонякин А.В., Гераскина Л.А., Машин В.В., Трунова Е.С., Машин В.В., Глебов М.В. Практическая кардионеврология. М.: ИМА-ПРЕСС; 2010
- Машин В.В., Белова Л.А., Сапрыгина Л.В., Кравченко М.А., Варакин Ю.Я., Гнедовская Е.В., Суслина З.А. Факторы риска развития цереброваскулярных заболеваний по данным скрининга популяции среднего возраста г. Ульяновска. Анналы клинической и экспериментальной неврологии. 2014;8(1): 4-9.
- Belova L, Mashin V, Belova N. Hypertensive Encephalopathy: the Role of Arteriovenous Interrelations in the Formation of Its Clinical-pathogenetic Subtypes. Exp Clin Cardiol. 2014;20(7):892-898.
- Siegler JE, Martin-Schild S. Early Neurological Deterioration (END) after stroke: the END depends on the definition. Int J Stroke Organization. 2011;6:211-212. doi:10.1111/j.1747-4949.2011.00596.x.
- Vellante F, Cornelio M, Acciavatti T, Cinosi E, Marini S, Dezi S, De Risio L, Di Iorio G, Martinotti G, Di Giannantonio M. Treatment of resistant insomnia and major depression. J Gerontol Nurs. 2013:1-8. doi:10.3928/00989134-20131029-06, Clin Ter. 2013;164(5): 429-435. doi: 10.7417/01.2013.1609.
- Белова Л.А., Колотик-Каменева О.Ю., Машин В.В., Сапрыгина Л.В., Машин Е.В. Эффективность энергокорректора цитофлавина при лечении больных гипертонической энцефалопатией. Терапевтический архив. 2014;86(9):65-71.
- Одинак М.М., Скворцова В. И., Вознюк И. А., Румянцева С.А., Стаховская Л.В., Клочева Е.Г., Новикова Л.Б., Янишевский С.Н., Голохвастов С.Ю., Цыган Н.В.. Оценка эффективности цитофлавина у больных в остром периоде ишемического инсульта. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010;110(12):29.
- Белова Л.А., Машин В.В., Колотик-Каменева О.Ю., Прошин А.Н. Влияние терапии Цитофлавином на функцию эндотелия и церебральную гемодинамику у больных гипертонической энцефалопатией. Антибиотики и химиотерапия. 2014;59(7-8):30-36.
- Белова Л.А., Машин В.В., Колотик-Каменева О.Ю., Белова Н.В., Бырина А.В., Евстигнеева А.Ю., Абрамова В.В. Эффективность Цитофлавина у больных гипертонической энцефалопатией с конституциональной венозной недостаточностью. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;8:21-26.
- Рекомендации по лечению артериальной гипертонии. ESH/ ESC 2013. Российский кардиологический журнал. 2014;1(105):7-94.
- Radloff LS. The CES-D Scale: A self-report depression scale for research in the general population. Applied Psychological Measurement. 1977;1(3):385-401. doi: 10.1177/014662167700100306.
- Александровский Ю.А. Психофармакотерапия. М.: Издательский центр «Академия»; 2005.
- Вейн А.М., Левин Я.И. Принципы современной фармакотерапии инсомнии. Журнал неврологии и психиатрии им. С.С. Корсакова. 1998;5:39-42.
- Белова Л.А., Машин В.В. Венозная дисциркуляция при хронических формах цереброваскулярной патологии: [монография]. Ульяновск: УлГУ; 2015.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)