Современные подходы к церебропротекторной терапии недоношенных новорожденных в условиях отделения реанимации и интенсивной терапии
Статьи
Опубликовано в журнале:
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ »» 2011, № 1, С. 26—31
К.м.н., доц. С.О. Рогаткин, акад. РАМН, д.м.н., проф. Н.Н. Володин, д.м.н., проф. М.Г. Дегтярева, к.м.н. О.В. Гребенникова, асп. М.Ш. Маргания, асп. Н.Д. Серова
Цель работы состояла в изучении клинической эффективности цитофлавина (раствор для инфузий) для профилактики и лечения постгипоксических поражений ЦНС у недоношенных новорожденных. Работа выполнена в рамках многоцентрового исследования, фрагмент которого представлен в статье. Под наблюдением находились 120 недоношенных новорожденных (срок гестации 28—36 нед), родившихся в тяжелом состоянии и нуждавшихся в проведении интенсивной терапии после оказания первичной реанимационной помощи. Терапию цитофлавином, которую начали проводить в первые 2—4 ч после рождения, получал 61 ребенок. Группу контроля составили 59 новорожденных, лечившиеся без применения цитофлавина. Для оценки эффективности проводимого лечения, наряду со стандартными методами клинико-инструментального и лабораторного мониторинга, использовали определение уровня нескольких нейроспецифических белков (GFAP, NSE, MBP) в сыворотке крови. Полученные результаты показали выраженный церебропротекторный эффект цитофлавина. В основной группе новорожденных, получавших цитофлавин, была отмечена достоверно более быстрая нормализация показателей КОС, pO2, pCO2 и устранение лактат-ацидоза, чему соответствовало снижение тяжести и частоты развития ишемических и геморрагических поражений ЦНС и достоверно более низкие уровни нейроспецифических белков в крови по сравнению с детьми контрольной группы.
Ключевые слова: недоношенные новорожденные, церебральная гипоксия-ишемия, интенсивная терапия, церебропротекторная терапия, нейроспецифические белки, GFAP,NSE,MBP, цитофлавин.
Current approaches to cerebroprotective treatment of newborns in reanimation and intensive therapy departments
S.O. Rogatkin, N.N. Volodin, M.G. Degtyareva, O.V. Grebennikova, M.Sh. Margania, N.D. Serova
This work was conducted in the frames of a multicenter clinical trial. The aim was to study efficacy of cytoflavin (infusion solution) in the prevention and treatment of posthypoxic CNS lesions in premature newborns. The study included 120 premature newborns (gestation period 28—36 weeks) who was born in severe distress and needed the intensive therapy after primary reanimation measures. Cytoflavin was prescribed in the first 2—4 h after the delivery to 61 newborns. The control group included 59 newborns who did not receive the drug. To assess treatment efficacy, the determination of some plasma neurospecific proteins (GFAP, NSE, MBP) was carried out along with standard clinical/instrumental and laboratory monitoring. The results revealed the marked cerebroprotective effect of cytoflavin. The significantly higher rate of normalization of KOC, pO2, pCO2 and elimination of lactate acidosis that led to the reduction of severity and frequency of ischemic and hemorrhagic CNS lesions as well as lower levels of plasma neurospecific proteins were seen in the main group compared to the control one.
Key words: premature newborns, cerebral hypoxia-ischemia, intensive therapy, cerebroprotective treatment, neurospecific proteins, GFAP, NSE, MBP, cytoflavin.
Успехи неонатальной реанимации и интенсивной терапии позволили значительно увеличить выживаемость недоношенных новорожденных не только с низкой массой тела, но и экстремально низкой массой тела. Однако кардиореспираторные нарушения и патогенетически связанные с ними постгипоксические поражения головного мозга у таких детей остаются серьезной проблемой. Нестабильность функционирования системы «ауторегуляции мозгового кровотока» в силу морфофункциональной незрелости всех ее компонентов сопровождается крайне высокой частотой ишемических и геморрагических поражений мозга, последствиями которых являются различные по тяжести отклонения в нервно-психическом развитии и ранняя детская инвалидность. По данным статистики, до 85% всех перинатальных поражений ЦНС у недоношенных детей возникает в течение первой недели жизни [4, 9, 13, 24].
Изучение патофизиологических механизмов постгипоксического поражения головного мозга недоношенных новорожденных позволило обосновать концепцию необходимости раннего фармакологического вмешательства в каскад инициированных ишемией процессов, которое может в ряде случаев предотвратить или существенно снизить тяжесть повреждения нервной ткани и улучшить неврологический прогноз [9, 11, 21, 22].
Промежуток времени — «терапевтическое окно», в течение которого фармакологическое вмешательство с церебропротекторной целью может оказаться эффективным, по данным литературы [21, 24], колеблется от 2 до 48 ч после гипоксически-ишемического воздействия.
В настоящее время в качестве перспективных антигипоксантов рассматриваются лекарственные препараты, содержащие естественные метаболиты и регуляторы интрацеллюлярного энергетического обмена [5, 7, 8, 24].
Отечественный препарат цитофлавин (разработан компанией «Полисан», Санкт-Петербург) выпускается в виде раствора для внутривенного введения в ампулах по 10 мл. В своем составе он содержит сукцинат натрия, инозин (рибоксин), рибофлавин и никотинамид. Перечисленные компоненты оказывают комплексное корригирующее воздействие на внутриклеточный энергетический обмен как в условиях тканевой гипоксии-ишемии, так и в период постишемической реперфузии, характеризующийся активацией процессов свободнорадикального окисления [1, 3, 8, 17, 19, 21].
Целью настоящего исследования явилась оценка эффективности цитофлавина у недоношенных новорожденных с церебральной ишемией II—III степени, нуждавшихся в проведении реанимации и интенсивной терапии.
Материал и методы
Работа проводилась в рамках многоцентрового рандомизированного контрольно-сравнительного исследования1.
1Разрешение Росздравнадзора №73 от 20.02.07 г. и Комитета по этике при Федеральном органе контроля качества лекарственных средств №84 от 25.01.07 г.
На базе 4 исследовательских центров обследовали 304 ребенка, из которых 154 вошли в основную группу и 150 — в контрольную.
Представленный в настоящей статье фрагмент работы выполнен на клинических базах кафедры неонатологии Российского государственного медицинского университета, расположенных в отделениях реанимации и интенсивной терапии новорожденных (ОРИТН №1 и №2), и отделениях патологии новорожденных городской больницы № 8 (глав. врач — А.Б. Дуленков) Департамента здравоохранения Москвы.
В данной работе представлен анализ результатов динамического наблюдения, лабораторно-инструментального обследования и лечения 120 новорожденных детей. Срок гестации новорожденных варьировал от 28 до 36 нед, масса тела при рождении составила от 1060—3150 г (1781,7±508,98 г), рост от 25 до 50 см (40,6±3,93 см). Среди всех обследованных новорожденных мальчиков было 73, девочек — 47. Новорожденных из двойни было 24, из тройни — 4. Из 104 рожениц, дети которых были включены в исследование, первые роды были у 71 женщины, повторные — у 33. Оперативное родоразрешение путем операции кесарево сечение было проведено в 46 случаях. В 50 наблюдениях была зарегистрирована хроническая внутриутробная гипоксия плода, в 6 случаях имела место острая интранатальная гипоксия. В зависимости от характера терапии, проводимой в раннем неонатальном периоде, в ходе исследования все пациенты были разделены на две группы — основную и контрольную. Рандомизация проводилась методом «конвертов».
В основную группу был включен 61 недоношенный новорожденный ребенок, которым наряду с базовой интенсивной терапией внутривенно медленно в течение первых 5 сут после рождения вводился цитофлавин в дозе 2 мл/кг/сут после разведения в 10% растворе глюкозы в соотношении 1:5. Скорость введения полученного раствора колебалась от 1 до 4 мл/ч. Препарат вводили параллельно с парентеральным питанием, с растворами, используемыми для коррекции водно-электролитного баланса и объема циркулирующей крови. Общая продолжительность курса лечения цитофлавином составила 5 сут.
В контрольную группу были включены 59 недоношенных новорожденных детей, которым проводилась только необходимая базовая интенсивная терапия.
В основной группе мальчиков было 35, девочек — 26. В контрольной группе соответственно мальчиков — 38, девочек — 21. Срок гестации у детей основной группы составил 31,9±2,1 нед, в группе контроля, 32,3±2,5 нед (рис. 1).
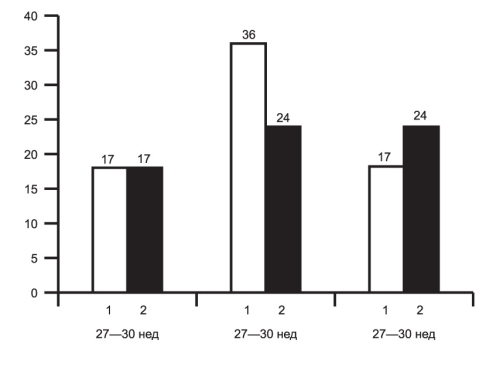
Рис. 1. Распределение детей основной (1) и контрольной (2) групп по срокам гестации.
По оси абсцисс — сроки гестации, по оси ординат — число детей.
Средняя масса тела детей при рождении в основной группе составила 1721,45±454,15 г, рост 40,6±3,25 см; в контрольной группе — 1846,3±558,5 г, рост 41±3,87 см соответственно (различия недостоверны).
Оценка по шкале Апгар в основной группе на 1-й минуте составила от 3 до 7 баллов (6,29±1,09), на 5-й минуте от 4 до 8 баллов (7,0±0,74), а в контрольной группе — от 2 до 7 баллов (6,08±1,35) на 1-й минуте и от 3 до 8 баллов (6,87±0,99) на 5-й минуте. Хроническая внутриутробная гипоксия плода у детей основной и контрольной групп была зафиксирована в равном числе наблюдений (по 25 детей), что составило 40,9 и 42,4% соответственно.
Летальных случаев среди всех наблюдавшихся детей зарегистрировано не было. Анализ продолжительности пребывания детей основной и контрольной групп в ОРИТН №1 и №2 показал, что достоверных различий по данному показателю между группами не было.
Общая продолжительность пребывания в стационаре среди детей обеих групп также достоверно не отличалась и составила 40,7±15,2 сут и 41,3±19,3 сут соответственно (различия недостоверны).
В связи с выраженными нарушениями кардиореспираторной адаптации в раннем неонатальном периоде все наблюдавшиеся новорожденные дети нуждались в респираторной поддержке. Из 61 ребенка основной группы в проведении искусственной вентиляции легких (ИВЛ) с первых часов после рождения нуждался 21 (34,4%) новорожденный, в группе контроля из 59 детей ИВЛ потребовалась 26 (44,1%) новорожденным. Респираторная терапия в виде «спонтанного дыхания с постоянным положительным давлением в дыхательных путях» (CPAP) проводилась с рождения 31 (57,4%) ребенку основной группы и 35 (52,5%) новорожденным в группе контроля.
В качестве критериев для оценки эффективности терапии использованы результаты инструментального и лабораторного мониторинга ряда функций, общепринятого в неонатальной реанимации и интенсивной терапии [9, 14, 21].
Наряду с указанным мониторингом проводилось определение содержания в сыворотке крови нейроспецифических белков (НСБ): глиального фибриллярного кислого протеина (GFAP), нейроспецифической енолазы (NSE) и основного белка миелина (МВР). Их определение позволяет адекватно оценивать состояние практически всех основных клеточных популяций нервной ткани.
NSE — γ -γ димер нейроспецифического белка 14-3-2 содержится преимущественно в цитоплазме и дендритах нейронов и на сегодняшний день считается одним из наиболее специфических маркеров их поражения [6, 10, 13, 16, 25].
GFAP — цитоплазматический белок, входящий в состав микрофиламентов, образующих цитоскелет астроцитарных глиоцитов. В зрелой нервной ткани иммунологическими методами GFAP обнаруживается внутри микрофиламентов протоплазматических астроцитов серого вещества и в фиброзных астроцитах белого вещества. Большое количество GFAP содержится также в субэпендимальных астроцитах в перивентрикулярных областях. Кроме того, данный НСБ был выявлен в незначительных количествах в эпифизе, нейрогипофизе и незрелых олигодендроглиоцитах [6, 10, 13, 15, 20, 25].
МВР представляет собой набор мембранных белков, функцией которых является адгезия цитоплазматических мембран миелинового бислоя. Процессы формирования и созревания миелиновых оболочек на аксонах и дендритах сопровождается постепенным снижением концентрации MBP в сыворотке крови у новорожденных детей от момента рождения к концу неонатального периода. Напротив, разрушение миелина или олигодендроглиоцитов, т.е. демиелинизация, возникающая вследствие повреждения белого вещества головного и спинного мозга, сопровождается повышением концентрации MBP в сыворотке крови свыше 2 нг/мл [6, 18, 23].
Определение перечисленных белков проводилось по стандартизированным тестам-системам на основе моноклональных антител к различным НСБ. Известно, что эти методы, обладая высокой диагностической чувствительностью и специфичностью, дают возможность использовать для исследования малые объемы сыворотки (0,2—0,5 мл), что весьма важно для неонатальной практики [2, 6, 10, 11, 13, 15, 18, 20]. Первый забор крови для исследования производился из пуповинной крови при рождении или при катетеризации пупочных сосудов для проведения инфузионной терапии. Повторные заборы крови осуществлялись из периферической вены новорожденных в объеме 0,5—1,0 мл приблизительно в одно и то же время суток (9.00—10.00 утра) на 5-е, 14-е сутки жизни и в скорректированном возрасте (СВ) 1-го и 3-го месяцев жизни. Количественный анализ выше перечисленных НСБ в сыворотке крови проводился по методике, разработанной в лаборатории иммунохимии (зав. — д.м.н. О.И. Гурина) Государственного научного центра судебной и социальной психиатрии им. В.П. Сербского. Эти методы описаны в литературе [6, 13].
Статистический анализ данных выполнялся с помощью пакета программ Statistica 6.0 с использованием критериев, адекватных типам данных и поставленным задачам [12]. Данные представлены в формате: M±m (sd), где М — средняя арифметическая, m — ошибка средней, sd — стандартное отклонение. Применяли t-критерий Стьюдента для зависимых и независимых выборок. Различия считались статистически значимыми при р<0,05.
Результаты и обсуждение
При инфузии раствора, содержащего цитофлавин, у детей основной группы с первых часов лечения происходила быстрая нормализация показателей кислотноосновного соотношения (КОС) за счет устранения метаболической составляющей смешанного ацидоза. Через 6—12 ч после начала лечения величина дефицита оснований (ВЕ) в группе детей, получавших цитофлавин была достоверно меньше по сравнению с контрольной группой, а в дальнейшем, к концу 2 суток жизни, отрицательные значения BE у новорожденных основной группы трансформировались в положительные значения, которые сохранялись вплоть до окончания 5-дневного курса терапии. Начиная с 3 суток лечения показатели BE у новорожденных основной группы оставались достоверно более высокими (рис. 2). Кроме того, устранение метаболической составляющей ацидоза сопровождалось у детей основной группы достоверно более быстрой нормализацией уровня сывороточного лактата (рис. 3). Уже через несколько часов после начала лечения в основной группе концентрация лактата в сыворотке крови не превышала нормативных показателей. В то время как в группе контроля лактат-ацидоз сохранялся вплоть до 2 суток жизни.
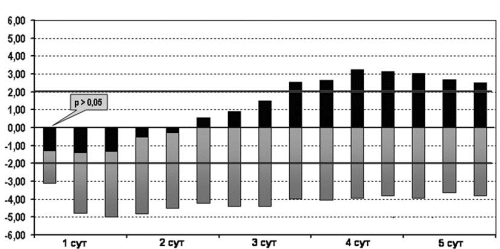
Рис. 2.Динамика изменений ВЕ крови у детей основной и контрольной групп на 5-е сутки жизни.
Здесь и на рис. 3—6: по оси абсцисс — возраст детей (сут); по оси ординат — величина ВЕ; верхняя граница нормы 3,00, нижняя — 5,00.
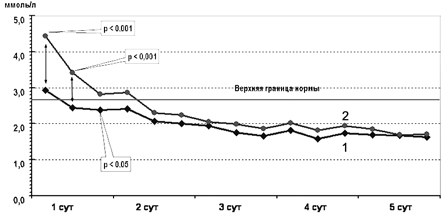
Рис. 3. Динамика уровня лактата (в моль/л) у больных основной (кривая 1) и контрольной (кривая 2) групп.
В течение первых часов лечения концентрацию О2 в дыхательной смеси у новорожденных основной группы удалось снизить до 35, а затем и до 25%. Таким образом, уже к исходу 1-х суток дети основной группы получали дыхательную смесь, содержащую нетоксичные концентрации кислорода. У детей группы контроля концентрация О2 в дыхательной смеси исходно была достоверно более высокой, что диктовалось показателями КОС и данными транскутанного мониторинга SaO2. Несмотря на то что концентрацию О2 в дыхательной смеси у детей группы контроля пытались снижать, достичь безопасных его концентраций в этой группе удалось только к исходу 2-х, началу 3-х суток жизни (рис. 4).
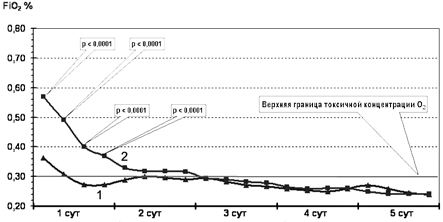
Рис. 4. Содержание кислорода (FiO2%) в дыхательной смеси у детей основной (кривая 1) и контрольной (кривая 2) групп.
При этом количество новорожденных среди детей основной группы, получавших респираторную поддержку с помощью метода CPAP, постоянно увеличивалось. Так, если в 1-е сутки жизни среди 61 ребенка основной группы 34% (21) новорожденных нуждались в проведении ИВЛ, то уже к 4-м суткам жизни продолжение ИВЛ потребовалось только 15 (24,5%) детям. В то время как из 59 новорожденных контрольной группы с рождения находились на ИВЛ 44% детей, а к исходу 4-х суток жизни 33,8% детей нуждались в продолжении искусственной вентиляции легких. Нормализация показателей КОС у детей контрольной группы наступила поздней и сопровождалась гипероксией за счет респираторной компенсации метаболического ацидоза. Об этом косвенно свидетельствует и анализ динамики такого показателя, как уровень pCO2 в смешанной капиллярной крови (рис. 5).
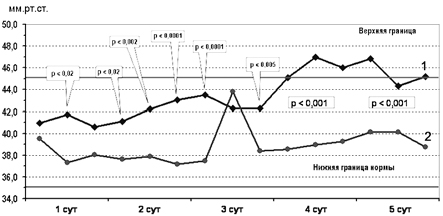
Рис. 5. Изменение pCO2 в крови детей основной (1) и контрольной (2) групп.
Сравнительный анализ показателей pCO2 капиллярной крови у детей обеих групп выявил, что на фоне нормализации pH и BE у получавших цитофлавин отмечалась тенденция к росту концентрации углекислоты в капиллярной крови. Однако, несмотря на достоверно более высокие значения по сравнению с контрольной группой, уровень pCO2 у детей основной группы оставался в пределах физиологических границ 35—45 мм рт.ст. При этом динамическое наблюдение за показателями пульсоксиметрии позволило обнаружить, что у новорожденных контрольной группы соответствующие значения насыщения крови были близки к токсическим, а с 3—5 сут наблюдения превышали нормативные показатели (рис. 6).
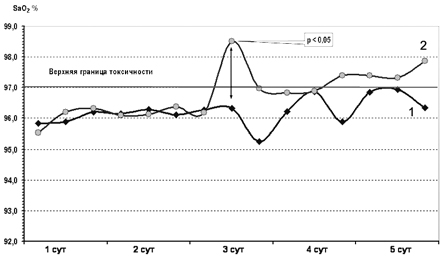
Рис. 6. Показатели насыщения крови кислородом у детей основной (1) и контрольной (2) групп.
Несмотря на то что среди детей основной группы новорожденных со сроком гестации менее 33 нед было больше (53 ребенка) по сравнению с контролем (41 ребенок), к 14-м суткам жизни в проведении ИВЛ нуждались всего 3 (5%) новорожденных из 61, в то время как в контрольной группе — 10 (17%) новорожденных. К 2-недельному возрасту среди новорожденных основной группы 92% детей находились уже на спонтанном дыхании, в то время как в группе контроля доля таковых составила 83%. Общая продолжительность пребывания в стационаре детей основной и контрольной групп достоверно не отличались.
Анализ частоты выявления неврологических нарушений и инвалидизирующих заболеваний, свойственных недоношенным детям, перенесшим перинатальную гипоксию и нуждавшихся в проведении интенсивной терапии, показал, что у детей основной группы не было тяжелых форм пери- и интравентрикулярных кровоизлияний (ПИВК) и перивентрикулярных лейкомаляций (ПВЛ)2, а неонатальные судороги регистрировались почти в 2 раза реже, чем в контрольной группе. Бронхолегочные дисплазии и ретинопатии у недоношенных регистрировались с одинаковой частотой, почти у детей основной группы преобладали легкие формы этих заболеваний. Приведем соответствующие диагнозы при выписке у детей основной и контрольной групп.
В контрольной группе распределение диагнозов было следующим: задержка психомоторного развития — 28%, неонатальные судороги — 24,6%, ретинопатия недоношенных — 19,3%, бронхолегочная дисплазия — 8,8%, ПИВК I степени — 8,8%, ПИВК II степени — 3,5%, ПИВК III степени — 3,5%, кистозные ПВЛ — 5,3%.
В основной группе распределение диагнозов было таким: задержка психомоторного развития — 23,7%, неонатальные судороги — 13,5%, ретинопатия недоношенных — 20,3%, бронхолегочная дисплазия — 5%, ПИВК I степени — 11,8%.
Анализ динамики содержания GFAP в сыворотке показал, что исходно уровень этого белка был значительно повышен как в основной, так и в контрольной группах. При рождении его уровень в крови у обследованных новорожденных превышал нормативные показатели в 2 раза (8 нг/мл при норме 4 нг/мл), а у детей из группы контроля имел тенденцию к росту в течение 1-й недели жизни (рис. 7).
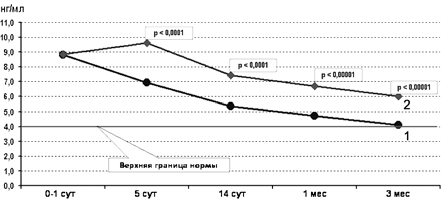
Рис. 7. Содержание GFAP в сыворотке крови больных основной (1) и контрольной (2) групп.
Здесь и на рис. 9: по оси абсцисс — возраст детей (нед и мес).
Известно, что любые повреждения микрососудов головного мозга сопровождаются значительным повышением концентрации GFAP в крови, что обусловлено деструкцией клеток астроцитарной глии [20, 23]. Действительно, у детей из обеих групп уже в течение первых дней жизни были выявлены ПИВК I—II степени. Однако у новорожденных контрольной группы субэпендимальные кровоизлияния ПИВК I степени прогрессировали, и у 5 детей по данным НСГ к концу 1-й недели жизни они выросли до ПИВК II—III степени.
К 14-м суткам жизни у всех обследованных детей было отмечено значительное снижение концентрации GFAP в сыворотке, а в последующем уровень данного белка неуклонно снижался, оставаясь при этом выше нормативных показателей. Эти изменения, на наш взгляд, обусловлены постепенной нормализацией системной и церебральной гемодинамики. При этом у новорожденных основной группы нормализация состояния клеток нервной ткани началась достоверно раньше и происходила достоверно быстрее. Так, показатели GFAP в сыворотке крови у детей основной группы достигли верхней границы нормы уже к 3 скорректированным месяцам, в то время как у детей группы контроля они оставались в 1,5 раза выше нормативных.
Анализ содержания в сыворотке NSE показал, что изменения концентрации данного нейроспецифического белка в крови у обследованных детей разных групп сходны (рис.8). До начала лечения цитофлавином концентрация NSE в крови у детей групп сравнения была одинаково высокой и значительно превосходила возрастные нормативы [2, 6, 10, 13]. Но у новорожденных основной группы на фоне терапии цитофлавином отмечалось достоверно более быстрое снижение уровня NSE и почти полная нормализация его содержания в крови к 2 нед жизни. К СВ 1-го и СВ 3-го месяца жизни у младенцев основной группы его уровни в сыворотке крови уже соответствовали нормативным показателям.
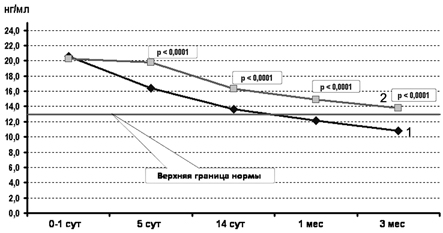
Рис. 8. Содержание NSE в сыворотке крови больных основной (1) и контрольной (2) групп.
В то же время у детей контрольной группы в течение всей первой недели жизни уровень NSE оставался таким же, как при рождении, а затем начинал постепенно снижаться, оставаясь даже к СВ 3 мес жизни выше нормативных показателей. Анализ динамики содержания в сыворотке NSE, отражающей состояние нейроцитов, указывает на то, что повреждение и деструкция нейрональных клеток у детей группы контроля особенно интенсивно протекали в течение 1-й недели жизни с постепенным уменьшением к 3 скорректированным месяцам жизни. Однако даже спустя такой значительный период времени уровни NSE оставались выше нормативных показателей, что свидетельствует о продолжавшейся гибели нейронов у детей из группы контроля [17].
Динамика изменений сывороточных уровней MBP у детей обеих групп сравнения имела значительные отличия от GFAP и NSE (рис. 9).
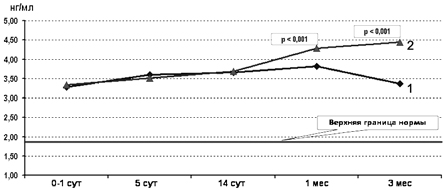
Рис. 9. Содержание в сыворотке крови МВР у детей основной (1) и контрольной (2) групп.
В течение первых 2 нед жизни у всех детей уровень белка был повышен по сравнению с нормативными показателями и имел тенденцию к постепенному нарастанию [6, 10, 13, 24]. Однако к СВ 1-го месяца у детей основной группы его сывороточный уровень был уже достоверно ниже по сравнению с контрольной группой и продолжал прогрессивно снижаться, в то время как у детей контрольной группы после 2-недельного возраста отмечен рост сывороточной концентрации МВР вплоть до 3 мес СВ. По нашему мнению, это отражает продолжающиеся процессы деградации миелиновых оболочек и задержкой образования полноценного «зрелого» миелина на аксонах и дендритах в контрольной группе. Подтверждением данной точки зрения являются результаты исследований, свидетельствующих о том, что биологическая роль МВР состоит в стабилизации многослойных мембран миелиновых оболочек нервных проводников [6, 11, 18, 23].
Проведенное исследование позволяет сделать следующие выводы: 1. Раннее, в первые 2-4 ч постнатальной жизни, применение у недоношенных новорожденных, перенесших церебральную гипоксию-ишемию, препарата цитофлавин в дозе 2 мл/кг/сут оказывает отчетливое системное антигипоксантное действие. Это подтверждается быстрым снижением потребности в высоких концентрациях кислорода при проведении респираторной поддержки (ИВЛ, CPAP), устранением признаков централизации кровообращения, улучшением тканевой перфузии, нормализацией показателей рН и ВЕ, устранением лактатацидоза. 2. Пятидневный курс терапии цитофлавином позволяет снизить частоту и тяжесть неврологических и соматических осложнений у недоношенных новорожденны, получающих лечение в условиях ОРИТН за счет создания условий для более успешного перехода внутриклеточного энергетического обмена от анаэробного к аэробному гликолизу. 3. Церебропротекторные свойства цитофлавина подтверждаются отсутствием у детей основной группы тяжелых форм перивентрикулярных кровоизлияний и внутрижелудочковых кровоизлияний (ПВК/ВЖК) и ПВЛ, более быстрой нормализацией содержания нейроспецифических белков в сыворотке крови.
ЛИТЕРАТУРА
1. Афанасьев В.В. Цитофлавин в интенсивной терапии: Пособие для врачей. Ст-Петербург 2005; 36.
2. Блинов Д.В. Иммуноферментный анализ нейроспецифических анти- генов в оценке проницаемости гематоэнцефалического барьера при гипоксически-ишемических поражениях ЦНС в перинатальном пе- риоде (клинико-экспериментальное исследование): Автореф. дис. … канд. мед. наук. М 2004.
3. Бульон В.В., Хныченко Л.С., Сапронов Н.С. Коррекция последствий постишемического реперфузионного повреждения головного мозга цитофлавином. Бюл эксперим биол 2000; 129: 2: 149—151.
4. Володин Н.Н., Рогаткин С.О., Медведев М.И. Актуальные проблемы перинатальной неврологии на современном этапе. Журн неврол и психиат 2001; 101: 7: 4—9.
5. Володин Н.Н., Рогаткин С.О. Современные подходы к комплексной терапии перинатальных поражений ЦНС у новорожденных. Фарма- тека 2004; 1: 72—83.
6. Гурина О.И. Моноклональные антитела к нейроспецифическим ан- тигенам. Получение, иммунохимический анализ, исследование про- ницаемости гематоэнцефалического барьера: Автореф. дис. … д-ра мед. наук. М 2005.
7. Заржецкий Ю.В., Мутускина Е.А., Трубина И.Е. и др. Влияние сукци- ната натрия на функциональные, биохимические и морфологические показатели восстановления ЦНС у крыс после 10-минутной останов- ки кровообращения. М — Пущино 1997; 96—103.
8. Кондрашева М.Н. Механизмы физиологической активности янтар- ной кислоты и рекомендации к ее применению. Клинические и пато- генетические проблемы нарушения клеточной энергетики (митохон- дриальная патология). М 1999; 33—34.
9. «Неонатология». Национальное руководство. Под ред. акад. РАМН Н.Н. Володина. М: ГЭОТАР-Медиа 2007; 848.
10. Рогаткин С.О., Блинов Д.В., Володин Н.Н. и др. Перспективы приме- нения иммуноферментного анализа нейроспецифических антигенов в перинатальной неврологии. Вопр гин акуш и перинатол 2003; 2: 4: 8—13.
11. Рогаткин С.О., Людковская Е.В., Володин Н.Н. Лечение детей, пере- несших перинатальную гипоксию в периоде ранней неонатальной адаптации. Вопр гин акуш и перинатол 2005; 4: 3: 37—40.
12. Реброва О.Ю. Статистический анализ медицинских данных. Приме- нение пакета прикладных программ Statistica. М: МедиаСфера 2006; 312.
13. Чехонин В.П., Дмитриева Т.Б., Жирков Ю.А. Иммунохимический ана- лиз нейроспецифических антигенов. М: Медицина 2000; 415.
14. Avery B. Gordon, MacDonald G. Mhairi, Martha D. Mullett, Mary M. Seshia. Avery’s Neonatology: Pathophysiology and management of the newborn (6-th edition). Lippincott Williams & Wilkins 2005; 1504.
15. Blennow M., Savman K., Ilves P et al. Brain-specific proteins in the cerebrospinal fluid of severely asphyxiated newborn infants. Acta Paediat 2001; 90: 1171—1175.
16. Ezgu F.S., Atalay Y., Gucuyener K. et al. Neuron-specific enolase levels and neuroimaging in asphyxed preterm end term newborns. Ankara, Turkey. J Child Neurol 2002; 17: 11: 824—829.
17. Hawdon J.M., Ward Piatt M.P., Aynsley-Green A. Patterns of metabolic adaptation for preterm and term infants in the first neonatal week. Arch Dis Child 1992; 67: 357—365.
18. Hirayama A., Okoshi Y., Hachiya Y. et al. Early immunohistochemical detection of axonal damage and glial activation in extremely immature brains with periventricular leukomalacia. Clin Neuropathol 2001; 20: 87—91.
19. Johnston M.V., Trescher W.H., Ishida A. et al. Neurobiology of hypoxicischemic injury in the developing brain. Pediat Res 2001; 49: 735—741.
20. Nagdyman N., Komen W., Ko H.K. et al. Early biochemical indicators of hypoxic-ischemic encephalopathy after birth asphyxia. Pediat Res 2001; 49: 502—506.
21. Perlman J.M. Neurology: neonatology questions and controversies. Consulting editor, Richard A. Polin. Saunders—Elsevier 2008; 225.
22. Raju Tonse N.K., Ariagno R.L., Higgins R. et al. Research in Neonatology for the 21st Century: Executive Summary of the National Institute of Child Health and Human Development—American Academy of Pediatrics Workshop. Part I: Academic Issues. Pediatrics 2005; 115: 468—474.
23. Verkhratsky A., Butt A. Glial neurobiology: a textbook. John Wiley & Sons Ltd. England 2007; 209.
24. Volpe J.J. Neurology of the Newborn 5th ed. Philadelphia: Elsevier 2008; 1042.
25. Vos P.E., Lamers K.J., Hendriks J.C. et al. Glial and neuronal proteins in serum predict outcome after severe traumatic brain injury. Neurology 2004; 62: 8: 1303—1310.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)