Патогенетические аспекты применения цитофлавина в лечении хронической посттравматической головной боли
Статьи
Опубликовано в журнале:
Журнал неврологии и психиатрии, 11, 2016
Д.А. Искра
ФГБВОУ ВПО «Военно-медицинская академия им. С.М. Кирова», Санкт-Петербург, Россия
Цель исследования. Оценка результатов применения цитофлавина в лечении хронической посттравматической головной боли (ХПТГБ) с анализом возможных механизмов реализации его терапевтических эффектов. Материал и методы. В исследование были включены 76 пациентов, 23 мужчины и 53 женщины, в возрасте от 29 до 57 лет (средний — 38,2±8,3 года). Все пациенты получали стандартную базовую терапию простыми и комбинированными анальгетиками. Помимо стандартного лечения 36 пациентам был дополнительно назначен цитофлавин по 2 таблетки 2 раза в день в течение 30 дней. Результаты и заключение. В начале курса лечения, в конце и через 30 дней после его завершения тестировали интенсивность, частоту головной боли, выраженность астенических и депрессивных проявлений. В результате проведенного лечения в группе пациентов, получавших цитофлавин, наблюдался значительный регресс астенической и депрессивной симптоматики, что соответствует данным предыдущих исследований. Положительная динамика анализируемых показателей коррелировала с уменьшением частоты цефалгий. Поскольку цитофлавин не обладает анальгетическим действием, полученные результаты косвенно свидетельствуют о значимости психопатологических факторов в патогенезе ХПТГБ.
Ключевые слова: хроническая посттравматическая головная боль, астения, депрессия, эмоциональное состояние, цитофлавин.
Pathogenic aspects of the use of cytoflavine in the treatment of сhronic post-traumatic headache
D.A. Iskra
Kirov Military Medical Academy, Saint-Petersburg, Russia
Objective: To evaluate the results of using cytoflavin in the treatment of chronic post-traumatic headache and analyze possible mechanisms for implementation of therapeutic effects of the drug. Material and methods: The study included 76 patients (23 men and 53 women) aged 29 - 57 years (mean age – 38.2 ± 8.3). All patients received standard basic therapy with simple or combination analgesics. In addition to standard treatment, 36 patients received cytoflavin in the dosage of two tablets twice a day for 30 days. Results and Conclusion: At the beginning, at the end and 30 days after the completion of treatment, the intensity and frequency of headache as well as the severity of asthenic and depressive symptoms were analyzed. As a result of treatment in the cytoflavin group, there was a significant regression of asthenic and depressive symptoms, which was consistent with the previous studies. Positive changes in the indicators analyzed were correlated with the decrease in the frequency of cephalalgia. Since cytoflavin has no analgesic properties, the results are indirect evidence for the significance of psychopathological factors in the pathogenesis of chronic post-traumatic headache.
Keywords: chronic post-traumatic headache, asthenia, depression emotional, cytoflavin
Хроническая посттравматическая головная боль (ХПТГБ) — вторичная цефалгия, которая вызвана черепно-мозговой травмой (ЧМТ) и сохраняется более 3 мес. Головная боль наблюдается у 30—90% пациентов с травмами головы и/или шеи. У 32—44% пострадавших цефалгии, связанные с ЧМТ, являются хроническими и сохраняются не менее 6 мес, а у 25% из них — 4 года и более [1—5]. Несмотря на значительную распространенность, патогенетическая терапия ХПТГБ остается малоэффективной, что связано прежде всего с недостаточной изученностью механизмов возникновения и развития этой цефалгии. Показано, что в основе патогенеза ХПТГБ лежат психопатологические и структурно-функциональные неврологические нарушения [6—8]. В настоящее время доминирует точка зрения, согласно которой органические дефекты, полученные в результате ЧМТ, играют значимую для развития ХПТГБ роль лишь в дебюте цефалгии. Частота возникновения ХПТГБ у пациентов, получивших ЧМТ в момент изменения положения головы (при ее наклонах, поворотах), существенно возрастает. Предполагается, что при этом чаще поражаются стволовые структуры. К значимым для патогенеза морфологическим дефектам нервной системы, обнаруживаемым и после легкой ЧМТ, относятся нарушения церебральной гемодинамики и повреждения аксонов церебральных нейронов, приводящие к дисрегуляции функционирования стволовых ноцицептивных путей [2, 9, 10].
Функциональные нарушения, выявляемые при ХПТГБ, сходны с таковыми при первичных цефалгиях (мигрень, головная боль напряжения (ГБН)): нарушения метаболизма возбуждающих аминокислот, нейропептидов, серотонина, катехоламина, эндогенных опиатов, магния в мозговой ткани; снижение порога возбуждения клеток ядер тройничного нерва и корковых нейронов. Такая схожесть позволяет считать описанные функциональные расстройства лишь конечными звеньями реализации специфичных для ХПТГБ процессов [2, 4—7].
В проведенных еще в прошлом веке исследованиях было обнаружено, что риск развития ХПТГБ выше при легкой ЧМТ по сравнению с тяжелым повреждением. Тогда это объяснялось невнимательным отношением к лечению больных с легкой ЧМТ, в результате чего прогрессировало органическое поражение мозгового вещества [7, 11].
В настоящее время все больше исследователей склоняется к мысли о том, что психопатологические расстройства в патогенезе ХПТГБ играют более важную роль по сравнению со структурно-функциональными нарушениями. Психопатологические расстройства обусловлены физическим и эмоциональным стрессом, наблюдаемым при любой ЧМТ. Они проявляются посттравматической диссомнией, нарушениями эмоциональной мотивации и колебаниями настроения, например, в связи с беспокойством пациента по поводу возможности выздоровления и восстановления профессиональных навыков. Определенное значение могут иметь социальные аспекты ЧМТ — судебные разбирательства, желание получить материальную компенсацию и др. [5, 6].
Значимость психопатологических нарушений определяется генетической предрасположенностью и личностными особенностями пациента, его преморбидными характеристиками, социальным статусом. ХПТГБ чаще развивается у женщин, у лиц с низким образовательным и социально-экономическим уровнем, злоупотребляющих алкоголем, имеющих психические расстройства или цефалгии до травмы [5, 12].
Не вызывает сомнения, что эффективность назначаемой терапии напрямую зависит от понимания ведущих механизмов развития ХПТГБ. Применение простых и комбинированных анальгетиков для купирования приступов краниалгии оправдано, однако категорически недопустимо их нерациональное использование. Несоблюдение режима дозирования способствует длительному сохранению цефалгии после травмы, развитию головной боли, связанной с избыточным приемом лекарственных препаратов. Альтернативой обезболивающим средствам являются антидепрессанты и транквилизаторы. Логика их применения основана на необходимости коррекции тревожно-депрессивной симптоматики, часто наблюдаемой при любой хронической боли. Однако использование этих препаратов имеет ряд ограничений, связанных прежде всего с их низкой эффективностью для купирования других проявлений посткоммоционного синдрома: диссомнии, астении и др. [2, 4, 5].
В последнее время появилось значительное число работ, посвященных терапевтическим эффектам комбинированного препарата цитофлавин (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург). В отличие от других ноотропов, применение цитофлавина не только улучшает состояние когнитивных функций, но и оказывает антиастенический и антидепрессивный эффекты, что связано с его антиоксидантными, антигипоксантными и энергокорригирующими свойствами [13—5]. Это позволяет рассматривать его в качестве потенциального средства для патогенетического лечения последствий ЧМТ.
Цель исследования — оценка результатов применения цитофлавина в лечении ХПТГБ с анализом возможных механизмов реализации его терапевтических эффектов.
Материал и методы
Проанализированы результаты лечения 76 пациентов, 23 мужчин и 53 женщин в возрасте 29—57 лет (средний возраст — 38,2±8,3 года) с верифицированным диагнозом ХПТГБ (код по МКБ 10: G44.3).
Критериями включения в исследование явились: возникновение головной боли в течение 7 дней после одного из событий: легкой ЧМТ (подтвержденные сотрясение головного мозга или ушиб легкой степени); восстановления сознания после ЧМТ; прекращения приема лекарств, снижающих способность ощущать головную боль после ЧМТ или сообщать о ней; сохранение цефалгии в течение 3 мес и более после травмы. Критерии исключения из исследования: психотические расстройства; неврологические или соматические заболевания в стадии декомпенсации; алкоголизм или наркомания; беременность.
Все пациенты были разделены на две группы, сопоставимые по полу и возрасту: основную составили 38 больных, 11 мужчин 27 женщин, средний возраст 38,5±10,9 года, получавших цитофлавин по 2 таблетки 2 раза в день 25 дней, в группу сравнения вошли 38 пациентов, 12 мужчин и 26 женщин, средний возраст 37,9±10,5 года), которые получали только симптоматическую терапию, включая обезболивающие препараты.
Помимо стандартного клинико-лабораторного обследования, пациентам было проведено тестирование болевого синдрома с помощью шкалы Мак-Гилла, депрессивных расстройств — по шкале Бека, выраженность астении оценивалась с помощью многомерного опросника на утомляемость и шкалы оценки общей астении. Все пациенты ежедневно в течение 2 мес вели дневник головной боли. Обследование проведено в динамике: до начала лечения и через 30 и 60 дней.
Статистическая обработка полученных данных проводилась с использованием пакета программ SPSS17. За достоверные показатели принимались различия при р<0,05.
Результаты и обсуждение
Анализ исходных данных выявил схожесть изучаемых социальных характеристик в группах сравнения: значительную часть обследованных составляли лица среднего возраста, преобладали женщины. Только треть пациентов — 10 (26,3%) основной и 12 (31,5%) группы сравнения имели высшее образование, у 11 (28,9%) пациентов основной группы и у 10 (26,3%) — группы сравнения отмечались цефалгии до ЧМТ (см. таблицу). Длительность цефалгии от момента получения травмы составила 3,2±0,5 года в основной группе и 3,7±0,2 года в группе сравнения, среднее число «болевых» дней в месяц — 12,4±0,11 и 13,8±03 соответственно, причем у 6 (15,8%) пациентов основной группы и у 5(13,2%) группы сравнения число болевых дней составило более 15, что является важным критерием оценки ХПТГБ. В ходе опроса было выявлено, что 9 (23,7%) пациентов основной группы и 10 (26,3%) группы сравнения принимали избыточное количество анальгетиков.
Исходные результаты обследованных больных (M±m)
| Показатель, (баллы) |
Группа сравнения (n=38) |
Основная группа (n=38) |
| Опросник Мак-Гилла |
8,7±1,3 |
8,3±0,8 |
| Многомерный опросник для выявления утомляемости |
62,1±5,2 |
61,2±3,6 |
| Шкала депрессии Бека |
17,4±1,9 |
18,2±2,7 |
| Шкала общей астении |
13,4±2,1 |
14,2±0,9 |
У всех обследованных независимо от цефалгии ХПТГБ всегда наблюдалась в совокупности с такими клиническими проявлениями, как головокружение, диссомния, тревожность, раздражительность, снижение памяти, концентрации внимания и психомоторной активности. Это обстоятельство позволяло утверждать, что частота указанных симптомов, входящих вместе с ХПТГБ в структуру посткоммоционного синдрома, не зависит от тяжести цефалгии. В ходе исследования не было выявлено специфических клинических проявлений ХПТГБ: у 29 (76,3%) пациентов основной группы и у 31 (81,6%) группы сравнения ХПТГБ напоминала головную боль напряжения с интенсивностью около 5 баллов, у остальных пациентов интенсивность цефалгии оценивалась как выраженная (около 7 баллов) с отдельными признаками мигрени без ауры.
Большинство больных в обеих группах занимались самолечением, нередко с избыточным применением анальгетиков. В соответствие с критериями МКГБ-3 под избыточным приемом понималось использование более 15 простых анальгетиков, а комбинированных препаратов — более 10 дней в месяц в течение 3 мес и более [3]. В то же время головная боль у этих пациентов не соответствовала критериями абузусной, поэтому они были включены в группы сравнения. Важно отметить, что корреляционной связи между выраженностью ряда клинических признаков посткоммоционного синдрома и тяжестью ХПТГБ (интенсивность, количество болевых дней) обнаружено не было.
Отмечалась положительная динамика изучавшихся показателей у всех пациентов, более выраженная в основной группе: уменьшение интенсивности головной боли (по шкале опросника Мак-Гилла) на 28,3% (с 8,3±0,8 до 2,35±0,5 баллов; р<0,03). Улучшение достоверно коррелировало со снижением астенической и депрессивной симптоматики. Выраженность депрессии (по шкале Бека) также уменьшилась к концу курса лечения в основной группе на 65,4%, а в группе сравнения — на 56,8%; p<0,01 (рис. 1).
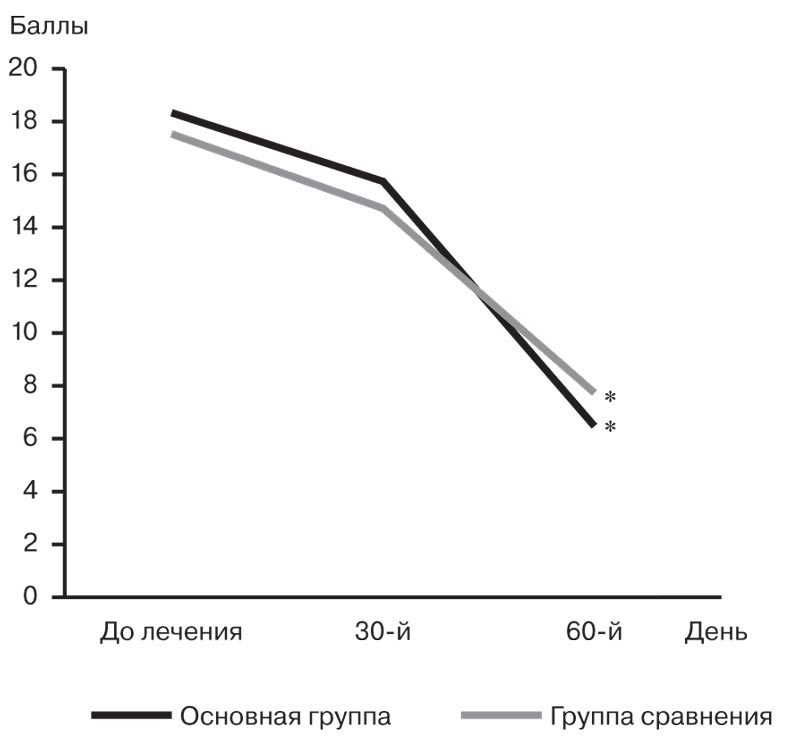
Рис. 1. Динамика выраженности депрессии по шкале Бека в двух группах.
1 — основная группа; 2 — группа сравнения. * — различия достоверны при сравнении с исходными значениями (р<0,01).
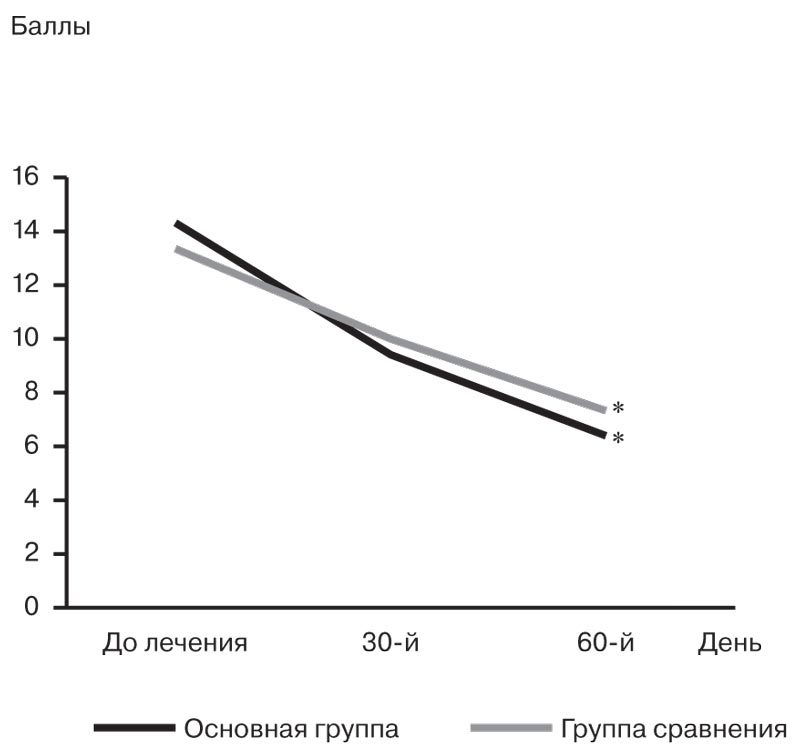
Рис. 2. Динамика астенического синдрома в двух группах.
1 — основная группа; 2 — группа сравнения. * — различия достоверны при сравнении с исходными значениями (р<0,01).
При анализе выраженности утомляемости было отмечено ее уменьшение у пациентов основной группы на 16,5% (с 61,2±3,6 до 51,1±2,3 балла; p<0,01). По шкале общей астении выявлено улучшение показателей в основной группе на 55,6% (с 14,2±0,9 до 7,2±1,5 баллов; p<0,01) и на 46,2% (с 13,4±2,1 до 6,3±1,7 баллов; р<0,03) — в группе сравнения.
Таким образом, результаты проведенного исследования позволяют сделать выводы о генезе ХПТГБ и стратегии ее лечения. Отсутствие зависимости тяжести и частоты возникновения ХПТГБ, а также выраженности других симптомов посткоммоционного синдрома свидетельствуют об определенных различиях в их патогенезе. В то же время большое значение для развития ХПТГБ имеет преморбидный фон — исходная сенситизация центральных нейронов — важнейшего фактора, обусловливающего развитие первичных цефалгий, определяемых у значительной части обследованного контингента до ЧМТ. К предикторам развития ХПТГБ следует отнести особенности эмоционального восприятия болевых ощущений. Вероятно, что специфическая эмоциональная окраска боли определяет большую частоту возникновения цефалгии у женщин и у лиц с низким образовательным уровнем в силу их меньшей социальной защищенности и переживаний по поводу возможной утраты источника доходов.
У всех пациентов с ХПТГБ, независимо от степени ее выраженности, наблюдалась астенодепрессивная симптоматика. Астенические и депрессивные нарушения являются наиболее частыми проявлениями посткоммоционного синдрома. Они могут наблюдаться у пациентов с последствиями ЧМТ и без головной боли [9]. Вероятно, именно эти расстройства являются определяющими в патогенезе ХПТГБ при формировании последствий ЧМТ, что косвенно подтверждается эффективностью цитофлавина при лечении таких пациентов.
Препарат не обладает анальгетической активностью, однако имеет доказанные антиастенические и антидепрессивные свойства [13, 14], что было подтверждено в проведенном исследовании. Следовательно, зарегистрированное значительное уменьшение тяжести ХПТГБ было обусловлено регрессом психопатологических симптомов. Все пациенты получили лечение цитофлавином в полном объеме, развития нежелательных явлений на введение препарата выявлено не было.
Таким образом, в настоящем исследовании было установлено, что у пациентов с ХПТГБ на фоне умеренного болевого синдрома развивается умеренная депрессия и астения; включение в схему лечения цитофлавина дает возможность повысить эффективность терапии: уменьшить интенсивность головной боли — на 28,3%, выраженности депрессии — на 65,4%, астении — на 55,6% и утомляемости — на 16,5%; эффективность цитофлавина наряду с его безопасностью, позволяет рекомендовать его включение в схемы лечения пациентов с ХПТГБ.
Литература
- Одинак М.М., Искра Д.А. Систематизация первичных головных болей: ближайшие и отдаленные перспективы. Военно-медицинский журнал. 2014;335(2):22-31.
- Formisano R, Bivona U, Catani S, D’Ippolito M, Buzzi G. Post-traumatic headache: facts and doubts. J Headache Pain. 2009;10(3):145-152.
doi: 10.1007/s10194-009-0108-4
- Headache Classification Committee of the International Headache Society (IHS). The International Classification of Headache Disorders, 3rd edition (beta version). Cephalalgia. 2013;33(9):629-808.
doi: 10.1177/0333102413485658
- Martins HA, Ribas VR, Martins BB, Ribas R de M, Valenca MM. Posttraumatic headache. Arq Neuropsiquiatr. 2009;67(1):43-45.
doi: 0.1590/S0004-282X2009000100011
- Solomon S. Post-traumatic headache: commentary: an overview. Headache. 2009;49(7):1112-1115.
doi: 10.1111/j.1526-4610.2009.01462.x
- Nampiaparampil DE. Prevalence of chronic pain after traumatic brain injury: A systematic review. JAMA. 2008;300(6):711-719.
doi: 10.1001/jama.300.6.711
- Sheftell FD, Tepper SJ, Lay CL, Bigal ME. Post-traumatic headache: Emphasis on chronic types following mild closed head injury. Neurol Sci. 2007;28(S2):203-207.
doi: 10.1007/s10072-007-0777-1
- Yang CC, Hua MS, Tu YK, Huang SJ. Early clinical characteristics of patients with persistent post-concussion symptoms: A prospective study. Brain Inj. 2009;23(4): 299-306.
doi: 10.1080/02699050902788543
- Couch JR, Lipton RB, Stewart WF, Scher AI. Head or neck injury increases the risk of chronic daily headache: A population-based study. Neurology. 2007;69(11):1169-1177.
doi: 10.1212/01.wnl.0000276985.07981.0a
- Obermann M, Nebel K, Schumann C, Holle D, Gizewski ER, Maschke M, Goadsby PJ, Diener H-C, Katsarava Z. Gray matter changes related to chronic posttraumatic headache. Neurology. 2009;73(12):978-983.
doi: 10.1212/WNL.0b013e3181b8791a
- Stovner LJ, Schrader H, Mickeviciene D, Surkiene D, Sand T. Headache after concussion. Eur J Neurol. 2009;16(1):112-120.
doi: 10.1111/j.1468-1331.2008.02363.x
- Lenaerts ME. Post-traumatic headache: from classification challenges to biological underpinnings. Cephalalgia. 2008;28(1):(suppl):12-15.
doi: 10.1111/j.1468-2982.2008.01608.x
- Полунина А.Г., Осиновская Н.А., Гудкова А.Н., Гехт А.Б. Влияние цитофлавина на симптомы астении, эмоциональное состояние и вегетативную регуляцию у пациентов с органическим астеническим расстрой ством. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(2):28-32.
- Скоромец А.А., Пугачева Е.Л. Исследование эффективности комплексного препарата цитофлавин для коррекции последствий легкой черепно-мозговой травмы. Поликлиника.2011;5(1):50-54.
- Суслина З.А., Румянцева C.А., Танашян М.М., Скоромец А.А., Клочева Е.Г., Федин А.И., Коваленко А.Л., Силина А.В., Шоломов И.И. Комплексная энергокоррекция хронической ишемии мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2011;111(3):25-39.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)