Исследование эффективности комплексного препарата цитофлавин для коррекции последствий легкой черепно-мозговой травмы
Статьи
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 3, 2010
Акад. РАМН А.А. Скоромец, Е.Л. Пугачева
Efficacy of the complex drug cytoflavin in the treatment of consequences of mild brain injury
A.A. Skoromets, E.L. Pugacheva
Санкт-Петербургский государственный медицинский институт им. акад. И.П. Павлова
Обследованы 60 амбулаторных больных в возрасте 18—50 лет, перенесших легкую черепно-мозговую травму (сотрясение головного мозга, ушиб головного мозга легкой степени) сроком от 21 до 180 дней до включения в исследование. Пациенты основной группы получали таблетки цитофлавина 425 мг по 2 таблетки 2 раза в день в течение 25 дней, пациенты контрольной группы получали таблетки аминалона 500 мг по 2 таблетки 3 раза в день в течение 25 дней. Для контроля эффективности терапии применялся комплекс нейропсихологических шкал; оценка производилась на 1-й, 30-й, 60-й дни исследования. Доказана эффективность и безопасность применения цитофлавина в режиме монотерапии у пациентов с отдаленными последствиями легкой черепно-мозговой травмы. По сравнению с аминалоном эффект цитофлавина развивается достоверно быстрее, в основной группе отмечена достоверно лучшая динамика по шкалам выраженности болевого синдрома, психоэмоциональных нарушений (тревога, депрессия, астения), качество сна, вегетативной дисфункции, когнитивных нарушений (память, концентрация внимания, скорость переработки информации, продуктивность). На фоне приема цитофлавина по сравнению с аминалоном достоверно уменьшается длительность дополнительного приема анальгетиков и снотворных препаратов. Выявлено последействие препарата: его эффект сохранялся к 60-му дню исследования после 30 дней с момента отмены. Побочные эффекты цитофлавина в виде некоторого подъема артериального давления, диссомнии и абдоминалгии носили кратковременный характер, не требовали дополнительной терапии, отмены или снижения дозировки препарата.
Ключевые слова: легкая черепно-мозговая травма, отдаленные последствия, цитофлавин, аминалон, психоэмоциональные нарушения, когнитивные нарушения.
Sixty outpatients, aged 18—50 years, with mild cranial-brain trauma (brain concussion, mild brain injury), occurred 21—180 days before the enrollment in the study, were examined. Patients of the main group received cytoflavin in dose 425 mg, 2 tablets twice a day during 25 days, patients of the control group received aminalon in dose 500 mg, 2 tablets 3 times a day during 25 days. The therapeutic efficacy was assessed on days 1, 30 and 60 with the battery of neuropsychological scales. The efficacy and safety of cytoflavin in the monotherapy of patients with remote consequences of mild cranial-brain trauma was shown. The effect of cytoflavin was developed significantly more rapidly compared to aminalon. There were positive changes on scales of pain severity, psychoemotional disorders (anxiety, depression, asthenia), sleep quality, autonomic dysfunctions as well as in the performance on neurocognitive tests assessing memory, sustained attention, information processing speed, productivity. The duration of using analgesics and sedatives as add-on drugs was reduced significantly. The drug remained effective till the 60th day after the 30 day withdrawal. Side-effects of cytoflavin (the short-term rise of arterial pressure, insomnia and abdominalgia) did not last long and no additional treatment, withdrawal or reduction of cytoflavin dose was needed.
Key words: mild brain injury, remote consequences, cytoflavin, aminalon, psychoemotional disorders, cognitive disorders.
Эпидемиологические исследования свидетельствуют о чрезвычайно высокой частоте черепно-мозговой травмы (ЧМТ) — до 4 случаев на 1000 населения в год [5, 6, 8] с ее увеличением, по данным ВОЗ, на 2% ежегодно. В России ЧМТ фиксируются не менее чем у 600 000 человек вгод [5, 6, 8].
Частота инвалидизации как исхода острой ЧМТ у взрослых при тяжелых травмах составляет 59,1%, травмах средней тяжести — 5,7%, легких травмах — 0,5%. В последующие 2—9 лет контингент инвалидов пополняется на17,9% за счет инвалидности в результате отдаленных последствий ЧМТ [4, 7, 11].
К последствиям перенесенной ЧМТ относится комплекс неврологических и психических нарушений. У 90% пациентов обнаруживают нервно-психические расстройства через 2—10 лет после травмы. Ряд авторов [3, 4, 6] отмечают, что у перенесших как легкие, так и тяжелые ЧМТ на отдаленном этапе психические нарушения преобладают над неврологическими, определяя социальную дезадаптацию вплоть до инвалидизации. Во многих работах, описывающих нарушения эмоциональной сферы, расстройства интеллектуально-мнестических функций, личности и поведения после ЧМТ, подчеркивается преобладание пограничного спектра нервно-психической патологии у данного контингента больных. Пациенты с последствиями ЧМТ составляют 10% всех больных, наблюдаемых в психоневрологических диспансерах, причем 65% из них — мужчины и только 35% — женщины. Если в острый период травмы больные наблюдаются у нейрохирургов и неврологов стационарно и амбулаторно, то в промежуточный и отдаленный период, когда и развиваются в основном последствия ЧМТ, они зачастую остаются предоставленными самим себе.
Травматическая энцефалопатия — самая распространенная форма психических расстройств в отдаленном периоде травмы головного мозга [4]. Выделяют несколько ее вариантов. Травматическая астения (церебрастения) выражается, в основном, в раздражительности и истощаемости. Больные жалуются на рассеянность, забывчивость, невозможность сосредоточиться, нарушения сна, а также головные боли, головокружения, усиливающиеся при плохой погоде, перемене атмосферного давления. Травматическая апатия проявляется в сочетании повышенной истощаемости с вялостью, заторможенностью, снижением активности. Интересы ограничиваются узким кругом забот о собственном здоровье и необходимых условиях существования. Память обычно нарушена. Посттравматическая головная боль (ПТГБ) — также наиболее частая жалоба больных после травмы головы, как в остром, так и в отдаленном периоде. Нередко именно ГБ становятся причиной инвалидизации этих больных в течение длительного времени. Хронические ПТГБ рассматривают как часть посткоммоционного синдрома (ПКС), включающего также жалобы на быструю утомляемость, нарушение концентрации внимания, снижение работоспособности, нарушение сна, головокружение, раздражительность, тревожность, депрессию и вегетативные расстройства.
Изучение патогенетических механизмов ЧМТ свидетельствует о нарушении функционирования регуляторных систем организма и напряжении адаптационно-компенсаторных процессов.
В остром периоде легкой ЧМТ преобладающее значение имеют цереброваскулярные нарушения и возникающие несоответствия между энергетическими запросами мозга и кровотоком, приводящие к оксидантному стрессу.
В основе патогенеза промежуточного и отдаленного периодов ЧМТ лежат локальные или отдаленные от места поражения деструктивно-дистрофические и репаративно-дегенеративные процессы. При благоприятном течении наступает полное или почти полное клиническое уравновешивание обусловленных ЧМТ патологических сдвигов, при неблагоприятном течении — клиническое проявление запущенных травмой спаечных, рубцовых, атрофических, гемо- и ликвороциркуляторных, вегетовисцеральных, аутоиммунных и других процессов, приводящих к возникновению травматической болезни головного мозга. Отсутствие корреляций между тяжестью травмы и интенсивностью и длительностью цефалгического синдрома указывает на то, что головная боль может быть напрямую не связана со структурным поражением мозга после травмы.
Таким образом, при ЧМТ весьма важно правильно лечить пациентов как в острый период, так и производить коррекцию последствий травмы. Одно из ведущих мест в лечении занимает медикаментозная терапия, направленная на предотвращение гипоксии мозга, улучшение обменных процессов, восстановление активной умственной деятельности, нормализацию эмоциональных и вегетативных проявлений [10].
Этим требованиям отвечает нейропротектор, антигипоксант и антиоксидант цитофлавин [1, 2, 9]. Доказанная в многоцентровых исследованиях эффективность препарата при астенических и эмоциональноволевых расстройствах (снижение уровня тревоги и депрессии), когнитивных нарушениях, ГБ, в том числе мигрени, позволяет сделать предположение о востребованности цитофлавина при терапии последствий ЧМТ, учитывая минимальные и редкие побочные эффекты его применения.
Целью настоящего исследования было изучение эффективности таблетированной формы цитофлавина в сравнении с аминалоном у больных, перенесших легкую ЧМТ, осложнившуюся в восстановительном периоде нарушением когнитивных функций, цефалгическим, астенотревожным или другими синдромами.
Материал и методы
Обследовали 60 амбулаторных больных в возрасте 18—50 лет (средний — 37,8±10,14 года), перенесших легкую ЧМТ (сотрясение головного мозга, ушиб головного мозга легкой степени) сроком от 21 до 180 дней (в среднем — 59,4 дня) до включения в исследование, длительность настоящих жалоб (на ГБ, плохое настроение, плохой сон, снижение работоспособности, внимания, памяти) в среднем составляла 28,08 дня.
Критерием включения в исследование было наличие не менее 2 следующих синдромов — цефалгический, астенический, тревожный, диссомнический, нарушение когнитивных функций — и их связь с перенесенной ЧМТ, что определялось по следующим признакам: тест Спилбергера — значение любой из субшкал от 15 до 50 баллов; самоопросник депрессии CES-D — до 26 баллов; шкала астении — более 50 баллов; вегетативная анкета — более 15 баллов по субъективной субшкале, более 25 баллов по объективной субшкале; шкала качества сна — более 9 баллов; жалобы на ГБ; жалобы на головокружение. Критериями исключения пациентов из исследования были: перенесенная ЧМТ средней и тяжелой степени; любые другие перенесенные или текущие заболевания, сопровождающиеся поражением ЦНС (ишемический и геморрагический инсульты, эпилепсия, рассеянный склероз, болезнь Паркинсона, гидроцефалия, перенесенные острые воспалительные и онкологические заболевания ЦНС); злокачественные новообразования любой локализации; шизофрения, депрессия и другие психические расстройства; поведенческие проблемы, из-за которых выполнение протокола может быть затруднено; злоупотребление или зависимость от алкоголя или других психоактивных веществ; соматические заболевания в стадии декомпенсации (инфаркт миокарда в анамнезе, тяжелые формы ишемической болезни сердца, сердечная, легочная, почечная, печеночная недостаточность, подъемы АД выше 160 мм рт.ст. в анамнезе до травмы); эндокринные заболевания, требующие заместительной или корригирующей терапии; показатели крови — гемоглобин ниже 90 г/л; эритроциты менее 3,51012; лейкоциты менее 3,5-109 и более 10-109; СОЭ более 15 мм/ч; вирусный гепатит B, C, D в активной фазе и стадии хронизации (при наличии измененных биохимических показателей); ВИЧ-инфекция; венерические заболевания в активной фазе; аллергические реакции на любой компонент как основной, так и базисной терапии; беременность и лактация.
Пациенты были разделены на 2 группы. Больные основной группы получали таблетки цитофлавина 425 мг по 2 таблетки 2 раза в день (последний прием не позже 18.00 ч) в течение 25 дней. Пациенты контрольной группы получали таблетки аминалона 500 мг по 2 таблетки 3 раза в день в течение 25 дней. Длительность исследования составила 60 дней.
Диагноз ставился на основании совокупности клинико-лабораторных данных в соответствии с МКБ-10 (рубрики F07.2, T90.5, G44.3). Для нейропсихологического исследования и оценки качества жизни использовались следующие шкалы [12]: памяти Векслера, астении, Спилбергера (оценка реактивной, или ситуационной, и личностной тревожности), самоопросник депрессии CES-D, вегетативная анкета, качество сна, визуальная аналоговая шкала (ВАШ) боли, тест Ландольта, унифицированный опросник качества жизни. Оценка производилась на 1-й, 30-й, 60-й дни исследования, а по ВАШ боли, шкале оценки качества сна и эффективности терапии еще на 10-е и 180-е сутки. Основным критерием клинической оценки терапевтической эффективности препарата явились сроки уменьшения основных симптомов заболевания, приема анальгетиков, снотворных и антидепрессантов, при этом учитывались побочные реакции на препарат.
Ранее получали анальгетики в адекватной дозе более 3 мес 61% пациентов. У 77,8% пациентов, получавших анальгетики, был хороший обезболивающий эффект, но при этом хорошо переносили препарат лишь половина принимавших (51,7%). До начала исследования применяли снотворные 50,2% пациентов, при этом у подавляющего большинства (83,3%) наблюдался хороший седативный эффект, но плохая и удовлетворительная переносимость была почти у половины (42,8 и 35,6% соответственно). Ранее получали стандартную витаминотерапию 81,4% с хорошим эффектом и переносимостью у 90,9% больных, 13,6% ранее получали антидепрессанты с хорошим эффектом (81,65%) и плохой переносимостью (74,15%). Только у 14,75% пациентов не было сопутствующих заболеваний, остальные имели сопутствующие заболевания до ЧМТ: гипертоническая болезнь, вегетососудистая дистония, мигрень, невралгия тройничного нерва, остеохондроз, гастрит или сочетание 2—3 нозологических форм.
Полученные в процессе исследования медико-биологические данные были обработаны с использованием пакета статистических программ SPSS 12RU.
Результаты и обсуждение
Анализ сроков наступления первого эффекта выявил достоверное (p=0,048) уменьшение этого показателя в основной группе пациентов по сравнению с контрольной и составил 7,4±0,83 и 9,7±1,13 дня соответственно. Таким образом, сроки наступления первого эффекта в основной группе пациентов по сравнению с контрольной оказались меньше на 23,7%. Достоверность изменений подтверждается и анализом выживаемости функции Каплана— Мейера, который представлен на рис. 1.
Рис. 1. Сроки наступления первого эффекта терапии в основной и контрольной группах пациентов с ЧМТ.
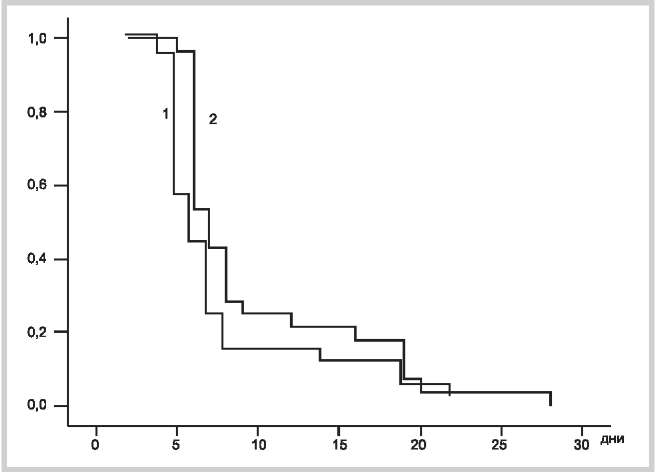
По оси ординат — вероятность наступления первого эффекта при применении цитофлавина (график 1) и аминалона (график 2). По оси абсцисс — срок наступления первого эффекта.
Отмечено достоверное уменьшение длительности приема анальгетиков и снотворных у пациентов, имевших головную боль и/или нарушения сна в основной группе по сравнению с контрольной. Анализ выживаемости функции Каплана—Мейера, по которому также можно судить о длительности приема сопутствующих препаратов (анальгетиков и снотворных), и который подтверждает достоверность вышеуказанных изменений, представлен на рис. 2 и 3. Оценка суточной потребности в анальгетиках показала достоверное (p=0,027) уменьшение сроков применения анальгетиков у пациентов, получавших цитофлавин (8,7±0,65 дня), по сравнению с пациентами, получавшими аминалон (11,4±1 день). Длительность приема анальгетиков в основной группе оказалась на 23,68% ниже по сравнению с контрольной (см. рис. 2).
Рис. 2. Длительность приема анальгетиков в основной (график 1) и контрольной (график 2) группах пациентов с ЧМТ.
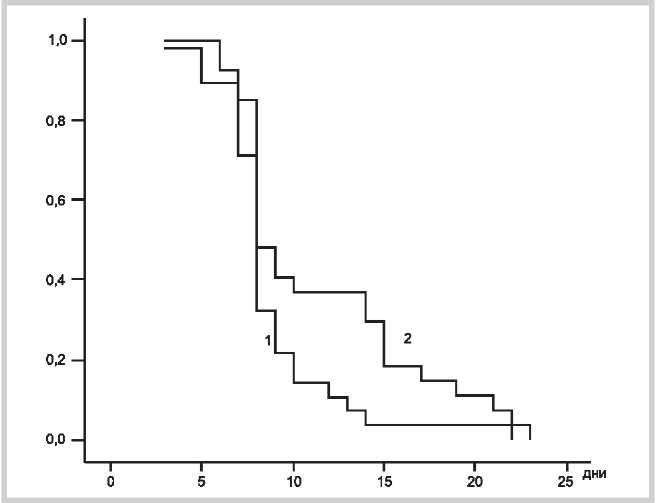
По оси ординат — вероятность прекращения приема анальгетиков. По оси абсцисс — длительность приема анальгетиков.
Рис. 3. Длительность приема снотворных в основной (график 1) и контрольной (график 2) группах пациентов с ЧМТ.
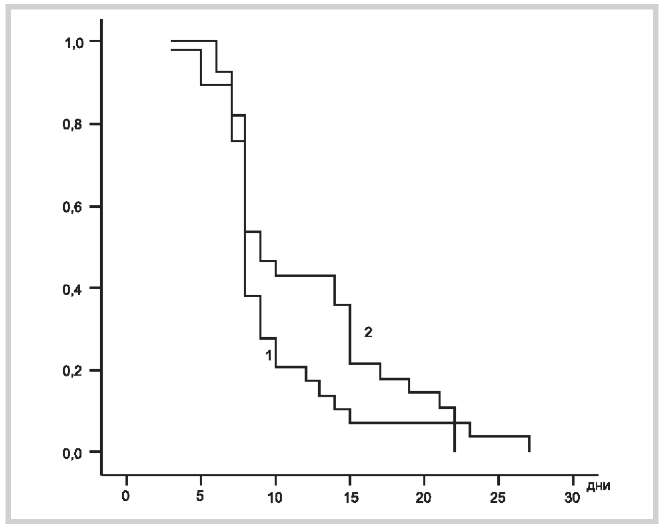
По оси ординат — вероятность прекращения приема снотворных. По оси абсцисс — длительность приема снотворных.
Оценка потребности в снотворных у пациентов с жалобами на диссомнию выявила аналогичные достоверные (p=0,049) изменения и составила 9,4±0,80 дня в основной группе и 12,2±1,12 дня — в контрольной. Длительность приема снотворных в основной группе оказалась на 22,95% ниже по сравнению с контрольной.
Оценка эффективности применения препарата исследователем выявила достоверные отличия (p=0,022, p=0,032) в исследуемой и контрольной группах на 10-й, 30-й, 60-й и 180-й дни исследования. Так, на 10-й день применения улучшение было у 83,9% пациентов, получавших цитофлавин, и только у 53,6%, получавших аминалон. На 30-й день улучшение выявлялось у 83,9% больных в основной группе по сравнению с контрольной группой (71,4%); отсутствовал эффект у 16,1% пациентов, получавших цитофлавин по сравнению с 21,4% пациентов, получавших аминалон. Это положение подтверждается дальнейшей динамикой на 60-й день, являясь эффектом последействия после 30 дней отмены препаратов. На 60-й день процент улучшений составил 57,1 у пациентов, применявших аминалон по сравнению с пациентами, получавшими цитофлавин (74,2%), т.е. оставался на уровне 10-го и 30-го дней приема. Анализ катамнестических данных через 180 дней не дал различий между исследуемыми группами. Анализ эффективности применения препарата самими пациентами также обнаружил аналогичные отличия между группами.
При анализе динамики болевого синдрома, качества сна и качества пробуждения MACOVA — многомерный многофакторный анализ с ковариатами (длительность заболевания и возраст) — все 3 оценки показывали достоверное уменьшение во времени (X Вилкса F1,51=4,242, p=0,045) от визита к визиту в основной и контрольной группах. Эффект препарата особенно значимым оказался при оценке изменений качества сна (F1,51=8,399, p=0,006), в особенности качества пробуждения и уменьшения дневной сонливости. При анализе болевого синдрома, качества сна, пробуждения и бодрствования мужчинами и женщинами оказалось, что достоверно все 3 шкалы оценивались ими по-разному. Женщины всегда оценивали болевой синдром выше. Эта разница сохранялась и в общей оценке болевого синдрома, качества сна и пробуждения от визита к визиту. На результаты оценки боли, качества сна и бодрствования, особенно пробуждения, также оказывал значимое влияние возраст пациента (F1,51=20,089,p<0,0001; F1,51=4,935,p=0,031). Чем старше был пациент, тем больше были данные показатели: более пожилые пациенты оценивают болевой синдром выше, а качество сна и пробуждения хуже. Длительность заболевания также оказывала влияние на результаты оценки боли (F1,51=7,901, p=0,007). Чем дольше длился болевой синдром, тем выше был показатель оценки боли, по-видимому, имела место хроническая боль, возможно, присоединение нейропатической боли и/или снижение антиноцицептивной системы, а также присоединение психоэмоциональных расстройств в виде тревоги и депрессии.
На начальном этапе исследования у пациентов обеих групп были высокие показатели астении, реактивной и личностной тревоги, что, несомненно, снижало показатели качества жизни. При анализе полученных данных было обнаружено, что к концу приема препарата в обеих группах снизились показатели астении, реактивная и личностная тревога, однако степень этих изменений была с высокой долей достоверности существенно больше в группе принимавших цитофлавин. Эти изменения сохранялись в основной группе и после 30-дневной отмены препарата, причем степень астении и реактивной тревоги продолжала уменьшаться. Перед началом исследования уровень депрессии в обеих группах был практически одинаков и составлял 19—20 баллов (умеренно сильная), что также не могло не влиять на уровни интенсивности болевого синдрома, качества сна, бодрствования и качества жизни. К концу лечения показатели депрессии снизились как в основной, так и в контрольной группах, однако степень этих изменений была достоверно выше у пациентов, получавших цитофлавин. К 30-му дню в основной группе депрессия составила 11,1 балла (мягкая степень), а в контрольной — 17,2 балла (мягкоумеренная степень). Подобные изменения стали особенно выражены у пациентов, принимавших цитофлавин на 60-е сутки (7,2 балла), т.е. показатели достигли нормы, а в контрольной группе составили 15,0 баллов, т.е. оставались на границе мягкой и умеренной депресии. На рис. 4 показана степень изменений в эмоциональной сфере в основной и контрольной группах пациентов.
Рис. 4. Степень изменения (в баллах) показателей тревоги и депрессии в основной и контрольной группах пациентов с ЧМТ на 60-й день.
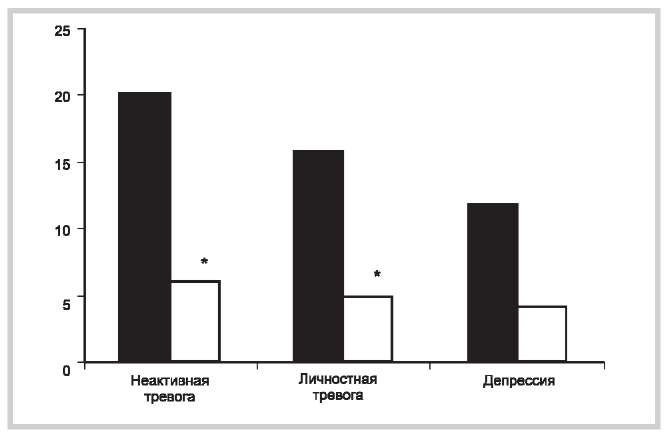
Светлые столбцы — основная группа, темные столбцы — контрольная группа.
* — достоверность различий между основной и контрольной группами на уровне p<0,05.
Уровень вегетативных дисфункций оценивался с помощью анкеты субъективных и объективных нарушений. Средние показатели выраженности вегетативной дисфункции в основной и контрольной группах в начале лечения достоверно не различались и были очень высоки — 47 и 42 балла при норме 25 и 15 баллов соответственно. Однако к концу приема препаратов, особенно к 60-му дню исследования, оба показателя в основной группе стали значительно ниже, а при объективном осмотре достигли нормальных величин (22,2 баллов). Динамика изменений вегетативной дисфункции в основной и контрольной группах показана на рис. 5.
Рис. 5. Динамика изменений (в баллах) показателей вегетативной дисфункции в основной и контрольной группах пациентов с ЧМТ на 60-й день терапии.
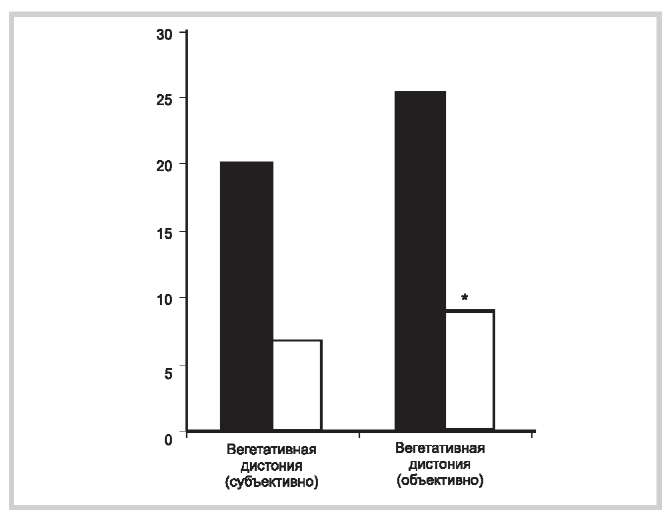
Светлые столбцы — основная группа, темные столбцы — контрольная группа.
* — достоверность различий между основной и контрольной группами на уровне p<0,05.
Аналогичные изменения выявлялись и при оценке гипервентиляционного синдрома.
Что касается когнитивных функций, то необходимо отметить, что все пациенты имели высокий уровень оценки по скрининговой шкале MMSE (29 баллов), а также по соответствующим субтестам шкалы памяти Векслера: 1-й субтест (личные и общественные данные) — 6 баллов (норма); 2-й субтест (ориентировка) — 5 баллов (норма); 3-й субтест (психический контроль) — 7,75 балла при максимальном значении 9 баллов (норма). Снижение последнего показателя происходило в пункте 3 (числовом) в виде случайных ошибок и/или удлинения времени ответа, что скорее говорит о нарушении внимания, а не интеллектуальных функций. Таким образом, исследуемая популяция представляла собой пациентов не с интеллектуально-мнестическими нарушениями, а лишь с нарушениями внимания, быстрой истощаемостью, низкой продуктивностью, что входило в структуру астено-тревожного и астено-депрессивного синдромов. При оценке влияния исследуемых препаратов на логическую, кратковременную, зрительную и ассоциативную память, выявляемых с помощью 4-го, 5-го, 6-го и 7-го субтестов шкалы памяти Векслера, было обнаружено, что все пациенты основной и контрольной групп имели умеренно сниженные показатели по всем субтестам. К концу приема препаратов через 30 дней с высокой степенью достоверности (p=0,004) улучшилась логическая память (до 19—20 баллов) в обеих группах; умеренно-кратковременная память (повторение цифр), что сопровождалось довольно большим разбросом в выборке и говорит скорее об особенностях мышления, образования, профессиональной тренировке, а не об интеллектуально-мнестическом дефекте. К 60-му дню данный уровень показателей сохранялся, но был достоверно выше в группе больных, принимавших цитофлавин (p=0,004). Обнаружено также улучшение результатов зрительной памяти на 30-й и 60-й дни в обеих группах, но динамика изменений в основной группе была достоверно выше (p=0,004). На 30-е сутки уровень ассоциативной памяти был достоверно выше в основной группе (p=0,0035), улучшение происходило в основном за счет сложноассо-циативной памяти и сохранялось достоверно выше на 60-е сутки в основной группе.
Влияние исследуемых препаратов на такие параметры, как концентрация внимания, скорость переработки информации и продуктивность оценивалось с помощью теста Ландольта и имело следующие особенности. Исходно параметры точности — концентрации внимания находились на низком уровне, т.е. менее 0,79 в обеих исследуемых группах, и статистически не отличались, параметры скорости переработки информации обнаруживали средние значения и находились в пределах 0,74—1,19 с довольно большим разбросом значений. На 30-й день исследования достоверно выросли параметры концентрации внимания в обеих исследуемых группах (p=0,005) и скорости переработки в группе пациентов, получавших цитофлавин (p=0,005), тогда как параметры продуктивности имели лишь недостоверную тенденцию к повышению. Однако к 60-му дню параметры продуктивности в основной группе резко возросли и достигли у некоторых пациентов значений выше среднего — до 240,2 (p=0,005) при той же точности.
Переносимость препаратов и выраженность побочных эффектов лечения регистрировались по балльной шкале в регистрационной карте по мере необходимости.
Переносимость обоих препаратов была хорошая — 89—98% и не выявила различий между группами. Основными жалобами были: небольшая тошнота, которая проходила при изменении режима приема препарата (применение после еды); у 3 пациентов были подъемы АД, не требующие отмены или уменьшения дозы, и, возможно, не имеющие прямого отношения к приему препарата; у 7 в начале приема до 10 дней возникали некоторые проблемы с засыпанием, что корригировалось более ранним приемом вечерней дозы препарата (до 18.00 ч).
Таким образом, в ходе настоящего исследования доказана эффективность и безопасность применения цитофлавина в режиме монотерапии у пациентов с отдаленными последствиями легкой ЧМТ. Эффективность цитофлавина сопоставима с применяемым при данной патологии аминалоном и даже превосходит ее.
Цитофлавин в стандартной разрешенной дозировке — 2 таблетки по 425 мг 2 раза в день — может применяться для уменьшения болевых ощущений, обусловленных хронической ПТГБ, головными болями напряжения, абузусными головными болями, а также болевым синдромом в структуре тревожных и депрессивных расстройств у пациентов в отдаленном периоде ЧМТ, создавая предпосылки для метаболической коррекции антиноцицептивной системы. Цитофлавин способен достоверно улучшать качество сна, качество пробуждения и уменьшать дневную сонливость. Применение цитофлавина позволяет снизить дозу или полностью отменить принимаемые анальгетики и снотворные у пациентов с последствиями ЧМТ, что подтверждает нормализующее действие препарата на звенья формирования хронического болевого синдрома и метаболическую коррекцию диссомний. Лечебное действие препарата является стойким, начинается с 10-го дня и сохраняется спустя 150 дней после окончания приема.
Цитофлавин в стандартной разрешенной дозировке способен достоверно уменьшать уровень астении, реактивной и личностной тревоги, депрессии и улучшать качество жизни. Полученная нормализация психоэмоциональной сферы сохраняется по прошествии 30 дней с момента отмены препарата. Последействие препарата очень важно для рекомендаций по кратности его применения и несет экономическую выгоду.
Цитофлавин способен достоверно уменьшать выраженность вегетативных дисфункций, оцениваемых как объективно с последействием до 60 дней, так и субъективно пациентами.
Выявлено достоверное положительное влияние цитофлавина на когнитивные функции (логическую, кратковременную, зрительную, ассоциативную память, концентрацию внимания, скорость переработки информации, продуктивность) с высокой степенью достоверности сохраняющееся до 60 дней.
Механизмы реализации психокорригирующего, вегетокорригирующего, когнитивнокорригирующего эффектов цитофлавина, лежащих в основе улучшения качества жизни, связаны с основными путями синтеза ГАМК с учетом эффекта Вэлша (компартментализация метаболизма глутамата, глутамина и ГАМК). Обеспечение цитофлавином энергетического баланса ткани с помощью сукцинатдегидрогеназной реакции, а также поддержание таких необходимых реакций, как глутаматдегидрогеназная и трансаминазная, регулирует такие процессы, как проведение нервных импульсов, поддержание пространственной ориентации и конформации структурных единиц нейрона, образование синаптических структур, функционирование синапсов, нейрональная память, трансмембранный перенос субстратов, нейромедиаторов, аксональный и ретроградный ток [2, 9].
Цитофлавин в стандартной разрешенной дозировке при монотерапии у пациентов с последствиями легкой ЧМТ выявил хорошую переносимость. Побочные эффекты в виде кратковременного подъема артериального давления, диссомнии и абдоминалгии носили кратковременный характер, не требовали дополнительной терапии, отмены или снижения дозировки препарата. Коррекция производилась изменением режима приема (прием препарата после еды при абдоминалгии и до 18 ч при диссомнии).
Высокая эффективность, удобство применения и хорошая переносимость позволяют рекомендовать цитофлавин в таблетированной форме в виде монотерапии для ведения пациентов с последствиями легкой ЧМТ с цефалгическим, диссомническим, умеренным тревожным и/или депрессивным синдромами, а также начальными нарушениями в когнитивной сфере.
ЛИТЕРАТУРА
1. Агафьина А., Коваленко А.Л. и др. Эффективность нейрометаболического протектора Цитофлавина у больных, перенесших ишемический инсульт, в раннем восстановительном периоде. Врач 2006;1.
2. Афанасьев В.В. Цитофлавин в интенсивной терапии. Ст-Петербург 2007.
3. Вейн А.М. Заболевания вегетативной нервной системы. М: Медицина 1991.
4. Даминов В.Д., Германович В.В. Применение глиатилина в комплексном лечении больных, перенесших черепно-мозговую травму. Фар-матека 2007;15.
5. Лихтерман Л.Б. Черепно-мозговая травма. Мед газета 2000;16:12—13.
6. Макаров А.Ю. Последствия черепно-мозговой травмы и их классификация. Неврол журн 2001;2.
7. Одинак М.М., Вознюк И.А. Применение глиатилина при острой черепно-мозговой травме. Военно-мед журн 2000;32.
8. Путилина М.В., Радишевский М.В. Оптимизация программы реабилитации пациентов с черепно-мозговыми травмами. Рус мед журн 2005;13:22.
9. Романцова М.Г., Коваленко А.Л. Реамберин в клинической практике (исследования, проведенные в 2005—2007 гг.). Ст-Петербург 2007.
10. Слизкова Ю.Б. Исследование эффективности препарата луцетам при сосудистых заболеваниях и посттравматических поражениях ЦНС. Новые лекарственные препараты 2004;3.
11. Чикина Е.С., Левин В.В. Черепно-мозговые травмы: применение современных ноотропных препаратов в острый период и при лечении посттравматической энцефалопатии. Рус врач 2005;11.
12. Белова А.Н., Щепетова О.Н. (ред.). Шкалы, тесты и опросники в медицинской реабилитации. М 2002;71—93.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)