Эффективность применения Цитофлавина в комплексной терапии пациентов с COVID-19
Статьи
Е.В Екушева1,2, В.Б. Войтенков1,3, О.А. Ризаханова4
1Академия постдипломного образования ФГБУ «Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий Федерального медико-биологического агентства», Москва, Россия;
2ФГАОУ ВО «Белгородский государственный национальный исследовательский университет», Белгород, Россия;
3ФГБУ «Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства», Санкт-Петербург, Россия
4ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия
Резюме
Цель исследования. Изучение эффективности терапии, включающей последовательное курсовое назначение препарата Цитофлавин, на динамику неврологического и соматического статуса пациентов с COVID-19.
Материал и методы. Наблюдали 47 пациентов с COVID-19, поступивших в стационар в состоянии средней тяжести согласно критериям Временных методических рекомендаций Минздрава России по профилактике, диагностике и лечению COVID, (19, версия 9 от 26.10.20). Применяли клинико-неврологическое исследование, лабораторные и инструментальные методы обследования до и после курса проводимой терапии.
Результаты. При применении у пациентов с COVID-19 последовательной схемы назначения Цитофлавина наряду со стандартной терапией наблюдается достоверное улучшение неврологического и общего статуса, а также значимая положительная динамика результатов лабораторных и инструментальных методов исследования (маркеров системной воспалительной реакции, нарушений гемостаза и оксигенации), что свидетельствует о значимом влиянии Цитофлавина на процессы воспаления и гиперкоагуляции при COVID-19.
Заключение. Применение препарата Цитофлавин в комплексной терапии пациентов с COVID-19 является патогенетически обоснованным и целесообразным. Полученные данные позволяют рекомендовать включение препарата Цитофлавин в протоколы лечения пациентов с COVID-19 для оптимизации терапии и улучшения исходов заболевания, как и более длительное применение Цитофлавина и повторные курсы его использования у пациентов с COVID-19.
Ключевые слова: коронавирусная инфекция, COVID-19, реабилитация, Цитофлавин, восстановление после COVID-19.
Для цитирования: Екушева, В. Е. Эффективность применения Цитофлавина в комплексной терапии пациентов с COVID-19 / В. Е. Екушева, В. Б. Войтенков, О. А. Ризаханова // Журнал неврологии и психиатрии им. C.C. Корсакова. – 2021. – Т. 121. – № 12. – С. 33-39. – DOI 10.17116/jnevro202112112133. – EDN LDNTOY.
The effectiveness of cytoflavin in complex therapy of patients with the coronavirus infection COVID-19
E.V. Ekusheva1,2, V.B. Voitenkov1,3, O.A. Rizakhanova4
1Federal Research and Clinical Centre for Specialized Medical Care and Medical Technologies, Moscow, Russia;
2Belgorod State National Research University, Belgorod, Russia;
3Pediatric Research and Clinical Center for Infectious Diseases, St. Petersburg, Russia;
4Mechnikov North-Western State Medical University, St. Petersburg, Russia
Abstract
Objective. To study therapy, including a sequential course of the drug Cytoflavin, on the dynamics of neurological and general status in patients with new coronavirus infection COVID-19.
Material and methods. 47 patients with a new coronavirus infection COVID-19, admitted to the hospital and having a state of moderate severity, according to the criteria of the Interim Guidelines of the Ministry of Health of the Russia for the prevention, diagnosis and treatment of a new coronavirus infection (COVID-19, version 9 of 10.26.2020). Clinical and neurological research, laboratory and instrumental examination methods were used before and after the course of therapy.
Results. When a sequential Cytoflavin regimen is used in patients with COVID-19 infection, along with standard therapy, a significant improvement in neurological and general status is observed, as well as a significant positive dynamics in the results of laboratory and instrumental research methods (markers of a systemic inflammatory response, hemostasis and oxygenation disorders), which indicates on the influence of the significant effect of Cytoflavin on the processes of inflammation and hypercoagulability in COVID-19 infection.
Conclusion. The use of the drug Cytoflavin in the complex therapy of patients with COVID-19 infection is pathogenetically justified and expedient. The data obtained make it possible to recommend the inclusion of Cytoflavin in the treatment protocols for patients with COVID-19 coronavirus infection to optimize therapy and improve the course and outcome of the disease, as well as a longer use of Cytoflavin and repeated courses of its use in patients with COVID-19 infection.
Keywords: coronavirus infection, COVID-19, rehabilitation, Cytoflavin, recovery from COVID-19.
Несмотря на то что структуры центральной нервной системы (ЦНС) хорошо защищены от большинства инфекционных возбудителей, в том числе вирусных, гематоэнцефалическим и гематоликворным барьерами, предотвращающими проникновение вирусов в цереброспинальную жидкость и нейроны, а также микроглией, обеспечивающей иммунную защиту нервной системы [1], семейство коронавирусов хорошо известно нейротропностью и нейроинвазивностью или способностью проникать в клетки ЦНС. В частности, при контактном, воздушно-капельном заражении коронавирусы, внедрившись в эпителиальные клетках полости носа и носоглотки, размножаясь в них, способны мигрировать по аксонам терминальных ветвей блуждающего и краниальных нервов ретроградно, антероградно и транссинаптически [2—4]. Поражение нервной системы при коронавирусной инфекции связано с прямым избирательным воздействием вируса SARS-CoV-2 на черепные нервы и ткань головного мозга, чему способствует выработка вирусом нейротоксинов, активация медиаторов воспаления и вторичное повреждение ЦНС вследствие острого или подострого аутоиммунного процесса, а также с внедрением коронавируса в ткань ЦНС через эндотелий церебральных сосудов [5].
Симптомы поражения нервной системы могут предшествовать инфекционным проявлениям, возникать одновременно или развиваться на фоне дыхательной и/или сердечно-сосудистой недостаточности [6], вместе с тем описан широкий спектр неврологических проявлений у пациентов, перенесших инфекцию COVID-19, возникающих в подостром периоде или после острого периода заболевания — постковидным синдром (ПКС) [7—9]. Среди наиболее частых проявлений ПКС можно выделить астенические, когнитивные и вегетативные нарушения.
Астенический синдром является одним из наиболее частых среди длительно существующих симптомокомплексов у пациентов, перенесших COVID-19 [10, 11], нередко наблюдаясь в течение >100 дней после первоначального инфицирования [12]. Как у пациентов трудоспособного возраста (39±15 лет) со среднетяжелым течением COVID-19, так и у пожилых больных астенический синдром может возникать уже в дебюте заболевания в одинаковом проценте случаев — 63,3 [12, 13]. У 1/2 пациентов моложе 70 лет астенические проявления отмечаются через 1 мес от начала заболевания, у 40% — через 2 мес [14]. Особенно тяжелая и выраженная астения наблюдается у 55% больных старше 70 лет, перенесших COVID-19 [15].
Когнитивные нарушения (КН) наряду с быстрой утомляемостью или общей слабостью относятся к частым проявлениям ПКС. По данным онлайн-опроса 4182 пациентов, перенесших COVID-19, 85,1% исследуемых имели КН, описывая их как «туман в голове» [9]. При подробном анализе КН выявлено, что чаще всего у больных наблюдались снижение концентрации внимания (74,8%), трудности при выполнении интеллектуальной работы (64,9%), нарушение управляющих функций (57,6%), проблемы в принятии решений (54,1%) и замедленность мышления (49,1%) [9]. Нарушение внимания является одним из пяти наиболее частых проявлений перенесенного COVID-19, отмечаясь почти у 1/2 (44%) пациентов [16]. Анализ данных 431 051 больных, перенесших COVID-19, из Биобанка Великобритании обнаружил, что только один фактор инфицирования COVID-19 является статистически значимым для последующего развития КН [17], при этом механизмы и патогенетические процессы данных расстройств не до конца понятны.
Показано, что коронавирус может также поражать вегетативную нервную систему [18, 19]. Вегетативные нарушения после перенесенного COVID-19, обусловленные недостаточностью или избыточной активностью симпатических или парасимпатических систем, на сегодняшний день недостаточно изучены, вместе с тем наблюдается широкий спектр их проявлений, представленность которых составляет от 2,5 до 26% случаев [9, 20]. В частности, в периоде реконвалесценции у 26% пациентов наблюдается нарушение потоотделения [9]. У больных, перенесших COVID-19, отмечается сочетанное возникновение гипергидроза и постуральной ортостатической тахикардии с устойчивым увеличением частоты сердечных сокращений ≥30 ударов в 1 мин в течение 10 мин после нахождения в вертикальном положении [21]. Среди нарушений ритма сердца, связанных с вегетативными нарушениями вследствие COVID-19, выделяют синусовую тахикардию и другие наджелудочковые тахикардии [12, 13, 22—24], а также устойчивое повышение артериального давления в периоде реконвалесценции [25].
Накопленные данные обсервационных исследований, описывающих последствия инфекции COVID-19, послужили основанием для включения ПКС в Международную классификацию болезней 10-го пересмотра [26], представляя раздел под кодом U09.9 — «Состояние после COVID-19 неуточненное», включающее в себя также ПКС. Лечение пациентов с COVID-19 проводится в соответствии с национальными клиническими рекомендациями, учитывающими особенности течения заболевания [27], при этом в настоящее время не существует каких-либо алгоритмов или рекомендаций, основанных на принципах доказательной медицины, по лечению неврологических нарушений у этой категории больных. Поэтому терапия пациентов с ПКС осуществляется исходя из имеющегося клинического опыта и данных клинических исследований лечения больных с широким спектром расстройств вследствие различных неврологических заболеваний.
С целью коррекции КН и устранения астенических проявлений инфекции COVID-19 оправданный интерес представляет препарат Цитофлавин (ООО «НТФФ ПОЛИСАН», Россия, Санкт-Петербург) — комбинированное нейропротективное лекарственное средство, состоящее из янтарной кислоты, никотинамида, инозина и рибофлавина, неоднократно показавшее эффективность и безопасность в большом количестве исследований (пилотных, многоцентровых рандомизированных, плацебо-контролируемых) при острой и хронической неврологической патологии, что дает основание широко применять Цитофлавин в клинической практике в нашей стране и за рубежом. Известны такие клинические эффекты данного препарата, как положительное влияние на когнитивные функции (концентрация внимания, качество кратко- и долговременной памяти), биоэлектрическую активность головного мозга и качество жизни пациентов [28], антиоксидантный и противоастенический эффекты, позволяющие значимо снизить выраженность постинфекционных расстройств [29, 30], а также саногенетическое влияние на функциональное состояние ЦНС [31, 32].
Цель исследования — изучение эффективности терапии, включающей последовательное курсовое назначение препарата Цитофлавин, на динамику неврологического и соматического статуса пациентов с COVID-19.
Материал и методы
В открытом рандомизированном сравнительном клиническом (в условиях стационара и на амбулаторном этапе) исследовании приняли участие 47 пациентов с лабораторно подтвержденным COVID-19 в состоянии средней тяжести согласно критериям Временных методических рекомендаций Минздрава России по профилактике, диагностике и лечению новой коронавирусной инфекции [33].
Критерии включения в исследование: возраст от 25 до 65 лет, лабораторно подтвержденный COVID-19, начало курса терапии в условиях стационара, среднетяжелое течение заболевания и подписанное информированное согласие на участие в данном исследовании.
Критерии невключения в исследование: повышенная чувствительность или индивидуальная непереносимость Цитофлавина или одного из составляющих его активных веществ, прием других сукцинат-содержащих лекарственных средств в течение последних 2 нед, тяжелое или крайне тяжелое течение COVID-19, в том числе острый респираторный дистресс-синдром, острая дыхательная недостаточность с необходимостью респираторной поддержки или нестабильная гемодинамика, психические, онкологические, декомпенсированные или нестабильные соматические болезни или иные состояния, угрожающие жизни или ухудшающие прогноз пациента, алкоголизм, наркомания, беременность, период грудного вскармливания, неспособность пациентов следовать инструкциям врача, ориентироваться в целях исследования и принимать рекомендуемую терапию.
Для объективизации степени выраженности неврологических симптомов использовали шкалу субъективной оценки астении MFI-20 (англ.: Multidimensional Fatigue Inventory-20), скрининговый тест для выявления КН Mini-Cog и опросник оценки вегетативных изменений А.М. Вейна (ОВИ), шкалу общего клинического впечатления CGI (англ.: Clinical Global Impression) оценки тяжести болезни (CGI-S) и общего улучшения (CGI-I). Для оценки выраженности и анализа динамики патологических процессов, сопровождающих инфекционное заболевание, выполняли лабораторные и инструментальные методы исследования (клинический и биохимический анализы крови, гемостазиограмму и пульсоксиметрию).
Все пациенты с COVID-19, включенные в исследование, были рандомизированы на две группы методом случайных конвертов. Больные основной группы (ОГ, n=27) получали стандартную необходимую терапию в соответствии с актуальными рекомендациями Минздрава России по профилактике, диагностике и лечению COVID-19 [33] вместе с последовательным приемом Цитофлавина: внутривенно капельно в дозе 20 мл/сут в разведении в 200 мл 0,9% раствора натрия хлорида 1 раз в день в первой половине дня в течение 10 дней с последующим пероральным приемом препарата по 2 таблетки 2 раза в день за 30 мин до еды (последний прием не позднее 18.00 ч) в течение 25 дней. Пациенты группы сравнения (ГС, n=20) получали только стандартную терапию [30]. Оценка состояния пациентов, проведение клинико-неврологического исследования с использованием объективизирующих шкал, опросников и лабораторно-инструментального обследования проводилась непосредственно перед началом исследования (1-й визит), через 5 дней (2й визит) и через 30 дней (3-й визит) от начала исследования.
Работа выполнена в соответствии с этическими нормами Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы проведения научных медицинских исследований с участием человека» с поправками 2013 г. и «Правилами клинической практики в Российской Федерации», утвержденными Приказом Минздрава России №266 от 19.06.03. Протокол исследования одобрен локальным этическим комитетом Академии постдипломного образования ФГБУ «ФНКЦ ФМБА России» (№12 от 19.11.20). Расчет групп проведен с учетом пилотного характера исследования и ожидаемого результата, был выбран максимально возможный в условиях планирования объем пациентов (n=47).
Обработка результатов исследования выполнялась в среде IBM SPSS v. 23. В соответствии с поставленными вопросами использовали метод MANOVA в режиме общей линейной модели с повторными измерениями, в качестве многомерного и наиболее устойчивого критерия выбран след Пиллая (V). Для уточнения влияния значимых эффектов различных факторов и/или ковариатов применялся метод ANOVA и анализ трендов. Величина эффекта оценивалась по проценту объясненной дисперсии (п2). Анализ ANOVA повторных измерений проводился при необходимости с поправками на отсутствие сферичности (поправки Гринхауза—Гайссера и Хайн—Фельдта по результатам оценки критериев Моучли и Эпсилон). При выявлении значимых эффектов уточнение конкретных межгрупповых различий осуществлялось при помощи парного t-критерия Стьюдента (в модификации Уэлча при неравенстве дисперсий по критерию Левене). Поиск различий у пациентов по данным трех визитов проведен при помощи критерия Тьюки (или Геймса—Хоуэлла при неравенстве дисперсий по критерию Левене). Уровень значимости, при котором отвергалась нулевая гипотеза, выбран p<0,05; при значении 0,05≤p≤0,1 говорилось о статистической тенденции. С учетом того, что в основе MANOVA лежат операции с выборочными средними, описание данных и их дисперсии рекомендуется делать в виде: M (95%ДИ—; 95%ДИ+), где M — выборочное среднее, в скобках — нижняя и верхняя границы доверительного интервала.
Результаты
Анализ общего и неврологического статуса у пациентов с COVID-19 по результатам применения анализа ANOVA между двумя группами продемонстрировал значимые различия по шкалам CGI-S (субшкала тяжести состояния: F=8,89; p=0,002; η2=0,169) и ОВИ (F=11,19; p<0,001; η2=0,199), причем наиболее существенные отличия обнаружены по результатам парных сравнений по указанным шкалам на 3-м визите, т.е. после окончания курса терапии (по шкале CGI — t=3,50; d.f.=43,50; p=0,001 и по ОВИ — t=4,10; d.f.=29,08; p<0,001) (табл. 1, рис. 1, 2). Следует отметить, что в ОГ наблюдалась значимая положительная динамика показателей шкал CGI (CGI-S и CGI-I) и ОВИ после окончания лечения по сравнению с первыми двумя визитами (перед началом лечения и на 5-й день терапии). Аналогичной динамики не наблюдалось у больных ГС. Обращало на себя внимание, что разнообразные вегетативные нарушения в обеих группах были наиболее выражены на 5-й день терапии по сравнению с исходными показателями (см. табл. 1).
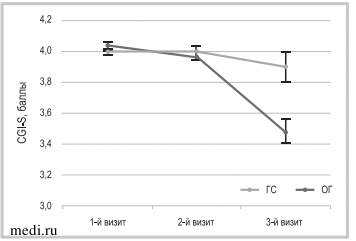 Рис. 1.
Рис. 1. Динамика показателей по шкале CGI-5.
Fig. 1. Dynamics of indicators on the CGI-S scale.
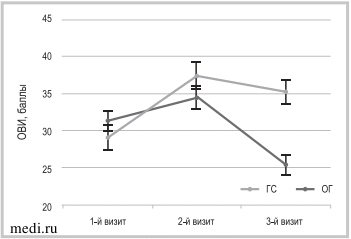 Рис. 2.
Рис. 2. Динамика показателей по шкале ОВИ.
Fig. 2. Dynamics of indicators on the ОВИ scale.
Таблица 1.
Динамика показателей по шкалам CGI и ОВИ у обследованных больных, баллы, M (95% ДИ-; 95% ДИ+)
Table 1.
Dynamics of indicators on the CGI and OVI scales in the examined patients, points, M (95% CI-; 95% CI+)
| Шкала |
Визит |
ОГ (n=20) |
ГС (n=20) |
| CGI |
1 |
4,04 (3,98; 4,09) |
4 (3,93; 4,07) |
|
|
2 |
3,96 (3,91; 4,02) |
4 (3,93; 4,07) |
|
|
3 |
3,48 (3,31; 3,65) |
3,9 (3,7; 4,1) |
| ОВИ |
1 |
31,37 (28,36; 34,38) |
29,05 (25,55; 32,55) |
|
|
2 |
34,52 (31,28; 37,76) |
37,4 (33,64; 41,16) |
|
|
3 |
25,37 (22,4; 28,34)* |
35,3 (31,85; 38,75)* |
Примечание. * — статистически значимые различия между группами,p<0,05.
Note. * — statistically significant differences between the groups, p<0.05.
У пациентов ОГ наблюдалось существенное уменьшение выраженности астенических проявлений после окончания курса терапии по сравнению с исходным уровнем по шкале MFI-20 (t=7,54; d.f.=45; p<0,001), значимо отличающееся от результатов в ГС (межгрупповые различия — t=7,54; d.f.=45; p<0,001 согласно анализу MANOVA, значимые достоверные изменения в ОГ — Z=—4,56; p<0,001).
Статистический анализ полученных данных продемонстрировал значимые различия показателя сатурации в ОГ по сравнению с ГС (F=4,03; p=0,027; η2=0,086) (табл. 2).
Таблица 2.
Динамика показателей пульсоксиметрии обследованных больных, %, M (95% ДИ-; 95% ДИ+)
Table 2.
Dynamics of pulseoximetry indicators of examined patients, %, M (95% CI-; 95% CI+)
| Группа |
Результаты пульсоксиметрии |
| 1-й визит |
2-й визит |
3-й визит |
| ОГ |
95,24 |
96,30 |
97,43 |
|
|
(94,89; 95,6) |
(95,61; 96,98) |
(96,96; 97,89) |
| ГС |
94,89 |
96,78 |
96,39 |
|
|
(94,45; 95,32) |
(95,94; 97,62) |
(95,82; 96,96) |
Согласно данным анализа ANOVA, были выявлены значимые различия показателей международного нормализованного отношения (МНО), протромбинового времени (ПТВ), концентрации D-димера и фибриногена у пациентов ОГ и ГС (табл. 3, рис. 3—7). Важно отметить, что наибольшие изменения наблюдались у пациентов ОГ в отношении показателя фибриногена (на 35,6%), что в 2—4 раза больше, чем остальных показателей (табл. 4). Таким образом, с учетом анализа однонаправленной положительной динамики анализируемых маркеров воспаления можно заключить, что применение Цитофлавина у пациентов с COVID-19 имеет значимое влияние на процессы системного воспаления.
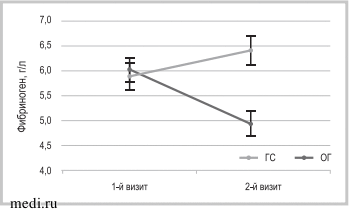 Рис. 3.
Рис. 3. Динамика концентрации в крови фибриногена.
Fig. 3. Dynamics of fibrinogen concentration in blood.
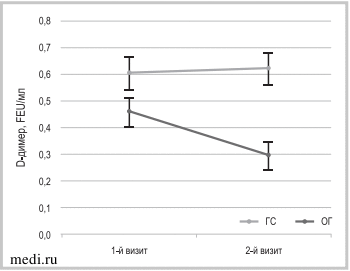 Рис. 4.
Рис. 4. Динамика концентрации в крови D-димера.
Fig. 4. Dynamics of D-dimer concentration in blood.
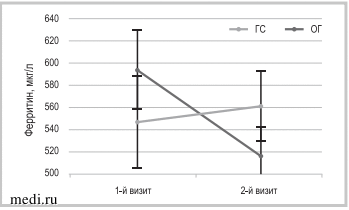 Рис. 5.
Рис. 5. Динамика концентрации в крови ферритина.
Fig. 5. Dynamics of ferritin concentration in blood.
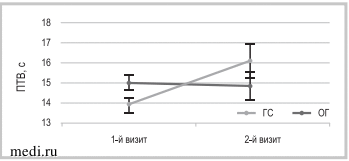 Рис. 6.
Рис. 6. Динамика значений протромбинового времени.
Fig. 6. Dynamics of prothrombin time values.
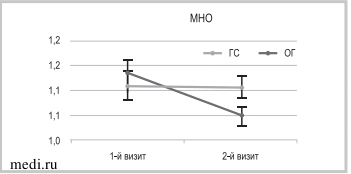 Рис. 7.
Рис. 7. Динамика значений МНО.
Fig. 7. Dynamics of INR values.
Таблица 3.
Динамика лабораторных показателей у наблюдавшихся больных, M (95% ДИ-; 95% ДИ+)
Table 3.
Dynamics of laboratory parameters in observed patients, M (95% CI-; 95% CI+)
| Шкала |
Визит |
ОГ |
ГС |
| МНО |
1-й |
1,14 (1,08; 1,19) |
1,11 (1,05; 1,17) |
|
|
2-й |
1,05 (1,01; 1,09)* |
1,11 (1,06; 1,15)* |
| D-димер, нг/мл |
1-й |
0,46 (0,35; 0,57) |
0,61 (0,48; 0,74) |
|
|
2-й |
0,3 (0,19; 0,41)* |
0,62 (0,5; 0,75)* |
| ПТВ, с |
1-й |
15,05 (14,32; 15,78) |
13,92 (13,07; 14,77) |
|
|
2-й |
14,87 (13,37; 16,37)* |
16,14 (14,39; 17,88)* |
| Фибриноген, г/л |
1-й |
6,02 (5,52; 6,51) |
5,89 (5,32; 6,46) |
|
|
2-й |
4,93 (4,41; 5,46)* |
6,4 (5,79; 7,02)* |
Примечание. * — статистически значимые различия между группами, p<0,05.
Note. * — statistically significant differences between the groups, p<0.05.
Таблица 4.
Статистическая значимость динамики лабораторных показателей у наблюдавшихся больных
Table 4.
Statistical significance of the dynamics of laboratory parameters in the observed patients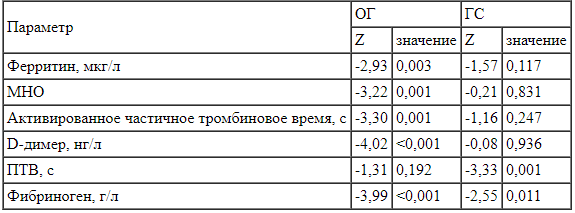 Важно отметить, что все пациенты хорошо переносили комплексную терапию, включающую парентеральный и пероральный прием Цитофлавина. Серьезных или значимых нежелательных явлений выявлено не было.
Важно отметить, что все пациенты хорошо переносили комплексную терапию, включающую парентеральный и пероральный прием Цитофлавина. Серьезных или значимых нежелательных явлений выявлено не было.
Заключение
Проведенное исследование показало, что использование у пациентов с COVID-19 с первых дней заболевания последовательной схемы применения Цитофлавина (парентеральный и пероральный этапы) в схеме стандартной терапии способствует достоверному улучшению динамики неврологического и общего статуса (уменьшение выраженности астенических, вегетативных нарушений и повседневной активности). Эти клинические данные сочетаются со значимой положительной динамикой результатов лабораторных методов исследования (маркеров системной воспалительной реакции, нарушений гемостаза и оксигенации), что свидетельствует о значимом влиянии Цитофлавина на процессы воспаления и гиперкоагуляции при COVID-19.
Полученные данные, вероятно, связаны широким спектром входящих в состав Цитофлавина компонентов, играющих важную роль в регуляции метаболических и энергопродуцирующих процессов [34]. Янтарная кислота является эндогенным внутриклеточным метаболитом цикла Кребса, участвующим в энергосинтезирующих процессах, в частности она стимулирует аэробный гликолиз и синтез АТФ в клетках и улучшает тканевое дыхание за счет активации транспорта электронов в митохондриях. Никотинамид (витамин PP) также активирует клеточное дыхание, стимулирует синтез АТФ и уменьшает выработку IL-2, -5, -6, ФНО-а, оказывая противовоспалительное действие [35]. Последние годы обсуждается важная роль никотинамида в формировании и поддержании иммунитета организма, в том числе при коронавирус-ной инфекции [36—39]. Инозин, являющийся производным пурина — предшественника АТФ, стимулирует синтез ключевых ферментов-нуклеотидов — ФАД и НАД, подавляет продукцию воспалительных цитокинов посредством посттранскрипционного механизма и последующих сигнальных реакций, защищает от шока, обусловленного эндотоксинами, оказывает противовоспалительное и иммуномодулирующее действие [40, 41]. Рибофлавин активирует сукцинатдегидрогеназу и другие окислительно-восстановительные реакции цикла Кребса. Кроме того, поскольку сукцинат активно участвует в ресинтезе эндогенной гамма-аминомасляной кислоты в нервных клетках через а-кетоглютаровую кислоту и янтарный полуальдегид, то в совокупности с рибоксином и никотинамидом это свойство янтарной кислоты расширяет возможности применения Цитофлавина в качестве неконкурентного антагониста NMDA-рецепторов и является предпосылкой для назначения Цитофлавина для лечения не только острых состояний, но и хронических заболеваний, в основе которых лежат процессы эксайтотоксичности [34].
Таким образом, в условиях коронавирусной инфекции, характеризующейся выраженным патологическим повышением перекисного окисления липидов, эндотелиальной дисфункцией и нарушением клеточного дыхания с энергодефицитом [4, 5, 9], применение Цитофлавина патогенетически обосновано. В связи с этим целесообразно включение Цитофлавина с последовательным курсом в схемы и протоколы лечения пациентов с новой коронавирусной инфекцией COVID-19 для оптимизации терапии и улучшения течения и исходов заболевания, кроме того, обосновано более длительное применение Цитофлавина и его повторные курсы у пациентов, перенесших COVID-19.
Авторы заявляют об отсутствии конфликта интересов.
Authors declare no conflict of interests.
ЛИТЕРАТУРА/REFERENCES
1. Desforges M, Coupanec AL, Dubeau P, et al. Human coronaviruses and other respiratory viruses: underestimated opportunistic pathogens of the central nervous system? Viruses. 2019;12(1):14-20.
2. Buzhdygan TP, DeOre BJ, Baldwin-Leclair A, et al. The SARS-CoV-2 spike protein alters barrier function in 2D static and 3D microfluidic in-vitro models of the human blood — brain barrier. Neurobiology of Diseases. 2020;146:105131.
3. Mori I. Transolfactory neuroinvasion by viruses threatens the human brain. Acta Virologica. 2015;59:338-349.
4. Singh AK, Bhushan B, Maurya A, et al. Novel coronavirus disease 2019 (COVID-19) and neurodegenerative disorders. Dermatologic Therapy. 2020;33(4):13591.
5. Yuki K, Fujiogi M, Koutsogiannaki S. COVID-19 pathophysiology: a review. Clinical Immunology. 2020;215:108427.
6. Белопасов В.В., Яшу Я., Самойлова Е.М., Баклаушев В.П. Поражение нервной системы при COVID-19. Клиническая практика. 2020;11(2) 60-80. Belopasov VV, Yachou Y, Samoilova EM, Baklaushev VP. The nervous system damage in COVID-19. Klinicheskaya Praktika. 2020;11(2):60-80. (In Russ.).
7. Iqbal FM, Lam K, Sounderajah V, Clarke JM, et al. Characteristics and predictors of acute and chronic post-COVID syndrome: a systematic review and meta-analysis. EClinical Medicine. 2021;36:100899.
8. Jacobson KB, Rao M, Bonilla H, et al. Patients with uncomplicated COVID-19 have long-term persistent symptoms and functional impairment similar to patients with severe COVID-19: a cautionary tale during a global pandemic. Clinical Infectious Diseases. 2021;73(3):826-829.
9. Sudre CH, Murray B, Varsavsky T, et al. Attributes and predictors of long COVID. Nature Medicine. 2021;27(4):626-631.
10. Lopez-Leon S, Wegman-Ostrosky T, Perelman C, et al. More than 50 Longterm effects of COVID-19: a systematic review and meta-analysis. MedRx-iv. 2021: 2021.01.27.21250617.
11. Townsend L, Dyer AH, Jones K, et al. Persistent fatigue following SARS-CoV-2 infection is common and independent of severity of initial infection. PLoS One. 2020;15(11):e0240784.
12. Desai AD, Boursiquot BC, Melki L, Wan EY. Management of arrhythmias associated with COVID-19. Current Cardiology Reports. 2020;23(1):2.
13. Kanjwal K, Jamal S, Kichloo A, Grubb BP. New-onset postural orthostatic tachycardia syndrome following coronavirus disease 2019 infection. The Journal of Innovation in Cardiac Rhythm Management. 2020;11(11):4302-4304.
14. Carvalho-Schneider C, Laurent E, Lemaignen A, et al. Follow-up of adults with non-critical COVID-19 two months after symptoms’ onset. Clinical Microbiol and Infection. 2021;27(2):258-263.
15. Annweiler C, Sacco G, Salles N, et al. National French survey of Coronavirus disease (COVID-19) symptoms in people aged 70 and over. Clinical Infectious Diseases. 2021;72(3):490-494.
16. Hellmuth J, Barnett TA, Asken BM, et al. Persistent COVID-19-associated neurocognitive symptoms in non-hospitalized patients. The Journal of Neurovirology. 2021;27(1):191-195.
17. Batty GD, Deary IJ, Luciano M, et al. Psychosocial factors and hospitalisations for COVID-19: Prospective cohort study based on a community sample. Brain, Behavior, and Immunity. 2020;89:569-578.
18. Almeria M, Cejudo JC, Sotoca J, et al. Cognitive profile following COVID-19 infection: clinical predictors leading to neuropsychological impairment. Brain, Behavior, & Immunity — Health. 2020;9:100163.
19. Gu Y, Zhu Y, Xu F, et al. Factors associated with mental health outcomes among patients with COVID-19 treated in the Fangcang shelter hospital in China. Asia-Pacific Psychiatry. 2021;13:e12443.
20. Dani M, Dirksen A, Taraborrelli P, et al. Autonomic dysfunction in ‘long COVID’: rationale, physiology and management strategies. The Clinical Medicine (Lond). 2021;21(1):63-67.
21. Davido B, Seang S, Tubiana R, de Truchis P. Post-COVID-19 chronic symptoms: a postinfectious entity? Clinical Microbiology and Infection. 2020;26(11):1448-1449.
22. Goldstein DS. The extended autonomic system, dyshomeostasis and COVID-19. Clinical Autonomic Research. 2020;30(4):299-315.
23. Umapathi T, Poh MQW, Fan BE, et al. Acute hyperhidrosis and postural tachycardia in a COVID-19 patient. Clinical Autonomic Research. 2020;30(6):571-573.
24. Miglis MG, Prieto T, Shaik R, et al. A case report of postural tachycardia syndrome after COVID-19. Clinical Autonomic Research. 2020;30(5):449-451.
25. Saeed S, Tadic M, Larsen TH, et al. Coronavirus disease 2019 and cardiovascular complications: focused clinical review. Journal of Hypertension. 2021;39(7):1282-1292.
26. Summary of ICD coding for COVID-19.
27. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 12 (21.09.21). 2021;232.
Temporary guidelines. Prevention, diagnosis and treatment of coronavirus infection (COVID-19). Version 12. (21.09.21). 2021;232. (In Russ.).
28. Федин А.И., Румянцева С.А., Пирадов М.А. и др. Клиническая эффективность Цитофлавина у больных с хронической ишемией головного мозга (многоцентровое плацебо-контролируемое рандомизированное исследование). Врач. 2007;4(12):29-34.
Fedin AI, Rumyantseva SA, Piradov MA, et al. Clinical efficacy of Cyto-flavin in patients with chronic cerebral ischemia (multicenter, placebo-controlled, randomized trial. Vrach. 2007;4(12):29-34. (In Russ.).
29. Полунина А.Г., Осиновская Н.А., Гудкова А.Н., Гехт А.Б. Влияние цитофлавина на симптомы астении, эмоциональное состояние и вегетативную регуляцию у пациентов с органическим астеническим расстройством. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;2:28-33.
Polunina AG, Osinovskaya NA, Gudkova AN, Guekht AB. Influence of cytoflavin on symptoms of asthenia, emotional disorders and autonomic regulation in patients with organic asthenic disorder. Zhurnal Nevrologii i Psihiatrii im. S.S. Korsakova. 2014;2:28-33 (In Russ.).
30. Шабанов П.Д., Мокренко Е.В. Синтетические индукторы интерферона в лечении и профилактике острых воспалительных заболеваний верхних дыхательных путей. Поликлиника. 2015;3:117-120.
Shabanov PD, Mokrenko EV. Synthetic inducers of interferon in the treatment and prevention of acute inflammatory diseases of the upper respiratory tract. Poliklinika. 2015;3:117-120. (In Russ.).
31. Парфенов С.А., Белов В.Г., Парфенов Ю.А. Динамика показателей функционального состояния центральной нервной системы у операторов Военно-морского флота после длительного рабочего цикла на фоне приема цитофлавина. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(8):55-58.
Parfenov SA, Belov VG, Parfenov JuA. Dynamics of indicators of the functional state of the central nervous system in the operators of the Navy after a long working cycle while taking Cytoflavin. Zhurnal Nevrologii i Psihiatrii im. S.S. Korsakova. 2017;117(8):55-58. (In Russ.).
32. Парфенов Ю.А., Василевская М.А., Парфенов С.А. и др. Обоснование показаний к применению БОС-терапии и цитофлавина в лечении неврологических осложнений остеохондроза среди пожилых пациентов. Медицинские новости Грузии. 2018;283:89-96.
Parfenov YuA, Vasilevskaya MA, Parfenov SA, et al. Justification of indications for the use of biofeedback therapy and cytoflavin in the treatment of neurological complications of osteochondrosis among elderly patients. Georgian Medical News. 2018;283:89-96. (In Russ.).
33. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 9 (26.10.20). 2020;236.
Temporary guidelines. Prevention, diagnosis and treatment of coronavirus infection (COVID-19). Version 9. (26.10.20). 2020;236. (In Russ.).
34. Екушева Е.В. Роль сукцинатсодержащих препаратов в процессах нейропластичности после ишемического инсульта. Экспериментальная и клиническая фармакология. 2018;8(81):37-44.
Ekusheva EV. The role of succinate-containing drugs in the processes of neuroplasticity after ischemic stroke. Eksperimental’naya i Klinicheskaya Farmakologiya. 2018;8(81):37-44. (In Russ.).
35. Xie N, Zhang L, Gao W, et al. NAD+ metabolism: pathophysiologic mechanisms and therapeutic potential. Signal Transduction and Targeted Therapy. 2020;5:227.
36. Heer CD, Sanderson DJ, Voth LS, et al. Coronavirus infection and PARP expression dysregulate the NAD metabolome: An actionable of innate immunity. Metabolism. 2020;295(52):17986-17996.
37. Mehmel M, Jovanovic N, Spitz U. Nicotinamide riboside-the current state of research and therapeutic uses. Nutrients. 2020;12(6):1616.
38. Omran HM, Almaliki MS. Influence of NAD+ as an ageing-related immunomodulator on COVID 19 infection: A hypothesis. Journal of Infection and Public Health. 2020;13(9):1196-1201.
39. Badawy AA. Immunotherapy of COVID-19 with poly (ADP-ribose) polymerase inhibitors: starting with nicotinamide. Bioscience Reports. 2020;40(10):BSR20202856.
40. Hasko G, Kuhel DG, Nemeth ZH, et al. Inosine inhibits inflammatory cytokine production by a posttranscriptional mechanism and protects against endotoxin-induced shock. The Journal Immunology. 2000;164(2):1013-1019.
41. Welihinda AA, Kaur M, Raveendran KS, Amento EP. Enhancement of ino-sine-mediated A2AR signaling through positive allosteric modulation. Cell Signaling Technology. 2018;42:227-235.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)