Результаты наблюдательной программы ЦИТОТРЕК (применение препарата Цитофлавин Таблетки) у пациентов с головными болями напряжения на фоне астЕнического синдрома с учетом Коморбидности
Статьи
© М.В. ПУТИЛИНА1, Н.И. ШАБАЛИНА2, И.А. БЛИНОВА3
1ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия;
2ЧУЗ «Центральная клиническая больница «РЖД-медицина», Москва, Россия;
3ГБУ «Городская поликлиника №220 Департамента здравоохранения города Москвы», Москва, Россия
Резюме
Цель исследования. Изучение эффективности и безопасности применения препарата Цитофлавин (Инозин + Никотинамид + Рибофлавин + Янтарная кислота) в комплексной терапии коморбидных пациентов с частой эпизодической головной болью напряжения (ГБН), сочетающейся с напряжением перикраниальных мышц на фоне астенического синдрома (АС).
Материал и методы. Обследованы 150 пациентов в возрасте 44,2±5,0 года с частой ГБН, сочетающейся с напряжением перикраниальных мышц, артериальной гипертензией 1—2 ст., выраженным астеническим синдромом. Все пациенты методом случайной выборки разделены на 3 группы в зависимости от получаемой терапии: 1 -я группа получала нестероидные противовоспалительные средства (ибупрофен 400 мг) 7 дней+толперизон 150 мг 3 раза в день 14 дней; 2-я группа — ибупрофен 400 мг/сут 7 дней+толперизон 150 мг 3 раза в день 14 дней+таблетированную форму препарата Цитофлавин (2 таблетки 2 раза в день) 25 дней; 3-я группа — ибупрофен 400 мг/сут 7 дней и таблетированную форму препарата Цитофлавин по утвержденной протоколом схеме без назначения миорелаксанта. Все пациенты были обследованы в день обращения, на 30+2 дня, через 60±2 дня; промежуточный телефонный опрос— на 15-й день. Проводился анализ динамики жалоб, клинических проявлений ГБН, показателей шкал, данных дневника головной боли, фиксировались побочные эффекты терапии. Аля клинической оценки использовались шкала астенических состояний (ШАС); индекс головной боли (HIT-6); визуальная аналоговая шкала (ВАШ); шкала тревоги и депрессии (HADS); Питтсбургский опросник качества сна; шкалы оценки качества жизни (EQ-5D) и обшей оценки состояния.
Результаты. После проведенной терапии на 30±2 дня во всех группах наблюдалась положительная динамика: снижение частоты, длительности, уменьшения интенсивности ГБН, более выраженная в группах с применением препарата Цитофлавин. К 60±2 дню наблюдения фиксировалось снижение частоты эпизодов ГБН во 2-й и 3-й группах на 76,7 и 62,5% соответственно по сравнению с 1 -й группой. Длительность приступов ГБН снижалась на 32,3% (1-я группа), 62,96% (2-я группа) и 38,1% (3-я группа). Во 2-й и 3-й группах снизились показатели индекса HIT-6 (на 47%), ВАШ (на 68%) по сравнению с 1-й группой (р<0,001), проявлений тревоги (на 57,5%) и депрессии (на 68%), нарушений сна (на 86%) по сравнению 1-й группой (р<0,001). Выраженность астении уменьшилась во 2-й группе на 64,51%, в 3-й — на 58,77%. Качество жизни пациентов 2-й и 3-й групп повысилось на 91% (57% — в 1-й группе). За время наблюдения ни у одного пациента не было отмечено серьезных нежелательных явлений и побочных эффектов, связанных с приемом препарата.
Заключение. Результаты исследования позволяют рассматривать препарат Цитофлавин в схемах ведения коморбидных пациентов с ГБН на фоне астенического синдрома.
Ключевые слова: головная боль напряжения, астения, тревога, депрессия, нарушения сна, Цитофлавин, инозин, никотинамид, рибофлавин, янтарная кислота.
Информация об авторах:
Путилина М.В. — orcid.org/0000-0()02-8655-8501
Шабалина Н.И. - orcid.org/0000-0002-18l4-3531
Блинова И.А. — orcid.org/0009-0009-8519-1312
Автор, ответственный за переписку: Путилина М.В. — e-mail: profput@mail.ru
Как цитировать: Путилина М.В.. Шабалина Н.И., Блинова И.А. Результаты наблюдательной программы ЦИТОТРЕК (применение препарата Цитофлавин Таблетки) у пациентов с головными болями напРяжения на фоне астЕнического синдрома с учетом Коморбидности. Журнал неврологии и психиатрии им. С.С. Корсакова. 2025; 125(10): 104-112. httрs://doi.Org/10.l 7116/jnevro2025125101104
Хронические болевые синдромы (ХБС) — одна из актуальных проблем современной медицины [1]. Среди всех локализаций ХБС одно из лидирующих мест занимает головная боль напряжения (ГБН) [2]. ГБН характеризуется повторяющимися эпизодами головных болей (ГБ) легкой или средней интенсивности продолжительностью от 30 мин до нескольких суток [3]. Распространенность ГБН в общей популяции варьирует от 30 до 78% [3,4]. Глобальное бремя ГБН в период с 1990 по 2021 г. увеличилось на 38%, что позволило поставить ее на 3 место по распространенности болевых синдромов [2]. Новая коронавирусная инфекция также способствовала увеличению числа пациентов с ГБ [5—8], астенические, тревожно-депрессивные расстройства обнаружены у 25% пациентов с ГБН [9].
До настоящего времени нет полной ясности о механизмах, вызывающих ГБН, особенно при наличии коморбидности и сопутствующего астенического синдрома (АС) [9]. Триггерами ГБН, вероятно, являются тревога, депрессия, эмоциональный стресс, офисная работа, синдром выгорания, длительная фиксированная поза за компьютером, гиподинамия [6]. Эти состояния могут быть следствием повторяющихся приступов ГБ или неэффективности терапии [10]. Высокий процент сердечно-сосудистых заболеваний, таких как артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), инсульты, транзиторная ишемическая атака, коморбиден ГБН [9, 11]. Астения, сердечно-сосудистые заболевания и гипертоническая болезнь имеют общие патофизиологические механизмы, к которым относятся: окислительный стресс, системное воспаление, дисфункция центральных моноаминергических систем, нарушения метаболизма нейротрансмиттеров, в частности глутамата и гамма-аминомасляной кислоты (ГАМК) [12]. В связи с этим эффективность терапии при ГБН в сочетании с АС, вероятно, может быть существенно повышена, если перечисленные стратегии будут дополнены метаболической коррекцией — комплексом целенаправленных воздействий на реакции клеточного метаболизма, лимитирующие энергетическое обеспечение жизненно важных функций организма. Препаратом, отвечающим всем этим требованиям и хорошо зарекомендовавшим себя, является Цитофлавин (Инозин + Никотинамид + Рибофлавин + Янтарная кислота). Преимущества этого лекарственного средства заключаются в синергичных механизмах действия компонентов, возможности потенцировать действия друг друга. Компоненты препарата Цитофлавин являются естественными метаболитами организма, стимулируют тканевое дыхание, участвуют в цикле трикарбоновых кислот, за счет чего повышаются образование энергии в клетках мозга и скорость утилизации кислорода, снижается выраженность оксидантного стресса и избыточного выброса возбуждающих нейротрансмттеров. Это положительно отражается на состоянии центральной нервной системы (ЦНС), позволяет купировать астенические состояния и вторично улучшать состояние церебральной гемодинамики, когнитивных функций [10—14]. Показана эффективность препарата Цитофлавин в лечении пациентов с ГБН [10]. Учитывая вышесказанное, очевидна необходимость дальнейшего изучения методов метаболической терапии ГБН в сочетании с астеническим состоянием и/или другой коморбидностью.
Цель исследования — изучение эффективности и безопасности применения препарата Цитофлавин в комплексной терапии коморбидных пациентов с частой эпизодической ГБН, сочетающейся с напряжением перикраниальных мышц на фоне АС.
Материал и методы
Наблюдательное исследование проведено в 3 клинических центрах Москвы. Все пациенты подписали информированное согласие на визите 1 (скрининг). Исследование проводилось в соответствии с требованиями Национального стандарта РФ ГОСТ Р 52379-2005 «Надлежащая клиническая практика»; Хельсинкской декларации 2013 г.; Правилами Надлежащей клинической практики ЕАЭС (решение от 03.11.2016 №79), Приказом 200н «Об утверждении правил надлежащей клинической практики» от 01.04.2016. Протокол исследования утвержден на заседании НЭК (протокол № 100/5 от 10 октября 2024 г.). Набор пациентов в исследование осуществлялся по определенным критериям включения (с учетом показаний к назначению Цитофлавина) и критериям исключения.
Критерии включения: мужчины и женщины от 18 до 45 лет включительно; наличие АГ более 2 лет; частая эпизодическая ГБН, сочетающаяся с напряжением пери-краниальных мышц; значения по опроснику влияния головной боли (HIT-6) выше 60 баллов; наличие признаков умеренной астении по шкале астенического состояния (ШАС) (>76 баллов); подписанное информированное согласие об участии пациента в исследовании.
Критерии невключения: возраст моложе 18 и старше 45 лет; соматогенный АС органической природы; хронические заболевания в фазе декомпенсации; беременность и период грудного вскармливания; индивидуальная непереносимость препарата Цитофлавин или его компонентов; посттравматические головные боли; выраженная тревога и/или депрессия (значения по госпитальной шкале тревоги и депрессии (HADS) 11 баллов и выше); инсульт давностью менее 1 года; психиатрические заболевания, требующие наблюдения врача-психиатра и/или постоянного приема терапии; острый инфекционный процесс (давностью менее 4 недель); прием ноотропных и/или психотропных препаратов за 2 недели до включения в исследование или в течение курса лечения; тяжелое или нестабильное течение АГ, уровень артериального давления (АД) >200/115 мм рт. ст.; тяжелые соматические заболевания (тяжелые формы ИБС, онкологические заболевания, хроническая легочная, почечная и печеночная недостаточность и др.), другие (несосудистые) заболевания центральной нервной системы; эпилепсия; неспособность пациента следовать назначениям врача; другие состояния, которые, по мнению врача-исследователя, могут препятствовать проведению исследования.
Критерии исключения: отзыв пациентом информированного согласия; несоблюдение режима терапии и наблюдения; развитие нежелательных явлений (НЯ) в связи с назначенными препаратами с последующей сменой тактики лечения.
В исследовании приняли участие 150 пациентов, находившихся на амбулаторном лечении в 3 консультативно-диагностических центрах Москвы, соответствующих критериям включения. Средний возраст составил 44,2±5,0 года, женщин было больше (71,3%), чем мужчин (табл. 1). У пациентов были диагностированы: АГ 1—2 ст., гипертоническая энцефалопатия 1 —2 ст., выраженный АС, частая эпизодическая ГБН, сочетающаяся с напряжением перикраниальных мышц (в соответствии с МКГБ-3) [15]. В зависимости от получаемой терапии пациенты были разделены на три группы (см. табл. 1, 2). Пациенты 1-й группы (/7=50) получали только стандартную базисную терапию ГБН согласно клиническим рекомендациям: ибупрофен 400 мг/сут 7 дней + толперизон 150 мг 3 раза в день 14 дней, учитывая наличие выраженной дисфункции перикраниальных мышц [4]. Пациенты 2-й группы (n=50) получали ибупрофен 400 мг/сут 7 дней + толперизон 150 мг 3 раза в день 14 дней и таблетированную форму препарата Цитофлавин по утвержденной протоколом схеме по 2 таблетки 2 раза в день длительностью 25 дней. Пациенты 3-й группы (n=50) получали ибупрофен 400 мг/сут 7 дней и таблетированную форму препарата Цитофлавин по утвержденной протоколом схеме без назначения миорелаксанта.
Таблица 1. Исходные характеристики групп пациентов
Table 1. Baseline characteristics of patient groups

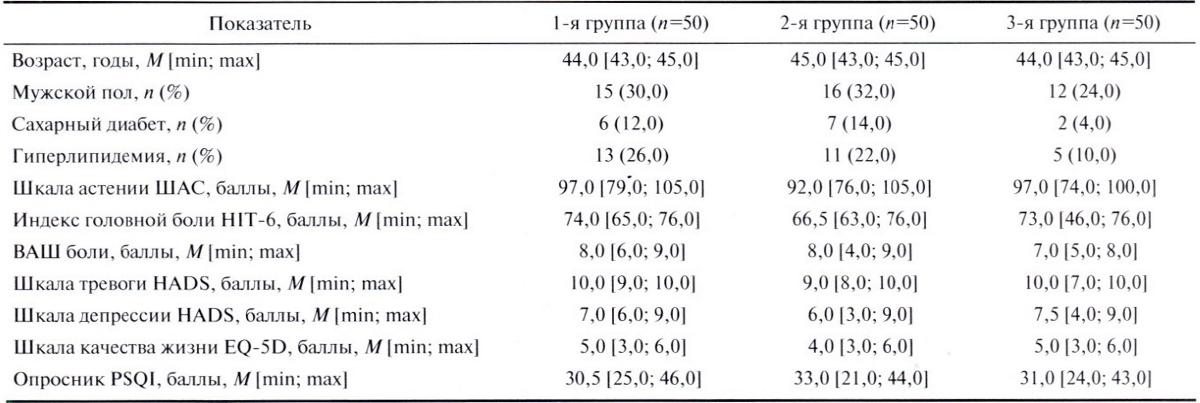
Примечание. Здесь и в табл. 3: ВАШ — визуально-аналоговая шкала; HADS — госпитальная шкала тревоги и депрессии; HIT-6 — опросник влияния головной боли; PSQI — Питтсбургский опросник качества сна; ШАС — шкала астенического состояния; EQ-5D — шкала опенки качества жизни.
Note. Here and in Table 3; ВАШ — visual analogue scale; HADS - Hospital Anxiety and Depression Scale; HIT-6 — Headache Impact Questionnaire; PSQI — Pittsburgh Sleep Quality Index; ШАС — Scale of Asthenic Condition; EQ-5D — Quality of Life Assessment Scale.
Таблица 2. Клинические характеристики головной боли у пациентов до начала лечения
Table 2. Clinical characteristics of headache in patients before treatment


Примечание. p1 — значимость отличий между 1-й и 2-й группами; р2 — значимость отличий между 1-й и 3-й группами; р3 — значимость отличий между 2-й и 3-й группами.
Note, р1 — two-sided significance between groups 1 and 2; p2 — two-sided significance between groups 1 and 3; p3 — two-sided significance between groups 2 and 3.
Среди сопутствующих заболеваний у пациентов в трех группах превалировали гиперлипидемия, атеросклероз, остеохондроз различной локализации.
Продолжалась ранее назначенная базовая терапия (гипотензивные, гипогликемические препараты, статины, антиагреганты). В рамках наблюдательной программы не проводились дополнительные исследования вне стандартно используемых в рутинной клинической практике.
Все пациенты были обследованы в день обращения в медицинское учреждение, на визите 1 (скрининг) проводились: отбор для участия в исследовании по заявленным критериям, сбор анамнеза, жалоб, осмотр; разъяснения по заполнению дневника головной боли; подписание информированного согласия. Следующим, через 15±2 дня, проводился промежуточный опрос по телефону (без личного присутствия пациента) для выявления и оценки НЯ, наличия жалоб, информации о сопутствующей терапии (если она требовалась). На визите 2 (через 30±2 дня) проводился анализ динамики жалоб, клинических проявлений ГБН, показателей шкал, данных Дневника головной боли, фиксировались побочные эффекты терапии (если они были). На визите 3 (через 60±2 дня) проводилось аналогичное обследование. Пациентами заполнялась шкала субъективной оценки состояния после курса терапии.
Оценка состояния проводилась на всех визитах по показателям ШАС, визуально-аналоговой шкалы (ВАШ), HADS, опросника качества жизни (EQ-5D), Питтсбургского опросника качества сна (PSQI), шкалы общей оценки состояния (ШООС), HIT-6.
Статистический анализ проведен с использованием программного пакета SPSS 23.1. Бинарные данные представлены в формате: n/N% (95% ДИ], где п — число пациентов с признаком, N—размер группы без учета пропусков, % — доля пациентов с признаком, 95% ДИ — верхняя граница 95% доверительного интервала по Клопперу—Пирсону. Количественные данные представлены в формате: M±SD. Me [Q35; Q75] или M [min; max], где M — среднее значение, SD — стандартное квадратическое отклонение, Me — медиана, Q,5; Q75— 25% и 75% квартили, min; max — минимальное и максимальное значения. Сравнение групп проведено в режиме попарного сравнения при помощи критериев Фишера (для бинарных данных), t-теста Стьюдента—Уэлча (для количественных данных). Анализ внутригрупповой динамики проведен парным /-тестом Стьюдента—Уэлча как для клинических данных на всех трех визитах, так и для сумм по искомым показателям дневников наблюдения для периодов 0—30 и 31—60 дней. Поправки на множественные сравнения делались про помощи метода Холма. Пороговое значение р<0,05.
Результаты
На визите 2 во всех группах наблюдалась положительная динамика, проявлявшаяся в снижении частоты, длительности и интенсивности эпизодов ГБН. В 1-й группе снижение частоты эпизодов ГБН отметили 38 (76,0%) из 50 пациентов. Длительность эпизодов значимо не изменилась, составив 465±36 мин, но отмечалось достоверное снижение их интенсивности. Во 2-й и 3-й группах было зарегистрировано сочетанное снижение всех изучаемых параметров: частоты, длительности и интенсивности эпизодов ГБН. Во 2-й группе среднее количество эпизодов снизилось до 4 в месяц, а их средняя длительность — до 135±25 мин. В 3-й группе количество эпизодов составило 5 в месяц, а средняя длительность — 210±38 мин (отличия по сравнению с 1-й группой — р<0,001 и р<0,01 соответственно).
Указанная динамика коррелировала со значимым снижением частоты приема нестероидных противовоспалительных препаратов(НПВП) во 2-й и 3-й группах. Так, пациенты 2-й группы после окончания 7-дневного курса терапии в рамках исследования полностью прекратили прием НПВП. В то же время в 1-й группе дополнительный прием НПВП отмечался у 10 (20%) пациентов, а в 3-й — у 5 (10%). К визиту 3 выявленные различия между 2-й и 3-й группами достигли статистической значимости по частоте приема НПВП (p<0,01). Несмотря на положительную динамику снижения частоты и длительности эпизодов ГБН во всех группах, именно во 2-й и 3-й группах было зафиксировано наибольшее уменьшение данных показателей (рис. 1).
Рис. 1. Динамика изменений частоты эпизодов ГБН за весь период наблюдения.
Fig. 1. Dynamics of changes in the frequency of episodes of GBN over the entire observation period.
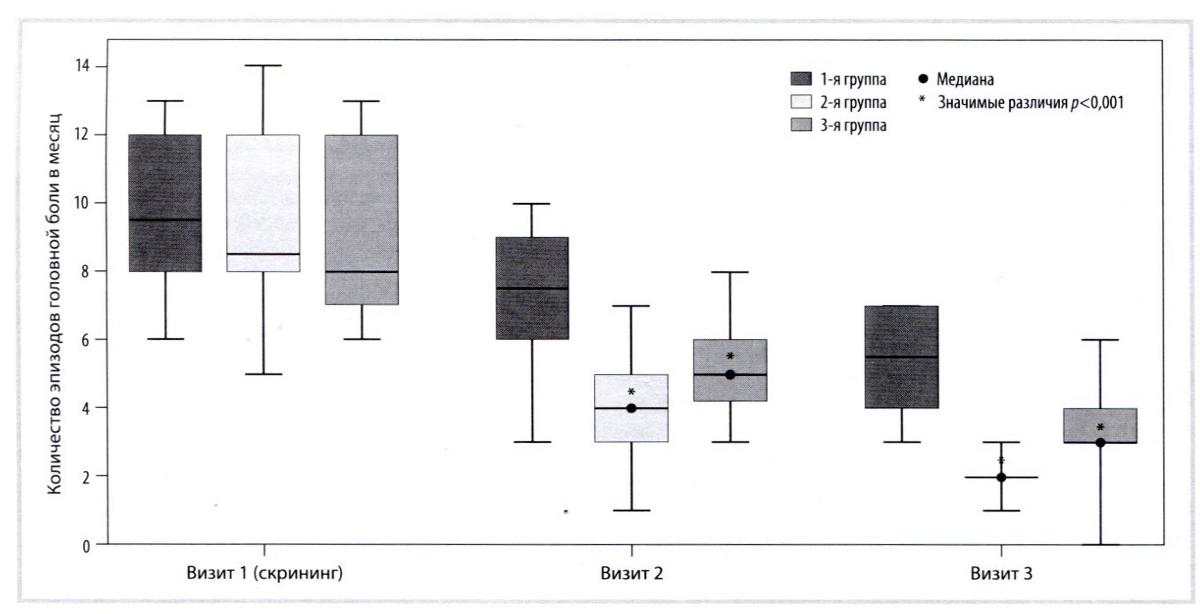
Визит 1: 2-я группа vs 1-я группа: />=0.636; 3-я группа vs l-я группа: />=0,202; 3-я группа vs 2-я группа: />=0,636; визит 2: 2-я группа vs l-я группа: /><0,001; 3-я группа vs 1-я группа: р<0,001; 3-я группа vs 2-я группа: p<0,001; визит 3: 2-я группа vs 1-я группа: /><0,001; 3-я группа vs 1-я группа: /><0,001.
Visit I: Group 2 vs. Group 1: p=0.636; Group 3 vs. Group I: />=0.202; Group 3 vs. Group 2: />=0.636; Visit 2: Group 2 vs. Group I: /><0.001; Group 3 vs. Group 1: p<0.001; Group 3 vs. Group 2:p<0.001; Visit 3: Group 2 vs. Group 1: p<0.001; Group 3 vs. Group 1: p<0.001, Group 3 vs. Group 2: p<0.001.
Процентное снижение частоты эпизодов ГБН к визиту 3 в 1-й группе составило 26,7%, во 2-й — 50%, в 3-й — 40%. Положительный эффект терапии был заметен уже к визиту 2: снижение частоты эпизодов в 1-й группе на 42,1%, во 2-й — на 76,7%, в 3-й — на 62,5%. Полученные данные согласуются с результатами исследования Л.С. Чутко и соавт. [14], в котором Цитофлавин в комплексной терапии ГБН способствовал снижению интенсивности ГБ, уменьшению тревожности и улучшению когнитивных функций (памяти и внимания).
Длительность эпизодов ГБН от визита 2 к визиту 3 уменьшилась на: 32,3% (1-я группа); 62,96% (2-я группа); 38,10% (3-я группа) (рис. 2).
Рис. 2. Динамика длительности эпизода головной боли за весь период наблюдения).
Fig. 2. Dynamics of the duration of a headache episode over the entire observation period.
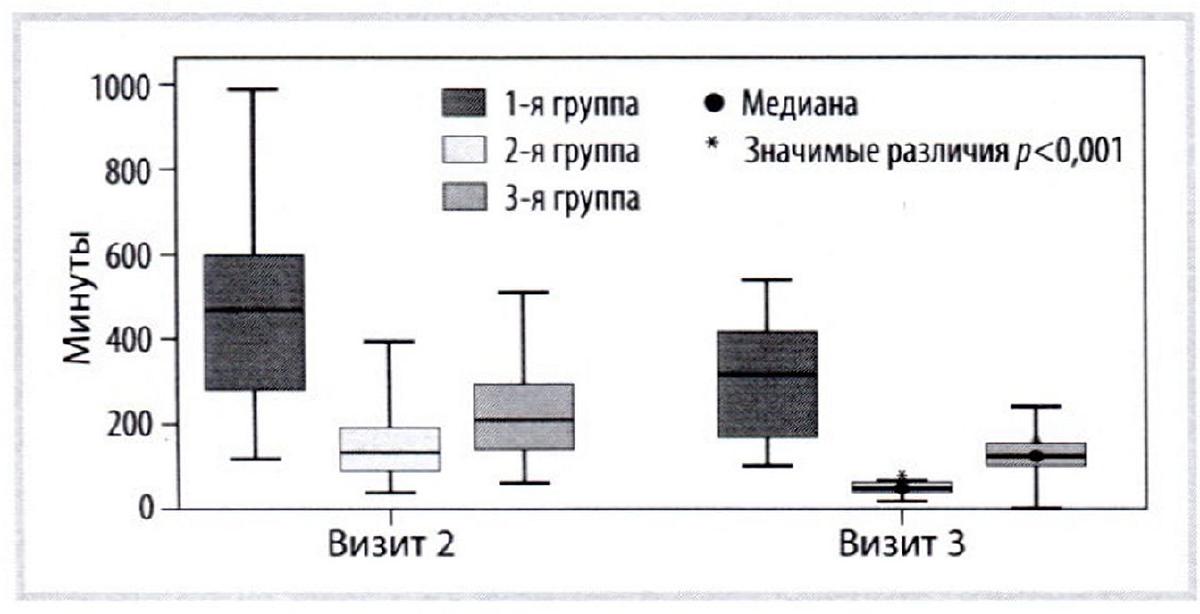
Визит 2: 2-я группа vs 1-я группа: p<0,001; 3-я группа vs I -я группа: p<0,001; 3-я группа vs 2-я группа: p=0,005; визит 3: 2-я группа vs 1-я группа: p<0,001; 3-я группа vs 1-я группа: p<0,001; 3-я группа vs 2-я группа: p=0,002.
Visit 2: Group 2 vs. Group 1:p<0.001; Group 3 vs. Group 1: p<0.001; Group 3 vs. Group 2: p=0.005; Visit 3: Group 2 vs. Group 1: p<0.001; Group 3 vs. Group 1: /><0.001, Group 3 vs. Group 2: p=0.002.
У всех пациентов с неизменной частотой и длительностью приступов на визитах 2 и 3 сохранялось напряжение перикраниальных мышц: в 1-й группе на визите 2 — у 8 (16%) пациентов, на визите 3 — у 20 (40%); во 2-й группе: у 1 (0,5%) — на визите 2 и у 5 (10%) — на визите 3; в 3-й группе: у 10 (20%) — на визитах 2 и 3. На визите 3 у 90% пациентов 1-й группы отмечались эпизоды повышения цифр АД, часто ассоциированные с приступами ГБ и употреблением НПВП в более высоких дозах. В 1-й группе 10 пациентов отмечали ночное повышение АД, требовавшие дополнительной медикаментозной коррекции. У пациентов 2-й и 3-й групп такие случаи были единичными (от 1 до 5 пациентов), при этом цифры АД снижались на меньшей дозе антигипертензивных средств. В этих группах не потребовалось коррекции антигипертензивной терапии, тогда как 20% пациентов 1-й группы, принимающих длительно НПВП, потребовалось изменение схемы антигипертензивной терапии. Пациенты, в комплексную терапию которых входил Цитофлавин, уже к визиту 2 не предъявляли жалоб на нарушения сна, общую слабость, забывчивость, головокружение, шум в ушах. Цитофлавин при добавлении к комплексной терапии улучшил клинические показатели, что можно объяснить антигипоксическим, антиишемическим, антиоксидантным действием препарата. Объективная динамика изменений характеристик ГБН представлена в табл. 3.
Таблица 3. Динамика показателей шкал за весь период наблюдения, баллы, M±SD
Table 3. Dynamics of the Scales indicators over the entire observation period, points, M±SD
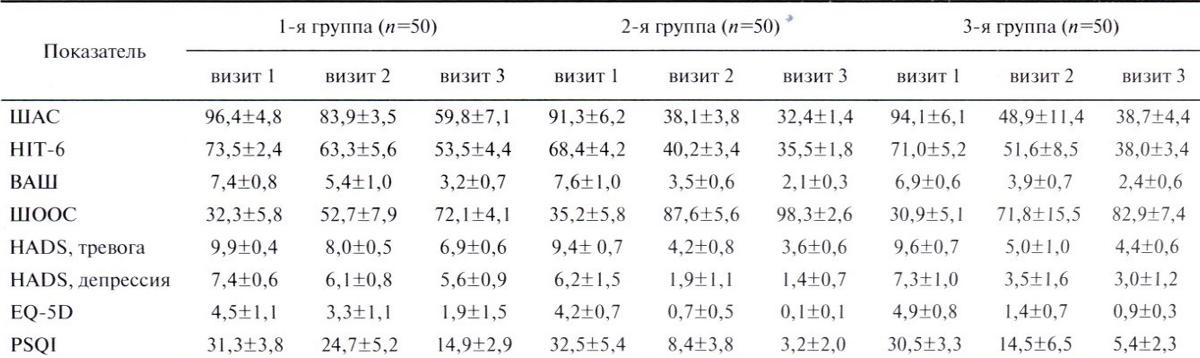
 У всех пациентов до лечения фиксировались проявления АС (см. табл. 3). Однако уже к визиту 2 появились различия в регрессе симптомов: в 1-й группе выраженность уменьшилась на 12,9%; во 2-й — на 58,2%; в 3-й — на 48,3%. Эта тенденция сохранилась к визиту 3: в 1-й группе выраженность уменьшилась на 37,9%; во 2-й — на 64,51%; в 3-й — на 58,7%. Эти показатели еще раз подтвердили высокий антиастенический эффект препарата Цитофлавин (рис. 3).
У всех пациентов до лечения фиксировались проявления АС (см. табл. 3). Однако уже к визиту 2 появились различия в регрессе симптомов: в 1-й группе выраженность уменьшилась на 12,9%; во 2-й — на 58,2%; в 3-й — на 48,3%. Эта тенденция сохранилась к визиту 3: в 1-й группе выраженность уменьшилась на 37,9%; во 2-й — на 64,51%; в 3-й — на 58,7%. Эти показатели еще раз подтвердили высокий антиастенический эффект препарата Цитофлавин (рис. 3).
Рис. 3. Динамика показателей шкалы астенических состояний (ШАС) за весь период наблюдения.
Fig. 3. Dynamics of indicators of the asthenic conditions scale (SHAS) over the entire observation period.
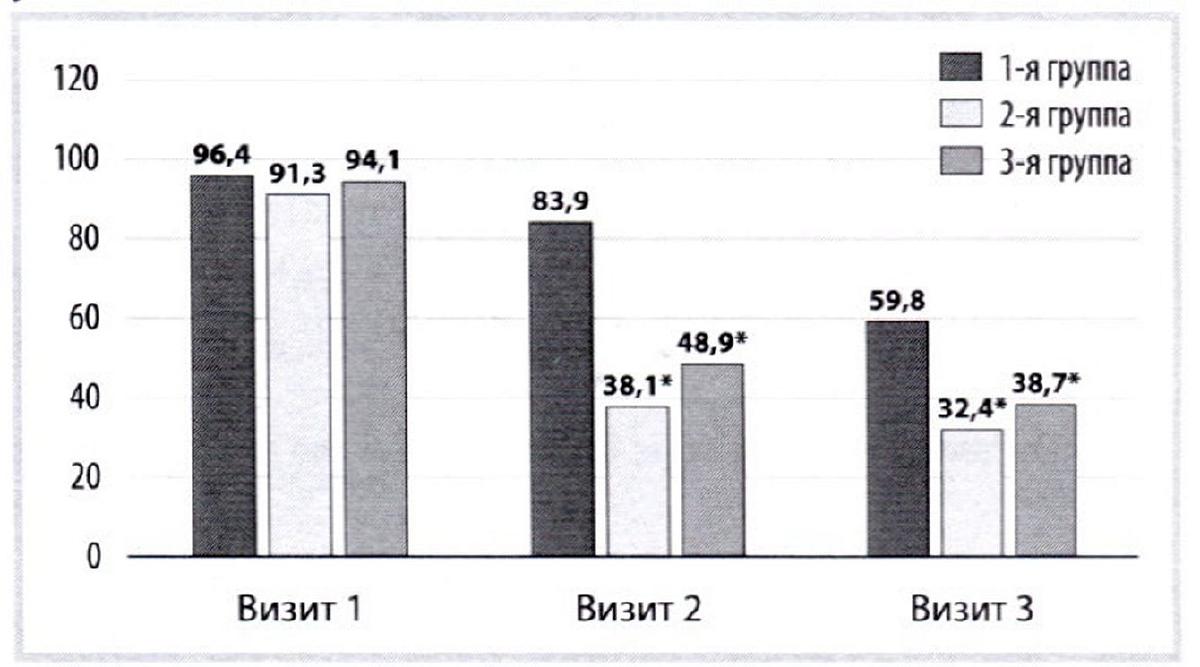
*-p<0.001.
Позитивная тенденция изменения HIT-6 проявилась уже к визиту 2: в 1-й группе показатель уменьшился с 73,5±2,4 до 53,5±4,4 балла р<0,001), во 2-й группе — с 68,4±2,4 до 35,5±4,4 балла (/><0,001), в 3-й группе — с 71 ±5,2 до 38±3,4 балла (p<0,001) (рис. 4).
Рис. 4. Динамика показателей индекса HIT-6.
Fig. 4. Dynamics of the HIT-6 index indicators
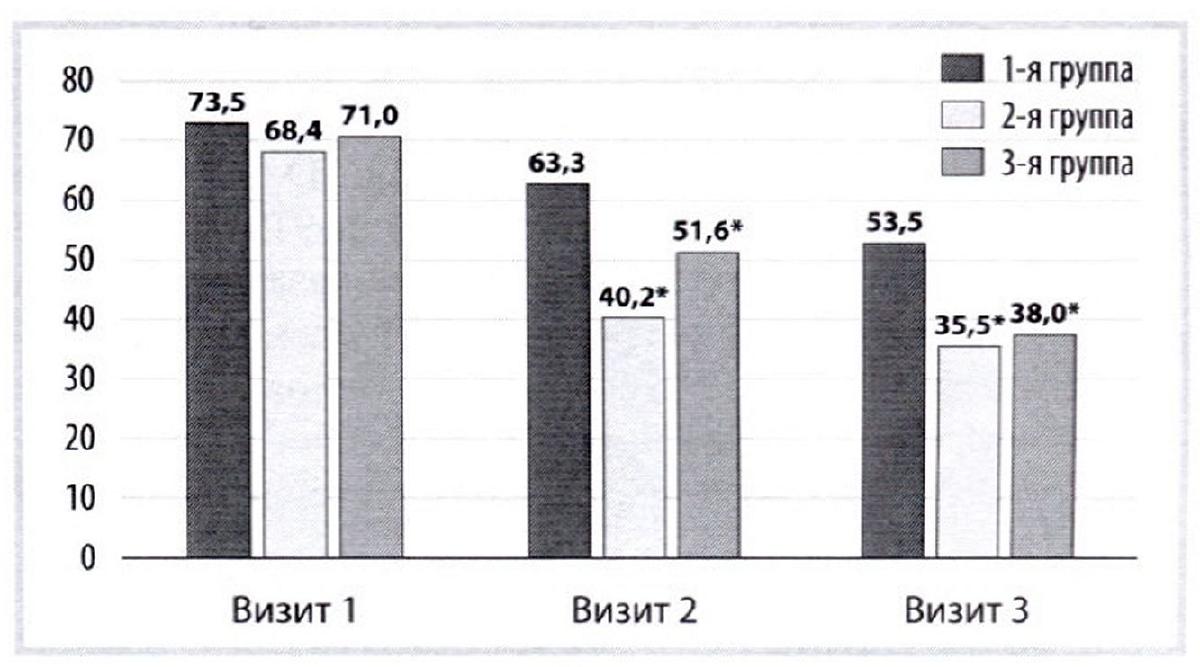
* - p<0,001.
К визиту 3 индекс HIT-6 у пациентов 2-й группы снизился на 48,1%, 3-й группы — на 46,8%, 1-й группы — на 27,2%, что коррелируете результатами оценки по ВАШ (см. табл. 3). У пациентов 2-й и 3-й групп зафиксировано выраженное снижение баллов по шкале ВАШ от визита 1 к визиту 3: от 7,6±0,4 до 2,1 ±0,4 (2-я группа) и от 6,9±0,4 до 2,4±0,4 (3-я группа). В 1-й группе также фиксировалась положительная динамика, но в меньшей степени. Данные результаты коррелируют с показателями шкалы HADS (тревога/депрессия) (рис. 5). В 1-й группе выраженность тревожных расстройств снизилась на 30,3%, депрессивных — на 24,3%; во 2-й группе — на 61,7 и 77,4% соответственно, в 3-й группе — на 54,2 и 58,9% соответственно.
 Рис. 5. Динамика показателей шкалы HADS за весь периол наблюдения.
Рис. 5. Динамика показателей шкалы HADS за весь периол наблюдения.
Fig. 5. Dynamics of HADS scale indicators over the entire observation period.
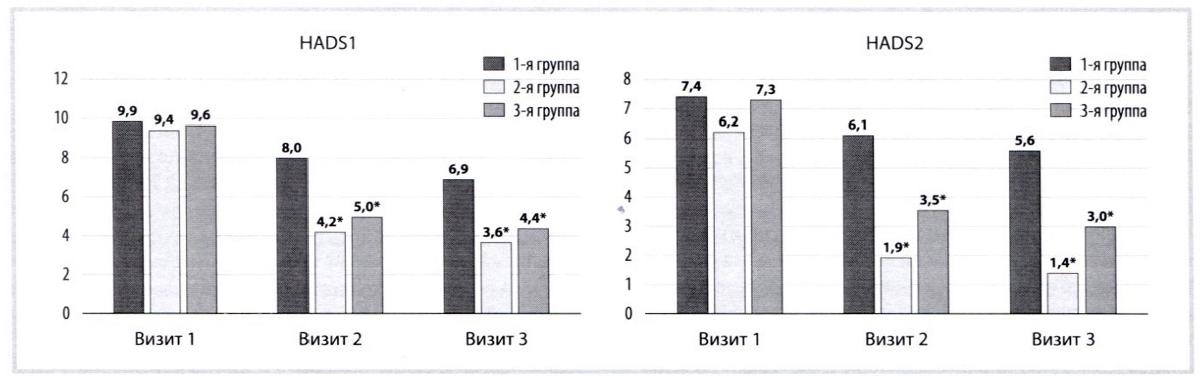
* -p<0,001.
HADS1
HADS2
До лечения все пациенты жаловались на нарушения сна. Общий балл по опроснику PSQI до лечения во всех группах составлял 31,3± 1,5 балла, к окончанию исследования количество жалоб по опроснику достоверно уменьшилось: в 1-й группе — в 2 раза, во 2-й группе — в К) раз, в 3-й группе — в 6 раз (см. табл. 3). Полученные данные свидетельствуют о выраженном влиянии препарата Цитофлавин на нормализацию сна, причем это улучшение фиксировали пациенты с различной коморбидностью, без гендерных различий. Согласно опроснику EQ-5D, у пациентов 2-й и 3-й групп улучшились показатели на 91% по сравнению с 57% в 1-й группе (см. табл. 3). По показателям шкалы ШООС зафиксировано значительное улучшение уже на ви-зите 2 — в среднем на 52±6 баллов (2-я группа) и 51 ±6 баллов (4-я группа) по сравнению с 20±6 баллов в 1-й группе. К визиту 3 эта динамика отчетливо сохранялась (см. табл. 3).
Обсуждение
Полученные результаты могут быть объяснены следующим образом: в патогенезе ГБН одну из центральных ролей играет мышечно-тонический синдром перикраниальных мышц [6, 16—19]. При ГБН формируется патологический «порочный круг»: мышечный спазм приводит к гипоксии, которая вызывает боль и эмоциональный стресс, что, в свою очередь, усугубляет мышечное напряжение ]19, 20]. Дополнительными триггерными факторами выступают нарушения сна, длительное нахождение в вынужденной позе (например, работа за компьютером), а также колебания АД, зарегистрированные в нашем исследовании в 1-й и 3-й группах на фоне приема НПВП. Длительное мышечно-тоническое напряжение усугубляет ишемию и способствует развитию нейровоспаления с высвобождением провоспалительных цитокинов — медиаторов боли. Это приводит к повышению возбудимости периферических ноцицептивных нейронов (периферическая сенситизация) и высвобождению альгогенных пептидов (вещество Р), что дополнительно усиливает болевые ощущения. Хотя стандартная терапия (НПВП) и Цитофлавин оказывают положительное влияние, частично нивелируя последствия гипоксии и ишемии, они не устраняют первичный мышечный спазм и не уменьшают количество миофасциальных триггерных точек [19, 20]. Пролонгированное тоническое сокращение активирует ноцицепторы, запуская механизмы вторичной гипералгезии и вовлекая в патологический процесс ЦНС [ 19—22]. Формирование феномена центральной сенситизации является характерной чертой как эпизодической, так и хронической ГБН. Важным отягощающим фактором в нашем исследовании выступала коморбидная АГ, диагноз которой был ранее верифицирован у всех пациентов. В последние годы в литературе все чаще выделяют фенотип ГБН, ассоциированной с АГ [21 ]. Оба состояния имеют общие патогенетические механизмы, такие как эндотелиальная дисфункция, вегетативная дисрегуляция и гиперактивация ренин-ангиотензин-альдостероновой системы [22]. Хронический вазоспазм и изменение активности барорецепторов на фоне АГ сами по себе Moiyr провоцировать и поддерживать гипералгезию, что клинически выражается в увеличении длительности и частоты эпизодов ГБН [21].
Таким образом, ограниченная эффективность монотерапии НПВП в 1-й группе может быть объяснена ее исключительно симптоматическим действием, не влияющим на ключевые звенья патогенеза: мышечный спазм, центральную сенситизацию, оксидативный стресс и эндотелиальную дисфункцию. Добавление миорелаксантов, хотя и решает проблему мышечно-тонического синдрома, также не воздействует на последние два компонента [23]. Сопутствующие АГ, скелетно-мышечные боли, астения, нарушения венозного оттока могут ускорять процесс хронизации [24—28]. Наличие денрессии/тревоги — один из ведущих факторов хронизации боли [25, 26]. Выраженность депрессии коррелирует c изменениями пластичности нейронов и уменьшением объема структур головного мозга, что ассоциировано с когнитивными и поведенческими нарушениями [7, 10]. В ходе исследования отмечалось снижение показателей по шкале HADS в большей степени у пациентов, получавших терапию препаратом Цитофлавин. Цитофлавин купирует проявления инсомнии, когнитивной дисфункции, снимает повышенную утомляемость, шум в ушах, головокружение, головную боль [13, 29—33]. Вероятно, более выраженный терапевтический эффект препарата Цитофлавин во 2-й и 3-й группах может быть связан сего комплексным влиянием на метаболизм ишемизированной ткани, антигипоксантным и антиоксидантным действием, что способствует разрыву патологических звеньев «порочного круга» ГБН на нескольких уровнях одновременно. За время наблюдения ни у одного пациента не было отмечено серьезных НЯ и побочных эффектов, связанных с приемом препарата.
Выводы
Пациенты с коморбидным состоянием, характеризующимся сочетанием ГБН и АС, нуждаются в углубленном обследовании для разработки более эффективных стратегий терапии и профилактики. На фоне добавления Цитофлавина к стандартной комплексной терапии зарегистрировано статистически значимое снижение частоты эпизодов ГБН в группе, получавшей в составе терапии ибупрофен, миорелаксант и Цитофлавин, — с 8,0±5,2 до 2,0± 1,0 балла (р<0,001); в группе, получавшей ибупрофен и Цитофлавин, — с 8,5±5,0 до 3,5±2,5 балла (р<0.001), т.е. на 76,7 и 62,5% по сравнению с группой, получавшей только стандартную терапию.
Длительность приступов эпизодической ГБН при назначении комплексной терапии с добавлением препарата Цитофлавин снижалась в среднем на 62,96 и 38,1%. Длительность эпизодов ГБН в группе стандартной терапии снизилась только на 32,2%. При этом уровень интенсивности ГБН коррелировал с изменениями длительности эпизодов. Выраженность болевого синдрома ГБН при комплексной терапии с добавлением препарата Цитофлавин снижается быстрее, что объективно отражается в показателях шкал: НIT-6 — в среднем на 47%, ВАШ — на 68% по сравнению со стандартной терапией. Снижение проявлений тревоги (на 57,5%) и депрессии (на 68%), нарушений сна (на 86%), по сравнению со стандартной терапией, наблюдалось в группах терапии с добавлением препарата Цитофлавин. Комплексная терапия с препаратом Цитофлавин быстрее купирует проявления АС, что заключалось в более выраженном снижении показателей ШАС.
Препарат Цитофлавин в таблетках в стандартной дозе по 2 таблетки 2 раза в день хорошо переносится пациентами, не вызывает нежелательных лекарственных взаимодействий при приеме с другими препаратами (антигипертензивными, антиагрегантами, статинами).
Заключение
Результаты исследования позволяют рассматривать включение препарата Цитофлавин в схемы лечения эпизодической ГБН у коморбидных пациентов с АС. Полученные данные свидетельствуют о терапевтическом эффекте в том числе у пациентов, не получавших миорелаксанты, что можно рассматривать перспективным направлением для дальнейшего изучения применения препарата при ГБН без напряжения перикраниальных мышц и/или с противопоказаниями для назначения миорелаксантов.
Авторы заявляют об отсутствии конфликта интересов. The authors declare no conflicts of interest.
ЛИТЕРАТУРА/REFERENCES
1. Rometsch C, Martin A, Junne F, Cosci F. Chronic pain in European adult populations: a systematic review of prevalence and associated clinical features. Pain. 2025;166(4):719-731. doi.org/10.1097/j.pain.0000000000003406
2. Liu C, Wang Y, Liu M, et al. Global, regional, and national burden and trends of tension-type headache among adolescents and young adults (15— 39 years) from 1990 to 2021: findings from the Global Burden of Disease study 2021. Sci Rep. 2025;15(67):18254. doi.org/10.1038/s41598-025-02818-x
3. Азимова Ю.Э., Алферова В.В., Амелин А.В. и др. Клинические рекомендации. Головная боль напряжения (ГБН). Журнал неврологии и психиатрии им. С.С. Корсакова. 2022;122(2-3):4-28.
Azimova YE, Alferova VV, Amelin AV, et al. Clinical Guidelines for Headache Stress (HBS). S.S. Korsakov Journal of Neurology and Psychiatry. 2022;122(2-3):4-28. (In Russ.). doi.org/10.17116/jnevro20221220234
4. Головная боль напряжения. Клинические рекомендации. Всероссийское общество неврологов, Межрегиональная общественная организация «Российское общество по изучению головной боли», Общероссийская общественная организация «Союз реабилитологов России». Головная боль напряжения (ГБН), 2024 г. (одобрено НПС МЗ РФ).
Golovnaya bol’ napryazheniya. Klinicheskie rekomendatsii. Vserossiiskoe ob-shchestvo nevrologov, Mezhregional’naya obshchestvennaya organizatsiya «Rossiiskoe obshchestvo po izucheniyu golovnoi boli», Obshcherossiiskaya obshchestvennaya organizatsiya «Soyuz reabilitologov Rossii». Golovnaya bol’ napryazheniya (GBN), 2024. (In Russ.).
5. Carvalho LCLS, Silva PAD, Rocha-Filho PAS. Persistent headache and chronic daily headache after COVID-19: a prospective cohort study. Korean J Pain. 2024;37(3):247-255. doi.org/10.3344/kjp.24046
6. Parsaei M, Taebi M, Arvin A, Moghaddam HS. Brain structural and functional abnormalities in patients with tension-type headache: A systematic review of magnetic resonance imaging studies. J Neurosci Res. 2024;102(1): e25294. doi.org/10.1002/jnr.25294
7. Громова О.А., Торшин И.Ю., Семенов В.А. и др. О прямых и косвенных неврологических проявлениях COVID-19. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(11):11-21.
Gromova OA, Torshin IYu, Semenov VA, et al. On the direct and indirect neurological manifestations of COVID-19. S.S. Korsakov Journal of Neurology and Psychiatry. 2020;120(11):11-21. (In Russ.). doi.org/10.17116/jnevro202012011111
8. Путилина М.В. Боль в спине, ассоциированная с новой короновирусной инфекцией SARS COVID-19. Российский журнал боли. 2022;20(1):42-47. Putilina MV. Back pain associated with a new coronavirus infection COVID-19. Russian Journal of Pain. 2022;20(1):42-47. (In Russ.). doi.org/10.17116/pain20222001142
9. Caponnetto V, Deodato M, Robotti M, et al.; European Headache Federation School of Advanced Studies (EHF-SAS). Comorbidities of primary headache disorders: a literature review with meta-analysis. J Headache Pain. 2021;22(1):71. doi.org/10.1186/s10194-021-01281-z
10. Мирзаева Л.М., Лобзина А.С., Ахмедова К.Н. и др. Терапия ко-морбидной патологии при эпизодической мигрени и головной боли напряжения. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(9):52-57.
Mirzaeva LM, Lobzina AS, Akhmedova KN, et al. Therapeutic approaches to comorbid pathology in episodic migraine and tension-type headache. S.S. Korsakov Journal of Neurology and Psychiatry. 2023;123(9):52-57. (In Russ.). doi.org/10.17116/jnevro202312309152
11. Bhoi SK, Jha M, Chowdhury D. Advances in the Understanding of Pathophysiology of TTH and its Management. Neurol India. 2021;69(Supp) S116-S123. doi.org/10.4103/0028-3886.315986
12. Федин А.И. Окислительный стресс в патогенезе хронической головной боли. Журнал неврологии и психиатрии им. С.С. Корсакова. 2024;124(10):35-40.
Fedin AI. Oxidative stress in the pathogenesis of chronic headache. S.S. Korsakov Journal of Neurology and Psychiatry. 2024;124(10):35-40. (In Russ.). doi.org/10.17116/jnevro202412410135
13. Путилина М.В., Теплова Н.В., Баирова К.И. и др. Эффективность и безопасность Цитофлавина при реабилитации больных с постковид-ным синдромом: результаты проспективного рандомизированного исследования ЦИТАДЕЛЬ. Журнал неврологии и психиатрии им. С.С. Корсакова. 2021;121(10):39-45.
Putilina MV, Teplova NV, Bairova KI, et al. The result of prospective randomized study CITADEL — the efficacyand safety of drug Cytoflavin in postcovid rehabilitation. S.S. Korsakov Journal of Neurology and Psychiatry. 2021;121(10):39-45. (In Russ.). doi.org/10.17116/jnevro202112110145
14. Чутко Л.С., Сурушкина С.Ю., Яковенко Е.А. и др. Возможности применения Цитофлавина при лечении когнитивных и эмоциональных нарушений у пациентов с головными болями напряжения. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(11):32-36.
Chutko LS, Surushkina SYu, Yakovenko EA, et al. Possibilities of using Cytoflavin in thetreatment of cognitive and emotional disorders in patients with tension headaches. S.S. Korsakov Journal of Neurology and Psychiatry. 2019;119(11):32-36. (In Russ.). doi.org/10.17116/jnevro201911911132
15. The International Classification of Headache Disorders, 3rd edition (ICHD-3). Cephalalgia. 2018;38(1):1-211. doi.org/10.1177/0333102417738202
16. Kosinski M, Bayliss MS, Bjorner JB, et al. A six-item short-form survey for measuring headache impact: the HIT-6. Qual Life Res. 2003;12(8):963-974. doi.org/10.1023/a:1026119331193
17. Cho SJ, Song TJ, Chu MK. Sleep and Tension-Type Headache. Curr Neurol Neurosci Rep. 2019;19(7):44. doi.org/10.1007/s11910-019-0953-8
18. Shah N, Asuncion RMD, Hameed S. Muscle Contraction Tension Headache. [Updated 2024 Dec 11]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan. Available from: https://www.ncbi.nlm.nih.gov/books/NBK562274/
19. Осипова В.В. Дисфункция перикраниальных мышц при первичной головной боли и ее коррекция. Неврология, нейропсихиатрия, психосоматика. 2010;2(4):29-36.
Osipova VV. Pericranial muscle dysfunction in primary headache and its correction. Nevrologiya, neiropsikhiatriya, psikhosomatika =Neurology, Neuropsychiatry, Psychosomatics. 2010;2(4):29-36. (In Russ.). doi.org/10.14412/2074-2711-2010-113
20. Lee HJ, Cho SJ, Seo JG, et al. Update on Tension-type Headache. Headache Pain Res. 2025;26(1):38-47. doi.org/10.62087/hpr.2024.0025
21. Москалева П.В., Храмченко М.А., Карпенкова А.Д. и др. Современные представления о патогенезе головной боли напряжения и механизмах развития фенотипа головной боли напряжения и артериальной гипертензии. Российский неврологический журнал. 2022;27(2):22-33.
Moskaleva PV, Khramchenko MA, Karpenkova AD, et al. Modern concepts about pathogenesis of the tension-type headache and mechanisms of development of the tension-type headache and arterial hypertension phenotype. Russian Neurological Journal (Rossijskij Nevrologicheskiy Zhurnal). 2022;27(2):22-33. (In Russ.). doi.org/10.30629/2658-7947-2022-27-2-22-33
22. Путилина М.В. Роль артериальной гипертензии в развитии хронического нарушения мозгового кровообращения. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(9):124-128.
Putilina MV. The role of arterial hypertension in the development of chronic cerebrovascular accident. S.S. Korsakov Journal of Neurology and Psychiatry. 2014;114(9):124-128. (In Russ.).
23. Путилина М.В. Эндотелий — мишень для новых терапевтических стратегий при сосудистых заболеваниях головного мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(10):122-130.
Putilina MV. Endothelium as a target for new therapeutic strategies in cerebral vascular diseases. S.S. Korsakov Journal of Neurology and Psychiatry. 2017;117(10):122-130. (In Russ.). doi.org/10.17116/jnevro2017117101122-130
24. Li C, Huang H, Xia Q, Li Z. Association between sleep duration and chronic musculoskeletal pain in US adults: a cross-sectional study. Front Med. 2024;11(8):23386. doi.org/10.3389/fmed.2024.1461785
25. Kang MK. Tension-Type Headache and Primary Stabbing Headache: Primary Headaches Beyond Migraine. Headache Pain Res. 2025;26(2):89-90. doi.org/10.62087/hpr.2025.0007
26. Lee HJ, Cho SJ, Seo JG. Tension-type Headache. Headache Pain Res. 2025;26(1):38-47. doi.org/10.62087/hpr.2024.0025
27. Chen B, He Y, Xia L, et al. Cortical plasticity between the pain and pain-free phases in patients with episodic tension-type headache. J Headache Pain. 2016;17(1):105. doi.org/10.1186/s10194-016-0698-6
28. Путилина М.В., Ермошкина Н.Ю. Венозная энцефалопатия. Возможности диагностики и терапии. Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(9):89-93.
Putilina MV, Ermoshkina NYu. Venous encephalopathy. Diagnostic and therapeutic possibilities. S.S. Korsakov Journal of Neurology and Psychiatry. 2013;113(9):89-93. (In Russ.).
29. Журавлева М.В., Городецкая Г.И., Резникова Т.С. и др. Метаанали-тическая оценка клинической эффективности комплексного метаболического нейропротектора у больных с хронической ишемией головного мозга. Антибиотики и химиотерапия. 2021;66(9-10):39-53.
Zhuravleva MV, Gorodetskay GI, Reznikova TS, et al. Meta-analytical evaluation of the clinical efficacy of a complex metabolic neuroprotector in patients with chronic cerebral ischemia. Antibiot Khimioter=Antibiotics and Chemotherapy. 2021;66(9-10):39-53. (In Russ.). doi.org/10.37489/0235-2990-2021-66-9-10-39-53
30. Гудкова А.Н., Осиновская Н.А., Полунина А.Г., Гехт А.Б. Исследование влияния цитофлавина на симптомы депрессии и вегетативные нарушения у пациентов с органическим депрессивным расстройством. Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(12):50-55.
Gudkova AN, Osinovskaia NA, Polunina AG, Guekht AB. Investigation of the effects of cytoflavin on symptoms of depression and autonomic dysfunction in patients with organic depressive disorder. S.S. Korsakov Journal of Neurology and Psychiatry. 2013;113(12):50-55. (In Russ.).
31. Маджидова Е.Н., Юсупалиев Б.К., Шарипов Ф.Р. и др. Эффективность цитофлавина у пациентов с высоким риском развития цереброваскулярных заболеваний. Клиническая медицина. 2020;98(6):456-460.
Madzhidova YN, Yusupaliev BK, Sharipov FR, et al. Effectiveness of cytoflavin in patients with high risk development of cerebrovascular diseases. Clinical Medicine (Russian Journal). 2020;98(6):456-460. (In Russ.). doi.org/10.30629/0023-2149-2020-98-6-456-460
32. Строков И.А., Трахтенберг Ю.А., Коваленко А.Л. Эффективность и безопасность применения Цитофлавина в терапии диабетической полинейропатии: результаты многоцентрового двойного слепого плацебо-контролируемого рандомизированного исследования ЦИЛИНДР. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(5):100-107.
Strokov IA, Trakhtenberg YuA, Kovalenko AL. Efficacy and safety of Cyto-flavin in the treatment of diabetic polyneuropathy: results of a multicenter, double-blind, placebo-controlled, randomized CYLINDER study. S.S. Korsakov Journal of Neurology and Psychiatry. 2023;123(5):100-107. (In Russ.). doi.org/10.17116/jnevro2023123051100
33. Путилина М.В. Лекарственная безопасность как приоритетное направление отечественной медицины. Лечебное дело. 2019;4:7-14.
Putilina MV. Drug safety as a priority area of domestic medicine. General Medicine. 2019;4:7-14. doi.org/10.24411/2071-5315-2019-12152
Results of the observational program CITOTREK (use of the drug CITOflavin in Tablets) in patients with tension headaches against the backgRound of asthenic syndromE taking into account comorbidity
© M.V. PUTILINA1, N.I. SHABALINA2, I.A. BLINOVA3
'Pirogov Russian National Research Medical University, Moscow, Russia;
2Central Clinical Hospital «RZhD-Meditsina», Moscow, Russia; 3City Polyclinic No. 220, Moscow, Russia
Abstract
Objective. To study the efficacy and safety of Cytoflavin (Inosine + Nicotinamide + Riboflavin + Succinic Acid) tablets in the combination therapy of comorbid patients with tension-type headaches (TTH) associated with asthenic syndrome (AS).
Material and methods. The study included 150 patients aged 44.2+5.0 years, diagnosed with stage 1—2 arterial hypertension, severe asthenic syndrome. Frequent episodic TTH combined with pericranial muscle tension. All patients were randomly divided into 3 groups, age-matched, depending on the therapy they received: Group 1 — Nonsteroidal anti-inflammatory drugs — ibuprofen 400 mg) 7 days+tolperisone 150 mg 3 times a day for 14 days; Group 2 — ibuprofen 400 mg) 7 days+tolperisone 150 mg 3 times a day for 14 days+tablet form of Cytoflavin according to the protocol-approved regimen of 2 tablets 2 times per day for a duration of 25 days; Group 3 — ibuprofen 400 mg for 7 days and a tablet form of Cytoflavin according to the protocol approved regimen without the appointment of a muscle relaxant. All patients were examined on the day of treatment, on day 30±2, and after 60±2 days. A telephone survey was conducted on day 15. The analysis of the dynamics of complaints, clinical manifestations of TH, scale indicators, and Headache Diary data was conducted, and side effects of therapy were recorded. For clinical assessment, the following were used: the scale of asthenic conditions SHAS; headache index HIT-6; visual analog scale VAS; anxiety and depression scale HADS; Pittsburgh sleep quality questionnaire; quality of life assessment scales (EQ-5D) and overall clinical impression. Results. After the therapy, positive dynamics were observed on day 30+2 in all groups: a decrease in the frequency, duration, and intensity of TH, more pronounced in the groups with Cytoflavin. By day 60±2 there was a decrease in the number of TTH episodes in groups 2 and 3 by 76.7% and 62.5%, respectively, compared to the group receiving only standard therapy (group 1). The duration of TTH attacks decreased 32.3% (group 1), 62.96% (group 2) and 38.10% (group 3). In groups 2—3, the HIT-6 index decreased by 47%, VAS by 68% compared to standard therapy (p<0.001), manifestations of anxiety by 57.5% and depression by 68%; sleep disorders by 86% compared to the 1 group (p<0.001). The severity of asthenia in group 1 decreased by 37.9%; in group 2 — by 64.51%; in 3—58.77%. The quality of life of patients in groups 2—3 improved by 91% compared to 57% in the standard therapy group without Cytoflavin. During the observation period, no patient had serious adverse events or side effects associated with taking the drug.
Conclusion. The results of the study allow us to consider the drug Cytoflavin in the treatment regimens for comorbid patients with TTH in asthenic disorders.
Keywords: tension headache, asthenia, anxiety, depression, sleep disorders, Cytoflavin, inosine, nicotinamide, riboflavin, succinic acid.
Information about the authors:
Putilina M.V. - orcid.org/0000-0002-8655-850l
Shabalina N.I. - orcid.org/0000-0002-l8l4-353l
Blinova I.A. — orcid.org/0009-0009-85l9-13l2
Corresponding author: Putilina M.V. — e-mail: profput@mail.ru
To cite this article: Putilina MV, Shabalina Nl, Blinova 1A. Results of the observational program CITOTREK (use of the drug CITOflavin in Tablets) in patients with tension headaches against the backgRound of asthenic syndromE taKing into account comorbidity. S.S. Korsakov Journal of Neurology and Psychiatry. 2025; 125( 10): 104—112. (In Russ.). doi.org/10.17H6/jnevro2025125l01104
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)