Цитофлавин как компонент реабилитационного лечения пациентов с ишемическим инсультом, осложненным ПИТ-синдромом
Статьи
А.А. Белкин1, И.Н. Леидерман1, А.Л. Коваленко2, О.А. Ризаханова3, С.А. Парфенов4, К.В. Сапожников4
1АНО «Клинический институт мозга», Свердловская область, г. Березовский, Россия;
2ФГБУН «Институт токсикологии» ФМБА России, Санкт-Петербург, Россия;
3ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия;
4«Северо-Западный институт управления ФГБОУ ВО «Российская академия народного хозяйства и государственной службы при Президенте Российской Федерации», Санкт-Петербург, Россия
Резюме
Цель исследования. Оценка влияния Цитофлавина на результаты реабилитационного лечения и повышение толерантности к физической нагрузке у пациентов с инсультом, осложненным синдромом после интенсивной терапии (ПИТ).
Материал и методы. Проанализированы данные 53 пациентов, прошедших нейрореабилитацию в условиях отделения реанимации и интенсивной терапии после ишемического инсульта. В зависимости от схемы лечения больные были разделены на 2 группы: основную (n=36), в схему лечения которой в дополнение к комплексу нейрореабилитационных мероприятий был добавлен препарат Цитофлавин: в/в капельно в объеме 10 мл раствора для инъекций на 200 мл 0,9% раствора натрия хлорида в течение 10 дней, и группу сравнения (n=17), больным которой на протяжении 10 дней проводился только стандартный комплекс нейрореабилитационных мероприятий. Эффективность проводимой терапии оценивалась с помощью непрямой калориметрии, рассчитывался индекс кислородной и энергетической цены нагрузки. Для оценки переносимости методов реабилитации использовалась вертикализационная проба. Переносимость лечения оценивалась по частоте развития нежелательных реакций в каждой группе.
Результаты и заключение. Компоненты энерготропного действия, содержащиеся в препарате Цитофлавин, могут оказывать положительное модулирующее действие на повышение переносимости реабилитационных мероприятий по лечению синдрома последствий интенсивной терапии у пациентов с ишемическим инсультом. Требуются дальнейшие исследования.
Ключевые слова: нейрореабилитация, инсульт, толерантность к физическим нагрузкам, вертикализационная проба, Цитофлавин.
Cytoflavin as a modulator of rehabilitation treatment of patients with ischemic stroke complicated by post-intensive care syndrome
A.A. Belkin1, I.N. Leiderman1, A.L. Kovalenko2, O.A. Rizakhanova3, S.A. Parfenov4, K.V. Sapozhnikov4
1Clinical Institute of the Brain, Sverdlovsk Region, Berezovsky, Russia;
2Institute of Toxicology, Federal Biomedical Agency, St. Petersburg, Russia;
3Mechnikov North-Western State Medical University, St-Petersburg, Russia;
4North-West Institute of Management of RANEPA, St-Petersburg, Russia
Abstract
Objective. To assess an effect of cytoflavin on the results of rehabilitation treatment and the increase in exercise tolerance in patients with stroke complicated by post-intensive care syndrome (PICS).
Material and methods. The data of 53 patients who underwent neurorehabilitation in the ICU after ischemic stroke were analyzed. Depending on the treatment regimen, the patients were divided into two groups. Group 1 (main, n=36) received cytoflavin (iv drip in a volume of 10 ml of a solution for injections per 200 ml of a 0,9% solution of sodium chloride) for 10 days in addition to the complex of neurorehabilitation measures. Group 2 (control, n=17) included patients, who had only a standard set of neurorehabilitation measures for 10 days. The efficacy of the therapy was evaluated using indirect calorimetry, and the oxygen and energy load price index was calculated. To assess the tolerability of rehabilitation methods, a verticalization test was used. Treatment tolerance was assessed by the incidence of adverse reactions in each group.
Results and Conclusion. The components of the energytropic effect of cytoflavin can have a positive modulating effect, increasing the tolerance of rehabilitation measures for the treatment of PICS in patients with ischemic stroke. Further research is required.
Keywords: neurorehabilitation, stroke, exercise tolerance, verticalization test, cytoflavin.
Приоритетной задачей терапии любой неотложной патологии является восстановление исходного уровня состояния. Если раньше единственным критерием эффективности интенсивной терапии было сохранение жизни пациента, то теперь, по мере развития этой дисциплины и неуклонного снижения летальности, все актуальнее становится показатель «качество жизни после выписки из госпиталя» [1].
Использование для спасения пациента активных стратегий лечения (искусственная вентиляция легких, глубокая седация и пр.) приводит к формированию после купирования критического состояния новых патологических детерминант, объединенных в понятие синдром «После Интенсивной Терапии» (ПИТ-синдром, или PICS (Post Intensive Care Syndrome)). ПИТ-синдром — совокупность ограничивающих повседневную жизнь пациента соматических, неврологических и социально-психологических последствий пребывания в условиях отделения реанимации и интенсивной терапии (ОРИТ). Патофизиологическую основу ПИТ-синдрома составляет состояние вынужденной иммобилизации в постели, создающее нефизиологические ограничения двигательной и когнитивной активности пациента. По статистике, частота развития ПИТ-синдрома у пациентов с острой церебральной недостаточностью и длительностью пребывания в ОРИТ >48 ч достигает 55—98% [2]. Наиболее тяжелыми клиническими формами ПИТ-синдрома являются полимионейропатия критических состояний (ПМКС) и снижение гравитационного градиента (ГГ).
ПМКС — это приобретенный вследствие критического состояния синдром нервно-мышечных нарушений по типу полинейропатии и/или миопатии, клинически проявляющийся диффузной мышечной слабостью, симметричными вялыми парезами. Клиническим критерием диагноза является уровень снижения силы в конечностях при оценке по шкале Medical Research Council (MRC) <4 баллов, выявленный дважды с интервалом >24 ч в непарализованных конечностях [3].
ГГ — максимальный угол подъема пациента, не приводящий к развитию признаков ортостатической недостаточности. Нормальное значение соответствует 90°. ГГ отражает способность поддержания витальных параметров стабильными в любом положении тела по отношению к гравитационному полю Земли [4].
Основной стратегией профилактики и лечения ПИТ-синдрома является ранняя кинезитерапия, в частности вертикализация и пассивные велокинетические тренировки [5]. Одной из проблем процесса реабилитации больных с ПИТ-синдромом является риск развития жизнеугрожающих состояний (острый коронарный синдром, аритмии, дыхательная недостаточность, инфаркт миокарда, тромбоэмболия легочной артерии), которые связаны в том числе со сниженной толерантностью к физическим нагрузкам и дисбалансом метаболического статуса [6].
Наличие ПИТ-синдрома осложняет реабилитационный процесс, особенно у пациентов с первичным очаговым поражением нервной системы на фоне острого нарушения мозгового кровообращения и черепно-мозговой травмы. Ортостатическая недостаточность в результате снижения ГГ затрудняет процесс вертикализации. Диффузная мышечная слабость на фоне ПМКС замедляет регресс первичного двигательного дефицита.
Это мотивирует поиск фармакологических агентов, способных модулировать реабилитационный процесс, в частности повысить устойчивость пациента к нагрузкам разных модальностей. Как одно из перспективных в этом направлении лекарственных средств можно рассматривать Цитофлавин (ООО «НТФФ» ПОЛИСАН», Россия) — препарат на основе янтарной кислоты, обладающий тропностью к мышечной и нервной тканям, энергопротектор с системной фармакодинамикой, основанной на сигнальном (гормональном) и субстратном механизмах действия янтарной кислоты и других митохондриальных субстратов и кофакторов [7]. Цитофлавин представляет собой лекарственное средство, разработанное на основе комбинации янтарной кислоты (100 мг) с инозином (20 мг), никотинамидом (10 мг) и рибофлавином (2 мг). Комплексное действие этих метаболитов и коферментов анаэробного и аэробного гликолиза способно влиять на синтез аденозинтрифосфата (АТФ), предотвращая прогрессирование метаболического и окислительного дисбалансов, вызванных ишемией [8, 9].
Учитывая принадлежность препарата к классу метаболотропных энергокорректоров, представляет интерес изучение эффективности и переносимости Цитофлавина в комплексной программе нейрореабилитации больных с ПИТ-синдромом после инсульта. Ключевой проблемой в исследованиях, посвященных оценке переносимости физических нагрузок в ходе реабилитации, является отсутствие адекватных методов прикроватного мониторинга. Ее решением стало применение метода непрямой калориметрии с использованием штатного метаболографа [10]. Основываясь на этом подходе, было проведено исследование «Реабилитация ПИТ-синдрома. Цитофлавин». «PICS-Rehabilitation — Cytoflavin» NCT04194229.
Цель исследования — оценка влияния Цитофлавина на результаты реабилитационного лечения и повышение толерантности к физическим нагрузкам у пациентов с инсультом, осложненным ПИТ-синдромом.
Материал и методы
Наблюдательное исследование проведено на базе Клинического института мозга (Екатеринбург) на пациентах, госпитализированных для курса реабилитации непосредственно после завершения 1-го этапа лечения в первичных сосудистых отделениях по поводу ишемического инсульта.
Критерии включения: пациенты, перенесшие ишемический инсульт, находившиеся в ОРИТ не менее 3 сут с признаками ПИТ-синдрома: ПМКС с уровнем слабости по шкале MRC (Medical Research Council) <48 баллов и снижение ГГ ниже 60° [2, 4, 11].
Критерии невключения: тяжелая сопутствующая патология и/или состояние, включающее острую недостаточность одной или нескольких систем органов; гнойно-воспалительные заболевания любой локализации; иные значительные отклонения от нормы, в том числе по результатам клинических и лабораторных исследований; хирургическое лечение поражения ЦНС; применение других метаболических средств, кроме Цитофлавина, применение физических методов реабилитации, кроме вертикализации и велокинетических тренировок в период проведения исследования, отказ пациента от проведения вертикализации, велокинетических тренировок.
Критерии исключения: несоблюдение либо невозможность соблюдения режима терапии и проведения диагностических процедур в соответствии с протоколом; отказ от проведения реабилитационных мероприятий в полном запланированном объеме; назначение других метаболических средств, кроме Цитофлавина, либо физических методов реабилитации, кроме вертикализации и велокинетических тренировок, отказ пациента от проведения вертикализации, велокинетических тренировок.
Наблюдение за пациентами осуществлялось в течение 10 дней с записью данных в индивидуальные регистрационные карты.
Всего для участия в исследовании были отобраны 53 пациента, разделенные на 2 группы. В схему лечения пациентов группы 1 (основная, п=36) к комплексу нейрореабилитационных мероприятий (программа вертикализации, велокинетические тренировки) по решению лечащего врача был добавлен препарат Цитофлавин: в/в капельно в объеме 10 мл раствора для инъекций на 200 мл 0,9% раствора натрия хлорида в течение 10 дней. Больным группы 2 (сравнения, п=17) на протяжении 10 дней проводился только стандартный комплекс нейрореабилитационных мероприятий без назначения препарата Цитофлавин.
Реабилитационные мероприятия (вертикализация, вело-кинетические тренировки) проводились специально обученным персоналом. Вертикализация осуществлялась в соответствии с клиническими рекомендациями [9]. Энергетическая стоимость реабилитационных мероприятий оценивалась с использованием непрямой калориметрии (метаболический мониторинг), основанной на одновременном измерении показателей потребления кислорода и экскреции углекислоты в условиях спонтанного или аппаратного дыхания. Для оценки толерантности к нагрузкам использовался индекс кислородной и энергетической цены нагрузки:
— индекс кислородной цены нагрузки (ieVo2, мл/кг/мин/ нагрузка (Вт));
— индекс энергетической цены нагрузки (eREE, кКал/ кг/сут/нагрузка (Вт)).
Пограничным значением индекса кислородной цены нагрузки при высокой толерантности считалось значение <0,5 мл/кг/Вт.
Для оценки переносимости методов реабилитации использовалась вертикализационная проба под контролем тонометрии артериального давления, частоты сердечных сокращений и электрокардиограммы с учетом индивидуальных особенностей пациента, отличающаяся тем, что дополнительно у больного определяют сердечный индекс, общее периферическое сопротивление сосудов, потребление кислорода и фактическую энергопотребность. Затем осуществлялась кинезитерапия на верхних и нижних конечностях в пассивном режиме, в последующем и в режиме активной нагрузки выделялось по 5 мин на каждый вариант нагрузок. Если 2 из измеренных показателей и более изменялись на >30% от исходных значений — расценивали как «стоп-точку» и занятие прекращали. Если указанные выше параметры существенно не менялись при проведении 5-минутных нагрузок в режиме: угол вертикализации 0, 20, 40, 60, 80°, то данные мониторинга заносили в регистрационную карту для фиксации переносимости больным активных нагрузок, которые не вызывают развития побочных реакций и осложнений.
Для анализа были выбраны следующие данные:
— пол, возраст, соматический статус;
— количество дней до достижения целевого ГГ 80—90° — если пациент за 10 дней не достигал его, то ставилась отметка «не достиг»;
— значения шкал Рэнкина, Бартел, шкалы слабости (MRC) на 1—5—10-й день;
— переносимость лечения оценивалась по частоте развития нежелательных реакций в каждой группе;
— данные энергозатрат на вертикализацию и велокинетическую тренировку в последний день наблюдения. Из них интерес представляли интегральные показатели: кислородная и энергетическая цена велокинетической нагрузки, энергетическая цена вертикализации.
Статистическая обработка полученных данных проводилась на базе персонального компьютера в табличном процессоре Excel 2013 и пакете прикладных программ SPSS Statistics 22,0. Доверительные интервалы для частот рассчитывались с применением метода Вальда с коррекцией по Агре-сти—Коулу. Анализ качественных данных производился в режиме четырехпольных таблиц сопряженности с помощью критерия χ 2 Пирсона, при необходимости к нему применялась поправка Йейтса на непрерывность (критический уровень значимости p=0,05). При анализе количественных данных на первом этапе выполнялась оценка нормальности распределения изучаемых параметров с помощью критерия Шапиро—Уилка. Работа с выбросами ввиду малого размера групп не проводилась, возможное искажение данных выбросами компенсировано применением непараметрического инструментария (поправок к параметрическому). Независимые выборки сравнивались по критерию Краскелла—Уоллиса (критический уровень значимости /=0,05). Динамика по ранговым шкалам (Бартел и Рэнкина) оценивалась критерием Фридмана, динамика шкалы MRC — при помощи ANOVA в режиме общей линейной модели с повторными измерениями, с предварительной проверкой сферичности критерием Моучли и поправками по Грингаузу—Гайссеру и Хуинн—Фельдту. Апостериорные сравнения проводились с помощью Т-критерия Вилкоксона с поправкой Бонферрони для сравнения трех этапов (скорректированный p=0,017) и по Шидаку соответственно. Для оценки влияния исходного статуса пациентов на успешность применения Цитофлавина случаи, не имеющие к концу наблюдения индекса вертикали-зации 80—90°, считали как безуспешные. Также производился расчет относительного риска (relative risk — RR), показывающего, во сколько раз возрастет риск возникновения негативного исхода, т.е. недостижения ГГ 80—90°, при отсутствии Цитофлавина в терапии. Показатель представляется в виде Х (нижняя граница 95% ДИ; верхняя граница 95% ДИ), где Х— величина RR, ДИ — доверительный интервал. Расчет показателя Number Needed to Treat (NNT). Чем меньше величина NNT, тем выше эффективность добавления Цитофлавина к стандартной терапии. Рассчитано с помощью онлайн-калькулятора: medstatistic.ru/calculators/calcrisk.html. В качестве фактора риска рассмотрено состояние «цитофлавин не назначался», в качестве исхода рассмотрено значение «не достиг». Анализ выживаемости проведен по Каплан—Майер с оценкой влияния назначения Цитофлавина с помощью регрессии Кокса и сравнением кривых с помощью критерия Мантел—Кокса. Под «выживаемостью» понимается процент пациентов, достигших ГГ 80—90°. Оценивался «риск» сесть у пациентов при приеме Цитофлавина и без него.
Результаты
Выявлено, что половозрастной состав в группах не отличался: медиана возраста в группе 1 составила 61 (40; 71) год, в группе 2 — 50 (40; 62) лет, группы были сопоставимы по количеству мужчин — 52,78% (36,19%; 68,82%) в группе 1 и 58,83% (33,62%; 80,67%) в группе 2. За весь период наблюдения не выявлено ни одного нежелательного явления, связанного с приемом Цитофлавина. Результаты сравнения групп по результативности нейрореабилитации представлены в табл. 1.
Первичные значения шкалы Рэнкина также не отличались. В группе Цитофлавина значимо выше был исходный показатель шкалы Бартел, который остался таковым по сравнению с группой сравнения во втором и третьем измерениях. Во втором измерении шкала Рэнкина в основной группе оказалась значимо ниже, чем в группе сравнения, однако к третьему измерению различий уже не было. Значимые различия по шкале MRC имели место при втором измерении.
Таблица 1.
Результаты нейрореабилитации
Table 1.
The results of neurorehabilitation
|
Шкала, баллы
|
Группа 1 (n=36)
|
Группа 2 (n=17)
|
Достоверность
|
|
Рэнкин на 1-е сутки
|
5 (5; 5)
|
5*
|
χ2=1,47
p=0,225
|
|
Рэнкин на 5-е сутки
|
5 (4; 5)
|
5*
|
χ2=6,43
p=0,011
|
|
Рэнкин на 10-е сутки
|
4 (4; 5)
|
5 (4; 5)
|
χ2=1,5
p=0,221
|
|
Бартел на 1-е сутки
|
4 (4; 5)
|
4 (4; 4)
|
χ2=8,97
p<0,01
|
|
Бартел на 5-е сутки
|
4 (4; 6)
|
4 (4; 4,5)
|
χ2=4,89
p=0,027
|
|
Бартел на 10-е сутки
|
5 (4; 9)
|
4 (4; 6,5)
|
χ2=4,46
p=0,035
|
|
MRC на 1-е сутки
|
30 (19,25; 39)
|
18 (12,5; 30)
|
χ2=3,45
p=0,063
|
|
MRC на 5-е сутки
|
32 (23; 40,75)
|
18 (12,5; 30)
|
χ2=4,47
p=0,034
|
|
MRC на 10-е сутки
|
34 (23; 45)
|
30 (14; 36)
|
χ2=2,21
p=0,138
|
Примечание. * — значение в группе представляет собой константу, описательная статистика не вычисляется. Значимые различия выделены жирным.
Note. * — the value in the group is a constant, descriptive statistics are not calculated, significant differences are highlighted in bold.
Таблица 2.
Результаты нейрореабилитации по вертикализации
Table 2.
The results of neurorehabilitation verticalization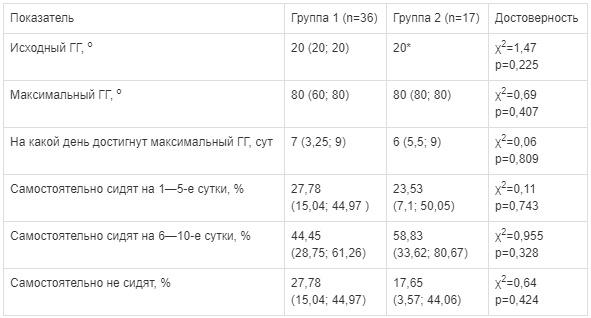 Примечание. * — значение в группе представляет собой константу, описательная статистика не вычисляется.
Примечание. * — значение в группе представляет собой константу, описательная статистика не вычисляется.
Note. * — the value in the group is a constant, descriptive statistics are not calculated.
По скорости вертикализации группы не различались (табл. 2). По доле негативных исходов, т.е. недостижения вертикализации, различий между группами также не было. Число пациентов, способных самостоятельно сесть, на 1—5-е и 6—10-е сутки в группах не различалось.
Комплексная оценка динамики показателей шкал Рэнкина, Бартел, MRC представлена в табл. 3.
Согласно полученным данным (см. табл. 3), в группе 1 динамика была более выражена по сравнению с группой 2: интегральный показатель оказался на 33,23% больше.
Таблица 3.
Результаты комплексной оценки динамики неврологического дефицита
Table 3.
The results of a comprehensive assessment of the dynamics of neurological deficit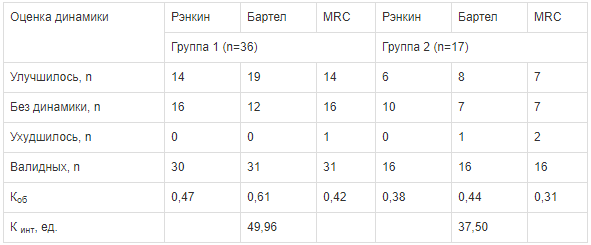 Примечание. Кинт — интегральный коэффициент динамики нескольких показателей в малых группах.
Примечание. Кинт — интегральный коэффициент динамики нескольких показателей в малых группах.
Note. Кинт — integral coefficient of dynamics of several indicators in small groups.
Таблица 4.
Данные оценки энергозатрат
Table 4.
Energy evaluation data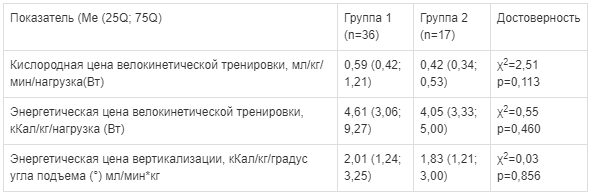 Рассматривая динамику каждого индекса в отдельности, отметим, что в группе сравнения значимо отличались значения по шкале Ренкина на третьем измерении от первых двух, в то время как в группе Цитофлавина значимая положительная динамика была на всех этапах изменения шкал Рэнкина и Бартел, а также на третьем измерении MRC по сравнению со вторым.
Рассматривая динамику каждого индекса в отдельности, отметим, что в группе сравнения значимо отличались значения по шкале Ренкина на третьем измерении от первых двух, в то время как в группе Цитофлавина значимая положительная динамика была на всех этапах изменения шкал Рэнкина и Бартел, а также на третьем измерении MRC по сравнению со вторым.
Таким образом, можно предположить положительное влияние Цитофлавина на качество реабилитации. Результаты оценки энергозатрат на велокинетическую тренировку и вертикализацию представлены в табл. 4.
У пациентов не происходило достоверного изменения показателей кислородной и энергетической цены велокинетической тренировки и вертикализации в группе, которая получала Цитофлавин. Несмотря на отсутствие статистически значимых различий, можно увидеть сочетанную тенденцию нескольких показателей к увеличению энергозатрат на вертикализацию и велокинетическую тренировку в группе Цитофлавина, что косвенно указывает на повышение потребления кислорода и калорий в процессе реабилитации на фоне введения препарата.
По результатам дискриминантного анализа с включением таких переменных, как пол, возраст, соматический статус, первичные данные шкал Рэнкина, Бартель и MRC, предикторов, оказывающих отрицательное или положительное влияние на успешность применения Цитофлавина, не выявлено. Все переменные исключены из анализа, валидная математическая модель не построена. При отсутствии приема Цитофлавина риск не достигнуть вертикализации значимо не увеличивается (RR 0,635 (0,200; 2,015)). Для того, чтобы предотвратить такой исход у 1 пациента, необходимо давать Цитофлавин 10 больным (NNT=9,87). Анализ выживаемости показал, что вероятность самостоятельно сидеть у пациентов, получавших Цитофлавин, не отличается от таковой у пациентов, не получавших препарат (см. рисунок). Оценка влияния Цитофлавина на достигаемость требуемого ГГ, проведенная с помощью расчета регрессии Кокса (p=0,766) и сравнения кривых с помощью критерия Мантел—Кокса (χ2=0,11; p=0,741), показала отсутствие влияния препарата на данный показатель.
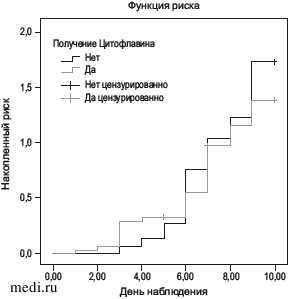
Оценка «риска» достичь целевого ГГ.
Assessment of the «risk» to reach the target gravitational coefficient.
Резюмируя данные статистики, можно выделить несколько ключевых результатов:
— имеется некоторое положительное влияние раствора Цитофлавина в дозировке 10 мл/сут внутривенно капельно курсом 10 дней на качество реабилитационных мероприятий при поражениях ЦНС, которое заключается в более выраженной положительной динамике индексов, характеризующих неврологический дефицит, при сопоставлении с группой сравнения;
— пол, возраст, соматическое состояние не влияют на эффективность применения Цитофлавина у пациентов с поражением ЦНС;
— переносимость Цитофлавина при комплексной реабилитации поражений ЦНС оценивается как хорошая.
Обсуждение
В ходе проведенного исследования было выявлено, что включение Цитофлавина в качестве компонента реабилитационного процесса пациентам с ишемическим инсультом, осложненным ПИТ-синдромом, не улучшает интегральные показатели состояния. Если не считать некоторых отличий в динамике уровня независимости по шкале Рэнкин, прочие показатели не отреагировали на фармакомодуляцию. Не получены достоверные отличия в показателях энергозатрат, производимых пациентами при восстановлении ГГ при вертикализации и велокинетических тренировках. Тем не менее отчетливо проявилась тенденция к увеличению потребления кислорода на фоне инфузионного применения препарата. Иными словами, гипотеза о энерготропном влиянии комбинации янтарной кислоты (100 мг) с инозином (20 мг), никотинамидом (10 мг) и рибофлавином (2 мг) на восстановление мышечной активности, необходимой для обеспечения ГГ и баланса прямостояния, не отвергнута. По нашему мнению, основным фактором, способным усилить модулирующий эффект Цитофлавина, может быть более раннее назначение терапии. Действительно, осложнения иммобилизации развиваются после 48 ч пребывания в ОРИТ. Ранняя реабилитация начинается в это же время. Следовательно, одновременно должна быть начата и модулирующая фармакотерапия. Это будет учтено в дизайне последующих исследований. Бесспорным достижением проведенного исследования следует признать эффективность применения метаболографии для мониторинга энергетического баланса реабилитационного процесса.
Вывод
Компоненты энерготропного действия, содержащиеся в препарате Цитофлавин, могут оказывать положительное модулирующее действие на повышение переносимости реабилитационных мероприятий по лечению ПИТ-синдрома. Требуются дальнейшие исследования.
ЛИТЕРАТУРА/REFERENCES
1. Pun BT, Balas MC, Barnes-Daly MA, Thompson JL, Aldrich JM, Barr J, Byrum D, Carson SS, Devlin JW, Engel HJ, Esbrook CL, Hargett KD, Harmon L, Hielsberg C, Jackson JC, Kelly TL, Kumar V, Millner L, Morse A, Perme CS, Posa PJ, Puntillo KA, Schweickert WD, Stollings JL, Tan A, D’Agostino McGowan L, Ely EW. Caring for Critically Ill Patients With the ABCDEF Bundle: Results of the ICU Liberation Collaborative in Over 15,000. Adults Crit Care Med. 2019 Jan;47(1):3-14.
2. Белкин АА. Синдром последствий интенсивной терапии (ПИТ-синдром). Вестник интенсивной терапии им. А.И. Салтанова. 2018;2:12-23.
Belkin AA. Syndrome of the consequences of intensive care (pit syndrome). Vestnik intensivnoj terapii im. A.I. Saltanova. 2018;2:12-23. (In Russ).
3. Белкин А.А., Алашеев А.М. Нейромышечные расстройства. Национальное руководство по интенсивной терапии. Т.1. М. 2009;357-360.
Belkin AA, Alasheev AM. Neyromyishechnyie rasstroystva. Natsionalnoe rukovodstvo po intensivnoy terapii. T.1. M. 2009;357-360. (In Russ).
4. Balocchi R, Di Garbo A, Michelassi C, Chillemi S, Varanini M, Barbi M, Legramante JM, Raimondi G, Zbilut JP: Heart rate and blood pressure response to short-term head-down bed rest: a nonlinear approach. Methods Inf Med. 2000; 39:157-159.
5. Белкин А.А., Алашеев А.М., Давыдова Н.С., Левит А.Л., Халин А.В. Обоснование реанимационной реабилитации в профилактике и лечении синдрома «после интенсивной терапии» (ПИТ-синдром). Вестник восстановительной медицины. 2014;1:37-43.
Bel kin AA, Alasheev AM, Davyidova NS, Levit AL, Khalin AV. Basing for emergency rehabilitation in the prevention and treatment of «post intensive care» syndrome (PIC syndrome). Vestnik vosstanovitel noy meditsinyi. 2014;1:37-43. (In Russ).
6. Lan Zhang, Weishu Hu, Zhiyou Cai, Jihong Liu, Jianmei Wu, Yangmin Deng, Keping Yu, Xiaohua Chen, Li Zhu, Jingxi Ma, Yan Qin. Early mobilization of critically ill patients in the intensive care unit: A systematic review and meta-analysis. Pios One. 2019 Oct 3;14(10):e0223185.
7. Антонов А.Г., Буркова А.С., Им В.Л., Рогаткин С.О. Эффективность применения цитофлавина в интенсивной терапии недоношенных новорожденных с церебральной ишемией. Российский вестник перинатологии и педиатрии. 2010;55(1):26-32.
Antonov AG, Burkova AS, Im VL, Rogatkin SO. Efficiency of using cyto-flavin in intensive therapy of premature neonates with cerebral ischemia Rossijskij vestnik perinatologii i pediatrii. 2010;55(1):26-32. (In Russ).
8. Романцов М.Г., Коваленко АЛ., Суслина З.А., Клочева Е.Г., Румянцева СА, Багненко СФ. Фармакотерапевтическая эффективность Цитофлавина в интенсивной терапии жизнеугрожаемых состояний (клинический обзор). Профилактическая и клиническая медицина. 2009;2: 125-133. Romantsov MG, Kovalenko AL, Suslina ZA, Klocheva EG, Rumyantseva SA, Bagnenko SF. Pharmacotherapeutic efficacy of Cytoflavin in intensive care of life-threatening conditions (clinical review). Profilakticheskaya i klinicheskaya meditsina. 2009;2:125-133. (In Russ).
9. Патент RU № 2497447. Способ оценки переносимости методов реабилитации у больных с острой церебральной недостаточностью.
Patent RU No. 2497447. A method for assessing the tolerability of rehabilitation methods in patients with acute cerebral insufficiency. (In Russ).
10. Белкин А.А., Алашеев А.М., Давыдова Н.С., Лейдерман И.Н., Почеп-ко Д.В., Халин А.В. Гравитационный градиент при bed-rest режиме у пациентов с острой церебральной недостаточностью. Вестник Уральской медицинской академической науки. 2015;1(52):22-28.
Belkin AA, Alasheev AM, Davydova NS, Lejderman IN, Pochepko DV, Khalin AV. Gravity gradient in bed-rest mode in patients with acute cerebral insufficiency. Vestnik Ural’skoj meditsinskoj akademicheskoj nauki. 2015;1(52):22-28. (In Russ).
11. Вертикализация пациентов в процессе реабилитации. Клинические рекомендации. М., 2014.
Verticalization of patients during rehabilitation. Clinical recommendations. M., 2014. (In Russ).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)