Урогенитальный хламидиоз: Современные аспекты урогенитальной хламидийной инфекции
Статьи
Опубликовано в:
УРОГЕНИТАЛЬНЫИ ХЛАМИДИОЗ
Иркутск, 2007
1.1. Медицинское, эпидемиологическое и социальное значение хламидийной инфекции
Актуальность ИППП объясняется широким распространением и высоким уровнем заболеваемости населения по всему миру (Аковбян В. А. и др., 1998). В России в 2004 г. зарегистрировано свыше 700 тысяч больных с ИППП, при этом показатель заболеваемости составил 517,1 случая на 100 тысяч населения (Кубанова А. А., Тихонова Л. И., 2005).
Урогенитальная инфекция, вызванная С. trachomatis, обусловленная серотипами D-K, является наиболее распространенной ИППП как у мужчин, так и у женщин в странах Европы (Тоскин И. А. и др., 2000; Stary A., 2000), США (Коэн К. Р., Бранэм Р. К., 1999; Centers for Disease Control and Prevention (CDC), 2004; Miller W. С et al., 2004) и Канаде (Федотов В. П. и др., 2005). УГХ встречается в 2-5 раз чаще гонореи (Сухова Л. П. и др., 2000; Федотов В. П. и др., 2004) и в 7,5 раза чаще сифилиса (Лебедев В. А., Давыдов А. И., 2002).
Примечателен тот факт, что с 1994 г. УГХ включен в группу инфекционных заболеваний, подлежащих обязательному статистическому учету, что подчеркивает медико-социальную значимость данной патологии (Светачев М. М., Юрасов И. В., 2002). За период с 1995 по 2000 г. заболеваемость возросла более чем в 3 раза (на 40%) (Кубанова А. А., 2002). Так, по официальным данным, в 2000 г. частота регистрации УГХ в России составила 126,2 на 100 тысяч населения. В последние годы наблюдается тенденция к некоторому снижению случаев выявления УГХ в Российской Федерации (Кубанова А. А., 2002): заболеваемость в 2002 г. составила 107,4, а в 2003 — 101,0 на 100 тысяч населения (Ресурсы и деятельность кожно-венерологических учреждений. Заболеваемость за 2002-2003 годы (статистические материалы), 2005). Между тем уровень заболеваемости УГХ в различных регионах России подвержен существенным колебаниям.
Так, регистрация УГХ в Сибирском федеральном округе несколько ниже общероссийской и составляет 90,5 на 100 тысяч (в 2003 г.), в то время как в Иркутской области этот показатель один из самых высоких в регионе — 181,8 на 100 тысяч населения (Ресурсы и деятельность кожно-венерологических учреждений. Заболеваемость за 2002-2003 годы (статистические материалы), 2005). Однако представленные цифры, по-видимому, не отражают реальной картины заболеваемости. Существует мнение, что в действительности истинная заболеваемость значительно превышает данные официальной статистики (Иванов О. Л. и др., 2002; Халдин А. А., 2004), имея признаки эпидемии (Молочков В. А., Зур Н. Н., 2003). По некоторым оценкам, в Российской Федерации в год заболевает УГХ от 1,5 до 2 млн человек (Калинина С. Н. и др., 2003), при этом в большинстве наблюдений этиологический диагноз болезни не устанавливается (Лебедев В. А., Давыдов А. И., 2002). Удельный вес хламидийной инфекции среди ИППП по некоторым данным составляет 30-50% (Светачев М. М., Юрасов И. В., 2002), а С. trachomatis является наиболее частым возбудителем негонококковых уретритов (Молочков В. А., Зур Н. Н., 2003; Kilic D. et al., 2004). Уровень заболеваемости достаточно высок не только среди взрослого населения и подростков, ведущих активную половую жизнь, но и среди детей младшего возраста, не живущих половой жизнью. Так, при обследовании мальчиков до 12 лет, обратившихся в детский кабинет УГИ, у 67,4% была выявлена С. trachomatis. При этом клиническая картина УГХ соответствовала уретриту, а у 7,9% детей по УЗИ имелись следы перенесенного простатита (Малова И. О., Сокольникова Н. В., 2001).
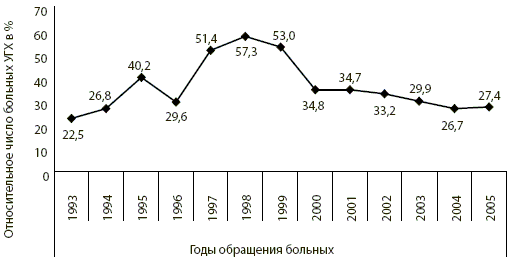
Анализ структуры ИППП в мужском кабинете анонимного обследования и лечения клиник Иркутского медицинского университета показал, что УГХ занимает значительную долю среди УГИ. Регистрация УГХ в кабинете ведется с 1993 года, когда наблюдалась самая низкая заболеваемость данной инфекцией и составляла 22,5% от всех выявленных в этом году ИППП (рис. 1). В течение 13 лет наблюдалось увеличение доли УГХ в структуре урогенитальной патологии с пиком регистрации в 1998 году (57,3%). Затем заболеваемость хламидийной инфекцией постепенно снижалась, составив 27,4% среди всех выявленных в 2005 году.
Рис. 1. Доля урогенитального хламидиоза в структуре ИППП по данным кабинета анонимного обследования и лечения
Кроме того, исследованиями было показано, что наличие УГХ способствует заражению и передаче половому партнеру ВИЧ-инфекции (Centers for Disease Control and Prevention (CDC), 2002; Nusbaum M. R. et al., 2004), при этом штаммы ВИЧ, выделенные от таких больных, обладают более высокой степенью вирулентности (Молочков В. А., 2004).
Согласно определению К. D. E. Everett et al. (1999), порядок Chlamydiales включает облигатные внутриклеточные бактерии, которые характеризуются наличием грамположительных или грамотрицательных инфекционных элементарных телец с более чем восьмидесятипроцентным уровнем гомологии по последовательности 16S и 23S рРНК генов. С. trachomatis является представителем рода Chlamydia и обладает способностью накапливать гликоген в цитоплазматических вакуолях. С. trachomatis является паразитом исключительно человека и относится к безусловно-патогенным микроорганизмам (Кисина В. И. и др., 2003).
С. trachomatis обладает уникальным внутриклеточным циклом развития, в котором выделяют две формы возбудителя: «элементарные тельца» — адаптированные к внеклеточному существованию, диаметром 0,2-0,3 мкм, устойчивые к факторам внешней среды и малочувствительные к действию антибактериальных препаратов. «Ретикулярные тельца» — внутриклеточные спороподобные, диаметром 0,5-1,0 мкм, метаболически активные, живущие за счет АТФ клетки-хозяина, обеспечивающие репродукцию, не способные к выживанию вне клетки.
Современная классификация урогенитальной хламидийной инфекции подразделяется на хламидийную инфекцию нижних отделов (неосложненную) (эндоцервицит, уретрит, цистит, вульвовагинит) и инфекцию верхних отделов мочеполового тракта (осложненную) (эпидидимит, воспалительные заболевания органов малого таза у женщин, орхит).
Кроме того, выделяют хламидийную инфекцию аноректальной области, хламидийные фарингиты, а также хламидийную инфекцию других локализаций. Роль С. trachomatis как этиологического фактора в развитии болезни Рейтера — самой частой причины острых артритов у мужчин в возрасте 18-40 лет — в настоящее время не вызывает сомнений. Более того, данное заболевание рассматривается как наиболее тяжелое осложнение УГХ с генетически обусловленным дефектом иммунной системы.
Приобретенные при сексуальных контактах С. trachomatis чаще всего вызывают уретриты или эндоцервициты, реже встречаются конъюнктивиты, проктиты и фарингиты.
В последнее время достаточно много исследований посвящено изучению биологии и морфологии возбудителя. Кроме того, благодаря проведенным эпидемиологическим, клиническим, патогистологическим исследованиям, разработаны достаточно чувствительные и специфичные методы диагностики (Хамидуллин Р. Ф., 2000). Созданы новые антибактериальные препараты, схемы и методы лечения. Тем не менее заболеваемость УГХ продолжает повсеместно увеличиваться (Шинский Г. Э. и др., 1999).
Причинами достаточно высокой заболеваемости УГХ в настоящее время являются как биологические особенности возбудителя, так и социально-экономические факторы (Молочков В. А., 2004). К первым можно отнести увеличение частоты выявления персистентных форм возбудителя, устойчивых к противохламидийным антибиотикам, вызванное их бесконтрольным и нерациональным приемом, а также самолечением (Рентой А. М. и др., 1999; Лебедев В. А., Давыдов А. И., 2002; Николаева Н. В., 2003; Охотникова Л. А., Обухов А. П., 2003). Социальными факторами являются демографические сдвиги — рост численности одиноких лиц, повышение частоты бракоразводных процессов, увеличение городского населения, развитие туризма, безработица, материальная необеспеченность, поведенческие факторы риска: ранний возраст вступления в половую жизнь, частая смена половых партнеров, коммерциализация сексуальных отношений, промискуитет, наркомания, алкоголизм, невысокий уровень информированности об ИППП и средствах предохранения (Довжанский С. И., 1998; Калмыкова Т. Д., Мухамадеев Р. X., 2000; Лебедев В. А., Давыдов А. И., 2002; Рассказов Д. Н. и др., 2003; Юцковский А. Д. и др., 2005; Haley N. et al., 2002). Кроме того, УГХ имеет тенденцию к длительному торпидному и малосимптомному характеру течения (Бурчик В. К. и др., 2003; Молочков В. А., Зур Н. Н., 2003; Юцковский А. Д. и др., 2005). При рутинном скрининге или обследовании половых партнеров все чаще обнаруживают С. trachomatis у лиц без каких-либо симптомов или признаков урогенитальной инфекции (Мерзляков В. А. и др., 1999; Анчупане И. С, Милтинып А. П., 2000; Потекаев Н. С. и др., 2000; Сухова Л. П. и др., 2000; Тоскин И. А. и др. 2000; Иванов О. Л. и др., 2002; Кисина В. И. и др., 2003; Хрянин А. А., 2004; Quinn Т. et al, 1981; Ostergaard Г., 2000; Centers for Disease Control and Prevention (CDC), 2002). Такое состояние носительства в большей степени характерно для мужчин (Мортон Р. С, Кингхорн Дж. Р., 2000; Butler С. et al, 2003).
Доказанным считается факт, что УГХ является одной из основных причин развития вторичного бесплодия у женщин и мужчин (Башмакова М. А. и др., 1999; Мерзляков В. А. и др., 1999; Потекаев Н. С. и др., 2000; Скрипкин Ю. К., Пашинян М. Г., 2000; Бурчик В. К. и др., 2003; Cates W., Wasserheit J. N.. 1991; Eggert-Kruse W. et al., 1997; Morrison R. P., 2003), при этом каждая седьмая супружеская пара вынуждена оставаться бездетной (Westorm L., 1996). Клинические данные и результаты лабораторных исследований при обследовании бесплодных семейных пар показали, что УГХ — одна из наиболее частых причин (около 60% случаев) нарушения репродуктивной функции (Шинский Г. Э. и др., 1999; Мавров И. И., 2002).
На долю мужского бесплодия приходится около 45% нарушений репродуктивной функции, с тенденцией к его увеличению. В 50% случаев у бесплодных мужчин с наличием ИППП выявляется С. trachomatis (Калиниченко С. Ю. и др., 2000). Имеются исследования о связи бессимптомного течения УГХ с нарушением репродуктивной функции у мужчин. Так, у больных с маркерами С. trachomatis при отсутствии клинических симптомов и субъективных ощущений нарушения показателей спермограммы встречались в 5 раз чаще, чем в группе здоровых мужчин (Епифановский А. И. и др., 2004).
В настоящее время установлено, что С. trachomatis способна вызывать нарушения сперматогенеза (Аладышева В. В., Потекаев Н. Н., 2002; Mazzoli S. et al., 2000). Изучение состава незрелых половых клеток эякулята у больных УГХ выявило нарушение мейотических процессов в клетках-предшественниках сперматозоидов (Кубанова А. А. и др., 2000). Исследования S. Hosseinzadeh et al. (2003) выявили токсичность ЛПС клеточной стенки С. trachomatis для сперматозоидов. Оценивая подвижность, жизнеспособность и акросомальную реакцию сперматозоидов, авторы обнаружили спермицидные свойства ЛПС. Воспалительный процесс, обусловленный С. trachomatis, вызывает изменение рН эякулята со сдвигом в щелочную сторону, что приводит к нарушению подвижности сперматозоидов вплоть до тотальной некроспермии (Калиниченко С. Ю. и др., 2000). Одна из вероятных причин мужского бесплодия при УГХ заключается также в появлении антиспермальных антител, которые вызывают агглютинацию сперматозоидов, их обездвиживание и цитотоксическое уничтожение (Калмыкова Т. Д., Мухамадеев Р. X., 2000). Все воспалительные процессы, в том числе вызванные С. trachomatis, могут привести к облитерирующим повреждениям в семенном тракте (Eggert-Kruse W. et al., 2000). С. Ю. Калиниченко и соавт. (2000) при исследовании спермограммы выявили у 95% больных УГХ астенотератозооспермию, причем патологические формы сперматозоидов составляли более 80%. В результате длительно протекающего воспалительного процесса в половых органах заболевание нередко сопровождается половыми расстройствами (у мужчин в 31% случаев), наиболее часто — преждевременной эякуляцией, ослаблением эрекции и невротическими расстройствами (Молочков В. А., 2004). Сочетание С. trachomatis с другими ИППП приводит к более частым сексуальным нарушениям у мужчин, чем при моноинфекции (Мавров Г. И., 1995).
Из урогенитальных осложнений у мужчин наблюдаются простатиты, эпидидимиты, орхоэпидидимиты, циститы, проктиты и стриктуры уретры (Ильин И. И., 1991; Quinn Т. et al., 1981; Somani J. et al, 2000). На сегодняшний день имеются исследования, где достаточно убедительно показана роль С. trachomatis в генезе хронического простатита (Гомберг М. А., Ковалык В. П., 2002; Сафина О. Н., 2003; Валиева С. А. и др., 2005; Mardh P. A. et al., 1978; Ostaszewska-Puchalska I. et al., 2004). При исследовании вовлеченности в патологический процесс ПЖ было отмечено, что в группе больных УГХ простатит встречался в 2 раза чаще, чем в группе с отрицательными результатами обследования на С. trachomatis (Епифановский А. И. и др., 2004). S. Mazzoli et al. (2000) получили данные, которые подтверждают наличие С. trachomatis в эякуляте и секрете ПЖ у пациентов с хроническим простатитом.
Присутствие С. trachomatis в организме может стимулировать развитие аутоиммунной патологии (Васильев М. М., Николаева Н. В., 2003). Белок теплового шока с молекулярной массой 60 кД (hsp60), содержащийся в клеточной стенке С. trachomatis, приводит к антигенной перегрузке организма. Данный белок играет важную роль в иммунопатогенезе хламидийной инфекции и поддержании постоянной воспалительной реакции (LinJ. S. et al., 1992). При этом происходит гиперпродукция IgA и IgG, эффект теплового шока у клетки-хозяина и стимуляция аутоиммунного ответа за счет антигенного сродства с белками эукариот (Koehler L. et al., 1994). У некоторых мужчин и женщин бессимптомная генитальная хламидийная инфекция ассоциируется с развитием аутоиммунных реакций на hsp60 и бесплодием (Козлова В. И., Пухнер А. Ф., 2003; Weinstock H. et al., 1994).
Роль С. trachomatis как этиологического фактора в развитии болезни Рейтера — самой частой причины острых артритов у мужчин в возрасте 18-40 лет — в настоящее время не вызывает сомнений (Дубенский В. В., 1999; СафинаО. Н., 2001; Молочков В. А., 2004; Wollenhaupt J., Zeidler Н., 1990). Более того, данное заболевание рассматривается как наиболее тяжелое осложнение УГХ с генетически обусловленным дефектом иммунной системы (Аладышева В. В., Потекаев Н. Н., 2002; Tayler-Robinson D., Thomas В., 1998; Appel H. et al., 2004).
1.2. Состояние общей и локальной иммунологической реактивности при УГХ
Ведущую роль в патогенезе УГХ играют иммунопатологические механизмы (BeattyW. L. et al., 1994). На патогенез УГХ оказывают влияние как бактериальные факторы, так и факторы организма-хозяина (Коэн К. Р., Бранэм Р. К., 1999). Защита слизистых оболочек обеспечивается совокупностью различных факторов, к которым относят нормальную микрофлору, секреторные и сывороточные иммуноглобулины, бактерицидные продукты (комплемент, лизоцим, лактоферрин и др.), а также фагоцитирующие клетки (Зиганшин О. Р., Долгушин И. И., 2001; Cohen M. S. et al., 1999). Известна противохламидийная активность влагалищного и цервикального секретов (Mahmoud E. A. et al., 1994). В моче были обнаружены «фосфатные ингибиторы» хламидийной инфекции. Кроме того, находящаяся в половых путях Clostridium difficile секретирует креозол-подобное вещество, а инфицированные клетки эпителия выделяют азотную кислоту, которая подавляет размножение хламидий (Мортон Р. С, Кингхорн Дж. Р., 2000).
К хламидийной инфекции нет естественного иммунитета. В результате инфицирования, реинфекций и рецидивов заболевания развивается нестойкий приобретенный иммунитет (Козлова В. И., Пухнер А. Ф., 2003).
В целом иммунный ответ на С. trachomatis характеризуется клеточными и гуморальными иммунными реакциями (Коваленко Е. В. и др., 1998; Молочков В. А., Зур Н. Н., 2003). Первая немедленная защитная реакция организма состоит в локальном образовании секреторного IgA с последующим присоединением неспецифических факторов, проявляющихся в первые часы после заражения (Pudney J. et al., 2005). Эти факторы в основном направлены на повышение фагоцитарной активности и переваривающей способности макрофагов. На ранней стадии ЭТ находятся в эндосоме и защищены от действия ферментов лизосом. Нейтрофилы способны уничтожать хламидий при слиянии внутриклеточных ЭТ с лизосомами. В последующем запускается специфический этап иммунного ответа — Т-клеточное звено.
Иммунный ответ при УГХ носит преимущественно Т-хелперный характер, и ему принадлежит решающая роль в выздоровлении (Joseph U. I. et al, 1998; Belland R. J. et al., 2003; Weir E., 2004; Barr E. L. et al., 2005). При активации Т-лимфоцитов происходит образование цитокинов (Бутов Ю. С. и др., 2000; Joseph U. I. et al., 1998; WardM. E., 2000). Цикл развития С. trachomatis заканчивается образованием новых ЭТ, при этом гибнущие эпителиальные клетки также выделяют цитокины, которые приводят к усилению кровотока, повышению проницаемости базальных мембран и миграции лейкоцитов в очаг воспаления. В отличие от быстрой индукции цитокинов, наблюдающейся при инфекциях, вызванных внеклеточными бактериями, появление цитокинов при хламидийной инфекции регистрируется только через 20-24 часа после заражения.
Необходимым условием для реализации иммунного ответа с образованием цитокинов является синтез бактериальных белков. ЛПС, ассоциированный с мембраной хламидий, индуцирует продукцию цитокинов моноцитами и макрофагами (Фрейдлин И. С, Тотолян А. А., 2001), что в свою очередь стимулирует выработку TNF — потенциального инициатора воспалительного процесса. Цитокины могут выступать в роли хемоаттрактантов и активаторов нейтрофилов, моноцитов и Т-лимфоцитов. Другие цитокины вызывают плейотропный эффект, включающий появление молекул адгезинов на поверхности клеток эндотелия, а также секрецию белков острой фазы клетками эпителия и макрофагами. К наиболее значимым антихламидийным факторам иммунитета относятся IFN, TNF, IL-1 (Morrison R. Р., 2003).
IFN вырабатываются и хранятся во всех ядросодержащих клетках крови, эпителиоидных клетках слизистых оболочек и не обладают специфичностью действия. При этом срок их жизни в свободном (несвязанном) состоянии около 2 часов (Хахалин Л. Н., 1999). Пул IFN в организме человека образован 3 типами: а- (продуцируются в основном лейкоцитарными клетками), b- (продуцируются в основном фиксированными в тканях макрофагами — фибробластами) и у-молекулами (продуцируются лимфоцитами), причем последние обладают наибольшим эффектом. Биологические свойства IFN-a и IFN-b, насколько они известны, одинаковы. По совокупности эти интерфероны проявляют противовирусное действие и усиливают экспрессию антигенов главного комплекса гистосовместимости — MHC-I (но не МНС-П в отличие от IFN-y) (Ward M. E., 2000).
Продуцентами IFN-y являются Т-лимфоциты — субпопуляции Тh1, CD8+ (цитотоксические лимфоциты) и NK (Mavoungou E. et al., 1999; Ward M. E., 2000). Исследования, проведенные на мышах, показали, что выздоровление от хламидийной инфекции связано с продукцией IFNy Т-лимфоцитами (Cotter Т. W. et al., 1998). Продукция IFN особенно важна на ранней стадии хламидийной инфекции при индукции иммунного ответа в эпителиальных клетках. При мутации в генах обеих цепей рецептора для IFN-y у больных может наблюдаться иммунодефицит со снижением резистентности к внутриклеточным бактериальным инфекциям. В настоящее время описано более 100 эффектов IFN. Посредством IFN-y Т-лимфоциты и NK «нанимают» макрофаги для выполнения деструктивных функций в отношении поврежденных антигеном С. trachomatis клеток в очаге воспаления (Фрейдлин И. С, Тотолян А. А., 2001). При этом IFN-y повышает эффективность фагоцитоза С. trachomatis другими клетками, в особенности моноцитами и макрофагами. Через рецепторы к IFN-y и TNF происходит активация макрофагов с усилением их микробицидности и других свойств (Хаитов Р. М. и др., 2000). Кроме того, IFN-y активирует NK к осуществлению ими цитолиза клеток-мишеней (Федотов В. П. и др., 2005), являясь локальным кофактором в направлении дифференцировки CD4+ — ThO-клеток в ТЫ, и участвует в переключении биосинтеза подклассов иммуноглобулинов (Гомберг М. А. и др., 2000; Хаитов Р. М. и др., 2000).
Проведенные исследования показали, что развитие персистирующей хламидийной инфекции зависит от изменения концентрации IFNy (Belland R. J. et al., 2003). Высокие дозы IFN-y ингибируют рост С. trachomatis, низкие — индуцируют развитие морфологически аберрантных форм (Wyrick Р. В. et al, 1994).
Исследование фагоцитарной активности при УГХ выявило снижение спонтанного и стимулированного фагоцитоза, которое сопровождалось высокой поглотительной способностью нейтрофилов и активизацией метаболических процессов (Якубович А. И., Скворцова Р. Г., 2000).
Со стороны факторов гуморального иммунитета при хламидийной инфекции наряду с повышением относительного и абсолютного показателей В-лимфоцитов отмечено снижение содержания Ig классов А и М. Некоторые исследователи при УГХ отмечают гиперпродукцию IgA и IgG (Харахордина Ю. Е. и др., 2004). В последнее время появились исследования по обнаружению видоспецифических антихламидийных IgA в сперме и секрете предстательной железы (Mazzoli S. et al., 2000). Считается, что IgA секретируется локально в ответ на инфицирование, поэтому он является индикатором активной или недавно перенесенной инфекции (Епифановский А. И. и др., 2004).
Несмотря на наличие большого количества исследований иммунологической резистентности при УГХ, до настоящего времени остаются дискутабельными многие аспекты антихламидийной защиты организма (Батыршина С. В., 1998).
Н. Appel et al. (2004) при обследовании НГА-В27-позитивных больных реактивным артритом с выявленной С. trachomatis обнаружили уменьшение содержание IFN-y в синовиальной жидкости.
Е. Mavoungou et al. (1999) приводят данные о том, что NK, выделенные от лиц с УГХ, характеризуются слабой литической активностью, меньшей способностью убивать клетки-мишени и низким уровнем продукции TNF-a и IFN-y.
Исследование Т-клеточного звена иммунитета у больных УГХ показало снижение абсолютного количества Т-клеток, Т-хелперов и Т-супрессоров. При сравнении частоты встречаемости Т-клеточного иммунодефицита различной степени тяжести у больных активной и хронической формами хламидиоза было выявлено увеличение частоты тяжелых иммунодефицитных состояний при хронической форме заболевания (Janeway Ch. et al., 1999).
При изучении состояния иммунной системы и иммунитета больных, у которых был диагностирован вялотекущий УГХ, выявлено 3 группы нарушений: с недостаточностью функции клеточного иммунитета (соотношение Т-хелперы/Т-супрессоры снижено, содержание Т-супрессоров повышено); с субкомпенсацией клеточной иммунной системы (соотношение Т-хелперы/Т-супрессоры нормальное, но повышено содержание Т-хелперов); с декомпенсацией системы (соотношение Т-хелперы/Т-супрессоры увеличено на фоне выраженного повышения содержания Т-хелперов и тенденции к снижению содержания Т-супрессоров). Для терапии больных первой группы использовали иммуномодуляторы, стимулирующие образование Т-хелперов, а для больных второй и третьей групп — угнетающие образование Т-хелперов (Анчупане И. С, Милтинып А. П., 2000).
При хроническом персистирующем УГХ М. А. Гомберг и соавт. (1997) выявили у 75% больных различные нарушения иммунного статуса. В Т-клеточном звене эти нарушения носили вариабельный характер, у 50% больных сопровождались изменением ИРИ. Статистически достоверно по сравнению с контрольной группой были снижены относительные и абсолютные показатели NK (CD16+), HLA-DR-клеток, В-клеток (CD72+ и CD21+).
По данным М. В. Шапрана (2003), изменения со стороны клеточного иммунитета больных при УГХ характеризовались по большей части незначительным Т-иммунодефицитом, а также дисбалансом иммунорегуляторных субпопуляций с преимущественным снижением количества Т-хелперов. Кроме того, наблюдалась тенденция к увеличению содержания Т-супрессоров и, как следствие, снижение ИРИ.
S. Mazzoli et al. (1995) исследовали иммунный ответ при хроническом хламидийном простатите, который характеризовался продукцией секреторного IgA, а также Ig классов G и М, медиаторов воспаления — цитокинов, таких как IFN-y, IL-4, IL-6 и др., в сыворотке крови, сперме и секрете простаты в более высоких концентрациях, чем у здоровых мужчин.
В целом иммунный ответ при УГХ имеет важное значение при элиминации возбудителя, кроме того, им же обусловлены стадии болезни, постинфекционный иммунитет и случаи рецидивов заболевания (Молочков В. А., Зур Н. Н., 2003).
1.3. Проблемы, связанные с лечением УГХ
В настоящее время предложено достаточно большое количество противохламидийных препаратов. Выбор того или иного антибиотика проводится в соответствии с действующими инструкциями и схемами лечения, которые представлены в стандартах лечения (Методические материалы по диагностике и лечению наиболее распространенных ИППП и заболеваний кожи. Протоколы ведения больных, лекарственные средства, 2003). Однако терапия больных УГХ отличается сложностью и нередко низкой эффективностью (Молочков В. А., Зур Н. Н., 2003). Несмотря на соблюдение принципов, схем и методов терапии, далеко не всегда можно гарантировать элиминацию С. trachomatis (Хамидуллин Р. Ф., 2000; Хрянин А. А., Лыкова С. Г., 2001; Баткаев Э. А., Рюмин Д. В., 2003; Николаева Н. В., 2003; Rigway С, 2000). Частота рецидивов УГХ, по данным различных исследователей, достаточно высока и составляет от 2 до 50% (Герасимова Н. М., Скидан Н. И., 2001; Баткаев Э. А., Рюмин Д. В., 2003; Кунцевич Л. Д., Комов Н. Н., 2004). Причины возникновения рецидивов носят разнообразный характер и связаны с устойчивостью С. trachomatis к антибиотикам, персистенцией возбудителя, наличием осложнений.
Актуальной проблемой в венерологии является совершенствование качества лечения больных хроническим УГХ с осложнениями (Батыршина С. В., 1998; Молочков В. А. и др., 1998; Хрянин А. А., 2004). Нередко пациенты обращаются за медицинской помощью уже на стадии развития осложнений. По данным О. Л. Иванова и соавт. (2002), 30-40% мужчин, больных УГХ, на момент обращения уже имеют осложнения в виде простатитов, везикулитов и орхитов. Неэффективность противохламидийной терапии при хроническом простатите может быть обусловлена несколькими факторами: аутоиммунным механизмом заболевания, недостаточным проникновением препаратов в ткань простаты, более выраженными изменениями иммунологической реактивности организма (Молочков В. А. и др., 1998).
Одной из возможных причин может быть формирование антибиотикорезистентности у С. trachomatis (Somani J. et al, 2000). С 1980 года начали появляться сообщения о резистентности С. trachomatis к антибиотикам только in vitro, особенно часто к тетрациклину, доксициклину, эритромицину и клиндамицину (Mourad A. et al., 1980; Jones R. В. et al, 1990; Rice R. J. et al., 1995). В дальнейшем в литературе появились данные об устойчивости С. trachomatis in vivo к широко используемым в лечении препаратам (refevre J. С. et al., 1997) и даже описан случай одновременной резистентности к азитромицину, офлоксацину и доксициклину (Somani J. et al., 2000). В то же время один из ведущих специалистов в области антибиотикотерапии УГХ Г. Л. Риджуэй (2000) не располагает убедительными данными, подтверждающими наличие штаммов С. trachomatis, устойчивых к макролидам и тетрациклинам. При этом автор допускает в некоторых случаях возможность возникновения резистентности к фторхинолонам, которая обусловлена изменениями в гене gyrA (Рентой А. М. и др., 1999; Rigway G., 2000).
Развитие устойчивости к антимикробным препаратам формируется по двум основным направлениям. Первое — это хромосомный тип, обусловленный мутациями в генах, кодирующих ферменты, которые являются «мишенью» антибиотика, или в генах, стимулирующих выработку собственных ферментов-антагонистов, блокирующих действие препарата. Второй механизм связан с нарушением проницаемости наружной клеточной мембраны, в результате чего затрудняется проникновение лекарственного средства в клетку (Халдин А. А., 2004). В настоящее время механизм формирования резистентности С. trachomatis к макролидам не изучен (Somani J. et al, 2000).
Одним из факторов, влияющих на результативность лечения и эпидемиологическую ситуацию, является способность С. trachomatis к персистирующему существованию (Richard J. H. et al., 2004). Персистенция представляет собой долговременную ассоциацию С. trachomatis с биологической мишенью, при этом возбудитель находится в инфицированной клетке на стадии заблокированного перехода РТ в ЭТ с сохранением способности к восстановлению типичного цикла развития при создании оптимальных условий (Куляш Г. Ю., 2003). В результате приостанавливается деление С. trachomatis, изменяются антигенные характеристики, при этом хламидийная инфекция находится в состоянии равновесия с организмом человека (Глазкова Л. К., Акилов О. Е., 1999). В период персистенции С. trachomatis метаболически неактивна и неконтагиозна, более того, возбудитель становится нечувствительным к антибактериальным препаратам (Битти В. Л. и др., 1995; Шинский Г. Э. и др., 1999; Cotter Т. W. et al., 1997; Dean D. et al, 1998).
Характерной особенностью С. trachomatis является способность стимулировать собственный эндоцитоз пораженной клеткой, а затем ингибировать слияние лизосом с содержащей С. trachomatis фагосомой. В результате этого, находясь в вакуолях, С. trachomatis остается под невольной защитой клетки-хозяина и способна к длительной персистенции (Потекаев Н. С. и др., 2000; Koehler L. et al., 1994).
1.4. Этиотропное и патогенетическое лечение УГХ
В терапии УГХ следует придерживаться строго индивидуального подхода при этиологически и патогенетически оправданном лечении (Хрянин А. А., 2001).
Препараты для лечения ИППП, по рекомендации Всемирной организации здравоохранения, должны обладать следующими характеристиками:
- эффективность не ниже 95%;
- доступная цена;
- низкая токсичность и хорошая переносимость;
- медленное наступление устойчивости возбудителя болезни;
- возможность однократного приема;
- пероральный прием;
- возможность использования во время беременности и лактации;
- возможность применения у детей.
Учитывая внутриклеточную локализацию С. trachomatis, в лечении должны применяться препараты, хорошо проникающие внутрь клетки (Лыкова С. Г., Хрянин А. А., 1998; Гранитов В. М., 2000). По степени проникновения противомикробные препараты условно делят на группы с низкой степенью (пенициллины, цефалоспорины, нитроимидазолы), средней степенью (тетрациклины, аминогликозиды, рифампицин, фторхинолоны) и высокой степенью (макролиды). Основными антибактериальными препаратами, применяемыми для лечения УГХ, являются антибиотики тетрациклинового ряда, макролиды и фторхинолоны (Савичева А. М. и др., 1999; КисинаВ. И., 2000; Хрянин А. А., 2001; Методические материалы по диагностике и лечению наиболее распространенных ИППП и заболеваний кожи, 2003; Молочков В. А., Молочков А. В., 2005; Федотов В. П. и др., 2005; Rigway G., 2000; Kilic D. et al., 2004). Перспективы повышения эффективности лечения ХИ могут быть связаны с внедрением антибиотиков новой группы — кетолидов (телитромицин и др.) (Pavletic A. J. et al., 1999).
Российские протоколы ведения больных (2003), а также рекомендации ВОЗ, Европейского руководства по лечению ИППП, Центра по контролю заболеваемости США предусматривают следующие схемы для лечения неосложненного хламидиоза нижних отделов мочеполовых органов.
- Макролиды: азитромицин (сумамед, зитролид, хемомицин) взрослым и детям с массой тела более 50 кг 1,0 г внутрь однократно за 1 ч до еды или через 2 ч после еды. Все упомянутые руководства к препаратам выбора при лечении хламидиоза относят азитромицин. Этому способствуют уникальные фармакокинетические характеристики азитромицина: продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, а также возможность проникновения внутрь клетки. Благодаря тому, что высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее 7 суток, с появлением азитромицина впервые возникла возможность эффективного лечения больных хламидийной инфекцией однократным приемом антибиотика внутрь. Наиболее известным из таких препаратов является сумамед, который используется в РФ с начала 90-х годов прошлого века.
Джозамицин (вильпрафен) 500 мг внутрь 2 раза в сутки 10 дней.
В настоящее время при лечении УГХ широко применяются макролиды, которые демонстрируют определенные преимущества перед другими группами антибиотиков. Как правило, макролиды оказывают бактериостатическое действие, но в более высоких концентрациях способны к бактерицидному эффекту против грамположительных и грамотрицательных микроорганизмов, а также хламидий и микоплазм. Преимуществами всех современных макролидных антибиотиков перед эритромицином являются улучшенная фармакокинетика, хорошая переносимость и меньшая кратность приема. За последние годы получены новые макролидные антибиотики второго поколения, которые по сравнению с эритромицином обладают улучшенными химическими, биологическими и фармакокинетическими свойствами (Шахтмейстер И. Я., 1999). Одним из препаратов этой группы, используемых в лечении УГХ, является вильпрафен (джозамицин) (Потекаев Н. С, 2000; Аладышева В. В., Потекаев Н. Н., 2002; Методические материалы по диагностике и лечению наиболее распространенных ИППП и заболеваний кожи, 2003; Якубович А. И., Малышев В. В., 2003; Rigway G., 2000). Вильпрафен хорошо абсорбируется из желудочно-кишечного тракта при пероральном приеме, при этом пик концентрации в сыворотке крови отмечается примерно через 1 час, а период полувыведения составляет около 2 часов (Калиниченко С. Ю. и др., 2000). Фармакокинетика препарата благодаря высокой липофильности характеризуется быстрым его распределением во внесосудистом пространстве (Аладышева В. В., Потекаев Н. Н., 2002). Важным для клинического применения свойством является тот факт, что концентрация препарата в полиморфноядерных лейкоцитах и моноцитах приблизительно в 20 раз выше, чем во внеклеточном пространстве (Бутов Ю. С, Волкова Е. Н., 2000). При этом фагоцитарная активность этих клеток повышается, а в очаг воспаления поступает антибиотик вместе с мигрирующими фагоцитами (Васильев М. М. и др., 2005). Благодаря особенностям метаболизма джозамицин гораздо реже, чем другие макролиды, оказывает побочное действие (Хамидуллин Р. Ф., 2000; Хамаганова И. В., Карамова А. Э., 2002). Кроме того, препарат обладает широким спектром действия и высокой эффективностью при лечении УГХ (Скрипкин Ю. К., Пашинян М. Г., 2000; Карамова А. Э. и др., 2003; Юцковский А. Д. и др., 2005). По данным различных исследований, вильпрафен, применяемый 2-3 раза в сутки как в комплексе, так и виде монотерапии, эффективен у 90-97% больных УГХ (Савичева А. М. и др., 1999; Аладышева В. В., Потекаев Н. Н., 2002; Васильев М. М. и др., 2005; Stary A., Moritz A. J. et al., 1985).
Хорошие результаты были получены О. Б. Лоран и соавт. (1994) при лечении вильпрафеном хламидийных уретритов и простатитов. Вильпрафен эффективен при лечении хронических больных, резистентных к терапии другими антибиотиками (Аладышева В. В., Потекаев Н. Н., 2002). Макролиды в отличие от антибиотиков тетрациклинового ряда не оказывают негативного влияния на сперматогенез, поэтому их предпочтительнее использовать при лечении УГХ у мужчин, особенно с бесплодием (Калиниченко С. Ю. и др., 2000; Хамидуллин Р. Ф., 2000).
- Тетрациклины. Среди антибиотиков тетрациклинового ряда предпочтение отдается полусинтетическому производному тетрациклина — доксициклину. Преимущества использования доксициклина— достаточно высокая эффективность (95-100%) и относительно невысокая стоимость лечения. Доксициклин по сравнению с тетрациклином имеет более высокую биодоступность, более длительный период полувыведения и лучше переносится. Кроме того, при использовании доксициклина, в отличие от других тетрациклинов, нет необходимости соблюдать диету, учитывающую возможность связывания тетрациклинов с ионами Са2+. Следует помнить, что все препараты тетрациклинового ряда противопоказаны при почечной недостаточности, беременности и для лечения детей до 8 лет. Наиболее частыми побочными эффектами при приеме препаратов тетрациклинового ряда являются тошнота, рвота, диарея, аллергические проявления. Эти реакции значительно менее выражены при использовании доксициклина моногидрата, а не традиционного доксициклина гидрохлорида. В период лечения препаратами этой группы больным необходимо избегать инсоляции из-за возможности фотосенсибилизации.
Доксициклин (юнидокс солютаб, вибрамицин), взрослым и детям с массой тела более 50 кг 200 мг внутрь — первый прием, затем 100 мг 2 раза в сутки в течение 7 дней.
Альтернативные схемы терапии:
- макролиды: эритромицин-основание (500 мг внутрь 4 раза в сутки в течение 7 дней),
- или рокситромицин (рулид) 150 мг внутрь 2 раза в сутки в течение 7 дней;
- фторхинолоны: офлоксацин (300 мг внутрь после еды 2 раза в сутки в течение 7 дней или 400 мг 1 раз в сутки в течение 7 дней).
При осложненных формах и хламидийной инфекции верхних отделов мочеполового тракта рекомендуются антибиотики из группы макролидов:
- азитромицин (сумамед, зитролид, хемомицин, азитрал) взрослым и детям с массой тела более 50 кг 1 г внутрь 1 раз в неделю (1, 7 и 14-й дни), в курсовой дозе 3 г.;
- джозамицин 500 мг внутрь 2 раза в сутки 14 дней.
Кроме того, в литературе встречаются следующие схемы лечения урогенитального хламидиоза: - метациклин (рондомицин) — в 1-й день 600 мг, затем по 300 мг 3 раза в день 7-10 дней;
- азитромицин (сумамед, зитролид, хемомицин, азитрал) — 1-й день однократно 1 г в сутки, последующие 4 дня по 500 мг в день, курсовая доза 3 г;
- кларитромицин (клацид, клабакс, фромилид) 250 мг внутрь 2 раза в сутки в течение 7-10 дней или 1 г в первый день и по 0,5 г внутрь 1 раз в сутки в течение 4 дней. Одним из представителей 14-членных полусинтетических макролидов является кларитромицин, который обладает высокой активностью в отношениии С. trachomatis, превосходящей таковую у широко используемых в клинике противохламидийных препаратов. Этот антибиотик обладает более высокой пенетрацией и способностью накапливаться в клетках макроорганизма, в том числе иммунокомпетентных. В отличие от азитромицина, кларитромицин не создает длительных субингибирующих концентраций, поэтому риск развития резистентности к данному препарату значительно ниже. Установлено, что кларитромицин — единственный уроселективный макролид с высоким процентом выведения через почки. Хорошая переносимость и безопасность кларитромицина подтверждена, побочные реакции редки и не требуют отмены препарата. Применяется препарат в дозировке по 250 мг два раза в день в течение 10-14 дней. Кларитромицин относится к числу препаратов первого ряда (вместе с традиционными доксициклином и азитромицином) для лечения УГХ;
- спирамицин 3 000 000 ЕД 3 раза в сутки в течение 10 дней, а также мидекамицин (макропен), пристиномицин.
Особое место в рекомендациях Всемирной организации здравоохранения, Центра по контролю заболеваемости (CDC, США), в Европейских руководствах по лечению ИППП занимают фторхинолоны — высокоэффективные препараты широкого антимикробного действия. Для фторхинолонов характерны низкое связывание с белками сыворотки крови, большой объем распределения, длительный период полувыведения, высокая биодоступность, элиминация почечными и внепочечными путями (Кисина В. И. и др., 2003). Фторхинолоны обладают высокой терапевтической эффективностью при пероральном приеме (Чуприн А. Е., 2005). Антибиотики из группы фторхинолонов оказывают угнетающее действие на бактерии и препятствуют синтезу ДНК в клетках микроорганизма. Препараты этой группы обладают различной активностью in vitro в отношении С. trachomatis. Единственными препаратами этой группы, которые современные руководства рекомендуют для лечения хламидиоза в качестве альтернативных, являются офлоксацин и левофлоксацин. Ограничения в использовании фторхинолонов для лечения хламидийной инфекции связаны с тем, что в сравнении с антибиотиками других групп в большей степени способны вызывать резистентность С. trachomatis и формировать персистенцию возбудителя. Наибольшей активностью в отношении хламидий, помимо офлоксацина, обладают:
- пефлоксацин (абактал) по 400 мг 2 раза в день в течение 7-14 дней;
- левофлоксацин (таваник) по 250 мг 2 раза в день в течение 7-10 дней или по 500 мг 1 раз в сутки 10 дней. Левофлоксацин более активен в отношении хламидий и, учитывая прием 1 раз сутки, имеет более высокую комплаентность;
- ломефлоксацин (по 0,6 г 1 раз в сутки в течение 7 дней), пефлоксацин и другие фторхинолоны взрослым и детям в возрасте старше 12 лет.
G. Rigway (2000) сообщает о высокой противохламидийной активности спарфлоксацина in vitro и эффективности в лечении негонококковых уретритов. Важно подчеркнуть, что спарфлоксацин относится к фторхинолонам с наиболее длительным периодом полувыведения, хорошо проникает в микробную клетку и характеризуется высокой бактерицидной активностью (Падейская Е. Н., 2002). Клиническая эффективность его при неосложненных хламидийных уретритах по стандартной схеме лечения (в 1-й день 400 мг, со 2-го дня 200 мг в сутки; курс 10-14 дней) составляла 90-100%, а элиминация возбудителя отмечена в 75-100% случаев (Самцов А. В., Сухарев А. В., 2003; Чернова Н. И. и др., 2003; Suzuki К. et al., 1991; Kawada Y., 1992). При осложненных процессах, в том числе простатитах, клиническая эффективность при той же дозировке составила 65-79%, а элиминация возбудителя наблюдалась в 75-97,6% случаев (Зуев А. В., 2002; Усова С. А., Баранова Т. М., 2003; Suzuki К. et al., 1991; Kawada Y., 1992; Naber К. G. et al., 1996). Побочные реакции отмечаются со стороны желудочно-кишечного тракта (диарея, тошнота, рвота), частота которых колеблется от 2 до 11%, со стороны центральной нервной системы (нарушение сна, головная боль) — 2-4%, кожные реакции (в том числе и фоточувствительность) — 2-5% (Падейская Е. Н., Яковлев В. П., 1998; Carbon С. J., 1995; Schentag J. J., 2000). При применении фторхинолонов возможно удлинение интервала QT. Этот эффект относится к очень редким (0,01% и реже) нежелательным реакциям. Показанием к использованию фторхинолонов при хламидиозе может быть смешанная гонорейно-хламидийная инфекция или сочетание С. trachomatis с другими микроорганизмами, демонстрирующими чувствительность к этим антибиотикам, т. е. требующая терапии сопутствующая кокковая или палочковая флора.
Препараты из группы фторхинолонов противопоказаны беременным и детям до 18 лет, больным с нарушением функции печени и почек. Из побочных реакций после приема фторхинолонов могут наблюдаться диспепсические расстройства, тошнота, рвота, головокружение, аллергические реакции, тендиниты. Для всех препаратов этой группы характерен фотосенсибилизирующий эффект, о чем необходимо напоминать больному.
При осложненных формах длительность лечения рекомендуется увеличивать до 14-21 дня.
Лечение УГХ без коррекции иммунных нарушений является малоэффективным или недостаточно эффективным, особенно при хронической или рецидивирующей инфекции. Для лечения хронического хламидиоза терапию антибиотиками дополняют иммуномодулирующими препаратами (циклоферон, неовир, ридостин, виферон, Т-активин и др.) после определения по возможности чувствительности к ним интерферонпродуцирующих клеток пациента (Прилепская В. Н., Абакарова П. Р., 2004).
В лечении хронического УГХ, помимо назначения противохламидийных препаратов, должны проводиться мероприятия, направленные на повышение иммунореактивных способностей организма (Молочков В. А., Зур Н. Н., 2003).
Существуют различные методики комплексного лечения УГХ с применением различных иммунотропных препаратов.
С помощью ультраструктурного анализа было показано, что при использовании комплекса «пефлоксацин и иммуномодулятор (тимоген)» незавершенная фагоцитарная реакция становилась завершенной, фагоцитоз носил многоступенчатый характер, а морфологический анализ лейкоконцентрата крови свидетельствовал об усилении переваривающей способности полиморфноядерных лейкоцитов (Делекторский В. В. и др., 1994).
О необходимости этапного лечения УГХ сообщали Л. К. Глазкова и В. С. Полканов (1994). Авторы рекомендовали на первом этапе повышать неспецифическую резистентность организма с помощью иммуномодуляторов, затем (основной этап) проводить специфическую базисную терапию антибиотиками с включением протеолитических ферментов, прооксидантов, кальциевых блокаторов и аналогов энкефалинов. Заключительный этап — восстановительная терапия с применением адаптогенов, гепатопротекторов и антиоксидантов. В. П. Кузнецова (1993) наблюдала мужчин с гонорейно-хламидийной инфекцией УГТ, получавших доксициклин и офлоксацин. Присоединение к проводимой терапии лейкинферона сокращало сроки лечения и уменьшало количество осложнений и рецидивов. Э. В. Малинина (1997) показала наличие прямой зависимости результатов лечения УГХ антибиотиками от уровня спонтанной индукции интерферона в организме пациентов. Наибольшая эффективность (95%) была достигнута при комплексном лечении УГХ антибиотиками в сочетании с протеолитическими ферментами, препаратами экзогенного (виферон) и индукторами эндогенного (ларифан или ридостин) интерферона.
Исходя из данных о неэффективности применения антибиотиков у больных хроническим персистирующим УГХ при наличии иммунологических нарушений (Кисина В. И., Канищева Е. Ю., 2002), М. А. Гомберг и соавт. (1997) провели таким больным курс иммунотерапии, не назначая антибиотиков. В зависимости от иммунного статуса пациентов применяли различные иммуномодуляторы и адаптогены: тактивин, миелопид, метилурацил и полиоксидоний. В результате иммунокоррекции достоверно уменьшался лейкоцитоз, увеличивалось содержание лимфоцитов, восстанавливалось соотношение иммунорегуляторных субпопуляций Т-лимфоцитов, происходило увеличение относительных и абсолютных показателей В-клеток (CD72+ и CD21+), причем показатели CD72+ приходили в соответствие с показателями доноров. Из 27 пациентов этиологическое излечение было достигнуто в 85% случаев, у 3 больных произошла реверсия, и при исследовании обнаружены обычные формы С. trachomatis. Такой же эффект отмечен Л. К. Глазковой и О. Е. Акиловым (1999) при использовании IFN-y, который в больших дозах полностью ингибирует рост хламидий. Р. М. Хаитов и Б. В. Пинегин (1999) считают, что при одновременном применении антибиотика и иммуномодуляторов достигается больший терапевтический эффект, чем при их раздельном использовании. По возбудителю наносится двойной удар, и достигается большая эффективность комплексного лечения.
Часть врачей предпочитает не использовать иммунотропные средства, так как это требует и специальных знаний, и дополнительного обследования больного, эмпирическое же применение этих препаратов может быть неэффективным или вызывать побочные эффекты. Назначение любых препаратов должно быть строго обоснованным (Хрянин А. А., Лыкова С. Г., 2001), в частности нерациональное или необоснованное применение цитомединов (тималин, тимоптин, тимоген) создает угрозу сложноконтролируемых аутоиммунных процессов в связи с избыточной стимуляцией Т-лимфоцитов. При использовании липополисахаридов (пирогенал, продигиозан) стимуляция В-лимфоцитов и перегрузка макрофагов способны привести к повышенной продукции иммуноглобулинов и другим нарушениям, вследствие чего могут развиваться иммунопатологические состояния, в том числе и болезнь Рейтера (Кисина В. И., 1998).
Выбор тактики лечения должен основываться на изучении иммунного статуса с целью подбора индивидуальной иммунокоррекции (Глазкова Л. К., Акилов О. Е., 1999). Нередко широко известные препараты используются без иммунологического обследования больных и учета фазы инфекции (Малашенкова И. К. и др., 2004).
Более безопасным следует считать применение иммуномодуляторов для местного использования (Харахордина Ю. Е. и др., 2004). В последнее время разрабатываются методы стимуляции местного иммунного ответа слизистых УГТ (Ward М. Е., 2000). И. И. Мавров и А. В. Шатилов (1994) дали обоснование местного применения иммуномодуляторов в комплексном лечении хламидийных уретритов у мужчин. У больных были изучены изменения эпителия уретры, а также исследовано влияние на процессы метаплазии и дифференцировки эпителиальных клеток внутриуретральных инстилляций препаратов тимуса (тимогена и тимоптина), оказывающих модулирующее воздействие на хелперную субпопуляцию Т-лимфоцитов. Установлено, что у больных хламидий-ным уретритом изменена морфология эпителия мочеиспускательного канала путем метаплазии многослойного призматического эпителия в многослойный плоский, чему способствовало традиционное местное лечение — инстилляций препаратов серебра, тампонады и бужирование. Авторы отмечали, что после этиотропного лечения хламидийного уретрита нормальная цитоморфологическая структура эпителия уретры не восстанавливается, в то время как инстилляций иммуномодуляторов способствуют усилению его регенерации, стимулируя нормальную дифференцировку эпителиальных клеток.
Все чаще в комплексном лечении УГХ в последнее время применяют препараты интерферона (Молочков В. А., Зур Н. Н., 2003). Перспективным направлением в иммунокоррекции УГХ является применение индукторов интерферона. Стимуляция синтеза в организме собственных (эндогенных) интерферонов лишена недостатков, присущих введению экзогенного интерферона. Индукторы IFN представляют собой весьма разнообразное по составу семейство высоко- и низкомолекулярных природных и синтетических соединений. В отличие от наиболее широко используемых в настоящее время рекомбинантных IFN, индукторы IFN не обладают антигенностью. Синтез IFN сбалансирован и контролируется организмом, что предотвращает побочные эффекты, наблюдаемые при передозировках IFN. Даже однократное введение индукторов приводит к длительной продукции IFN в терапевтических дозах, тогда как для достижения подобных концентраций при использовании экзогенных IFN требуется многократное введение значительных доз, так как срок полужизни этих препаратов невелик. Последнее значительно повышает стоимость интерферонотерапии, особенно при длительном использовании. Некоторые индукторы IFN обладают уникальной способностью «включать» синтез IFN в определенных популяциях клеток и органах. Из потенциальных индукторов синтеза интерферона лишь около 10 оказались пригодными для клинического применения.
Одним из наиболее хорошо изученных препаратов этого ряда является циклоферон — низкомолекулярный синтетический индуктор IFN. Циклоферон является водорастворимым синтетическим аналогом природного алкалоида из культуры Citrus grandis, солью акридонуксусной кислоты и N-метилглюкамина, представляет собой порошок светло-желтого цвета, в растворе слегка опалесцирует. У человека активность IFN в сыворотке крови не превышает 100 МЕ/мл, через 48 часов IFN в крови обнаружить не удается. В тканях и органах, содержащих лимфоидные элементы, циклоферон индуцирует высокий уровень IFN, сохраняющийся в течение 72 часов. Клетками-продуцентами IFN являются иммунокомпетентные клетки: моноциты, макрофаги, лимфоциты и купферовские клетки печени (Коваленко А. Л., Алексеева Л. Е., 2002).
Установлено, что введение циклоферона приводит к повышению биосинтеза высокоавидных антител, т. е. функционально полноценных, способствующих более эффективной терапии. Выявлено стимулирующее влияние циклоферона на функциональную активность нейтрофилов in vitro, увеличивающее их провоспалительный потенциал и возможность к высокой генерации активных форм кислорода, с повышением при этом бактерицидных свойств крови (Долгушин И. И., Зиганшин О. Р., 2004). На фоне применения циклоферона наблюдались положительные изменения в содержании исходно измененных субпопуляций Т-лимфоцитов: повышение CD3+, CD4+, CD16+ и иммунорегуляторного индекса; снижение CD8+- и СБ72+-лимфоцитов (Дидковский Н. А. и др., 2002; Исаков В. А., 2003). Использование циклоферона приводит к повышению уровня IgA и к нормализации содержания IgM и IgG (Долгушин И. И., Зиганшин О. Р., 2004). Циклоферон вызывает образование провоспалительных и противовоспалительных цитокинов, что позволяет рассматривать его как биорегулятор цитокиновой сети. Препарат сочетает высокую биологическую активность с отсутствием мутагенного, канцерогенного и эмбриотоксического действия на организм человека. При применении в рекомендованных дозировках побочные эффекты крайне редки (Исаков В. А., 2003). Выводится из организма почками в течение 24 часов в неизмененном виде. При введении циклоферона в среднетерапевтической дозе было установлено, что у большинства больных его эффект снижается через 3-4 недели применения (Малашенкова И. К. и др., 2004). Хорошо сочетается с традиционными терапевтическими средствами (антибиотиками, иммунотропными препаратами и т. д.) (Кубанова А. А., Кисина В. И., 2005). Существенным достоинством акридонуксусной кислоты является отсутствие метаболического расщепления в печени и кумулирования в организме (Романцов М. Г., Коваленко А. Л., 2002). Циклоферон проявляет широкий спектр антивирусной, антипротозойной, антибактериальной и противохламидийной активности, оказывает мягкое иммуностимулирующее действие.
Как противовирусный препарат и препарат для повышения иммунобиологической резистентности циклоферон используется при гриппе, ОРВИ, герпесе, гепатите (Голубев С. Ю., Бржеский В. В., 2002; Исаков В. А. и др., 2002; Мезенцева М. В. и др., 2002; Радченко В. Г., Стельмах В. В., 2002; Сологуб Т. В. и др., 2002; Тищенко М. С, Серебряков М. Ю., 2002). Его эффективность была доказана при лечении опухолевых процессов. Высокие результаты (70% и более) были достигнуты при лечении В- и Т-клеточных злокачественных новообразований крови, а также при лечении солидных опухолей (Ершов Ф. И., 2002). Выявлено, что при лучевой терапии новообразований циклоферон повышает гематологические показатели иммунитета, уменьшая побочные действия лечения (Иванов С. Д. и др., 1998). Применение циклоферона явилось важным компонентом терапии наружного генитального эндометриоза (Сельков С. А., Ярмолинская М. И., 2004). Кроме того, проведены исследования по использованию препарата при атопическом дерматите (Хиштовани Э., Г Дискаришвили Н., 2000; Соколовский Е. В. и др., 2002), псориазе (Левашов И. Н. и др., 1999; Соколов Г. Н., Соколовский Е. В., 2002; Тищенко Л. Д. и др., 2002), различных формах алопеции (Шарова Н. М., Грязнова Т. В., 2004), заболеваниях суставов (Кисина В. И. и др., 2003), язвенной болезни двенадцатиперстной кишки (Романцов М. Г., 2002), инфекционных заболеваниях различных органов (Алексеев С. А., 2002; Арефьева Н. А., 2002; Морозова Ю. В., 2002).
В комплексном лечении с использованием циклоферона хронических воспалительных заболеваний половой системы у мужчин клиническая эффективность достигала 95,3%, а элиминация возбудителя отмечена в 94,9% случаев (Долгушин И. И., Зиганшин О. Р., 2004). Доказана эффективность индукторов IFN при хламидийной инфекции (Кубанова А. А., Кисина В. И., 2005). G. I. Mavrov, G. M. Bondarenko (2000) применяли циклоферон в комплексном лечении больных с реактивным артритом хламидийной этиологии. В комплексном лечении УГХ В. С. Дмитрук и А. В. Зуев (2001) применяли аутотрансфузию УФ-облученной крови с добавлением в нее 12,5% раствора циклоферона на фоне традиционной терапии, что позволило повысить эффективность лечения и уменьшить количество рецидивов.
Перспективным направлением является применение циклоферона местно в виде линимента. Циклоферон обладает регенерирующим действием на поврежденные ткани и слизистые оболочки, нормализует обменные процессы в клетках.
О. В. Галкина и соавт. (1998) использовали линимент циклоферона в виде монотерапии, которая оказалась эффективной в 81,2% случаев при бактериальном и кандидозном вульвовагините. Причем по окончании курса лечения у значительной части больных было отмечено повышение фагоцитарной активности нейтрофилов, а также снижение интегрального показателя концентрации иммуноглобулинов в сыворотке крови и вагинальном секрете. Использование линимента циклоферона как в виде монотерапии, так и в комбинированном лечении УГХ у мужчин показало хорошие результаты и отсутствие побочных эффектов (Исаков В. А., 2003).
При УГХ целесообразно использовать в качестве патогенетического лечения системную энзимотерапию (вобэнзим, флогэнзим) (Батыршина С. В., 1998; Золотухина Ю. Л., Самойленко О. Н., 2005; Ремезов А. П., Кнорринг Г. Ю., 2005; Юнусова Е. И., 2005). Совместное применение ферментных препаратов и антибиотиков повышает концентрацию последних в очаге воспаления на 15-20% (Sukhikh G. et al., 1997).
Резюме
Таким образом, из представленного обзора следует, что УГХ продолжает оставаться важной медико-социальной проблемой в силу своей распространенности и негативного влияния на здоровье человека. Изучение различных сторон патогенеза и разработка эффективных методов терапии этого заболевания не теряют своей актуальности в связи с достаточно высоким процентом неэффективности лечения и возникновением рецидивов.
Известно, что ведущую роль в патогенезе УГХ играют иммунопатологические механизмы, при этом иммунный ответ носит преимущественно Т-клеточный характер. Выздоровление больных и элиминация С. trachomatis связаны с продукцией IFN-y Т-лимфоцитами. В то же время недостаточно изучены компоненты локальной иммунологической реактивности, в частности роль подклассов IgG в хроническом течении заболевания и излечении от хламидийной инфекции.
Клинико-экспериментальные данные применения циклоферона при различных формах патологии явились теоретической предпосылкой для проведения настоящего исследования с целью усовершенствования методики интерферонотерапии при хроническом УГХ.
УРОГЕНИТАЛЬНЫИ ХЛАМИДИОЗ
Иркутск, 2007
Далее »» ГЛАВА 2.
МЕТОДЫ ИССЛЕДОВАНИЯ БОЛЬНЫХ ХРОНИЧЕСКИМ УРОГЕНИТАЛЬНЫМ ХЛАМИДИОЗОМ
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)