Опыт применения противовирусного препарата в лечении ротавирусной инфекции у детей
Статьи
О.В. Борисова1, Н.М. Бочкарева1, Н.С. Полежаева1, Т.А. Жилякова2, Н.Г. Царёва1, Е.В. Бердникова1
1 Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89
2 Самарская городская клиническая больница №2 имени Н.А. Семашко; 443008, Россия, Самара, ул. Калинина, д. 32
Опубликовано в : Борисова О.В., Бочкарева Н.М., Полежаева Н.С., Жилякова Т.А., Царёва Н.Г., Бердникова Е.В. Опыт при- менения противовирусного препарата в лечении ротавирусной инфекции у детей. Медицинский совет. 2022;16(1):165–170. doi.org/10.21518/2079-701X-2022-16-1
Резюме
Введение. Ротавирусная инфекция является ведущей причиной острых гастроэнтеритов у детей раннего возраста. В связи с отсутствием этиотропного лечения вирусных гастроэнтеритов интерес ученых и практических врачей к использованию противовирусных препаратов возрастает. В исследованиях отечественных авторов доказано, что низкомолекулярный индуктор интерферона (меглюмина акридонацетат) обладает противовирусной, иммунорегуляторной и противовоспалительной активностью.
Цель исследования. Оценить эффективность и безопасность противовирусного препарата меглюмина акридонацетата при лечении острого гастроэнтерита ротавирусной этиологии у детей 4-7 лет в условиях стационара.
Материалы и методы. Проведен проспективный анализ случаев лечения ротавирусного гастроэнтерита средней тяжести препаратом меглюмином акридонацетатом у детей дошкольного возраста (п = 29, 1-я группа). Группу сравнения составили пациенты, получавшие стандартную терапию (п = 31, 2-я группа). Наличие ротавирусной инфекции подтверждено обнаружением антигена возбудителя в кале. Препарат меглюмина акридонацетат назначался по схеме через день парентерально.
Результаты и обсуждение. Эффективность терапии противовирусным препаратом на 3-и сутки лечения ротавирусного гастроэнтерита средней тяжести составила 79,3% (р < 0,05). Ликвидация основных клинических симптомов заболевания отмечалась на 2-е-3-и сутки: наблюдалось снижение интоксикации, лихорадки, достоверное уменьшение продолжительности рвоты и диареи (р < 0,05), сокращение периода элиминации возбудителя на 2,67 суток (р < 0,01). У всех пациентов переносимость препарата была хорошей, побочные и нежелательные эффекты выявлены не были.
Выводы. Препарат меглюмина акридонацетат может быть рекомендован для комплексного лечения ротавирусной инфекции средней тяжести с первых дней заболевания.
Ключевые слова: дети, острый гастроэнтерит, ротавирусная инфекция, меглюмина акридонацетат, проспективный анализ
Experience with the use of the drug cycloferon in the treatment of rotaviral infection in children
Olga V. Borisova1, Nataliya M. Bochkareva1, Nataliya S. Polezhaeva1, Tamara A. Zhilyakovа2, Nataliya G. Tsaryova1, Ekaterina V. Berdnikova1
1 Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia
2 Semashko Samara City Clinical Hospital No. 2; 32, Kalinin St., Samara, 443008, Russia
Abstract
Introduction. Rotavirus infection is the leading cause of acute gastroenteritis in young children. Due to the lack of etiotropic treatment of viral gastroenteritis, the interest of scientists and practitioners in the use of antiviral drugs is increasing. Studies of domestic authors have proven that the low molecular weight interferon inductor - meglumine acridonacetate has antiviral, immunoregulatory and anti-inflammatory activity.
Aim. Evaluation of the efficacy and safety of the antiviral drug meglumine acridonacenate in the treatment of acute gastroenteritis of rotavirus etiology in children aged 4-7 years in a hospital setting.
Materials and methods. A prospective analysis of cases of treatment with meglumine acridonacetate for moderately severe rotavirus gastroenteritis in preschool children (n = 29, group I) was carried out. The comparison group consisted of patients receiving standard therapy (n = 31, group II). The presence of rotavirus infection was confirmed by the detection of the pathogen antigen in the feces. Meglumine acridonacetate was prescribed according to the scheme, parenterally, every other day.
Results and discussion. The effectiveness of therapy with an antiviral drug on the 3rd day of treatment of moderately severe rotavirus gastroenteritis was 79.3% (p < 0.05). The elimination of the main clinical symptoms of the disease was noted on days 2-3: a decrease in the symptoms of intoxication, fever, a significant decrease in the duration of vomiting and diarrhea (p < 0.05), a reduction in the pathogen elimination period by 2.67 days (p < 0.01), meglumine acridonacetate was well tolerated, no side effects of the drug were detected.
Conclusions. Meglumine acridonacetate can be recommended for the complex treatment of moderate rotavirus infection from the first days of the disease.
Keywords: children, acute gastroenteritis, rotavirus infection, meglumine acridonacetate, prospective analysis
Введение
Ротавирусная инфекция является наиболее частой причиной диареи у детей до 5 лет [1, 2]. Несмотря на введение вакцинопрофилактики против данного заболевания во всем мире почти 15 лет назад, ротавирусная инфекция приводит к более чем 200 000 смертей ежегодно в основном в странах с низким уровнем доходов [3]. На фоне пандемии COVID-19 в 2020 г. заболеваемость ротавирусной инфекцией в РФ снизилась в 2 раза по сравнению с 2019 г. и составила 33,94 случая заболевания на 100 000 населения, в то время как в 2019 г. было выявлено 70,26 заболевших на 100 000 чел.).1
1 Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2020 году». М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека; 2021. 256 с.
Ротавирус вызывает диарейный синдром вследствие двух реализуемых механизмов: осмотической диареи, которая развивается из-за мальабсорбции (вторична по отношению к повреждению и гибели энтероцитов или снижению абсорбционной функции эпителия) и секреторной диареи, появляющейся из-за эффектов неструктурного белка энтеротоксина NSP4 и активации кальций-зависимых хлоридных каналов [4]. Восприимчивость к ротавирусной инфекции моделируется как иммунологическими, так и не иммунологическими факторами (дифференциальная экспрессия ротавирусных рецепторов в кишечнике, состав желудочного сока и др.) [5].
Ротавирусы распознаются рецепторами (PRR) в энтероцитах или в клетках иммунной системы, в т. ч. в макрофагах, дендритных клетках или в адаптивных В-клетках и Т-клетках. Вирус избегает воздействия направленных на него факторов врожденного иммунитета, синтезируя антагонист интерферонов - NSP1-протеин, - который воздействует на клеточные белки, необходимые для продукции IFN, а также ингибирует активацию STAT1, который вызывает транскрипцию IFN-стимулированных генов (ISG) и повышает продукцию IFN [3, 6, 7]. Таким образом, ротавирус блокирует ответы IFN I и III типов (рис. 1).
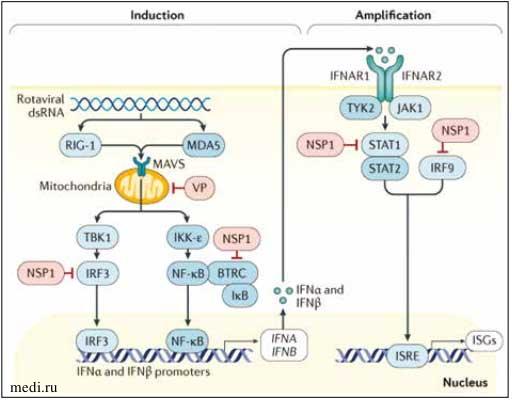 Рисунок 1.
Рисунок 1. Ротавирус-опосредованное ингибирование индукции и амплификации интерферона [3]
Figure 1. Rotavirus-mediated inhibition of interferon induction and amplification [3]
Индукторы интерферона - это семейство природных и синтетических соединений, стимулирующих пролиферацию и дифференцировку клеток костного мозга с использованием механизмов врожденного и адаптивного иммунитетов [8]. Представителем низкомолекулярных индукторов IFN является Циклоферон (меглюмина акридонаце-тат), противовирусная активность которого связана с выработкой эндогенного интерферона и прямым воздействием на репликацию вируса. Препарат обладает иммунорегуляторной активностью вследствие активации IFN-γ и противовоспалительной активностью: он оказывает ингибирующее влияние на синтез провоспалительных цитокинов IL-1, IL-8, TNF-a. Кроме этого, Циклоферон активирует гуморальный и клеточный ответы, фагоцитоз, усиливает функциональную активность нейтрофильных гранулоцитов, способствует выработке всех трех типов интерферона - I, II, III (альфа-, бета-, гамма-интерферон и лямбда-интерферон) [8, 9]. Эндогенная интерферонизация (использование индукторов интерферона) имеет преимущества перед введением экзогенного IFN. При введении Циклоферона синтезируется собственный IFN, который не обладает антигенной активностью.
В Российской Федерации проводятся многочисленные исследования, посвященные эффективности использования индукторов интерферона в лечении острых респираторных вирусных инфекций. Так, Мазина Н.К. и др. в исследовании, проведенном в 2017 г., проанализировали 531 публикацию по оценке клинической эффективности Циклоферона при вирусных инфекциях органов дыхания и иммунодефицитных состояниях у детей и взрослых [10]. Однако известно не так много исследований применения препарата при кишечных инфекциях вирусной этиологии. Согласно данным научной работы Романцова М.Г. и др., осуществленной в 2010 г., Циклоферон в таблетках чаще назначается при ОРВИ (в 62,5% случаев) и герпесвирусных инфекциях (в 32% случаев), тогда как его применение при кишечных инфекциях составляет лишь 13,6% [8].Ученые Смоленского государственного медицинского университета изучили эффективность препарата у пациентов с хроническим эрозивным гастритом, ассоциированным с Helicobacter pylori, и герпесвирусной инфекцией [11]. Применение Циклоферона на фоне эрадикационной терапии позволяет сократить частоту обострений заболевания и увеличить срок ремиссии.
Гордеец А.В. и др. в 2007 г. провели плацебо-контролируемые исследования больных ротавирусной инфекцией, которые получали препарат Циклоферон (86 детей) и плацебо (22 ребенка). Авторы выявили высокую эффективность Циклоферона: основные симптомы заболевания (рвота, диарея, лихорадка) исчезали на 1,5-2 дня раньше по сравнению с группой контроля. Отмечено повышение продукции IL-2 до 60 кг/мл, что в 6 раз выше по сравнению с пациентами, получающими плацебо (10 кг/мл). Исследователи рекомендуют использовать препарат с первых дней заболевания в комплексной терапии ротавирусной инфекции [12].
Романцовым М.Г. и Тихомировой О.В. показана зависимость течения кишечных инфекций вирусной этиологии от интенсивности антительного ответа и индукции IFN-a, что является основанием применения Циклоферона в комплексной терапии кишечных инфекций [13]. Исследователями доказано, что использование препарата привело к сокращению продолжительности основных клинических проявлений ротавирусной инфекции (лихорадка, интоксикация, катаральные явления, диарея и др.). У пациентов, получавших препарат, отмечено снижение ротавирусного антигена в 7,1 раза на фоне стимуляции противовирусных антител, которые увеличились в 2,9 раза [13].
Таким образом, основываясь на данные научных исследований вышеуказанных авторов, при лечении ротавирусной инфекции Циклофероном значимое улучшение симптомов заболевания наступает на 2-й-3-й день терапии, отмечается также эффективность и хорошая переносимость лекарственного средства.
Целью нашего исследования является оценка эффективности и безопасности препарата Циклоферон при лечении ротавирусной инфекции у детей 4-7 лет.
Материалы и методы
Проведено проспективное исследование на базе инфекционного отделения Самарской городской клинической больницы №2 имени Н.А. Семашко (клиническая база кафедры детских инфекций Самарского государственного медицинского университета). В исследование вошли 60 детей, средний возраст которых составил 5,8 лет [4,2; 6,7], по половому составу преобладали мальчики (58,3%). У всех детей было диагностировано среднетяжелое течение ротавирусной инфекции. Пациенты были разделены на две группы:
1- я группа - дети с ротавирусной инфекцией (п = 29), которые получали Циклоферон (меглюмина акридонаце-тат) в инъекциях в дополнение к стандартной терапии [13]. В соответствии с инструкцией по использованию препарата детям были назначены инъекции 1 раз в сутки через день в дозировке 10 мг/кг;
2- я группа - дети с ротавирусной инфекцией (п = 31), получавшие стандартную терапию [14].
Критерии включения пациентов в исследование были следующими: наличие ротавирусной инфекции, подтвержденной обнаружением антигенов ротавируса в кале больных до начала терапии; отсутствие других вирусных и бактериальных агентов, поражающих желудочно-кишечный тракт; среднетяжелая форма заболевания; поступление в стационар не позднее 1-2 суток от начала заболевания. Критерии исключения: пациенты с легкими и тяжелыми формами ротавирусной инфекции; дети с иммунодефицитами и отягощенным преморбид-ным фоном (аллергические заболевания, дисбиотические проявления).
Всем пациентам проводились такие лабораторные исследования, как общеклинический анализ крови и мочи, биохимическое исследование крови, бактериологическое исследование кала на кишечную группу бактерий. Обнаружение антигенов ротавируса в образцах кала проведено методом иммунохроматографии с помощью набора 360 R Ротавирус (H&R Rotavirus, Испания). Методом иммунохроматографии исключали вирусную микст-инфекцию: адено-, астро- и норовирусы.
Протокол исследования был утвержден этическим комитетом Самарского государственного медицинского университета. Также было получено информированное письменное согласие законных представителей обследованных детей.
Статистическая обработка числового материала проводилась с использованием статистического пакета Statistica 7.0 (StatSoft, США). Для оценки различий показателей применялся U-критерий Манна-Уитни. Результаты считались статистически значимыми при р < 0,05.
Результаты и обсуждение
Диагноз ротавирусной инфекции устанавливался на основании характерных клинико-эпидемиологических данных: зимний/зимне-весенний сезон, локальность семейных очагов, наличие гастроэнтерита, рвоты, предшествующей им диареи или всех симптомов одновременно, у части детей присутствовали катаральные проявления. У всех пациентов заболевание началось с остро или умеренно выраженных симптомов интоксикации: дети поступали в стационар с жалобами на вялость, снижение аппетита, боль в животе, рвоту и диарею. У всех обследованных детей была среднетяжелая форма заболевания. Тяжелая форма болезни, осложненная токсикозом с эксикозом, чаще регистрировалась у детей в возрасте до 3 лет. Основные клинические симптомы при госпитализации детей представлены на рис. 2.
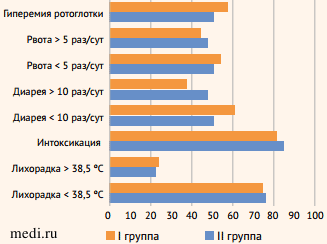 Рисунок 2.
Рисунок 2. Основные клинические симптомы у детей с ротавирусной инфекцией
Figure 2. The main clinical symptoms in children with rotavirus infection
Всем пациентам была назначена стандартная базисная терапия: оральная или по показаниям парентеральная регидратация, диета, сорбенты (смектит диоктаэдрический - 1-2 пакетика в сутки), ферменты (креон, мезим форте, панкреатин), антипиретики (при лихорадке >38,5 оС рекомендовано применять литическую смесь или парацетамол в возрастных дозировках внутрь). В лечении всех изученных пациентов не использовались противовирусные препараты и пробиотики. В дополнение к вышеуказанной терапии пациентам 1-й группы был назначен Циклоферон в инъекциях через день. Средняя продолжительность клинических симптомов ротавирусной инфекции у детей в зависимости от терапии представлена в табл. 1.
Таблица 1.
Table 1.
Продолжительность основных симптомов ротавирусной инфекции в зависимости от проводимой терапии
The duration of the main symptoms of rotavirus infection, depending on the therapy
|
Основные клинические симптомы/синдромы
|
Средняя продолжительность (сутки)
|
| 1-я группа |
2-я группа |
р |
| температура |
2,4 [1,6 ÷ 3,0] |
3,5 [2,5 ÷ 4,7] |
0,04* |
| интоксикация |
2,3 [1,9 ÷ 3,2] |
3,0 [3,7 ÷ 7,2] |
0,07 |
| рвота |
1,5 [1,1 ÷ 2,7] |
2,6 [2,0 ÷ 3,9] |
0,04* |
| диарея |
3,3 [2,8 ÷ 4,9] |
5,2 [3,2 ÷ 6,5] |
0,02* |
| снижение аппетита |
2,2 [1,7 ÷ 4,0] |
5,5 [2,4 ÷ 5,1] |
0,06 |
| гиперемия ротоглотки |
2,6 [1,7 ÷ 3,4] |
4,8 [4,1 ÷ 6,3] |
0,02* |
* U-критерий Манна-Уитни, критерии значимы при р < 0,05
Согласно полученным данным, снижение температуры было отмечено на 3-й день лечения у пациентов 1-й группы, в то время как во 2-й группе лихорадка наблюдалась в течение 4-х дней (р < 0,05). При сравнении пациентов обеих групп симптомы интоксикации были купированы в среднем на один день раньше. Рвота прекратилась после 1-го дня лечения (в группе сравнения -к 3-му дню), диарея в среднем остановилась к 3-му дню госпитализации детей (р < 0,05). Кроме этого, Циклоферон значительно повлиял на гиперемию ротоглотки: использование препарата сократило продолжительность данного симптома до 2,6 дней (р < 0,05).
Таким образом, клинический эффект препарата Циклоферон проявился воздействием на оба ведущих синдрома заболевания: сокращение длительности рвоты было отмечено на 1,1 день раньше (р < 0,05), а диареи -на 1,9 день раньше (р < 0,05). Применение лекарственного средства у пациентов с ротавирусным гастроэнтеритом способствовало значительному сокращению длительности основных клинических симптомов заболевания в среднем ко 2-му-3-му дню терапии, тогда как у детей 2-й группы эти симптомы были купированы к 3-му-4-му дню. Длительность выделения возбудителя у детей обеих групп представлена на рис. 3.
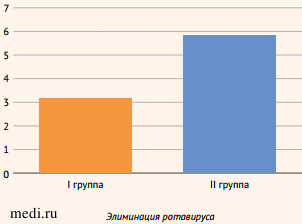 Рисунок 3.
Рисунок 3. Элиминация ротавируса у пациентов обеих групп
Figure 3. Elimination of rotavirus in patients of both groups
* p < 0,01
Согласно нашим данным, элиминация возбудителя (прекращение выделения антигена ротавируса в кале) у пациентов, получающих Циклоферон в дополнение к стандартной терапии, отмечалась на 2,67 дня раньше (р < 0,01). Следовательно, эффективность лечения была достигнута на 3-й день терапии Циклофероном и составила 79,3% (отношение шансов (ОШ): 0,22 (0,05-0,72), р < 0,05).
Безопасность препарата оценивалась по следующим критериям: переносимость и возникновение побочных реакций. Согласно проведенному исследованию Цикло-ферон обладает хорошей переносимостью, побочных нежелательных эффектов препарата выявлено не было.
Клинический случай
Мальчик, 6 лет, заболел остро: повышение температуры до 37,6 °С, двукратная рвота, на 2-е сутки болезни появился жидкий водянистый стул до 10-12 раз в день. При лихорадке в 38,5 оС машиной скорой помощи ребенок был доставлен в инфекционный стационар. В семье были больны еще двое детей-школьников. При объективном осмотре состояние пациента было средней тяжести: кожные покровы чистые бледные, губы сухие, слизистые ротоглотки гиперемированы. Живот умеренно вздут, отмечалась умеренная болезненность при пальпации. Печень и селезенка не увеличены. Обильный пенистый водянистый стул без видимых патологических примесей, с кислым запахом. Мочился достаточно. В общем анализе крови воспалительные изменения не обнаружены, СОЭ -10 мм/ч. Изменения копрограммы соответствовали поражению тонкого кишечника: наблюдалось умеренное количество непереваренной клетчатки, нейтрального жира и мышечных волокон. В кале обнаружен антиген ротавируса. В связи с этим был поставлен диагноз - ротавирусный гастроэнтерит средней тяжести.
Пациенту было назначено следующее лечение: диета, оральная регидратация, Циклоферон в дозе 10 мг/кг через день в/м, диоктаэдрический смектит, креон, литическая смесь при температуре выше 38,5 °С.
После 6-8 ч проводимой терапии состояние ребенка улучшилось: температура понизилась до 37,2 °С, рвота прекратилась, улучшился стул (3 раза в день, разжиженный, необильный). На 2-е сутки лечения наблюдалась нормализация температуры, стул - 2 раза в день, кашицеобразный. На 3-и сутки прекратилась диарея, температура тела имела нормальные показатели, восстановился аппетит, гиперемия ротоглотки не была выявлена.
Таким образом, использование Циклоферона привело к купированию основных симптомов болезни на 3-й день. Уже на 4-е сутки отмечалось полное выздоровление ребенка. Побочных эффектов при приеме препарата не было выявлено. Препарат Циклоферон доказал свое противовирусное и иммунорегуляторное действие. Показана его высокая эффективность и безопасность при лечении ротавирусного гастроэнтерита средней тяжести у детей.
Выводы
Согласно данным отечественных исследователей, при терапии вирусных инфекций отмечается высокая эффективность препарата Циклоферон. По данным нашего исследования, в комплексной терапии ротавирусной инфекции при использовании препарата парентерально эффективность лечения на 3-и сутки составила 79,3% (р < 0,05). Также включение Циклоферона в комплексную терапию ротавирусного гастроэнтерита способствует регрессу симптомов интоксикации, лихорадки (р < 0,05), достоверному уменьшению продолжительности рвоты и диареи (р < 0,05), сокращению периода элиминации возбудителя на 2,67 суток (р < 0,01), уменьшению длительности заболевания в среднем на 2-е суток. Исходя из этого, низкомолекулярный индуктор интерферона - препарат Циклоферон - может быть использован в комплексном лечении ротавирусной инфекции с первых дней развития заболевания.
Информация об авторах:
Борисова Ольга Вячеславовна, д.м.н., профессор, заведующая кафедрой детских инфекций, Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89.
Бочкарева Наталия Михайловна, к.м.н., доцент, доцент кафедры детских инфекций, Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89.
Полежаева Наталья Сергеевна, к.м.н., доцент, доцент кафедры детских инфекций, Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89.
Жилякова Тамара Анатольевна, ассистент кафедры детских инфекций, заведующая инфекционным отделением, Самарская городская клиническая больница №2 имени Н.А. Семашко; 443008, Россия, Самара, ул. Калинина, д. 32.
Царёва Наталия Герасимовна, ассистент кафедры детских инфекций, Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89.
Бердникова Екатерина Викторовна, аспирант кафедры детских инфекций, Самарский государственный медицинский университет; 443099, Россия, Самара, ул. Чапаевская, д. 89.
Information about the authors:
Olga V. Borisova, Dr. Sci. (Med.), Professor, Head of the Department of Children’s Infections, Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia.
Nataliya M. Bochkareva, Cand. Sci. (Med.), Associate Professor of the Department of Children’s Infections, Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia.
Nataliya S. Polezhaeva, Cand. Sci. (Med.), Associate Professor of the Department of Children’s Infections, Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia.
Tamara A. Zhilyakovа, Assistant of the Department of Children’s Infections, Head of the Department of Infectious Diseases, N.A. Semashko Samara City Clinical Hospital No. 2; 32, Kalinin St., Samara, 443008, Russia.
Nataliya G. Tsareva, Assistant of the Department of Children’s Infections, Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia.
Ekaterina V. Berdnikova, Postgraduate Student of the Department of Children’s Infections, Samara State Medical University; 89, Chapaevskaya St., Samara, 443099, Russia.
Список литературы / References
1. Горбунов С.Г, Мазанкова Л.Н., Майкова И.Д., Демина О.И., Коваль Е.П. Особенности иммунного ответа и эффективность иммунотерапии при ротавирусной инфекции у детей. Детские инфекции. 2018;17(3):38-46.
Gorbunov S.G., Mazankova L.N., Maykova I.D., Demina O.I., Koval E.P Features of the immune response and efficacy immunotherapy for rotavirus infection in children. Children Infections. 2018;17(3):38-46.
2. Matthijnssens J., Ruggeri F., Esona M.D., Steyer A., Estes M., Banyai K. et al. Rotavirus Classification Working Group: RCWG. KU Leuven Laboratory of Viral Metagenomics; 2017.
3. Crawford S.E., Ramani S., Tate J.E., Parashar U.D., Svensson L., Hagbom M., Franco M.A. et al. Rotavirus infection. Nat Rev Dis Primers. 2017;3:17083.
4. Wiegering V., Kaiser J., Tappe D., Weissbrich B., Morbach H., Girschick J.H. Gastroenteritis in childhood: a retrospective study of 650 hospitalized pediatric patients. Int J Infect Dis. 2011;15;e401-e407.
5. Venkataram P.B.V., Shanker S., Hu L., Choi J.-M., Crawford S.E., Ramani S. et al. Structural basis of glycan interaction in gastroenteric viral pathogens. Curr Opin Virol. 2014;7:119-127.
6. Broquet A.H., Hirata Y., McAllister C.S., Kagnoff M.F. RIG-I/MDA5/MAVS are required to signal a protective IFN response in rotavirus-infected intestinal epithelium. J Immunol. 2011;186(3):1618-1626.
7. Lin J.D., Feng N., Sen A., Balan M., Tseng H.-C., McElrath C. et al. Distinct Roles of Type I and Type III Interferons in Intestinal Immunity to Homologous and Heterologous Rotavirus Infections. PLoS Pathog. 2016;12(4):e1005600.
8. Романцов М.Г, Горячева Л.Г, Бехтерева М.К., Сологуб Т.В., Коваленко А.Л. Эффективность циклоферона при вирусных и бактериальных инфекциях у детей (клинический обзор). Антибиотики и химиотерапия. 2010;55(11-12):39-51.
Romantsov M.G., Goryacheva L.G., Bekhtereva M.K., Sologub T.V., Kovalenko A.L. Cycloferon Efficacy in Viral and Bacterial Diseases of Children (Clinical Review). Antibiotiki i Khimioterapiya. 2010;55(11-12): 39-51. (In Russ.)
9. Коваленко А.Л., Григорян С.С., Романцов М.Г, Петров А.Ю., Музыкин М.А., Исаева Е.И. Интерферониндуктивная активность и продукция интерферонов под влиянием солей акридонуксусной кислоты. Экспериментальная и клиническая фармакология. 2014;77(11):16-19.
Kovalenko A.L., Grigoryan S.S., Romantsov M.G., Petrov A.Yu., Muzykin M.A., Isaeva E.I. Interferon inductor activity and interferon production under the action of acridonacetic acid. Eksperimentalnaya i Klinicheskaya Farmakologiya. 2014;77(11):16-19.
10. Мазина Н.К., Шешунов И.В., Мазин П.В., Мазин В.П., Коваленко А.Л., Заплутанов В.А. Клиническая эффективность иммуномодулятора циклоферона (таблетки) при вирусных инфекциях органов дыхания: результаты систематического обзора и матаанализа. Терапевтический архив. 2017;89(11):84-92. Mazina N.K., Sheshunov I.V., Mazin P.V., Mazin V.P., Kovalenko A.L., Zaplutanov V.A. Clinical efficacy of the immunomodulatory agent cyclofer-on (tablets) in viral respiratory infections: Results of a systematic review and meta-analysis. Terapevticheskii Arkhiv. 2017;89(11):84-92.
11. Афанасенкова Т.Е., Дубская Е.Е. Влияние Циклоферона на результаты лечения пациентов с хроническим эрозивным гастритом, ассоциированным с Helicobacter pylori и герпес-вирусной инфекцией. Кубанский научный медицинский вестник. 2017;1(2):14-17.
Afanasenkova T.E., Dubskaya E.E. Effect of cycloferon on the results of treatment of patients with chronic erosive gastritis associated with Helicobacter pylori and herpes infection. Kuban Scientific Medical Bulletin. 2017;1(2):14-17.
12. Гордеец А.В., Седулина О.Ф., Юрусова Е.Н., Аникина О.Л., Яшеня О.В. Циклоферон в лечении ротавирусной диареи у детей. Детские инфекции. 2007;(2):62-64.
Gordeets A.V., Sedulina O.F., Yurusova E.N., Anikina O.L., Yashenya O.V. Cycloferon used for curing rotaviral diarrhea in children. Children Infections. 2007;(2):62-64.
13. Романцов М.Г, Тихомирова О.В. Терапия кишечных инфекций у детей. Фундаментальные исследования. 2010;(3):122-137.
Romantsov M.G., Tikhomirova O.V. Therapy of intestinal infections at children. Fundamental Research. 2010;(3):122-137.
14. Новокшонов А.А., Мазанкова Л.Н., Учайкин В.Ф. Клинические рекомендации по диагностике и лечению ОКИ у детей в зависимости от типа диареи. Лечение и профилактика. 2013;(4):62-73.
Novokshonov A.A., Mazankova L.N., Uchaykin V.F. Clinical guidelines for the diagnosis and treatment of acute intestinal infections in children, depending on the type of diarrhea. Disease Treatment and Prevention. 2013;(4):62-73.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)


 Рисунок 1. Ротавирус-опосредованное ингибирование индукции и амплификации интерферона [3]
Рисунок 1. Ротавирус-опосредованное ингибирование индукции и амплификации интерферона [3] Рисунок 2. Основные клинические симптомы у детей с ротавирусной инфекцией
Рисунок 2. Основные клинические симптомы у детей с ротавирусной инфекцией Рисунок 3. Элиминация ротавируса у пациентов обеих групп
Рисунок 3. Элиминация ротавируса у пациентов обеих групп