Влияние препарата циклоферон на флору миндалин у часто болеющих детей
Статьи
Опубликовано в журнале:
« Экспериментальная и клиническая фармакология » № 3, 2013 С.А. Ляликов, П.Г. Бедин, СЮ. Ермак, Р.В. Янович
УО «Гродненский государственный медицинский университет». Кафедра клинической лабораторной диагностики и иммунологии (заведующий кафедрой профессор С.А. Ляликов). Беларусь, г. Гродно.
Резюме. Для оценки способности препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей (ЧБД) была изучена микрофлора миндалин до и после стандартного курса этого препарата у 68 дошкольников, относящихся к категории ЧБД. Установлено, что микробный пейзаж поверхности миндалин детей после курса циклоферона характеризовался уменьшением разнообразия микрофлоры и снижением титра бактерий, в том числе и золотистого стафилококка, а также уменьшением количества штаммов, резистентных к бензилпенициллину, клиндамицину и ванкомицину. Таким образом, препарат циклоферон можно рекомендовать для реабилитации ЧБД. Ключевые слова: часто болеющие дети, циклоферон, микрофлора миндалин.
Введение.
По современным литературным данным в группу часто болеющих детей (ЧБД) входят на том или ином возрастном этапе от 15 до 65% детской популяции [10], в связи с этим частые респираторные заболевания является актуальной проблемой педиатрии [4, 9]. В 1986 году В.Ю. Альбицким и А.А. Барановым была предложены критерии включения детей в группу часто болеющих. К (ЧБД) относят детей, страдающих острыми респираторными заболеваниями (ОРЗ) свыше 4-х раз в год в возрасте до 1 года, 6-и раз – в 1-3 года, 5-и раз – в 4-5 лет и 4-х раз – после 5 лет [1].
Система иммунитета в детском возрасте характеризуется относительно пониженным уровнем нейтрофилов – основных эффекторных клеток врожденного звена иммунного ответа, а также низкой продукцией иммуноглобулинов на фоне повышенного числа Т- и В-лимфоцитов, что свидетельствует о неполноценности адаптивного звена [8]. Это в совокупности с анатомо-физиологическими особенностями органов дыхания [6], недостаточными гигиеническими навыками и расширением контактов с окружающим миром делает детей дошкольного возраста особенно уязвимыми для инфекций.
Несмотря на то, что вирусы являются этиологическими агентами более чем в 80% случаев ОРЗ [2], по данным литературы в практической медицине для их лечения в большинстве случаев, даже при неосложнённом течении, используются антибактериальные (АБ) препараты [13, 14], что способствует развитию дисбиоза. Показано, что после перенесенного эпизода ОРЗ дисбиотические изменения микрофлоры зева сохраняются до 1,5 месяцев [11]. Гибель резидентной микрофлоры приводит к заселению биотопа условно-патогенными микроорганизмами. Существуют данные, что 35% детей, относящихся к группе ЧБД, имеют хроническую ЛОР патологию [10]. Не менее, чем в 30% случаев, ЧБД являются носителями β-гемолитического стрептококка группы А [3, 7]. Не менее 50% детей являются носителями золотистого стафилококка [7, 9].
В эксперименте на мышах было продемонстрировано, что введение интерферона 1 типа сокращало сроки персистенции золотистого стафилококка и количество персистирующих бактерий, способствовало нормализации показателей иммунного статуса и повышению выживаемости при стафилококковой инфекции [5]. Иммуномодулирующий эффект интерферона II типа ещё более выражен. Установлено, что ?-интерферон активно стимулирует макрофаги, усиливает экспрессию молекул МНС I и II, стимулирует дифференцировку Т-хелперов нулевого типа в Т-хелперы первого типа [12].
Приведенное выше факты определили цель нашего исследования: оценить способность индуктора эндогенного интерферона – препарата циклоферон влиять на микробиологический пейзаж поверхности миндалин у часто болеющих детей.
Материалы и методы.
Было обследовано 68 детей (32 девочки и 36 мальчиков) в возрасте от 4 до 7 лет, медиана (Ме) – 5,1 лет, нижняя квартиль (Q25) – 4,5 года, верхняя квартиль (Q75) – 5,8 лет. Все дети посещали специализированные детские сады (№94 и №95) г. Гродно для ЧБД. Критериями включения в исследование были добровольное информированное согласие законных представителей детей, возраст 4-7 лет, отсутствие острых инфекционных заболеваний на момент обследования, наличие в анамнезе 6-и и более эпизодов ОРЗ за предшествующие 12 месяцев. Обследование включало клинический осмотр детей, анкетирование родителей и выкопировку данных из амбулаторной карты (форма №112-у).
Двукратно, до начала приема препарата циклоферон и через 2 недели после окончания приема детям выполнили посев микрофлоры с поверхности миндалин. Материал – слизь с поверхности миндалин – брали стерильными ватными тампонами натощак и помещали в универсальную гелевую транспортную среду Стюарта фирмы Copan (Италия). В течение 2 часов полученный материал доставлялся в лабораторию. Для идентификации микрофлоры и определения её чувствительности к антибактериальным препаратам была использована автоматизированная система VITEC-2 фирмы BioMerieux (Франция). Тестирование чувствительности к антибактериальным препаратам осуществлялось методом минимальных ингибирующих концентраций.
Препарат циклоферон (таблетки по 0,15) назначался двумя курсами (с перерывом в 1 месяц) по схеме, указанной в аннотации: на курс по 1 таблетке 1 раз в день за полчаса до еды в 1, 2, 4, 6, 8, 11, 14, 17, 20 и 23 дни.
Статистический анализ проводился с использованием стандартного пакета прикладных программ Statistica версия 6.0. При сравнении двух независимых групп изучаемой переменной использовали тест Манна-Уитни (U), в случае зависимости групп – тест Вилкоксона (Z). При сравнении долей (процентов) использовался метод Фишера (Fisher exact test). Нулевая гипотеза об отсутствии различий между переменными отвергалась на уровне значимости α=0,05 (p ≤0,05) для каждого из использованных тестов. Для представления результатов статистической обработки использовали величины медианы (Me), верхней (Q75) и нижней квартилей (Q25) в формате Me (Q25-Q75).
Результаты и обсуждение.
В мазках из зева, полученных до лечения, были выделены представители 25 семейств, родов и видов микроорганизмов (таблица 1). Наиболее частой находкой был золотистый стафилококк. В титрах 1*104 - 1*106 он обнаруживался практически у половины обследованных. У 44 детей (64,71%) была идентифицирована 1 культура, у 14 (20,58%) – 2, у 9 (13,24%) – 3, у 1 (1,47%) – 4 культуры бактерий.
Таблица 1.
Микрофлора с поверхности миндалин ЧБД, выделенная при первом обследовании
| Название | Количество культур | % носителей |
|---|
| Aerococcus viridans | 1 | 1,47 |
| Candida famata | 3 | 4,41 |
| Dermococcus nishinomiyaensis | 1 | 1,47 |
| Erisipelotrix rusiopathiae | 4 | 5,88 |
| Fackmalia hominis | 1 | 1,47 |
| Granulicatella adiacens | 3 | 4,41 |
| Granulicatella elegans | 1 | 1,47 |
| Kocuria kristinae | 1 | 1,47 |
| Kocuria rosea | 4 | 5,88 |
| Leuconostoc mesenterioides | 1 | 1,47 |
| Leuconostoc mesenteroides cremosis | 3 | 4,41 |
| Rothia mucilaginosa | 1 | 1,47 |
| S. aureus | 33 | 48,53 |
| S. epidermidis | 1 | 1,47 |
| S. haemolyticus | 1 | 1,47 |
| S. hominis | 7 | 10,29 |
| S. ludgunensis | 3 | 4,41 |
| S. vitulinus | 1 | 1,47 |
| Serratia marcescens | 1 | 1,47 |
| Sphingomonas thalpophilium | 1 | 1,47 |
| Str. oralis | 12 | 17,65 |
| Str. parasanguinis | 2 | 2,94 |
| Str. pneumoniae | 11 | 16,18 |
| Str. salivarius | 2 | 2,94 |
| Str. spp. | 4 | 5,88 |
| Всего | 103 | |
При повторном обследовании спектр микроорганизмов значительно сузился. В мазках с поверхности миндалин у детей были обнаружены представители только 16 семейств, родов и видов микроорганизмов (таблица 2). Как и при первом исследовании, золотистый стафилококк выявлялся практически у половины обследованных, но в более низких титрах (по сравнению с исходными р=0,04) (рисунок 1). У 11 детей (25,58%) рост бактерий отсутствовал, у 24 детей (55,81%) была идентифицирована 1 культура, у 6 (13,96%) – 2, у 2 (13,96%) – 3 культуры бактерий.
Таблица 2.
Микрофлора с поверхности миндалин ЧБД, выделенная при повторном обследовании
| Название | Количество культур | % носителей |
|---|
| Нет роста | 11 | 25,58 |
| Acinetobacter ursingii | 1 | 2,32 |
| Candida | 3 | 6,98 |
| E.coli | 1 | 2,32 |
| Enterobacter cloacae | 2 | 4,65 |
| Kocuria roseae | 1 | 2,32 |
| Micrococcus luteus | 1 | 2,32 |
| Pantoteae spp. | 1 | 2,32 |
| Ps.aeruginosa | 1 | 2,32 |
| S.aureus | 19 | 44,19 |
| S.epidermidis | 1 | 2,32 |
| S.warneri | 1 | 2,32 |
| Stenotrophomonas maltophyla | 1 | 2,32 |
| Str.oralis | 3 | 6,98 |
| Str.parasanguinis | 1 | 2,32 |
| Str.sanguinis | 2 | 4,65 |
| Str.spp. | 3 | 6,98 |
| Всего | 42 | 100,0 |
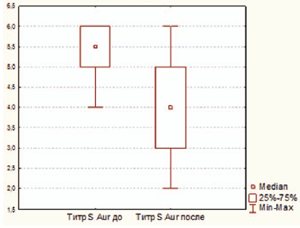
Рисунок 1. Динамика титра S. aureus у ЧБД, принимавших циклоферон
При анализе чувствительности к антибиотикам золотистого стафилококка, высеянного с поверхности миндалин ЧБД, при повторном исследовании было установлено несущественное уменьшение доли метициллин-, рифампицин-, эритромицин-, тетрациклин резистентных штаммов и достоверное снижение процента штаммов устойчивых к бензилпенициллину, ванкомицину и клиндамицину по сравнению с исходными показателями (таблица 3).
Таблица 3.
Доля (%) S. aureus, резистентных к антибиотикам до и после лечения
| Антибиотики | До приема циклоферона | После приема циклоферона | Р |
|---|
| MRSA | 10,00 | 5,26 | - |
| Бензилпенициллин | 84,09 | 63,64 | 0,05 |
| Ванкомицин | 26,67 | 4,55 | 0,03 |
| Клиндамицин | 20,93 | 0,0 | 0,02 |
| Линезолид | 0,0 | 0,0 | - |
| Моксифлоксацин | 0,0 | 0,0 | - |
| Оксациллин | 15,56 | 4,55 | - |
| Рифампицин | 4,44 | 0,0 | - |
| Эритромицин | 11,11 | 9,09 | - |
| Гентамицин | 0,0 | 0,0 | - |
| Ципрофлоксацин | 0,0 | 0,0 | - |
| Левофлоксацин | 0,0 | 0,0 | - |
| Тетрациклин | 6,67 | 0,0 | - |
| Нитрфурантоин | 0,0 | 0,0 | - |
| Бисептол | 0,0 | 0,0 | - |
| Дальфопристин | 0,0 | 0,0 | - |
На фоне приема циклоферона изменилась не только обсемененность поверхности миндалин золотистым стафилококком, но и непатогенной микрофлорой. При повторном обследовании среднее количество обнаруженных непатогенных видов бактерий и их титры были достоверно ниже (в обоих случаях p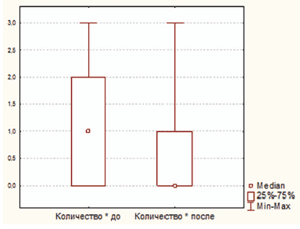
Рисунок 2. Количество непатогенных видов микроорганиз
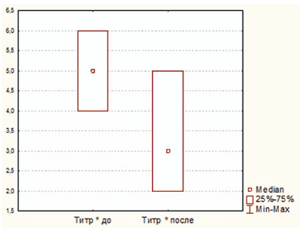
Рисунок 3. Динамика титра непатогенной микрофлоры у ЧБД, принимавших циклоферон
Поскольку циклоферон не обладает прямой антибактериальной активностью, можно предположить, что снижение обсемененности и видового разнообразия микроорганизмов поверхности миндалин обусловлено иммунокоррегирующими свойствами этого препарата.
Уменьшение количества устойчивых к антибиотикам штаммов на фоне приема циклоферона, несомненно, представляется весьма интересным и важным эффектом ввиду всеобщей тенденции к развитию резистентности к используемым в повседневной практике антибактериальным препаратам. Таким образом, препарат циклоферон можно рекомендовать к применению в составе комплексной терапии и для реабилитации ЧБД.
Выводы
Прием двух курсов препарата циклоферон (с перерывом в 1 месяц) по схеме, указанной в аннотации снижает у ЧБД видовое разнообразие микрофлоры поверхности миндалин, достоверно уменьшает обсеменённость поверхности миндалин микрофлорой, в том числе золотистым стафилококком.
Приём препарата циклоферон приводит к значимому снижению количества штаммов золотистого стафилококка устойчивых к бензилпенициллину, ванкомицину и клиндамицину. Список литературы
В. Ю. Альбицкий, А. А. Баранов, Частоболеющие дети. Клинико-социальные аспекты. Пути оздоровления, Саратов (1986). А. Г.
Бойцов В.П. Иванов, О.Н. Ластовка, А.А. Порин, Введение в клиническую микробиологию, издательство СПбГМА им. И.И. Мечникова, Санкт Петербург (1999).
И. В. Василевский, Реабилитация часто болеющих детей: учебебно-методическое пособие, БелМАПО, Минск (2006).
И. В. Василевский, Медицина, № 2, 93 – 99 (2008).
Н. Я. Спивак, В.Г. Лисовенко, В.С. Зуева [и др.], Журнал микробиологии, эпидемиологии и иммунобиологии, № 5, 74 – 77 (1984).
Т. В. Капитан, Пропедевтика детских болезней с уходом за детьми, МЕДпресс-информ, Москва (2004).
О. В. Лутовина, Вестник новых медицинских технологий, 15(3), 56 – 60 (2008).
С. А. Ляликов, Медико-биологические проблемы жизнедеятельности, 5(1), 109 – 115 (2011).
Т. П. Маркова, Д. Г. Чувиров, Ремедиум, № 6, 26 – 28 (2010).
Г. А. Самсыгина, Г. С. Коваль, Педиатрия им. Г.Н. Сперанского, 89(2), 137 – 145 (2010).
Л . В. Феклисова, Е.Р. Мескина, Е.А. Воропаева, Л.В. Пожалостина [и др.], Эпидемиология и инфекционные болезни, № 4, 14 – 18 (2007).
А. А. Ярилин, Иммунология, Медицина, Москва (1999).
R. Gonzales, D.C. Malone, J.H. Maselli, M.A. Sande, Clin. Infect. Dis., 33, 757 – 762 (2001).
H. Goossens, M. Ferech, R.V. Stichele, M. Elseviers, The Lancet, 365, 579 – 587 (2005).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)





