Оценка эффективности противовирусной терапии активной инфекции, вызванной ВГЧ-6А/В, у детей 4 лет и старше
Статьи
- Опубликовано в журнале:
Вопросы практической педиатрии, 2020, том 15, №2, с. 32-40
DOI: 10.20953/1817-7646-2020-2-32-40
Е.В. Мелехина, А.Д. Музыка, Ж.Б. Понежева
Центральный НИИ эпидемиологии Роспотребнадзора, Москва, Российская Федерация
Цель. Инфекция ВГЧ-6А/В, благодаря существованию вируса в двух различных вариантах и возможности хромосомной интеграции в геном хозяина, занимает особое место в группе герпесвирусных инфекций. Рациональный подбор противовирусной терапии в зависимости от стадии заболевания определяет дальнейшее течение, формирование соматической патологии и последующей реактивации инфекции.
Пациенты и методы. В настоящем исследовании оценивалась эффективность противовирусной терапии у 42 детей от 4 лет и старше, госпитализированных в стационар с клиническими проявлениями острой респираторной инфекции и активной инфекцией ВГЧ-6А/В, подтвержденной обнаружением ДНК и/или антигенов ВГЧ-6А/В в крови. В основную группу 1 вошли 15 детей, получавшие препарат меглумина акридонацетат, в основную группу 2-14 детей, получавшие препарат ацикловир в таблетках; группу сравнения составили 13 пациентов, получавших только симптоматическое лечение респираторной инфекции.
Результаты. Назначение препарата меглумина акридонацетат детям с активными формами герпесвирусных инфекций и проявлениями острого респираторного заболевания приводило к более быстрому купированию клинических проявлений заболевания по сравнению с группой, получавшей ацикловир.
Заключение. Повторное обследование перед выпиской из стационара через 10±2 дня и через 30±7 дней от начала заболевания продемонстрировало наиболее выраженный противовирусный эффект препарата меглумина акридонацетат в отношении ВГЧ-6А/В по сравнению с ацикловиром не только к моменту купирования основных клинических проявлений заболевания, но и через 30 дней после выписки из стационара.
Ключевые слова: ВГЧ-6А/В, ацикловир, меглумина акридонацетат, дети
Для цитирования: Мелехина Е.В., Музыка А.Д., Понежева Ж.Б. Оценка эффективности противовирусной терапии активной инфекции, вызванной ВГЧ-6А/В, у детей 4 лет и старше. Вопросы практической педиатрии. 2020; 15(2): 32-40. (In Russian). DOI: 10.20953/1817-7646-2020-2-32-40
Для корреспонденции:
Мелехина Елена Валериевна, доктор медицинских наук, доцент по специальности педиатрия, старший научный сотрудник клинического отдела инфекционной патологии Центрального НИИ эпидемиологии Роспотребнадзора
Адрес: 111123, Москва, ул. Новогиреевская, За
Efficacy of antiviral therapy for active HHV-6A/B infection in children aged 4 years and older
E.V.Melekhina, A.D.Muzyka, Zh.B.Ponezheva
Central Research Institute of Epidemiology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow, Russian Federation
Objective HHV-6A/B infection occupies a special place among herpesviruses due to the existence of the virus in two different variants and the possibility of chromosomal integration into the host genome. Rational selection of antiviral therapy, depending on the stage of the disease, determines the further course, the formation of somatic pathology and subsequent reactivation of the infection.
Patients and methods. This study evaluated the effectiveness of antiviral therapy in 42 children 4 years and older who were hospitalized with clinical manifestations of acute respiratory infection and active HHV-6A/B, confirmed by the detection of DNA and/or HHV-6A/B antigens in the blood. The main Group1 included 15 children who received the drug meglumin acridonacetate, the main Group 2-14 children who received the drug Acyclovir in tablets; the comparison group consisted of 13 patients who received only symptomatic treatment of respiratory infection.
Results. Administration of the drug meglumin acridonacetate to the treatment of children with active forms of herpesvirus infection and manifestation of acute respiratory disease, led to faster relief of clinical manifestations of the disease compared to the group acyclovir.
Conclusion. Examination before discharge from the hospital after 10±2 days and 30±7 days from the onset of the disease demonstrated the most pronounced antiviral effect of the drug meglumin acridonacetate, at the time of relief of the main clinical manifestations of the disease and 30 days after discharge from the hospital.
Key words: HHV-6A/B, aciciovir, meglumine acridonacetate, children
For citation: Melekhina E.V., Muzyka A.D., Ponezheva Zh.B. Efficacy of antiviral therapy for active HHV-6A/B infection in children aged 4 years and older. Vopr. prakt. pediatr. (Clinical Practice in Pediatrics). 2020; 15(2): 32-40. (In Russian). DOI: 10.20953/1817-7646-2020-2-32-40
For correspondence:
Elena V. Melekhina, MD, PhD, DSc, associate professor in pediatrics, senior researcher, clinical department of infectious diseases, Central Research Institute of Epidemiology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being
Address: 3a Novogireevskaya str., Moscow, 111123, Russian Federation
Рациональный подбор противовирусной терапии в зависимости от стадии заболевания определяет дальнейшее течение герпесвирусных инфекций, формирование соматической патологии и последующей реактивации инфекции [1-3]. Противовирусные препараты (ганцикловир, фоскарнет, цидофовир), по мнению большинства зарубежных авторов, являются эффективными в отношении активной инфекции вируса герпеса человека 6А/В (ВГЧ-6А/В), но показания к применению и режимы дозирования до сих пор официально не утверждены [3-5].
Мнения зарубежных ученых относительно терапии инфекции ВГЧ-6А/В противоречивы. Так, часть авторов полагает, эта инфекция у иммунокомпетентных детей самоограничена и не требует лечения [3-6]. Однако у людей с ослабленным иммунитетом реактивация латентного вируса может вызывать опасные для жизни осложнения. Поскольку эффективная вакцина отсутствует, необходимы безопасные и надежные лекарства для лечения инфекций ВГЧ-6А/В [7].
В зарубежной литературе описаны 3 препарата, эффективность которых изучалась в отношении инфекции ВГЧ-6А/В: ганцикловир, фоскарнет и цидофовир. Ганцикловир и цидофовир должны последовательно пройти через три или две стадии фосфорилирования внутри клетки, чтобы перейти в активную форму, оказывающую противовирусный эффект, в то время как фоскарнет действует напрямую, без каких-либо изменений. Фосфорилирование происходит под действием клеточных киназ, за исключением первого этапа процесса фосфорилирования ганцикловира, который катализируется вирусной фосфотрансферазой (или протеинкиназой), кодируемой геном ВГЧ-6 U69. Этот ген расположен в локусе, подверженном мутациям, что приводит к возникновению штаммов ВГЧ-6А/В, устойчивых к противовирусным препаратам: в составе гена U69 для устойчивости к ганцикловиру и ген U38 для устойчивости ко всем трем противовирусным молекулам [8, 9].
Описаны результаты немногочисленных клинических исследований, изучавших эффективность противовирусной терапии у реципиентов после трансплантации гематопоэтических стволовых клеток и с реактивацией ВГЧ-6А/В-инфекции [10]. В частности, ранняя реактивация с увеличением вирусной нагрузки была связана с лихорадкой, кожной сыпью, диареей, легочными осложнениями и неврологическими расстройствами [11]. В плацебо-контролируемом исследовании было показано, что профилактический прием ганцикловира у пациентов после трансплантации костного мозга снижает вероятность кожных высыпаний, интерстициального пневмонита, диареи и тромботической микроангиопатии вследствие реактивации инфекции ВГЧ-6А/В [12]. Однако уже через несколько лет другими научными группами было продемонстрировано, что профилактический прием ганцикловира значимо не оказывает влияния на возникновение реактивации ВГЧ-6 [12, 13].
В отличие от альфа- и гамма-герпесвирусов, бета-герпесвирусы не экспрессируют тимидинкиназу, необходимую для перевода ацикловира в активную форму, но кодируют фосфотрансферазу, которая способна превращать аналоги нуклеозидов в их монофосфат. Два последующих фосфорилирования до активной трифосфатной формы осуществляются с помощью клеточных ферментов дезоксигуанилаткиназа и нуклеозиддифосфаткиназа [14, 15]. В связи с этим ацикловир и его пролекарство (валацикловир) не обладают, по мнению ряда авторов [7, 16], значительной активностью в полученных концентрациях у пролеченных пациентов. Однако, согласно исследованию Agut Н. et al., разрешенный в нашей стране препарат ацикловир эффективен в отношении ВГЧ-6А/В только в очень высоких концентрациях in vitro [4].
В исследовании Perruccio К. et al. проведено сравнение профилактического действия ацикловира и фоскарнета у детей после аллогенной трансплантации гемопоэтических стволовых клеток. В обеих группах была выявлена ранняя ДНК-емия ВГЧ-6А/В после трансплантации. Все пациенты ответили на противовирусное лечение и никто не умер от инфекции, хотя у двоих наблюдались долгосрочные неврологические осложнения. Авторы считают, основываясь на исследованиях in vitro, демонстрирующих инфицирование ВГЧ-6А/В только СD4+-фракций трансплантата, что совместное культивирование CD4+ Т-клеток с CD56+ естественными киллерами может элиминировать вирус, и подчеркивают основную роль NK-клеток в противовирусном иммунном ответе [17].
Мюкке Н.А. была показана эффективность препарата ацикловир в отношении ВГЧ-6А/В-инфекции у детей младше 3 лет и рекомендовано применение внутривенного ацикловира в дозе 30 мг/кг/сут в комбинации с внутривенным введением иммуноглобулина [18]. В более позднем российском исследовании было показано, что подключение ацикловира к комплексной терапии детей с активными формами инфекции ВГЧ-6А/В не приводит к более быстрому купированию симптомов заболевания, но способствует более длительному сохранению астенического синдрома [19].
В ряде работ показана клиническая эффективность валацикловира в терапии хронической инфекции верхних дыхательных путей, связанной с реактивацией герпесвирусных инфекций, в том числе ВГЧ-6А/В [20]. Было продемонстрировано уменьшение (и/или исчезновение) выделения ДНК ВГЧ-6А/В в материале мазков из ротоглотки и цельной крови у часто болеющих взрослых с хроническими воспалительными заболеваниями верхних дыхательных путей на фоне приема валацикловира в дозе 500 мг 3 раза в день, курсом 14 дней [21].
В целом ряде исследований выявлено, что после перенесенных острых первичных форм инфекции, вызванной ВГЧ-6А/В, протекающих в форме мононуклеозоподобного синдрома или тяжелой респираторной инфекции, у детей формируется хроническая соматическая патология на фоне реактивации герпесвирусной инфекции [2, 22, 23]. В связи с вышесказанным встает вопрос о необходимости проведения противовирусной терапии у детей с активными формами инфекции, вызванной ВГЧ-6А/В.
В нашей стране у детей с активными формами герпесвирусных инфекций рекомендованы к применению ацикловир (с рождения) и валацикловир (с 12 лет), инозин пранобекс (с 3 лет), глюкозаминилмурамилдипептид (с 1 года), интерферон-альфа (с рождения), интерлейкин-2 (с рождения), а также меглумина акридонацетат (с 4 лет), пидотимод (с 3 лет) и тилорон (с 7 лет), в соответствии со «Стандартом оказания специализированной медицинской помощи детям при хронических герпесвирусных инфекциях» от 2012 г. [24, 25].
Препарат меглумина акридонацетат (Циклоферон, ООО «НТФФ «ПОЛИСАН», Россия) является интерфероноиндуктором, способствует увеличению продукции интерферона-α в В-клетках, макрофагах и нейтрофилах. Обладает широким спектром фармакологических эффектов, может использоваться как в лечебных, так и в профилактических целях у пациентов с инфекционной и сопутствующей хронической соматической патологией [26]. Принимает участие в программировании иммунного ответа по клеточному или гуморальному типу, будучи регулятором цитокинов: индуцирует интерлейкины ИЛ-2, ИЛ-10, ИЛ-12 и TGF-β, переключает Th0 с синтеза Th2-цитокинов на Th1-ответ [27]. Влияет на состав субпопуляций лимфоцитов: повышается относительное и абсолютное число исходно сниженных общих Т-лимфоцитов (CD3+), Т-хелперов (CD4+), иммунорегуляторного индекса и естественных киллеров (CD16+); снижается – CD8+ и CD72+-лимфоцитов, кроме того, повышается уровень иммуноглобулина А и снижается концентрация иммуноглобулина Е. Препарат меглумина акридонацетат увеличивает провоспалительный потенциал нейтрофилов периферической крови, повышает функциональную активность фагоцитирующих клеток за счет генерации активных форм кислорода, обеспечивая бактерицидность клеток [28, 29].
Противовирусный эффект меглумина акридонацетата обусловлен тем, что под его воздействием образующиеся вирусные частицы становятся преимущественно дефект-интерферирующими (т.е. не содержат капсида и/или клеточной стенки и не способны к дальнейшему повреждению тканей хозяина и размножению). Кроме того, в доклинических исследованиях показано, что под действием препарата происходит ингибирование функций основных ферментов дыхательной цепи митохондрий (опосредованное противовирусное действие) [27]. Молекула интерферона связывается с интерфероновыми рецепторами клеток, в результате чего происходит активация генов, программирующих синтез более 20 внутриклеточных белков, способствующих возникновению резистентности к вирусам, блокируется синтез белков вирусов [30, 31].
Чрезвычайно актуальна тема изучения клинических эффектов индукторов интерферона, в том числе циклоферона, в свете широкого распространения микст-инфицирования, вирусно-вирусных, вирусно-бактериальных, вирусно-хламидийных и других ассоциаций.
Суммируя вышеизложенное, можно сказать, что в отношении использования препаратов с прямым противовирусным действием при инфекции ВГЧ-6А/В нет однозначного мнения. Несмотря на их доказанный механизм действия, высокая токсичность и побочные эффекты ограничивают сферу их применения до жизненных показаний (реципиенты гемопоэтических трансплантатов и трансплантатов солидных органов). Учитывая способность ВГЧ-6А/В к мутациям в локусе протеаз, необходимых для фосфорилирования циклических нуклеозидов, и, как следствие, выработку к ним резистентности, ведется разработка новых противовирусных молекул с принципиально другими механизмами действия на вирусные частицы, таких как brincidofovir [32, 33], CMV423 [34, 35]. Однако до применения в клинической и тем более в педиатрической практике эти препараты должны пройти еще не одно клиническое испытание.
Таким образом, инфекция ВГЧ-6А/В, благодаря особенностям патогенеза и существования вируса в двух различных вариантах, занимает особое место в группе герпесвирусных инфекций. Остается много нерешенных вопросов, касающихся терапии различных форм инфекции ВГЧ-6А/В, в том числе активных форм болезни у детей.
Цель исследования – оценить эффективность применения противовирусной терапии при активной инфекции, вызванной ВГЧ-6А/В у детей.
Пациенты и методы
В настоящем исследовании оценивалась эффективность и безопасность препарата меглумина акридонацетат в таблетках для приема через рот, препарата ацикловир в таблетках для приема через рот, группа сравнения получала только симптоматическую терапию. Рандомизацию пациентов проводили по номеру истории болезни.
Для оценки клинической и лабораторной эффективности противовирусной терапии у детей было проанализировано течение заболевания у 42 пациентов 4 лет и старше с активными формами ВГЧ-6А/В инфекции (острой первичной – 15 пациентов и реактивированной – 27 пациентов), госпитализированных в инфекционное отделение с клиническими проявлениями острой респираторной инфекции (ОРИ).
Критериями включения в исследование были: возраст от 4 лет и старше; подтвержденный лабораторными методами диагноз активной инфекции, вызванной ВГЧ-6А/В; отсутствие указаний в анамнезе на аллергические реакции на препараты; отсутствие тяжелой соматической патологии; подписание родителями пациента добровольного информированного согласия.
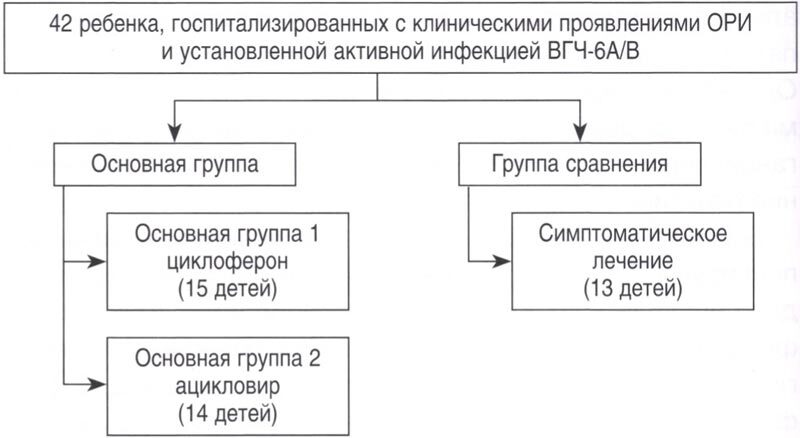
В основную группу были включены 29 детей (17М/12Д), получавших противовирусное лечение. Дети были рандомизированы на основную группу 1, получавшую препарат меглумина акридонацетат (15 детей; 9М/6Д); основную группу 2, получавшую препарат ацикловир в таблетках (14 детей; 8М/6Д). Группу сравнения составили 13 пациентов (6М/7Д), получавших только симптоматическое лечение риносинусита, тонзиллофарингита, а также противокашлевые препараты.
Группы были сопоставимы по полу, возрасту и форме инфекции, вызванной ВГЧ-6А/В (табл. 1).
Таблица 1. Характеристика групп при исследовании противовирусной терапии
Table 1. Characteristics of patient groups
| Параметры / Parameters | Основная группа 1, меглумина акридонацетат / Experimental group 1, meglumine acridonacetate (n =15) | Основная группа 2, ацикловир / Experimental group 2, acyclovir (n = 14) | Группа сравнения / Control group (n = 13) |
| n | % | n | % | n | % |
| Пол / Gender |
| М / Male | 9 | 60 | 8 | 57 | 6 | 46 |
| Ж / Female | 6 | 40 | 6 | 43 | 7 | 54 |
| Возраст, M±m / Age, M±m | | 6,0±0,6 | 6,5±0,7 | | |
|
| Этиология / Etiology |
| Моно-ВГЧ-6 / Mono-HHV-6 | 4 | 27 | 4 | 29 | 3 | 23 |
| Микст-герпесвирусные инфекции / Mixed herpesvirus infections | 11 | 73 | 10 | 71 | 10 | 77 |
| ВГЧ-6+ВЭБ / HHV-6+EBV | 2 | 13 | 2 | 14 | 2 | 15 |
| ВГЧ-6+ЦМВ / HHV-6+CMV | 1 | 7 | 1 | 7 | 1 | 8 |
| ВГЧ-6+ВПГ-1 / HHV-6+HSV-1 | 1 | 7 | 0 | 0 | 0 | 0
|
| ВГЧ-6+2,3 герпесвирусные инфекции / HHV-6+2,3 herpesvirus infections | 7 | 47 | 8 | 57 | 7 | 54 |
| Отягощенный преморбидный фон по аллергическим заболеваниям / Concomitant allergic diseases | 6 | 40 | 6 | 43 | 5 | 38 |
ВЭБ – вирус Эпштейна-Барр, ЦМВ – цитомегаловирус,
EBV – Epstein-Barr virus, CMV – cytomegalovirus.
Моно-инфекция ВГЧ-6А/В установлена у 11 (26%) детей, микст-инфекция с другими герпесвирусами в активной форме – у 16 (38%), в латентной форме – у 15 (36%). У детей были выявлены различные клинические варианты течения инфекции, вызванной ВГЧ-6А/В, в том числе у 18 детей – инфекционный мононуклеоз, у 20 детей – респираторная форма инфекции, у 2 – лимфаденит, у 2 – фебрильные судорожные приступы.
Все дети, госпитализированные с клиническими проявлениями ОРИ, получали симптоматическое лечение в зависимости от уровня поражения органов респираторного тракта. В случае развития аллергической реакции, или сохранения лихорадки и ухудшения общего состояния через 48 ч после начала антибактериальной терапии, или нарастания воспалительного синдрома по анализам крови решался вопрос о смене антибактериального препарата в соответствии с действующими рекомендациями.
Пациентам основных групп 1 и 2 была назначена этиотропная терапия. В соответствии с клиническими рекомендациях Российской Федерации по лечению детей с герпесвирусными инфекциями [25] мы использовали препарат меглумина акридонацетат (циклоферон) в таблетках (1 таб. – 150 мг) по схеме в соответствии с инструкцией фирмы производителя на 1,2, 4, 6, 8-й дни и препарат ацикловир в таблетках (1 таб. – 200 мг) по 200 мг 5 раз в день на 7 дней.
Для оценки клинической эффективности проводимых схем терапии анализировались средняя длительность основных симптомов заболевания (лихорадки, катаральных явлений в ротоглотке, гепатолиенального синдрома, нарушения носового дыхания), а также продолжительность пребывания в стационаре.
Статистическую обработку полученных данных проводили на основании принятых в доказательной медицине методов анализа. Для данных, распределенных по нормальному закону распределения, использовался критерий Стьюдента. Сравнение групп по качественному бинарному признаку (анализ частот) проводилось с помощью критерия χ². Различия между группами считали статистически достоверными при р <0,05, недостоверными – при р >0,05. Для проведения статистического анализа применялась операционная система Windows 10. Использовались современные пакеты статистического анализа: STATGRAPHICS plus, STATISTICA for Windows версии 8. Для оформления результатов исследований применялись пакеты из системы Microsoft Office.
Результаты исследования и их обсуждение
Среднее время до купирования симптомов представлено в табл. 2. Анализ полученных данных показал, что включение препарата меглумина акридонацетат в комплексную терапии пациентов с инфекцией ВГЧ-6А/В сокращает сроки пребывания в стационаре на 2,8 дня относительно группы сравнения (р >0,05, t-критерий Стьюдента). Показано достоверно более быстрое купирование таких симптомов заболевания, как лихорадка, катаральные явления в ротоглотке, нарушение носового дыхания и гепатолиенальный синдром (р <0,05, t-критерий Стьюдента).
Таблица 2. Средняя продолжительность госпитализации и симптомов заболевания, дни
Table 2. Mean duration of hospitalization and disease symptoms, days
| Средняя продолжительность, дни / Mean duration, days | Основная группа 1, меглумина акридонацетат / Experimental group 1, meglumine acridonacetate (n = 15) | Основная группа 2, ацикловир / Experimental group 2, acyclovir (n = 14) | Группа сравнения / Control group (n=13) |
| M | m | M | m | M | m |
| Длительность госпитализации / Length of in-hospital stay | 6,7 | 0,7 | 8,9 | 1,6 | 9,5 | 1,7 |
| Длительность лихорадки / Duration of fever | 4,6* | 0,5 | 6,7 | 0,8 | 7,5* | 1,3 |
| Длительность катаральных явлений в ротоглотке / Duration of catarrhal symptoms in the oropharynx | 5,2* | 0,5 | 6,9 | 1,5 | 8,2* | 1,3 |
| Нарушение носового дыхания / Nasal congestion | 4,9* | 0,7 | 7,0 | 0,7 | 7,9* | 0,9 |
| Уменьшение шейной лимфоаденопатии / Reduced cervical lymphadenopathy | 6,4 | 0,8 | 7,5 | 0,5 | 8,1 | 0,8 |
| Уменьшение гепатолиенального синдрома / Reduced hepatosplenic syndrome | 4,3* | 0,7 | 6,8 | 1,2 | 7,2* | 0,9 |
* достоверность показателей основной группы 1 по отношению к группе сравнения р <0,05 (t-критерий Стьюдента).
* significance of differences between the experimental group 1 and the control group p <0.05 (Studenfs t-test).
Ни по одному из анализируемых параметров не было получено достоверных различий между группой, получавшей ацикловир, и группой, не получавшей противовирусную терапию.
Оценка противовирусной активности проводимых схем терапии у обследованных пациентов проводилось на основании двукратного контрольного обследования пациентов: перед выпиской на 10±2 дня терапии, а также амбулаторно через 30±7 дней после начала противовирусной терапии. Исследование включало прямые методы диагностики для выявления ДНК и антигенов ВГЧ-6А/В в крови и материале мазка из ротоглотки. На основании комплексного обследования была установлена активность инфекции до начала терапии, после купирования основных клинических проявлений (10±2 дня) и через 30±7 дней после начала терапии.
Результаты оценки активности инфекции ВГЧ-6А/В на фоне терапии представлены на диаграмме (рис. 1).
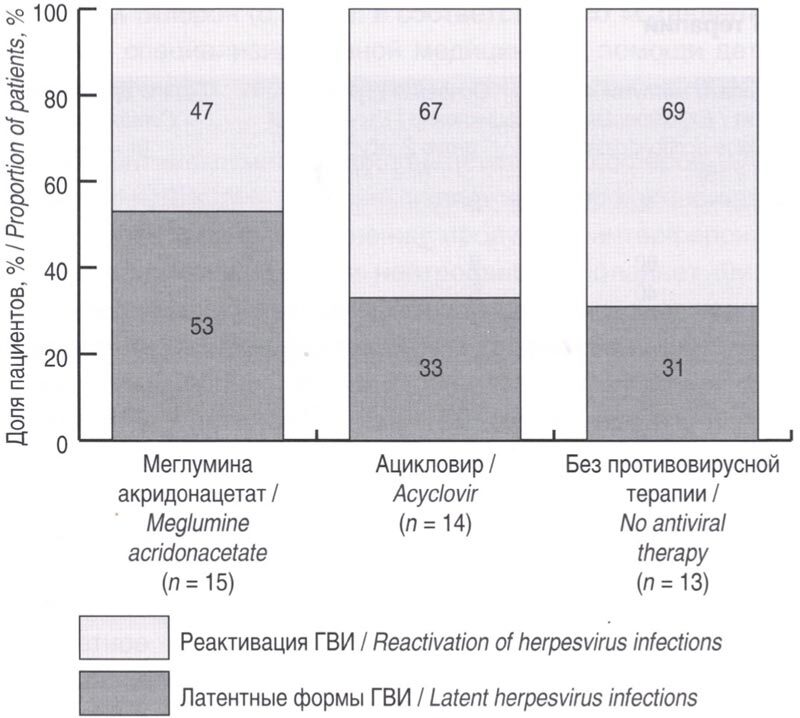 Рис. 1. Результаты обследования пациентов перед выпиской из стационара через 10±2 дня от начала терапии.
Рис. 1. Результаты обследования пациентов перед выпиской из стационара через 10±2 дня от начала терапии.
Fig. 1. Results of patient examination before discharge from the hospital; 10±2 days following treatment initiation.
Перед выпиской из стационара на 10±2 сутки терапии только у 17 из 42 обследованных пациентов не выделяли антигенов и/или ДНК ВГЧ-6 в крови и в мазках из ротоглотки (по 5 человек из основной группы 2 и группы сравнения и 8 пациентов в основной группе 1). В группе, получавшей меглумина акридонацетат, только у 1 ребенка были обнаружены поздние антигены ВГЧ-6 в крови, в группе, получавшей ацикловир, – у 3 детей, в группе сравнения – также у 3 детей. Наиболее частым маркером активности инфекции ВГЧ-6 перед выпиской из отделения было обнаружение ДНК и/или антигенов ВГЧ-6А/В в мазках из ротоглотки у 17 детей суммарно. Достоверных различий по выделению ДНК и/или антигенов ВГЧ-6А/В между группами получено не было.
После выписки из стационара пациенты основной группы 1 (n = 15) получали препарат меглумина акридонацетат по схеме до 23 дня, пациенты основной группы 2 (n = 14) получали ацикловир по 200 мг 2 раза в день 14 дней, пациенты из группы сравнения (n = 13) не получали противовирусной терапии. Дети были обследованы повторно через 1 месяц (30±7 дней) от начала лечения. Результаты представлены на диаграмме (рис. 2).
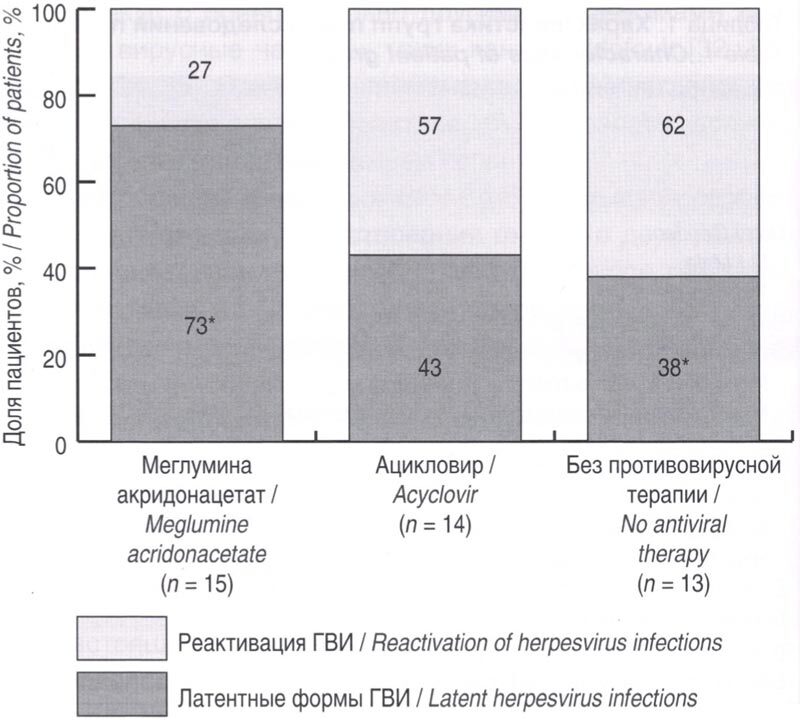 Рис. 2. Результаты обследования пациентов с инфекцией ВГЧ-6А/В через 30±7 дней от начала лечения в стационаре.
Рис. 2. Результаты обследования пациентов с инфекцией ВГЧ-6А/В через 30±7 дней от начала лечения в стационаре.
*р <0,05, критерий χ² с поправкой на правдоподобие.
Fig. 2. Results of examination of patients with HHV-6A/B infection 30±7 days following treatment initiation.
*p <0.05; likelihood ratio chi-square test.
У 11 детей на фоне терапии препаратом меглумина акридонацетат по схеме, согласно инструкции производителя, при повторном обследовании после окончания курса терапии не выявлены лабораторные признаки активной ВГЧ-6А/В-инфекции. В группе сравнения доля пациентов с неактивными формами инфекции составила не более 38%, что достоверно ниже по сравнению с основной группой (р <0,05, критерий χ² с поправкой на правдоподобие) (рис. 2). В группе детей, получавших ацикловир, только у 43% пациентов не было зафиксировано активности герпесвирусных инфекций, что было в 1,5 раза реже, чем в основной группе 1, и подобно изменениям, зафиксированным в группе сравнения.
По результатам исследования в возрастной группе пациентов от 4 лет и старше, госпитализированных в стационар с клиническими проявлениями ОРИ и активной инфекцией ВГЧ-6 было проведено рандомизированное исследование с целью сравнения эффективности препаратов ацикловир и меглумина акридонацетат в сравнении с детьми, не получавшими противовирусной терапии. В ходе анализа полученных данных показано, что клинический и вирусологический эффект ацикловира в группе пациентов с активной ВГЧ-6-инфекцией был подобен таковому в группе сравнения как перед выпиской, так и через 30±7 дней от начала терапии.
В работе были подтверждены данные предыдущих клинико-экспериментальных исследований (in vitro и клинических), демонстрирующих минимальный противовирусный эффект ацикловира в отношении инфекции ВГЧ-6. Ранее в работах Романцовой М.Г., Дриневского В.П. было показано выраженное и длительное снижение сывороточного уровня интерферона-альфа у детей с респираторными инфекциями протекающими на фоне обострения герпесвирусных инфекций [36, 37]. Полученные нами данные согласуются с результатами предыдущих исследований, показавших, что подключение препарата меглумина акридонацетат к терапии детей с активными формами микст-герпесвирусных инфекций и острыми проявлениями респираторного заболевания, в том числе инфекционного мононуклеоза [37-40], приводило к более быстрому купированию клинических проявлений заболевания и уменьшению активности герпесвирусных инфекций.
Заключение
Таким образом, при оценке эффективности различных провивовирусных препаратов при активной инфекции ВГЧ-6А/В у детей от 4 лет и старше наибольший противовирусный эффект был получен в группе с пролонгированной схемой терапии препаратом меглумина акридонацетат в таблетированной форме однократно в 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-й дни. В группе детей, получавших терапию препаратом ацикловир, доля пациентов, выделяющих антигены и/или ДНК ВГЧ-6А/В в крови и материале мазков из ротоглотки, не отличалась от аналогичного показателя в группе, не получавшей противовирусную терапию.
При активной инфекции ВГЧ-6А/В у детей старше 4 лет целесообразно включать в комплексную терапию препарат меглумина акридонацетат в таблетированной форме.
Информация о финансировании
Финансирование данной работы не проводилось.
Financial support
No financial support has been provided for this work.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests
The authors declare that there is no conflict of interest.
Литература
- Герпесвирусные инфекции человека. Руководство для врачей. Под ред. В.А.Исакова. СПб.: СпецЛит; 2013.
- Боковой АГ, Егоров АИ. Герпесвирусные инфекции у детей и родителей: учебное пособие для врачей педиатров, инфекционистов, иммунологов. Хабаровск: Полиграф-Партнер; 2016.
- Pantry SN, Medveczky PG. Latency, Integration, and Reactivation of Human Herpesvirus-6. Viruses. 2017;9(7):194-206.
- Agut H, Bonnafous P, Gautheret-Dejean A. Laboratory and clinical aspects of human herpesvirus 6 infections. Clin Microbiol Rev. 2015 Apr;28(2):313-35. DOI: 10.1128/CMR.00122-14
- Human Herpesviruses HHV-6A, HHV-6B, and HHV-7. Diagnosis and Clinical Management / Edited by Flamand L. Amsterdam: Elsevier; 2014.
- Prichard MN, Whitley RJ. The development of new therapies for human herpesvirus 6. Curr Opin Virol. 2014 Dec;9:148-53. DOI: 10.1016/j.coviro. 2014.09.019
- De Bolle L, Naesens L, De Clercq E. Update on human herpesvirus 6 biology, clinical features, and therapy. Clin Microbiol Rev. 2005 Jan;18(1 ):217-45. DOI: 10.1128/CMR. 18.1.217-245.2005
- Manichanh C, Olivier-Aubron C, Lagarde JP, Aubin JT, Bossi P, Gautheret-Dejean A, et al. Selection of the same mutation in the U69 protein kinase gene of human herpesvirus-6 after prolonged exposure to ganciclovir in vitro and in vivo. J Gen Virol. 2001 Nov;82(Pt 11):2767-2776. DOI: 10.1099/0022-1317-82-11-2767
- Bonnafous P, Naesens L, Petrella S, Gautheret-Dejean A, Boutolleau D, Sougakoff W, et al. Different mutations in the HHV-6 DNA polymerase gene accounting for resistance to foscarnet. Antivir Ther. 2007;12(6):877-88.
- Zerr DM, Fann JR, Breiger D, Boeckh M, Adler AL, Xie H, et al. HHV6 reactivation and its effect on delirium and cognitive functioning in hematopoietic cell transplantation recipients. В Blood. 2011 May 12;117(19):5243-9. DOI: 10.1182/ blood-2010-10-316083
- Dulery R, Salleron J, Dewilde A, Rossignol J, Boyle EM, Gay J, et al. Early human herpesvirus type 6 reactivation after allogeneic stem cell transplantation: a large-scale clinical study. Biol Blood Marrow Transplant. 2012 Jul;18(7):1080-9. DOI: 10.1016/j.bbmt.2011.12.579
- Tokimasa S, Нага J, Osugi Y, Ohta H, Matsuda Y, Fujisaki H, et al. Ganciclovir is effective for prophylaxis and treatment of human herpesvirus-6 in allogeneic stem cell transplantation. Bone Marrow Transplant. 2002 Apr;29(7):595-8.
- Ogata M, Phan TL, Fukuda T. Antiviral therapy for the treatment of HHV-6-associated syndromes after transplant. Am J Transplant. 2019 Jan;19(1 ):306-307. DOI: 10.1111/ajt.15069
- Gallois-Montbrun S, Schneider B, Chen Y, Giacomoni-Fernandes V, Mulard L, Morera S, et al. Improving nucleoside diphosphate kinase for antiviral nucleotide analogs activation. J Biol Chem. 2002 Oct 18;277(42):39953-9. DOI: 10.1074/jbc. M206360200
- Matthews T, Boehme R. Antiviral activity and mechanism of action of ganciclovir. Rev Infect Dis. 1988 Jul-Aug;10 Suppl 3:S490-4. DOI: 10.1093/clinids/10. supplement_3.s490
- Agut H, Bonnafous P, Gautheret-Dejean A. Update on infections with human herpesviruses 6A, 6B, and 7. Med Mai Infect. 2017 Mar;47(2):83-91. DOI: 10.1016/j. medmal.2016.09.004
- Perruccio K, Sisinni L, Perez-Martinez A, Valentin J, Capolsini I, Massei MS, et al. High Incidence of Early Human Herpesvirus-6 Infection in Children Undergoing Haploidentical Manipulated Stem Cell Transplantation for Hematologic Malignancies. Biol Blood Marrow Transplant. 2018 Dec;24(12):2549-2557. DOI: 10.1016/j. bbmt.2018.07.033
- Мюкке НА. Герпетическая инфекция 6-го типа у детей. Научный центр здоровья детей НИИ педиатрии. 2006; №25.
- Музыка АД. Диагностика, клинико-лабораторные особенности и лечение активных форм инфекции вируса герпеса человека 6-го типа у детей. Автореф. дисс.... канд. мед. наук. М., 2017.
- Пирогов НН. Эффективность противовирусной терапии при хроническом фаринготонзиллите на фоне персистирующей герпетической инфекции ротоглотки. Российская оториноларингология. 2018;1 (92):93-7.
- Щубелко РВ, Зуйкова ИН, Шульженко АЕ. Герпесвирусные инфекции человека: клинические особенности и возможности терапии. РМЖ. 2018; 26(8-1 ):39-45.
- Comar М, Grasso D, dal Molin G, Zocconi E, Campello C. HHV-6 infection of tonsils and adenoids in children with hypertrophy and upper airway recurrent infections. Int J Pediatr Otorhinolaryngol. 2010 Jan;74(1):47-9. DOI: 10.1016/j. ijporl.2009.10.008
- Вашура ЛВ, Савенкова MC. Герпес 6-го типа (эпидемиология, диагностика, клиника). Лечащий врач. 2014;11:18.
- Лекарственные препараты в России. Справочник. М.: АстраФармСервис; 2016.
- Об утверждении стандарта специализированной медицинской помощи детям при хронических герпесвирусных инфекциях: Приказ Министерства здравоохранения Российской Федерации от 9 ноября 2012 г. № 876н.
- Романцов МГ, Горячева ЛГ, Коваленко АЛ. Противовирусные и иммунотропные препараты в детской практике. Рук-во для врачей. СПб.: МедиКа; 2008.
- Романцов МГ, Шульдякова ОГ. «Многоцелевая монотерапия» циклофероном как средство экстренной профилактики ОРЗ. Информационное письмо для врачей. СПбГМА им. И.И.Мечникова, СГМУ; 2004.
- Дидковский НА, Наровлянский АН, Коваленко АЛ. Циклоферон в клинической практике. СПб., 2000.
- Фрейдлин ИС. Дефекты иммунной системы. СПб., 1998.
- Ершов ФИ, Киселев ОБ. Интерфероны и их индукторы (от молекулы до лекарства). М.: ГЭОТАР-Медиа; 2005.
- Киселев 0И, Ткаченко БИ, Ершов ФИ. Новые подходы к созданию функциональных индукторов. Фундаментальные направления молекулярной медицины. СПб., 2005.
- Bidanset DJ, Beadle JR, Wan WB, Hostetler KY, Kern ER. Oral activity of ether lipid ester prodrugs of cidofovir against experimental human cytomegalovirus infection. J Infect Dis. 2004 Aug 1;190(3):499-503. DOI: 10.1086/421912
- Marty FM, Winston DJ, Rowley SD, Vance E, Papanicolaou GA, Mullane KM, et al. CMX001 to prevent cytomegalovirus disease in hematopoietic-cell transplantation. N Engl J Med. 2013 Sep 26;369(13):1227-36. DOI: 10.1056/ NEJMoal 303688
- Naesens L, Bonnafous P, Agut H, De Clercq E. Antiviral activity of diverse classes of broad-acting agents and natural compounds in HHV-6-infected lymphoblasts. J Clin Virol. 2006 Dec;37 Suppl 1:S69-75. DOI: 10.1016/S1386-6532(06)70015-4
- De Bolle L, Andrei G, Snoeck R, Zhang Y, Van Lommel A, Otto M, et al. Potent, selective and cell-mediated inhibition of human herpesvirus 6 at an early stage of viral replication by the non-nucleoside compound CMV423. Biochem Pharmacol. 2004 Jan 15;67(2):325-36. DOI: 10.1016/j.bcp.2003.08.042
- Вершинина EH, Иванова BB, Говорова ЛВ. Терапевтическая коррекция иммунных расстройств при респираторных заболеваниях у детей с герпесвирусным инфицированием. Информационно-методическое письмо для врачей СПб., 2007.
- Романцов МГ, Ершов ФИ. Часто болеющие дети. Современная фармакотерапия. М.: ГЭОТАР-Медиа; 2009.
- Бортникова ЮЮ. Клинико-иммунологическое обоснование применения индуктора интерферона в комплексной терапии острой пневмонии у детей. Автореф. дисс. ... канд. мед. наук. М., 2015.
- Краснов ВВ, Кулова АА, Воробьева ВВ, Бушуев МГ, Обрядина АП, Астраханцева ИВ. Эффективность применения циклоферона у часто болеющих детей, имеющих маркеры активности герпесвирусных инфекций. Вестник Санкт-Петербургской государственной академии им. И.И.Мечникова. 2009; 1:148-53.
- Гордеец АВ, Савина ОГ, Бениова СН, Черникова АА. Этиология, иммунологические варианты инфекционного мононуклеоза и способ их коррекции. Экспериментальная и клиническая фармакология. 2011 ;74(11 ):29-32.
References
- Gerpesvirusnye infektsii cheloveka [Herpesvirus infections]. Edited by V.A.Isakov. St. Petersburg: "SpetsLit" Publ.; 2013. (In Russian).
- Bokovoi AG, Egorov Al. Gerpesvirusnye infektsii u detei i roditelei [Herpesviral infections in children and parents], Khabarovsk: "Poligraf-Partner" Publ.; 2016. (In Russian).
- Pantry SIM, Medveczky PG. Latency, Integration, and Reactivation of Human Herpesvirus-6. Viruses. 2017;9(7):194-206.
- Agut H, Bonnafous P, Gautheret-Dejean A. Laboratory and clinical aspects of human herpesvirus 6 infections. Clin Microbiol Rev. 2015 Apr;28(2):313-35. DOI: 10.1128/CMR.00122-14
- Human Herpesviruses HHV-6A, HHV-6B, and HHV-7. Diagnosis and Clinical Management / Edited by Flamand L. Amsterdam: Elsevier; 2014.
- Prichard MN, Whitley RJ. The development of new therapies for human herpesvirus 6. Curr Opin Virol. 2014 Dec;9:148-53. DOI: 10.1016/j.coviro.2014.09.019
- De Bolle L, Naesens L, De Clercq E. Update on human herpesvirus 6 biology, clinical features, and therapy. Clin Microbiol Rev. 2005 Jan;18(1 ):217-45. DOI: 10.1128/CMR.18.1.217-245.2005
- Manichanh C, Olivier-Aubron C, Lagarde JP, Aubin JT, Bossi P, Gautheret-Dejean A, et al. Selection of the same mutation in the U69 protein kinase gene of human herpesvirus-6 after prolonged exposure to ganciclovir in vitro and in vivo. J Gen Virol. 2001 Nov;82(Pt 11):2767-2776. DOI: 10.1099/0022-1317-82-11-2767
- Bonnafous P, Naesens L, Petreila S, Gautheret-Dejean A, Boutolleau D, Sougakoff W, et al. Different mutations in the HHV-6 DNA polymerase gene accounting for resistance to foscarnet. Antivir Ther. 2007;12(6):877-88.
- Zerr DM, Fann JR, Breiger D, Boeckh M, Adler AL, Xie H, et al. HHV6 reactivation and its effect on delirium and cognitive functioning in hematopoietic cell transplantation recipients. В Blood. 2011 May 12;117(19):5243-9. DOI: 10.1182/blood-2010-10-316083
- Dulery R, Salleron J, Dewilde A, Rossignol J, Boyle EM, Gay J, et al. Early human herpesvirus type 6 reactivation after allogeneic stem cell transplantation: a large-scale clinical study. Biol Blood Marrow Transplant. 2012 Jul;18(7):1080-9. DOI: 10.1016/j.bbmt.2011.12.579
- Tokimasa S, Нага J, Osugi Y, Ohta H, Matsuda Y, Fujisaki H, et al. Ganciclovir is effective for prophylaxis and treatment of human herpesvirus-6 in allogeneic stem cell transplantation. Bone Marrow Transplant. 2002 Apr;29(7):595-8.
- Ogata M, Phan TL, Fukuda T. Antiviral therapy for the treatment of HHV-6-associated syndromes after transplant. Am J Transplant. 2019 Jan;19(1 ):306-307. DOI: 10.1111/ajt.15069
- Gallois-Montbrun S, Schneider B, Chen Y, Giacomoni-Fernandes V, Mulard L, Morera S, et al. Improving nucleoside diphosphate kinase for antiviral nucleotide analogs activation. J Biol Chem. 2002 Oct 18;277(42):39953-9. DOI: 10.1074/jbc. M206360200
- Matthews T, Boehme R. Antiviral activity and mechanism of action of ganciclovir. Rev Infect Dis. 1988 Jul-Aug;10 Suppl 3:S490-4. DOI: 10.1093/clinids/10. supplement_3.s490
- Agut H, Bonnafous P, Gautheret-Dejean A. Update on infections with human herpesviruses 6A, 6B, and 7. Med Mai Infect. 2017 Mar;47(2):83-91. DOI: 10.1016/j. medmal.2016.09.004
- Perruccio K, Sisinni L, Perez-Martinez A, Valentin J, Capolsini I, Massei MS, et al. High Incidence of Early Human Herpesvirus-6 Infection in Children Undergoing Haploidentical Manipulated Stem Cell Transplantation for Hematologic Malignancies. Biol Blood Marrow Transplant. 2018 Dec;24(12):2549-2557. DOI: 10.1016/j. bbmt.2018.07.033
- Myukke NA. Herpetic infection of type 6 in children. National Medical Research Center for Children's Health. 2006; №25. (In Russian).
- Muzyka AD. Diagnostika, kliniko-laboratornye osobennosti i lechenie aktivnykh form infektsii virusa gerpesa cheloveka 6-go tipa u detei. Diss. Moscow, 2017. (In Russian).
- Pirogov NN. The efficacy of antiviral therapy in chronic pharyngotonsillitis associated with persistent herpes infection of the oropharynx. Russian Otorhinolaryngology. 2018;1 (92):93-7. (In Russian).
- Shubelko RV, Zuykova IN, Shulzhenko AE. Human herpesviruses infections: clinical features and opportunities of therapy. RMJ. 2018;26(8-1 ):39-45. (In Russian).
- Comar M, Grasso D, dal Molin G, Zocconi E, Campello C. HHV-6 infection of tonsils and adenoids in children with hypertrophy and upper airway recurrent infections. Int J Pediatr Otorhinolaryngol. 2010 Jan;74(1):47-9. DOI: 10.1016/j. ijporl.2009.10.008
- Vashura LV, Savenkova MS. Gerpes 6-go tipa (epidemiologiya, diagnostika, klinika). Lechashchii vrach. 2014;11:18. (In Russian).
- LekarstvernyepreparatyvRossii [Medicines in Russia]. Moscow: "AstraFarmServis" Publ.: 2016. (In Russian).
- Order of the Ministry of health of the Russian Federation No. 876n of November 9, 2012 «Approval of the standard of specialized medical care for children with chronic herpesvirus infections». (In Russian).
- Romantsov MG, Goryacheva LG, Kovalenko AL. Protivovirusnye i immunotropnye preparaty v detskoi praktike [Antiviral and immunotropic drugs in children s practice], St. Petersburg: "MediKa" Publ.; 2008. (In Russian).
- Romantsov MG, ShuEdyakova OG. Multi-purpose monotherapy with cyclopherone as a means of emergency prevention of acute respiratory infections. Information Sheet. SGMU; 2004. (In Russian).
- Didkovskii NA, Narovlyanskii AN, Kovalenko AL. Tsikloferon v klinicheskoi praktike [Cycloferon in clinical practice], St. Petersburg, 2000. (In Russian).
- Freidlin IS. Defekty immunnoi sistemy [Defects of the immune system], St. Petersburg, 1998. (In Russian).
- Ershov FI, Kiselev OV. Interferony i ikh induktory (ot molekuly do lekarstva) [Interferons and their inducers], Moscow: "GEOTAR-Media" Publ.; 2005. (In Russian).
- Kiselev Ol, Tkachenko Bl, Ershov FI. Novye podkhody k sozdaniyu funktsional'nykh induktorov. Fundamentalnye napravleniya molekulyarnoi meditsiny [New approaches to functional inducers. Fundamental directions of molecular medicine], St. Petersburg, 2005. (In Russian).
- Bidanset DJ, Beadle JR, Wan WB, Hostetler KY, Kern ER. Oral activity of ether lipid ester prodrugs of cidofovir against experimental human cytomegalovirus infection. J Infect Dis. 2004 Aug 1;190(3):499-503. DOI: 10.1086/421912
- Marty FM, Winston DJ, Rowley SD, Vance E, Papanicolaou GA, Mullane KM, et al. CMX001 to prevent cytomegalovirus disease in hematopoietic-cell transplantation. N Engl J Med. 2013 Sep 26;369(13):1227-36. DOI: 10.1056/NEJMoa1303688
- Naesens L, Bonnafous P, Agut H, De Clercq E. Antiviral activity of diverse classes of broad-acting agents and natural compounds in HHV-6-infected lymphoblasts. J Clin Virol. 2006 Dec;37 Suppl 1:S69-75. DOI: 10.1016/S1386-6532(06)70015 4
- De Bolle L, Andrei G, Snoeck R, Zhang Y, Van Lommel A, Otto M, et al. Potent, selective and cell-mediated inhibition of human herpesvirus 6 at an early stage of viral replication by the non-nucleoside compound CMV423. Biochem Pharmacol. 2004 Jan 15;67(2):325-36. DOI: 10.1016/j.bcp.2003.08.042
- Vershinina EN, Ivanova VV, Govorova LV. Therapeutic correction of immune disorders in respiratory diseases in children with herpesvirus infection. Information Sheet. St. Petersburg, 2007. (In Russian).
- Romantsov MG, Ershov FI. Chasto boleyushchie deti. Sovremennaya farmakoterapiya [Current pharmacotherapy], Moscow: “GEOTAR-Media" Publ.; 2009. (In Russian).
- Bortnikova YuYu. Kliniko-immunologicheskoe obosnovanie primeneniya induktora interferona v kompleksnoi terapii ostroi pnevmonii u detei. Diss. Moscow, 2015. (In Russian).
- Krasnov VV, Kulova AA, Vorobyeva VV, Bushuev MG, Obryadina AP, Astrakhantseva IV. Efficiency of cycloferon use in frequently ill children having markers of herpetic infections activity in the closed child care centers. Vestnik Sankt-Peterburgskoi gosudarstvennoi akademii im. I.I.Mechnikova. 2009;1:148-53. (In Russian).
- Gordeets AV, Savina OG, Beniova SN, Chernikova AA. Infectious Mononucleosis: Etiology, Immunological Variants, Methods of Correction. Russian Journal of Experimental and Clinical Pharmacology. 2011 ;74(11 ):29-32. (In Russian).
Информация о соавторах:
Музыка Анна Драгиевна, кандидат медицинских наук, научный сотрудник клинического отдела инфекционной патологии Центрального НИИ эпидемиологии Роспотребнадзора
Адрес: 111123, Москва, ул. Новогиреевская, За
Понежева Жанна Бетовна, доктор медицинских наук, руководитель клинического отдела инфекционной патологии Центрального НИИ эпидемиологии Роспотребнадзора
Адрес: 111123, Москва, ул. Новогиреевская, За
Information about co-authors:
Anna D. Muzyka, MD, PhD, researcher, clinical department of infectious diseases, Central Research Institute of Epidemiology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being
Address: 3a Novogireevskaya str., Moscow, 111123, Russian Federation
Zhanna B. Ponezheva, MD, PhD, DSc, head, clinical department of infectious diseases, Central Research Institute of Epidemiology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being
Address: 3a Novogireevskaya str., Moscow, 111123, Russian Federation
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)



 Рис. 1. Результаты обследования пациентов перед выпиской из стационара через 10±2 дня от начала терапии.
Рис. 1. Результаты обследования пациентов перед выпиской из стационара через 10±2 дня от начала терапии.  Рис. 2. Результаты обследования пациентов с инфекцией ВГЧ-6А/В через 30±7 дней от начала лечения в стационаре.
Рис. 2. Результаты обследования пациентов с инфекцией ВГЧ-6А/В через 30±7 дней от начала лечения в стационаре.
