Влияние Мексидола на качество жизни и функциональный статус пациентов с хронической ишемией головного мозга и хронической сердечной недостаточностью с низкой фракцией выброса
СтатьиВ.В. Толкачева1, Э.Р. Казахмедов1, Ж.Д. Кобалава1, С.А Галочкин1, А.В. Щулькин2
1ФГАОУ ВО «Российский университет дружбы народов», Москва, Россия;
2ФГБОУ ВО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Рязань, Россия
Резюме
Цель исследования. Изучить влияние Мексидола на функциональное состояние миокарда, уровень мозгового натрийуретического пептида (NT-proBNP), переносимость физической нагрузки, качество жизни, выраженность окислительного стресса, воспалительной реакции и эндотелиальной дисфункции у пациентов с хронической ишемией головного мозга (ХИМ) и хронической сердечной недостаточностью (ХСН) II—III функционального класса (ФК) по классификации NYHA при последовательном внутривенном и пероральном введении препарата Мексидол в течение 13 нед на фоне стандартной базисной терапии.
Материал и методы. В исследование были включены 44 пациента с ХИМ и ХСН II—III ФК по NYHA. Средний возраст составил 65,5±11,8 года (75% мужчин); 21 пациент был в группе базисной терапии ХСН с дополнительным назначением Мексидола, 23 пациента — в группе базисной терапии. Исходно, на 7-й день и на 13-й неделе проводилась оценка эхокардиографических показателей, уровня NT-proBNP, переносимости физической нагрузки (тест с 6-минутной ходьбой, Т6МХ), оценка клинического состояния пациента по шкале ШОКС (модификация В.Ю. Мареева), параметров окислительного стресса (уровень малонового диальдегида (МДА) и активность супероксиддисмутазы (СОД)), воспалительной реакции (уровень С-реактивного белка (СРБ), фактора некроза опухоли (ФНО-а)), а также содержания гомоцистеина и уровня циста-тина С. Исходно и в конце исследования оценивали качество жизни по результатам Миннесотского опросника качества жизни больных ХСН (Minnesota Living With Heart Failure Questionnaire, MLHFQ) и Канзасского опросника больных кардиомиопатией (Kansas City Cardiomyopathy Questionnaire, KCCQ).
Результаты. У пациентов в группе «Мексидол+базисная терапия» выявлены более выраженное улучшение показателей качества жизни, более высокий прирост по результатам Т6МХ, более выраженное улучшение клинического состояния по шкале ШОКС, достоверное снижение показателей конечно-диастолического и конечно-систолического размеров ЛЖ, а также достоверно более выраженное снижение уровня NT-proBNP на 7-й день и через 13 нед терапии по сравнению с группой базисной терапии. Применение Мексидола в дополнение к базисной терапии приводило к снижению концентрации МДА и повышению активности СОД на 7-е сутки и через 13 нед наблюдения. Выявлено достоверное уменьшение уровня СРБ и ФНО-а как на 7-е сутки, так и через 1 3 нед наблюдения на фоне дополнительного применения Мексидола. Выявлено замедление нарастания гомоцистеина в группе терапии Мексидолом. Достоверных различий по показателям цистатина С между группами не выявлено.
Вывод. Мексидол при добавлении к базисной терапии пациентов с ХИМ и ХСН II—III ФК оказывает благоприятное влияние на качество жизни, функциональный статус, улучшает клиническое состояние, показатели внутрисердечной гемодинамики, обладает достоверной антиоксидантной активностью, снижает выраженность воспалительной реакции, замедляет нарастание уровня гомоцистеина, не оказывает влияния на функцию почек (цистатин С).
Ключевые слова: хроническая ишемия мозга, сердечная недостаточность, качество жизни, когнитивный статус, этилметил-гидроксипиридина сукцинат, Мексидол, окислительный стресс, воспаление, эндотелиальная дисфункция.
Информация об авторах:
Толкачева В.В. — orcid.org/0000-0001-6847-8797
Казахмедов Э.Р. — orcid.org/0000-0002-6274-8933
Кобалава Ж.Д. — orcid.org/0000-0002-5873-1768
Галочкин С.А. — orcid.org/0000-0001-7370-8606
Щулькин А.В. — orcid.org/0000-0003-1688-0017
Автор, ответственный за переписку: Толкачева В.В. — e-mail: tolkachevav@mail.ru
Как цитировать: Толкачева В.В., Казахмедов Э.Р., Кобалава Ж.Д., Галочкин С.А, Щулькин А.В. Влияние Мексидола на качество жизни и функциональный статус пациентов с хронической ишемией головного мозга и хронической сердечной недостаточностью с низкой фракцией выброса. Кардиология и сердечно-сосудистая хирургия. 2021;14(1):80-89. doi.org/10.17116/kardio20211401180
Введение
Хроническая сердечная недостаточность (ХСН) — одна из основных причин госпитализаций пациентов старше 65 лет, которая характеризуется крайне неблагоприятным прогнозом. Ежегодная смертность от ХСН неуклонно растет [1—3].
Когнитивные нарушения как дополнительный фактор снижения всех видов активности пациентов (физической, психической, социальной) широко встречаются у больных с ХСН как с низкой, так и с сохранной фракцией выброса левого желудочка (ЛЖ). Частота когнитивных нарушений у лиц с ХСН выше, чем без нее. Формирование когнитивной дисфункции у лиц с сердечно-сосудистыми заболеваниями обусловлено наличием хронической ишемии головного мозга (ХИМ), а также целым рядом нейрохимических процессов, протекающих в головном мозге, которые формируют порочный круг. Причем достаточно часто признаки ишемии мозга из-за снижения ударного объема крови наблюдаются значимо ранее, чем проявления застоя в других органах и тканях. ХИМ вследствие нарушения церебральной гемодинамики обусловлена как экстра-церебральными, так и интрацеребральными факторами, что способствует усугублению проявлений хронической гипоксии головного мозга и, как следствие, когнитивной дисфункции. В качестве возможных предикторов когнитивных нарушений у лиц с ХСН рассматриваются пожилой возраст, индекс массы тела, фракция выброса левого желудочка, дистанция 6-минутной ходьбы (Т6МХ), уровень BNP, анемия, тяжелая хроническая болезнь почек, систолическое АД (САД) <130 мм рт.ст. Показано, что депрессия как одно из клинических проявлений когнитивных нарушений связана с повышением частоты желудочковых аритмий, увеличением риска как внезапной остановки сердца, так и летальности [4]. В основе ХСН и депрессии лежат общие патофизиологические механизмы, такие как активация симпатической нервной системы, гиперкоагуляция, увеличение выработки провоспалительных цитокинов, включая интерлейкины и фактор некроза опухоли (ФНО-а).
К числу основных задач в лечении ХСН относится улучшение качества жизни пациента с одновременным предупреждением или замедлением когнитивных нарушений. Приверженность пациентов к терапии является ключевой составляющей эффективного лечения. В исследовании CHARM показано, что у пациентов с высокой приверженностью к терапии продолжительность и качество жизни значимо превышали данные показатели у пациентов с низкой приверженностью к лечению. Самой частой причиной нарушения режима лечения пациентами с ХСН является забывчивость. При этом 40% больных отмечают, что не следуют назначенным схемам терапии вследствие ухудшения памяти [5]. С другой стороны, важно отметить, что благоприятное влияние на качество жизни и улучшение общего самочувствия на фоне получаемой терапии побуждают пациентов продолжать лечение.
Качество жизни — это способность индивидуума функционировать в обществе соответственно своему положению и получать удовлетворение от жизни. Понятие «качество жизни» является многофакторным, т.е. включает в себя множество компонентов. В связи с этим наряду с другими (экономическими, психосоциальными, технологическими и т.д.) были выделены и медицинские аспекты качества жизни. Под медицинскими аспектами качества жизни следует понимать влияние самого заболевания (его симптомов и признаков), ограничение физической активности, которое наступает на этом фоне, а также влияние терапии на каждодневную активность пациента.
Взаимосвязь между качеством жизни и показателями приверженности к лечению подтверждена в многочисленных исследованиях [6—9]. Применяются специальные опросники, позволяющие оценить исходное состояние и динамику разных аспектов качества жизни на фоне лечения. Наиболее часто применяются Миннесотский опросник качества жизни больных ХСН (Minnesota Living With Heart Failure Questionnaire, MLHFQ) и Канзасский опросник больных кардиомиопатией (Kansas City Cardiomyopathy Questionnaire, KCCQ).
К числу наиболее уязвимых аспектов качества жизни, помимо физической составляющей, относятся снижение жизненной активности, ограничение социальных контактов, обусловленное ухудшением эмоционального состояния, что ведет к ухудшению клинического состояния.
Улучшение качества жизни является одной из ключевых задач терапии пациентов с ХСН и низкой ФВ, которая широко обсуждается в литературе [11, 12] и получила отражение в современных рекомендациях [13]. Ряд препаратов, которые оказывают благоприятный эффект на конечные точки (смертность и частота госпитализаций), например бета-блокаторы и ингибиторы ангио-тензинпревращающего фермента, не оказывают влияния на симптомы, функциональный статус и качество жизни пациентов [10].
Учитывая множество этиологических факторов и патогенетических механизмов прогрессирования ХСН, в последнее время в литературе описаны отдельные «фенотипы» ХСН, которые были выделены на основании результатов клинико-лабораторных и инструментальных исследований [14]. Поэтому можно предположить, что подход, основанный на отдельных фенотипах ХСН, является достаточно перспективным и не только поможет оценить патогенетические варианты воздействия на определенные механизмы заболевания, но и улучшит тактику ведения пациента [15, 16].
Мексидол (этилметилгидроксипиридина сукцинат) — оригинальный препарат с доказанной антиоксидантной и антигипоксантной активностью, более 20 лет успешно применяется в реальной клинической практике для терапии острого и хронического нарушения мозгового кровообращения, тревожных расстройств, черепно-мозговой травмы, астенических состояний [17]. В ряде исследований показано благоприятное действие Мексидола в комплексной терапии пациентов с сердечно-сосудистыми заболеваниями, в частности у больных с ХСН [18].
Цель данного исследования — оценка влияния Мексидола на гемодинамику, функциональное состояние миокарда, уровень NT-proBNP, переносимость физической нагрузки, качество жизни, выраженность окислительного стресса, воспалительной реакции и эндотелиальной дисфункции у пациентов с ХИМ и ХСН II—III функциональных классов (ФК) по классификации NYHA при последовательном внутривенном и пероральном введении препарата Мексидол в течение 13 нед на фоне стандартной базисной терапии.
Материал и методы
В рандомизированное исследование в параллельных группах были включены пациенты с ХИМ и ХСН II— III ФК по классификации NYHA, которые соответствовали критериям включения и находились в стационаре. Пациенты были рандомизированы в одну из двух групп лечения: 1) базисная терапия ХСН+Мексидол; 2) базисная терапия ХСН.
Основными критериями включения являлись возраст >18 лет, диагноз ХИМ, дисциркуляторной энцефалопатии, ХСН II—III ФК по NYHA, установленный не менее чем за 3 мес до скрининга при наличии клинических симптомов декомпенсации, несмотря на использование стандартной терапии ХСН в течение 4 нед в стабильных дозах, ухудшение клинических симптомов менее чем за 1 мес до скрининга, ФВ ЛЖ <50% по данным эхокардиографии и САД >100 мм рт.ст. на визите скрининга.
Критериями исключения были 20 кг/м2 > индекс массы тела (ИМТ) >40 кг/м2, САД <100 мм рт.ст., неконтролируемая гипертензия с САД >180 мм рт.ст. и/или диастолическим АД (ДАД) >100 мм рт.ст., одышка некардиогенного генеза, вызванная острыми или хроническими заболеваниями дыхательной системы (хроническая обструктивная болезнь легких и бронхиальная астма, бронхит, пневмония), которые могут затруднять объяснение первичной причины одышки, клинические признаки острого коронарного синдрома в настоящий момент времени или в течение 30 сут до скрининга, ХСН, связанная с клинически значимыми аритмиями (стойкая желудочковая тахикардия, брадикардия со стойким снижением частоты сокращений желудочков <45 уд/мин, фибрилляция/трепетание предсердий со стойким ответом со стороны желудочков >130 уд/мин), тяжелое нарушение функции почек (eGFR <30 мл/мин/1,73 м2), нарушение функции печени (активность трансаминаз в >2 раза выше верхней границы нормы), индивидуальная чувствительность к этилметилгидроксипиридину, наличие в анамнезе алкогольной или наркотической зависимости в течение 6 мес до скрининга, беременность, лактация, прием препаратов этилметилгидроксипиридина сукцината, триметазидина или мельдония в течение 2 мес до начала исследования.
Исследуемый препарат (Мексидол) применялся в виде последовательной терапии 2 лекарственными формами: 1000 мг (Мексидол, раствор для внутривенного и внутримышечного введения, 50 мг/мл (ООО «НПК «ФАРМА-СОФТ», Россия) 1 раз в сутки внутривенно капельно в 50 мл 0,9% раствора NaCl в течение 7 дней, а затем Мек-сидол ФОРТЕ 250 (таблетки, покрытые пленочной оболочкой, 250 мг (ООО «НПК «ФАРМАСОФТ», Россия)) внутрь по 1 табл 3 раза в сутки в течение 12 нед.
Таблица 1. Характеристика базисной терапии пациентов
Table 1. Characteristics of basic therapy
|
Препарат |
Исходно |
7 сут |
13 нед |
|
иАПФ/АРА, n (%) |
44 (100) |
44 (100) |
22 (76,5) |
|
АРНИ, n (%) |
0 |
0 |
8 (23,5) |
|
АМКР, n (%) |
31 (70,5) |
31 (70,5) |
34 (100) |
|
БАБ, n (%) |
44 (100) |
44 (100) |
34 (100) |
|
Дигоксин, n (%) |
23 (52,3) |
19 (43,2) |
9 (26,4) |
|
Петлевые диуретики, n (%) |
44 (100) |
44 (100) |
34 (100) |
Примечание. АРА — антагонисты рецепторов ангиотензина, АРНИ — ингибиторы ангиотензиновых рецепторов и неприлизина, АМКР — антагонисты минералокортикоидных рецепторов, БАБ — бета-адреноблокаторы.
Таблица 2. Клинико-демографические параметры пациентов
Table 2. Clinical and demographic characteristics of patients
|
Параметр |
Общая группа (n=44) |
Базисная терапия ХСН (n=23) |
Базисная терапия ХСН+Мексидол (n=21) |
p-критерий |
|
Мужчины/женщины, n (%) |
33 (75)/11 (25) |
19 (82,6)/4 (17,4) |
14 (66,7)/7 (33,3) |
0,3/0,3 |
|
Возраст, годы |
66,0±8,1 |
66,3±6,7 |
65,6±9,5 |
0,76 |
|
ИМТ, кг/м2 |
31,1±6,1 |
30,5±5,2 |
31,7±6,9 |
0,52 |
|
ИБС, n (%) |
33 (75) |
18 (78,3) |
15 (71,4) |
0,73 |
|
Инфаркт миокарда, n (%) |
25 (57) |
14 (60,9) |
11 (52,4) |
0,76 |
|
Гипертоническая болезнь, n (%) |
40 (91) |
21 (90,3) |
19 (90,5) |
1 |
|
Фибрилляция/трепетание предсердий, n (%) |
26 (59) |
15 (65,2) |
11 (52,4) |
0,54 |
|
Сахарный диабет, n (%) |
14 (32) |
7 (30,4) |
7 (33,3) |
1 |
|
Перенесенный инфаркт головного мозга, n (%) |
6 (14) |
3 (13) |
3 (14,3) |
1 |
|
Госпитализации с декомпенсацией ХСН за 6 мес, n (%) |
18 (40,1) |
10 (43,5) |
8 (38,1) |
0,77 |
Все диагностические процедуры проводили на основании письменного информированного согласия пациентов. Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования был одобрен этическим комитетом клинического центра.
Клинико-демографическая характеристика групп
В исследование были включены 44 пациента, рандомизированные в 2 группы. Первая группа (n=21) получала Мексидол в виде последовательной терапии: 1000 мг (Мек-сидол, раствор для внутривенного и внутримышечного введения, 50 мг/мл (ООО «НПК «ФАРМАСОФТ», Россия)) 1 раз в сутки внутривенно капельно в 50 мл 0,9% раствора NaCl в течение 7 сут, а затем Мексидол ФОРТЕ 250 (таблетки, покрытые пленочной оболочкой, 250 мг (ООО «НПК «ФАРМАСОФТ», Россия)) внутрь по 1 табл 3 раза в сутки в течение 12 нед. Вторая группа (n=23) получала стандартную базисную терапию (табл. 1).
Клинико-демографические параметры пациентов представлены в табл. 2.
Не было выявлено достоверных различий между группами при анализе клинико-демографических параметров.
В данном исследовании проводилась оценка клинических и лабораторных критериев эффективности. Клиническим критерием эффективности являлось влияние препарата на качество жизни, функциональный статус (переносимость физической нагрузки (Т6МХ) и динамика клинического состояния больного по шкале ШОКС в модификации В.Ю. Мареева) (суммарный балл всех вопросов), а также эхокардиографические показатели, измеренные при трансторакальной эхокардиографии по стандартному протоколу. В качестве лабораторных критериев эффективности анализировали влияние Мексидола на уровень NT-proBNP, выраженность окислительного стресса, воспалительной реакции, содержание гомоцистеина и ци-статина С. Полученные результаты описаны ранее [19].
Исходно, на 7-е сут и через 13 нед изучали переносимость физической нагрузки на основании Т6МХ, диаметр корня аорты, конечно-диастолический размер правого желудочка, толщину межжелудочковой перегородки, толщину задней стенки ЛЖ, фракцию выброса ЛЖ, конечно-диастолический и конечно-систолический размеры ЛЖ, относительную толщину стенок ЛЖ, систолическое давление в легочной артерии (СДЛА), уровень N-концевого пропеп-тида мозгового натрийуретического гормона (NT-proBNP). Анализировали также влияние Мексидола на концентрацию малонового диальдегида (МДА), активность суперок-сиддисмутазы (СОД), уровень С-реактивного белка (СРБ), ФНО-а, содержание гомоцистеина и цистатина С.
Биологические образцы для анализа были заслеплены.
Исходно и в конце исследования оценивали качество жизни по результатам Миннесотского опросника качества жизни больных с ХСН (Minnesota Living With Heart Failure Questionnaire, MLHFQ) и Канзасского опросника больных кардиомиопатией (Kansas City Cardiomyopathy Questionnaire, KCCQ).
Для Миннесотского вопросника качества жизни вычислялась общая сумма баллов всех вопросов. Канзасский опросник качества жизни представлен 8 шкалами: физические ограничения — сумма баллов по вопросу 1; симптомы — сумма баллов по вопросам 3—9; стабильность симптоматики — сумма баллов по вопросу 2; социальные ограничения — сумма баллов по вопросу 15; способность к самопомощи — сумма баллов по вопросам 10—11; качество жизни — сумма баллов по вопросам 12—14; функциональный статус — сумма баллов по вопросам 1—9; клиническое состояние — сумма баллов по вопросам 10—14. Клинически значимыми изменениями считали прирост >5 баллов по опроснику KCCQ в сравнении с исходным значением.
Распределение данных оценивали по критерию Колмогорова—Смирнова. При нормальном распределении статистическую значимость различий анализировали с помощью t -критерия Стьюдента для связанных и несвязанных выборок. При ненормальном распределении достоверность различий определяли с помощью критерия Манна—Уитни или критерия Вилкоксона для несвязанных и связанных выборок соответственно. В случае необходимости использовали поправку Бонферрони. Статистически значимыми считались различия при p<0,05.
Результаты
Влияние Мексидола на уровень NT-proBNP (маркер сердечной недостаточности)
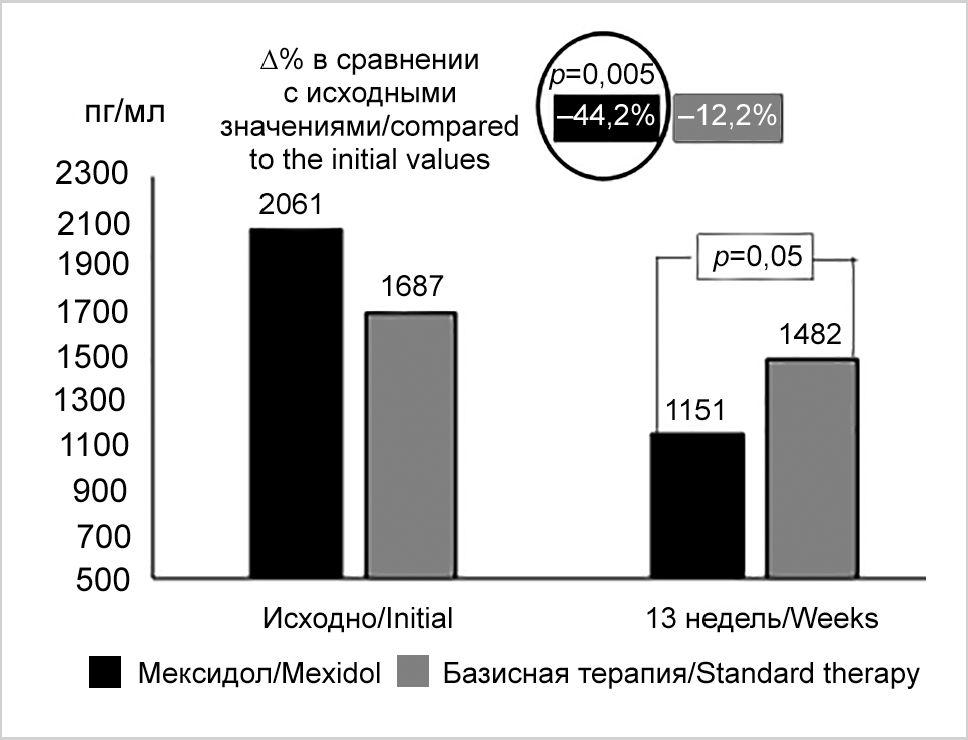
У пациентов с ХИМ и ХСН, получавших Мексидол дополнительно к базисной терапии, содержание NT-proBNP в плазме крови уменьшилось на 7-е сутки лечения на 29,2% (с 2061,9 до 1460,0 пг/мл, p=0,002), а к 13-й неделе — на 44,2% (с 2061,9 до 1151,5 пг/мл, p=0,005) по сравнению с исходными показателями. В группе базисной терапии концентрация NT-proBNP снижалась на 7-е сутки лечения на 32,5% (с 1687,0 до 1138,0 пг/мл, p=0,007), а на 13-й неделе достоверно не отличалась от исходных показателей (рис. 1).
При оценке динамики NT-proBNP к 13-й неделе терапии было показано более выраженное снижение данного показателя в группе «Мексидол+базисная терапия» по сравнению с группой базисной терапии (44,2% против 12,2%, p=0,05) (табл. 6), при этом различия между группами были достоверны.
Влияние Мексидола на концентрацию МДА и активность СОД
Мексидол в дополнение к базисной терапии снижал концентрацию МДА в плазме крови на 7-й день на 27,2% (p=0,02), а через 13 нед — на 31,1% (p=0,023) по сравнению с исходными показателями. В группе базисной терапии уровень МДА значимо не изменялся во все сроки терапии. При анализе показателей пациентов, получавших Мекси-ол в дополнение к базисной терапии и только базисную терапию, выявлено, что содержание МДА в группе Мекси-дола была ниже показателей группы базисной терапии на 24,2% (p=0,05) к 13-й неделе лечения.
Рис. 1. Влияние Мексидола на концентрацию NT-proBNP у пациентов с ХИМ и ХСН (медиана, верхний и нижний квартили).
Fig. 1. Effect of Mexidol on NT-proBNP concentration in patients with chronic brain ischemia and CHF (median, upper and lower quartiles).
 При сравнении изменений концентрации МДА в обеих группах на 7-й день лечения выявлено более выраженное снижение МДА в группе Мексидола (p=0,054), которое к 13-й неделе продолжало уменьшаться, а в группе базисной терапии данный показатель к 13-й неделе повысился. Различия между группами были статистически достоверны (p=0,036) (табл. 3, 6).
При сравнении изменений концентрации МДА в обеих группах на 7-й день лечения выявлено более выраженное снижение МДА в группе Мексидола (p=0,054), которое к 13-й неделе продолжало уменьшаться, а в группе базисной терапии данный показатель к 13-й неделе повысился. Различия между группами были статистически достоверны (p=0,036) (табл. 3, 6).
При оценке показателей двух групп активность СОД на 7-й день и через 13 нед при применении Мексидола была выше на 23,3% (p=0,011) и 17,1% (p=0,057) соответственно (табл. 3).
Таким образом, добавление Мексидола к базисной терапии пациентов с ХИМ и ХСН снижает выраженность окислительного стресса.
Влияние Мексидола на концентрацию СРБ и ФНО-а
У пациентов с ХИМ и ХСН в группе Мексидола уровень СРБ снижался на 7-й день на 40,9% (p=0,057), а через 13 нед на 74,7% (p=0,001) по сравнению с исходными значениями. В то же время в группе базисной терапии концентрация СРБ достоверно не изменялась во время исследования. Через 13 нед применения Мексидола уровень СРБ был ниже показателей группы базисной терапии на 71,4% (p=0,009) (табл. 4, 6).
Таблица 3. Влияние Мексидола на концентрацию МДА и активность СОД у пациентов с ХИМ и ХСН.
Table 3. Effect of Mexidol on MDA concentration and COD activity in patients with chronic brain ischemia and CHF
|
Параметр |
Группа |
Исходное значение |
7-е сутки |
13 нед |
|
МДА, мкмоль/л |
Мексидол+базисная терапия |
2,54±1,17 |
1,85±0,83* |
1,75±0,79*# |
|
Базисная терапия |
2,04±0,68 |
1,98±0,70 |
2,31±0,80 |
|
|
СОД, Ед/мг белка |
Мексидол+базисная терапия |
0,136±0,037 |
0,144±0,037# |
0,137±0,031# |
|
Базисная терапия |
0,119±0,038 |
0,117±0,03 |
0,117±0,03 |
Примечание: * — p<0,05 — достоверные различия с исходными значениями, # — p<0,05 — достоверные различия между группами «Мек-сидол + базисная терапия» и «базисная терапия».
Таблица 4. Влияние Мексидола на СРБ и ФНО-а у пациентов с ХИМ и ХСН.
Table 4. Effect of Mexidol on CRP and TNFa in patients with chronic brain ischemia and CHF
|
Параметр |
Группа |
Исходное значение |
7 сутки |
13 недель |
|
СРБ, мг/л |
Мексидол + базисная терапия |
11,83 [4,10; 19,22] |
6,99 [6,27; 12,42]* |
2,99 [0,00; 7,53]*# |
|
Базисная терапия |
6,21 [1,58; 16,22] |
6,28 [3,57; 11,67] |
10,48 [7,81; 14,50] |
|
|
ФНО-а, пг/мл |
Мексидол + базисная терапия |
15,50 [10,87; 37,22] |
1,00 [0,00; 9,23]* |
0,86 [0,00; 3,23]* |
|
Базисная терапия |
28,56 [18,76; 29,60] |
11,20 [0,00; 39,45] |
0,00 [0,00; 21,48] |
Примечание. * — p<0,05 — достоверные различия с исходными значениями, # — p<0,05 — достоверные различия между группами «Мексидол + базисная терапия» и «базисная терапия».
При сравнении изменений концентрации СРБ при применении Мексидола и базисной терапии и только базисной терапии на 7-й день лечения достоверных различий между группами получено не было, а через 13 нед применения Мексидола уровень СРБ снижался, а в группе базисной терапии повышался (p=0,016) (см. табл. 6).
У пациентов, уровень ФНО-а в плазме крови которых при поступлении был выше нормы (>8,21 пг/мл), применение Мексидола в дополнение к базисной терапии на 7-й день исследования вызывало снижение данного показателя на 93,5% (p=0,012), а через 13 нед — на 94,5% (p=0,017) по сравнению с исходными значениями. В то же время в группе базисной терапии достоверных изменений получено не было (см. табл. 6).
Таким образом, показано достоверное снижение содержания маркеров воспаления на фоне терапии Мекси-долом в дополнение к базисной терапии у пациентов с ХИМ и ХСН.
Влияние Мексидола на уровень гомоцистеина
Применение Мексидола в комплексной терапии пациентов с ХИМ и ХСН достоверно не влияло на уровень гомоцистеина в плазме крови. Данный показатель достоверно не изменялся по сравнению с исходными значениями. В то же время в группе пациентов, получавших базисную терапию, концентрация гомоцистеина имела тенденцию к повышению через 13 нед терапии на 17,5% (p=0,061) (см. табл. 6).
При сравнении изменений содержания гомоцистеина в плазме крови через 13 нед терапии на фоне Мек-сидола уровень гомоцистеина нарастал в 11,2 раза меньше (60,44 нг/мл против 679,74 нг/мл соответственно), чем при применении базисной терапии (p=0,052), что, в том числе, свидетельствовало о способности препарата сдерживать нарастание уровня аминокислоты, вызывающей, в том числе, дисфункцию эндотелия.
Влияние Мексидола на уровень цистатина С
Применение Мексидола в дополнение к базисной терапии, так же как и изолированная базисная терапия, достоверно не влияли на уровень цистатина С в плазме крови пациентов с ХИМ и ХСН на 7-й день и через 13 нед наблюдения. Не получено достоверных различий и при сравнении исследуемых групп между собой. Таким образом, длительная последовательная терапия Мексидолом не влияет на функцию почек, что является подтверждением высокого профиля безопасности Мексидола.
Влияние на качество жизни
Уменьшение суммарного балла по Миннесотскому опроснику, которое соответствует повышению оценки качества жизни, было зафиксировано в обеих группах. Однако в группе пациентов, получавших Мексидол в дополнение к базисной терапии, изменение относительно исходного уровня было выражено больше — 48% против 41% в группе базисной терапии.
Оценка качества жизни по Канзасскому опроснику складывалась из целого ряда параметров, которые были классифицированы в 8 различных категорий: физические ограничения, симптомы ХСН, стабильность симптоматики ХСН, социальные ограничения, способность к самопомощи, качество жизни, функциональный статус пациентов и их клиническое состояние. Затем рассчитывалась общая суммарная оценка (рис. 2). Выявлено, что в обеих группах в целом и в каждой из оцениваемых категорий наблюдалась положительная динамика, причем в группе «Мексидол+базисная терапия» она была более выраженной, чем в группе базисной терапии, особенно по категориям физических ограничений, симптомов, самопомощи, оценки функционального статуса, клинического состояния и общей суммарной оценки.
Оценка переносимости физической нагрузки проводилась на основании теста с 6-минутной ходьбой (Т6МХ). В группе «Мексидол+базисная терапия» выявлено статистически значимое увеличение расстояния на 60 м на 7-й день и на 90 м — через 13 нед лечения (p<0,001). В группе базисной терапии наблюдалось достоверное увеличение расстояния на 55 м на 7-й день и на 70 м — через 13 нед терапии (p<0,001). В группе пациентов, получавших Мекси-дол, улучшение показателя Т6МХ более чем на 80 м отмечалось у 52,9% больных, в группе базисной терапии — у 47,1%.
Рис. 2. Канзасский опросник. Динамика баллов по различным шкалам в группах наблюдения.
Fig. 2. Kansas questionnaire. Dynamics of scores on different items in both groups.
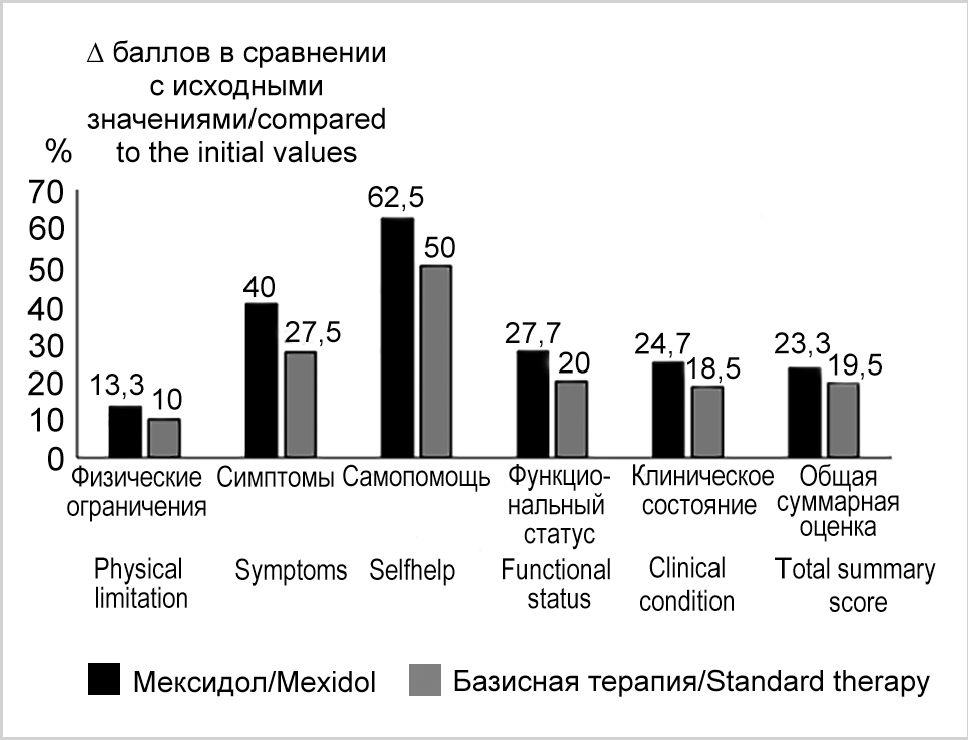
 Таблица 5. Динамика эхокардиографических показателей в группах наблюдения.
Таблица 5. Динамика эхокардиографических показателей в группах наблюдения.
Table 5. Echocardiography data in both groups
|
Параметр |
Группа |
Исходное значение |
13 нед |
|
КДР ЛЖ, см |
Мексидол+базисная терапия |
5,9 [5,1; 6,4] |
5,5 [5,0; 5,8]***л |
|
Базисная терапия |
5,9 [5,3; 6,4] |
5,8 [5,1; 6,3]*** |
|
|
КСР ЛЖ, см |
Мексидол+базисная терапия |
4,8 [4,0; 5,5] |
4,6 [3,8; 4,8]***л |
|
Базисная терапия |
4,9 [4,0; 5,6] |
4,8 [4,2; 5,3] |
|
|
ФВ ЛЖ,% |
Мексидол+базисная терапия |
32 [25; 39] |
33 [27; 42] |
|
Базисная терапия |
30 [24; 40] |
30 [25; 47] |
Примечание. ' — p<0,05 при сравнении между группами «базисная терапия» и «Мексидол+базисная терапия»; * — p<0,05, ** — p<0,01,
*** — p<0,001 при сравнении с исходными значениями.
Таблица 6. Динамика лабораторных критериев эффективности.
Table 6. Laboratory data
|
Показатель |
Мексидол+ базисная терапия |
p |
Базисная терапия |
p |
p -критерий между группами |
|
Динамика показателей окислительного стресса |
|||||
|
7-й день |
-27,2% |
0,020 |
-2,9% |
0,729 |
0,054 |
|
13 нед |
-31,1% |
0,023 |
+13,2% |
0,706 |
0,036 |
|
ДСОД |
|||||
|
7-й день |
23,3% |
0,506 |
-1,7% |
0,844 |
0,011 |
|
13 нед |
17,1% |
0,882 |
-1,7% |
0,399 |
0,057 |
|
Динамика маркеров воспаления |
|||||
|
7-й день |
-40,9% |
0,057 |
+1,1% |
0,378 |
0,518 |
|
13 нед |
-74,7% |
0,001 |
+68,8% |
0,535 |
0,016 |
|
Д ФНО-а |
|||||
|
7-й день |
-93,5% |
0,012 |
-60,8% |
0,678 |
0,743 |
|
13 нед |
-94,5% |
0,017 |
-100% |
0,500 |
0,943 |
|
Динамика маркера эндотелиальной дисфункции Дгомоцистеин |
|||||
|
7-й день |
+15,6% |
0,768 |
-6,8% |
0,951 |
0,664 |
|
13 нед |
+3,3% |
0,653 |
+17,5% |
0,061 |
0,052 |
|
Динамика NT-pro-BNP |
|||||
|
7-й день |
-29,2% |
0,002 |
-32,5% |
0,007 |
0,007 |
|
13 нед |
-44,2% |
0,005 |
-12,2% |
0,834 |
0,050 |
Оценка клинического состояния больного с ХСН
Оценку клинического состояния пациентов проводили при помощи интегральной оценки тяжести клинического статуса с использованием ШОКС (модификация В.Ю. Мареева). Выявлено статистически значимое снижение баллов по ШОКС в группе «Мексидол+базисная терапия» на 83% на 7-й день и на 86% — через 13 нед наблюдения (p<0,001). В группе базисной терапии наблюдались снижение баллов по ШОКС на 73% на 7-й день и на 78% — через 13 нед (p<0,001).
Оценка эхокардиографических показателей
Всем пациентам проводилась трансторакальная эхокардиография по стандартному протоколу исходно, через 7 сут и 13 нед наблюдения. Обращало на себя внимание достоверное уменьшение конечно-диастолического (КДР) и конечно-систолического (КСР) размеров ЛЖ на 7-й день и через 13 нед, наиболее выраженное в группе «Мексидол+базисная терапия». Различия между группами в отношении этих показателей через 13 нед терапии были достоверными (табл. 5). По другим оцениваемым параметрам статистически значимых различий выявлено не было.
Проводимое лечение ассоциировалось со значительным улучшением клинико-функционального статуса и снижением выраженности основных проявлений ХСН. Исходно число пациентов с ХСН II—III ФК в группах мексидола и базисной терапии было сопоставимым. На фоне лечения большинство пациентов перешли в более легкий функциональный класс. Количество пациентов с II—III ФК к 7-му дню терапии снизилось в группе «Мексидол+базисная терапия» до 52,4%, а в группе базисной терапии до 60,9%, к 13-й неделе показатель составил 35,3% в обеих группах.
Обсуждение
За последнее время произошли значимые изменения не только в структуре заболеваний, приводящих к ХСН, но и в профиле нарушений внутрисердечной гемодинамики, а также в научных взглядах на патогенез развития и прогрессирования ХСН. В связи с тем, что в основе патогенеза ХСН лежит целый ряд механизмов, для изучения его основ необходимо использовать комплексный подход. При этом качество жизни пациентов и возможность его улучшения с помощью лекарственных препаратов стали играть важную роль в комплексной терапии больных с ХСН.
Доказано, что в патогенезе ХСН наряду с другими патогенетическими звеньями значимую роль играет не только субклиническое воспаление, но и окислительный стресс, дисфункция эндотелия, активация ренин-ангиотензиновой и симпатико-адреналовой систем. Это подтверждает важность комплексного подхода в изучении патогенеза ХСН и свидетельствует о сложности и многокомпонентности этого процесса у пациентов с данным заболеванием. В настоящее время активно обсуждается выделение отдельных «фенотипов» ХСН с учетом комплекса клинико-лабораторных и инструментальных показателей, основанных на значениях воспалительной активации, окислительного стресса, типах реагирования сосудистого эндотелия, размерах и объеме ЛЖ [20]. Поэтому поиск современных лекарственных препаратов, которые будут оказывать влияние одновременно на комплекс клинических и лабораторных показателей, а также качество жизни пациентов, является актуальным.
Результаты ряда исследований свидетельствуют о том, что снижение уровня NT-proBNP на >30% коррелирует с клиническим эффектом терапии и исходами ХСН [20]. В данном исследовании назначение Мексидола в стандартной терапии ХСН приводило к достоверно более выраженному снижению NT-proBNP (44,2%) в отличие от группы базисной терапии (12,2%) (p=0,05), что является лабораторным критерием эффективности и свидетельствует о клиническом улучшении состояния пациентов и эффективности препарата.
Показано, что у пациентов с ХСН Мексидол оказывал антиоксидантное действие, что проявлялось в снижении концентрации конечного продукта окисления липидов (МДА) в плазме крови и повышении активности антиоксидантного фермента (СОД) по сравнению как с исходными значениями, так и с показателями группы стандартной терапии. Окислительный стресс играет важную роль в прогрессировании сердечно-сосудистых заболеваний и развитии неблагоприятных исходов [21], поэтому выявленное антиоксидантное действие Мексидола может быть полезным в комплексной терапии пациентов с ХСН.
При изучении влияния Мексидола на эндотелиальную дисфункцию у пациентов с ХИМ и ХСН было показано, что препарат к 13-й неделе лечения сдерживал нарастание уровня гомоцистеина (данный показатель повышался в 11,2 раза меньше, чем в группе базисной терапии), что может свидетельствовать о способности Мексидола предотвращать повреждение эндотелия, вызванное гомоцистеином.
Показано, что концентрация маркеров воспаления, таких как СРБ и ФНО-а, повышена у пациентов с ХСН и является независимым неблагоприятным прогностическим фактором сердечной смерти и сердечно-сосудистых событий [22]. Предполагают, что одним из основных факторов, способствующих выработке СРБ и ФНО-а, является системная тканевая ишемия и гипоксия. В данном исследовании показано, что на фоне дополнительного назначения Мексидола у пациентов с ХСН достоверно снижались показатели СРБ и ФНО-а на 7-е сутки и через 13 нед терапии по сравнению с исходным уровнем. Таким образом, длительная последовательная терапия Мексидолом при добавлении к стандартной терапии пациентов с ХСН достоверно уменьшает проявления окислительного стресса и снижает выраженность воспалительной реакции.
У пациентов с ХСН, получавших Мексидол в дополнение к стандартной терапии, концентрация цистати-на С в плазме крови достоверно не отличалась от значений при поступлении и от показателей в группе стандартной терапии. Полученные результаты свидетельствуют о том, что длительная последовательная терапия Мексидолом при добавлении к стандартной терапии не влияет на функцию почек.
При оценке влияния препарата на качество жизни положительная динамика была выявлена в обеих группах по данным обоих опросников (Канзасского и Миннесотского). При этом в группе «Мексидол+базисная терапия» она была более выраженной (см. рис. 2) по категориям физических ограничений, симптомов, самопомощи, оценки функционального статуса, клинического состояния и общей суммарной оценки по Канзасскому и Миннесотскому опросникам (улучшение на 48%) в отличие от группы базисной терапии (41%).
Функциональный статус пациентов оценивали на основании оценки переносимости физической нагрузки (Т6МХ), а также динамики клинического состояния больного с ХСН по ШОКС (в модификации В.Ю. Мареева). Показано, что для того, чтобы можно было судить об улучшении качества жизни у пациентов с ХСН, изменение показателей при Т6МХ должно составлять около 80 м [23]. Выявлено статистически значимое увеличение расстояния по данным теста на 90 м в группе «Мексидол+базисная терапия» и на 70 м — в группе базисной терапии. При этом в группе пациентов, получавших Мексидол, улучшение показателя Т6МХ более чем на 80 м отмечалось у 52,9% больных, в группе базисной терапии — у 47,1%, что согласуется с данными литературы [18]. Отмечено достоверное улучшение клинического состояния по ШОКС в обеих группах с более выраженным эффектом в группе пациентов, получавших Мексидол в дополнение к базисной терапии (86 и 78% соответственно). К 7-му дню терапии больший процент пациентов в группе «Мексидол+базисная терапия» перешел в более легкий ФК по сравнению с группой базисной терапии.
Таким образом, можно говорить об эффективности препарата в отношении вторичных точек, таких как качество жизни, а также функциональный статус пациентов с ХИМ и ХСН с низкой ФВ ЛЖ.
Важно отметить, что результаты теста 6-минутной ходьбы должны оцениваться вкупе с данными, отражающими динамику NT-proBNP, оценкой качества жизни, а также результатами эхокардиографии [20].
Оценка дополнительных критериев эффективности включала в себя анализ эхокардиографических показателей при трансторакальной эхокардиографии по стандартному протоколу. Эхокардиографическое исследование свидетельствует об улучшении показателей внутрисердечной гемодинамики у пациентов, получавших Мекси-дол в дополнение к базисной терапии. Выявлено достоверное уменьшение КДР и КСР ЛЖ через 13 нед наблюдения, наиболее выраженное в данной группе. Различия между группами по этим показателям были достоверными.
Таким образом, прием Мексидола в дополнение к стандартной терапии у пациентов с ХСН и ХИМ, помимо доказанной антиоксидантной и антигипоксантной активности, оказывает благоприятное влияние на качество жизни, функциональный статус, клинические и эхокардиографические параметры.
Необходимо упомянуть ряд ограничений данного исследования. В связи с тем, что настоящая работа проводилась в центре по лечению пациентов с ХСН, базисную терапию получали 100% пациентов данного исследования, что может не соответствовать картине, наблюдаемой в реальной клинической практике. Важно отметить небольшое число пациентов, включенных в данный проект, и малую длительность наблюдения. Полученные данные о благоприятном влиянии Мексидола на качество жизни и функциональный статус пациентов с ХИМ и ХСН можно рассматривать как пилотный проект, являющийся важной предпосылкой для дальнейшего изучения данных параметров в популяции.
Заключение
Полученные данные свидетельствуют о том, что длительная последовательная терапия препаратом Мексидол при добавлении к базисной терапии пациентов с ХИМ и ХСН, помимо улучшения клинического состояния (снижение уровня NT-proBNP) и показателей внутрисердечной гемодинамики (уменьшение КДР и КСР ЛЖ), улучшает качество жизни пациентов, обладает доказанной антиоксидантной активностью, снижает выраженность воспалительной реакции и не влияет на функцию почек.
Финансирование: спонсорская поддержка исследования отсутствует.
Информация о конфликте интересов: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
The authors declare no conflicts of interest.
ЛИТЕРАТУРА/REFERENCES
1. Benjamin EJ, Muntner P, Alonso A, Bittencourt MS, Callaway CW, Carson AP, Chamberlain AM, Chang AR, Cheng S, Das SR, et al; American Heart Association Council on Epidemiology and Prevention Statistics Committee and Stroke Statistics Subcommittee. Heart disease and stroke statistics-2019 update: a report from the American Heart Association. Circulation. 2019;139:56-528. https://doi.org/10.1161/CIR.0000000000000659
2. Heidenreich PA, Albert NM, Allen LA, Bluemke DA, Butler J, Fonarow GC, Ikonomidis JS, Khavjou O, Konstam MA, Maddox TM, et al; American Heart Association Advocacy Coordinating Committee; Council on Arteriosclerosis, Thrombosis and Vascular Biology; Council on Cardiovascular Radiology and Intervention; Council on Clinical Cardiology; Council on Epidemiology and Prevention; Stroke Council. Forecasting the impact of heart failure in the United States: a policy statement from the American Heart Association. Circ Heart Fail. 2013;6:606-619. https://doi.org/10.1161/HHF.0b013e318291329a
3. Bui AL, Horwich TB, Fonarow GC. Epidemiology and risk profile of heart failure. Nat Rev Cardiol. 2011;8:30-41. https://doi.org/10.1038/nrcardio.2010.165
4. Alagiakrishnan K, Mah D, Ahmed A, Ezekowitz J. Cognitive decline in heart failure. Heart Fail Rev. 2016;21:661-673. https://doi.org/10.1007/s10741-016-9568-1
5. Митрофанова И.С., Коц Я.И., Вдовенко Л.Г., Новые пути повышения эффективности лечения больных хронической сердечной недостаточностью. Сердечная недостаточность. 2016;4:164-166.
6. Alhaddad IA, Hamoui O, Hammoudeh A, Mallat S. Treatment adherence and quality of life in patients on antihypertensive medications in a Middle Eastern population: adherence. Vasc Health Risk Manag. 2016;27(12):407-413. https://doi.org/10.2147/VHRM.S105921
7. Perwitasari DA, Urbayatun S. Treatment Adherence and Quality of Life in Diabetes Mellitus Patients in Indonesia. SAGE Open. 2016;1-7. https://doi.org/10.1177/2158244016643748
8. Zioga E, Kazakos K, Dimopoulos E, et al. Adherence and quality of life in patients with type 2 diabetes mellitus in northern Greece. Mater Sociomed. 2016;28(4):258-262. https://doi.org/10.5455/msm. 2016.28.258-262
9. Марцевич С.Ю., Лукина Ю.В., Кутишенко Н.П., Воронина В.П., Лерман О.В., Гайсенок О.В., Гомова Т.Д., Ежов А.В., Куимов А.Д., Либис РА., Матюшин ГВ., Митрошина Т.Н., Нечаева ГИ., Резник И.И., Скибицкий В.В., Соколова Л.А., Чесникова А.И., Добрынина Н.В., Якушин С.С. Приверженность к лечению и качество жизни больных стабильной ишемической болезнью сердца при лечении никорандилом: взаимосвязь и взаимовлияние (по результатам наблюдательного исследования НИКЕЯ). Рациональная Фармакотерапия в Кардиологии. 2018;14(3):XX-XX. Martsevich SY, Lukina YV, Kutishenko NP, Voronina VP, Lerman OV, Gaisenok OV, Gomova TA, Ezhov AV, Kuimov AD, Libis RA, Matyushin GV, Mitroshina TN, Nechaeva GI, Reznik II, Skibitsky VV, Sokolova LA, Chesnikova AI, Dobrynina NV, Yakushin SS. Treatment Adherence and Quality of Life of Patients with Stable Ischemic Heart Disease in Treatment with Nicorandil: Interrelation and Interaction (According to the Results of the Observational Study NIKEA). Rational Pharmacotherapy in Cardiology. 2018;14(3):XX-XX. (In Russ). https://doi.org/10.20996/1819-6446-2018-14-3-XX-XX
10. Reddy P, Dunn AB. The effect of beta-blockers on health-related quality of life in patients with heart failure. Pharmacotherapy. 2000;20:679-689. https://doi.org/10.1592/phco.20.7.679.35178
11. Tsevat J, Weeks JC, Guadagnoli E, Tosteson AN, Mangione CM, Pliskin JS, Weinstein MC, Cleary PD. Using health-related quality-of-life information: clinical encounters, clinical trials, and health policy. J Gen Intern Med. 1994;9:576-582. https://doi.org/10.1007/bf02599287
12. Lewis EF, Johnson PA, Johnson W, Collins C, Griffin L, Stevenson LW. Preferences for quality of life or survival expressed by patients with heart failure. J Heart Lung Transplant. 2001;20:1016-1024. https://doi.org/10.1016/S1053-2498(01)00298-4
13. US FDA. Treatment for Heart Failure: Endpoints for Drug Development Guidance for Industry. 2019. https://wwwfdagov/regulatory-information/searchfda-guidancedocuments/treatment-heart-failure-endpoints-drug-developmentguidance-industry
14. Полунина Е.А., Воронина Л.П., Попов Е.А., Белякова И.С., Полунина О.С., Тарасочкина Д.С. Прогностические алгоритмы прогрессирования хронической сердечной недостаточности в зависимости от клинического фенотипа. Кардиоваскулярная терапия и профилактика. 2019;18(3):41-47. Polunina EA, Voronina LP, Popov EA, Belyakova IS, Polunina OS, Tarasochkina DS. Prognostic algorithms for the progression of chronic heart failure depending on the clinical phenotype. Cardiovascular Therapy and Prevention. 2019;18(3):41-47. (In Russ.). https://doi.org/10.15829/1728-8800-2019-3-41-47
15. Арутюнов А.Г., Драгунов Д.О., Арутюнов Г.П., Рылова А.К. Прогностически значимые клинические фенотипы больных с декомпенсацией кровообращения в РФ. Журнал Сердечная Недостаточность. 2015;16:5:270-278. Arutyunov AG, Dragunov DO, Arutyunov GP, Rylova AK. Prognostically significant clinical phenotypes of patients with circulatory decompensation in the Russian Federation. Russian Heart Failure Journal. 2015;16:5:270-278. (In Russ.). https://doi.org/10.18087/rhfj.2015.5.2135
16. D’Elia E, Vaduganathan M, Gori M, Gavazzi A. Role of biomarkers in cardiac structure phenotyping in heart failure with pre-served ejection fraction: critical appraisal and practical use. Eur J Heart Fail. 2015;17:12:1231-1239. https://doi.org/10.1002/ejhf.43
17. Воронина Т.А., Иванова Е.А. Комбинированное примене ние мексидола с известными лекарственными средствами. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(4):115-124. Voronina TA, Ivanova EA. Combined administration of mexidol with known medicines. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2019;119(4):115-124. (In Russ.). https://doi.org/10.17116/jnevro2019119041115
18. Стаценко М.Е., Евтерова Е.Д., Туркина С.В. и др. Новые возможности мексидола в лечении хронической сердечной недостаточности у больных с метаболическим синдромом. Российский кардиологический журнал. 2010;6(86):28-33. Statsenko ME, Evterova ED, Turkina SV, et al. New possibilities of mexicor in the treatment of chronic heart failure in patients with metabolic syndrome. Russian Journal of Cardiology. 2010;6(86):28-33. (In Russ.). https://doi.org/10.15829/1560-40712010-6-28-33
19. Щулькин А.В., Казахмедов Э.Р., Галочкин С.А., Толкачева В.В., Кобалава Ж.Д. Эффекты Мексидола у пациентов с ХИМ и ХСН II—III функционального класса. Кардиология и сердечно-сосудистая хирургия. 2020;13(5):427-434. https://doi.org/10.17116/kardio202013051427
20. Ferreira JP, Duarte K, Graves TL, et al. Natriuretic peptides, 6-min walk test, and quality-of-life questionnaires as clinically meaningful endpoints in HF trials. J Am Coll Cardiol. 2016;68:2690-2707. https://doi.org/10.1016/j.jacc.2016.09.936
21. D’Oria R, Schipani R, Leonardini A, Natalicchio A, Perrini S, Cignarelli A, Laviola L, Giorgino F. The role of oxidative stress in cardiac disease: from physiological response to injury factor. Oxidative medicine and Cellular longevity. 2020. https://doi.org/10.1155/2020/5732956
22. Yin W-H, Chen J-W, Jen H-L, Chiang M-C, Huang W-P, Feng A-N, Lin S-J. Independent prognostic value of elevated highsensitivity C-reactive protein in chronic heart failure. American Heart Journal. 2004;147(5):931-938. https://doi.org/10.1016/j.ahj.2003.11.021
23. Giannitsi S, et al. 6-minute walking test: a useful tool in the management of heart failure patients. Ther Adv Cardiovasc Dis. 2019;13:1-10. https://doi.org/10.1177/1753944719870084
Effect of Mexidol on the quality of life and functional status of patients with chronic cerebral ischemia and chronic heart failure with reduced left ventricular ejection fraction
© V.V. Tolkacheva1, E.R. Kazakhmedov1, Zh.D. Kobalava1, S.A. Galochkin1, A.V. Shchulkin2
- 1Peoples’ Friendship University of Russia, Moscow, Russia;
- 2Pavlov Ryazan State Medical University, Ryazan, Russia
Abstract
Objective. To study the effect of Mexidol on the functional state of myocardium, NT-proBNP level, exercise tolerance, quality of life, severity of oxidative stress, inflammatory response and endothelial dysfunction in patients with chronic brain ischemia and chronic heart failure NYHA class II-III in a 13-week sequential (intravenous and oral) therapy with Mexidol® and standard therapy.
Material and methods. The study included 44 patients with chronic brain ischemia and chronic heart failure NYHA class II—III. Mean age was 65.5±11.8 years, men accounted 75%. The group of Mexidol + standard therapy of chronic heart failure included 21 patients, the group of standard therapy — 23 patients. Echocardiography parameters, exercise tolerance test (six minute walk test, SMWT), patient’s clinical condition according to SHOKS scale (modification by V. Yu. Mareev), NT-proBNP concentration, markers of oxidative stress (malonic dialdehyde (MDA), superoxide dismutase (SOD)), inflammatory reaction (C-reactive protein (CRP), tumor necrosis factor a (TNFa)), homocysteine and cystatin C were examined initially, after 7 days and 1 3 weeks. The quality of life was assessed initially and at the end of the study using the Minnesota Living With Heart Failure Questionnaire (MLHFQ) and the Kansas City Cardiomyopathy Questionnaire (KCCQ).
Results. «Mexidol + standard therapy» group was characterized by more significant improvement in the quality of life, better SMWT data and SHOKS scores, significant decrease in end-diastolic and end-systolic LV dimensions, as well as NT-proBNP level after 7 days and 13 weeks compared to the basic therapy group. Mexidol administration reduced MDA concentration and increased SOD activity after 7 days and 13 weeks. We also observed a significant decrease in CRP and TNFa levels after 7 days and 13 weeks in the same group. Less augmentation of homocysteine was revealed in the Mexidol therapy group. There were no significant between-group differences in cystatin C levels.
Conclusion. Mexidol in addition to standard therapy of chronic brain ischemia and chronic heart failure class II-III has a favorable effect on the quality of life, functional status, improves clinical condition and intracardiac circulation, decreases concentration of NT-proBNP, promotes antioxidant activity, reduces inflammatory reaction, slows down increase of homocysteine and does not influence kidney function.
Keywords: chronic brain ischemia, heart failure, quality of life, cognitive status, oxidative stress, ethyl-methyl-hydroxypyridine succinate, Mexidol, inflammation, endothelial dysfunction.
Information about the authors:
Tolkacheva V.V. — orcid.org/0000-0001-6847-8797
Kazakhmedov E.R. — orcid.org/0000-0002-6274-8933
Kobalava Zh.D. — orcid.org/0000-0002-5873-1768
Galochkin S.A. — orcid.org/0000-0001-7370-8606
Shchulkin A.V. — orcid.org/0000-0003-1688-0017
Corresponding author: Tolkacheva V.V. — e-mail: tolkachevav@mail.ru
To cite this article:
Tolkacheva V.V., Kazakhmedov E.R., Kobalava Zh.D., Galochkin S.A., Shchulkin A.V. Effect of Mexidol on the quality of life and functional status of patients with chronic cerebral ischemia and chronic heart failure with reduced left ventricular ejection fraction. Russ. Jour. of Card. and Cardiovasc. Surg. = Kard. i serd.-sosud. khir. 2021;14(1):80-89. (In Russ.). doi.org/10.17116/kardio20211401180
