Мексидол в комплексной терапии стабильной стенокардии
СтатьиГ.И. Нечаева1, С.Д. Курочкина2, А.Д. Троценко3, Е.Ю. Булахова2
1Омская государственная медицинская академия; 2БУЗОО Городская клиническая больница 4; 3БУЗОО Медицинский центр Министерства здравоохранения Омской областик
Проведена оценка качества жизни и тревоги у 130 пациентов с ишемической болезнью сердца и стабильной стенокардией II функционального класса (ФК) в условиях поликлинического отделения БУЗОО «Городская клиническая больница №4». Изучены клинико-функциональные показатели у больных стабильной стенокардией, влияние заболевания на их качество жизни. Оценена клиническая эффективность препарата 2-этил-6-метил-3-гидроксипиридина сукцинат (мексидол) в комплексном лечении больных стабильной стенокардией II ФК. Разработан дифференцированный подход к фармакотерапии с учетом уровня тревоги личности у больных стенокардией II ФК.
Ключевые слова: ишемическая болезнь сердца, стабильная стенокардия II функционального класса, качество жизни.
Источник: Кардиология и сердечно-сосудистая хирургия. 2013. Т. 6. № 1. С. 33-39.
MEXIDOL IN COMLEX THERAPY OF A STABLE ANGINA
G.I. Nechaeva1, S.D. Kurochkina2, A.D. Trotsenko3, E.U. Bulachova2
It is carried out research of quality of life and alarm at 130 patients with stable angina FC II conditions of policlinic branch BUZOO City Clinical Hospital 4 Omsk. We have studied functional parameters at sick by a stable angina, influence of disease on quality of life. We have studied efficiency of preparation Mexidol in complex treatment of patients with a stable angina. We have developed the differentiated approach to pharmacotherapy in view of quality of life and a level of alarm of person.
Key words: ischemic heart disease, stable angina, quality of life.
Ишемическая болезнь сердца (ИБС) в течение многих лет является главной причиной смертности населения во многих экономически развитых странах. В настоящее время сердечно-сосудистые заболевания (ССЗ) играют решающую роль в эволюции общей смертности в России [1, 3, 4, 21]. ИБС в структуре ССЗ составляет 26,6%. Среди различных клинических форм ИБС ведущее место занимает стенокардия [10]. Стенокардия — хроническое заболевание, при котором больные длительно, часто пожизненно должны получать терапию [5, 10, 17]. Результаты многочисленных исследований свидетельствуют о значительном снижении качества жизни (КЖ) у больных со стабильной стенокардией по сравнению со здоровым населением [20], наблюдается корреляция между выраженностью депрессивных расстройств и тяжестью соматического состояния. Депрессии и тревожные расстройства могут не только провоцировать ишемическую болезнь сердца, но и оказывать влияние на клинические проявления кардиологического заболевания (рецидивирующие, продолжительные приступы стенокардии, нарушения сердечного ритма), способствовать усилению симптомов [16, 24]. В последние годы накапливается все больше доказательств, что тревога и некоторые другие психопатологические состояния являются независимыми факторами риска сердечно-сосудистых заболеваний, увеличивают заболеваемость и смертность от ишемической болезни сердца [8, 24]
В формировании стенокардии значительная роль принадлежит изменениям вегетативной регуляции деятельности сердца, что проявляется в особенностях течения заболевания [7, 12]. При ишемии наблюдается значительная активация симпатико-адреналовой системы, что сопровождается увеличением содержания в крови и миокарде повреждающих медиаторов, особенно адреналина [12, 19, 25]. Учитывая многогранность факторов, участвующих в формировании клинической картины стенокардии, ученые проводят постоянный поиск и разработку новых, наиболее эффективных способов оптимизации лечения [10, 17].
Нами предложено включить в схему терапии стенокардии II функционального класса (ФК) мексидол (2-этил-6-метил-3-гидроксипиридина сукцинат), обладающий антиоксидантным, вегетотропным, ноотропным, анксиолитическим и сосудистым эффектами [2, 6, 9, 11, 18, 22].
Материал и методы
Исследование проводилось на базе поликлинического отделения МУЗ «Городская клиническая больница №4». Для изучения клинико-функциональных ИБС стабильной стенокардии обследованы 250 больных, обратившихся за медицинской помощью к кардиологу.
Диагностику стабильной стенокардии [10] осуществляли в соответствии с рекомендациями Российского общества кардиологов.
Критерии включения пациентов в исследование: возраст от 43 до 60 лет; диагноз ИБС, стабильная стенокардия II ФК; стабильное течение заболевания в течение последнего месяца; отсутствие на начало исследования острых или обострения хронических воспалительных заболеваний; согласие пациента участвовать в исследовании.
Критерии исключения: острые формы ИБС; недостаточность кровообращения IIБ—III, ФК III—IV и другие противопоказания к проведению нагрузочных проб; беременность; обострение хронических или появление острых воспалительных заболеваний в процессе исследования; нежелание пациента участвовать в исследовании.
Медиана возраста (V0 5) пациентов группы наблюдения и контрольной группы составила 54 года (V0 25=41; V0 75= 60). В зависимости от уровня тревоги пациенты были разделены на две группы: с высоким уровнем тревоги — 1-я группа (n=66) и с низким уровнем тревоги — 2-я группа (n=64). Пациенты с высоким и низким уровнем тревоги были рандомизированы методом закрытых конвертов на две подгруппы: 1А (n=37) и 1Б (n=29), 2А (n=39) и 2Б (n=25). Подгруппы А получали стандартную терапию при стенокардии II ФК и мексидол, подгруппы Б — только стандартную терапию. Стандартная терапия включала p-блокаторы (бисопролол 5—10 мг), дезагреганты (аспирин 75—100 мг), ингибиторы ангиотензинпревращающего фермента (периндоприл 5—10 мг, симвастатин 40 мг/сут). При необходимости больные сублингвально принимали нитроглицерин или нитроспрей (изокет). Мексидол назначали в суточной дозе 375 мг в 3 приема. В период наблюдения каждый пациент сохранял выбранную ранее суточную дозу антиангинальных препаратов, кратность и время их приема, поддерживал прежний образ жизни, физической активности и характер питания. Оценку клинической эффективности лекарственной терапии проводили в динамике: исходно, 2, 4- и 12-я недели наблюдения.
Для решения поставленных задач исследование проводили по этапам: сбор анамнеза (отягощенный анамнез или наличие факторов риска); исследование клиникофункциональных особенностей с помощью записи электрокардиограммы (ЭКГ), эхокардиграфии (Эхо КГ), нагрузочных проб, оценка КЖ с помощью опросника MOS SF-36v2 («SF-36 v2 Health Status Survey») [20], личностную тревожность (J. Teylor). Оценивали физический (PH), психологический (Mh) компоненты здоровья и их важнейшие составляющие: физическое функционирование (HF), ролевое физическое функционирование (RP), ролевое эмоциональное функционирование (RE), интенсивность боли (BP), общее состояние здоровья (GH), полноценность ощущения жизни (VT), социальное функционирование (SF) и общий уровень психического здоровья (MH). Для изучения состояния вегетативной нервной системы проводили суточное мониторирование ЭКГ с определением показателей вариабельности ритма сердца — ВРС (SDNN, RMSSD, PNN50) и циркадного индекса (отношение среднедневной к средненочной частоте сердечных сокращений — ЧСС), суточное мониторирование артериального давления — АД (СМАД) с определением среднедневных и средненочных систолического (САД) и диастолического АД (ДАД), индекса времени, вариабельности САД и ДАД, суточного профиля АД, показателей утренней динамики САД и ДАД. Для оценки психического статуса применяли личностную шкалу тревоги, адаптированную Т.А. Немчиновым.
Оценку выборки и проверку нормальности распределения проводил с использованием метода Шапиро—Уилка, проверку гипотез о равенстве генеральных дисперсий — с помощью критерия Левене. Статистическую обработку данных выполняли с использованием программ Statistica-6, Биостатистика, Microsoft Excel. Средние выборочные значения количественных признаков приведены в тексте в виде М±σ, где M — среднее выборочное, о — стандартное отклонение. При распределении отличном от нормального указывали медиану (V0,5), 25-й процентиль (V0, 25) и 75-й процентиль (V0, 75). Во всех процедурах статистического анализа критический уровень значимости р принимали равным 0,05. Для проверки статистических гипотез применяли непараметрические критерии: для сравнения двух независимых групп — z-критерий Манна—Уитни, для сравнения двух связанных групп — критерий Вилкоксона, для сравнения качественных данных двух групп — критерий χ2 Пирсона. Причинно-следственные связи определялись в ходе корреляционного анализа Спирмена (r) [13—15, 23].
Результаты и обсуждение
Большинство пациентов в 1-й и 2-й группах (62,1 и 63% соответственно) предъявляли жалобы на боли за грудиной, провоцируемые физическим и эмоциональным напряжением. Редко пациентов беспокоили нетипичные боли, без четкой связи с физической нагрузкой. Однако больные 1-й группы чаще жаловались на головные боли, слабость, утомляемость, беспокойство, чувство страха, снижение настроения, нарушение сна (p<0,05).
В группе высокого уровня тревоги отмечалось большее количество приступов стенокардии за неделю (р=0,001; T=2138; z=9,589) с большим количеством принимаемых таблеток нитроглицерина (р=0,002; T=2981; z=5,603). Частота приступов стенокардии в группе с высоким уровнем тревоги составляла 7,0 (V0, 25=4,0;V0, 75=9,0) в неделю, а в группе низкой тревоги (n=66) — 3,0 (V0, 25=2,0;V0, 75= 5 , 0), число таблеток принимаемого нитроглицерина — 4,0 (V0, 25=3 , 0;V0, 75=6,0), 3,0 (V0, 25= 0;V0, 75=4,0) соответственно. При проведении корреляционного анализа коэффициент ранговой корреляции Спирмена в группе с высоким уровнем тревоги был равен 0,793 (р=0,001).
По данным объективного обследования, в обеих группах преобладали пациенты гиперстенического телосложения, повышенной массы тела. Индекс массы тела более 25 кг/м2 отмечался у 97 (74%) больных.
У 99 (76%) пациентов определялось смещение левой границы влево (0,5—1 см) от среднеключичной линии, без существенных различий по группам.
Показатели, полученные при лабораторном исследовании общего и биохимического анализа крови, статически значимо не различались в группах с высоким и низким уровнями тревоги. Среди пациентов исследуемых групп у 84 (84%) выявлены отклонения липидного состава крови, характерные для Па и у 12 (16%) — для комбинированного типа дислипидемии (р>0,05).
У 54 (82,3%) пациентов с высоким уровнем тревоги ЧСС в покое достигала 80 уд/мин и более (p=0,002), фиксировались более высокие цифры офисного САД (p=0,001) и ДАД (p=0,001). На ЭКГ у всех пациентов выявлялись изменения конечной части желудочкового комплекса, приблизительно у 73% (1-я группа — 73,8%, 2-я группа — 73%) признаки гипертрофии миокарда левых отделов сердца. В группе высокой тревоги отмечалось большее количество экстрасистол (p=0,014; T=3670,5; z=2448).
По исходным данным холтеровского мониторирования ЭКГ, в группе высокой тревоги фиксировалась более высокая средняя ЧСС (р=0,036), регистрировалось большее количество наджелудочковых (р=0,003) и желудочковых (p=0,004) экстрасистол, пароксизмальных нарушений ритма (p=0,001), частоты эпизодов депрессий сегмента ST (p=0,006).
У 50% пациентов обеих групп при анализе отмечалось снижение показателей ВРС (SDNN, RMSSD и RNNSS). При этом показатели ВРС SDNN (p=0,001; T=5270,5; z=5,037) и RMSSD в группе высокой тревоги (p=0,019; T=2032,5; z=2,343) были статистически значимо ниже, чем в группе низкой тревоги (p<0,05). Исходно снижение показателей ВРС в группе высокой тревоги сочеталось с низкими значениями циркадного индекса (менее 1,47) (p=0,001), что свидетельствует об усилении влияния симпатической активности.
По данным СМАД, во всех группах пациентов регистрировалось повышенное АД. В группе с высоким уровнем тревоги фиксировались более высокие показатели среднего САД (р=0,001; T=2914; z=5,978), ДАД (р=0,003; T=3564,5; z=2,946) в дневные часы. Отмечены также значимые различия по вариабельности САД и ДАД (р=0,001; T=1275; z=1275 и р=0,022; T=1404,5; z=2,283), среднего пульсового АД (р=0,044; T=1442; z=2,016). В утренние часы в группе высокой тревоги фиксировались более значимые утренние подъемы САД и ДАД (р=0,032; T=1423,5; z=2,149 и р=0,005; T=1815,5; z=0,747).
Результаты велоэргометрии в обеих группах отражали снижение толерантности к физическим нагрузкам, соответствующее стенокардии II ФК.
Данные ЭхоКГ обследованных пациентов в 1-й и 2-й группах фиксировали увеличение индекса массы миокарда левого желудочка, склерогенные изменения клапанного аппарата различной степени выраженности без статистически значимых различий.
При сравнении показателей КЖ, полученных при обработке опросника SF-36, все больные с ИБС стенокардией II ФК отмечали снижение всех показателей шкал КЖ. Однако показатели физического функционирования (PF), интенсивности боли, общего состояния здоровья (GH), составляющие физический компонент здоровья и по шкалам жизненной активности (VT), психического состояния (Mh) и общего уровня психологического здоровья, были хуже в 1-й группе (p=0,001; р=0,002; p=0,001; p=0,001 соответственно).
В процессе наблюдения к концу 12-й недели у всех пациентов статистически значимо уменьшилось количество жалоб на головную боль, утомляемость, нарушение сна, «мелькание мушек» перед глазами, шум в ушах, головокружение. Более выраженное уменьшение указанных жалоб отмечали пациенты в группе высокой тревоги на фоне комбинации стандартной терапии с мексидолом (p<0,05) по сравнению с группой высокой тревоги на фоне стандартной терапии.
На фоне лечения через 12 нед в подгруппе 1А (n=37) на 50% снизились количество приступов стенокардии в неделю (р=0,001) и потребность в таблетках нитроглицерина (р=0,003) по сравнению с группой высокой тревоги на фоне стандартной терапии. В 2-й группе с низким уровнем тревоги количество приступов стенокардии и количество принимаемого нитроглицерина через 12 нед не изменилось. Значимых различий между подгруппами 2А и 2Б не было (табл. 1).
Таблица 1
Динамика количества приступов стенокардии в неделю у пациентов 1-й и 2-й групп через 12 нед.
|
1-я группа |
2-я группа |
|||||||
| Показатель | исходно (n=66) | 1А (стандартная терапия и мексидол; n=37) | 1Б (стандартная терапия; n=29) | р | исходно (n=64) | 2А (стандартная терапия и мексидол; n=39) | 2Б (стандартная терапия; n=25) | р |
| Число приступов стенокардии | 7,0 (4,0; 9,0) | 3,0 (2,0; 5,0)*^ | 5,0 (2,0; 09)*^^ | *0,001 ^0,001 ^^0,003 |
3,0 (2,0; 5,0) | 3,0 (3,0; 5,0) | 3,0 (2,9;5,8) | 1,000 1,000 >0,054 |
| Коротко действующие нитраты | 4,0 (3,0; 6,0) | 2 (1,0; 3,0)*^ | 3(2,0; 3,0)*^^ | *0,016^ <0,0001 ^^0,012 |
2,0 (0; 4,0) | 2,0 (3,0; 4,0) | 2,0 (3,0; 5,0) | 1,000 1,000 1,000 |
При сравнении полученных результатов измерения АД на приеме у врача отмечено достоверное снижение САД и ДАД во всех группах, но в большей степени в подгруппе 1А (табл. 2).
Таблица 2
Динамика артериального давления (АД) и частоты сердечных сокращений (ЧСС) через 12 нед.
1-я группа | 2-я группа | |||||||
| Показатель | исходно (n=66) | 1А (стандартная терапия и мексидол; n=37) | 1Б (стандартная терапия; n=29) | р | исходно (n=64) | 2А (стандартная терапия и мексидол; n=39) | 2Б (стандартная терапия; n=25) | р |
| САД, мм рт.ст. | 150 (110; 170) | 120 (110; 135)*^ | 130 (110; 135)*^^ | *0,001 ^0,001 ^^0,003 | 135 (110; 156)* | 120,5 (110; 138)^* | 130 (103; 145)*^^ | 0,001 ^0,001 ^^0,006 |
| ДАД, мм рт.ст. | 90 (78; 100) | 75 (70; 80)*^ | 80 (70; 85)*^^ | *0,001 ^0,001 ^^0,006 | 89 (70; 100)* | 78 (70; 90)^* | 75 (74; 85)^^ | 0,001 ^0,001 ^^0,006 |
| ЧСС, уд/мин | 89 (70; 100) | 58,5 (54,76)*^ | 65 (54; 75)*^ | *0,001 ^0,001 ^^0,012 | 74 (56; 90)* | 55,5 (53,77)^* | 60,8 (58; 78)^^ | *0,071 ^0,000 ^^0,007 |
По данным СМАД в подгруппе 1А выявлено уменьшение среднесуточного САД в дневные часы на 10,8% (V0, 25=110; V0, 75=150; p=0,002). В подгруппе 1Б уменьшение среднесуточного САД составило 6,1% (p=0,034). Медиана среднесуточного ДАД снизилась на 9% по сравнению с исходными данными (p=0,001) со значимыми различиями с группой стандартной терапии (p=0,003). В ночные часы у пациентов подгруппы 1А произошло снижение среднесуточного САД на 3,6% (p=0,002), среднего ДАД на 1,5% (p=0,012) без значимых различий с группой стандартной терапии. Вариабельность САД и ДАД в дневные часы по сравнению с исходными данными в подгруппе 1А снизилась со значимыми различиями с группой стандартной терапии (p=0,003). Кроме того, отмечено понижение среднего пульсового АД в подгруппе 1А (p=0,001) со значимыми различиями с группой стандартной терапии (p=0,001). Во 2-й группе с низким уровнем тревоги фиксировалось снижение среднего САД (p=0,002) и ДАД (p=0,002) в дневные часы по сравнению с исходными данными без значимых различий между группами. В ночные часы во всех группах на фоне лечения достигнуты целевые уровни САД (p=0,001) и ДАД (p=0,001) без различий по группам (p=0,067 и p=0,569). Вариабельность САД (p=0,001) и ДАД (p=0,001) снизилась по сравнению с исходными данными без различий по группам (p=0,087 и p=0,091). Величина утреннего подъема САД в подгруппе 1А была более низкой, чем исходная (на 23%; p=0,004), и статистически значимо отличалась от группы стандартной терапии (p=0,001). Величина утреннего подъема САД во 2-й группе на фоне лечения была ниже, чем исходная, на 13% (p=0,001) без значимых различий между группами (p=0,081). По величине утреннего подъема ДАД зафиксировано снижение в подгруппе 1А на 14% со статистически значимыми различиями с подгруппой стандартной терапии (p=0,001), во 2-й группе — на 13% без статистически значимых различий.
Скорость утреннего подъема САД в подгруппе 1А снизилась по сравнению с исходной на 25% (p=0,002), ДАД — на 28% (p=0,021) со статистически значимыми различиями с подгруппой стандартной терапии (p=0,001 и p=0,001). Во 2-й группе в целом отмечена положительная динамика по снижению скорости утреннего подъема САД (p=0,002) и ДАД (p=0,002) без различий по подгруппам А и Б (p=0,091 и p=0,067).
Терапия с использованием мексидола в подгруппе 1А сопровождалось более высокими показателями ВСР (табл. 3).
Таблица 3
Динамика показателей вариабельности ритма сердца через 12 нед
Показатель | 1-я группа | 2-я группа | ||||||
| исходно (n=66) | 1А (стандартная терапия и мексидол; n=37) | 2А (стандартная терапия; n=29) | Р | исходно | 2А (стандартная терапия и мексидол; n=39) | 2Б (стандартная терапия; n=25) | Р | |
| SDN, мс | 120 (115; 126) | 131,8 (116; 140)*^ | 134,9 (117; 140)*^^ | *0,012 ^0,001 ^^0,001 | 134(116; 170) | 130 (117; 136)^ | 129,3 (116; 134)^^ | 0,067 ^0,001 ^^0,000 |
| RMSSD, мс | 18(15; 23) | 24,3 (11; 16)*^ | 21,9 (16; 24)*^^ | *0,001 ^0,002 ^^0,000 | 19(11,3; 18) | 22 (11; 24)^ | 21,7 (11; 23)^^ | 0,098 ^0,002 ^^0,000 |
| RNN 50/% | 9(8,0; 15) | 6,0 (4,5; 7,0)*^ | 7,60(5;8,0)^^ | *0,022 ^0,000 ^^0,000 | 10 (8; 13) | 7,0 (6,2; 8,2)^ | 7,0 (6,0; 8,0)^^ | 0,900 ^0,001 ^^0,000 |
| Циркадный индекс | 1,5 (1,43; 1,61) | 1,40 (1,4; 1,62)*^ | 1,48 (1,45;1,57)*^^ | *0,001 ^0,000 ^^0,000 | 1,35 (1,2; 1,46) | 1,45 (1,42; 1,56)^ | 1,43 (1,41; 1,55)^^ | 0,089 ^0,000 ^^0,002 |
По результатам суточного мониторирования, комплексное лечение мексидолом в составе стандартной терапии в подгруппах 1А и 2А привело к снижению средней ЧСС и максимальной ЧСС в подгруппе 1А со статистически значимыми различиями с группой 1Б (p=0,001), количества пароксизмальных нарушений ритма в группе высокой тревоги (1А) со значимыми различиями с подгруппой стандартной терапии (p=0,001), к снижению (60%) количества наджелудочковых экстрасистол по сравнению с исходными данными (p=0,002), со значимыми различиями с подгруппой 1Б (p=0,001), к снижению частоты эпизодов снижения сегмента ST (p=0,001), без статистически значимых различий между подгруппами (p=0,089), получавшими разное лечение.
По результатам нагрузочных проб, через 12 нед на фоне комбинированной терапии с использованием мексидола значительно возросли пороговая мощность (p=0,001 и p=0,001), переносимость физических нагрузок без статистически значимых различий между группами. Анализ данных, полученных при лабораторном исследовании крови после 12 нед применения мексидола в комбинации со стандартной терапией остался без изменений. Показатели липидного состава крови статистически значимо различались (p<0,05) с исходными значениями, но без значимых различий по группам.
При оценке динамики уровня тревоги через 12 нед лечения отмечено достоверно (p=0,001) снижение медианы уровня тревоги в группе пациентов с высоким уровнем тревоги на фоне комбинированной терапии с мексидолом с 42 до 13,5 балла. В подгруппе стандартной терапии (1Б) также произошло снижение уровня тревоги с 42 до 35 баллов (на 17%; p=0,001), однако уровень показателей тревоги по-прежнему соответствовал высокому.
По результатам опросника SF-36 у пациентов всех групп при разных вариантах лечения через 12 нед улучшились показатели по всем шкалам, с максимальным проявлением в группах высокой тревоги. Физическое функционирование (PF) увеличилось в подгруппе 1А на 24% (p=0,001), в подгруппе 1Б на 20% (p=0,001). В группах низкой тревоги также отмечена положительная динамика по сравнению с исходными данными: в подгруппе 2А — увеличение на 15% (p=0,013), в подгруппе 2Б — на 14% (p=0,002) без значимых различий между подгруппами (p=0,077). Показатель интенсивность боли (BP) и ее влияние на способность заниматься повседневной деятельностью, включая работу по дому и вне дома, на фоне лечения в комбинации с мексидолом в группе высокой тревоги не только улучшился (p=0,001), но и приобрел максимально возможное значение. Общее состояние здоровья (GH), характеризующее оценку больным своего состояния здоровья в настоящий момент и перспектив лечения, имело статистически значимое улучшение на фоне лечения всеми препаратами: стандартная терапия улучшила данный показатель на 18% (p=0,003) (подгруппа 1Б) и в комбинации с мексидолом — на 30% (p=0,002) (подгруппа 1А), на 7% в группе низкой тревоги на стандартной терапии (подгруппа 2Б) (p=0,012) и на 11% на фоне комбинированного лечения с мексидолом (p=0,002) (подгруппа 2А). Жизненная активность (VT) статистически значимо (p<0,05) возросла у пациентов в группах с высокой тревогой: на фоне приема мексидола на 30% (p=0,001) (подгруппа 1А), на фоне стандартной терапии — на 18% (р=0,002) (подгруппа 1Б). В группах низкой тревоги показатель VT увеличился на 13% (р=0,032) (подгруппа 2А) и на 12% (р=0,003) (подгруппа 2Б) без статически значимых различий между этими подгруппами.
Социальное функционирование (SF) улучшилось на фоне приема всех лекарственных препаратов. Стандартная терапия повысила показатель SF на 10% (р=0,002), комбинированная терапия с мексидолом — на 22% в группе высокой тревоги (подгруппа 1А) (p=0,001). В группах низкой тревоги: на 9% — в подгруппе 2А (p=0,003) и на 8% — в подгруппе 2Б (p=0,012) без статистически значимых различий между подгруппами.
Ролевое эмоциональное функционирование (RE) также улучшилось во всех группах пациентов, но более высокие показатели отмечались в подгруппе 1А — улучшение на 26% (p=0,001) со статически значимыми различиями с подгруппой 1Б стандартной терапии (p=0,021). В группах низкой тревоги отмечена положительная динамика показателя, но без значимых различий между подгруппами. При анализе психического состояния (Mh) увеличился показатель в подгруппе 1А на 29% (р=0,001), в 1Б подгруппе на 14% (р=0,001). В подгруппе 2А показатель психического состояния увеличился на 12% (р=0,002), в подгруппе 2Б — на 8% (р=0,002). При сопоставлении общих показателей физического компонента здоровья самые высокие параметры PH получены при лечении с добавлением мексидола — 75,5 балла (V0, 25=70,1 балла;У0, 75= 77,7 балла) в группе высокой тревоги (p=0,006). Анализ результатов психического компонента здоровья МН также выявил наибольшие показатели в группе высокой тревоги при лечении с добавлением мексидола — 81,17 балла (V0, 25= 78,5 балла;У0, 75=84,3 балла) со значимыми различиями с подгруппой стандартной терапии (p=0,001).
В результате лечения у пациентов с высоким уровнем тревоги в большей степени произошло улучшение показателей общего уровня психологического здоровья (МН) со значимыми различиями с подгруппой стандартной терапии (p<0,05). По шкалам, характеризующим общий уровень физического здоровья (PH), в группе высокой тревоги отмечена положительная динамика (на 15%) с различиями между группами (p=0,006). В группе низкой тревоги на фоне комбинированного лечения с мексидолом через 12 нед отмечено улучшение по шкалам физического и психологического здоровья, но без статистически значимых различий с подгруппой стандартной терапии.
Заключение
Таким образом у больных ИБС со стенокардией II ФК определяются снижение всех показателей КЖ, симптомы личностной тревоги различной степени выраженности и прямая корреляция количества приступов стенокардии и высокого уровня тревоги (r=0,793; p=0,001).
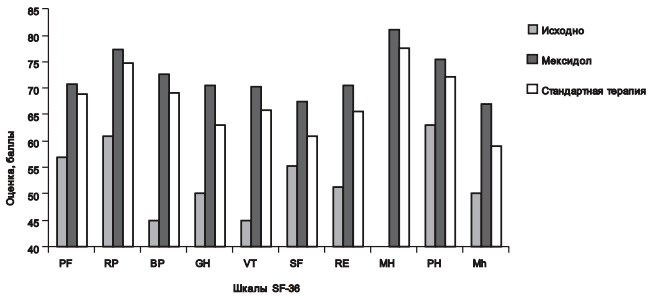
Динамика показателей качества жизни у пациентов с высокой тревогой.
Добавление мексидола к стандартной терапии у больных ИБС со стенокардией II ФК с высоким уровнем тревоги улучшает КЖ по шкале общего уровня здоровья (p<0,05), жизненной активности (p<0,05), шкалам психологического здоровья (p<0,05), шкале боли (p<0,05), снижает уровень тревоги (р<0,05).
Добавление мексидола к стандартной терапии у больных ИБС со стенокардией II ФК и высоким уровнем тревоги сопровождается снижением среднего САД и ДАД (р=0,0001), величины и скорости утреннего подъема АД (р<0,05), повышением показателей ВСР (р<0,05). Комбинация стандартной терапии с мексидолом у больных ИБС со стенокардией II ФК с высоким уровнем тревоги уменьшает ЧСС, количество наджелудочковых экстрасистол (p=0,002), количество пароксизмальных нарушений ритма (p=0,001), частоту приступов стенокардии (T=834,5; р=0,001), количество приемов короткодействующих нитратов (Т=897,5; р=0,0001).
Включение мексидола в стандартную терапию у больных ИБС со стенокардией II ФК позволяет существенно снизить обращаемость пациентов в лечебно-профилактические учреждения и временную нетрудоспособность (p<0,05).
ЛИТЕРАТУРА
1. Агеев Ф.Т. Сердечная недостаточность в Российской Федерации: новая эпидемия, угрожающая безопасности государства. Трудный пациент 2005; 10—11: 5—8.
2. Алешина Н.В. Опыт применения препарата Мексидол при фармакологическом лечении больных с разными клиническими формами неврозов. Бюл экпер биол 2006; 6—8: приложение 1.
3. Аронов Д.М. Первичная и вторичная профилактика сердечно-сосудистых заболеваний — интерполяция на Россию. Сердце 2002; 3: 109—112.
4. Аронов Д.М., Бубнова М.Г. Реальный путь снижения в России смертности от ишемической болезни сердца. КардиоСоматика 2010; 1: 11 — 17.
5. Беленков Ю.Н., Оганов Р.Г. Кардиология. Клинические рекомендации. М: ГЭОТАР-Медиа 2007; 640.
6. Белая О.Л., Байуер Л.М., Куропаева З.В., Фомина И.Г. Влияние Мексидола на антиоксидантный статус у больных ИБС. Клин мед 2005; 10: 58—60.
7. Березин Ф.Б., Безносюк Е.В., Соколова Е.Д. Психологические механизмы психосоматических заболеваний. Рос мед журн 1998; 2: 43—49.
8. Вершинина С.В. Акарачкова Е.С. Тревога в общей практике и ее лечение. РМЖ 2011; 18: 1161.
9. Воронина Т.А. Отечественный препарат нового поколения мексидол. М 2004; 21.
10. Всероссийское научное общество кардиологов. Диагностика и лечение стабильной стенокардии. Национальные клинические рекомендации Всероссийского научного общества кардиологов. М 2008; 503— 554.
11. Гацура В.В., Пичугин В.В., Сернов Л.Н., Смирнов Л.Д. Противоишемический кардиопротективный эффект Мексидола. Кардиология 1996; 11: 59—62.
12. Гиляревский С.Р. Косолапов Д.Л., Лопотовский П.Ю. и др. Стрессовая кардиомиопатия, или кардиомиопатия Takotsubo. Сердечная недостаточность 2010; 11: 59: 61: 306— 313.
13. Гланц С. Медико-биологическая статистика. Пер. с англ. М: Практика 1999; 459.
14. Далматов В.В. Применение методов математической статистики при проведении эпидемиологического анализа. Омск 2002.
15. Зайцев В.М., Лифляндский В.Г., Маринкин В.И. Прикладная медицинская статистика. СПб: Фолиант 2003; 432.
16. Зотов П.Б., Уманский М.С. Мексидол. Методические рекомендации/ депрессии в общемедицинской практике. М 2006; 26.
17. Карпов Ю.А. Лечение стабильной стенокардии: как предупредить осложнения и улучшить качество жизни. Consilium Medicum 2007; 11: 5—9.
18. Медведева Л.А. , Загорулько О.И., Гнездилов А.В. Мексидол в терапии пароксизмальных расстройств при вегетососудистой дистонии. М: Наука 2006; 23.
19. Метелица В.И. Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств. СПб: Бином 2002; 926.
20. Новик А.А., Ионова Т.И. Руководство по исследованию качества жизни в медицине. Под ред. Ю.Л. Шевченко. М: ОЛМА медиагрупп 2007; 320.
21. Оганов Р.Г. Масленникова Г.Я. Вклад сердечно-сосудистых заболеваний в здоровье населения России. Сердце 2003; 2: 58—61.
22. Павлов И.С. Мексидол в клинике пограничной психиатрии. М 2004; 21.
23. Петри А., Сэбин К. Наглядная статистика в медицине. Пер. с англ. В.П. Леонова. М: ГЭОТАР-МЕДИА 2003; 144.
24. Погосова Г.В. Современные подходы к лечению депрессий у больных с сердечнососудистыми заболеваниями. Фарматека 2003; 12: 75—79.
25. Погосова Н.В. Стресс у кардиологических больных. Клинические аспекты влияния на прогноз и тактика врача общей практики в коррекции стресса. Сердце 2007; 6: 6: 310—314.
Комментарии
ПРАКТИКА ПЕДИАТРА
