Оценка клинической эффективности, вазоактивного и метаболического эффектов мексидола у пациентов пожилого возраста с дисциркуляторной энцефалопатией
СтатьиОпубликовано в журнале:
«Неврологии и психиатрии», 11, 2011.
Ю.В. Абраменко
Кафедра нервных болезней факультета последипломного образования Тверской государственной медицинском академии; городская клиническая больница №7; поликлиника №1, Тверь
Обследованы 40 пациентов в возрасте от 55 до 74 лет с хронической ишемией головного мозга — дисциркуляторной энцефалопатией I—II стадии — на фоне артериальной гипертензии и атеросклероза. Больные были рандомизированы на 2 группы — основную и контрольную — по 20 человек в каждой. Пациенты основной группы получали антиоксидант мексидол внутримышечно по 100 мг в течение первых 10 дней, затем перорально по 125 мг 3 раза в день в течение 20 дней в сочетании с базисной терапией (диротон 5—20 мг в сутки, кардиомагнил 75 мг в сутки); пациенты контрольной группы получали в течение 30 дней только базисную терапию. До начала терапии, на 10-й и 30-й дни лечения оценивали эффективность мексидола по клиническим шкалам (выраженность жалоб, неврологического дефицита, когнитивных и эмоциональных нарушений), показателям церебральной гемодинамики по данным транскраниального дуплексного сканирования, лабораторным показателям состояния оксидантной и антиоксидантной систем (содержание в плазме крови малонового диальдегида и супероксиддисмутазы, общая антиокислительная активность плазмы). У пациентов, получавших мексидол, достоверно (р<0,05—0,01) по сравнению с показателями до начала лечения, а также с контрольной группой уменьшилась выраженность астенических и тревожных расстройств, улучшилось состояние статиколокомоторных и когнитивных функций. У получавших мексидол больных достоверно улучшились показатели церебральной гемодинамики за счет уменьшения периферического сосудистого сопротивления и нормализации венозного оттока из полости черепа. Прием мексидола достоверно снижал интенсивность перекисного окисления липидов и повышал общую антиокислительную активность крови. Полученные результаты позволяют рассматривать мексидол как эффективный препарат в комплексном лечении дисциркуляторной энцефалопатии у пациентов пожилого возраста.
Ключевые слова: хроническая ишемия мозга, дисциркуляторная энцефалопатия, антиоксиданты, нейропротекторы, мексидол.
The assessment of the clinical efficacy, vasoactive and metabolic effects of mexidol in elderly patients with discirculatory encephalopathy
YU.V. Abramenko
Forty patients, aged from 55 to 74 years, with chronic cerebral ischemia — discirculatory encephalopathy, stages I—II, against the background of arterial hypertension and atherosclerosis were studied. Patients were randomized into 2 equal groups. Patients of the main group received the antioxidant mexidol intramuscular in dose 100 mg during the first 10 days and then perorally in dose 125 mg three times a day during 20 days in the combination with the regular treatment (diroton in dose 5—20 mg daily, cardiomagnyl in dose 75 mg daily). Patients of the control group received regular treatment during 30 days. The efficacy was evaluated at baseline, on the 10th and 30th days after the treatment using clinical scales (the number of complaints, neurological deficit, cognitive and emotional disorders), parameters of cerebral hemodynamics measured with transcranial duplex scanning, laboratory indices of the state of oxidant and antioxidant systems (the content of malonic dialdehyde and superoxide dismutase in the blood plasma as well as the plasma total antioxidant activity). The statistically significant (p<0.05-0.01) reduction in the severity of asthenic and anxiety disorders, the improvement of static-locomotor and cognitive functions as well as of parameters of cerebral hemodynamics due to the decrease in the peripheral vascular resistance and the normalization of venous outflow from the cavity of scull was seen in patients treated with mexidol compared to the baseline and the control group. Mexidol significantly reduced the intensity of lipid peroxidation and increase the total antioxidant activity of the blood. The results obtained in the study allow to consider mexidol as the effective drug in the complex treatment of discirculatory encephalopathy in elderly patients.
Key words: chronic cerebral ischemia, discirculatory encephalopathy, antioxidants, neuroprotectors, mexidol.
Хроническая ишемия головного мозга, традиционно обозначаемая в нашей стране термином «дисциркуляторная энцефалопатия» (ДЭ) — длительно протекающая и неуклонно либо ступенеобразно (при развитии транзиторных ишемических атак и инсультов) нарастающая цереброваскулярная недостаточность. Ишемические инсульты у пожилых пациентов в большинстве случаев развиваются на фоне ДЭ и являются фактором, приводящим к нарастанию очаговых и диффузных ишемических или ишемически-дегенеративных изменений головного мозга, усугубляющих течение энцефалопатии и ускоряющих развитие у больных деменции [5, 10, 31]. ДЭ и ишемический инсульт, имеющие общую этиологию, патогенез и основные клинические проявления (двигательные, когнитивные и эмоциональные, в основном депрессивные, расстройства) с исходом в сосудистую или смешанную сосудисто-дегенеративную деменцию, в настоящее время считается возможным объединять в единый цереброваскулярный синдром [12].
Учитывая, что ДЭ является цереброваскулярным синдромом, а не самостоятельной нозологической формой, лечение больных должно быть прежде всего ориентировано на основные фоновые заболевания и факторы риска, которые являются общими для острых и хронических ишемических нарушений мозгового кровообращения. Наиболее эффективными мерами по замедлению дальнейшего прогрессирования заболевания и профилактике развития инсульта являются адекватная антигипертензивная терапия, коррекция дислипидемии, лечение кардиальной патологии и воздействие на модифицируемые факторы риска (избыточное потребление соли, курение, гиподинамия и др.) [10, 21]. Вместе с тем, исходя из современных представлений о патогенезе ДЭ, в комплексной терапии возможно также применение препаратов из других фармакологических групп, в частности нейропротекторов.
Суть нейропротекторной терапии — уменьшение объема поражения ткани головного мозга как при острых цереброваскулярных событиях, так и при хронической прогрессирующей энцефалопатии. Если при острой церебральной ишемии нейропротекция направлена на прерывание каскада патобиохимических реакций, приводящих к гибели клеток и формированию инфаркта, то при ДЭ целью нейропротекторной терапии является поддержание жизнедеятельности клеток мозга в условиях длительной гипоксии [3]. Уже при небольшой степени церебральной гипоксии нарушается работа дыхательной цепи митохондрий, развивается митохондриальная дисфункция, приводящая к энергодефициту (снижению синтеза АТФ) и оксидантному стрессу, т.е. к избыточному внутриклеточному накоплению свободных радикалов, активации процессов перекисного окисления липидов (ПОЛ) с избыточным накоплением его продуктов, что усугубляет перевозбуждение глутаматных рецепторов и усиливает глутаматные эксайтоксические эффекты [25, 37]. Ткань мозга особенно чувствительна к окислительному стрессу, так как чрезвычайно богата ненасыщенными липидами, входящими в состав мембранных фосфолипидов и являющимися основными субстратами свободнорадикального (перекисного) окисления [20]. Исходя из этого, важным направлением нейропротекции является терапия антиоксидантами, способными прерывать цепь реакций свободнорадикального ПОЛ или непосредственно разрушать молекулы перекисей [5, 24].
Применение антиоксидантов в настоящее время считается одним из перспективных методов неспецифической терапии хронических нарушений мозгового кровообращения [18]. Среди этой группы препаратов высокую эффективность в экспериментальных и клинических исследованиях показал отечественный препарат мексидол (2-этил-6-метил-3-гидроксипиридина сукцинат), представляющий собой по химической структуре соль янтарной кислоты. В условиях ишемии и гипоксии мексидол улучшает усвоение кислорода и усиливает аэробный гликолиз в мозговой ткани, подавляет свободнорадикальное окисление липидов клеточных мембран и повышает активность эндогенных антиоксидантных ферментов супероксиддисмутазы и церуллоплазмина, увеличивает концентрацию восстановленной формы глутатиона, предупреждает снижение активности глутатионзависимых ферментов. Мексидол способен оказывать положительное воздействие на церебральный метаболизм, а также нормализовать состояние микроциркуляции в первую очередь, за счет улучшения реологических свойств крови и снижения агрегации тромбоцитов [22, 24].
В настоящее время накоплен достаточно большой опыт применения мексидола в комплексной терапии хронической цереброваскулярной недостаточности [19, 20, 22, 26, 28]. Однако вопросы, связанные с применением препарата при ДЭ у больных пожилого возраста, остаются недостаточно изученными, что и определило целесообразность проведения настоящего исследования.
Цель исследования — оценка клинической эффективности, вазоактивного и метаболического эффектов мексидола у пациентов пожилого возраста на ранних стадиях ДЭ.
Материал и методы
В исследование включены 40 пациентов, 26 женщин и 14 мужчин, в возрасте от 55 до 74 лет (средний — 64,7±1,1 года) с ДЭ I—II стадии, обусловленной артериальной гипертензией или ее сочетанием с атеросклерозом.
Диагноз ДЭ и стадии заболевания устанавливали на основании принятых в нашей стране критериев [6]. Длительность заболевания варьировала от 2 до 8 лет, составляя в среднем 4,9±0,8 года.
Критериями включения больных в исследование были: среднее или высшее образование; наличие предшествовавшей исследованию стандартизованной лекарственной терапии; наличие информированного согласия на участие в исследовании. Критериями исключения являлись: энцефалопатия несосудистого генеза; тяжелые соматические, психические, эндокринные, гематологические, онкологические заболевания; васкулиты; деменция; перенесенные инсульты, черепно-мозговые травмы, инфекционные заболевания ЦНС; применение в течение последних 6 мес терапии, способной исказить результаты обследования (анксиолитики, антидепрессанты).
Больные ДЭ были рандомизированы методом конвертов на 2 группы по 20 человек в каждой. Пациенты основной группы, 14 женщин и 6 мужчин (средний возраст — 65,0±1,2 года), получали мексидол внутримышечно по 100 мг (2,0 мл 5% раствора) в течение первых 10 дней, затем перорально по 1 таблетке (125 мг) 3 раза в день в течение 20 дней. Также больным основной группы проводилась базисная терапия в следующем объеме: антигипертензивное лечение — диротон в дозе 5—20 мг в сутки, антиагреганты — кардиомагнил 75 мг в сутки. Пациенты контрольной группы, 12 женщин и 8 мужчин (средний возраст 64,3±1,0 года), получали в течение 30 дней лишь вышеуказанную базисную терапию. Исключался прием других вазоактивных и ноотропных препаратов.
Обследование пациентов обеих групп проводилось до начала терапии (1-й визит, включение в исследование), на 10-й (2-й визит, промежуточный контроль) и 30-й дни лечения (3-й визит, завершающий). Во время всех визитов проводился комплексный клинический осмотр пациентов, выяснялась переносимость препаратов, фиксировались любые побочные эффекты.
Динамику основных субъективных неврологических симптомов у пациентов с ДЭ оценивали по стандартизированной рейтинговой 5-балльной шкале: от 0 — нет нарушений до 4 — грубые нарушения [30]. Степень редукции объективных неврологических симптомов, в том числе нарушений равновесия, ходьбы и тонкой моторики, определяли по шкале NIH-NINDS, шкале двигательной активности M. Tinnetti [40] и методике М. Denckla [33]. Динамику когнитивных расстройств оценивали по суммарному баллу краткой шкалы оценки психического статуса (Mini Mental State Examination — MMSE) [35], отдельно определяли показатели памяти (субтест «память» по MMSE), внимания (проба Шульте) [1], беглости речи (субтест «беглость речи» батареи тестов лобной дисфункции — БТЛД, тест вербальных ассоциаций — литеральных и категориальных) [34, 36]. Уровень общей астении оценивали по шкале MFI-20 (Multidimensional Fatigue Inven-tiry), качество сна — по анкете федерального сомнологического центра [2]. Влияние препарата на эмоциональную сферу пациентов определяли по изменению показателей реактивной и личностной тревожности (шкала Спилбергера), а также депрессии (опросник Бека) [32, 39].
Для оценки влияния мексидола на церебральную гемодинамику у 15 больных основной и 12 пациентов контрольной группы проводили транскраниальное дуплексное сканирование (ТКДС) начальных сегментов средней мозговой артерии (СМА) на аппарате ACUSON Sequoia 512 («Siemens», Германия, датчик 10 МГц) с определением показателей, наиболее информативных для больных с хронической цереброваскулярной патологией — индексов пульсации (PI) и резистентности (IR), позволяющих судить о величине периферического сосудистого сопротивления (сопротивления мелких церебральных артерий и артериол, т.е. пиально-капиллярной сети головного мозга) [16]. Для оценки цереброваскулярной реактивности (ЦВР) исследовали кровоток по СМА в покое и при гиперкапнической пробе (произвольной задержке дыхания на 30—40 с) [13]. Исследуя динамику показателей интракраниального венозного кровотока, при ТКДС регистрировали среднюю линейную скорость кровотока (ЛСК) в среднем сегменте базальной вены (вены Розенталя) и прямом синусе.
Метаболические эффекты лечения оценивали по динамике показателей интенсивности ПОЛ, учитывая, что, с одной стороны, повышение уровня ПОЛ является отражением глубины метаболических расстройств у конкретного больного, а с другой — отражением нестабильности клеточных мембран [8, 14]. Количественную характеристику окислительного стресса в динамике до и после курса лечения осуществляли, определяя содержание в плазме крови пациентов одного из конечных продуктов ПОЛ — малонового диальдегида (МДА) тиобарбитуровым методом, содержание одного из ключевых антиоксидантных ферментов — супероксиддисмутазы (СОД) и общую антиокислительную активность (АОА) плазмы крови [7, 23].
Общая клиническая эффективность мексидола оценивалась на последнем визите по 9-ступенчатой шкале как: 1 — выздоровление, 2 — выраженное улучшение, 3 — умеренное улучшение, 4 — минимальное улучшение, 5 — без изменений, 6 — минимальное ухудшение, 7 — умеренное ухудшение, 8 — выраженное ухудшение, 9 — максимальное увеличение выраженности всех симптомов [36].
Статистический анализ проведен с помощью стандартного пакета программ SPSS 13.0. Использовали критерии t и χ2. Результаты считали достоверными при p<0,05.
Результаты и обсуждение
Клинические тесты
Все включенные в исследование пациенты его завершили. Установлено, что мексидол прежде всего положительно влиял на выраженность субъективных неврологических симптомов, отражающих наличие эмоциональных (раздражительность, чувство внутреннего напряжения и тревоги, пониженный фон настроения), в том числе астенических (повышенная утомляемость) нарушений. Достоверное уменьшение среднего рейтингового балла вышеуказанных жалоб наблюдалось уже на 10-й день лечения (р<0,05) и продолжало нарастать к 30-му дню исследования (р<0,01). Выраженность остальных субъективных симптомов, кроме головной боли, статистически значимо снижалась к окончанию курса лечения (р<0,01). Средний рейтинговый балл жалоб на раздражительность, чувство внутреннего напряжения и тревоги, пониженный фон настроения был достоверно меньше в основной группе по сравнению с контрольной на 10-й (р<0,05), а остальных субъективных симптомов — на 30-й день исследования (р<0,05—0,01). По отношению к такой частой при ДЭ жалобе, как головная боль, улучшение при лечении мексидолом оказалось статистически недостоверным (табл. 1).
Таблица 1.
Динамика субъективных неврологических симптомов у пациентов основной и контрольной групп (в баллах, М±m)
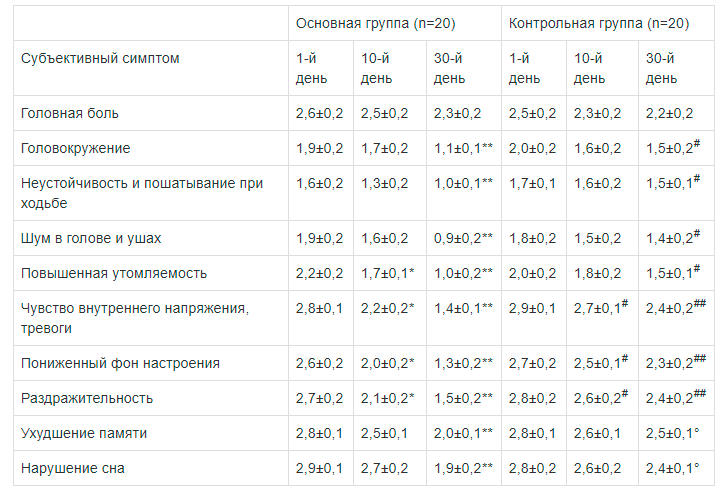 Примечание. Здесь и в табл. 2—8: * — р<0,05, ** — р<0,01 — достоверные различия показателя по сравнению с исходным; # — р<0,05, ## — р<0,01 — достоверные различия показателя основной и контрольной групп.
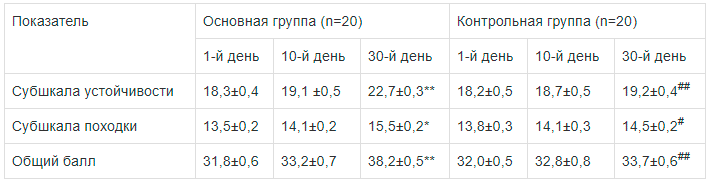
Примечание. Здесь и в табл. 2—8: * — р<0,05, ** — р<0,01 — достоверные различия показателя по сравнению с исходным; # — р<0,05, ## — р<0,01 — достоверные различия показателя основной и контрольной групп. По суммарному баллу шкалы NIH-NINDS достоверных различий в выраженности неврологической симптоматики у пациентов основной и контрольной групп как до начала лечения, так и после его завершения не получено. Вместе с тем на фоне терапии мексидолом на 30-й день у пациентов отмечена достоверная положительная динамика степени расстройств равновесия и ходьбы по шкале Tinnetti — от умеренно выраженной до легкой (р<0,05— 0,01), тогда как статико-локомоторные нарушения у пациентов контрольной группы при завершающем визите оставались почти на прежнем уровне (табл. 2).
Таблица 2.
Динамика нарушений равновесия и ходьбы по шкале Tinnetti у пациентов основной и контрольной групп (в баллах, М±т)
 По результатам исследования тонкой моторики и координации движений по методике Denckla у пациентов, принимавших мексидол, выявлена статистически значимая позитивная динамика при выполнении заданий на ходьбу и равновесие к окончанию курса лечения, у них достоверно (р<0,01) реже отмечались ошибки, использование вспомогательных движений рук и тенденция к падению. В контрольной группе пациентов достоверного улучшения данных показателей не отмечено. Больные основной группы лучше, чем пациенты группы контроля, справлялись с заданиями на чередование движений, при этом различия между группами обследованных были более отчетливыми на 30-й день исследования (р<0,01). Больные, получавшие мексидол, статистически значимо (р<0,01) быстрее и точнее пациентов контрольной группы выполняли задания на чередование движений как нижних, так и верхних правых конечностей на 30-й день исследования (табл. 3). Достоверных различий при выполнении проб для левых конечностей на данном материале не получено.
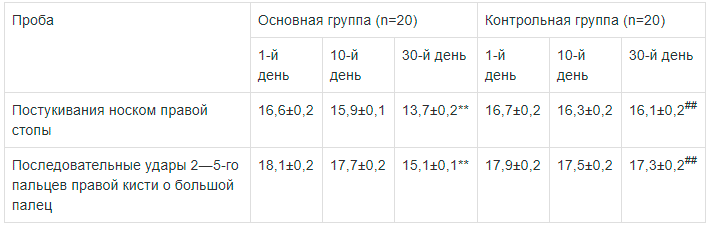
По результатам исследования тонкой моторики и координации движений по методике Denckla у пациентов, принимавших мексидол, выявлена статистически значимая позитивная динамика при выполнении заданий на ходьбу и равновесие к окончанию курса лечения, у них достоверно (р<0,01) реже отмечались ошибки, использование вспомогательных движений рук и тенденция к падению. В контрольной группе пациентов достоверного улучшения данных показателей не отмечено. Больные основной группы лучше, чем пациенты группы контроля, справлялись с заданиями на чередование движений, при этом различия между группами обследованных были более отчетливыми на 30-й день исследования (р<0,01). Больные, получавшие мексидол, статистически значимо (р<0,01) быстрее и точнее пациентов контрольной группы выполняли задания на чередование движений как нижних, так и верхних правых конечностей на 30-й день исследования (табл. 3). Достоверных различий при выполнении проб для левых конечностей на данном материале не получено. Таблица 3.
Динамика времени выполнения проб на тонкую моторику по методике Denckla у пациентов основной и контрольной групп (с, М±m)
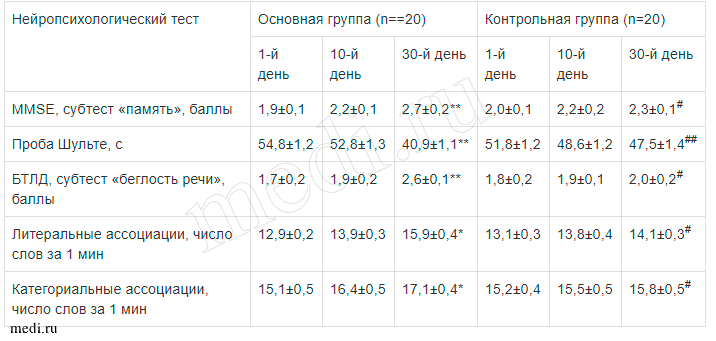
 По суммарному баллу MMSE достоверных изменений в выраженности когнитивных нарушений, а также различий между пациентами сравниваемых групп не выявлено. Вместе с тем отмечено положительное влияние терапии мексидолом на мнестические функции (кратковременная память) в виде статистически значимого улучшения результатов субтеста MMSE «память» на 30-й день исследования (р<0,01); пациенты основной группы к окончанию курса лечения демонстрировали существенно лучший результат по сравнению с пациентами контрольной группы (р<0,05). Положительное влияние препарата зафиксировано и в отношении нарушений нейродинамических функций мозга (способность к концентрации и поддержанию внимания, скорость образования ассоциаций и речевой продукции), которые развиваются уже на ранних стадиях ДЭ. У пациентов, принимавших мексидол, значительно улучшились показатели беглости речи и концентрации внимания на 30-й день лечения, в том числе и по сравнению с группой контроля (р<0,05—0,01) (табл. 4).
По суммарному баллу MMSE достоверных изменений в выраженности когнитивных нарушений, а также различий между пациентами сравниваемых групп не выявлено. Вместе с тем отмечено положительное влияние терапии мексидолом на мнестические функции (кратковременная память) в виде статистически значимого улучшения результатов субтеста MMSE «память» на 30-й день исследования (р<0,01); пациенты основной группы к окончанию курса лечения демонстрировали существенно лучший результат по сравнению с пациентами контрольной группы (р<0,05). Положительное влияние препарата зафиксировано и в отношении нарушений нейродинамических функций мозга (способность к концентрации и поддержанию внимания, скорость образования ассоциаций и речевой продукции), которые развиваются уже на ранних стадиях ДЭ. У пациентов, принимавших мексидол, значительно улучшились показатели беглости речи и концентрации внимания на 30-й день лечения, в том числе и по сравнению с группой контроля (р<0,05—0,01) (табл. 4). Таблица 4.
Динамика мнестических и нейродинамических функций у пациентов основной и контрольной групп (М±m)
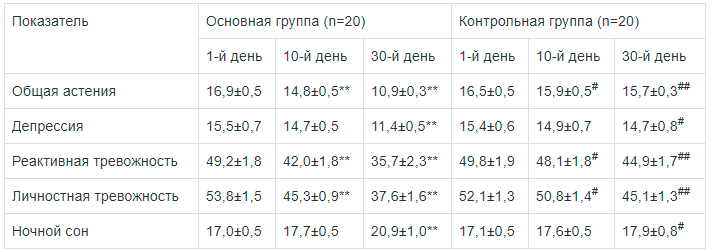
 Также зарегистрирован редуцирующий эффект мексидола на эмоциональные расстройства у больных ДЭ. У пациентов основной группы выявлено статистически значимое снижение уровней общей астении, реактивной и личностной тревожности как на 10-й, так и на 30-й день лечения, в том числе и по сравнению с контрольной группой (р<0,05—0,01). В то же время положительное влияние мексидола на уровень депрессии и качество сна у пациентов, его принимавших, достигало уровня достоверной значимости (р<0,05—0,01) только к окончанию курса лечения (табл. 5).
Также зарегистрирован редуцирующий эффект мексидола на эмоциональные расстройства у больных ДЭ. У пациентов основной группы выявлено статистически значимое снижение уровней общей астении, реактивной и личностной тревожности как на 10-й, так и на 30-й день лечения, в том числе и по сравнению с контрольной группой (р<0,05—0,01). В то же время положительное влияние мексидола на уровень депрессии и качество сна у пациентов, его принимавших, достигало уровня достоверной значимости (р<0,05—0,01) только к окончанию курса лечения (табл. 5). Таблица 5.
Динамика уровней общей астении, депрессии, тревожности и качества ночного сна у пациентов основной и контрольной групп (в баллах, М±m)
 Таким образом, при оценке клинической эффективности мексидола у пожилых пациентов с ДЭ установлено, что препарат оказывает наиболее выраженное действие на эмоциональные (в первую очередь — астенические и тревожные) нарушения. Более медленно на фоне лечения мексидолом регрессировали вестибуло-атактические и когнитивные (мнестические и нейродинамические) расстройства, что, в целом, согласуется с данными других исследователей [19, 20, 22, 26]. Избирательное действие препарата на субъективные и объективные неврологические симптомы ДЭ можно объяснить исходя из его фармакологических свойств. По направленности психотропного эффекта мексидол, производное 3-оксипиридинов, имеет сходство с транквилизаторами бензодиазепинового ряда, так как он модулирует рецепторные комплексы мембран мозга (в частности, ГАМК-бензодиазепиновый хлор-ионофорный комплекс) и усиливает их способность к связыванию с нейромедиаторами [4]. Ноотропное и церебропротекторное действие мексидола связано с блокированием синтеза простагландинов, влияющих на структурную лабильность нейрональных мембран, а также с повышением функциональной активности мембран с образованием устойчивых конформационных изменений и активацией синаптических процессов, что клинически проявляется улучшением когнитивных функций у пациентов с ДЭ [4, 22].
Таким образом, при оценке клинической эффективности мексидола у пожилых пациентов с ДЭ установлено, что препарат оказывает наиболее выраженное действие на эмоциональные (в первую очередь — астенические и тревожные) нарушения. Более медленно на фоне лечения мексидолом регрессировали вестибуло-атактические и когнитивные (мнестические и нейродинамические) расстройства, что, в целом, согласуется с данными других исследователей [19, 20, 22, 26]. Избирательное действие препарата на субъективные и объективные неврологические симптомы ДЭ можно объяснить исходя из его фармакологических свойств. По направленности психотропного эффекта мексидол, производное 3-оксипиридинов, имеет сходство с транквилизаторами бензодиазепинового ряда, так как он модулирует рецепторные комплексы мембран мозга (в частности, ГАМК-бензодиазепиновый хлор-ионофорный комплекс) и усиливает их способность к связыванию с нейромедиаторами [4]. Ноотропное и церебропротекторное действие мексидола связано с блокированием синтеза простагландинов, влияющих на структурную лабильность нейрональных мембран, а также с повышением функциональной активности мембран с образованием устойчивых конформационных изменений и активацией синаптических процессов, что клинически проявляется улучшением когнитивных функций у пациентов с ДЭ [4, 22]. Показатели церебральной гемодинамики
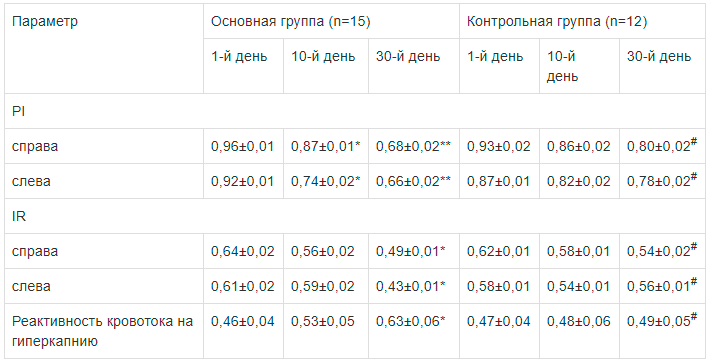
По данным ТКДС, достоверная (р<0,05) позитивная динамика PI в СМА у пациентов с ДЭ выявлена уже на 10-й день лечения мексидолом; к 30-му дню отмечалось дальнейшее снижение данного индекса (р< 0,01), что в свете данных литературы [16] указывало на улучшение микроциркуляции в веществе головного мозга за счет уменьшения величины периферического сосудистого сопротивления. Положительные изменения IR и коэффициента ЦВР в СМА в пробе на гиперкапнию достигали статистической значимости (р<0,05) к 30-му дню лечения (табл. 6).
Таблица 6.
Динамика индексов пульсации, резистентности и показателей цереброваскулярной реактивности в средней мозговой артерии у пациентов основной и контрольной групп (М±m)
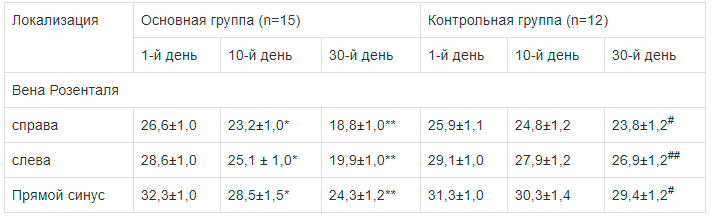
 Методом ТКДС установлено, что средняя ЛСК в среднем сегменте вены Розенталя и прямом синусе у пациентов с ДЭ обеих групп исходно превышала возрастную норму (соответственно 10 и 25 см/с), что в свете данных литературы [9, 29] указывало на наличие у них венозной церебральной дисциркуляции. На фоне лечения мексидолом данные показатели статистически значимо (р<0,05) снижались уже на 10-й день лечения; к 30-му дню отмечался их дальнейший регресс, в том числе и по сравнению с контрольной группой (р<0,05—0,01) (табл. 7), что свидетельствовало об улучшении венозного оттока из полости черепа под влиянием мексидола, которое отмечали и другие исследователи [15, 28].
Методом ТКДС установлено, что средняя ЛСК в среднем сегменте вены Розенталя и прямом синусе у пациентов с ДЭ обеих групп исходно превышала возрастную норму (соответственно 10 и 25 см/с), что в свете данных литературы [9, 29] указывало на наличие у них венозной церебральной дисциркуляции. На фоне лечения мексидолом данные показатели статистически значимо (р<0,05) снижались уже на 10-й день лечения; к 30-му дню отмечался их дальнейший регресс, в том числе и по сравнению с контрольной группой (р<0,05—0,01) (табл. 7), что свидетельствовало об улучшении венозного оттока из полости черепа под влиянием мексидола, которое отмечали и другие исследователи [15, 28]. Таблица 7.
Динамика показателей средней ЛСК в венах Розенталя и прямом синусе у пациентов основной и контрольной групп (см/с, М±m)
 В последние годы так называемая «нейроваскулярная единица» (функционально тесно связанные между собой нейроны, астроциты и сосудистые клетки) стала рассматриваться как одна из главных мишеней для терапевтического воздействия при ДЭ. Показано, что некоторые фармакологические препараты, в том числе, антиоксиданты, могут улучшать функциональное состояние нейроваскулярных единиц, повышая реактивность мелких сосудов и увеличивая перфузию активированных участков головного мозга [11]. Из приведенных результатов исследования следует, что мексидол способен нормализовывать состояние микроциркуляции. Вазоактивный эффект препарата связан в первую очередь с его модулирующим действием на систему кровь — сосудистая стенка за счет улучшения функции эндотелия и реологических свойств крови, а также ингибирования агрегации тромбоцитов [4, 17, 22, 24].
В последние годы так называемая «нейроваскулярная единица» (функционально тесно связанные между собой нейроны, астроциты и сосудистые клетки) стала рассматриваться как одна из главных мишеней для терапевтического воздействия при ДЭ. Показано, что некоторые фармакологические препараты, в том числе, антиоксиданты, могут улучшать функциональное состояние нейроваскулярных единиц, повышая реактивность мелких сосудов и увеличивая перфузию активированных участков головного мозга [11]. Из приведенных результатов исследования следует, что мексидол способен нормализовывать состояние микроциркуляции. Вазоактивный эффект препарата связан в первую очередь с его модулирующим действием на систему кровь — сосудистая стенка за счет улучшения функции эндотелия и реологических свойств крови, а также ингибирования агрегации тромбоцитов [4, 17, 22, 24]. Показатели состояния оксидантной и антиоксидантной систем
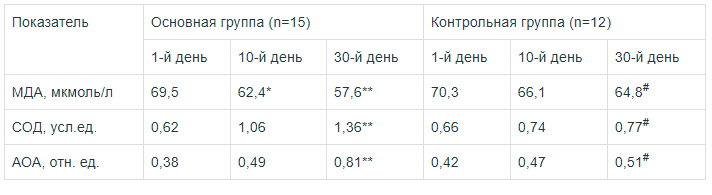
При исследовании динамики лабораторных показателей на фоне лечения мексидолом у больных основной группы в отличие от группы контроля, уже на 10-й день от начала приема препарата достоверно (p<0,05) уменьшалось содержание в крови одного из конечных продуктов ПОЛ — МДА на фоне тенденции к повышению содержания антиокислительного фермента СОД и общей АОА плазмы крови. После окончания курса лечения позитивные изменения показателей СОД и АОА плазмы крови достигли степени достоверности (р<0,01), в том числе и по сравнению с контрольной группой (р<0,05) (табл. 8).
Таблица 8.
Динамика показателей оксидантной и антиоксидантной систем у пациентов основной и контрольной групп (М±m)
 На основании полученных результатов можно заключить, что мексидол обладает положительным метаболическим действием у больных пожилого возраста с ДЭ со снижением активности оксидантной системы и активацией одного из ключевых ферментов антиоксидантной системы. Известно, что головной мозг даже здоровых пожилых людей обладает низкой резистентностью к ишемии и гипоксии, в том числе из-за возрастного дисбаланса оксидантной и антиоксидантной систем, а также снижения мозгового кровотока в процессе старения. В условиях церебральной ишемии и гипоксии происходит значительная активация цепи свободнорадикальных реакций на фоне ограниченного доступа через кровь антиоксидантов, в том числе, поступающих с пищей извне [38]. Выраженная активация свободнорадикальных процессов при относительной недостаточности эндогенных антиоксидантных систем является одним из ключевых патогенетических механизмов развития и прогрессирования хронических цереброваскулярных заболеваний, особенно у лиц пожилого возраста. Поэтому одним из актуальных подходов к лечению пожилых пациентов с ДЭ являются коррекция процессов свободнорадикального окисления и усиление антиоксидантной защитной системы организма [27], чего, как следует из данных проведенного исследования, вероятно, можно достигнуть и путем назначения мексидола.
На основании полученных результатов можно заключить, что мексидол обладает положительным метаболическим действием у больных пожилого возраста с ДЭ со снижением активности оксидантной системы и активацией одного из ключевых ферментов антиоксидантной системы. Известно, что головной мозг даже здоровых пожилых людей обладает низкой резистентностью к ишемии и гипоксии, в том числе из-за возрастного дисбаланса оксидантной и антиоксидантной систем, а также снижения мозгового кровотока в процессе старения. В условиях церебральной ишемии и гипоксии происходит значительная активация цепи свободнорадикальных реакций на фоне ограниченного доступа через кровь антиоксидантов, в том числе, поступающих с пищей извне [38]. Выраженная активация свободнорадикальных процессов при относительной недостаточности эндогенных антиоксидантных систем является одним из ключевых патогенетических механизмов развития и прогрессирования хронических цереброваскулярных заболеваний, особенно у лиц пожилого возраста. Поэтому одним из актуальных подходов к лечению пожилых пациентов с ДЭ являются коррекция процессов свободнорадикального окисления и усиление антиоксидантной защитной системы организма [27], чего, как следует из данных проведенного исследования, вероятно, можно достигнуть и путем назначения мексидола. Эффективность и безопасность лечения мексидолом
Средний показатель общей клинической эффективности мексидола в день завершения лечения составил 3,2± 0,5 балла, что соответствовало выраженному и умеренному улучшениям. В ходе исследования мексидол продемонстрировал высокую безопасность: за весь период наблюдения непереносимости препарата и каких-либо побочных явлений у больных не зафиксировано. Не отмечалось нежелательных взаимодействий мексидола с другими препаратами (гипотензивными и антиагрегантами) и клинически значимых изменений показателей артериального давления, частоты сердечных сокращений, температуры тела. Комплаентность к проводимой терапии у вошедших в исследование пациентов составила 100%.
На основании проведенного исследования можно заключить, что месячный курс лечения мексидолом у пациентов пожилого возраста с ДЭ приводит к уменьшению выраженности субъективных и объективных симптомов эмоциональных, особенно астенических и тревожных, расстройств, а также оказывает позитивное влияние на статико-локомоторные и когнитивные функции. У пожилых пациентов с ДЭ мексидол при курсовом применении улучшает церебральную гемодинамику, уменьшая периферическое сосудистое сопротивление и улучшая венозный отток из полости черепа. Мексидол обладает положительным метаболическим действием, снижая интенсивность ПОЛ и повышая общую антиокислительную активность крови, что наиболее актуально при лечении пациентов пожилого возраста, для которых характерно наличие выраженной активации свободнорадикальных процессов при относительной недостаточности эндогенных антиоксидантных систем. Полученные результаты позволяют рассматривать мексидол как эффективный препарат для терапии хронических форм цереброваскулярных заболеваний, особенно у лиц пожилого возраста.
Литература
1. Блейхер В.М., Крук И.В., Боков С.Н. Методики для исследования внимания и психомоторных реакций. Клиническая патопсихология. М 2002; 57-69.
2. Вейн А.М. и др. Депрессия в неврологической практике (клиника, диагностика, лечение). М: МИА 2002; 155.
3. Верткин А.Л., Дончинова А.А., Наумов А.В., Скорикова Ю.С. Система координат для выбора нейропротективной терапии. РМЖ 2007; 15: 16: 1211-1216.
4. Воронина Т.А., Смирнов Л.Д., Горяйнова И.И. Механизм действия и обоснование применения препарата мексидол в неврологии. М 2002; 14.
5. Гусев Е.И., Скворцова В.И. Хроническая ишемия мозга. М: Медицина 2003; 318.
6. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. Болезни нервной системы: Руководство для врачей: В 2 т. Т. 1. Под ред. Н.Н. Яхно, Д.Р. Штульмана. 2-е изд., перераб. и доп. М: Медицина 2001; 231-302.
7. Коробейникова Э.Н. Модификация определения продуктов перекисного окисления липидов в реакции с тиобарбитуровой кислотой. Лаб дело 1989; 7: 8-9.
8. Крыжановский Г.Н. Общая патофизиология нервной системы. М 1997; 352.
9. Лавров А.Ю., Яхно Н.Н., Бузиашвили Ю.И., Шумилина М.В. Характеристика артериальной и венозной церебральной гемодинамики на разных стадиях дисциркуляторной энцефалопатии. Приложение «Инсульт». Журн неврол и психиат 2005; 15: 4-12.
10. Левин О.С. Дисциркуляторная энцефалопатия: современные представления о механизмах развития и лечении. М: Сервье 2006; 24.
11. Левин О.С., Юнищенко Н.А. Диагностика и лечение когнитивных нарушений при дисциркуляторной энцефалопатии. Consilium Medicum 2008; 9: 8: 47-52.
12. Левин О.С. Диагностика и лечение деменции в клинической практике. МЕДпресс-информ 2010; 256.
13. Лелюк В.Г, Лелюк С.Э. Ультразвуковая ангиология. 2-е изд., дополн. и перераб. М: Реальное время 2003; 336.
14. Лещинский Л.Д. Обоснование и опыт применения ингибиторов перекисного окисления липидов (ПОЛ) у больных ишемической болезнью сердца. ТОП-медицина 1998; 4: 9-11.
15. Медведева Л.А., Загорулько О.И., Гнездилов А.В. Нейропротективная коррекция пароксизмальных расстройств при вегетососудистой дистонии. М 2006; 23.
16. Митьков В.В. Клиническое руководство по ультразвуковой диагностике. М 1999; 4: 211-212, 274.
17. Одинак М.М., Вознюк Н.А. Мексидол в лечении острой и хронической ишемии головного мозга. Вестн практич неврол 2003; 7: 21-26.
18. Румянцева С.А., Кравчук А.А., Силина Е.В. Антиоксиданты в терапии цереброваскулярных заболеваний. Лечащий врач 2006; 5: 42-47.
19. Семченко Л.Н., Дроздова Т.В., Зиновьева М.Н. Применение препарата мексидол для лечения больных с хронической цереброваскулярной недостаточностью с вестибулокохлеарными проявлениями. Приложение 1. Бюллетень экспериментальной биологии и медицины 2006; 75-78.
20. Смирнова И.Н., Федорова Т.Н., Танашян М.М., Суслина З.А. Клиническая эффективность и антиоксидантная активность мексидола при хронических цереброваскулярных заболеваниях. Атмосфера. Нервные болезни 2006; 1: 33-36.
21. Стаховская Л.В., Гудкова В.В. Место дисциркуляторной энцефалопатии в структуре цереброваскулярных заболеваний. Вопросы диагностики и лечения. Приложение к журналу Consilium medicum. Неврология 2009; 2: 28-34.
22. Суслина З.А., Смирнова И.Н., Танашян М.М. и др. Мексидол при хронических формах цереброваскулярных заболеваний. Лечение нервных болезней 2002; 3: 28-33.
23. Тупеев И.Р., Крыжановский Г.Н., Никушкин Е.В. и др. Антиоксидантная система в динамике комплексного лечения больных эпилепсией традиционными противосудорожными препаратами и антиоксидантом - альфа-токоферолом. Бюллетень экспериментальной биологии и медицины 1993; 10: 362-364.
24. Федин А.И. Оксидантный стресс и применение антиоксидантов в неврологии. Атмосфера. Нервные болезни 2002; 1: 15-18.
25. Федин А.И., Румянцева С.А. Интенсивная терапия ишемического инсульта. М: Мед книга 2004; 284.
26. Шалашова М.Л., Дудаева Н.Г., Головачева Т.В. Применение мексидола в комбинированной терапии с традиционными антигипертензивными средствами у больных артериальной гипертензией с признаками хронической церебрально-сосудистой недостаточности. Приложение 1. Бюллетень экспериментальной биологии и медицины 2006; 152-156.
27. Шанин Ю.Н. и др. Антиоксидантная терапия в клинической практике. Ст-Петербург: Изд-во ЭЛБИ 2003; 121.
28. Шетекаури С.А. Современные возможности антиоксидантной терапии и опыт лечения мексидолом хронической цереброваскулярной недостаточности. Приложение 1. Бюллетень экспериментальной биологии и медицины 2006; 156-159.
29. Шумилина М.В. и др. Дисбаланс венозного церебрального кровообращения в генезе энцефалопатии у больных с сердечно-сосудистыми заболеваниями. Анналы хир 2001; 4: 62-67.
30. Яхно Н.Н., Дамулин И.В., Захаров В.В. и др. Применение танакана при начальных стадиях сосудистой мозговой недостаточности: результаты открытого многоцентрового исследования. Неврологический журн 1998; 3: 6: 18-22.
31. Яхно Н.Н., Дамулин И.В., Захаров В.В. Дисциркуляторная энцефалопатия. М 2000; 32.
32. Beck А. Т. et al. An inventory for measuring depression. Arch Gen Psichiat 1961; 5: 561-571.
33. Denckla M.B. Revised neurological examination for subtle signs. Psychop-harm Bull 1985; 21: 773-789.
34. Dubois В., Slachevsky A., Litvan I., Pillon B. The FAB: a frontal assessment battery at bedside. Neurology 2000; 55: 1621-1626.
35. Foistein M.F., Filstein S.E., McHugh P.R. Mini-Mental State: a practical guide for grading the mental state of patients for the clinician. J Psychiat Res 1975; 12: 189-198.
36. Guy W., Bonato R. CGI - Clinical Global Impressions Manual for the EC-DEU Assessment Battery 2 Rev. National Institute of Menthal Health. Ed. Chevy Chase. Maryland 1976; 12: 1-6.
37. Lipton Р. Ischemic Cell Death in Brain Neurons. Physiological Reviews 1999; 79: 1431-1568.
38. Manno E.M., Atkinson J.L., Fulgham J.R. et al. Emerging medical and surgical management strategies in the evaluation and treatment of intracerebral hemorrhage. Mayo Clin Proc 2005; 80: 420-433.
39. Spilberger GD. et al. Manual for the State-Trait Anxiety Inventory. Palo Alto 1970; 38.
40. Tinnetti M.E. Performance-oriented assessment of mobility problems in elderly patients. J Am Geriat Soc 1986; 34: 119-126.
