Морфофункциональное обоснование применения Мексидола в лечении экспериментального острого панкреатита
СтатьиОпубликовано в журнале:
Электронный математический и медико-биологический журнал
Русская версия 2.0 - 1997 Том 3. Выпуск 3. 2000
Ю. В. Иванов, Н. А. Соловьев, С. М. Чудных, В. В. Яснецов
Научно-производственный центр “ГИДРОБИОС” Федерального Управления медико-биологических и экстремальных проблем при МЗ РФ (г. Москва).
Показано, что отечественный антиоксидантный препарат мексидол оказывает выраженное позитивное влияние на динамику морфофункциональных изменений в поджелудочной железе крыс при остром панкреатите. Однократное внутрибрюшинное введение мексидола в объеме 1 мл (100 мг/кг) крысам с острым панкреатитом предотвращает увеличение масштаба некроза ацинарной ткани, нагноение некротизированных долек, приводя их к склерозу и атрофии при сохранении больших зон неповрежденной паренхимы поджелудочной железы. Результаты настоящего исследования позволяют рекомендовать включение мексидола в комплексную терапию острого панкреатита.
В последнее десятилетие уходящего ХХ века в структуре смертности при острой хирургической патологии органов брюшной полости острый панкреатит (ОП) прочно занимает 1 место [2, 3]. Поэтому проблема успешного лечения ОП - приорететное направление научных изысканий большинства хирургических клиник.
Проводя широкий поиск новых средств терапии ОП, нами было обнаружено, что новый отечественный антиоксидантный препарат мексидол (производное группы 3-оксипиридина) оказывает эффективное влияние на течение и исход заболевания [5]. Это послужило основанием для дальнейшего изучения действия мексидола на поджелудочную железу (ПЖ) при ОП.
Цель работы: морфофункциональный анализ клеточной и тканевой реорганизации экзокринной части ПЖ при фармакотерапии мексидолом в ранние сроки экспериментального ОП.
Методика исследования
Опыты выполнены на 60 белых беспородных крысах самцах массой 250-300 г. ОП средней тяжести у крыс вызывали по методу [7] путем орошения ПЖ хлорэтилом. Операции проводили под гексеналовым наркозом (внутрибрюшинно 0,05-0,1 г/кг). Все оперированные животные были разделены поровну на 2 группы: крысам 1-й группы через 24 ч после воспроизведения ОП вводили однократно внутрибрюшинно мексидол в объеме 1 мл (100 мг/кг), а животным 2-й группы (контрольной) - изотонический раствор натрия хлорида в том же объеме.
Морфологические исследования* кусочков ткани ПЖ (после умерщвления животных под наркозом) проводили через 24 и 72 ч после введения мексидола. Для светооптической микроскопии парафиновые срезы из указанного материала окрашивали гематоксилином и эозином, метиленовым синим - азуром. Для электронной микроскопии кусочки ткани ПЖ фиксировали в 2,5% растворе глутаральдегида и постфиксировали в 1% растворе тетраоксида осмия. После обезвоживания в спиртах ткань заливали смесью эпоксидных смол - эпон 812 и аралдит. Ультратонкие срезы получали на ультратоме LKB-5, контрастировали в уранилацетате и цитрате свинца и исследовали в электронном микроскопе ЭМВ-100АК.
Результаты исследования
Светооптические и электронно-микроскопические исследования в группе контрольных животных показали этапный характер структурных изменений в ПЖ, свойственные течению ОП, что детально описано в литературе [1, 4, 6]. Так, например, в период от 24 до 72 ч эксперимента выявляется нарастание деструкции паренхиматозных элементов. Первоначальное и ведущее звенья патогенетического процесса – очаги микронекроза. Деструкция начинается с перефирии органа и распространяется вглубь по его междольковым и межклеточным пространствам, сопровождаясь резким отеком соединительной ткани. Характерным являются нарушения со стороны сосудов микроциркуляции - отек и деструкция эндотелиоцитов, разрыхление и разрушение базальных мембран, увеличение числа фенестр и пор. Нарастают паранекротические и деструктивные процессы в панкреоцитах в результате воздействия лизосомальных ферментов, гипоксии и секреторных продуктов, продуцируемых дискомплексированными концевыми отделами ПЖ. Мелкоочаговые изменения в железе имеют устойчивую тенденцию к генерализации к 72 ч опыта.
С помощью светооптической микроскопии выявлено, что через 24 ч после внутрибрюшинного введения мексидола крысам 1-й группы, имеются признаки распространенного внутридолькового отека с разобщением долек на мелкие фрагменты. В отечном междольковом и внутридольковом интерстиции четко определяются полнокровные сосуды, умеренно расширенные протоки и отсутствует воспалительная инфильтрация. В субкапсулярных отделах большей части долек на фоне их фрагментации выявляются дистрофические, очаговые некротические изменения ацинусов с миграцией сегментоядерных лейкоцитов в межацинарные пространства и цитоплазму отдельных ацинарных клеток. В части долек встречаются очаги завершенного некроза ацинусов с достаточно четкой границей зон повреждения, в виде узких переходных зон дискомплектации от неповрежденной ткани дольки (рис. А).
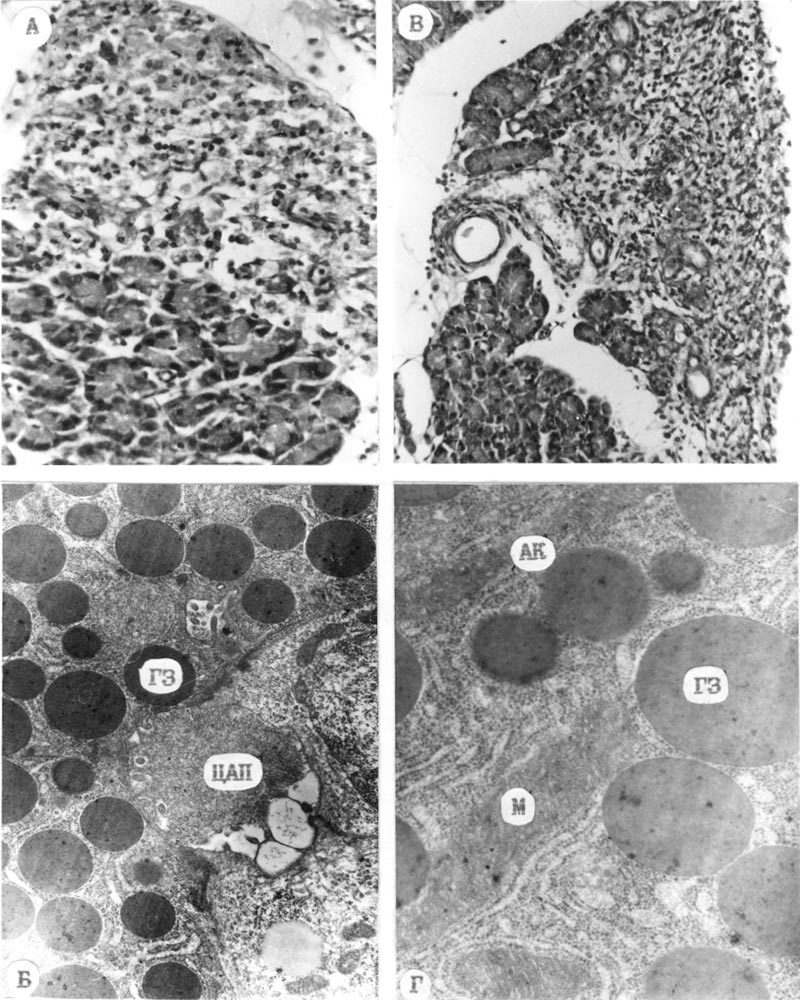
Светооптические (А, В) и электронно-микроскопические (Б, Г) изменения в поджелудочной железе крыс через 24 (А, Б) и 72 ч (В, Г) после внутрибрюшинного введения мексидола.
А - некроз ацинарной ткани дольки с умеренной воспалительной инфильтрацией. Б - копление зрелых гранул зимогена (ГЗ) вокруг центроацинозного протока (ЦАП), х 22000. В - атрофия ацинарной ткани дольки с протоковой трансформацией регенератов. Г – зрелые гранулы зимогена (ГЗ) и митохондрии (М) в цитоплазме ацинарной клетки (АК). А и В - окраска гематоксилином и эозином, х 400.
Особенностью зон некроза является сохранение жизнеспособных межацинарных капилляров и клеток соединительной ткани межацинарных пространств с минимальным воспалением. Междольковая субкапсулярная и перипанкреатическая жировая ткань характеризуется отсутствием крупномасштабных жировых некрозов. При этом признаки острого воспаления возникают вокруг жировых клеток и соединительно-тканных прослоек жировой клетчатки. Вне зоны повреждения ткани ПЖ в дольках прослеживаются правильно сформированные ацинусы с большим количеством секреторных гранул в апикальных и подъядерных отделах цитоплазмы.
Электронно-микроскопическое изучение ацинарных клеток интактных от повреждения зон показало отсутствие каких либо признаков повреждения плазматических и внутриклеточных мембран и сохранение способности к синтезу и выделению секрета в систему протоков. Околоядерные отделы цитоплазмы ацинарных клеток выполнены регулярно расположенными узкими цистернами гранулярной эндоплазматической сети с хорошо различимыми рибосомами на их мембранах. Крупные митохондрии имеют плотный матрикс и многочисленные кристы. Зрелые гранулы зимогена концентрируются вокруг центроацинозных протоков, просвет которых выполнен секретом (рис. Б). Уменьшение масштабов ферментативного некроза ацинарной и жировой ткани, сохранение синтеза ферментов, выделение секрета в просвет протоков, отсутствие дистрофических изменений в ацинарных клетках ПЖ указывает на стабилизацию клеточных мембран и отсутствие дальнейшего прогрессирования повреждений, характерных для острого панкреатита.
При светооптической микроскопии через 72 ч после внутрибрюшинного введения мексидола определяются умеренно выраженные междольковый и внутридольковый отек с разобщением долек на мелкиефрагменты. Воспалительные изменения в междольковом интерстиции отсутствуют. Отмечается полнокровие междольковых и внутридольковых вен с наличием периваскулярных воспалительных инфильтратов вокруг отдельных сосудов. В субкапсулярных краевых отделах долек отмечаются признаки атрофии ацинусов и замещение их ацинарно-протоковыми комплексами (рис. В). В прослойках соединительной ткани между ацинусами и трубчатыми структурами регенератов встречаются единичные лейкоциты, лимфоциты, макрофаги. В субкапсулярной жировой ткани крупномасштабных жировых некрозов не обнаружено. Кровеносные сосуды жировой клетчатки полнокровны с признаками периваскулярных воспалительных инфильтратов. Изучение полутонких срезов дольки выявило, что в ее краевых отделах имеются зоны регенерации поврежденной ткани с ацинарнопротоковой трансформацией. Эпителиальные клетки таких трубчатых структур не содержат в своей цитоплазме секреторных гранул. В зоне протоковой трансформации ацинарных клеток после их повреждения и между трубчатыми структурами имеются прослойки соединительной ткани, немногочисленные полнокровные капилляры. Воспалительные изменения в этих зонах регенерации отсутствуют. К очагам протоковой регенерации прилежат неповрежденные ацинусы с малым содержанием секреторных гранул в апикальных отделах цитоплазмы ацинарных клеток. В них отсутствуют дистрофические изменения, но видны крупные аутофагосомы.
Электронно-микроскопическое изучение зон ацинарных клеток на границе с ацинарно-протоковыми регенератами показало, что большие или маленькие отделы цитоплазмы жизнеспособных клеток заняты крупными аутофагосомами, отграниченными фокальными внутриклеточными некрозами. В цитоплазме ацинарных клеток, содержащих аутофагосомы, отмечается полная сохранность органелл - ядер, гранулярного ретикулума, митохондрий. В ацинарных клетках без признаков повреждения их органелл отмечается накопление зрелых гранул зимогена в апикальных отделах цитоплазмы (рис. Г). Митохондрии с многочисленными кристами подтверждают сохранение энергетического внутриклеточного обмена. Выявляются признаки активации процессов внутриклеточной регенерации, проявляющиеся гипертрофией митохондрий с гиперплазией их крист, умеренной дилятацией просвета цистерн гранулярной эндоплазматической сети с увеличением свободных полирибосом в цитоплазме, а также увеличением размеров ядрышек и краевой конденсацией ядерного хроматина.
Таким образом, однократное внутрибрюшинное введение мексидола животным с ОП предотвращает увеличение масштаба некрозов ацинарной паренхимы, которые не подвергаются нагноению, а атрофируются, претерпевая ацинарно-протоковую трансформацию с замещением соединительной тканью. Результаты настоящего исследования позволяют рекомендовать включение нового антиоксидантного препарата мексидола в комплексную терапию ОП.
* Авторы благодарят профессора Г. П. Титову за ценные советы и методическую помощь.
Литература
- Арабаджян К. П. Морфогенез экспериментального панкреонекроза. //Автореф. дис. ... канд. мед. наук. - Москва, 1983. - 24с.
- Брехов Е. И., Калинников В. В. //Кремлевская медицина. Клинический вестник. - 1998. - №4. - С. 52-55.
- Вафин А. З., Байчоров Э. Х., Гольтяпина И. А. и др. //Вестн. хирургии. - 1999. - №1. - С. 30-35.
- Гавриленко Г. А., Стадников А. А., Стадников Б. А. //Бюл. эксперим. биол. и медицины. - 1997. - №4. - С. 464-467.
- Мумладзе Р. Б., Чудных С. М., Васильев И.Т., Тувина Е. П. //Анналы хирургии. - 1997. - №1. - С. 67-70.
- Пермяков Н. К., Арабаджян К. П., Титова Г. П., Симаворян П. С. //Бюл. эксперим. биол. и медицины. - 1982. - №11. - С. 103-106.
- Симаворян П. С. //Пат. физиология и эксперим. терапия. - 1972. №3. - С. 69-72.
Morphofunctional justification of the use of mexidol in treatment of experimental acute pancreatitis
Y. V. Ivanov, N. A. Solovjov, S. M. Chudnych, V. V. Yasnetsov
It was shown that original domestic antioxidant Mexidol have prominent positive effect upon dynamics of morphofunctional changes in rat’s pancreas at the acute pacreatitis. Fore example, one introduction of Mexidol in volume of 1 ml (100 mg/ kg ) ito the peritoneum of rats with acute pancreatitis prevent increase in volume of necrosis in acinus tissue, prevent purification of lobular necrosis, leading to sclerosis and atrophy, at the same time keep intactive the large zone of pancreas tissue. The current study results give us a permission to recommend a Mexidol into the complex therapy of acute pancreatitis.
