Нейрометаболическая терапия как средство вторичной профилактики инсульта
СтатьиОпубликовано в журнале:
« Журнал неврологии и психиатрии » № 3, 2014
В.В. Ковальчук
СПб ГБУЗ Городская больница №38 им. Н.А. Семашко, Санкт-Петербург
Цель исследования - анализ эффективности препарата мексидол в отношении вторичной профилактики ишемического инсульта (ИИ).
Материал и методы. Проанализированы результаты лечения 3400 пациентов, перенесших ИИ, которые были разделены на 7 групп: пациенты с криптогенным ИИ, артериальной гипертензией, фибрилляцией предсердий, метаболическим синдромом, синдромом обструктивного апноэ/гипноэ сна, сахарным диабетом, васкулитами. Оценка эффективности терапии основывалась на отсутствии повторных ИИ в течение 5 лет терапии.
Результаты. Мексидол способствует уменьшению частоты повторных ИИ как у пациентов без сопутствующих патологических состояний, так и у больных с артериальной гипертензией, синдромом обструктивного апноэ/гипноэ сна, васкулитами, сахарным диабетом, фибрилляцией предсердий и метаболическим синдромом.
Заключение. Дальнейшие исследования эффективности применения мексидола в качестве средства вторичной профилактики ИИ представляются весьма перспективными.
Ключевые слова: инсульт, вторичная профилактика, мексидол.
Neurometabolic therapy in secondary prevention of stroke
V.V. Kovalchuck
Semashko City Hospital №38, St. Petersburg
Objective. To study the efficacy of mexidol in secondary prevention of stroke.
Material and methods: We analyzed 3400 patients with stroke which were stratified into 7 groups: patients with cryptogenic ischemic stroke (II), arterial hypertension, atrial fibrillation, metabolic syndrome, syndrome of sleep-induced obstructive apnea/hypnea, diabetes mellitus, vasculitis. The assessment of efficacy was based on the absence of repeated II within 5 years of therapy.
Results. Mexidol reduced the frequency of repeated II both in patients without concomitant diseases and in those with arterial hypertension, syndrome of sleep-induced obstructive apnea/hypnea, vasculitis, diabetes mellitus, atrial fibrillation and metabolic syndrome.
Conclusion. The reliable efficacy of mexidol in secondary prevention of stroke was found out.
Key words: stroke, secondary prevention, mexidol.
Инсульт остается важной медико-социальной проблемой современного общества, являясь одной из ведущих причин смертности и основной причиной стойкой инвалидизации [1-4]. Большой социально-экономический ущерб, возникающий вследствие инсульта, требует повышения эффективности профилактики как непосредственно инсультов, так и заболеваний, являющихся их причинами и факторами риска. Существенной медико-социальной проблемой являются повторные инсульты, которые приводят к летальным исходам в 1,5 раза чаще, чем первичные инсульты, и вызывают более выраженную инвалидизацию.
Доля повторных инсультов составляет от 5 до 31% всех сосудистых заболеваний головного мозга [5-8]. Вероятность возникновения повторного инсульта достигает 30%, превышая в 9 раз аналогичный показатель в популяции [9]. Распространенность повторного ишемического инсульта (ИИ) в течение 30 дней после перенесенного первичного ИИ достигает 7-8%, в течение 1-го года - от 6 до 20%, в течение 5 лет - 32% [8, 10-13]. Приведенные данные свидетельствуют о необходимости совершенствования системы вторичной профилактики инсультов, которая направлена на предотвращение развития повторных инсультов и базируется на принципах и методах первичной профилактики с более активной диспансеризацией.
Первичная профилактика осуществляется в рамках стратегии групп высокого риска и массовой стратегии. Стратегия групп высокого риска подразумевает выявление и лечение людей с особенно высоким риском развития инсульта. Выявление и адекватная терапия пациентов с артериальной гипертензией (АГ) и фибрилляцией предсердий (ФП) способствует снижению распространенности ИИ. Значительная часть ИИ возникает у лиц с умеренным и средним уровнем риска развития инсульта, поэтому концентрация профилактических усилий лишь на группах людей с высоким риском не увенчается ожидаемым успехом, поскольку вне поля зрения специалистов окажутся пациенты, например, с умеренной АГ. В связи с этим также необходимо использование массовой стратегии первичной профилактики ИИ. Данная стратегия предполагает незначительное снижение среднего артериального давления (АД) в популяции, но даже его снижение лишь на несколько мм рт. столба может оказать выраженное влияние на уменьшение заболеваемости ИИ в целом [14]. В снижении частоты и распространенности повторных ИИ существенную роль играет выявление и контролирование основных факторов риска ИИ, к которым прежде всего относятся АГ, атеросклероз, ФП, сахарный диабет (СД), васкулиты, коагулопатии и некоторые другие заболевания.
Учитывая основные патогенетические механизмы развития ИИ и прежде всего нарушения энергопродуцирующих процессов, которые оказывает негативное влияние на клетки головного мозга и способствуют развитию апоптоза, можно предполагать, что определенное значение для профилактики повторного ИИ имеет адекватное и своевременное использование препаратов метаболической защиты головного мозга, в первую очередь средств, обладающих энергокоррегирующими свойствами.
Цель настоящего исследования - изучение возможности повышения эффективности вторичной профилактики ИИ с применением препарата мексидол (этилметил-гидроксипиридина сукцинат).
Мексидол сочетает свойства энергокорректора и антиоксиданта, в значительной степени уменьшающего выраженность и последствия оксидантного стресса. Препарат способствует увеличению доставки клеткам и потребления ими сукцината, что в свою очередь приводит к стабилизации нейрональных мембран. Вызываемое им изменение функциональной активности мембран приводит к выраженному повышению активности мембраносвязанных ферментов, ионных каналов и рецепторных комплексов, в частности бензодиазепинового, ГАМК-рецепторного и ацетилхолинового, что также приводит к повышению их способности к связыванию с лигандами, увеличению активности нейромедиаторов и стимуляции синаптических процессов [15]. Мексидол активирует механизмы аэробного гликолиза, в результате чего повышается синтез АТФ, креатининфосфата [16]. Кроме того, при его применении улучшаются реологические свойства крови и антиагрегационная способность тромбоцитов. Важным свойством мексидола является его способность к нормализации липидного обмена, что проявляется в снижении концентрации общего холестерина, липопротеинов низкой и очень низкой плотности, триглицеридов и повышении концентрации липопротеинов высокой плотности [17].
Материал и методы
По дизайну настоящее исследование было проспективным сравнительным и открытым.
Анализу были подвергнуты результаты лечения 3400 пациентов, 1823 женщин и 1577 мужчин, перенесших ИИ. Их средний возраст составил 62,1 года (от 25 до 83 лет).
Все пациенты были разделены на две группы по 1700 человек (получавшие и не получавшие мексидол, соответственно основная группа и группа сравнения), которые были стандартизированы по принципу matched-controlled по таким показателям, как пол, возраст, степень выраженности неврологических и психоэмоциональных нарушений, уровень социально-бытовой адаптации, качество жизни, наличие сопутствующих заболеваний, а также применение различных препаратов, не относящихся к нейрометаболическим средствам (табл. 1).
Таблица 1. Стандартизация групп исследования
| Показатель | Основная группа | Группа сравнения | p | ||
| n | % | n | % | ||
| Пол | |||||
| женщины | 906 | 53,3 | 917 | 53,9 | 0,923 |
| мужчины | 794 | 46,7 | 783 | 46,1 | |
| Пациенты без выявленных патоморфологических причин инсульта | 47 | 2,8 | 47 | 2,8 | 1,000 |
| Сопутствующая патология | |||||
| депрессия | 498 | 29,3 | 539 | 31,7 | 0,703 |
| АГ без сопутствующей патологии | 415 | 24,4 | 415 | 24,4 | 1,000 |
| ФП | 170 | 10,0 | 170 | 10,0 | 1,000 |
| МС | 338 | 19,9 | 338 | 19,9 | 1,000 |
| синдром обструктивного апноэ/гипноэ сна | 257 | 15,1 | 257 | 15,1 | 1,000 |
| СД | 383 | 22,5 | 383 | 22,5 | 1,000 |
| васкулиты | 90 | 5,3 | 90 | 5,3 | 1,000 |
| Назначенная терапия | |||||
| антиаритмические препараты* | 170 | 10,0 | 170 | 10,0 | 1,000 |
| «синап»-терапия | 257 | 15,1 | 257 | 15,1 | 1,000 |
| инсулин | 114 | 6,7 | 88 | 5,2 | 0,812 |
| другие противодиабетические препараты** | 269 | 15,8 | 295 | 17,4 | 0,866 |
| вазоактивные препараты*** | 983 | 57,8 | 1022 | 60,1 | 0,754 |
| антиагрегаты и антикоагулянты**** | 1700 | 100,0 | 1700 | 100 | 1,000 |
| антидепрессанты и нейролептики***** | 498 | 29,3 | 539 | 31,7 | 0,703 |
| Возраст (средний) | 63,8 | 604 | 0,812 | ||
| Состояние неврологических функций (средний % от максимального восстановления) | 24,7 | 23,3 | 0,803 | ||
| Уровень социально-бытовой адаптации (средний % от максимального уровня) | 21,2 | 18,5 | 0,763 | ||
| Качество жизни (средний балл) | 78 | 80 | 0,854 | ||
Нарушение и восстановление неврологических функций определялись при помощи шкал Бартел [18], Линдмарка [19] и Скандинавской [20]. Уровень бытовой и социальной адаптации оценивали по шкале самооценки бытовых возможностей в повседневной жизни Мертон и Саттон [21]. Психоэмоциональное состояние определяли с помощью опросника Бека [22] и шкалы самооценки депрессии Уэйкфилда [23]. Качество жизни оценивали с помощью профиля влияния болезни (Sickness Impact Profile) [24].
Для проведения анализа эффективности вторичной профилактики все пациенты были разделены на семь групп: 1) пациенты без выявленных причин ИИ (94 человека); 2) пациенты с изолированной АГ (830); 3) пациенты с ФП (340); 4) пациенты с МС (676); 5) пациенты с синдромом обструктивного апноэ/гипноэ сна (514); 6) пациенты с СД (766); 7) пациенты с васкутатами: гигантоклеточный артериит, синдром антифосфолипидных антител (180).
В ряде случаев пациенты имели несколько возможных причин ИИ. Распределение подобных пациентов по экспериментальным группам осуществлялось следующим образом: сочетание ФП и любого другого заболевания - пациент относился к группе больных с ФП (190 человек); сочетание васкулита и любого другого заболевания кроме ФП - пациент относился к группе больных васкулитом [24]; сочетание СД и любого другого заболевания кроме ФП и васкулита - пациент относился к группе больных СД (420); сочетание синдрома обструктивного апноэ/гипноэ сна и МС - пациент относился к группе больных с синдромом обструктивного апноэ/гипноэ сна (335); сочетание МС и АГ - пациент относился к группе больных с МС (524); сочетание синдрома обструктивного апноэ/ гипноэ сна и АГ - пациент относился к группе больных с синдромом обструктивного апноэ/гипноэ сна (195).
Мексидол назначался на 1-, 6-, 12-м месяцах в течение 1-го года после перенесенного ИИ и в течение последующих 4 лет по 2 раза в год. Препарат вводился ежедневно внутривенно по 250 мг в течение 15 дней. Критериями включения пациентов в исследование были: ИИ подтвержденный нейровизуализационными методами (КТ или МРТ); для группы пациентов с ФП: наличие мягкой АГ (АД не превышает 160/100 мм рт.ст), умеренной АГ (АД достигает 180/110 мм рт.ст.) или тяжелой АГ (АД - до 220/120 мм рт.ст.) [18]); наличие АГ I, II или III стадии; для группы пациентов с ФП: наличие персистирующей, длительно персистирующей или постоянной форм ФП [25]; наличие нормосистолической, тахисистолической или брадисистолической форм ФП; для группы пациентов с МС - наличие 3 или более из следующих его критериев [26]: объем талии у женщин более 80 см, у мужчин - более 94 см; отношение объема талии к объему бедер - у женщин свыше 0,8, у мужчин - свыше 1,0; уровень триглицеридов в крови более 1,69 ммоль/л; уровень липопротеинов высокой плотности - у женщин менее 1,29 ммоль/л, у мужчин менее 1,04 ммоль/л; систолическое АД более 135 мм рт.ст. и/или диастолическое АД более 85 мм рт.ст; уровень глюкозы в крови натощак более 6,1 ммоль/л; для группы пациентов с синдромом обструктивного апноэ/гипноэ сна - индекс апноэ/гипноэ >5, сочетающийся с соответствующей клинической картиной [27]; для группы пациентов с СД - наличие СД 1 типа (инсулинозависимый сахарный диабет) или СД 2 типа (инсулиннезависимый сахарный диабет); для групп пациентов с васкулитами - гигантоклеточный артериит, подтвержденный результатами биопсии пораженных артерий с обнаружением гигантских клеток и инфильтрации сосудистой стенки мононуклеарными клетками; верификация синдрома антифосфолипидных антител на основании неоднократного повышения в сыворотке крови титра кардиолипиновых антител.
Оценка эффективности лечения основывалась на отсутствии повторных ИИ в течение 5 лет терапии.
Согласно положениям Хельсинкской декларации [28], пациенты имели возможность выйти из программы исследования в любое время. Исключенным из исследования считался больной, преждевременно окончивший участие в исследовании в связи с нежелательными явлениями или смертельным исходом, не связанным с повторным ИИ, а также пациент, прервавший участие по своему желанию. Число исключенных из исследования пациентов составило 119 человек (47 больных из основной группы, леченной мексидолом, и 82 пациента из контрольной группы) (табл. 2).
Таблица 2. Пациенты, исключенные из исследования и закончившие его
| Нозология | Основная группа | Группа сравнения | ||
| исключенные из исследования | закончившие исследование | исключенные из исследования | закончившие исследование | |
| Отсутствие патоморфологических причин ИИ | 0 | 47 | 0 | 47 |
| АГ | 11 | 404 | 15 | 400 |
| ФП | 26 | 144 | 38 | 132 |
| МС | 0 | 338 | 0 | 338 |
| Синдром обструктивного апноэ/гипноэ сна | 3 | 254 | 10 | 247 |
| СД | 7 | 376 | 19 | 364 |
| Васкулиты | 0 | 90 | 0 | 90 |
| Все группы | 47 | 1653 | 82 | 1618 |
Распределение (в %) перенесших повторный инсульт пациентов в группах с различными патоморфологическими причинами сосудистых заболеваний головного мозга в зависимости от применения мексидолa.
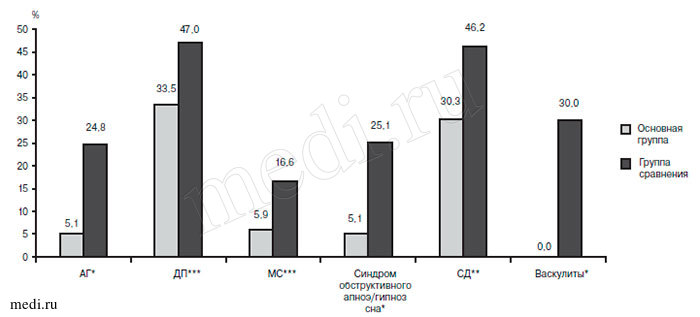
Различия, достоверные на уровне: * - p<0,0001; ** - p<0,001; *** - p<0,01; # - p<0,05.
Анализ результатов исследования проводился с использованием пакета программы SPSS 13.0. Для сравнения качественных признаков и процентных соотношений использовались критерий независимости качественных (категориальных) признаков χ2, точный критерий Фишера, а также коэффициент неопределенности. Наличие зависимости между изучаемыми признаками признавалось, когда доверительный уровень составлял p<0,05 (сравнение между числом пациентов, перенесших транзиторную ишемическую атаку или инсульт на фоне терапии, и числом пациентов, их не перенесших). При частоте изучаемого события менее 5 наблюдений в одной из ячеек таблицы использование критерия χ2признавалось некорректным и требовало использования точного критерия Фишера.
Результаты и обсуждение
Оказалось, что среди пациентов всех групп повторный ИИ в течение 5 лет развился у 13,4% (228) леченных мексидолом, а у не получавших его - у 29,7% (480) (р<0,001). Повторный ИИ среди пациентов с неуточненной причиной ИИ был зафиксирован у 2,1% (1) больных, получавших мексидол, и у 12,8% (6) его не получавших (р<0,05).
Повторный ИИ в течение 5 лет в группе пациентов с АГ без сопутствующей патологии наблюдался у 5,1% больных на фоне приема мексидола и у 24,8% больных, не получавших этот препарат (р<0,0001) (см. рисунок). Среди пациентов с ФП повторный ИИ в течение 5 лет развился у 33,5% получавших мексидол и у 47,0% не получавших его (р<0,05). Повторный инсульт развился у 5,9% пациентов с МС, леченных мексидолом, и у 16,6% не получавших препарат (р<0,01). У больных с синдромом обструктивного апноэ/гипноэ сна на фоне мексидола развился повторный ИИ в 5,1% случаев, и в 25,1% случаев без лечения мексидолом (р<0,0001). Повторный ИИ развился у 30,9% больных СД, получавших мексидол, и у 46,2% пациентов, не получавших его (р<0,001). Повторные ИИ не были зафиксированы ни у одного пациента с васкулитами, с гигантоклеточным артериитом и синдромом антифосфолипидных антител получавших мексидол, при этом ИИ развился у 30,0% пациентов, не получавших препарат (р<0,0001) (см. рисунок).
Таким образом, использование мексидола значительно повышает эффективность вторичной профилактики ИИ как у пациентов без установленной причины ИИ, так и у больных с АГ, ФП, МС, синдромом обструктивного апноэ/гипноэ сна, СД и васкулитами. Кроме того, результаты исследования свидетельствуют о том, что мексидол хорошо сочетается с другими лекарственными средствами в комплексной терапии пациентов с перечисленными заболеваниями. Применение мексидола оказалось наиболее эффективно в отношении вторичной профилактики ИИ у пациентов с синдромом обструктивного апноэ/гипноэ сна, васкулитами, особенно с АГ.
АГ является важным фактором риска сосудистых заболеваний головного мозга [29-31], приводя к выраженным структурно-функциональным изменениям мелких артерий и артериол мозга, что, в свою очередь, вызывает нарушение цереброваскулярной реактивности: снижается способность сосудов артериального русла к расширению при снижении АД и возрастает способность к сужению при его подъеме [32, 33]. Хроническая гипоксия белого вещества на фоне АГ приводит к распаду миелина и расширению периваскулярных пространств и гидроцефалии. В то же время, как показали результаты исследования, именно среди пациентов с АГ применение мексидола в наибольшей степени препятствует развитию повторных ИИ.
На основании проведенного исследования можно прийти к заключению, что применение мексидола препятствует развитию органических поражений головного мозга сосудистой природы. Использование препарата является оправданным для осуществления вторичной профилактики ИИ. Мексидол способствует уменьшению частоты повторных ИИ неуточненного генеза, а также у больных с АГ, синдромом обструктивного апноэ/гипноэ сна, васкулитами, СД, ФП и МС. Учитывая актуальность проблемы ИИ и небольшое число исследований эффективности препаратов метаболической защиты головного мозга как средства его профилактики, можно отметить, что дальнейшие исследования в данной области представляются весьма перспективными.
ЛИТЕРАТУРА
- Гусев Е.И., Скворцова В.И., Стаховская Л.В. Проблема инсульта в Российской Федерации: время активных совместных действий. Журн неврол и психиат 2007; 8: 4-10.
- Иванова Г.Е., Шкловский В.М., Петрова Е.А. и др. Принципы организации ранней реабилитации больных с инсультом. Качество жизни. Медицина 2006; 2: 13: 62-70.
- Скворцова В.И., Евзельман М.А. Ишемический инсульт. Орел 2006; 404.
- Суслина З.А., Варакин Ю.Я. Эпидемиологические аспекты изучения инсульта. Время подводить итоги. Анналы клинической и экспериментальной неврологии 2007; 1: 2: 22-28.
- Виленский Б.С. Инсульт. СПб: Мед информ агентст 1995; 287.
- Виничук С.М. Профилактика и реабилитация мозговых инсультов. Медицина 1996; 3: 19-23.
- Rundek Т., Mast H., Hartmann A. etal. Predictors of resource use after acute hospitalization. The Northern Manhattan Stroke Study. Neurology 2000; 55: 1180-1187.
- Sacco R.L., Wolf P.A., Gorelick P.B. Risk factors and their management for stroke prevention: outlook for 1999 and beyond. Neurology 1999; 53: Suppl 4: 15-24.
- Fujishige K., Kotera 1., Michibata II. et al. Cloning and characterization of a novel human phosphodiesterase that hydrolyzes both с A MP and cGMP (PDE 10Л). 1 Biol Chem 1999; 274: 18438-18445.
- Одинак М.М., Михайленко А.А., Иванов Ю.С., Семин Г.Ф. Сосудистые заболевания головного мозга. СПб: Гиппократ 1997; 160.
- Acheston I., Danta G, Hutchinson E.C. Controlled trial of dipyridamole in cerebral vascular disease. Br Med J 1996; 1: 614-616.
- Sacco R.L., Benjamin E.J., Broderick J.P. et al. ANA conference proceedings. Risk factors. Stroke 1997; 28: 7: 1507-1517.
- Sandercock P., Tangkanakul C. Very early of stroke recurrence. Cerebrovasc Dis 1997; 7: Suppl 1: 10-15.
- Warlow C.P., Dennis M.S., van Gijn J. et al. Stroke. A practical guide to management. London: Blackwell Science 1997; 664.
- Воронина Т.А. Антиоксидант мексидол. Основные нейропсихотропные эффекты и механизм действия. Психофармакология, биология, наркология 2001; 1: 2-12.
- Афанасьев В.В. Руководство по неотложной токсикологии. Краснодар: Просвещение-Юг 2012; 576.
- Ковальчук В.В. Медико-социальная реабилитация пациентов после инсульта: Практическое руководство. СПб-М 2013; 87.
- Machoney F, Barthel D. Functional evalution: the Barthel Index. Md State Med J 1965; 14: 61-65.
- Lindmark B. Evaluation of functional capacity after stroke with special emphasis on motor function and activities of daily living. Scand J Rehabil Med 1988; 21: 1-40.
- Scandinavian Stroke Study Group. Multicenter trial of hemodilution in ischemic stroke: background and study protocol. Stroke 1985; 16: 885-890.
- Kwantabisa N. Occupational therapy ADL checklist self maintenance. Merton and Sutton Community NHS Trust. Stroke Rehabilitation Team Protocol. London 1999; 7-9.
- House A., Dennis M., Hawton K. et al. Methods of identifying mood disorders in stroke patients: experience in the Oxfordshire Community Stroke Project. Age Ageing 1989; 21: 371-379.
- Hickie I., Lloyd A., Wakefield D. et al. The psychiatric status of patients with the chronic fatigue syndrome. Br J Psychiatry 1990; 156: 534-540.
- Bergner M., Bobbitt R.A., Carter W.B. et al. The Sickness Impact Profile: development and final revision of a health status measure. Med Care 1981; 19: 787-805.
- Camm A.J., P. Kirchhof, Gregory Y.H.L. et al. Guidelines for the management of atrial fibrillation. European Heart Journal 2010; 31: 2369-2429.
- Маколкин В.И. Метаболический синдром. М: МИА 2010; 144.
- Clinical Guideline for the Evaluation, Management and Long-term Care of Obstructive Sleep Apnea in Adults. J Clin Sleep Med 2009; 5: 263-276.
- World Medical Association. Declaration of Helsinki - ethical principles for medical research involving human subjects (DoH/0ct2008). Retrieved December 7, 2010, from: wma.net/en/30publications/10policies b3/index.html
- Гусев Е.И., Мартынов М.Ю., Ясаманова А.Н. и др. Этиологические факторы и факторы риска хронической сосудистой мозговой недостаточности и ишемического инсульта. Инсульт 2001; 1: 41-45.
- Парфенов В.А., Вербицкая С.В. Профилактика инсульта на основе снижения артериального давления и исследование POWER. Неврология. Нейропсихиатрия. Психосоматика 2013; 1: 64-68.
- Keli S., Bloemberg B., Kromhout D. Predictive value of repeated systolic blood pressure measurments for stroke risk: the Zutphen Study. Stroke 1992; 23: 347-351.
- Алмазов В.А., Арабидзе Г.Г., Белоусов Ю.Б. и др. Профилактика, диагностика и лечение первичной артериальной гипертонии в Российской Федерации. Клиническая фармакология и терапия 2000; 9: 1: 5-30.
- WHO-ISH Hypertension guidelines Committee, 1999. - World Heath Organization - International Society of Hypertension guidelines for the Management of Hypertension. J Hypertens 1999; 17: 151-185.
