Основные патогенетические механизмы развития сосудистой патологии мозга при атеросклерозе и метаболическом синдроме: поиск путей коррекции
СтатьиОпубликовано в журнале:
«Клиническая неврология» Том 10, №2, 2016.
М.М. Танашян, О.В. Лагода, К.В. Антонова, А.А. Раскуражев
ФГБНУ«Научный центр неврологии» (Москва)
Метаболический синдром (МС) является фактором риска возникновения острых и хронических сосудистых заболеваний мозга. Развивающийся в этих условиях окислительный стресс способствует прогрессированию атеросклеротического поражения брахиоцефальных артерий, что делает необходимым коррекцию выявленных патобиохимических нарушений. Применение препаратов антиоксидантного действия у больных с цереброваскулярными заболеваниями и МС способствует уменьшению таких проявлений последнего, как инсулинорезистентность, гипертриглицеридемия, гипергликемия. В статье представлены результаты исследований препарата мексидол у больных с хроническими цереброваскулярными заболеваниями на фоне атеросклероза и МС, демонстрирующие хорошие перспективы применения лекарственных соединений этой группы с целью комплексной коррекции различных звеньев патогенеза развивающейся патологии.
Ключевые слова: ишемические цереброваскулярные заболевания, метаболический синдром, антиоксидантная терапия, мексидол.
The main pathogenetic mechanisms of vascular cerebral pathology associated with atherosclerosis and metabolic syndrome: the search for correction approaches
M.M. Tanashyan, O.V. Lagoda, K.V. Antonova, A.A. Raskurazhev
Research Center of Neurology, Moscow, Russia
Keywords: ischemic cerebrovascular diseases, metabolic syndrome, antioxidant therapy, mexidol.
Metabolic syndrome (MS) is a risk factor for the development of acute and chronic vascular diseases of the brain. Oxidative stress developing under these conditions promotes the progression of atherosclerotic disease of the brachiocephalic arteries, which necessitates correction of the identified pathobiochemical abnormalities. The use of antioxidant drugs in patients with cerebrovascular diseases and MS reduces manifestations of the latter, including insulin resistance, hypertriglyceridemia, and hyperglycemia. The article presents the results of investigation of the drug mexidol in patients with chronic cerebrovascular diseases associated with atherosclerosis and MS. The findings demonstrate that drugs of this group have good prospects to be used for comprehensive correction of various pathogenic stages of the developing pathology.
Сердечно-сосудистые заболевания и, прежде всего, сосудистые заболевания головного мозга (или цереброваскулярные заболевания - ЦВЗ) как ведущая причина смерти населения являются глобальной проблемой современного здравоохранения. Несмотря на то, что стандартизированные по возрасту показатели смертности в результате инсульта за последние 20 лет снизились во всем мире, абсолютные показатели ежегодного числа инсультов, числа пациентов, выживших после инсульта, и связанных с инсультом смертельных случаев, а также общий показатель глобального бремени инсульта остаются очень высокими и продолжают увеличиваться [3, 12]. Достижения ангионеврологии позволили достичь определенных успехов в лечении ургентных форм сосудистой патологии мозга, что наряду с увеличением продолжительности жизни способствовало росту в общей популяции лиц с различными проявлениями хронических ЦВЗ (ХЦВЗ).
Важнейшей причиной ЦВЗ признается атеросклероз и его осложнения - атеростеноз, атеротромбоз, атеротромбоэмболия, обусловливающие развитие до 80% всей сосудистой патологии головного мозга [5]. Многогранность патогенетических механизмов развития и прогрессирования церебрального атеросклероза диктует необходимость изучения различных аспектов этой проблемы - от структурно-морфологических изменений сосудов и вещества мозга до различных характеристик крови (биохимических, реологических, провоспалительных и др.).
В большом числе исследований показано, что увеличение содержания в крови провоспалительных факторов способствует развитию атеросклеротического повреждения сосудистой стенки и прогрессированию ишемии мозга, полиморфизм генов, кодирующих молекулы воспаления, сопряжен с развитием ишемического инсульта. Так, результаты исследования Go-DARTS свидетельствуют, что различные полиморфизмы генов, кодирующих интерлейкин-6 (IL-6), молекулы межклеточной адгезии-1 (ICAM-1), селектин-Е (sel-E) и матриксную протеиназу-3 (MMP-3), ассоциированы с развитием ишемического инсульта [19].
При рассмотрении действия различных воспалительных молекул можно с определенной степенью условности разделить их на биомаркеры с про- и антиатерогенным (ангиопротективным) действием (табл. 1).
Таблица 1:
Биомаркеры атерогенеза.
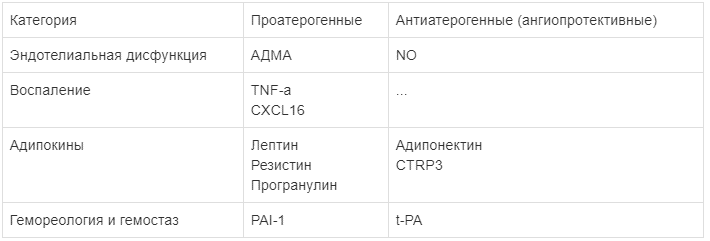 Примечание: АДМА - асимметричный диметиларгинин; NO - оксид азота; TNF-a - фактор некроза опухоли-a; CXCL16 - хемокины L16; CTRP3 - CT-подобный белок; PAI-1 - ингибитор активатора плазминогена; t-PA - тканевой активатор плазминогена.
Примечание: АДМА - асимметричный диметиларгинин; NO - оксид азота; TNF-a - фактор некроза опухоли-a; CXCL16 - хемокины L16; CTRP3 - CT-подобный белок; PAI-1 - ингибитор активатора плазминогена; t-PA - тканевой активатор плазминогена. Увеличение концентрации АДМА с последующим снижением образования NO предлагалось некоторыми исследователями в качестве одной из ведущих причин развития и прогрессирования атеросклероза [23]. Продемонстрировано сочетание высоких концентраций АДМА с другими факторами риска прогрессирования атеросклероза, которые являются составными частями МС: гиперхолестеринемией, артериальной гипертонией, гипертриглицеридемией, сахарным диабетом, инсулинорезистентностью, гипергомоцистеинемией [9, 11]. В исследовании Н. Miyazaki et al. (1999) методом пошагового регрессионного анализа была показана статистически значимая корреляция уровня АДМА и толщины комплекса интима-медиа сонных артерий, являющегося важным суррогатным маркером для определения риска развития сердечнососудистых событий [16]. АДМА влияет и на экспрессию генов, отвечающих за пролиферацию и рост эндотелиальных и гладкомышечных клеток [21]. Опосредованно АДМА запускает каскад реакций, сопровождающихся образованием реактивных форм кислорода, активацией толл-подобного рецептора 4 (TLR4) и усилением образования провоспалительных цитокинов (в частности, IL-6) [22]. У пациентов с атеросклерозом коронарных артерий выявлены более высокие уровни АДМА, чем у здоровых пациентов, а у лиц с нестабильной стенокардией активность этого соединения выше, чем у пациентов со стабильной формой коронарной недостаточности. Указанные факты свидетельствуют об АДМА как о потенциально проатерогенном факторе.
К формированию нестабильной атеросклеротической бляшки предрасполагает и низкая экспрессия рецепторов к адипонектину 1-го типа (ADR-1), что вкупе с гипоадипонектинемией, изначально имеющейся у пациентов высокого риска, может приводить к «озлокачествлению» атеросклероза с развитием цереброваскулярных катастроф. Также было показано, что хроническое повышение IL-6 ведет к ускоренному прогрессированию каротидного атеросклероза [18].
В наших собственных исследованиях было продемонстрировано значимое снижение активности NO у пациентов с выраженным атеросклерозом брахиоцефальных артерий, что может свидетельствовать об истощении антиатерогенного потенциала сосудистой стенки. Получены данные, свидетельствующие о том, что t-PA выступает как атеропротективный биомаркер атерогенеза, уровень которого значимо снижается у пациентов с выраженным атеросклерозом брахиоцефальных артерий. Статистически значимых различий в содержании изученных маркеров в крови в зависимости от пола получено не было (р=0,21 для t-PA и р=0,57 для PAI-1), однако у лиц мужского пола выявлена обратная зависимость содержания PAI-1 от активности NO (R= -0,33). В женской популяции такой корреляции не прослеживалось, что может косвенно подтверждать выявленную ранее в многочисленных исследованиях протективную роль гормонального фона в отношении развития и прогрессирования атеросклеротического процесса [8].
Среди биомаркеров воспаления, тесно ассоциированного с развитием атеросклероза, наибольшей специфичностью в отношении церебрального атеросклероза обладает липопротеид-ассоциированная фосфолипаза А2 (Lp-PLA2). Lp-PLA2 синтезируется макрофагами в атеросклеротических бляшках (АСБ), особенно интенсивно в бляшках сонных артерий, а затем через повреждения в покрышке атеромы проникает в общий кровоток, где связывается с циркулирующими в плазме атерогенными частицами липопротеидов низкой плотности. Установлена связь повышения массы и активности Lp-PLА2 с риском развития кардиоцеребральных событий [7].
При анализе взаимосвязи между строением АСБ (по данным дуплексного сканирования и исследования удаленных биоптатов) и биохимическими маркерами было установлено, что у пациентов с инсультом на фоне нестабильных АСБ уровень Lp-PLA2 был выше, чем в группе со стабильными АСБ - 348,27±54,56 нг/мл и 303,83±52,31 нг/мл соответственно (р=0,04) (рис. 1). Кроме того, при развитии острого цереброваскулярного эпизода у больных с нестабильными АСБ в крови достоверно выше содержание фибриногена и глюкозы.
 Рис. 1: Сопоставление структуры АСБ и ряда биохимических показателей у пациентов с атеросклерозом.
Рис. 1: Сопоставление структуры АСБ и ряда биохимических показателей у пациентов с атеросклерозом.
Широкое распространение МС в популяции способствует прогрессированию атеросклеротического поражения головного мозга. Ассоциация атерогенных эффектов основных компонентов МС - гиперинсулинемии, артериальной гипертонии, дислипидемии и ожирения - на фоне дизрегуляции системы гемостаза и гемореологии существенно увеличивает риск возникновения различных проявлений ЦВЗ, причем каждый из компонентов МС вносит вклад в развитие и прогрессирование ЦВЗ. Спровоцированные и/или усугубленные МС морфологические и функциональные изменения сосудов, сердца, крови определяют характер и возникновение острой и декомпенсацию хронической цереброваскулярной патологии. В проспективном исследовании, оценивающем влияние компонентов МС на риск развития инсульта, было показано, что артериальная гипертензия (АГ) и сахарный диабет 2 типа (СД2) независимо повышают возможность развития инсульта, а их сочетание сопровождается резким возрастанием этого риска [13].
Механизмы тесной связи между МС и атеросклерозом пока окончательно не определены. Некоторые авторы указывают на то, что атеросклероз, развивающийся в условиях метаболических нарушений, является результатом процессов, происходящих при недиабетическом атеросклерозе, но ускоренных, усиленных и протекающих более агрессивно. Так, у пациентов с СД2 повышено содержание в крови адгезивных молекул, оксидативных субстанций, цитокинов. Нарушения системы гемореологии и гемостаза, эндотелиальная дисфункция, возникающие на фоне МС, взаимно усиливают друг друга, что при отсутствии должной коррекции модифицируемых факторов риска МС приводит к необратимым последствиям - развитию субклинических ишемических поражений мозга и сосудистым катастрофам в виде острых ишемических и геморрагических нарушений мозгового кровообращения (НМК) [4, 10].
Метаболические нарушения приводят к формированию метаболического повреждения вещества мозга и играют роль в поражения его сосудов, причем иногда эти процессы независимы друг от друга. При МС в процесс вовлекаются сосуды разного калибра - изменения отмечаются как на макро-, так и на микрососудистом уровне. Наличие МС в 5 раз увеличивает вероятность раннего атеросклеротического поражения сонных артерий по сравнению с пациентами без каких-либо метаболических нарушений, причем возрастание риска развития этих изменений связывают с гиперинсулинемией и уровнем липопротеидов низкой плотности (ЛПНП) [14].
У лиц с МС на 36% увеличен риск возникновения и прогрессирования АСБ в сонных артериях, а также их большего объема [20]. Для больных с МС характерно комбинированное поражение артериальных бассейнов, диффузное (многосегментарное) поражение артерий, дистальное атеросклеротическое поражение сосудов, с большей кальцификацией сосудов и меньшим развитием коллатералей. По данным ультразвукового исследования, у больных с МС отмечается большая распространенность атеросклеротических поражений с неадекватным компенсаторным ремоделированием сосудистой стенки [2].
Эндотелиальная дисфункция - важнейший инициатор атеросклеротического процесса - характеризуется тенденцией к провоспалительному состоянию и протромботической активности, снижением способности к вазодилатации; она часто сочетается с инсулинорезистентностью [17].
При анализе биомаркеров у больных с сочетанием ЦВЗ и МС была обнаружена отрицательная корреляция уровней NO с плазменной концентрацией его эндогенного ингибитора - асимметричного диметиларгинина (АДМА). Оценка взаимосвязи воспалительных маркеров и прогрессирования атеросклероза сонных артерий выявила повышение значений Lp-PLA2 у лиц с ЦВЗ на фоне МС по сравнению с пациентами без сопутствующего МС (324 нг/мл (284; 361) и 302 нг/мл (255; 358) соответственно), причем более частая встречаемость у пациентов с МС неоднородности структуры АСБ с гипоэхогенным компонентом коррелирует с повышенным содержанием Lp-PLA2 в сыворотке крови (p<0,05) (рис. 2).
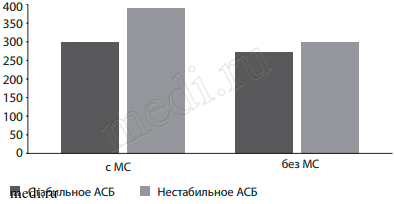 Рис. 2: Структура АСБ и содержание Lp-PLA2. в крови у пациентов с сочетанием ЦВЗ и МС.
Рис. 2: Структура АСБ и содержание Lp-PLA2. в крови у пациентов с сочетанием ЦВЗ и МС.
Проведенное нами исследование у пациентов с ЦВЗ, подвергшихся ангиореконструктивным операциям на сонных артериях, выявило, что гиперплазия неоинтимы и рестеноз в оперированной артерии чаще отмечались у больных с МС. Также у больных с МС по сравнению с пациентами без МС наблюдался значимо более высокий уровень Lp-PLA2, что позволяет предложить этот показатель в качестве маркера активности атеросклеротического процесса и прогрессирования проявлений ЦВЗ и МС [6].
Гипергликемия как один из основных компонентов МС играет важную роль в развитии микро- и макрососудистой цереброваскулярной патологии. Наличие инсулинорезистентности является самостоятельным предиктором атеросклероза и сосудистых событий даже при отсутствии других факторов риска. Следствием хронической гипергликемии являются расширение сосудов и гиперперфузия вещества головного мозга, что сопровождается повышением внутрикапиллярного давления, влиянием на эндотелий сосудов и базальную мембрану. Кроме того, увеличенное количество гликогемоглобина и других продуктов конечного гликозилирования также способствует развитию сосудистых осложнений при МС. Диагностированный СД2 сопровождается более активным прогрессированием атеросклероза брахиоцефальных артерий, причем выраженность и распространенность атеросклероза прямо коррелируют с увеличением длительности течения СД2 (р=0,007). Кроме того, для АСБ при СД2 характерны больший объем липидного ядра и воспалительная инфильтрация, а также более частое изъязвление бляшек и внутрисосудистое образование тромба, что может приводить к сужению просвета сосудов и повышенному риску ишемических событий [15].
Важным этапом патобиохимического каскада при цереброваскулярной патологии, особенно при ее сочетании с МС, является активизация процессов перекисного окисления липидов (ПОЛ). Свободные радикалы могут нарушать обмен оксида азота, который в норме уменьшает агрегацию тромбоцитов, замедляет адгезию моноцитов и лейкоцитов к эндотелию, ингибирует пролиферацию гладкомышечных клеток, а также препятствует окислению холестерина липопротеидов низкой плотности. Чувствительность мозга к токсическому воздействию свободных радикалов определяется высоким содержанием в мембранах нейронов мозга липидов с полиненасыщенными жирными кислотами и ионов металлов с переменной валентностью. Как было показано нами ранее, достижение целевого уровня показателей углеводного обмена не обеспечивает ликвидацию проявлений окислительного стресса у пациентов с МС/СД2 [1].
Таким образом, взаимопотенцирующее действие компонентов МС приводит к развитию и быстрому прогрессированию сосудистых заболеваний, в т.ч. и цереброваскулярных. Рациональная терапия таких компонентов МС, как артериальная гипертензия, атеросклероз, нарушение липидного и углеводного обмена, должна быть направлена не только на достижение целевых уровней соответствующих показателей, но и на стабилизацию проявлений недостаточности мозгового кровообращения. Коррекцию артериального давления (АД) необходимо проводить рационально, т.к. резкое снижение АД может способствовать нарастанию явлений энцефалопатии вследствие развития гипоперфузии мозга. При лечении нарушений углеводного обмена следует избегать эпизодов гипогликемии и гиперинсулинизма в крови, а гипотензивная и антилипидемическая терапия не должна обладать диабетогенным действием.
В попытке оказать максимальную помощь пациенту с ХЦВЗ врач вынужден выписывать несколько препаратов одновременно, тем самым увеличивая риск развития их потенцирующего влияния или несовместимости. Во избежание подобных ситуаций предпочтение следует отдавать препаратам с многофакторным поливалентным действием, имеющим достаточную доказательную базу эффективности и безопасности применения. Рассмотренные выше патогенетические особенности диктуют необходимость применения у данной категории пациентов фармакологических препаратов, избирательно блокирующих свободнорадикальные процессы и обладающих антиоксидантным действием. Одним из них является широко используемый в ангионеврологической практике отечественный препарат мексидол, клиническая активность которого у больных с острыми и хроническими ЦВЗ была изучена в большом количестве исследований.
Собственный опыт использования мексидола у больных ХЦВЗ свидетельствует об улучшении состояния пациентов и уменьшении выраженности наиболее часто встречающихся клинических проявлений данной патологии: астено-невротического, цефалгического и вестибуломозжечкового синдромов. При оценке биохимических проявлений МС (инсулинорезистентности, нарушений углеводного и липидного обмена) на фоне курсового лечения мексидолом (внутривенные инфузии мексидола по10 мл 5% раствора на 250 мл физиологического раствора в течение 14 дней, c последующим 3-месячным приемом препарата перорально в дозировке 125 мл 3 раза в день) был получен четкий и статистически значимый положительный эффект в виде существенного уменьшения явлений гиперинсулинизма и инсулинорезистентности.
Несмотря на то, что коррекция нарушений гликемии у больных с СД2 не была достигнута полностью (в среднем отмечалось снижение базального уровня на 0,9 ммоль/л, р=0,14), улучшение уровня гликемии отмечено у большинства (66%) больных. При этом снижение гликемии происходило не за счет гиперинсулинизма, а, наоборот, сопровождалось существенным улучшением чувствительности к инсулину. Эти процессы нашли отражение в значимом снижении индекса инсулинорезистентности НОМА-2 с 3,42±2,1 до 2,22±0,96 (р=0,001), чему сопутствовало также достоверное снижение уровня С-пептида с 4,03±2,52 до 2,7±1,09 нг/мл (р<0,003) (рис. 3).
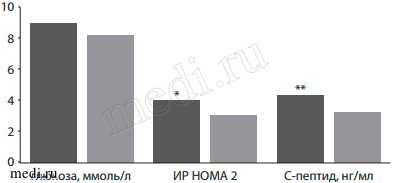 Рис. 3: Динамика показателей углеводного обмена у больных СД2 на фоне терапии мексидолом (*р=0,001, **р=0,0035).
Рис. 3: Динамика показателей углеводного обмена у больных СД2 на фоне терапии мексидолом (*р=0,001, **р=0,0035).
Улучшение показателей липидного спектра крови проявилось в виде существенного снижения уровня триглицеридов - с 2,3±0,9 ммоль/л (до лечения) до 1,9±0,77 ммоль/л (после) (р=0,00005). При этом отмечено также значимое снижение значений холестерина ЛПНП - с 3,05±0,83 ммоль/л до 2,77±0,67 ммоль/л (р=0,01).
Как видно на рис. 4, проведение вышеуказанного курса лечения способствовало значимому снижению плазменной концентрации важнейших маркеров атерогенеза - нитрита и NO (р<0,005).
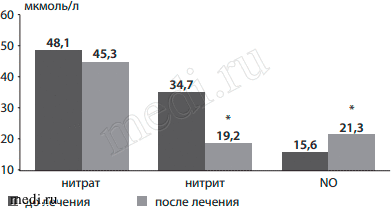 Рис.4: Динамика маркеров атерогенеза на фоне терапии мексидолом (*р=0,001).
Рис.4: Динамика маркеров атерогенеза на фоне терапии мексидолом (*р=0,001).
С полученными биохимическими изменениями коррелируют и структурные изменения сосудистой стенки (по данным ультразвукового исследования). Так, у пациентов с СД2, имевших исходное утолщение комплекса интима-медиа, на фоне проведенной антиоксидантной терапии в 26% случаев зарегистрировано уменьшение его толщины. Однако динамики со стороны структуры атеросклеротических бляшек по результатам ультразвукового исследования до и после курса лечения мексидолом отмечено не было. Это может быть обусловлено небольшим сроком наблюдения (3 месяца) и требует дальнейших исследований, предполагающих проведение более длительных курсов лечения.
Заключение
Биомаркерный профиль («биомаркерная отягощенность») пациентов с МС - важный фактор, имеющий потенциально большое значение для своевременной диагностики ассоциированных состояний. Изменение уровня биомаркеров на фоне МС свидетельствует о тесной связи между метаболическими нарушениями и прогрессированием атеросклероза, а также может служить предиктором клинического ухудшения. Динамика вышеуказанных биомаркеров наряду с дуплексным сканированием брахиоцефальных артерий, позволяющим оценить структуру и поверхность атеросклеротической бляшки сонной артерии, в сопоставлении с клиническими параметрами существенно помогают в оценке активности атеросклеротического процесса. Прогрессирующее и «злокачественное» течение атеросклероза на фоне МС может быть выявлено на ранних этапах, что позволит начать интенсивную и таргетную коррекцию указанной патологии. Следует сказать, что, не обладая абсолютной специфичностью и чувствительностью по отдельности, проатерогенные и антиатерогенные биомаркеры в совокупности способствуют выявлению группы пациентов высокого риска по развитию сердечно-сосудистых осложнений, а также формированию персонифицированного, многокомпонентного подхода к их лечению и профилактике возможных осложнений.
Таким образом, для замедления прогрессирования сосудистого поражения головного мозга у больных с МС очевидна необходимость мер, направленных на устранение метаболических нарушений (в первую очередь, нарушений жирового и углеводного обмена); эти меры должны включать назначение гемангиокорригирующих, антитромботических, антиоксидантных и эндотелиопротекторных препаратов. Необходима коррекция основных патогенетических механизмов сосудистого повреждения при СД - гипергликемии, дислипидемии, инсулинорезистентности. Подходы к ведению таких пациентов должны включать воздействие как на механизмы самого МС, так и на его осложнения, что при своевременном назначении терапии способствует улучшению прогноза и качества жизни пациента. Коррекция или стабилизация основных этапов формирования данной патологии на фоне лечения мексидолом определяют перспективу дальнейшего изучения вновь выявленных свойств препарата с целью расширения показаний к его применению.
Лагода Ольга Викторовна - канд. мед. наук, старш. науч. сотр. 1-го неврол. отд. ФГБНУ «Научный центр неврологии».
Танашян М.М. - зам. директора по научной и лечебной работе, зав. 1-м неврол. отд. ФГБНУ НЦН;
Антонова К.В. - врач-эндокринолог общеклинической группы ФГБНУ НЦН;
Раскуражев А.А. - науч. сотр. 1-го неврол. отд. ФГБНУ НЦН.
Список литературы
1. Антонова К.В. Влияние антиоксидантной терапии на показатели окислительного стресса. Автореф. дисс. ... канд. мед. наук. М., 2008.
2. Ануфриев П.Л., Танашян М.М., Гулевская Т.С. и др. Особенности атеросклероза церебральных артерий и патоморфологии инфарктов головного мозга при сахарном диабете 2 типа. Анн. клин. и эксперим. неврол. 2015; 5: 4-9.
3. Стаховская Л.В., Клочихина О.А., Богатырева М.Д, Коваленко В.В. Эпидемиология инсульта в России по результатам территориально-популяционного регистра (2009-2010). Журн. неврол. и психиатрии им. С.С. Корсакова. 2013; 5: 4-10.
4. Суслина З.А., Танашян М.М., Ионова В.Г. Ишемический инсульт: кровь, сосудистая стенка и антитромботическая терапия. М.: Медицинская книга, 2005.
5. Суслина З.А., Варакин Ю.Я. Эпидемиологические аспекты изучения инсульта. Время подводить итоги. Анн. клин. и эксперим. неврол. 2007; 1: 22-28.
6. Танашян М.М., Лагода О.В., Гулевская Т.С. и др. Клинико-морфологические и биохимические маркеры прогрессирования атеросклероза. Журн. неврол. им. Б.М. Маньковского. 2013; 1: 38-42.
7. Танашян М.М., Максюткина Л.Н., Лагода О.В. и др. Цереброваскулярные заболевания и каротидный атеросклероз: биомаркеры воспаления и коагуляции. Клин. неврол. 2013; 3: 16-23.
8. Танашян М.М., Раскуражев А.А., Шабалина А.А. и др. Биомаркеры церебрального атеросклероза: возможности ранней диагностики и прогнозирования индивидуального риска. Анн. клин. и эксперим. неврол. 2015; 3: 20-25.
9. Abbasi F., Asagmi T, Cooke J.P et al. Plasma concentrations of asymmetric dimethylarginine are increased in patients with type 2 diabetes mellitus. Am. J. Cardiol. 2001; 88: 1201-1203.
10. Boden-Albala B., Sacco R.L., Lee H.S. Metabolic syndrome and ischemic stroke risk: Northern Manhattan study. Stroke. 2008; 39: 30-35.
11. Boger R.H., Bode-Boger S.M., Szuba A. et al. Asymmetric dimethyl-arginine (АДМА): a novel risk factor for endothelial dysfunction: its role in hypercholesterolemia. Circulation 1998; 98: 1842-1847.
12. Feigin V.L., Forouzanfar M.H., Krishnamurthi R. et al. Global and regional burden of stroke during 1990-2010: findings from the Global Burden of Disease Study 2010. Lancet. 2014; 383 (9913): 245-254.
13. Hu G., Sarti C., Jousilahti P. et al. The impact of history of hypertension and type 2 diabetes at baseline on the incidence of stroke and stroke mortality. Stroke. 2005; 36: 2538-2543.
14. Kawamoto R., Tomita H., Oka Y. et al. Metabolic syndrome amplifies the LDL-cholesterol associated increases in carotid atherosclerosis. Intern. Med. 2005; 44: 1232-1238.
15. Maksimovic M., Vlajinac H, Radak D. et al. Frequency and characteristics of metabolic syndrome in patients with symptomatic carotid atherosclerosis. Rev. Med. Chile. 2009; 137: 329-336.
16. Miyazaki H, Matsuoka H, Cooke J.P. et al. Endogenous nitric oxide synthase inhibitor: a novel marker of atherosclerosis. Circulation. 1999; 99: 1141-1146.
17. Muniyappa R., Iantorno M., Quon M.J. An integrated view of insulin resistance and endothelial dysfunction. Endocrinol. Metab. Clin. North Am. 2008; 37: 685-711.
18. Okazaki S., Sakaguchi M., Miwa K. et al. Association of interleukin-6 with the progression of carotid atherosclerosis: a 9-year follow-up study. Stroke. 2014; 45: 2924-2929.
19. Palmer С., Kimber Ch., Doney A. Combined effect of inflammatory gene polymorphisms and the risk of ischemic stroke in a prospective cohort of subjects with type 2 diabetes: A Go-DARTS Study. Diabetes. 2010; 59; 2945-2948.
20. Rundek T., White H., Boden-Albala B. et al. The metabolic syndrome and subclinical carotid atherosclerosis: the Northern Manhattan Study. J. Cardiometab. Syndr. 2007; 2: 24-29.
21. Smith C.L., Anthony S., Hubank M. et al. Effects of АДМА upon gene expression: an insight into the pathophysiological significance of raised plasma АДМА. PLoS Med. 2005; 10: 1031-1043.
22. Yang Z.C., Wang K.S., Wu Y. et al. Asymmetric dimethylarginine impairs glucose utilization via ROS/TLR4 pathway in adipocytes: an effect prevented by vitamin E. Cell Physiol. Biochem. 2009; 24: 115-124.
23. Zoccali C. Asymmetric dimethylarginine (АДМА): a cardiovascular and renal risk factor on the move. J. Hypertens. 2006; 24: 611-619.
