Влияние субмаксимальных доз препарата мексидол на процессы оксидантного стресса и воспаления в острейшем периоде ишемического инсульта
СтатьиА.Р. Годунова*, А.А. Рахимова, О.И. Леонтьева, И.Г. Талипова, Р.М. Яхин, Ш.Г. Мусин
ГБУЗ Республики Татарстан «Больница скорой медицинской помощи», Набережные Челны, Россия
Цель исследования. Проследить динамику биохимических маркеров воспаления и показателей повреждения ткани головного мозга в острейшем периоде ишемического инсульта (ИИ) на фоне приема субмаксимальных доз препарата мексидол. Материал и методы. В исследование включили 60 пациентов, поступивших в первые 6 ч от начала заболевания, с верифицированным ИИ по шкале ASPECTS 7—9 баллов. Пациенты основной группы (n=30) получали субмаксимальные дозы мексидола — 750 мг препарата, разведенного в 250,0 мл физиологического раствора, 2 раза в сутки внутривенно капельно в течение 6 сут. Пациентам контрольной группы (n=30) была назначена стандартная терапия. Всем больным проводили определение биомаркеров, оценку неврологического статуса в течение 60 мин от момента поступления в стационар и на 7-е сутки. Результаты и заключение. В обеих группах показатели С-реактивного белка, интерлейкина-6 и фибриногена изменялись незначительно и достоверную значимость в оценке эффективности мексидола не имели. Показатели таких биомаркеров, как мозговой натрийуретический пептид и ассоциированный с беременностью протеин плазмы-А, а также средние показатели по шкалам NIHSS и MFI-20 в группе пациентов, получавших мексидол, значительно уменьшились по сравнению с контрольной группой. Полученные результаты свидетельствуют об уменьшении оксидантного стресса и признаков воспаления в острейшем периоде ИИ на фоне приема субмаксимальных доз препарата мексидол, снижении степени тяжести неврологического дефицита, повышении физической активности пациентов. С учетом сроков активации поврежденной антиоксидантной системы организма рекомендуемый срок медикаментозной поддержки составляет 3 мес.
Ключевые слова: антиоксидантный стресс, воспаление, острейший период, ишемический инсульт, мексидол.
Инсульт является важнейшей медико-социальной проблемой как в мире, так и в Российской Федерации (РФ), что обусловлено высокими показателями заболеваемости, смертности и инвалидизации. По данным статистического анализа, ежегодно в России инсульт поражает около 500 тыс. человек, частота заболеваемости — 3 случая на 1000 населения [1]. При том что заболеваемость инсультом оценивается как 400—450 тыс. случаев в год, на долю ишемического инсульта (ИИ) приходится около 80% (320—340 тыс. случаев в год) [2, 3].
Двумя стратегическими направлениями специфической терапии инсульта являются реперфузия, т.е. улучшение кровоснабжения области ишемического повреждения вещества головного мозга за счет восстановления проходимости сосудов и профилактики тромбообразования, и нейропротекция, т.е. поддержание метаболизма ткани мозга и защита ее от структурных повреждений.
Под нейропротекцией подразумевается любая стратегия лечения, которая защищает клетки головного мозга от гибели в результате ишемии — предотвращает, останавливает или замедляет повреждающие окислительные, биохимические и молекулярные процессы, которые имеют место при развитии необратимого ишемического повреждения [4]. Каждый год в неврологической и общемедицинской литературе публикуется более 200 работ по проблеме терапии инсульта. Только за период с 2001 по 2007 г. представлены результаты около 1000 экспериментальных и более 400 клинических исследований по этой теме [5].
Диагностика острого нарушения мозгового кровообращения (ОНМК) базируется прежде всего на методе нейровизуализации с использованием магнитно-резонансной (МРТ) и компьютерной томографии (КТ), а также на клинической верификации диагноза. Однако в последнее десятилетие в научной литературе активно обсуждаются надежные и доступные тесты для диагностики инфаркта головного мозга, определения его этиопатогенетических подтипов, тяжести неврологического дефицита, клинического течения и исхода заболевания. В результате многочисленных исследований выявлены различные механизмы повреждения нервной ткани при ишемии, установлены мишени для терапевтического вмешательства. Практически каждый элемент патофизиологического каскада является точкой приложения того или иного нейропротективного агента, в том числе противовоспалительного и антиоксидантного действия [6—8]. Расширение знаний о метаболических путях, участвующих в запуске патологического процесса, создание диагностических панелей биомаркеров увеличивают количество потенциальных терапевтических мишеней, участвующих в мониторировании лечения. Несмотря на это, по данным современной научной литературы, отмечается низкая диагностическая и прогностическая ценность многих биохимических показателей, поэтому приоритетной задачей клинической лабораторной диагностики является повышение их аналитической достоверности, а также разработка и внедрение в практику новых биохимических маркеров — биологически активных белков, выполняющих специфические функции, характерные для нервной системы. Лабораторные тесты, определяющие в крови биомаркеры мозга, процессов воспаления и оксидантного стресса, могут стать ключевыми компонентами успешной стратегии лечения и, что особенно важно, мониторинга исходов заболевания.
Нейропротективные препараты, обладающие антиоксидантной активностью, включены в Стандарты Минздрава [Приказ Министерства здравоохранения и социального развития Российской Федерации №513 от 01.08.07 «Об утверждении стандарта медицинской помощи больным с инсультом (при оказании специализированной помощи)». docs.cntd.ru/document/902275979]. Из них наиболее часто назначаются препараты, содержащие этилметилгидроксипиридина сукцинат (ЭМГПС): мексидол и др., которые описаны и в Федеральном руководстве по использованию лекарственных средств [Федеральное руководство по использованию лекарственных средств. XIII Выпуск. М. 2012;303.] как препараты для терапии ИИ в остром периоде. ЭМГПС представляет собой производное янтарной кислоты, которое оказывает антигипоксическое, мембранопротективное, ноотропное, противосудорожное, анксиолитическое действие. В ряде проведенных в РФ открытых исследований [9, 10] на небольших выборках пациентов в первые несколько суток от начала инсульта были продемонстрированы безопасность препарата и положительный эффект в плане уменьшения выраженности двигательного дефицита и восстановления повседневной активности, а также улучшения когнитивных функций. В рандомизированном двойном слепом плацебоконтролируемом исследовании эффективности и безопасности мексидола в комплексной терапии в остром периоде ИИ [11] были включены больные с ИИ (51 пациент, поступивший в первые 24 ч от начала заболевания), при применении ЭМГПС (мексидол) в дозе 300 мг/сут внутривенно в течение 14 сут отмечалось значимое уменьшение выраженности неврологического дефицита. Получено достоверное клиническое подтверждение эффективности мексидола в остром периоде ИИ (В.И. Скворцова и соавт., 2006) в каротидной системе атеротромботического или кардиоэмболического патогенетического типа, особенно при раннем (до 6 ч) его назначении.
В рандомизированное двойное слепое мультицентровое плацебо-контролируемое исследование эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах полушарного ИИ (Л.В Стаховская и соавт., 2017) был включен 151 пациент [12]. Больные 1-й группы получали терапию мексидолом по 500 мг/сут внутривенно капельно в течение 10 дней с последующим приемом по 1 таблетке (125 мг) 3 раза в сут в течение 8 нед. Пациенты 2-й группы получали плацебо по аналогичной схеме. Продолжительность участия в исследовании составила от 67 до 71 сут. В группе пациентов, получавших мексидол, отмечалось достоверно более выраженное по сравнению с плацебо улучшение жизнедеятельности, измеренное по модифицированной шкале Рэнкина. На момент окончания терапии неврологический дефицит был достоверно ниже в группе терапии мексидолом при тестировании по шкале инсульта Национального института здоровья (National Institutes of Health Stroke Scale — NIHSS) по сравнению с плацебо. Положительное воздействие терапии мексидолом также отмечено у пациентов с сопутствующим сахарным диабетом. Терапия мексидолом способствовала достоверному улучшению качества жизни, уже начиная со 2-го визита. Подавляющее большинство пациентов в группе терапии мексидолом отмечали, что у них не возникает никаких проблем с передвижением, самообслуживанием, выполнением повседневных дел, не испытывали боли и дискомфорта, тревоги и депрессии. В подгруппе пациентов с сахарным диабетом в группе терапии мексидолом качество жизни было также достоверно выше к моменту окончания терапии. Таким образом, в исследовании доказана безопасность длительной последовательной терапии мексидолом у пациентов с ИИ в остром и раннем восстановительном периодах. Результаты исследования свидетельствуют, что мексидол в режиме последовательной терапии обладает благоприятным профилем переносимости и безопасности.
Цель работы — проследить динамику биохимических маркеров воспаления и повреждения ткани головного мозга в острейшем периоде ИИ на фоне использования субмаксимальных доз препарата мексидол.
Материал и методы
В обследование включены 60 пациентов в возрасте 47—79 лет, поступивших в стационар в «терапевтическом окне» (до 6 ч от начала заболевания) с верифицированным инфарктом головного мозга со степенью тяжести по шкале оценки ранних КТ-изменений при инсульте головного мозга (Alberta Stroke Program Early CT Score — ASPECTS) 7—9 баллов. Пациенты были разделены на две равные группы: больные основной группы (n=30) получали субмаксимальные дозы мексидола — 1500 мг/сут, по 750 мг препарата, разведенного в 250,0 мл физиологического раствора, 2 раза в сутки внутривенно капельно в течение 6 сут, больным контрольной группы (n=30) была назначена стандартная терапия. В клиническое обследование входила оценка неврологического статуса по шкале инсульта NIHSS. В исследование включали пациентов с 4—15 баллами по шкале NIHSS [13], что соответствовало легкой и средней степени тяжести инсульта на момент поступления. Степень тяжести и динамику астенического синдрома оценивали по шкале субъективной оценки астении (Multidimensional Fatigue Inventory 20 — MFI-20), которая продемонстрировала надежность и валидность в многочисленных исследованиях у пациентов с астеническими состояниями различной этиологии [14—16]. Обследование больных проводилось при поступлении и в динамике на 3, 5 и 7-е сутки.
В настоящей работе были использованы следующие лабораторные методы:
- 1) клинический анализ крови;
- 2) биомаркеры:
— нейроспецифический биомаркер повреждения ткани центральной нервной системы — мозговой натрийуретический пептид (brain natriuretic peptide — BNP), который применяется для диагностики кардиоэмболического подтипа инфаркта мозга;
— биомаркеры воспаления - С-реактивный белок (С-reactive protein — CRP) и интерлейкин-6 (IL-6), которые участвуют в острой фазе воспалительного ответа, играют важную роль в диагностике и верификации риска инсульта;
— ассоциированный с беременностью протеин плазмы-А (pregnancy-associated plasma protein A - PAPP-A), который продуцируется клетками атеросклеротической бляшки, особенно нестабильной, и разрушает все виды белков внеклеточного матрикса [17—21];
— гемостатический биомаркер фибриноген, обеспечивающий необратимую агрегацию тромбоцитов и формирование стабильного тромбоцитарного тромба [22—26].
Всем пациентам биомаркеры определяли в течение 60 мин от момента поступления в стационар (до лечения) и на 7-е сутки (после лечения). Методы лучевой диагностики включали КТ, МРТ с использованием режимов Т1+- и Т2+-диффузионно-взвешенных изображений и оценку степени тяжести по шкале ASPECTS в интервале от 7 до 9 баллов.
Результаты и обсуждение
При поступлении в обследованных группах прослеживалась обратная зависимость показателей BNP и PAPP-A от показателей шкалы ASPECTS. Кроме того, как в основной, так и в контрольной группах отмечалось значительное увеличение показателя BNP у пациентов при кардиоэмболическом подтипе ОНМК (у 8 в основной и у 5 в контрольной) в первые часы от момента начала заболевания. В обеих группах среднее значение показателей CRP, IL-6 и уровень фибриногена на фоне лечения изменялись незначительно, поскольку для обследования отбирали пациентов с легкой и средней степенью тяжести инсульта по ASPECTS (7—9 баллов). Достоверную значимость в динамике показали изменения биомаркеров воспаления BNP и PAPP-A. В основной группе показатель BNP после лечения снизился в среднем в 2,58 раза, в контрольной группе — в 2,01 раза. Биомаркер PAPP-A в основной группе в среднем уменьшился на 16,43 мЕд/мл, в контрольной группе — на 9,61 мЕд/мл (см. таблицу). При оценке неврологического статуса после лечения у пациентов основной группы выявили снижение среднего показателя по шкале NIHSS на 2,5 балла, в контрольной группе — на 1,8 балла (рис. 1). Кроме того, в основной группе отмечался значительный регресс астенического синдрома по шкале MFI-20 на 3-и сутки, в то время как в контрольной группе активность пациентов возрастала на 5—7-е сутки (рис. 2).
Динамика изменений биомаркеров
|
Показатель |
До лечения (1-е сутки) |
После лечения (7-е сутки) |
||
|
основная группа |
контрольная группа |
основная группа |
контрольная группа |
|
|
CRP, МЕ/л |
21,90 |
20,98 |
23,73 |
20,61 |
|
IL-6, пг/мл |
17,50 |
16,10 |
16,77 |
15,26 |
|
BNP, пг/мл |
771,45 |
601,33 |
298,18 |
299,91 |
|
PAPP-A, мЕд/л |
21,36 |
16,20 |
4,93 |
6,59 |
|
Фибриноген, г/л |
3,28 |
3,42 |
3,35 |
3,48 |
Рис.1. Динамика средних значений по шкале NIHSS у обследуемых пациентов.
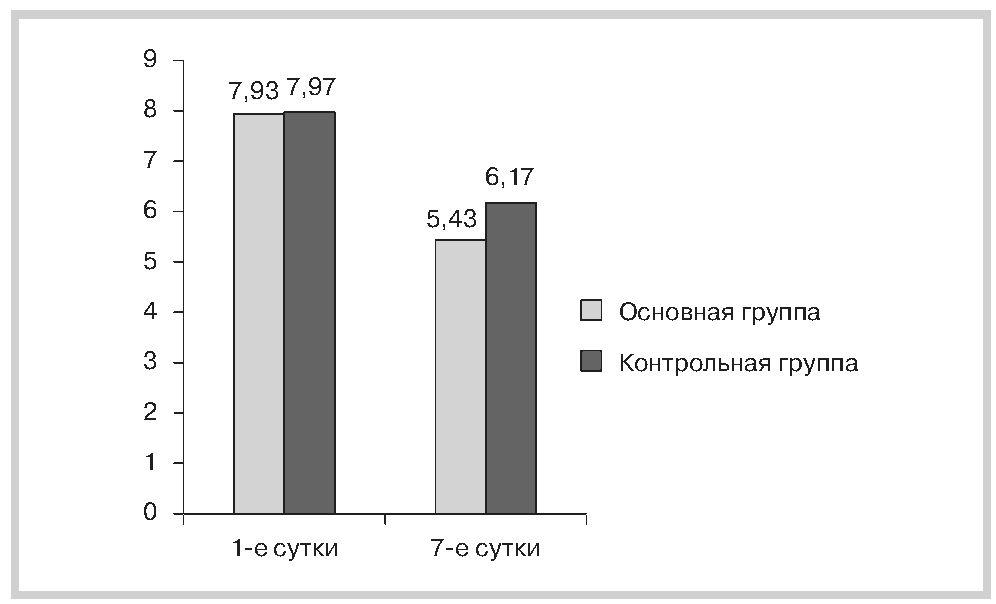
Здесь и на рис. 2: по оси ординат — баллы.
Рис. 2. Динамика уровня астении по шкале MFI-20 у обследуемых пациентов.
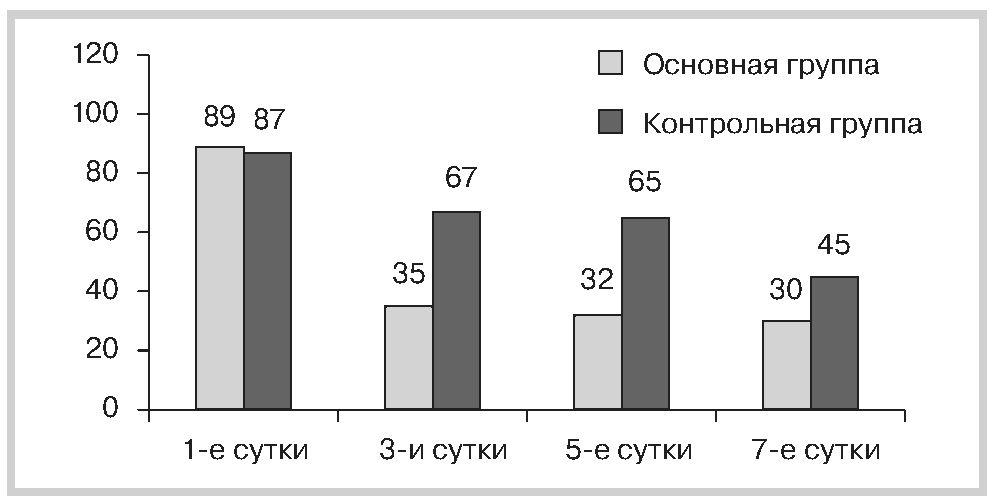
Таким образом, по результатам настоящего исследования можно сделать следующие выводы:
1. Исследование биодинамики маркеров оксидантного стресса и воспаления в острейшем периоде ИИ свидетельствует о положительном влиянии субмаксимальных доз препарата мексидол на процессы оксидантного стресса и воспаления в острейшем периоде ишемии головного мозга.
2. Уменьшение оксидантного стресса помогает повысить эффективность профилактических и лечебно-реабилитационных мероприятий, снижая степень тяжести неврологического дефицита, повышая физическую активность пациентов.
3. Учитывая, что на активацию поврежденной антиоксидантной системы организма требуется в среднем 3 мес [21], рекомендуемый срок медикаментозной антиоксидантной поддержки целесообразно определить в вышеуказанном диапазоне.
Авторы заявляют об отсутствии конфликта интересов.
ЛИТЕРАТУРА/REFERENCES
1. Стародубцева О.С., Бегичева С.В. Анализ заболеваемости инсультом с использованием информационных технологий. Фундаментальные исследования. 2012;8(2):424-427. [Starodubtseva OS, Begicheva SV. Anal- iz zabolevaemosti insul’tom s ispol’zovaniem informatsionnykh tekhnolo- gii. Fundamental’nye issledovaniya. 2012;8(2):424-427. (In Russ.)].
2. Гусев Е.И. Проблема инсульта в России. Журнал неврологии и психиат рии им. С.С. Корсакова (приложение Инсульт). 2003;9:3-10. [Gusev EI. Prob- lema insul’ta v Rossii. Zhurnal Nevropatologii i Psikhiatrii im. S.S. Korsakova (Prilozhenie «Insul’t»). 2003;9:3-10. (In Russ.)].
3. Суслина З.А., Пирадов М.А. Инсульт: диагностика, лечение, профи- лактика. М.: Медпресс-Информ; 2008. [Suslina ZA, Piradov MA. Insul’t: diagnostika, lechenie, profilaktika. М: Medpress-Inform; 2008. (In Russ.)].
4. Ginsberg MD. Neuroprotection For Ischemic Stroke: Past, Present And Future. Neuropharmacology. 2008;55(3):363-369.
5. Ginsberg MD. Current Status Of Neuroprotection For Cerebral Ischemia. Synoptic Overview. Stroke. 2009;40:111-114.
6. Laborde CM, Mourino-Alvarez L, Akerstrom F, Padial LR, Vivanco F, Gil-Dones F, Barderas MG. Potential Blood Biomarkers For Stroke. Ex- Pert Rev Proteomics. 2012;9(4):437-449.
7. Verma S, Buchanan MR, Anderson TJ. Endothelial Function Testing As A Biomarker Of Vascular Disease. Circulation. 2003;108:2054-2059.
8. Whiteley W, Chong WL, Sengupta A, Sandercock P. Blood Markers For The Prognosis Of Ischemic Stroke: A Systematic Review. Stroke. 2009;40(5):380-389.
9. Луцкий М.А. Анализ эффективности мексидола в комплексном лече- нии больных с ишемическим инсультом. Журнал неврологии и психиат- рии им. С.С. Корсакова. 2010;110(4):57-59. [Lutskii MA. Analiz effek- tivnosti meksidola v kompleksnom lechenii bol’nykh s ishemicheskim insul’tom. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2010;110(4):57- 59. (In Russ.)].
10. Румянцева С.А., Евсеев В.Н., Елисеев Е.В. Антиоксидантная терапия при остром ишемическом инсульте. Атмосфера. Нервные болезни. 2009;3:8-12. [Rumyantseva SA, Evseev VN, Eliseev EV. Antioksidantnaya terapiya pri ostrom ishemicheskom insul’te. Atmosfera. Nervnye bolezni. 2009;3:8-12. (In Russ.)].
11. Скворцова В.И., Стаховская Л.В., Нарциссов Я.Р., Бодыхов М.К., Кичук И.В., Гудков Ю.В., Солдатенков Т.Д., Кондрашова Т.Т., Ка- линина Е.В., Новичкова М.Д., Кербикова О.Б. Рандомизированное двойное слепое плацебо-контролируемое исследование эффектив- ности и безопасности мексидола в комплексной терапии ишемиче- ского инсульта в остром периоде. Журнал неврологии и психиатрии им. С.С. Корсакова (Приложение Инсульт). 2006;18:47-54. [Skvortsova V.I., Stakhovskaya L.V., Nartsissov Ya.R., Bodykhov M.K., Kichuk I.V., Gudkov Yu.V., Soldatenkov T.D., Kondrashova T.T., Kalinina E.V., Novichkova M.D., Kerbikova O.B. Randomizirovannoe dvoinoe slepoe plat- sebo-kontroliruemoe issledovanie effektivnosti i bezopasnosti meksidola v kompleksnoi terapii ishemicheskogo insul’ta v ostrom periode. Zhurnal Nev- rologii i Psikhiatrii im. S.S. Korsakova (Pril. Insul’t). 2006;18:47-54. (In Russ.)].
12. Стаховская Л.В., Шамалов Н.А., Хасанова Д.Р., Мельникова Е.В., Агафьина А.С., Голиков К.В., Богданов Э.И., Якупова А.А., Рошков- ская Л.В., Лукиных Л.В., Локштанова Т.М., Повереннова И.Е., Ще- панкевич Л.А. Результаты рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных груп- пах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и ран- нем восстановительном периодах полушарного ишемического ин- сульта (ЭПИКА). Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117:3(2):55-65. [Stakhovskaya LV, Shamalov NA, Khasanova DR, Melnikova EV, Agafiina AS, Golikov KV, Bogdanov EI, Yakupova AA, Roshkovskaya LV, Lukinykh LV, Lokshtanova TM, Poverennova IE, Shepankevich LA. Results of a randomized double blind multicenter placebo-controlled, in parallel groups trial of the efficacy and safety of prolonged sequential therapy with mexidol in the acute and early recovery stages of hemispheric ischemic stroke (EPICA). Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2017;117:3(2):55-65. (In Russ.)]. doi.org/10.17116/jnevro20171173255-65
13. Елкина Т.А., Осетров А.С. Динамика показателей клинических оце- ночных шкал в острейшем и остром периодах при отдельных подти- пах ишемического инсульта. Электронный журнал. Современные про- блемы науки и образования. 2013;5. [Elkina TA, Osetrov AS. Dinamika pokazatelei klinicheskikh otsenochnykh shkal v ostreishem i ostrom perio- dakh pri otdel’nykh podtipakh ishemicheskogo insul’ta. Sovremennye Prob- lemy Nauki i Obrazovaniya. 2013;5. (In Russ.)]. science-education.ru/ru/article/view
14. Fedin AI, Solovyova EY, Мironova OP, Fedotova АV. Treatment of asthen- ic syndrome in patients with chronic brain ischemia: results of the non-in- terventional observational program TRIUMPH. Zhurnal nevrologii i psikhi- atrii im. S.S. Korsakova. 2014;114(12):104-111. doi.org/10.17116/jnevro2014114121104-111
15. Smets EM, Garssen B, Bonke B, De Haes JC. The Multidimensional Fa- tigue Inventory (MFI) psychometric qualities of an instrument to assess fa- tigue. J Psychosom Res. 1995;39(3):315-325.
16. Lin JM, Brimmer DJ, Maloney EM, Nyarko E, BeLue R, Reeves WC. Fur- ther validation of the Multidimensional Fatigue Inventory in a US adult population sample. Popul Health Metr. 2009;7:18.
17. Ahluwalia N, Blacher J, de Edelenyi FS, Faure P, Julia C, Hercberg S, Ga- lan P. Prognostic value of multiple emerging biomarkers in cardiovascular risk prediction in patients with stable cardiovascular disease. Atherosclerosis. 2013;228(2):478-484.
18. Llombart V, Antolin-Fontes A, Bustamante A, Giralt D, Rost NS, Furie K, Fonseca A. B-type natriuretic peptides help in cardioembolic stroke diag- nosis: pooled data meta-analysis. Stroke. 2015;46(5):1187-1195.
19. Wang S, Jiang J, Qu C, Wang C, Sun Z. Predictive value of serum pregnancy-associated plasma protein A for patients with ischemic cerebrovascular disease. J Clin Lab Anal. 2017;31:22091. doi.org/10.1002/jcla.22091
20. Wang L, Jiang J, Du L, Zhang X, Wang C. The prognostic value of serum pregnancy-associated plasma protein A, S100 and high sensitivity C-reac- tive protein in acute ischemic stroke patients without heparin administra- tion. Clinical biochemistry. 2014;47(16-17):187-191.
21. Zitnanová I, Šiarnik P, Kollár B, Chomová M, Pazderová P, Andrezálová L, JeDoviIová M, Ko^ariková, Laubertová K, Krivošíková Z, Slezáková L, TurIáni P. Oxidative Stress Markers And Their Dynamic Changes In Pa- tients After Acute Ischemic Stroke Oxidative. Hindawi Publishing Corpora- tion Oxidative Medicine and Cellular Longevity. 2016;2016(Article ID 9761697);7. doi.org/10.1155/2016/9761697
22. Вельков В.В. На пути к ранней диагностике сердечно-сосудистых со- бытий: многомаркерные панели и ультрачувствительные тропонины. Медицинский Алфавит. Лаборатория. 2011;1:30-36. [Vel’kov VV. Na puti k rannei diagnostike serdechno-sosudistykh sobytii: mnogomarkernye paneli i ul’trachuvstvitel’nye troponiny. Meditsinskii Alfavit. Laboratoriya. 2011;1:30-36. (In Russ.)].
23. Сыскина Е.Н. Биохимические маркеры состояния ткани мозга и гемо- стаз у больных с тяжелыми формами инфарктов мозга в артериях каро- тидной системы: Дис. ... канд. мед. наук. М. 2011. [Syskina EN. Biokhi- micheskie markery sostoyaniya tkani mozga i gemostaz u bol’nykh s tyazhelymi formami infarktov mozga v arteriyakh karotidnoi sistemy: Dis. ... kand. med. nauk. M. 2011. (In Russ.)].
24. Шабалина А.А. Гемостаз и биохимические маркеры повреждения ткани мозга при атеротромботическом и лакунарном подтипах ишемического инсульта: Дис. ... канд. мед. наук. М. 2008. [Shabalina AA. Gemostaz i biokhimicheskie markery povrezhdeniya tkani mozga pri aterotromboticheskom i lakunarnom podtipakh ishemicheskogo insul’ta: Dis. ... kand. med. nauk. M. 2008. (In Russ.)].
25. Koh PO. Proteomic Analysis Of Focal Cerebral Ischemic Injury In Male Rats. J Vet Med Sci. 2010;72(2):181-185.
26. Whiteley W, Tseng MC, Sandercock P. Blood Biomarkers In The Diagnosis Of Ischemic Stroke. A Systematic Review. Stroke. 2008;39:2902-2909.
An influence of submaximal (submineximal) doses of mexidol on oxidant stress and inflammation in the acute period of ischemic stroke
A.R. GODUNOVA, A.A. RAKHIMOVA, O.I. LEONTYEVA, I.G. TALIPOVA, R.M. YAKHIN, SH.G. MUSIN
Emergency Hospital, Naberezhnye Chelny, Russia
Objective. To study an effect of submaximal doses of mexidol on the dynamics of biochemical markers of inflammation and damage to brain tissue in the acute period of ischemic stroke. Material and methods. A total of 60 patients admitted in the first 6h after disease onset with a verified ischemic stroke (7—9 points on the ASPECT scale) were enrolled in the study. Thirty patients in the study group received submaximal doses of mexidol: 750 mg infusion dropwise in 250 ml of 0.9% NaCl solution for 6 days. Thirty patients of the control group received standard therapy. Biomarkers and neurological status were evaluated within 60 minutes from the time of admission to the hospital and after 6 days. Results and conclusion. In both groups, the changes in CRP, IL-6, and fibrinogen did not contribute to the efficacy of mexidol. The brain natriuretic peptide (BNP) biomarker, plasma-A-associated pregnancy (PAPP-A) biomarker, average NIHSS score and mean cerebroasthenia score on the MFI-20 scale in the study group were significantly reduced compared to the control group. This study indicates a decrease in oxidative stress and signs of inflammation, a reduction of the severity of neurological deficit and an increase in physical activity of patients treated with submaximal doses of mexidol. Given the activation time of the damaged antioxidant system of the body, the recommended period of treatment is 3 months.
Keywords: antioxidant stress, inflammation, acute period, ischemic stroke, mexidol.
