Сравнительная оценка эффективности стандартной терапии и сочетания мексидола с конвульсаном на этапе ранней реабилитации больных опийной наркоманией
СтатьиМ.А.Мельников, А.М.Карпов*
Республиканский наркологический диспансер Министерства здравоохранения Республики Татарстан;*Казанская государственная медицинская академия
При лечении больных опийной наркоманией мексидолом и конвульсаном симптомы абстинентных и постабстинентных расстройств у них редуцировались быстрее и в большей степени, чем при лечении по стандартной методике. Больные раньше становились способны к социально-нормативному поведению, к конструктивным и продуктивным действиям в лечебно-реабилитационном процессе.
Ключевые слова: мексидол, конвульсан, ламотриджин, наркомания, абстинентные расстройства
В последние 20 лет наркомания стабильно позиционируется как основная угроза национальной и международной безопасности, продолжается ежегодный прирост числа больных на 3-5% в Российской Федерации и Республике Татарстан. Соответственно увеличивается число больных, нуждающихся в лечении и реабилитации, растут требования к эффективности медицинской и социально-психологической помощи наркозависимым.
Академиком РАМН профессором Н.Н.Иванцом [6] разработаны принципы лечения больных наркоманиями: этапность, добровольность, индивидуальность, комплексность и др., которые адекватно структурировали и направили исследования в этой области. Эти принципы органично вписываются в современную биопсихосоциальную научную парадигму, дополненную А.М.Карповым потребностно-иерархическим принципом увеличения масштабов потребностей человека и обще ства от биологических через социальные к духовным (психологическим) [7]. Принцип по-уровневого структурирования обнаруживается в последовательной смене 4 этапов лечения нарко-зависимых: отнятие наркотика, купирование абстинентных расстройств, купирование физической и психической зависимости, профилактика рецидивов [5,7]. Эти этапы отражают ступени движения лечебного процесса с биологического уровня на психический и социальный. Дифференциация этиологических факторов, патогенетических механизмов, клинических проявлений болезни и терапевтических воздействий на биологические, социальные и психологические составляющие является современным алгоритмом мышления врача, обеспечивающим оптимальную технологию работы [4-6]. Однако скорость реализации этого алгоритма может быть различной. Сокращение его длительности даст экономию времени и ресурсов больных и наркологической службы.
В специальной литературе недостаточно разработана терапевтическая тактика на этапе перехода с биологического уровня на личностно-социальный. Этот этап начинается после купирования компульсивного влечения и наиболее грубых симптомов острой абстиненции, в среднем на 8-12-й день после отнятия наркотика. На этом этапе начинается психотерапевтическая коррекция личностных и поведенческих расстройств, создание установок на выполнение реабилитационной программы и формирование мотивации на отказ от потребления всех психоактивных веществ на всю жизнь. Работа с личностью в это время лимитируется биологическими причинами — постабстинентными, метаболическими, соматовегетативными нарушениями. Для подготовки «биологической базы» для психотерапии на этом этапе применяются вазоактивные средства, ноотропы, антигипоксанты, антиоксиданты, витамины и другие препараты, обладающие нейротрансмиттерными, нейротрофическими и нейромодуляторными эффектами.
Для уточнения задач психофармакотерапии необходимы дифференциация патогенетических механизмов актуальных психических расстройств и выбор препаратов, спектр психотропной активности которых будет им соответствовать. Основными психопатологическими симптомами в постабстинентном периоде являются астения и раздражительность, эмоциональная и волевая неустойчивость, недо статочная целенаправленность и по следовательно сть в поведении, непродуктивность в занятиях. Патогенетические механизмы описанных расстройств включают дефициты всех нейромедиаторных систем, энергообразования и всех видов обмена [2]. Известно, что основным фармакотерапевтическим подходом для коррекции разбалансированности сопряженных нейромедиаторных, психических и соматовегетативных нарушений, формирующих абстинентные расстройства у больных опийной наркоманией (ОН), является применение препаратов, усиливающих активность тормозных — ГАМКергических и снижающих активно сть возбуждающих — глутаматных систем [2,5,6].
Стимуляция ГАМК-рецепторов транквилизаторами бензодиазепинами, вальпроатами, карбамазепином способствует уменьшению тревоги, раздражительности, бессонницы, а также снижению эмоциональной, волевой, интеллектуальной, поведенческой и социальной активности. Эти фармакотерапевтические эффекты востребованы в остром периоде абстиненции, когда приоритетной задачей является купирование соматовегетативных расстройств, компульсивного влечения и бессонницы, но эти же эффекты создают препятствия по окончании острого периода абстиненции, а также в постабстинентном периоде, когда начинают актуализироваться потребности социального характера, предполагающие волевые и интеллектуальные усилия пациентов. На этом этапе ГАМКергическая релаксация снижает мотивацию больных к собственным усилиям, даже может воспроизводить эффекты алкогольного опьянения и способствовать усилению тяги к алкоголю или наркотику [6].
Препараты, уменьшающие активность глутаматных рецепторов, имеют несколько иной спектр психотропной активно сти. Редукция тех же симптомов раздражительности, тревоги, бессонницы, патологического влечения к наркотику происходит с меньшей седацией и релаксацией. Ряд авторов считают, что препараты этой группы спо собствуют улучшению конгнитивных функций — внимания, мышления, памяти [8]. Возможно, это является следствием меньшей седации, что позволяет пациентам реализовать имеющиеся у них психические и личностные ресурсы. Эти фармакотерапевтические характеристики препаратов отвечают запросам лечения на этапе ранней реабилитации, когда нужно обеспечить эмоциональную стабильность не только без седации, но и с повышением функциональной активности внимания, мышления и памяти как необходимых элементов комплаенса — осознанного, мотивированного и продуктивного участия больных в реабилитационном процессе. Требующейся совокупностью эффектов обладает препарат конвульсан (ламотриджин) — блокатор потенциалзависимых Na+-каналов, подавляющий патологическое высвобождение глутаминовой кислоты.
Интересны результаты сравнительного изучения терапевтической эффективности ламотриджина с ГАМКергическими препаратами карбамазепином [3] и ретардированным вальпроатом натрия [6] при лечении больных алкоголизмом. Их авторы сделали вывод о том, что при алкогольной абстиненции ламотриджин превосходит по эффективности карбамазепин, в частности, по нормотимическому и противотревожному действию и по влиянию на инсомнические и неврологические (тремор, атаксию) расстройства. Ламотриджин превосходит вальпроат по влиянию на биологически обусловленное патологическое влечение к алкоголю и на когнитивные функции, облегчает комплаенс, повышает готовность больных следовать рекомендациям врача и спо собствует формированию адекватной установки на трезвость. Обе группы авторов отметили, что ламотриджин лучше переносится, не вызывает побочных эффектов, способствует повышению физической активности, работоспособности, стабилизации настроения, благодаря чему создает предпосылки для улучшения социального функционирования больных алкоголизмом на ранних этапах реабилитации. Эти сведения стали теоретической предпосылкой гипотезы о том, что ламотриджин проявит сходный эффект при лечении больных опийной наркоманией, т.к. патогенетические механизмы зависимостей от психоактивных веществ и алгоритмы лечения больных с зависимостями практически одни и те же [1,2]. Эта гипотеза нами проверена и подтверждена [8], что способствовало появлению предположения о том, что сочетание ламотриджина, корригирующего нейромедиаторные нарушения с мексидолом, корригирующим метаболические нарушения у больных ОН, еще больше повысит эффективность лечения больных на ранних этапах реабилитации.
Известно, что при наркотической зависимо сти наряду с патологией внутренних органов происходят резкие изменения обмена веществ. Среди биохимических показателей наиболее значительно изменяется антиоксидантная защита, активируется ПОЛ, что требует применения антиоксидантной терапии как патогенетически значимого звена комплексной терапии у наркозависимых. Из разнообразных антиоксидантных препаратов внимание наркологов привлек мексидол [5], который отличается водорастворимостью и хорошей биодоступностью, в связи с чем его удобнее использовать в качестве лекарственного препарата по сравнению с жирорастворимыми антиоксидантами (дибунол, ионол). Важно также то, что мексидол обладает выраженной способностью оказывать потенцирующее действие на эффекты транквилизирующих, нейролептических, антидепрессивных, снотворных, противосудорожных и анальгезирующих средств, что позволяет снизить их дозы и таким образом уменьшить побочные эффекты. В частно сти, при комбинации мексидола с ламотриджином дозу антиконвульсанта можно уменьшить в 2 раза без снижения его терапевтического эффекта. Сочетанное применение мексидола с ламотриджином имеет патогенетическое обоснование для оптимизации терапии больных ОН.
Цель исследования — оценка эффективности сочетанного применения мексидола и конвульсана на раннем этапе реабилитации больных ОН.
Методика исследования
Обследовали 40 пациентов-мужчин в возрасте 18-47 лет. Длительность заболевания составила 1-19 лет. У всех диагностирована 2 стадия зависимости от наркотика F11.2.
Пациентов делили на 2 группы, не различающие ся по клиническим, возрастным и социальным характеристикам. В основной группе (n=20) проводили лечение конвульсаном (аналогом ламотриджина) и мексидолом. Конвульсан назначали по схеме: с 5-го дня после отмены наркотика в течение 5 дней по 100 мг 2 раза в день, затем в течение 5 дней по 50 мг 2 раза в день, далее в течение 5 дней по 25 мг 2 раза в день, в последние 10 дней по 25 мг на ночь. Мексидол назначался в сочетании с конвульсаном в первые 5 дней по 250 мг 3 раза в день, последующие 20 дней — по 125 мг 3 раза в день. Общий курс лечения — 25 дней. Применение мексидола позволило снизить дозировку ламотриджина более чем в 2 раза по сравнению с ранее проведенным нами исследованием при монотерапии ламотриджином [8]. В контрольной группе (n=20) лечение проводили по стандартной методике, включавшей сонапакс 50-100 мг в день, феназепам 1-2 мг в день, карбамазепин по 200 мг 3 раза в день.
Отнятие наркотика и купирование компульсивного влечения, как проявления физической зависимости, проводилось в «острых» стационарных отделениях Республиканского наркологического диспансера МЗ РТ по стандартным методикам в течение 10 дней. На этом этапе терапия была преимущественно соматотропной, направленной на коррекцию нарушений деятельности внутренних органов, гомеостаза и грубых психических нарушений. Затем больные по ступали в 5-е реабилитационное отделение Республиканского наркологического диспансера МЗ РТ на первый — мотивационный (восстановительный) и далее адаптационный этапы реабилитации. Психопатологические проявления выявлялись в процессе расспроса пациентов и круглосуточного наблюдения за ними среднего медперсонала. Выявленные симптомы по качественным характеристикам квалифицировались по глоссарию, по количественным характеристикам оценивались по стандартным 4-балльным шкалам выраженности симптомов: отсутствие симптома — 0, слабая выраженность — 1, средняя — 2, высокая — 3 балла. Все параметры заносили в регистрационную карту, составленную на основе «Карты обследования больных наркоманиями» [9].
Сравнение степени и скорости редукции абстинентных и постабстинентных проявлений наркозависимости на фоне лечения проводили в результате вычисления среднеарифметических значений каждого симптома в группе до начала лечения, через 5, 10, 15, 20 и 25 дней.
Результаты исследования
Наблюдения и бе седы с больными обнаруживали сходные для всех участвовавших в исследовании расстройства. Все пациенты до начала лечения чувствовали себя некомфортно, жаловались на плохое самочувствие и настроение, общую слабость и «разбитость», раздражительность, головные боли, головокружение, бессонницу. Считая, что больным нужно отдыхать, они часто ложились, но из-за тревоги и дискомфорта поднимались с постели, бесцельно бродили по отделению, пытались читать реабилитационную литературу, писать задания, но им быстро все надоедало, появлялись скука и усталость, пропадал интерес. На беседы к врачу и психологу не стремились. Во время разговоров были вяловатыми, пассивными, проявляли озабоченность соматическим состоянием, высказывали много жалоб на здоровье, отмечали полную несостоятельность к каким-либо усилиям, признавали, что часто ощущали тягу к наркотику, что их огорчало и раздражало. Настроение было сниженным и неустойчивым, поведение бесцельным, представления о перспективах аморфными, планы краткосрочными, ограниченными соматической и психической несостоятельностью.
Симптомы абстинентных и постабстинентных расстройств у больных ОН в процессе лечения мексидолом и конвульсаном редуцировались быстрее и в большей степени, чем при лечении по стандартной методике (таблица). Разница выявлялась на 5-й день терапии. Психопатологические проявления абстиненции — раздражительность, тревога, апатия, ипохондрия в основной группе существенно редуцировались на 5-й день, в группе сравнения — на 10-й день. Соматовегетативные проявления — тяжесть в голове, головокружение, разбитость, колебания АД, нарушения сна также раньше и в большей степени редуцировались в результате лечения мексидолом и конвульсаном. Ключевой симптом — патологическое влечение к наркотику снижался на 5-й день и исчезал к 20-му дню при лечении мексидолом и конвульсаном, тогда как при стандартной терапии он снижался на 10-й день и в слабой степени сохранялся до 25-го дня.
Сравнение динамики редукции симптомов абстиненции у больных ОН в результате лечения по стандартной методике (числитель) и лечения мексидолом с конвульсаном (знаменатель) (M±m)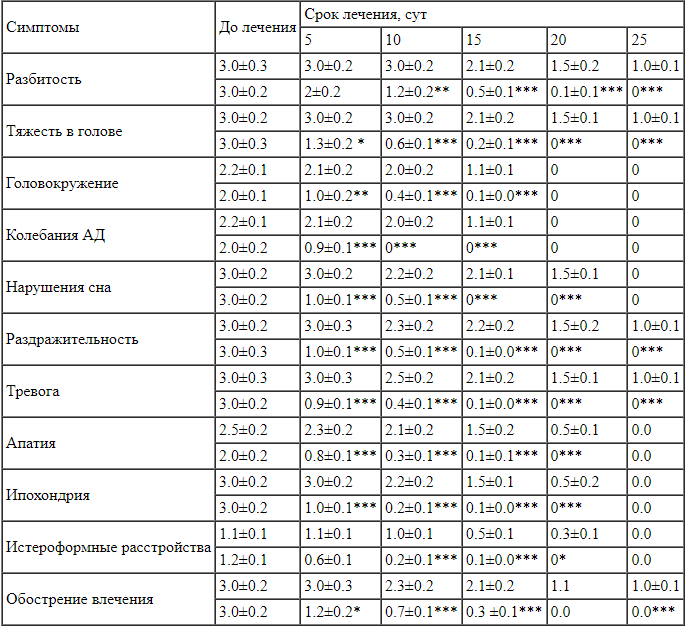 Примечание. *р<0.05, **р<0.01, ***р<0.001 по сравнению с лечением по стандартной методике.
Примечание. *р<0.05, **р<0.01, ***р<0.001 по сравнению с лечением по стандартной методике.
Сравнение поведения больных в отделении выявило, что больные основной группы раньше становились способны к социально-нормативному поведению, к конструктивным и продуктивным действиям в лечебно-реабилитационном процессе. Меньшая степень седации позволяла им сохранять более высокий уровень внимания, целенаправленности мышления и поведения. У них с первой недели лечения появлялось стремление выполнять гигиенические процедуры, поддерживать опрятность в одежде и в палате. На беседах они были более активны и заинтересованы, сами задавали вопросы о своих перспективах, в том числе социальных. Речь у них была более нормативной по подбору слов, с более четкими формулировками ответов на тестовые вопросы. Отношения с родственниками и с людьми из микросоциального окружения для них были более значимы, чем в группе сравнения. В лечебном процессе они проявляли инициативу в диагностических и лечебных процедурах, были более открыты, доступны и синтонны на занятиях с психологом и психотерапевтом. Они проявляли готовность к разработке планов не только соматического оздоровления, но и трудоустройства, создания семьи, повышения образования, социального, морального и духовного уровня. У пациентов этой группы на ранних этапах реабилитации, в течение 1 мес, удавалось сформировать стойкие мотивации на трезвый, здоровый образ жизни с актуализацией социальных и духовных потребностей.
Описанная положительная динамика отмечена у 18 пациентов (90%) группы. У 2 больных (10%) не удалось сформировать мотивации к отказу от наркотиков на всю жизнь, преодолеть безразличия к своему настоящему и будущему, эгоистически-иждивенческого отношения к медикам и родителям. Во время лечения они заявляли, что в настоящее время наркотизация для них не актуальна, но кардинально изменить образ жизни, круг друзей и занятий они не готовы. То есть, при наличии у пациентов высокого реабилитационного потенциала, особенно социального и духовного компонентов, лечение мексидолом и конвульсаном способствовало его реализации, а при низком реабилитационном потенциале положительные результаты фармакотерапии ограничивались улучшением со стояния больных на соматическом уровне.
Заключение
Сравнение фармакотерапевтических эффектов комплекса мексидола с конвульсаном и стандартной терапии больных ОН на этапах острой абстиненции и постабстинентных расстройств показало, что структура фармакотерапевтических эффектов зависела от фармакодинамических свойств препаратов. В структуре полученного результата лечения можно выделить два вида эффектов: нейромедиаторные и метаболические. Нейромедиаторные эффекты связаны с нормотимическим действием конвульсана в форме более быстрой и полной редукции психопатологических, соматовегетативных расстройств и стабилизации настроения. Метаболические эффекты, обусловленные применением мексидола, проявились более ранним восстановлением когнитивных функций, адекватной поведенческой активности, появлением интереса к собственной жизни и близкому окружению, расширением круга интересов. Благодаря более быстрому переходу с биологического уровня на социальный и духовный, реабилитационный потенциал больных реализуется в более полной степени, чем при стандартной терапии.
Литература
1. Альтшулер В.Б. Лекции по наркологии / Под ред. Н.Н.Иванца. М., 2000. С. 16-33.
2. Анохина И.П. // Руководство по наркологии / Под ред. Н.Н.Иванца. М., 2002. Т. 1. С. 33-41.
3. Винникова М.А., Агибалова Т.В., Гуревич Г.Л., Мищенко Л.В. // Психиатрия и психофармакотерапия. 2004. Т. 6, № 5. С. 245-248.
4. Дудко Т.Н., Райзман Е.М., Белокрылов И.В. и др. Реабилитация наркологических больных в условиях стационаров. Методические рекомендации. М., 2006.
5. Дудко Н.Н., Пузенко В.А., Меликова Е.Э., Алексеева Ю.А. Применение мексидола в комплексном лечении и реабилитации больных опийной (героиновой) наркоманией. Пособие для врачей психиатров-наркологов. М., 2001.
6. Иванец Н.Н., Винникова М.А. // Руководство по наркологии / Под ред. Н.Н.Иванца. М., 2002. Т. 2. С. 6-24.
7. Карпов А.М. Самозащита от саморазрушения. Образовательно-воспитательные основы профилактики и психотерапии зависимостей и стрессов. М., 2005.
8. Карпов А.М., Мельников М.А., Фаттахов Ф.З. // Неврол. вестн. 2010. Т. ХLII, Вып. 2. C. 38-42.
9. Рохлина М.Л., Козлов А.А. Наркомании. Медицинские и социальные последствия. Лечение. М., 2001.
