Подходы к фармакотерапии сосудистых умеренных когнитивных нарушений у пациентов различных возрастных групп
СтатьиВ.В. ЗАХАРОВ1, А.И. ФЕДИН2, Э.А. МХИТАРЯН2, 3
1ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия;
2ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия;
3Российский геронтологический научно-клинический центр ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия
В статье обсуждаются возможности фармакотерапии сосудистых умеренных когнитивных нарушений в различных возрастных группах. Приводятся результаты двойного слепого рандомизированного клинического исследования МЕМО с использованием антиоксидантного и антигипоксантного препарата Мексидол. С использованием комплекса тестов для оценки когнитивных функций показана высокая эффективность последовательного назначения парентеральной и пероральной форм Мексидола в каждой из трех анализируемых групп: 40—60, 61—75 и 76—-90 лет. Во всех возрастных группах Мексидол продемонстрировал высокий профиль безопасности.
Ключевые слова: сосудистые умеренные когнитивные нарушения, хроническая ишемия мозга, антиоксиданты, Мексидол.
Захаров В.В. — orcid.org/0000-0002-8447-3264
Федин А.И. — orcid.org/0000-0002-6996-2828
Мхитарян Э.А. — orcid.org/0000-0003-2597-981X
Автор, ответственный за переписку: Федин А.И. — e-mail: fedin.anatoly@gmail.com
Как цитировать: Захаров В.В., Федин А.И., Мхитарян Э.А. Подходы к фармакотерапии сосудистых умеренных когнитивных нарушений у пациентов различных возрастных групп. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(10):1—7. doi.org/10.17116/jnevro20231231011
Современная демографическая ситуация характеризуется беспрецедентным постарением населения. Согласно отчету ООН за 2019 г., численность лиц старше 60 лет растет быстрее, чем других возрастных групп [1]. Более 1/4 населения Европы (190 млн человек) уже достигли возраста старше 60 лет, доля россиян старше 65 лет в 2021 г. составила 15,8% [1, 2]. Самой быстрорастущей является группа населения в возрасте старше 80 лет, ожидается, что с 2015 по 2050 г. их число в мире увеличится более чем в 3 раза (со 125 до 434 млн) [3].
Увеличение продолжительности жизни сопровождается ростом распространенности когнитивных расстройств (КР) разной степени тяжести. В настоящее время деменцией в мире страдают примерно 50 млн человек, а к 2050 г. ожидается возрастание данного показателя до 132 млн [4]. Российская Федерация (РФ) входит в десятку стран, лидирующих по числу лиц с деменцией [5, 6], а их средний возраст в РФ (67 лет при болезни Альцгеймера (БА) и 75 лет при сосудистой деменции) ниже, чем в других европейских странах [7]. Деменция в подавляющем большинстве случаев носит необратимый характер, поэтому особое внимание врачей и исследователей в последние годы привлекают додементные стадии церебральных заболеваний. Обычно деменции предшествуют умеренные КР (УКР), распространенность которых примерно в 4 раза выше, чем деменции [8, 9]. Среди лиц старше 60 лет распространенность УКР составляет 6,7—25,2%, а после 65 лет увеличивается с каждым последующим годом жизни примерно на 1% [10]. Прогноз при УКР лучше, чем при деменции, так как при соответствующей коррекции факторов риска и адекватной терапии у 40% пациентов наблюдается регресс имеющихся нарушений [11].
В настоящее время не разработан единый подход к ведению пациентов с УКР [12]. Не вызывает сомнений целесообразность применения таких немедикаментозных методов лечения и профилактики, как когнитивный тренинг, регулярные физические упражнения и включение в рацион питания продуктов, богатых антиоксидантами (витамины C и E) [13, 14]. Данные об эффективности фармакотерапии противоречивы. Несмотря на большое количество препаратов, предложенных для профилактики/лечения БА, подавляющее большинство из них потерпело в клинических исследованиях неудачу [15, 16]. Не лучше складывается ситуация с препаратами для лечения сосудистой деменции. Недавние исследования продемонстрировали, что появлению характерных для БА амилоидных бляшек и нейрофибриллярных клубочков предшествуют патологические сосудистые изменения [17—19]. Результаты экспериментальных исследований показали, что отсутствие терапии сосудистых КР может быть причиной неэффективности перспективных препаратов для лечения БА [17—19].
С этой точки зрения большой интерес представляют результаты апостериорного анализа международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования МЕМО, в котором оценивались эффективность и безопасность последовательной терапии пациентов разных возрастных групп с хронической ишемией мозга (ХИМ) препаратами Мексидол (этилметилгидроксипиридина сукцинат) и Мексидол ФОРТЕ 250 [20, 21].
Эффективность Мексидола у пациентов с острыми и хроническими нарушениями мозгового кровообращения подтверждена результатами многочисленных исследований, в том числе с использованием двойного слепого дизайна [22—24]. Препарат отвечает основным критериям, предъявляемым к препаратам для лечения пациентов пожилого и старческого возраста. Механизм его действия обусловлен сочетанием антиоксидантного, ан-тигипоксантного и мембранопротективного эффектов. Наиболее значимыми клиническими эффектами являются нейропротективный, антиамнестический, анксиолитический, антистрессорный, антиатеросклеротический, антиагрегантный, вегетотропный и др. Профиль фармакологического воздействия позволяет применять Мексидол при сердечно-сосудистых заболеваниях [25, 26], острой и хронической цереброваскулярной патологии [27, 28], в офтальмологии [29, 30]. Мультимодальность действия Мексидола позволяет сократить количество получаемых пациентом препаратов или их дозы, снижая, таким образом, риск развития нежелательных явлений (НЯ) и неблагоприятных последствий лекарственных взаимодействий и повышая приверженность пациентов лечению. Мексидол совместим со всеми препаратами для лечения соматической патологии. При его применении не зафиксировано нежелательных лекарственных взаимодействий с препаратами базисной терапии [31]. Безопасность и хорошая переносимость Мексидола пожилыми пациентами была продемонстрирована во всех его исследованиях. Так, субанализ рандомизированного двойного слепого мультицентрового плацебо-контролируемого исследования ЭПИКА показал сопоставимую клиническую эффективность и безопасность Мексидола в остром и раннем восстановительном периодах полушарного ишемического инсульта у пациентов разных возрастных групп — молодого и среднего (до 60 лет), пожилого (60—75 лет) и старческого (76—90 лет) возраста [32].
В 2021 г. были опубликованы результаты исследования МЕМО, проведенного в 15 клинических центрах РФ и Республике Узбекистан [20]. В исследовании приняли участие 318 пациентов в возрасте от 40 до 90 лет с синдромом УКР на фоне ХИМ. Пациенты основной группы получали Мексидол внутривенно в дозе 500 мг 1 раз в сутки на протяжении 14 сут, а затем Мексидол ФОРТЕ 250 внутрь по 250 мг 3 раза в сутки в течение последующих 60 сут. Пациенты группы сравнения получали аналогичное по внешнему виду плацебо. Первичной конечной точкой эффективности была выбрана динамика значений (абсолютная разница между суммой баллов до начала лечения и на 75-й день терапии) по Монреальской шкале оценки когнитивных функций (MoCA). Значения по шкале MoCA <25 баллов явились критерием включения в исследование. Когнитивные функции оценивались также на основании динамики результатов теста замены цифровых символов (англ.: Digit Symbol Substitution Test, DSST), который позволяет оценить темп умственной деятельности, концентрацию внимания, управляющие функции (планирование и контроль) и оперативную память, показатели его динамики рассматривались в качестве вторичной конечной точки.
Было продемонстрировано статистически значимое преимущество последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 над плацебо по достижении первичной конечной точки (p<0,000001), тесту DSST, а также ряду других критериев, позволявших оценить двигательные функции, выраженность вегетативных нарушений, астении, тревожности и качество жизни. Профиль безопасности последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 в общей группе пациентов не отличался от такового у плацебо [20].
Апостериорный анализ показателей эффективности последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 проводился в трех возрастных подгруппах: 40—60 (n=163), 61—75 (n=141) и 76—90 (n=13) лет [21]. Исходная тяжесть КР в каждой из них была сопоставима в основной группе и группе сравнения (табл. 1). В подгруппе 40—60 лет основной группы к концу исследования (через 75 дней) сумма баллов по шкале MoCA оказалась больше, а доля пациентов с КР — в 1,7 раза меньше, чем в группе плацебо. Аналогичные результаты получены и в подгруппе 61—75 лет, у которых к окончанию исследования число пациентов с КР снизилось в 1,5 по сравнению с группой сравнения. В подгруппу 76—90 лет были включены небольшое число участников, тем не менее анализ с использованием методов непараметрической статистики показал, что через 75 дней применения препаратов Мексидол и Мексидол ФОРТЕ 250 доля больных с УКР уменьшилась на 1/3, а в группе сравнения осталась неизменной. В данной подгруппе наблюдалась тенденция к изменению показателей первичной конечной точки, сходная с двумя другими возрастными группами, однако из-за малого количества наблюдений различия не достигали статистической значимости. Динамика значений по шкале MoCA в разных возрастных подгруппах представлена на рис. 1—3.
Таблица 1. Динамика изменения когнитивных функций при оценке по шкале MoCA в разных возрастных подгруппах, баллы, Me [Q25%; Q75%].
Table 1. Dynamics of changes in cognitive functions as assessed by the MoCA scale in different age groups, points, Me [Q25%; Q75%]
|
Показатель |
Основная группа |
Группа сравнения |
p |
|
Подгруппа 40—60 лет |
|||
|
исходно |
22,5 [21; 24] |
23 [21; 24] |
0,656 |
|
через 75 дней |
26 [25; 28] |
24 [23; 26] |
<0,001 |
|
абсолютная разница |
4 [3; 5] |
2 [1; 3] |
<0,001 |
|
p исходно -75 дней |
<0,001 |
<0,001 |
— |
|
Подгруппа 61—75 лет |
|||
|
исходно |
21 [19; 23] |
22 [21; 23] |
0,524 |
|
через 75 дней |
25 [23; 27] |
24 [22; 25] |
0,002 |
|
абсолютная разница |
4 [2; 6] |
3 [1; 3] |
<0,001 |
|
p исходно -75 дней |
<0,001 |
<0,001 |
— |
|
Подгруппа 76—90 лет |
|||
|
исходно |
18 [17; 18] |
19 [17; 20] |
0,253 |
|
через 75 дней |
24 [22; 26] |
21 [21; 24] |
0,153 |
|
абсолютная разница |
7 [6; 7] |
2 [1; 5] |
0,054 |
|
p исходно -75 дней |
0,028 |
0,018 |
— |
Рис. 1. Динамика значений по шкале MoCA в подгруппе пациентов 40—60 лет, баллы, Me [Q25%; Q75%].
Fig. 1. Dynamics of scores on the MoCA scale in patients aged 40—60 years, points, Me [Q25%; Q75%].
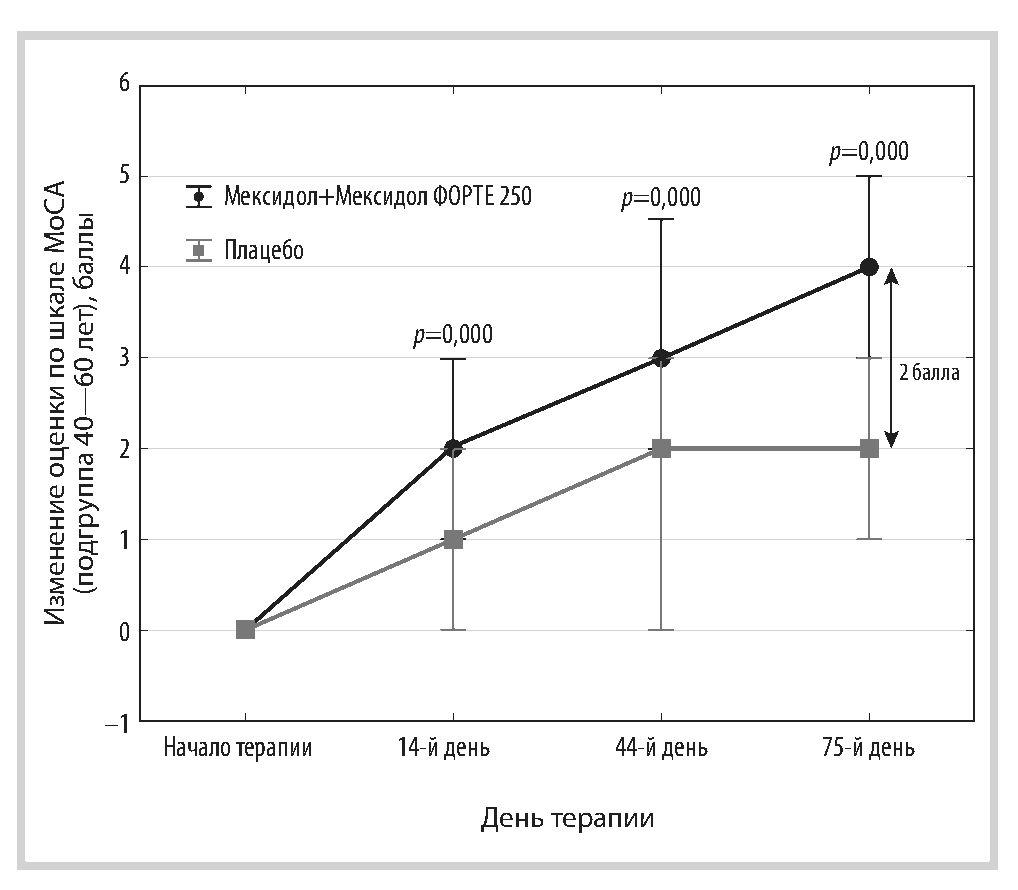
 Рис. 2. Динамика значений по шкале MoCA в подгруппе пациентов 61—75 лет, баллы, Me [Q25%; Q75%].
Рис. 2. Динамика значений по шкале MoCA в подгруппе пациентов 61—75 лет, баллы, Me [Q25%; Q75%].
Fig. 2. Dynamics of scores on the MoCA scale in patients aged 61—75 years, points, Me [Q25%; Q75%].
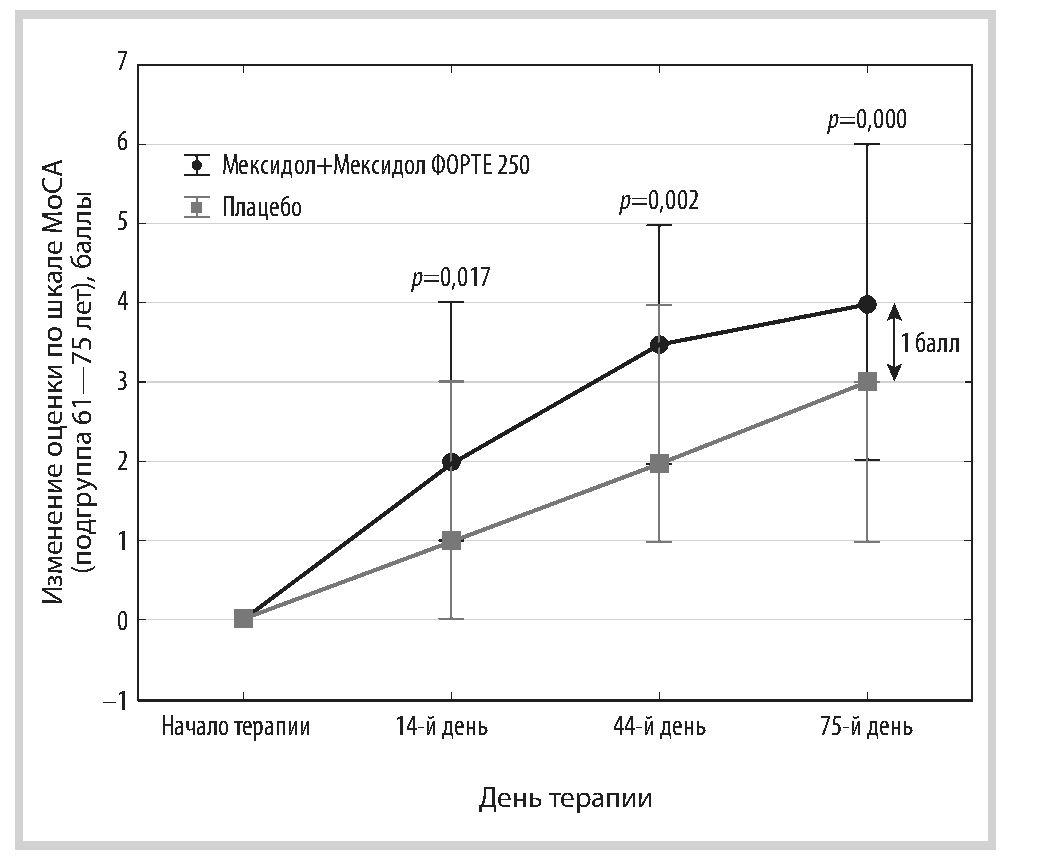
 Рис. 3. Динамика значений по шкале MoCA в подгруппе пациентов 76—90 лет, баллы, Me [Q25%; Q75%].
Рис. 3. Динамика значений по шкале MoCA в подгруппе пациентов 76—90 лет, баллы, Me [Q25%; Q75%].
Fig. 3. Dynamics of scores on the MoCA scale in patients aged 76—90 years, Me [Q25%; Q75%].
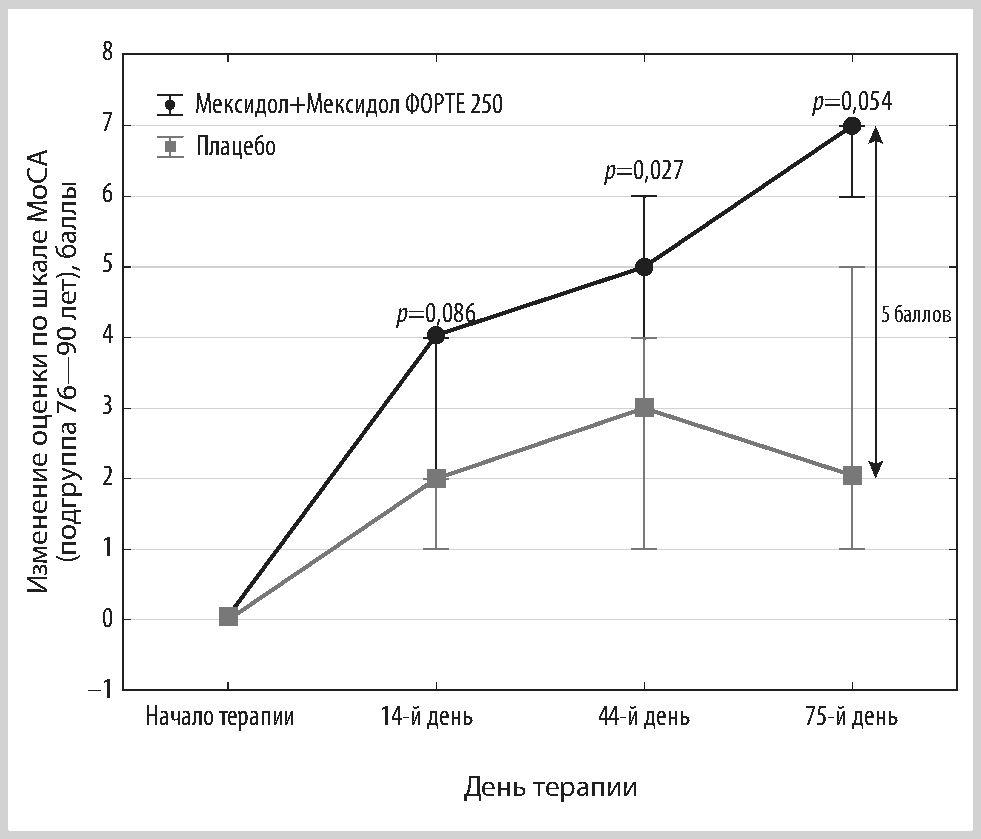
Таблица 2. Динамика изменения когнитивных функций при оценке по тесту DSST в подгруппах 40—60 и 61—75 лет, баллы, Me [Q25%; Q75%]
Table 2. Dynamics of changes in cognitive functions when assessed by the DSST test in the age groups 40—60 and 61—75 years, points, Me [Q25%; Q75%]
|
Показатель |
Основная группа |
Группа сравнения |
p |
|
Подгруппа 40—60 лет |
|||
|
исходно |
35 [28,5; 41,5] |
35 [27; 41] |
0,829 |
|
через 75 дней |
46 [36; 53] |
39 [30; 47] |
0,004 |
|
абсолютная разница |
6,5 [3,5; 16] |
5 [1; 8] |
0,003 |
|
p исходно -75 дней |
<0,001 |
<0,001 |
— |
|
Подгруппа 61—75 лет |
|||
|
исходно |
30 [24; 36] |
33,5 [25,5; 39,5] |
0,166 |
|
через 75 дней |
39,0 [30; 51] |
39 [30; 48] |
0,486 |
|
абсолютная разница |
8 [4; 15] |
4 [0; 12] |
0,016 |
|
p исходно -75 дней |
<0,001 |
<0,001 |
— |
Динамика результатов выполнения теста DSST в подгруппах 40—60 и 61—75 лет представлена в табл. 2. Несмотря на то что положительная динамика наблюдалась в обеих группах, ее выраженность была достоверно большей в основной группе. Различия абсолютной динамики баллов выполнения теста DSST на последнем визите, по сравнению с исходным уровнем, между группами были статистически значимыми.
В подгруппе 76—90 лет (табл. 3) в связи с небольшим числом участников рассчитывалась не медиана, а средняя арифметическая и стандартное отклонение (M±SD), статистическая значимость различий оценивалась по критерию Стьюдента. Динамика баллов теста DSST в трех подгруппах представлена на рис. 4—6.
Таким образом, проведенный субанализ показал клиническую эффективность последовательной терапии препаратами Мексидол в дозе 500 мг внутривенно в течение 14 дней и Мексидол ФОРТЕ 250 по 250 мг 3 раза в день в течение 60 дней в отношении УКР сосудистой этиологии на фоне ХИМ. Были показаны как достоверное улучшение интегрального показателя состояния когнитивных функций (шкала MoCA), так и положительная динамика в специфических для цереброваскулярного заболевания доменах (внимание и управляющие функции).
Таблица 3. Динамика результатов выполнении теста DSST в подгруппе 71—90 лет, баллы, M±SD
Table 3. Dynamics of changes in DSST test in the age group 71—90 years, points, M±SD
Показатель | Основная группа | Группа сравнения | p |
Исходно | 24,7±11,8 | 25,1±5,7 | 0,926 |
Через 75 дней | 37,8±12,1 | 28,9±5,8 | 0,107 |
Абсолютная разница | 13,2±8,0 | 3,7±6,1 | 0,035 |
p исходно -75 дней | <0,001 | <0,001 | — |
Рис. 4. Динамика баллов по тесту DSST в подгруппе 40—60 лет, Me [Q25%; Q75%].
Fig. 4. Dynamics of scores on the test of DSST in the population of patients aged 40—60 years, Me [Q25%; Q75%].
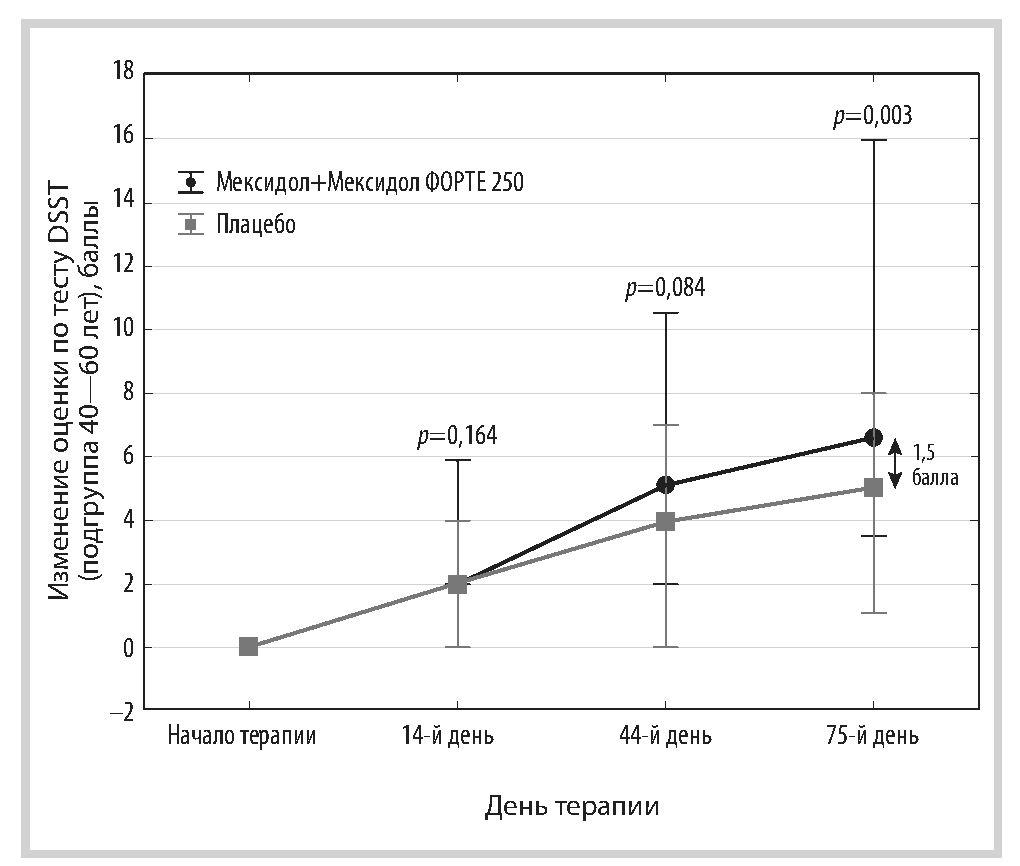
Рис. 5. Динамика баллов по тесту DSST в подгруппе 61—75 лет, Me [Q25%; Q75%].
Fig. 5. Dynamics of scores on the test for DSST in a population of patients aged 61—75 years, Me [Q25%; Q75%].
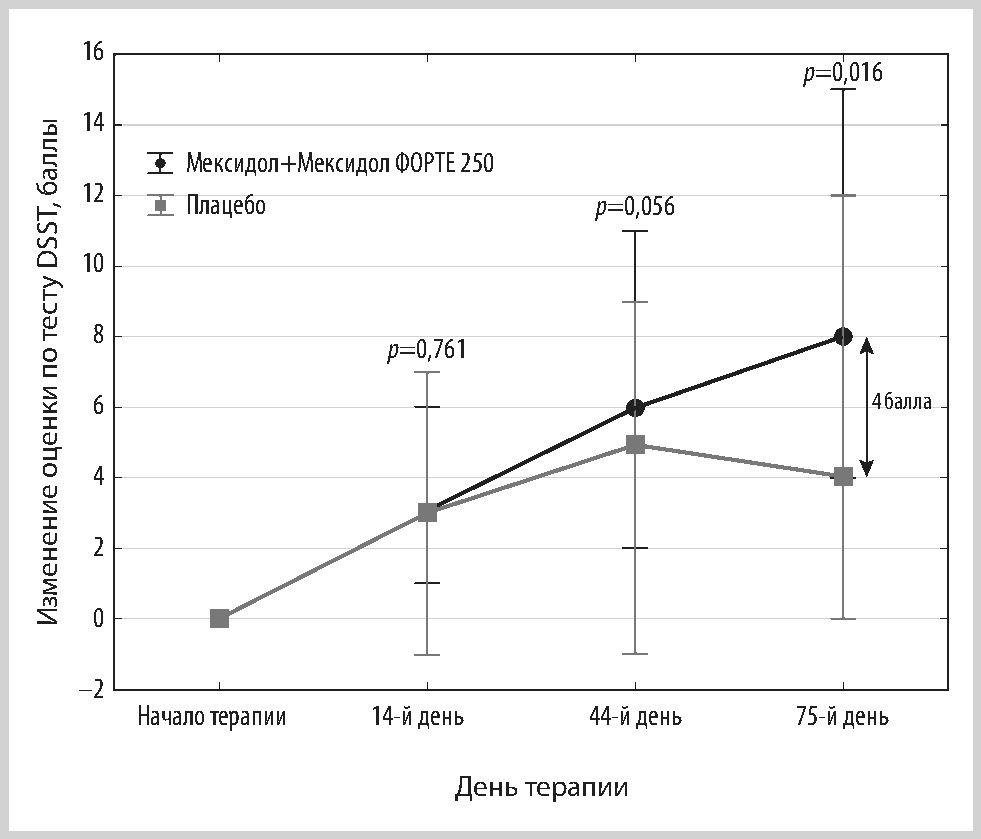
 Рис. 6. Динамика значений выполнения теста DSST в подгруппе 76—90 лет (M±SD).
Рис. 6. Динамика значений выполнения теста DSST в подгруппе 76—90 лет (M±SD).
Fig. 6. Dynamics of scores on the test of DSST in the population of patients aged 76—90 years (M±SD).
Следует подчеркнуть, что до настоящего времени медикаментозная терапия ХИМ проводится главным образом, исходя из теоретических представлений о патогенезе повреждения нейронов при хронической ишемии и механизмов действия лекарственных препаратов. В то же время количество рандомизированных клинических исследований лекарственных препаратов, подтверждающих теоретические предпосылки, невелико, они касаются главным образом сосудистой деменции или постинсультных КР. Таким образом, результаты исследования МЕМО представляют собой важный этап в обосновании терапии ХИМ в соответствии с современными принципами медицины, основанной на доказательствах.
Заключение
Проведенный субанализ свидетельствует, что последовательная терапия препаратами Мексидол и Мексидол ФОРТЕ 250 оказывает сопоставимый клинический эффект у пациентов различных возрастных групп, включая больных старческого возраста. Поскольку последняя группа включала небольшое число участников, изучение эффективности Мексидола в этой возрастной категории следует продолжить в последующих исследованиях. Как в исследовании МЕМО [20, 21], так и в предыдущих рандомизированных клинических исследованиях (ЭПИКА), количество значимых НЯ при применении Мексидола не отличалось от группы плацебо. При этом профиль безопасности и переносимости был сопоставимым в различных возрастных группах [22, 32].
Полученные данные о клинической эффективности, безопасности и переносимости последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 позволяют рекомендовать данную схему для лечения сосудистых КР, не достигающих выраженности деменции, пациентам различных возрастных групп, в том числе старческого возраста.
Авторы заявляют об отсутствии конфликта интересов. The authors declare no conflicts of interest.
ЛИТЕРАТУРА/REFERENCES
1. Krivanek TJ, Gale SA, McFeeley BM, et al. Promoting Successful Cogni- tive Aging: A Ten-Year Update. J Alzheimers Dis. 2021;81(3):871-920. https://doi.org/10.3233/JAD-201462
2. Численность населения Российской Федерации по полу и возрасту на 1 ян- варя 2021 года. Ссылка доступна на 23.06.23. The population of the Russian Federation by gender and age as of January 1, 2021. The link is available on 06/23/2023. (In Russ.). https://rosstat.gov.ru/storage/mediabank/Bul_chislen_nasel-pv_01-01-2021.pdf
3. Ukkonen M, Jämsen E, Zeitlin R, et al. Emergency department visits in old- er patients: a population-based survey. BMC Emerg Med. 2019;19(1):20. https://doi.org/10.1186/s12873-019-0236-3
4. Wetterberg H, Najar J, Rydén L, et al. Dementia remains the major predictor of death among octogenarians. A study of two population cohorts of 85-year- olds examined 22 years apart. Eur J Epidemiol. 2021;36(5):507-517. https://doi.org/10.1007/s10654-021-00745
5. GBD 2016 Neurology Collaborators (2019) Global, regional, and national burden of neurological disorders, 1990—2016: A systematic analysis for the Global Burden of Disease Study. Lancet Neurol. 2016;23(18):459-480.
6. Мхитарян Э.А., Воробьева Н.М., Ткачева О.Н. и др. Распространен- ность когнитивных нарушений и их ассоциация с социально-эконо- мическими, демографическими и антропометрическими факторами и гериатрическими синдромами у лиц старше 65 лет: данные россий- ского эпидемиологического исследования ЭВКАЛИПТ. Неврология, нейропсихиатрия, психосоматика. 2022;14(3):44-53.Mkhitaryan EA, Vorobieva NM, Tkacheva ON, et al. Prevalence of cognitive impairments and their association with socioeconomic, demographic and anthropometric factors and geriatric syndromes in persons over 65 years of age: data from the Russian epidemiological study EUCALYPTUS. Neurolo- gy, Neuropsychiatry, Psychosomatics. 2022;14(3):44-53. (In Russ.). https://doi.org/10.14412/2074-2711-2022-3-44-53
7. Kostev K, Osina G. Treatment Patterns of Patients with All-Cause Demen- tia In Russia. J Alzheimers Dis Rep. 2020;4(1):9-14. https://doi.org/10.3233/ADR-190144
8. Пилипович А.А., Воробьева О.В. Умеренные когнитивные расстрой- ства: современные аспекты диагностики и терапии. Журнал невроло- гии и психиатрии им. С.С. Корсакова. 2020;120(11):124-130. Pilipovich AA, Vorobieva OV. Moderate cognitive disorders: modern aspects of diagnosis and therapy. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2020;120(11):124-130. (In Russ.). https://doi.org/10.17116/jnevro2020120111124
9. Старчина Ю.А. Недементные когнитивные нарушения: современ- ный взгляд на проблему. Неврология, нейропсихиатрия, психосомати- ка. 2017;9(2):71-76. Starchina YuA. Non-Demented Cognitive Impairment: A Modern View On The Problem. Neurology, Neuropsychiatry, Psychosomatics. 2017;9(2):71-76. (In Russ.).
10. Eshkoor SA, Hamid TA, Mun CY, et al. Mild cognitive impairment and its management in older people. Clin Interv Aging. 2015;10:687-693. https://doi.org/10.2147/CIA.S73922
11. Jongsiriyanyong S, Limpawattana P. Mild Cognitive Impairment in Clin- ical Practice: A Review Article. Am J Alzheimers Dis Other Demen. 2018;33(8):500-507. https://doi.org/10.1177/1533317518791401
12. Щепанкевич Л.А., Грибачева И.А., Попова Т.Ф. и др. Вопросы тера- пии умеренных когнитивных нарушений. Неврология, нейропсихиа- трия, психосоматика. 2022;14(6):110-114. Shchepankevich LA, Gribacheva IA, Popova TF, et al. Questions of thera- py of moderate cognitive impairments. Neurology, Neuropsychiatry, Psycho- somatics. 2022;14(6):110-114. (In Russ.). https://doi.org/10.14412/2074-2711-2022-6-110-114
13. Новикова М.С., Захаров В.В., Вахнина Н.В. Эффективность комби- нации нелекарственных методов у пациентов с недементными сосу- дистыми когнитивными нарушениями. Неврология, нейропсихиатрия, психосоматика. 2023;15(1):57-64. Novikova MS, Zakharov VV, Vakhnina NV. The effectiveness of a combination of non-drug methods in patients with non-dementic vascular cognitive impairment. Neurology, Neuropsychiatry, Psychosomatics. 2023;15(1):57-64. (In Russ.). https://doi.org/10.14412/2074-2711-2023-1-57-64
14. Ngandu T, Lehtisalo J, Solomon A, et al. A 2 year multidomain interven- tion of diet, exercise, cognitive training, and vascular risk monitoring ver- sus control to prevent cognitive decline in at-risk elderly people (FINGER): a randomized controlled trial. Lancet. 2015;385(9984):2255-2263. https://doi.org/10.1016/S0140-6736(15)60461-5
15. Cummings J. Drug Development for Psychotropic, Cognitive-Enhancing, and Disease-Modifying Treatments for Alzheimer’s Disease. J Neuropsychi- atry Clin Neurosci. 2021;33(1):3-13. https://doi.org/10.1176/appi.neuropsych.20060152
16. Cummings JL, Morstorf T, Zhong K. Alzheimer’s disease drug-development pipeline: few candidates, frequent failures. Alzheimers Res Ther. 2014;6(4):37. https://doi.org/10.1186/alzrt269
17. Linton AE, Weekman EM, Wilcock DM. Pathologic sequelae of vascular cognitive impairment and dementia sheds light on potential targets for in- tervention. Cereb Circ Cogn Behav. 2021;2:100030. https://doi.org/10.1016/j.cccb.2021.100030
18. Vemuri P, Knopman DS. The role of cerebrovascular disease when there is concomitant Alzheimer disease. Biochim Biophys Acta. 2016;1862(5):952-956. https://doi.org/10.1016/j.bbadis.2015.09.013
19. Николенко В.Н., Ризаева Н.А., Булыгин К.В. и др. Роль оксидатив- ного стресса в развитии болезни Альцгеймера. Неврология, нейропси- хиатрия, психосоматика. 2022;14(4):68-74. Nikolenko VN, Rizaeva NA, Bulygin KV, et al. The role of oxidative stress in the development of Alzheimer’s disease. Neurology, Neuropsychiatry, Psy- chosomatics. 2022;14(4):68-74. (In Russ.). https://doi.org/10.14412/2074-2711-2022-4-68-74
20. Федин А.И., Захаров В.В., Таняшян М.М. и др. Результаты между- народного многоцентрового рандомизированного двойного слепо- го плацебо-контролируемого исследования оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами мексидол и мексидол форте 250 (иссле- дование МЕМО). Журнал неврологии и психиатрии им. С.С.Корсакова. 2021;121(11):7-16. Fedin AI, Zakharov VV, Tanyashyan MM, et al. Results of an international multicenter, randomized, double-blind, placebo-controlled study of the ef- ficacy and safety of sequential therapy of patients with chronic cerebral isch- emia with Mexidol and Mexidol forte 250 (MEMO study). Zhurnal Nevrolo- gii i Psikhiatrii im. S.S. Korsakova. 2021;121(11):7-16. (In Russ.). https://doi.org/10.17116/jnevro20211211117
21. Захаров В.В., Ткачева О.Н., Мхитарян Э.А., Федин А.И. Эффек- тивность М ексидола у пациентов разных возрастных групп с хро- нической ишемией головного мозга и когнитивными нарушения- ми (результаты субанализа международного многоцентрового ран- домизированного двойного слепого плацебо-контролируемого исследования МЕМО). Журнал неврологии и психиатрии им. С.С. Кор- сакова. 2022;122(11 вып. 2):1-8. Zakharov VV, Tkacheva ON, Mkhitaryan EA, Fedin AI. The effectiveness of Mexidol in patients of different age groups with chronic cerebral isch- emia and cognitive impairment (results of a sub-analysis of the internation- al multicenter randomized, double-blind, placebo-controlled study ME- MO). Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2022;122(11-2):1-8. (In Russ.). https://doi.org/10.17116/jnevro202212211273https://doi.org/10.17116/jnev- ro2022121121
22. Стаховская Л.В., Шамалов Н.А., Хасанова Д.Р. и др. Результаты ран- домизированного двойного слепого мультицентрового плацебо-кон- тролируемого в параллельных группах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(3-2):55-65.Stakhovskaya LV, Shamalov NA, Khasanova DR, et al. Results of a random- ized, double-blind, multicenter, placebo-controlled, parallel-group study of the efficacy and safety of mexidol in long-term sequential therapy in patients in the acute and early recovery periods. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2017;117(3-2):55-65. (In Russ.). https://doi.org/10.17116/jnevro20171173255-65
23. Чуканова Е.И., Чуканова А.С. Эффективность и безопасность препа- рата Мексидол ФОРТЕ 250 в рамках последовательной терапии у па- циентов с хронической ишемией мозга. Журнал неврологии и психиа- трии им. С.С. Корсакова. 2019;119(9):39-45. Chukanova EI, Chukanova AS. Efficacy and safety of Mexidol FORTE 250 in sequential therapy in patients with chronic cerebral ischemia. Zhur- nal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2019;119(9):39-45. (In Russ.). https://doi.org/10.17116/jnevro201911909139
24. Журавлева М.В., Прокофьев А.Б., Сереброва С.Ю. и др. Эффектив- ность и безопасность применения этилметилгидроксипиридина сук- цината у пациентов с хронической ишемией головного мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(6):119-124. Zhuravleva MV, Prokofiev AB, Serebrova SYu, et al. Efficacy and safety of ethylmethylhydroxypyridine succinate in patients with chronic cerebral isch- emia. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2020;120(6):119-124. (In Russ.). https://doi.org/10.17116/jnevro2020120061119
25. Оганов Р.Г. Положительный опыт применения этилметилгидрокси- пиридина сукцината в лечении кардиологических больных. Кардиова- скулярная терапия и профилактика. 2017;16(5):91-94. Oganov RG. Positive experience of using ethylmethylhydroxypyridine suc- cinate in the treatment of cardiac patients. Cardiovascular therapy and pre- vention. 2017;16(5):91-94. (In Russ.). https://doi.org/10.15829/1728-8800-2017-5-91-94
26. Толкачева В.В., Казахмедов Э.Р., Кобалава Ж.Д. и др. Влияние Мексидола на качество жизни и функциональный статус пациентов с хронической ишемией головного мозга и хронической сердечной не- достаточностью с низкой фракцией выброса. Кардиология и сердечно- сосудистая хирургия. 2021;14(1):80-89. Tolkacheva VV, Kazakhmedov ER, Kobalava ZhD, et al. Influence of Mex- idol on the quality of life and functional status of patients with chronic cere- bral ischemia and chronic heart failure with low ejection fraction. Cardiolo- gy and Cardiovascular Surgery. 2021;14(1):80-89. (In Russ.). https://doi.org/10.17116/kardio20211401180
27. Мартынов М.Ю., Журавлева М.В., Васюкова Н.С. и др. Окислитель- ный стресс в патогенезе церебрального инсульта и его коррекция. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(1):16-27. Martynov MYu, Zhuravleva MV, Vasyukova NS, et al. Oxidative stress in the pathogenesis of cerebral stroke and its correction. Zhurnal Nevrologii i Psikh- iatrii im. S.S. Korsakova. 2023;123(1):16-27. (In Russ.). https://doi.org/10.17116/jnevro202312301116
28. Журавлева М.В., Камчатнов П.Р., Васюкова Н.С. и др. Результаты клинических исследований эффективности и безопасности примене- ния препаратов этилметилгидроксипиридина сукцината у пациентов с хронической ишемией головного мозга. Журнал неврологии и психи- атрии им. С.С. Корсакова. 2022;122(11):29-39. Zhuravleva MV, Kamchatnov PR, Vasyukova NS, et al. Results of clinical studies of the efficacy and safety of the use of ethylmethylhydroxypyridine succinate preparations in patients with chronic cerebral ischemia. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2022;122(11):29-39. (In Russ.). https://doi.org/10.17116/jnevro202212211129
29. Леонова Е.С., Поляков С.В., Позднякова М.А. и др. Опыт нейропро- текторной терапии первичной открытоугольной глаукомы на осно- ве применения различных форм М ексидола. Вестник офтальмологии. 2015;6:90-93. Leonova ES, Polyakov SV, Pozdnyakova MA, et al. Experience in neuro- protective therapy of primary open-angle glaucoma based on the use of var- ious forms of Mexidol. Bulletin of Ophthalmology. 2015;6:90-93. (In Russ.).
30. Мовсисян А.Б., Оганезова Ж.Г., Егоров Е.А. Возможности и резуль- таты применения антиоксидантной терапии в офтальмологической практике. Вестник офтальмологии. 2022;138(5):122-128.
Поступила 22.08.2023
Received 22.08.2023
Принята к печати 24.08.2023
Accepted 24.08.2023
Pharmacotherapy approaches to vascular mild cognitive impairment in patients of different age groups
© V.V. ZAKHAROV1, A.I. FEDIN2, E.A. MHITARYAN2, 3
- 1Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
- 2Pirogov Russian National Research Medical University, Moscow, Russia;
- 3Russian Clinical and Research Center of Gerontology, Pirogov Russian National Research Medical University, Moscow, Russia
The article discusses the possibilities of pharmacotherapy of moderate vascular cognitive impairment in different age groups. The results of a double-blind randomized clinical trial «MEMO» using the antioxidant and antihypoxic drug Mexidol are presented. On the basis of cognitive scales, when using a sequential course of parenteral and oral administration of mexidol, its reliable effectiveness was shown in each of the three analyzed groups: 40—60 years old, 61—75 years old and 76—90 years old. Mex-idol showed an optimal safety profile in all age groups.
Keywords: vascular mild cognitive impairment, chronic brain ischemia, antioxidants, Mexidol.
Information about the authors:
Zakharov V.V. — orcid.org/0000-0002-8447-3264
Fedin A.I. — orcid.org/0000-0002-6996-2828
Mhitaryan E.A. — orcid.org/0000-0003-2597-981X
Corresponding author: Fedin A.I. — e-mail: fedin.anatoly@gmail.com
To cite this article: Zakharov VV, Fedin AI, Mhitaryan EA. Pharmacotherapy approaches to vascular mild cognitive impairment in patients of different age groups. 5.5. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2023;123(10):1—7. (In Russ.). doi.org/10.17116/jnevro20231231011
