Эффективность препарата Мексидол в коррекции постковидного синдрома у пациентов с хроническими цереброваскулярными заболеваниями
СтатьиЕ.Б. КУЗНЕЦОВА, Е.А. САЛИНА, Н.С. КУЗНЕЦОВ
ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России, Саратов, Россия
Резюме
Цель исследования. Оценить эффективность последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 в коррекции постковидного синдрома (ПКС) у пациентов с хроническими цереброваскулярными заболеваниями (ХЦВЗ).
Материал и методы. Проведен анализ результатов обследования и лечения 110 пациентов с ХЦВЗ, перенесших COVID-19. Пациенты основной группы (ОГ, n=55) получали Мексидол (по 5 мл в/в капельно в течение 14 дней с последующим переходом на таблетированную форму Мексидол ФОРТЕ 250 по 1 таблетке 3 раза в сутки в течение 2 мес); 55 пациентов группы сравнения (ГС) антиоксидантов не получали. Всем включенным в исследование пациентам проведены МРТ-обследование и развернутое нейропсихологическое тестирование.
Результаты. У больных ОГ имели место значительное улучшение состояния когнитивных функций, регресс симптомов астении, улучшение ночного сна. Отличия носили статистически значимый характер по сравнению как с исходным уровнем, так и с ГС.
Заключение. Назначение препарата не требует возрастной коррекции дозы и хорошо сочетается с базисной терапией. Рекомендованная схема применения Мексидола: 14 дней по 5 мл в/в или в/м, затем прием препарата Мексидол ФОРТЕ 250 в дозе по 1 таблетке 3 раза в сутки в течение 2 мес.
Ключевые слова: хронические цереброваскулярные заболевания, постковидный синдром, Мексидол, лечение.
Информация об авторах:
Кузнецова Е.Б. — https://orcid.org/0000-0002-3979-3453
Салина Е.А. — orcid.org/0000-0002-8945-2120
Кузнецов Н.С. — orcid.org/0000-0003-4879-4121
Автор, ответственный за переписку: Кузнецова Е.Б. — e-mail: elenfeb77@mail.ru
Как цитировать:
Кузнецова Е.Б., Салина Е.А., Кузнецов Н.С. Эффективность препарата Мексидол в коррекции постковидного синдрома у пациентов с хроническими цереброваскулярными заболеваниями. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(5):117-122. https://doi.org/10.17116/jnevro2023123051117
Современным подходом к профилактике и терапии хронических цереброваскулярных заболеваний (ХЦВЗ) является контроль традиционных факторов риска с помощью фармакологического лечения и изменения образа жизни. Признаки болезни мелких сосудов выявляются при нейровизуализационном исследовании даже при отсутствии явных неврологических проявлений. Данная патология широко распространена среди стареющего населения и увеличивает риск последующего инсульта, деменции или смерти [1—3]. Пандемия COVID-19 показала, что пациенты с ХЦВЗ находятся в группе риска тяжелого течения заболевания, что явилось основанием для проведения ряда исследований, посвященных изучению причин развития, прогрессирования и декомпенсации сосудистой патологии мозга у данной категории больных [4—9]. Хотя COVID-19, вызванный вирусом SARS-CoV-2, является в первую очередь респираторным заболеванием, он может привести к разрушительным последствиям, обусловленным поражением многих систем организма, включая ЦНС [8, 9].
Установлены следующие факторы, ухудшающие течение ХЦВЗ при COVID-19: нарушение реологических свойств крови, коагулопатии, цитокиновый шторм, гипоперфузия и гипоксия мозга. На фоне коронавирусной инфекции развиваются макро- и микроангиопатии, эндотелиальная дисфункция, что приводит к тромбообра-зованию не только в сосудах легких, но и в сосудах головного мозга. Интенсивный воспалительный ответ, известный как цитокиновый шторм, может быть опосредован окислительным стрессом, вызванным повышенным уровнем активных форм кислорода. Глобальный энергодефицит, развивающийся на фоне COVID-19, является важным патогенетическим механизмом неврологических и нейрометаболических нарушений у пациентов с ХЦВЗ [7, 10, 11].
Наряду с проявлениями острой коронавирусной инфекции, все больший интерес привлекает постковидный синдром (ПКС), который характеризуется стойкими клиническими проявлениями. Данные нарушения появляются после перенесенного COVID-19, сохраняются более 12 нед и не могут быть объяснены альтернативным диагнозом. Симптомы могут носить непостоянный характер, течение ПКС может принимать рецидивирующий характер. ПКС — гетерогенное состояние, наиболее распространенными симптомами которого являются утомляемость, одышка, тревога, депрессия, нарушение внимания, концентрации, памяти и сна. Биологические механизмы развития ПКС неизвестны, наиболее вероятно, что важную роль могут играть аномальные или чрезмерные аутоиммунные и воспалительные реакции [5—7, 10].
Применение антиоксидантов при таких патологических состояниях, как сепсис, острый респираторный дистресс-синдром, острое повреждение легких, способствует регрессу части симптомов. Антиоксиданты улучшают скорость оксигенации, повышают уровень глутатиона, стабилизируют иммунный ответ. Астения, одно из наиболее частых проявлений ПКС, по данным большинства авторов, является следствием энергетического дисбаланса, причина которого — дисфункция митохондрий. Данное нарушение стимулирует образование свободных радикалов, которые оказывают прямое повреждающее действие на клетки организма [5, 6, 8—12]. Описана важная особенность препарата Мексидол — мультимодальное воздействие при гипоксии и ишемии. Препарат обладает выраженным мембранопротективным эффектом, улучшает реологические свойства крови, восстанавливает энергетические процессы в цикле Кребса [12—16]. При выборе терапевтической стратегии для пациентов с ХЦВЗ с ПКС необходимо оценивать потенциальную пользу и риски в аспекте лечебного эффекта, вероятности развития нежелательных эффектов и побочного лекарственного взаимодействия.
Цель исследования — оценить эффективность последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 в коррекции ПКС у пациентов с ХЦВЗ.
Материал и методы
Проведен анализ результатов обследования и лечения 110 пациентов с ХЦВЗ, перенесших COVID-19 не более 6 мес назад. Диагноз ХЦВЗ был подтвержден данными нейровизуализации (табл. 1). Пациенты, участвовавшие в исследовании, методом случайной выборки были разделены на две группы: 55 больных основной группы (ОГ) получали терапию антиоксидантами (препарат Мексидол вводился по 5 мл в/в капельно в течение 14 дней с последующим переходом на таблетированную форму Мексидол ФОРТЕ 250 по 1 таблетке 3 раза в сутки в течение 2 мес); 55 пациентов группы сравнения (ГС) антиоксидантов не получали. Группы сопоставимы по полу, возрасту, тяжести ПКС, клиническим проявлениям ХЦВЗ, характеру базисной терапии.
Критерии включения: наличие ХЦВЗ; возраст от 45 до 80 лет; подтвержденная перенесенная новая коронавирусная инфекция не позднее 6 мес до включения в исследование; подписанное информированное согласие на участие пациента в исследовании.
Критерии невключения: любые другие неврологические заболевания в настоящее время либо в анамнезе; выраженные когнитивные нарушения; тяжелые (декомпенсированные) соматические заболевания, а также заболевания, диагностированные анамнестически, при клиническом и/или лабораторно-инструментальном обследовании, которые могли препятствовать участию пациентов в исследовании и оказать влияние на его результаты.
Дополнительно к стандартному инструментальному и лабораторному исследованию всем пациентам дважды с интервалом 45 дней проводилось расширенное нейропсихологическое тестирование с помощью следующих методик: Монреальской шкалы оценки когнитивных функций (MoCA), краткой шкалы оценки психического статуса (MMSE), шкалы оценки астении (MFI-20), Питтсбургского индекса качества сна (PSQI), шкалы астенического состояния (ШАС), шкалы Шпигеля. МРТ головного мозга проводилась на аппарате Philips Achieva 1,5 Тл. Качественную и количественную оценку результатов проводили по шкале Fazekas: 0 баллов — нет гиперинтенсивности белого вещества (ГИБВ); 1 балл — мягкая ГИБВ; 2 балла — умеренная сливающаяся ГИБВ; 3 балла — тяжелая ГИБВ.
Обследование больных осуществлялось на двух визитах — до начала лечения и спустя 65 дней.
Статистическая обработка результатов исследования. Для математического и статистического анализа полученных результатов использовались пакеты компьютерных программ Statistica v. 10.0 («StatSoft Inc.», США) и SPSS 13.0 forWindows («SPSS Inc.», США). Применялись методы непараметрического анализа, включая вычисление медианы (Me) и межквартильного размаха (25-й и 75-й квартили — Q25—Q75). При проверке статистических гипотез использовали критерий Манна—Уитни при сравнении двух независимых групп и непараметрический аналог дисперсионного анализа (критерий Краскела—Уоллиса). Критический уровень значимости p для всех используемых процедур статистического анализа принимали равным 0,05.
Результаты
Общая характеристика обследованных пациентов представлена в табл. 1. Пациенты ОГ и ГС не отличались по возрасту, в ОГ преобладали женщины (63,6 против 36,4%). Артериальная гипертензия (АГ) диагностирована у 98% пациентов, фибрилляция предсердий (ФП) — у 12, сахарный диабет 2-го типа (СД 2-го типа) — у 22. В неврологическом статусе у всех обследованных отмечалась рассеянная неврологическая симптоматика в виде повышения сухожильных и периостальных рефлексов, мозжечкового, экс-трапирамидного синдромов, рефлексов орального автоматизма. У 34% больных отмечено нарушение вкусовой чувствительности, у 40% — нарушение обоняния.
По результатам МРТ преобладали пациенты с ГИБВ 1 и 2 балла, у 5 больных — 3 балла, группы не отличались по выраженности поражения белого вещества головного мозга. Большая часть пациентов, участвовавших в исследовании, перенесли COVID-19 средней степени тяжести; больные ОГ и ГС были сопоставимы по тяжести COVID-19, 10 пациентов ОГ и 7 — ГС были госпитализированы с явлениями дыхательной недостаточности (тяжелая форма).
На момент включения в исследование все пациенты ОГ и ГС имели астенический синдром, что подтверждается анализом жалоб больных и результатами, полученными в ходе нейропсихологического тестирования. После курса терапии все больные ОГ и ГС отмечали улучшение самочувствия. Показатели по шкале MFI-20 перед началом лечения были сопоставимы в обеих группах. При повторном тестировании после окончания курса терапии показатели по всем субшкалам опросника MFI-20 были достоверно ниже в ОГ по сравнению с ГС (p<0,05). Пациенты ОГ отмечали уменьшение выраженности умственной и физической утомляемости, повышение общей активности, мотивации (рис. 1).
Таблица 1. Общая характеристика обследованных пациентов
Table 1. General characteristics of the examined patients
|
Параметр |
Все больные (n=110) |
ОГ (n=55) |
ГС (n=55) |
|
Возраст, годы |
68 [45; 83] |
70 [45; 81] |
69 [50; 83] |
|
Пол |
|||
|
мужчины, n (%) |
52 (47,3) |
20 (36,4) |
32 (58,2) |
|
женщины, n (%) |
58 (52,7) |
35 (63,6) |
23 (41,8) |
|
Фоновые заболевания: |
|||
|
АГ, n (%) |
98 (89) |
45 (81,8) |
43 (78,2) |
|
СД 2-го типа, n (%) |
22 (20) |
12 (21,8) |
10 (18,2) |
|
ФП, n (%) |
12 (10,9) |
8 (14,5) |
4 (7,3) |
|
Ожирение, n (%) |
34 (30,9) |
21 (38,2) |
13 (23,6) |
|
ГИБВ |
|||
|
0 баллов, n (%) |
2 (1,8) |
0 (0) |
2 (1,8) |
|
1 балл, n (%) |
62 (56,4) |
30 (54,5) |
32 (58,2) |
|
2 балла, n (%) |
38 (34,5) |
20 (36,4) |
18 (32,7) |
|
3 балла, n (%) |
8 (7,3) |
5 (9,1) |
3 (5,5) |
|
Степень тяжести перенесенного COVID-19: |
|||
|
легкая, n (%) |
35 (31,8) |
16 (29,1) |
19 (34,5) |
|
средняя, n (%) |
58 (52,7) |
28 (50,9) |
30 (54,5) |
|
тяжелая, n (%) |
17 (15,5) |
10 (18,2) |
7 (12,7) |
Рис. 1. Показатели по шкале MFI-20 до и после лечения в ОГ и ГС, баллы.
Fig. 1. Indicators on the MFI-20 scale before and after treatment in OG and GS, points.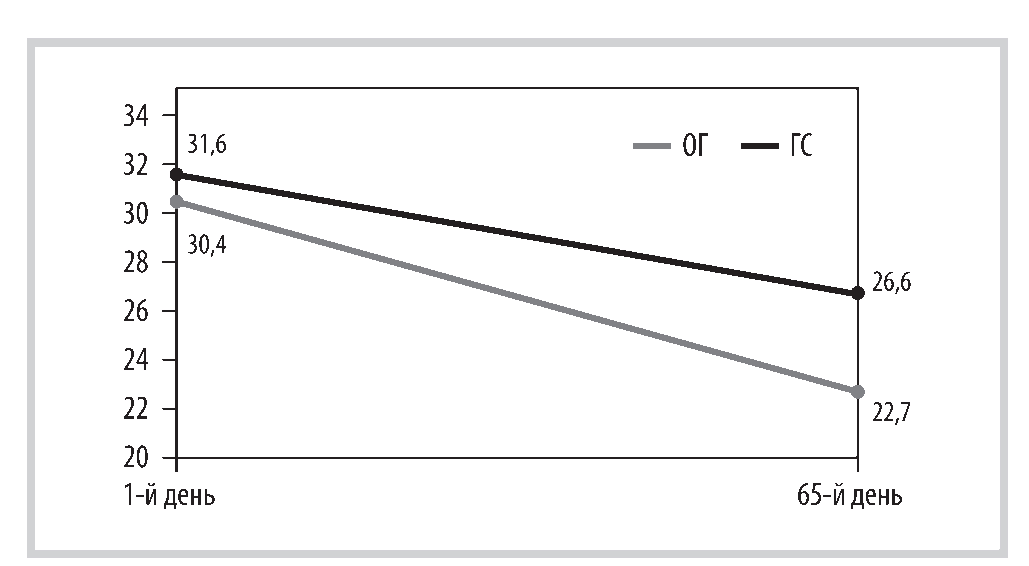
 Согласно оценке по шкале ШАС, перед курсом терапии у пациентов обеих групп отмечалась выраженная астения. После лечения более заметная положительная динамика была выявлена в ОГ, что соответствовало легкой астении, тогда как в ГС после проведенной терапии преобладала умеренная астения (p<0,05). Вероятно, поддержание энергетических процессов на определенном уровне обусловлено мощным антиоксидантным эффектом Мексидола, его защитным действием в отношении митохондрий за счет ингибирования перекисного окисления. Больные ОГ отмечали прилив сил, повышение концентрации внимания, снижение утомляемости в течение дня (рис
Согласно оценке по шкале ШАС, перед курсом терапии у пациентов обеих групп отмечалась выраженная астения. После лечения более заметная положительная динамика была выявлена в ОГ, что соответствовало легкой астении, тогда как в ГС после проведенной терапии преобладала умеренная астения (p<0,05). Вероятно, поддержание энергетических процессов на определенном уровне обусловлено мощным антиоксидантным эффектом Мексидола, его защитным действием в отношении митохондрий за счет ингибирования перекисного окисления. Больные ОГ отмечали прилив сил, повышение концентрации внимания, снижение утомляемости в течение дня (рис
Анализ результатов по опроснику MoCA демонстрирует наличие когнитивного расстройства легкой и умеренной степени в ОГ и ГС до начала терапии. При повторном исследовании пациенты ОГ более уверенно выполняли задания, отмечалась активация запоминания и воспроизведения информации, уменьшилось количество допустимых ошибок при выполнении тестов. У пациентов ГС в когнитивном статусе зафиксирована менее значимая положительная динамика (рис. 3).
Тестирование по шкале MMSE до и после лечения продемонстрировало сопоставимые результаты с данными обследования при помощи опросника MoCA, при этом важно отметить, что в ОГ результат на визите 2 достиг нормы (рис. 4).
Значения индекса PSQI до лечения свидетельствовали о нарушении сна как по отдельным компонентам, так и по суммарному показателю в обеих группах. Повторное тестирование показало, что у пациентов ОГ показатели качества сна нормализовались (p<0,05). В ОГ отмечалось увеличение продолжительности сна, больные реже имели проблемы с засыпанием и поддержанием сна, характеризовали качество сна как достаточно хорошее, реже наблюдалась дневная сонливость. В ГС не отмечалось достоверного повышения качества сна (табл. 2).

Таким образом, у пациентов ОГ была отмечена более высокая эффективность терапии по сравнению с ГС, что подтверждается полученными результатами исследования (см. табл. 2).
Рис. 2. Показатели по шкале ШАС до и после лечения в ОГ и ГС, баллы.
Fig. 2. Indicators on the SHAS scale before and after treatment in OG and GS, points.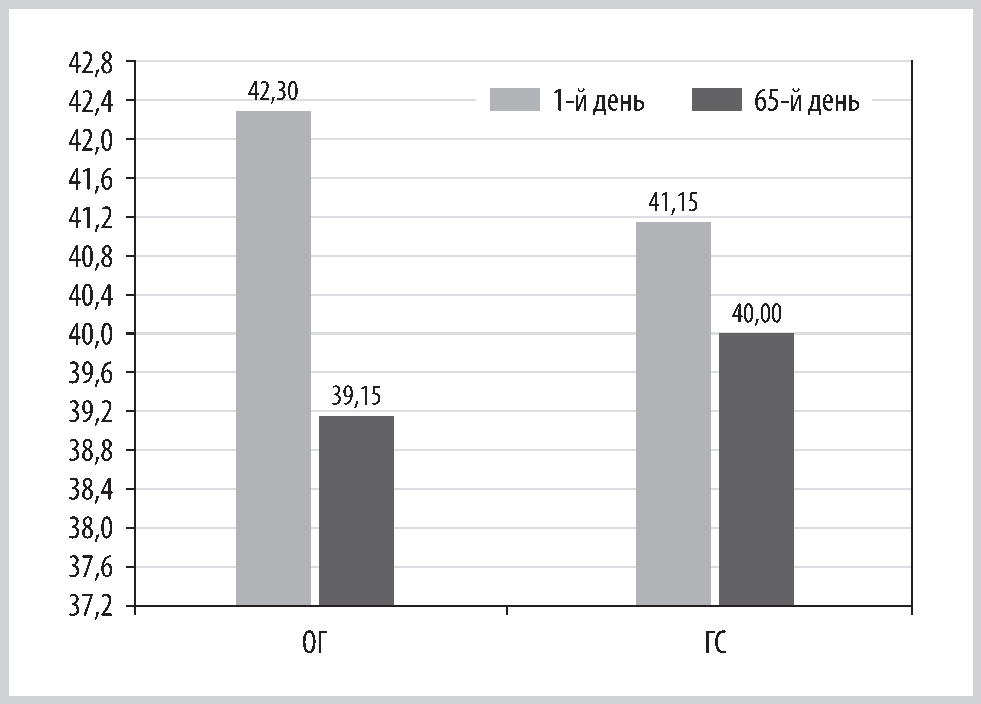
Рис. 3. Результаты обследования пациентов ОГ и ГС по опроснику MoCA до и после лечения, баллы.
Fig. 3. The results of the examination of patients with OG and GS according to the MoCA questionnaire before and after treatment, points, points
Рис. 4. Результаты обследования по опроснику MMSE до и после лечения в ОГ и ГС, баллы.
Fig. 4. The results of the MMSE questionnaire examination before and after treatment in OG and GS, points.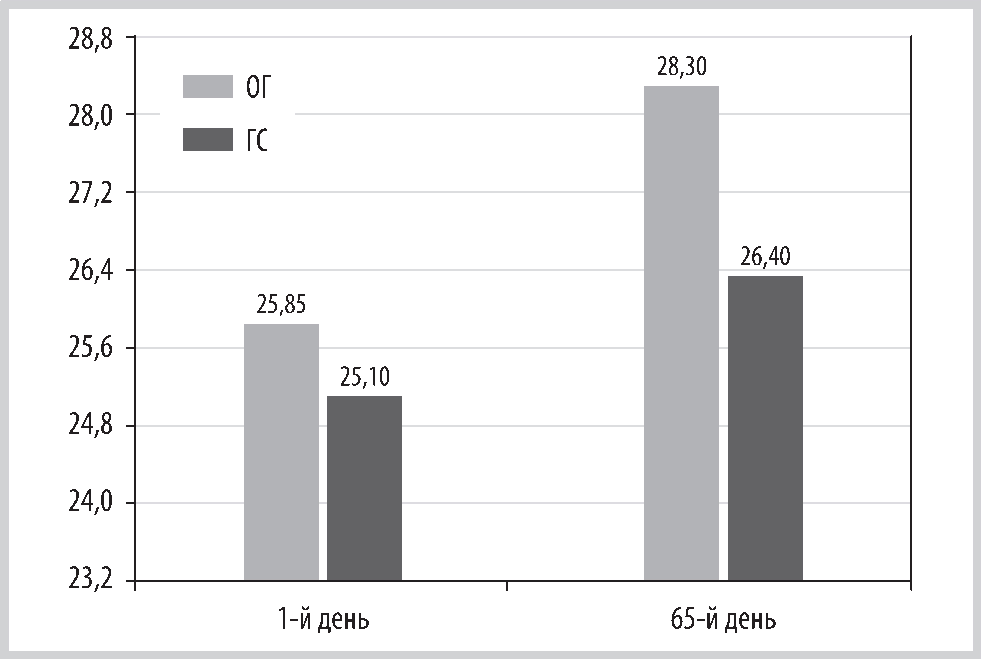
Заключение
Полученные в результате исследования данные достоверно свидетельствуют о целесообразности применения антиоксидантов у пациентов с ХЦВЗ и ПКС, что позволяет нивелировать последствия перенесенной новой коронавирусной инфекции, оказывая многофакторное влияние на функциональную активность мозговых структур. За период наблюдения не было отмечено нежелательных явлений или побочных эффектов, связанных с приемом препарата Мексидол. Назначение препарата не требует возрастной коррекции дозы и хорошо сочетается с базисной терапией. Рекомендованная терапия, продемонстрировавшая свою эффективность: Мексидол по 5 мл в/в или в/м в течение 14 дней с последующим переходом на таблетированную форму Мексидола ФОРТЕ 250 в дозе по 1 таблетке 3 раза в сутки в течение 2 мес.
Авторы заявляют об отсутствии конфликта интересов. The authors declare no conflicts of interest.
ЛИТЕРАТУРА/REFERENCES
1. Ferrer I, Vidal N. Neuropathology of cerebrovascular diseases. Handb Clin Neurol. 2017;145:79-114. https://doi.org/10.1016/B978-0-12-802395-2.00007-9
2. Maccarrone M, Ulivi L, Giannini N, et al. Endothelium and Oxidative Stress: The Pandora’s Box of Cerebral (and Non-Only) Small Vessel Dis- ease? Curr Mol Med. 2017;17(3):169-180. https://doi.org/10.2174/1566524017666170822114739
3. Offner H, Ihara M, Schäbitz WR, et al. Stroke and other cerebrovascular dis- eases. Neurochem Int. 2017;107(6):1-3. https://doi.org/10.1016/j.neuint.2017.04.003
4. Ковальчук В.В., Ершова И.И., Молодовская Н.В. Возможности по- вышения эффективности терапии пациентов с хронической ишемией головного мозга на фоне COVID-19. Журнал неврологии и психиатрии им. С.С. Корсакова. 2021;121(3/2):60-66. Kovalchuk VV, Ershova II, Molodovskaya NV. Possibilities of improving the effectiveness of therapy in patients with chronic cerebral ischemia against the background of COVID-19. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsako- va. 2021;121(3/2):60-66. (In Russ.). https://doi.org/10.17116/jnevro202112103260
5. Камчатнов П.Р., Черемин Р.А., Скипетрова Л.А., Чугунов А.В. Невро- логические проявления постковидного синдрома. Журнал неврологии и психиатрии им. С.С. Корсакова. 2022;122(3):7-15. Kamchatnov PR, Cheremin RA, Skipetrova LA, Chugunov AV. Neurologi- cal manifestations of postcovid syndrome. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2022;122(3):7-15. (In Russ.). https://doi.org/10.17116/jnevro20221220317
6. Екушева Е.В., Ковальчук В.В., Щукин И.А. Неврологические ослож- нения COVID-19 и постковидный синдром. М.: ООО «АСТ345»; 2022. Yakusheva EV, Kovalchuk VV, Shchukin IA. Neurological complications of COVID-19 and postcovid syndrome. M.: «AST345» LLC; 2022. (In Russ.).
7. Ковальчук В.В. Роль новой коронавирусной инфекции (COVID-19) в прогрессировании и развитии сосудистых заболеваний головного мозга. Грамотный выбор средств патогенетической терапии — залог успеха лечения и профилактики. Взгляд специалиста из «красной зо- ны». Неврология, нейропсихиатрия, психосоматика. 2021;13(1):57-66. Kovalchuk VV. The role of the new coronavirus infection (COVID-19) in the progression and development of vascular diseases of the brain. A competent choice of pathogenetic therapy means is the key to the success of treatment and prevention. The view of a specialist from the «red zone». Neurology, Neu- ropsychiatry, Psychosomatics. 2021;13(1):57-66. (In Russ.). https://doi.org/10.14412/2074-2711-2021-1-57-66
8. Кулеш А.А. Особенности ведения пациентов с хронической ишемией головного мозга в период пандемии COVID-19. Неврология, нейропси- хиатрия, психосоматика. 2021;13(3):4-11. Kulesh AA. Features of management of patients with chronic cerebral isch- emia during the Covid-19 pandemic. Neurology, Neuropsychiatry, Psychoso- matics. 2021;13(3):4-11. (In Russ.). https://doi.org/10.14412/2074-2711-2021-3-4-11
9. Кузнецова Е.Б., Напшева А.М., Колоколов О.В. и др. Влияние COVID-19 на состояние структур продолговатого мозга: клинико- морфологический анализ. Саратовский научно-медицинский журнал. 2022;18(1):122-125. Kuznetsova EB, Napsheva AM, Kolokolov OV, et al. The effect of COVID-19 on the state of the structures of the medulla oblongata: clinical and morpho- logical analysis. Saratov Scientific and Medical Journal. 2022;18(1):122-125. (In Russ.).
10. Шаварова Е.К., Казахмедов Э.Р., Алексеева М.В. и др. Роль антиок- сидантной терапии у пациентов с новой коронавирусной инфекцией COVID-19 среднетяжелого и тяжелого течения. Инфекционные болез- ни. 2021;19(1):159-164. Shavarova EK, Kazakhmedov ER, Alekseeva MV, et al. The role of antiox- idant therapy in patients with the new coronavirus infection COVID-19 of moderate and severe course. Infectious Diseases. 2021;19(1):159-164. (In Russ.). https://doi.org/10.20953/1729-9225-2021-1-159-164
11. Щулькин А.В., Филимонова А.А. Роль свободнорадикального окис- ления, гипоксии и их коррекции в патогенезе COVID-19. Терапия. 2020;5:187-194. Shchulkin AV, Filimonova AA. The role of free radical oxidation, hypoxia and their correction in the pathogenesis of COVID-19. Therapy. 2020;5:187-194. (In Russ.). https://doi.org/10.18565/therapy.2020.5.187-194
12. Воронина Т.А. Антиоксиданты/антигипоксанты — недостающий пазл эффективной патогенетической терапии пациентов с COVID-19. Ин- фекционные болезни. 2020;18(2):97-102. Voronina TA. Antioxidants/antihypoxants — the missing puzzle of effec- tive pathogenetic therapy of patients with COVID-19. Infectious Diseases. 2020;18(2):97-102. (In Russ.). https://doi.org/10.20953/1729-9225-2020-2-97-102
13. Кирова Ю.И., Шакова Ф.М., Германова Э.Л. и др. Влияние Мек- сидола на церебральный митохондриогенез в молодом возрасте и при старении. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(1):62-69. Kirova YuI, Ushakova FM, Germanova EL, et al. The effect of Mexidol on cerebral mitochondriogenesis at a young age and during aging. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2020;120(1):62-69. (In Russ.). https://doi.org/10.17116/jnevro202012001155
14. Федин А.И., Захаров В.В., Танашян М.М. и др. Результаты между- народного многоцентрового рандомизированного двойного слепо- го плацебо-контролируемого исследования оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами Мексидол и Мексидол ФОРТЕ 250 (ис- следование МЕМО). Журнал неврологии и психиатрии им. С.С. Корса- кова. 2021;121(11):7-16. Fedin AI, Zakharov VV, Tanashyan MM, et al. Results of an international multicenter, randomized, double-blind, placebo-controlled study evaluating the efficacy and safety of sequential therapy of patients with chronic cere- bral ischemia with Mexidol and Mexidol FORTE 250 (MEMO study). Zhur- nal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2021;121(11):7-16. (In Russ.). https://doi.org/10.17116/jnevro20211211117.
15. Журавлева М.В., Васюкова Н.С., Архипов В.В. и др. Результаты кли- нических исследований эффективности и безопасности примене- ния препаратов этилметилгидроксипиридина сукцината у пациентов с хронической ишемией головного мозга. Журнал неврологии и психи- атрии им. С.С. Корсакова. 2022;122(11):1-11. Zhuravleva MV, Vasyukova NS, Arkhipov VV, et al. Results of clinical stud- ies of the efficacy and safety of the use of ethylmethylhydroxypyridine suc- cinate in patients with chronic cerebral ischemia. Zhurnal Nevrologii i Psikh- iatrii im. S.S. Korsakova. 2022;122(11):1-11. (In Russ.). https://doi.org/10.17116/jnevro202212211129
16. Стаховская Л.В., Шамалов Н.А., Хасанова Д.Р. и др. Результаты ран- домизированного двойного слепого мультицентрового плацебо-кон- тролируемого в параллельных группах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(3-2):55-65. Stakhovskaya LV, Shamalov NA, Khasanova DR, et al. Results of a random- ized double-blind multicenter placebo-controlled parallel group study of the efficacy and safety of mexidol in long-term sequential therapy in patients in acute and early recovery period. Zhurnal Nevrologii i Psikhiatrii im. S.S. Kor- sakova. 2017;117(3-2):55-65. (In Russ.). https://doi.org/10.17116/jnevro20171173255-65.
Efficacy of Mexidol in the correction of postcovid syndrome in patients with chronic cerebrovascular diseases
© E.B. KUZNETSOVA, E.A. SALINA, N.S. KUZNETSOV
Razumovsky Saratov State Medical University, Saratov, Russia
Abstract
Objective. To evaluate the effectiveness of sequential therapy with Mexidol and Mexidol FORTE 250 in the correction of postcovoid syndrome (PKS) in patients with chronic cerebrovascular diseases (CVD).
Material and methods. The analysis of the results of examination and treatment of 110 patients with CVD who underwent COVID-19 was carried out. Patients of the main group (OH, n=55) received Mexidol (5 ml IV drip for 14 days, followed by the transition to the tablet form of Mexidol FORTE 250 1 table 3 times/day for 2 months); 55 patients of the comparison group (GS) did not receive antioxidants. All patients included in the study were conducted MRI examination and extensive neuropsychological testing.
Results. There was a significant improvement in the state of cognitive functions, regression of symptoms of asthenia, improvement of night sleep in patients with OG. The differences were statistically significant both in comparison with the baseline level and the HS.
Conclusion. The administration of the drug does not require age-related dose adjustment and is well combined with basic therapy. The recommended regimen for the use of Mexidol: 14 days of 5 ml i/v or i/m, then taking the drug Mexidol FORTE 250 at a dose of 1 table 3 times/day for 2 months.
Keywords: chronic cerebrovascular diseases, postcovid syndrome, Mexidol, treatment.
Information about the authors:
Kuznetsova E.B. — orcid.org/0000-0002-3979-3453
Salina E.A. — https://orcid.org/0000-0002-8945-2120
Kuznetsov N.S. — https://orcid.org/0000-0003-4879-4121
Corresponding author: Kuznetsova E.B. — e-mail: elenfeb77@mail.ru
To cite this article: Kuznetsova EB, Salina EA, Kuznetsov NS. Efficacy of Mexidol in the correction of postcovid syndrome in patients with chronic cerebrovascular diseases. S.S. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2023;123(5):117-122. (In Russ.). doi.org/10.17116/jnevro2023123051117
