Международное многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами Мексидол® и Мексидол® ФОРТЕ 250
СтатьиИсследование МЕМО: результаты субанализа у пациентов с артериальной гипертонией
В.В. Захаров1, О.Д. Остроумова1,2, А.И. Кочетков2, М.В. Клепикова2, А.И. Федин3
1 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
2 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, г. Москва
3 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
Аннотация. Хроническая ишемия мозга (ХИМ) – одно из наиболее часто встречающихся в клинической f практике неврологических патологических состояний.
Цель – оценить эффективность и безопасность последовательной терапии препаратом Мексидол® внутривенно и Мексидол® ФОРТЕ 250 перорально в группах пациентов с артериальной гипертонией (АГ) и без таковой в аспекте влияния препарата на когнитивное функционирование, а также выраженность астенических, тревожных, вегетативных и двигательных нарушений и качество жизни в условиях ХИМ.
Материал и метод. В рамках субанализа пациенты с ХИМ были разделены на 4 подгруппы: 1-я – пациенты с АГ, получавшие препараты Мексидол® и Мексидол® ФОРТЕ 250 (n=144); 2-я – пациенты с АГ, получавшие плацебо (n=146); 3-я – пациенты без АГ, получавшие Мексидол® и Мексидол® ФОРТЕ 250 (n=15); 4-я – пациенты без АГ, получавшие плацебо (n=12).
Результаты. В конце периода наблюдения были выявлены статистически значимые различия в динамике баллов по шкале МоСА между группами пациентов, получавших Мексидол® и плацебо (p=0,000), свидетельствующие о превосходящей эффективности применения Мексидола в подгруппе пациентов с АГ. На фоне терапии препаратом Мексидол®, в отличие от плацебо, медианное значение балла по шкале МоСА в конце периода наблюдения достигло уровня нормы у всех пациентов. При оценке вторичных конечных точек эффективности статистически значимое преимущество Мексидола над плацебо в популяции пациентов с АГ на конечном визите было достигнуто по следующим параметрам: тест замены цифровых символов, шкала оценки астении MFI-20, шкала тревоги Бека, шкала Тинетти, психологический компонент здоровья по опроснику SF-36. Установлен сопоставимый характер профиля безопасности Мексидола и плацебо.
Заключение. Полученные результаты дают основания рекомендовать длительное последовательное применение препарата Мексидол® в комплексном лечении пациентов с АГ и ХИМ в качестве инструмента защиты головного мозга как органа-мишени АГ и средства патогенетически обоснованной терапии когнитивных, эмоциональных, астенических, вегетативных и двигательных нарушений.
Ключевые слова: хроническая ишемия головного мозга, артериальная гипертония, когнитивные нарушения, этилметигидроксипиридина сукцинат, Мексидол®, Мексидол® ФОРТЕ 250.
Конфликт интересов: статья подготовлена при поддержке фармацевтической компании ООО «Векторфарм».
Для цитирования: В.В. Захаров, О.Д. Остроумова, А.И. Кочетков, М.В. Клепикова, А.И. Федин. Международное многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами Мексидол® и Мексидол® ФОРТЕ 250 (исследование МЕМО): результаты субанализа у пациентов с артериальной гипертонией.
Терапия. 2023; 9(1): 145-159.
Doi: dx.doi.org/10.18565/therapy.2023.1.145-159
International multicenter randomized double-blind placebo-controlled study assessing the efficacy and safety of sequential therapy with Mexidol® and Mexidol® FORTE 250 in patients with chronic brain ischemia (MEMO): subanalysis in patients with arterial hypertension
Zakharov V.V.1, Ostroumova O.D.1,2, Kochetkov A.I.2, Klepikova M.V.2, Fedin A.I.3
1 M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of Russia (Sechenov University)
2 Russian Medical Academy of Continuous Professional Education of the Ministry of Healthcare of Russia, Moscow
3 N.I. Pirogov Russian National Research Medical University of the Ministry of Healthcare of Russia, Moscow
Abstract. Chronic brain ischemia (CBI) is one of the most common neurological disorders in clinical practice.
Objective: to evaluate the efficacy and safety of sequential therapy with Mexidol® solution intravenously and Mexidol® FORTE 250 film-coated tablets, 250 mg orally in patients with and without arterial hypertension (AH) in terms of the drug effect on cognitive functioning, as well as the severity of asthenic, anxiety, vegetative and motor disorders, and quality of life in CBI.
Material and methods. In a subanalysis patients with CBI were divided into four subgroups: 1st – AH patients receiving Mexidol® and Mexidol® FORTE 250 (n=144); 2nd – AH patients receiving placebo (n=146); 3rd – patients without AH receiving Mexidol® and Mexidol® FORTE 250 (n=15); 4th – patients without AH receiving placebo (n=12).
Results. At the end of the follow-up, significant differences were found in the dynamics of the MoCA scores between the patients receiving Mexidol® and placebo (p=0,000), which allows to state a superior efficacy of Mexidol in the subgroup of patients with AH. Also in the long-term sequential therapy with Mexidol®, in contrast to the placebo, the median value of the MoCA score at the end of the follow-up reached normal levels in patients with and without AH. When assessing secondary efficacy endpoints, a significant advantage of Mexidol® over placebo in the population of patients with AH at the end of follow-up was achieved on the following parameters: The Digit Symbol Substitution Test, MFI-20, the Beck Anxiety Inventory, Tinetti Performance-Oriented Mobility Assessment, psychological component of health according to SF-36 questionnaire. A comparable character of the safety profile of Mexidol® and placebo was established.
Conclusion. The obtained results allow to recommend the use of long-term sequential therapy with Mexidol in the complex therapy of patients with AH and CBI as a tool for the brain protection as a AH target organ and as a tool of pathogenetically substantiated therapy of cognitive, emotional, asthenic, vegetative and motor disorders.
Key words: chronic brain ischemia, arterial hypertension, cognitive impairment, ethylmethyhydroxypyridine succinate, Mexidol®, Mexidol® FORTE 250.
Conflict of interests: the article was prepared with the support of the pharmaceutical company «Vectorpharm».
For citation: Zakharov V.V., Ostroumova O.D., Kochetkov A.I., Klepikova M.V., Fedin A.I. International multicenter randomized double-blind placebo-controlled study assessing the efficacy and safety of sequential therapy with Mexidol® and Mexidol® FORTE 250 in patients with chronic brain ischemia (MEMO): subanalysis in patients with arterial hypertension.
Therapy. 2023; 9(1): 145-159.
Doi: dx.doi.org/10.18565/therapy.2023.1.145-159
Введение
Цереброваскулярные заболевания относятся к наиболее часто встречающимся в клинической практике неврологическим патологическим состояниям [1-3]. Особое место среди них занимает так называемая хроническая ишемия головного (ХИМ). По некоторым данным, в нашей стране она встречается с частотой 5,6 тыс. случаев на 100 000 человек и диагностируется примерно у 5% населения. ХИМ ассоциирована с широким спектром неврологических нарушений, включая двигательные, психоэмоциональные, когнитивные расстройства, что оказывает крайне негативное влияние на качество жизни пациентов [4]. Следует отметить, что среди них исключительную значимость имеют когнитивные нарушения (КН), которые также широко распространены в практике, характеризуются прогредиентным течением и в конечных своих стадиях приводят к деменции с возникновением зависимости пациента от посторонней помощи во всех аспектах повседневной жизни [4].
ХИМ характеризуются мультифакторной этиологией, в которой важнейшее значение имеют изменения со стороны церебрального сосудистого русла [5]. При этом одним из наиболее сильных факторов риска сосудистых КН служит артериальная гипертония (АГ) [6], поскольку головной мозг входит в число органов-мишеней этого заболевания. Повышенное артериальное давление (АД) становится причиной формирования болезни мелких сосудов, вызывающей появление в веществе головного мозга широкого спектра изменений, таких как лейкоареоз, лакунарные инфаркты, микрокровоизлияния. Указанные сосудистые поражения непосредственно ведут к развитию и прогрессированию КН [6, 7]. В действующих клинических рекомендациях по АГ как Минздрава России 2020 г. [6], так и Европейского общества по артериальной гипертензии (ESH) [8] эксперты обращают внимание на необходимость тестирования когнитивных функций у пациента с этим заболеванием, поскольку их снижение относится к самым ранним признакам поражения головного мозга как органа-мишени АГ.
Соответственно не вызывает сомнений актуальность поиска эффективных стратегий защиты головного мозга у пациентов с АГ как от осложнений, ассоциированных с поражением сосудистого русла, в целом, так и от развития и прогрессирования КН в частности. В связи с этим представляют интерес возможности применения этиметилгидроксипиридина сукцината (Мексидол®), который реализует на уровне организма мультимодальный спектр протективных эффектов (антигипоксантный, антиоксидантный, мембраностабилизирующий, защита от глутаматной эксайтотоксичности, стимуляция ангиогенеза), воздействуя в первую очередь на нейрональные и сосудистые нарушения и тем самым улучшая мозговое кровообращение, микроциркуляцию и оказывая нейропротекцию [9, 10].
Мексидол® имеет обширную доказательную базу клинической эффективности и безопасности у различных категорий пациентов [1, 9-14]. В частности, в 2021 г. были опубликованы результаты международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования МЕМО (МЕксидол – хроническая ишемия МОзга) по оценке эффективности и безопасности последовательной терапии препаратами Мексидол® и Мексидол® ФОРТЕ 250 у пациентов с ХИМ, общие результаты и выводы которого приведены в опорной публикации [1].
В настоящей статье представлены данные исследования МЕМО как субанализа сравнительной эффективности и безопасности Мексидола в группах пациентов с АГ и без нее в аспекте влияния препарата на когнитивное функции, а также на выраженность астенических, тревожных, вегетативных, двигательных нарушений и качество жизни в условиях хронической ишемии головного мозга.
Материал и методы
Подробное описание дизайна исследования МЕМО, критериев включения, невключения, первичных и вторичных критериев эффективности, изучаемых показателей безопасности дано в опорной публикации [1].
Результаты
Для выполнения субанализа исследования МЕМО, посвященного сравнительной оценке эффектов препарата Мексидол® у пациентов с АГ, все участники были разделены на четыре подгруппы: 1-я (n=144) – пациенты с АГ, получавшие длительную последовательную терапию Мексидол® + Мексидол® ФОРТЕ 250; 2-я (n=146) – пациенты с АГ, получавшие плацебо; 3-я (n=15) – пациенты без АГ, получавшие длительную последовательную терапию Мексидол® + Мексидол® ФОРТЕ 250; 4-я (n=12) – пациенты без АГ, получавшие плацебо.
Исходная характеристика пациентов представлена в таблицах 1 и 2. Группы были сопоставимы между собой по всем исходным характеристикам и изучаемым параметрам, за исключением уровней систолического и диастолического АД, которые были выше в популяции пациентов с АГ (см. табл. 1). Статистически значимые различия (р=0,007) также имелись в исходном уровне баллов по шкале МоСА между группами пациентов, получавших Мексидол®, у которых АГ либо отсутствовала, либо имелась (см. табл. 2).
Таблица 1. Исходная характеристика пациентов, включенных в субанализ
| Показатель | Пациенты с АГ | Пациенты без АГ | |||
| Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | ||
| Возраст, годы | 60,7±9,9 | 60,9±9,1 | 54,3±7,0 | 57,9±8,3 | |
| ИМТ, кг/м² | 28,5±4,1 | 28,3±4,3 | 28,6±7,9 | 29,8±6,1 | |
| Пол, n (%) | мужской | 38 (26,4) | 35 (24,0) | 2 (13,3) | 2 (16,7) |
| женский | 106 (73,6) | 111 (76,0) | 13 (86,7) | 10 (83,3) | |
| Раса, n (%) | европеоидная | 137 (95,1) | 140 (95,9) | 12 (80,0) | 10 (83,3) |
| монголоидная | 7 (4,9) | 6 (4,1) | 3 (20,0) | 2 (16,7) | |
| САД, мм рт.ст. | 130 [121; 134] | 130 [122; 132] | 120 [110; 124] | 123 [114; 128] | |
| ДАД, мм рт.ст. | 80 [75; 82] | 80 [76; 84] | 76 [70; 80] | 75,5 [71; 81] | |
| ЧСС, уд/мин | 70 [64; 76] | 70 [65; 74] | 67 [64; 72] | 69 [64; 77] | |
Примечание: данные представлены в виде медианы и 25-го и 75-го процентилей (Me [Q1; Q3]) для ненормально распределенных показателей и в виде среднего и стандартного отклонения (M±SD) для показателей, подчиняющихся нормальному распределению.
АГ – артериальная гипертония; ДАД – диастолическое артериальное давление; ИМТ – индекс массы тела; САД – систолическое артериальное давление; ЧСС – частота сердечных сокращений.
Таблица 2. Результаты исходного обследования пациентов согласно применявшимся в исследовании шкалам
| Показатель | Пациенты с АГ | Пациенты без АГ | ||
| Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | |
| Шкала МоСА | 22 [19,5; 23] | 22 [21; 23] | 24 [22; 24] | 22,5 [21; 24] |
| SF-36 (физический компонент здоровья) | 44 [38; 51] | 45 [39; 50] | 47 [40; 50] | 43 [39,5; 51] |
| SF-36 (психологический компонент здоровья) | 45 [36; 51,5] | 46 [39; 52] | 43 [35; 56] | 43,5 [40; 47] |
| Шкала MFI-20 | 60,33±13,36 | 58,76±14,06 | 54,40±12,41 | 59,17±10,37 |
| Шкала тревоги Бека | 10 [6; 15,5] | 9 [6; 15] | 8 [7; 16] | 8 [5,5; 9,5] |
| Опросник Вейна | 26 [16; 36] | 23 [17; 36] | 29 [18; 36] | 28,5 [23; 38] |
| Тест замены цифровых символов | 32 [24,5; 39,5] | 34 [27; 40] | 30 [19; 41] | 21 [15; 37] |
| Шкала Тиннети | 33 [30; 36] | 34 [30; 37] | 35 [32; 37] | 34,5 [30,5; 37,5] |
Примечание: данные представлены в виде медианы и 25-го и 75-го процентилей (Me [Q1; Q3]) для ненормально распределенных показателей и в виде среднего и стандартного отклонения (M±SD) для показателей, подчиняющихся нормальному распределению.
АГ – артериальная гипертония.
В соответствии с протоколом исследования основным критерием эффективности являлось среднее значение изменения балла по шкале MоCA на этапе завершения исследования пациентом (визит 5) по сравнению с исходным уровнем (визит 0; табл. 3). По результатам исследования, статистически значимые изменения баллов по шкале MoCA на этапе завершения исследования пациентом (визит 5) были выявлены при сравнении динамики между группами Мексидол® + Мексидол® ФОРТЕ 250 в подгруппе пациентов с АГ и Плацебо в подгруппе пациентов с АГ (p=0,000). Нижняя граница 95% доверительного интервала (ДИ) для разности средних основного показателя эффективности в группах Мексидол® + Мексидол® ФОРТЕ 250 в подгруппе пациентов с АГ и Плацебо в подгруппе пациентов с АГ составила 1,51. Данная граница является положительной величиной, что позволяет констатировать превосходство в эффективности последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250 над Плацебо в подгруппе пациентов с АГ.
Для других сравнений подтвержденных статистически значимых различий выявлено не было. Кроме того, именно в группах длительной последовательной терапии препаратами линейки Мексидол® медианное значение балла по шкале МоСА в конце периода наблюдения (визит 5) достигло уровня нормы (26 баллов) как у пациентов с АГ, так и без таковой. В группе плацебо медиана суммарного балла по шкале МоСА на визите 5 составила 24 балла для пациентов с АГ и 25,5 – для лиц без этого заболевания (см. табл. 3).
Таблица 3. Динамика результатов тестирования когнитивных функций у исследованных пациентов по шкале MoCA (визит 5 в сравнении с визитом 0)
| Группы пациентов | Показатели оценки по шкале MoCA в конце периода наблюдения (визит 5) | Разница значений по шкале МоСА между визитом 5 и визитом 0 внутри групп | Среднее значение разности [Р5%ДИ] между группами | р |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) | 26 [24; 27] | 4,37±2,60 | 2,26 [1,51; 3,01] | 0,000 |
| Плацебо, АГ(+) | 24 [22; 26] | 2,10±2,24 | ||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) | 26 [25; 28] | 2,87±2,17 | -0,13 [-2,58; 1,32] | 1,000 |
| Плацебо, АГ (-) | 25,5 [24; 26,5] | 3,00±1,35 |
Примечание: Р – уровень значимости различий для среднего значения разности динамики между соответствующими группами по шкале МоСА (визит 5 в сравнении с визитом 0).
ДИ – доверительный интервал; АГ – артериальная гипертония.
При сравнении медианы изменения баллов по шкале MoCA на разных визитах относительно исходного уровня уже начиная со 2-го визита были отмечены статистически значимые различия динамики баллов между группами Мексидол® + Мексидол® ФОРТЕ 250 в подгруппе пациентов с АГ и Плацебо в подгруппе пациентов с АГ (p=0,000 во всех случаях при сравнении динамики между группами на визитах 2, 4, 5). Далее на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250 была отмечена нарастающая положительная динамика в подгруппе пациентов с АГ (рис. 1).
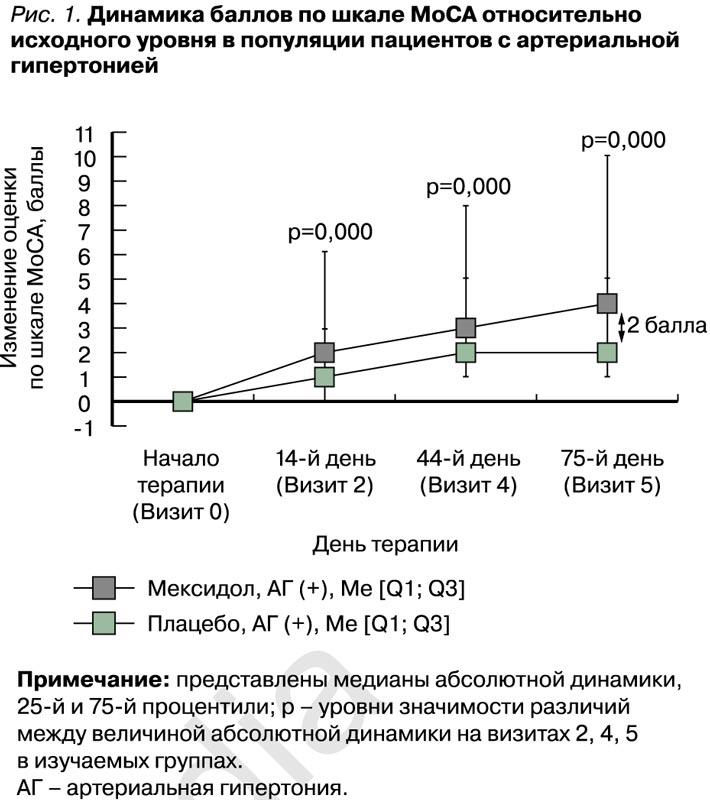
Динамика состояния пациентов, согласно тесту замены цифровых символов, оценивалась по результатам, полученным на визитах 2, 4 и 5 в сравнении с данными, зафиксированными на визите рандомизации (визит 1). В популяции пациентов с АГ были выявлены статистически значимые (p=0,000) различия между группами Мексидол® + Мексидол® ФОРТЕ 250 и Плацебо в величине медиан абсолютной динамики (8,00 [4,00; 16,00] и 4,00 [0,00; 10,00] баллов соответственно) в тесте замены цифровых символов на визите В относительно исходного уровня (табл. 4, рис. 2). Других статистически значимых различий в абсолютной динамике результатов между группами в этом тесте обнаружено не было. Таким образом, в группе пациентов с АГ, получавших Мексидол®, по сравнению с группой пациентов с АГ, получавших плацебо, в тесте замены цифровых символов была выявлена статистически значимо большая величина положительной динамики показателей: различия в медианах абсолютной динамики между группами составили 4 балла в пользу группы пациентов с АГ, применявших Мексидол®.
Таблица 4. Динамика баллов в тесте замены цифровых символов у исследованных пациентов по визитам в сравнении с исходным уровнем
| Группы пациентов | Визит 2 | p | Визит 4 | p | Визит 5 | p |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) |
3,00 [1,00; 7,00] | 0,146 | 5,00 [2,00; 12,00] | 0,0501 | 8,00 [4,00; 16,00] | 0,000 |
| Плацебо, АГ(+) | 2,00 [0,00; 5,00] | 4,00 [-1,00; 8,00] | 4,00 [0,00; 10,00] | |||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) |
2,00 [-1,00; 6,00] | 5,00 [3,00; 9,00] | 1,000 | 8,00 [1,00; 11,00] | 1,000 | |
| Плацебо, АГ (-) | 3,50 [1,00; 7,00] | 5,00 [4,00; 8,00] | 7,5 [5,00; 10,50] |
Примечание: представлены медианы абсолютной динамики и соответствующие им значения 25-го и 75-го процентилей (Me [Q1; Q3]).
АГ – артериальная гипертония.
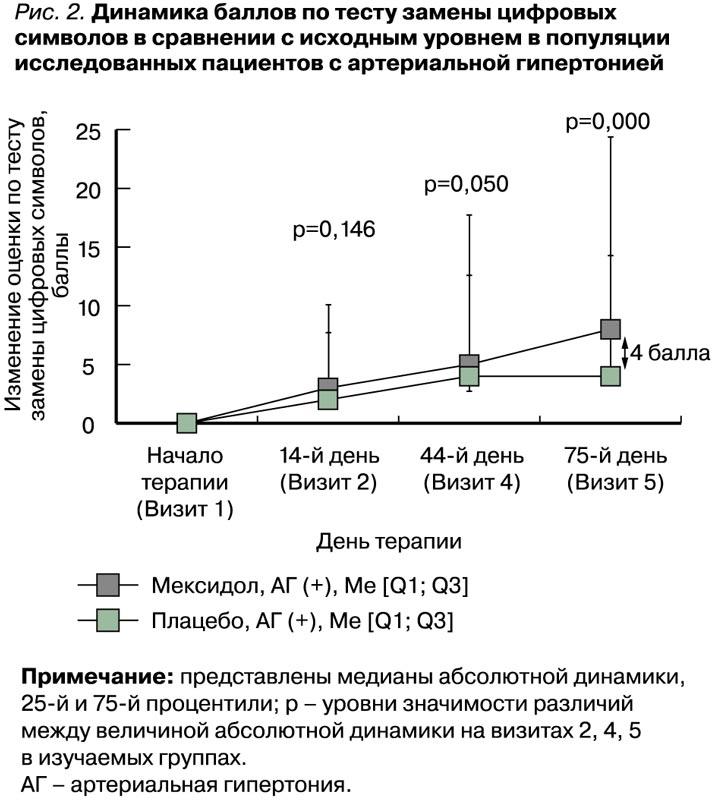
При оценке результатов по шкале астении MFI-20 на визите 5 в сравнении с их исходным уровнем на визите 1 были выявлены статистически значимые различия в абсолютной динамике баллов между подгруппами Мексидол® + Мексидол® ФОРТЕ 250 (АГ+) и Плацебо (АГ+), причем статистической значимости они достигли уже на визите 4 (p=0,000 табл. 5). Такие результаты свидетельствуют о нарастающей положительной динамике при оценке по шкале MFI-20 на фоне длительной последовательной терапии препаратами линейки Мексидол® у пациентов с АГ. Других статистических значимых различий при попарных сравнениях динамики на визитах 2, 4, 5 по сравнению с исходным уровнем по шкале MFI-20 в изучаемых подгруппах обнаружено не было.
Таблица 5. Динамика баллов по шкале MFI-20 у исследованных пациентов по визитам в сравнении с исходным уровнем
| Группы пациентов | Визит 2 | p | Визит 4 | p | Визит 5 | p |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) |
-3,58±9,74 | 0,155 | -6,46±11,81 | 0,000 | -8,40±12,76 | 0,000 |
| Плацебо, АГ (+) | -1,56±7,35 | -3,33±10,16 | -4,25±11,42 | |||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) |
-0,20±7,42 | -5,47±9,81 | 1,000 | -7,67±12,27 | 1,000 | |
| Плацебо, АГ (-) | -3,08±5,82 | -9,50±8,42 | -11,33±9,68 |
Примечание: представлены средние значения абсолютной динамики и соответствующие им значения стандартного отклонения (M±SD).
АГ – артериальная гипертония.
Изменения показателей по шкале Бека оценивались по результатам, полученным на визитах 2, 4 и 5, относительно результатов на визите рандомизации (визит 1). В популяции пациентов с АГ, начиная с визита 4, были установлены статистически значимые различия между группами Мексидол® + Мексидол® ФОРТЕ 250 и Плацебо в величине медиан абсолютной динамики по шкале Бека в сравнении с исходными значениями (табл. 6): к визиту 5 эти показатели составили -4,00 [-8,00; -1,00] и -1,00 [-4,00; 1,00] баллов соответственно (p=0,000). Других статистически значимых различий в абсолютной динамике результатов между группами по рассматриваемой шкале зафиксировано не было. Подобные результаты свидетельствуют о нарастающей положительной динамике в виде уменьшения уровня тревоги на фоне длительной последовательной терапии препаратами Мексидол® + Мексидол® ФОРТЕ 250 у пациентов с АГ.
Таблица 6. Динамика баллов по шкале Бека у исследованных пациентов на разных визитах в сравнении с исходным уровнем
| Группы пациентов | Визит 2 | p | Визит 4 | p | Визит 5 | p |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) |
-1,00 [-4,00; 0,00] | 0,150 | -3,00 [-7,00; 0,00] | 0,003 | -4,00 [-8,00; -1,00] | 0,000 |
| Плацебо, АГ(+) | 0,00 [-2,00; 1,00] | -1,00 [-4,00; 1,00] | -1,0 0 [-4,00; 1,00] | |||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) |
0,00 [-4,00; 0,00] | -1,00 [-6,00; 0,00] | 1,000 | -1,00 [-8,00; 0,00] | 1,000 | |
| Плацебо, АГ (-) | 0,00 [-5,00; 1,00] | -1,50 [-3,50; 1,00] | -2,0 0 [-4,00; -0,50] |
Примечание: представлены медианы абсолютной динамики и соответствующие им значения 25-го и 75-го процентилей (Me [Q1; 03]). АГ – артериальная гипертония.
При анализе результатов тестирования по опроснику Вейна в динамике статистически значимых различий выявлено не было. Вместе с тем наблюдалась тенденция к прогрессивному снижению количества баллов по данному опроснику среди пациентов с АГ, получавших последовательную терапию препаратами Мексидол® + Мексидол® ФОРТЕ 250, начиная с визита 4 (по сравнению с визитом 1), что, в свою очередь, указывает на некоторое уменьшение выраженности вегетативных нарушений на фоне изучаемой терапии.
Изменения баллов по шкале Тинетти оценивались по результатам, полученным на визитах 2, 4 и 5, в сопоставлении с результатами на визите рандомизации (визит 1). При анализе этих изменений в популяции пациентов с АГ были обнаружены статистически значимые различия между группами Мексидол® + Мексидол® ФОРТЕ 250 и Плацебо в величине медиан абсолютной динамики по сравнению с исходным уровнем уже на визитах 2 и 4, а к визиту 5 они составили соответственно, 3,00 [1,00; 6,00] и 1,00 [0,00; 4,00] баллов (р=0,000; табл. 7 и рис. 3). Других статически значимых различий между группами в динамике результатов по шкале Тинетти установлено не было. Таким образом, при длительной последовательной терапии препаратами Мексидол® + Мексидол® ФОРТЕ 250 у пациентов с АГ отмечалась нарастающая в своей выраженности положительная динамика показателей по шкале равновесия и ходьбы Тиннети.
Таблица 7. Динамика баллов по шкале Тинетти у исследованных пациентов на разных визитах в сравнении с исходным уровнем
| Группы пациентов | Визит 2 | p | Визит 4 | p | Визит 5 | p |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) |
1,00 [0,00; 3,00] | 0,011 | 2,00 [0,00; 5,00] | 0,005 | 3,00 [1,00; 6,00] | 0,000 |
| Плацебо, АГ (+) | 0,00 [0,00; 2,00] | 0,00 [0,00; 3,00] | 1,00 [0,00; 4,00] | |||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) |
0,00 [0,00; 1,00] | 1,000 | 1,00 [0,00; 3,00] | 1,000 | 2,00 [0,00; 3,00] | 1,000 |
| Плацебо, АГ (-) | 0,00 [0,00; 2,00] | 1,00 [-0,50; 3,00] | 0,00 [-1,00; 4,50] |
Примечание: представлены медианы абсолютной динамики и соответствующие им значения 25го и 75го процентилей (Me [Q1; Q3]). АГ – артериальная гипертония.
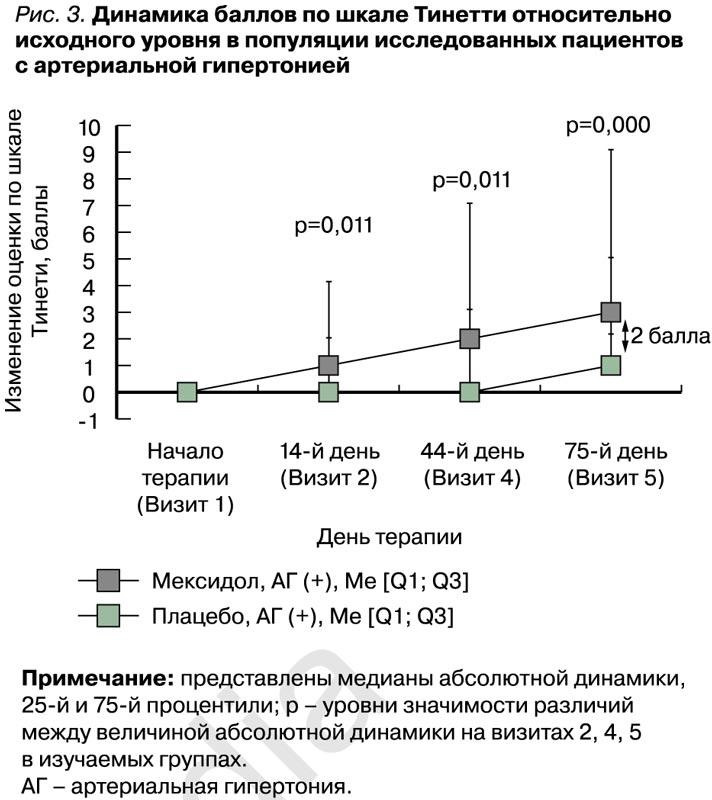
В динамике баллов по опроснику SF-36 (физический компонент здоровья) ни на одном из визитов статистически значимых различий выявлено не было. Вместе с тем наблюдалась тенденция к нарастанию количества баллов по данному опроснику среди пациентов с АГ, получавших последовательную терапию препаратами Мексидол® + Мексидол® ФОРТЕ 250, начиная с Визита 4 (по сравнению с Визитом 1), что указывает на тенденцию к улучшению физического компонента здоровья.
При анализе изменений в психологическом компоненте здоровья согласно опроснику SF-36 среди пациентов с АГ были обнаружены статистически значимые (p=0,000) различия между группами Мексидол® + Мексидол® ФОРТЕ 250 и Плацебо в величине медиан абсолютной динамики на визите 5 относительно исходного уровня: 5,50 [1,00; 11,00] и 1,00 [-2,00; 8,00] баллов соответственно, т.е. +4,5 балла в пользу группы активной терапии (табл. 8, рис. 4). Других статистически значимых различий между группами в абсолютной динамике результатов этого теста обнаружено не было. Полученные результаты демонстрируют статистически значимое улучшение в психологическом аспекте качества жизни в группе пациентов с АГ, применявших Мексидол® + Мексидол® ФОРТЕ 250, по сравнению с группой больных с АГ, получавших плацебо.
Таблица 8. Динамика баллов по опроснику SF-36 (психологический компонент здоровья) у исследованных пациентов на разных визитах в сравнении с исходным уровнем
| Группы па циентов | Визит 2 | p | Визит 4 | p | Визит 5 | p |
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (+) |
1,00 [-1,00; 5,50] | 0,623 | 3,00 [0,00; 9,00] | 0,083 | 5,50 [1,00; 11,00] | 0,010 |
| Плацебо, АГ(+) | 0,00 [-1,00; 4,00] | 1,00 [-1,00; 6,00] | 1,00 [-2,00; 8,00] | |||
| Мексидол® + Мексидол® ФОРТЕ 250, АГ (-) |
1,00 [0,00; 4,00] | 2,00 [0,00; 13,00] | 3,00 [-2,00; 14,00] | 1,000 | ||
| Плацебо, АГ (-) | 0,50 [-2,00; 5,00] | 7,00 [-1,00; 10,00] | 7,50 [-2,50; 12,00] |
Примечание: представлены медианы абсолютной динамики и соответствующие им значения 25-го и 75-го процентилей (Me [Q1; Q3]). АГ – артериальная гипертония.
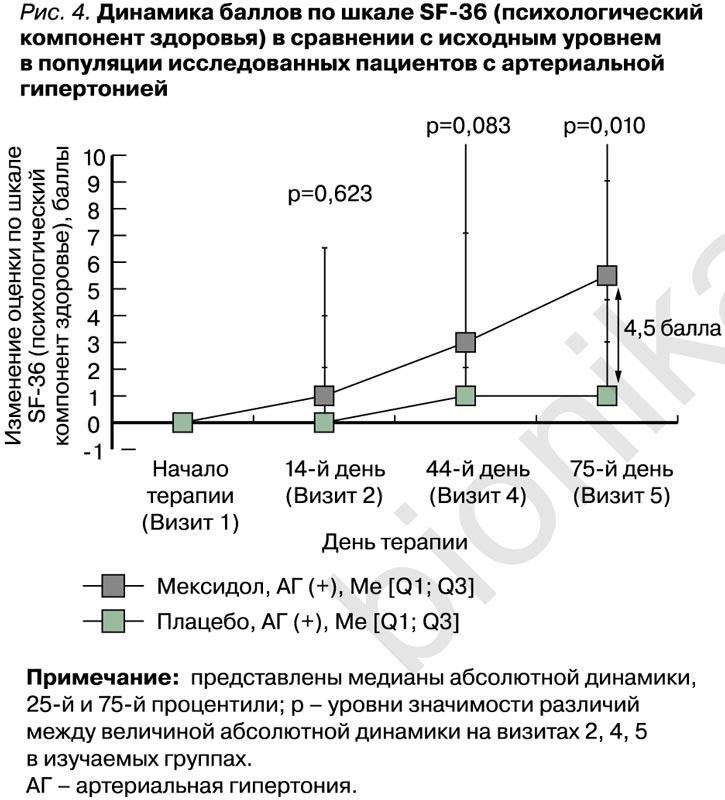
Динамика показателей Шкалы общего клинического впечатления (CGI) оценивалась по значениям, зафиксированным на визитах 2 и 5 (табл. 9 и 10), в сравнении с данными, полученными на визите рандомизации (визит 1).
Таблица 9. Динамика состояния исследованных пациентов согласно Шкале общего клинического впечатления (GCI) на визите 2
| CGI | Пациенты с артериальной гипертензией в анамнезе | Пациенты без артериальной гипертензии в анамнезе | |||
| Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | Мексидол® + Мексидол® ФОРТЕ 250 |
Плацебо | ||
| 01 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ отсутствуют) | Абс. | 19 | 9 | 1 | 0 |
| % | 13,19% | 6,21% | 6,67% | 0,00% | |
| 03 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ оказывают значительное влияние на жизнедеятельность пациента) | Абс. | 2 | 1 | 0 | 0 |
| % | 1,39% | 0,69% | 0,00% | 0,00% | |
| 04 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ превосходят терапевтическое воздействие) | Абс. | 0 | 1 | 1 | 0 |
| % | 0,00% | 0,69% | 6,67% | 0,00% | |
| 05 (Умеренное улучшение. Частичная ремиссия симптомов. НЯ отсутствуют) | Абс. | 14 | 9 | 2 | 0 |
| % | 9,72% | 6,21% | 13,33% | 0,00% | |
| 09 (Незначительное улучшение, которое не изменяет объем требуемой помощи пациенту. НЯ отсутствуют) | Абс. | 71 | 49 | 4 | 4 |
| % | 49,31% | 33,79% | 26,67% | 33,33% | |
| 10 (Незначительное улучшение, которое не изменяет объем требуемой помощи пациенту. НЯ не оказывают существенного влияния на жизнедеятельность пациента) | Абс. | 3 | 2 | 1 | 0 |
| % | 2,08% | 1,38% | 6,67% | 0,00% | |
| 11 (Незначительное улучшение, которое не изменяет объем требуемой помощи пациенту. НЯ оказывают значительное влияние на жизнедеятельность пациента) | Абс. | 1 | 0 | 0 | 0 |
| % | 0,69% | 0,00% | 0,00% | 0,00% | |
| 13 (Состояние не изменилось или ухудшилось. НЯ отсутствуют) | Абс. | 34 | 74 | 6 | 8 |
| % | 23,61% | 51,03% | 40,00% | 66,67% | |
| Различия между группами | Критерий χ² Пирсона: p=0,003 | ||||
Примечание: НЯ – нежелательные явления.
Таблица 10. Динамика состояния исследованных пациентов согласно Шкале общего клинического впечатления (GCI) на визите 5
| CGI | Пациенты с артериальной гипертензией в анамнезе | Пациенты без артериальной гипертензии в анамнезе | |||
| Мексидол®+ Мексидол® ФОРТЕ 250 |
Плацебо | Мексидол®+ Мексидол® ФОРТЕ 250 |
Плацебо | ||
| 01 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ отсутствуют) | Абс. | 42 | 6 | 3 | 1 |
| % | 29,58% | 4,20% | 20,00% | 8,33% | |
| 03 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ оказывают значительное влияние на жизнедеятельность пациента) | Абс. | 0 | 0 | 1 | 0 |
| % | 0,00% | 0,00% | 6,67% | 0,00% | |
| 04 (Значительное улучшение. Полная или почти полная ремиссия всех симптомов. НЯ превосходят терапевтическое воздействие) | Абс. | 0 | 1 | 0 | 0 |
| % | 0,00% | 0,70% | 0,00% | 0,00% | |
| 05 (Умеренное улучшение. Частичная ремиссия симптомов. НЯ отсутствуют) | Абс. | 37 | 16 | 2 | 0 |
| % | 26,06% | 11,19% | 13,33% | 0,00% | |
| 09 (Незначительное улучшение, которое не изменяет объем требуемой помощи пациенту. НЯ отсутствуют) | Абс. | 45 | 47 | 9 | 9 |
| % | 31,69% | 32,87% | 60,00% | 75,00% | |
| 10 (Незначительное улучшение, которое не изменяет объем требуемой помощи пациенту. НЯ не оказывают существенного влияния на жизнедеятельность пациента) | Абс. | 3 | 0 | 0 | 0 |
| % | 2,11% | 0,00% | 0,00% | 0,00% | |
| 13 (Состояние не изменилось или ухудшилось. НЯ отсутствуют) | Абс. | 15 | 73 | 0 | 2 |
| % | 10,56% | 51,05% | 0,00% | 16,67% | |
| Различия между группами | Критерий χ² Пирсона: p=0,000 | ||||
Примечание: НЯ – нежелательные явления.
Обращает на себя внимание, что, согласно шкале CGI, именно среди пациентов, получавших последовательную терапию препаратами Мексидол® + Мексидол®, и преимущественно в группе участников с АГ наблюдалась более частая встречаемость положительного терапевтического эффекта, описываемого как улучшение разной степени выраженности и сочетавшегося в большинстве случаев с полным отсутствием нежелательных явлений. Подобная статистически значимая структура результатов отмечалась, начиная уже с визита 2, и становилась более отчетливой и значимой на визите 5.
Безопасность терапии. Среди участников исследования с АГ было зарегистрировано 50 нежелательных явлений (НЯ), ни одно из которых не было серьезным. НЯ были выявлены у 15 (10,42%) пациентов в группе Мексидол® + Мексидол® ФОРТЕ 250 (всего 19 НЯ) и у 19 (12,93%) – в группе Плацебо (всего 31 НЯ). Различия между группами по частоте обнаружения НЯ оказались статистически незначимы (p=0,505). Все зарегистрированные в настоящем исследовании НЯ имели легкую и умеренную степени тяжести, причем в обеих группах подавляющее большинство НЯ (45) соответствовало легкой степени: 19 (100,00%) в группе Мексидол® + Мексидол® ФОРТЕ 250 и 26 (83,87%) в группе Плацебо. Различия между группами по степени тяжести побочных эффектов также были статистически незначимы (p=0,142). В большинстве случаев (36) НЯ в обеих группах разрешались самостоятельно (13 (68,42%) в группе Мексидол® + Мексидол® ФОРТЕ 250 и 23 (74,19%) в группе Плацебо), и никакие дополнительные действия для их купирования не требовались.
Обсуждение
В исследовании МЕМО первичным критерием эффективности служила динамика среднего балла по шкале МоСА. MoCA-тест представляет собой инструмент диагностики КН, в том числе сосудистого генеза, который оценивает различные когнитивные функции: внимание, планирование и контроль, память, зрительно-пространственные способности, абстрагирование, способность к счету и ориентацию [15-17]. Максимально возможное количество баллов по данному тесту составляет 30, нормальным считается показатель ≥26 баллов. В представленном субанализе исследования МЕМО длительная последовательная терапия препаратами Мексидол® + Мексидол® ФОРТЕ 250 у пациентов с АГ продемонстрировала более высокую эффективность по сравнению с плацебо в отношении когнитивного функционирования при его оценке по шкале МоСА. Эффективность указанной терапии подтверждалась нарастающей положительной динамикой результатов MoCA-теста, уже начиная с визита 2, и ее статистически значимо большей выраженностью по сравнению с группой плацебо. Показателен факт достижения уровня нормы по этому тесту (согласно медиане общего балла) среди больных, получавших Мексидол® + Мексидол® ФОРТЕ 250, как в подгруппе пациентов с АГ, так и без таковой.
В дополнение к этому в популяции исследованных пациентов с АГ, получавших длительную последовательную терапию препаратами Мексидол® + Мексидол® ФОРТЕ 250, наблюдалось статистически значимо (p=0,000) более выраженное увеличение баллов по тесту замены цифровых символов на визите 5 относительно исходного уровня в сравнении с больными АГ, рандомизированными в группу плацебо; это также доказывает улучшение когнитивного функционирования на фоне изучаемой терапии. Тест замены цифровых символов [18-20] оценивает в целом состояние психомоторных процессов: скорость обработки зрительно-пространственной информации, оперативную память, концентрацию и поддержание внимания. Считается [21], что преимущество этого теста заключается в его способности выявлять лиц с самыми начальными признаками КН.
Результаты настоящего субанализа в аспекте регресса когнитивных расстройств на фоне активной терапии соотносятся, в частности, с данными исследования Е.В. Болотовой с соавт. [10], в котором изучались эффективность и переносимость препарата Мексидол® как корректора КН у пациентов с АГ и клиническими проявлениями хронической недостаточности мозгового кровообращения. Было сформировано две группы пациентов с АГ: в первой пациенты получали только антигипертензивную терапию, во второй в дополнение к ней назначался Мексидол®. На фоне последовательной терапии препаратом Мексидол® (внутривенно струйно в суточной дозировке 200 мг в течение 10 дней, далее перорально 500 мг/сут в продолжение еще 6,5 нед, улучшение памяти отметили 50%, концентрацию внимания – 55%, исчезновение тревожности – 67% пациентов. В группе активной терапии этилметилгидроксипирина сукцинатом наблюдалась статистически значимо (р <0,02) более выраженная положительная динамика в тесте рисования часов, достигшая уровня +0,95 балла; в группе рутинной антигипертензивной терапии аналогичный показатель составил +0,54. Только в группе Мексидола имело место статистически значимое увеличение количество баллов по шкале МоСА (с 24,4±0,7 исходно до 26,5±0,9 баллов в конце периода наблюдения) и краткой шкале оценки психического статуса (с 26,85±1,1 исходно до 28,71±0,8 в конце периода набдения; р<0,001 в обоих случаях). Полученные результаты свидетельствуют об эффективности Мексидола в плане регресса КН сосудистого и нейродегенеративного генеза.
В исследовании МЕМО способность к двигательной активности оценивалась с помощью шкалы Тинетти [22, 23]. В подгруппе пациентов с АГ в настоящем субанализе была выявлена нарастающая по своей выраженности положительная динамика показателей шкалы Тинетти на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250, что говорит об улучшении двигательной активности, включая улучшение показателей равновесия и ходьбы.
Такие результаты соотносятся с выводами исследования Е.И. Чукановой и А.С. Чукановой [14], в котором выполнялся анализ эффективности и безопасности применения этиметилгидроксипиридина сукцината в форме внутривенных капельных инфузий (500 мг 1 раз/сут) на протяжении 14 дней с дальнейшим переходом на пероральный прием препарата (Мексидол® ФОРТЕ 250 в дозе 250 мг 3 раза/сут) в течение последующих 60 дней у пациентов с хронической ишемией головного мозга на фоне АГ и атеросклеротического поражения сосудов. В это исследование вошли 60 пациентов, составивших две группы по 30 человек: первая группа получала Мексидол® по описанной выше схеме, вторая представляла собой группу контроля, сопоставимую с основной по возрасту, факторам риска и степени выраженности неврологических нарушений. Пациенты обеих групп получали базисную терапию, направленную на коррекцию имеющихся факторов риска и сопутствующих состояний (антигипертензивные, кардиотропные, антитромботические средства по показаниям). Двигательные нарушения анализировались посредством шкалы Тинетти. При исходной оценке параметров двигательной активности по этой шкале у пациентов основной группы, получавших Мексидол®, средний балл составлял 25,9± 1,9. В последующем на втором визите (на 14-е сутки терапии) этот показатель возрос на 7,3 балла и составил 33,2±2,4 (р <0,05 по сравнению с исходным уровнем), а в конце периода наблюдения (третий визит на 74-е сутки) статистически значимо увеличился до 38,7±2,1 баллов (р <0,01 относительно исходного уровня). В группе контроля динамика балльной оценки по шкале Тинетти статистически значимо не изменялась и равнялась 25,5±1,8 баллов исходно, 26,2±1,9 баллов на визите 2 и 25,2±2,3 баллов на визите 3.
В ходе исследования МЕМО и настоящего субанализа анализировалось влияние терапии препаратом Мексидол® на выраженность симптомов астении по шкале MFI-20 [24]. В настоящем субанализе также была установлена нарастающая положительная динамика при оценке по шкале MFI-20 на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250 у пациентов с АГ, что доказывает регресс выраженности астении.
Сходные результаты были получены в работе Е.И. Чукановой с соавт. [12], где изучались эффективность и безопасность включения Мексидол® ФОРТЕ 250 в комплексную терапию хронической церебральной венозной недостаточности. Было сформировано 3 группы участников: в первой (n=40) пациентам назначались перорально Мексидол® ФОРТЕ 250 и диосмин + гесперидин в течение 74 дней в сочетании с двумя курсами L-лизина эсцината внутривенно на 1-е и 30-е сутки от начала лечения; во второй (n=40) применялись перорально Мексидол® ФОРТЕ 250 и диосмин + гесперидин в течение 74 дней; в третьей (n=40) использовался только пероральный препарат, содержащий диосмин + гесперидин, на протяжении тех же 74 дней. Среди прочих результатов в первой и второй группах (где в комплексную терапию добавлялся этилметилгидроксипиридина сукцинат) отмечалась статистически значимая положительная динамика показателей по шкале MFI-20, иллюстрирующая уменьшение симптоматики астении: уже на 37-е сутки от начала наблюдения произошло снижение среднего балла по указанной шкале с 23,5±5,0 до 12,2±4,5 и с 22,0±4,6 до 11,9±3,0 в первой и второй группах соответственно (p <0,05 в обоих случаях). В дальнейшем положительная динамика сохранялась, и к 74-м суткам наблюдения общий балл по MFI-20 снизился до 10,0±4,2 балла в первой группе и до 10,1±4,1 во второй (р <0,001 в обоих случаях). При этом статистически значимых изменений результатов по шкале MFI-20 у пациентов третьей группы, не получавших этилметилгидроксипиридина сукцинат, выявлено не было.
В субанализе исследования МЕМО в популяции пациентов с АГ была обнаружена нарастающая положительная динамика в виде уменьшения уровня тревоги по шкале Бека на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250, причем абсолютная величина динамики этого показателя была статистически значимо более выражена на визитах 4 и 5 (р=0,003 и р=0,000) по сравнению с группой плацебо.
Выраженность вегетативных нарушений оценивалась согласно опроснику Вейна [25]. В настоящем субанализе наблюдалась тенденция к прогрессивному снижению количества баллов по опроснику Вейна среди пациентов с АГ, получавших Мексидол® + Мексидол® ФОРТЕ 250, начиная с визита 4 (по сравнению с визитом 1), что демонстрирует уменьшение выраженности вегетативных нарушений на фоне изучаемой терапии.
В упомянутой выше работе Е.И. Чукановой с соавт. [12] были получены схожие результаты. В ней уровень тревоги оценивали с помощью шкалы тревоги Гамильтона. У пациентов первой группы, где в комплексной терапии применялся Мексидол®, отмечалась положительная статистически значимая динамика по данной шкале: исходно больные имели 15,9±6,8 баллов, к 37-м суткам показатель снизился до 6,9±1,1 баллов (р <0,05), а на 74-е сутки достиг 3,1±0,7 (р <0,001), что говорит об отсутствии тревожных нарушений. Аналогичные результаты были получены и у пациентов второй группы, где в комплексное лечение также включался Мексидол®: при исходном показателе по шкале тревоги Гамильтона в 15,5±7,7 баллов к 37-м суткам терапии наблюдалась тенденция к нормализации эмоционального состояния в виде снижения суммарного балла до 8,1±2,4 баллов, а в конце периода наблюдения (на 74 сутки) результат составлял 3,7±1,1 баллов (р <0,05 по сравнению с исходным уровнем). В третьей группе пациентов, не получавших этилметилгидроксипиридина сукцинат в составе комплексной терапии, статистически значимых изменений по рассматриваемой шкале обнаружено не было. У пациентов, применявших Мексидол®, также снизилась тяжесть вегетативных нарушений по модифицированному опроснику Вейна с исходных 28,0±6,0 баллов в группе 1 и 26,1±6,5 баллов в группе 2 до 6,7±3,1 баллов (р <0,001) и 7,6±3,9 баллов (р <0,05) соответственно. В третьей группе статистически значимых изменений показателей по опроснику Вейна не отмечалось.
Показатели качества жизни в исследовании МЕМО оценивались посредством опросника SF-36 [26, 27]. В описываемом субанализе на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250 наблюдалась тенденция к нарастанию количества баллов в физическом компоненте здоровья по опроснику SF-36 среди пациентов с АГ. Также на визите 5 медиана абсолютной динамики психологического компонента здоровья по данным SF-36 была статистически значимо (р=0,000) выше у пациентов с АГ, получавших Мексидол® + Мексидол® ФОРТЕ 250, по сравнению с больными АГ, принимавшими плацебо.
Это соотносится с результатами исследования препарата Мексидол® у пациентов с хронической ишемией головного мозга [11], в котором на фоне проводимой терапии показатель оценки с пересчетом полезности по шкале качества жизни SF-36 при исходном значении в 0,6±0,07 баллов к 14-м суткам достиг 0,8±0,03 (р <0,05), а к концу периода наблюдения (74-е сутки) увеличился до 0,9±0,02 баллов (р <0,01). В то же время в группе сравнения в этой работе статистически значимых изменений по шкале SF-36 обнаружено не было.
Наконец, в настоящем субанализе преимущественно у пациентов с АГ на фоне длительной последовательной терапии Мексидол® + Мексидол® ФОРТЕ 250 в соответствии с данными Шкалы общего клинического впечатления (GCI) отмечалась более частая встречаемость положительного терапевтического эффекта, описываемого как улучшение разной степени выраженности и сочетающегося в большинстве случаев с полным отсутствием НЯ.
В целом подобные преимущества Мексидола у пациентов с АГ с ХИМ, и прежде всего его высокая эффективность в аспекте торможения прогрессирования и регресса сосудистых КН, можно объяснить мультимодальным спектром терапевтических влияний препарата, включающих выраженные антиоксидантные, мебмраностабилизирующие и антигипоксантные свойства [13]. Препарат обеспечивает также непосредственную нейрональную защиту посредством прямого действия на дыхательную цепь митохондрий, способствуя ее восстановлению при ишемии и гипоксии и активируя энергообмен в нейроне [13]. Мексидол® угнетает глутамат-индуцируемую эксайтотоксичность, аскорбат-зависимое и НАДФН2-зависимое перекисное окисление липидов, протекающее при участии ионов железа, связывает супероксидный анионрадикал, повышает активность селен-зависимой глутатионпероксидазы, обеспечивая подавление оксидативного стресса [28]. В дополнение к этому доказана способность Мексидола тормозить АДФ-индуцированную агрегацию тромбоцитов, улучшать функцию эндотелия и реологию крови за счет повышения соотношения простациклин/ тромбоксан А2 [14]. В условиях применения этилметигидроксипиридина сукцината улучшается антиагрегационный профиль сосудистой стенки и показатели эндотелий-зависимой вазодилатации [13]. Такой спектр мультимодальных плейотропных эффектов Мексидола может лежать в основе всех тех положительных эффектов на уровне центральной нервной системы, которые были продемонстрированы в приведенном субанализе исследования МЕМО у пациентов с АГ.
Заключение
Таким образом, принимая во внимание высокую клиническую эффективность препарата Мексидол®, сочетающуюся с благоприятным профилем безопасности, возможно рекомендовать использование этого препарата в клинической практике в комплексной терапии пациентов с АГ и ХИМ. В данном случае Мексидол® выступает в качестве фармакологического «инструмента» защиты головного мозга как органа-мишени при АГ и средства патогенетически обоснованной терапии когнитивных, эмоциональных, вегетативных и двигательных нарушений. Рекомендованная схема терапии, подтвердившая свою эффективность и высокий профиль безопасности у пациентов с ХИМ на фоне АГ: инъекции по 500 мг/сут в течение 14 дней с последующим применением таблеток Мексидол® ФОРТЕ 250 по 250 мг 3 раза/сут в течение 2 мес.
Литература/References
- Федин А.И., Захаров В.В., Танашян М.М. с соавт. Результаты международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами Мексидол и Мексидол ФОРТЕ 250 (исследование МЕМО). Журнал неврологии и психиатрии имени С.С. Корсакова. 2021; 121(11): 7-16. [Fedin A.I., Zakharov V.V., Tanashyan M.M. et al. Results of an international multicenter, randomized, double-blind, placebo-controlled study assessing the efficacy and safety of sequential therapy with Mexidol and Mexidol FORTE 250 in patients with chronic brain ischemia (MEMO). Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2021; 121(11): 7-16 (In Russ.)]. dx.doi.org/10.17116/jnevro20211211117. EDN: OBNTNH.
- Захаров В.В., Слепцова К.Б., Мартынова О.О. Хроническая ишемия мозга: взгляд из XXI века. РМЖ. 2021; 29(5): 45-49. [Zakharov V.V., Sleptsova K.B., Martynova O.O. Chronic cerebral ischemia: a view from the XXI century. Russkiy meditsinskiy zhurnal = Russian Medical Journal. 2021; 29(5): 45-49 (In Russ.)]. EDN: ISMXTS.
- Табеева Г.Р. Клиническая феноменология, механизмы формирования и патогенетическая терапия ранних проявлений хронической ишемии мозга. Клиническая фармакология и терапия. 2015; 24(4): 11-17. [Tabeeva G.R. Clinical phenomenology, mechanisms of formation and pathogenetic therapy of early manifestations of chronic brain ischemia. Klinicheskaya farmakologiya i terapiya = Clinical Pharmacology and Therapy. 2015; 24(4): 11-17 (In Russ.)]. EDN: VPRAOR.
- Мартынов А.И., Верткин А.Л., Данилов А.Б. с соавт. Консенсус по ведению пациентов с хронической ишемией мозга для терапевтов и врачей общей практики. Терапия. 2020; 6(7): 15-21. [Martynov A.I., Vertkin A.L., Danilov A.B. et al. Consensus for the management of patients with chronic ischemia of the brain for therapists and general practitioners. Terapiya = Therapy. 2020; 6(7): 15-21 (In Russ.)]. dx.doi.org/10.18565/therapy.20207.14-21. EDN: HNQCZT.
- Azarpazhooh M.R., Hachinski V. Vascular cognitive impairment: A preventable component of dementia. Handb Clin Neurol. 2019; 167: 377-91. dx.doi.org/10.1016/B978-0-12-804766-8.00020-0.
- Клинические рекомендации. Артериальная гипертензия у взрослых. Общероссийская общественная организация «Российское кардиологическое общество». Рубрикатор клинических рекомендаций Минздрава России. 2020. ID: 62. Доступ: https:// cr.minzdrav.gov.ru/schema/62_2 (дата обращения – 14.01.2023). [Clinical guidelines. Arterial hypertension in adults. Russian Society of Cardiology. Rubricator of clinical guidelines of the Ministry of Healthcare of Russia. 2020. ID: 62. URL: cr.minzdrav.gov.ru/schema/62_2 (date of access – 14.01.2023) (In Russ.)].
- Di Chiara T., Del Cuore A., Daidone M. et al. Pathogenetic mechanisms of hypertension-brain-induced complications: Focus on molecular mediators. Int J Mol Sci. 2022; 23(5): 2445. dx.doi.org/10.3390/ijms23052445
- Williams B., Mancia G., Spiering W. et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension [published correction appears in Eur Heart J. 2019; 40(5): 475]. Eur Heart J. 2018; 39(33): 3021-104. dx.doi.org/10.1093/eurheartj/ehy339.
- Каховская Л.В., Мхитарян Э.А., Ткачева О.Н. с соавт. Эффективность и безопасность Мексидола у пациентов разных возрастных групп в остром и раннем восстановительном периодах полушарного ишемического инсульта (результаты субанализа рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных группах исследования ЭПИКА). Журнал неврологии и психиатрии имени С.С. Корсакова. 2020; 120(8-2): 49-57. [Stakhovskaya L.V., Mkhitaryan E.A., Tkacheva O.N. et al. Efficacy and safety of Mexidol across age groups in the acute and early recovery stages of hemispheric ischemic stroke (results of additional sub-analysis of a randomized double blind multicenter placebo-controlled study, in parallel groups trial EPICA). Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2020; 120(8-2): 49-57 (In Russ.)]. dx.doi.org/10.17116/jnevro202012008249. EDN: JKKCFP.
- Болотова Е.В., Лушпай Т.Ю., Ковригина И.В. Повышение эффективности лечения гипертонической энцефалопатии препаратом Мексидол. Журнал неврологии и психиатрии имени С.С. Корсакова. 2018; 118(4): 61-64. [Bolotova E.V., Lushpay N.Yu., Kovrigina I.V. Improvement of the efficacy of treatment of hypertensive encephalohathy by using Mexidol. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2018; 118(4): 61-64 (In Russ.)]. dx.doi.org/10.17116/jnevro20181184161-64. EDN: USBEEW.
- Чуканова Е.И., Чуканова А.С., Мамаева Х.И. Результаты исследования эффективности и безопасности применения Мексидола у пациентов с хронической ишемией мозга. Журнал неврологии и психиатрии имени С.С. Корсакова. 2015; 115(2): 71-74. [Chukanova E.I., Chukanova A.S., Mamayeva Kh.I. The results of the study of the efficacy and safety of Mexidol in patients with chronic cerebral ischemia. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2015; 115(2): 71-74 (In Russ.)]. dx.doi.org/10.17116/jnevro20151152171-74. EDN: TVUMGL.
- Чуканова Е.И., Чуканова А.С., Мамаева Х.И. Клиническая эффективность антиоксидантной терапии Мексидолом ФОРТЕ 250 пациентов с хронической церебральной венозной недостаточностью. Журнал неврологии и психиатрии имени С.С. Корсакова. 2021; 121(3): 57-63. [Chukanova E.I., Chukanova A.S., Mamaeva Kh.I. The efficacy of antioxidant treatment with Mexidol FORTE in 250 patients with chronic cerebral venous insufficiency. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2021; 121(3): 57-63 (In Russ.)]. dx.doi.org/10.17116/jnevro202112103157. EDN: BJOCUH.
- Боголепова А.Н. Роль оксидантного стресса в развитии сосудистых когнитивных расстройств. Журнал неврологии и психиатрии имени С.С. Корсакова. 2020; 120(8): 133-139. [Bogolepova A.N. The role of oxidative stress in the development of vascular cognitive disorders. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2020; 120(8): 133-139 (In Russ.)]. dx.doi.org/10.17116/jnevro2020120081133. EDN: IJCKPO.
- Чуканова Е.И., Чуканова А.С. Эффективность и безопасность препарата Мексидол ФОРТЕ 250 в рамках последовательной терапии у пациентов с хронической ишемией мозга. Журнал неврологии и психиатрии имени С.С. Корсакова. 2019; 119(9): 39-45. [Chukanova E.I., Chukanova A.S. Efficacy and safety of the drug Mexidol FORTE 250 as part of sequential therapy in patients with chronic ischemia of the brain. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2019; 119(9): 39-45 (In Russ.)]. dx.doi.org/10.17116/jnevro201911909139. EDN: PEGQWJ.
- Nasreddine Z.S., Phillips N.A., Bedirian V. et al. The Montreal Cognitive Assessment, MoCA: A brief screening tool for mild cognitive impairment [published correction appears in J Am Geriatr Soc. 2019; 67(9): 1991]. J Am Geriatr Soc. 2005; 53(4): 695-99. dx.doi.org/10.1111/j.1532-5415.2005.53221.x.
- Захаров В.В. Нейропсихологические тесты. Необходимость и возможность применения. Consilium Medicum. 2011; 13(2): 98-106. [Zakharov V.V. Neuropsychological tests. Necessity and possibility of application. Consilium Medicum. 2011; 13(2): 98-106 (In Russ.)]. EDN: RAPIYF.
- Zaidi K.B., Rich J.B., Sunderland K.M. et al. Methods for improving screening for vascular cognitive impairment using the Montreal Cognitive Assessment. Can J Neurol Sci. 2020; 47(6): 756-63. dx.doi.org/10.1017/cjn.2020.121.
- Wechsler D. The measurement of adult intelligence. Baltimore, MD: The Williams & Wilkins Company. 1939.
- Wechsler D. Wechsler adult intelligence scale – Revised manual. New York: Psychological Corporation. 1981.
- Jaeger J. Digit symbol substitution test: The case for sensitivity over specificity in neuropsychological testing. J Clin Psychopharmacol. 2018; 38(5): 513-19. dx.doi.org/10.1097/JCP.0000000000000941.
- Chou M.Y., Nishita Y., Nakagawa T. et al. Role of gait speed and grip strength in predicting 10-year cognitive decline among community-dwelling older people. BMC Geriatr. 2019; 19(1): 186. dx.doi.org/10.1186/s12877-019-1199-7.
- Tinetti M.E. Performance-oriented assessment of mobility problems in elderly patients. J Am Geriatr Soc. 1986; 34(2): 119-26. https ://dx.doi.org/10.1111/j.1532-5415.1986.tb05480.x.
- VanSwearingen J.M., Brach J.S. Making geriatric assessment work: selecting useful measures. Phys Ther. 2001; 81(6): 1233-52. dx.doi.org/10.1093/ptj/81.6d233.
- Smets E.M., Garssen B., Bonke B., De Haes J.C. The Multidimensional Fatigue Inventory (MFI) psychometric qualities of an instrument to assess fatigue. J Psychosom Res. 1995; 39(3): 315-25. dx.doi.org/10.1016/0022-3999(94)00125-o.
- Вегетативные расстройства: клиника, лечение, диагностика. Под ред. А.М. Вейна. М.: Медицинское информационное агентство. 2000; 752 с. [Vegetative disorders: clinic, treatment, diagnosis. [Ed. by Vein A.M. Moscow: Meditsinskoye informatsionnoye agentstvo = Medical Information Agency. 2000; 752 pp. (In Russ.)]. ISBN: 5-89481-066-3.
- Ware J.E. Jr., Sherbourne C.D. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection. Med Care. 1992; 30(6): 473-83.
- Ware J.E. Jr. SF-36 health survey update. Spine (Phila Pa 1976). 2000; 25(24): 3130-39. dx.doi.org/10.1097/00007632-200012150-00008.
- Щулькин А.В. Влияние Мексидола на развитие феномена эксайтотоксичности нейронов in vitro. Журнал неврологии и психиатрии имени С.С. Корсакова. 2012; 112(2): 35-39. [Shchulkin A.V. Effect of Mexidol on the development of the phenomenon of the neuronal excitotoxicity in vitro. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova = S.S. Korsakov Journal of Neurology and Psychiatry. 2012; 112(2): 35-39 (In Russ.)]. EDN: PBZBVV.
Сведения об авторах:
Владимир Владимирович Захаров, д.м.н., профессор кафедры нервных болезней и нейрохирургии ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет). Адрес: 119991, г. Москва, ул. Трубецкая, д. 8, стр. 2. ORCID: orcid.org/0000-0002-8447-3264
Ольга Дмитриевна Остроумова, д.м.н., профессор, зав. кафедрой терапии и полиморбидной патологии им. академика М.С. Вовси ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России; профессор кафедры клинической фармакологии и пропедевтики внутренних болезней ФГАОУ ВО «Первый Московский медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет). Адрес: 125993, г. Москва, ул. Баррикадная, д. 2/1, стр. 1. ORCID: orcid.org/0000-0002-0795-8225. eLibrary SPIN: 3910-6585
Алексей Иванович Кочетков, к.м.н., доцент, доцент кафедры терапии и полиморбидной патологии им. академика М.С. Вовси ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России. Адрес: 125993, г. Москва, ул. Баррикадная, д. 2/1, стр. 1. ORCID: orcid.org/0000-0001-5801-3742. eLibrary SPIN: 9212-6010
Мария Викторовна Клепикова, к.м.н., доцент кафедры терапии и полиморбидной патологии им. академика М.С. Вовси ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России. Адрес: 125993, г. Москва, ул. Баррикадная, д. 2/1, стр. 1. ORCID: orcid.org/0000-0003-4258-1889
Анатолий Иванович Федин, д.м.н., профессор, профессор кафедры неврологии факультета ДПО ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, заслуженный врач РФ. Адрес: 117997, г. Москва, ул. Островитянова, д. 1. ORCID: orcid.org/0000-0002-6996-2828
About the authors:
Vladimir V. Zakharov, MD, professor of the Department of nervous diseases and neurosurgery, I.M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of Russia (Sechenov University). Address: 119991, Moscow, 8/2 Trubetskaya Str. ORCID: orcid.org/0000-0002-8447-3264
Olga D. Ostroumova, MD, professor, head of the Department of therapy and polymorbid pathology named after academician M.S. Vovsi, Russian Medical Academy of Continuous Professional Education of the Ministry of Healthcare of Russia; professor of the Department of clinical pharmacology and propaedeutics of internal diseases, I.M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of Russia (Sechenov University). Address: 125993, Moscow, 2/1 Barrikadnaya Str., bldg. 1. ORCID: orcid.org/0000-0002-0795-8225. eLibrary SPIN: 3910-6585
Alexey I. Kochetkov, PhD in Medical Sciences, associate professor, associate professor of the Department of therapy and polymorbid pathology named after academician M.S. Vovsi, Russian Medical Academy of Continuous Professional Education of the Ministry of Healthcare of Russia. Address: 125993, Moscow, 2/1 Barrikadnaya Str., bldg. 1. ORCID: orcid.org/0000-0001-5801-3742. eLibrary SPIN: 9212-6010
Maria V. Klepikova, PhD in Medical Sciences, associate professor of the Department of therapy and polymorbid pathology named after academician M.S. Vovsi, Russian Medical Academy of Continuous Professional Education of the Ministry of Healthcare of Russia. Address: 125993, Moscow, 2/1 Barrikadnaya Str, bldg. 1. ORCID: orcid.org/0000-0003-4258-1889
Anatoly I. Fedin, MD, professor, professor of the Department of neurology of the Faculty of additional professional education, N.I. Pirogov Russian National Research Medical University of the Ministry of Healthcare of Russia, Honored Doctor of the Russian Federation. Address: 117997, Moscow, 1 Ostrovityanova Str. ORCID: orcid.org/0000-0002-6996-2828
