Результаты применения синтетических антиоксидантов в лечении больных деструктивным панкреатитом
СтатьиОпубликовано в журнале:
« Хирургия » № 3, 2005
Профессора Н.А. Кузнецов и Г.В. Родоман, кандидаты мед. наук А.Т. Бронтвейн и Л.А. Лаберко, Н.В. Мальгина, И.Р. Сумеди
Российский государственный медицинский университет, городская клиническая больница №13, клиническая больница №1 Медицинского центра Управления делами Президента РФ, Москва
Работа основана на результатах обследования и лечения 103 больных панкреонекрозом, находившихся в клинике обшей хирургии на базе ГКБ №13 с 1997 по 2003 г. Исследовано влияние антиоксиданта мексидола на течение острого панкреатита (ОП). Установлено, что мексидол при ОП позволяет замедлить течение деструктивных процессов в поджелудочной железе, способствует быстрому отграничению воспалительного процесса, нормализует клинико-лабораторную картину заболевания, что в итоге позволяет существенно уменьшить частоту развития тяжелых осложнений ОП и снизить летальность.
Results of application of synthetic antioxidants in treatment of patients with destructive pancreatitis
N.A. Kuznetsov, G.V. Rodoman, A.T. Brontvein, L.A. Laberko, N.V. Malgina, I.R. Sumedi
Results of examination and treatment of 103 patients with pancreonecrosis are presented. Influence of antioxidant mexidol on acute pancreatitis (AP) was studied. It is demonstrated that mexidol in AP permits to slow down destructive processes in the pancreas, promotes localization of inflammation and normalization of clinical and laboratory picture of the disease that permits to decrease significantly number of severe complications of AP and reduce lethality.
Khirurgiia (Mosk) 2005; 3: 36-39
Острый панкреатит (ОП) является одной из наиболее актуальных проблем ургентной хирургии. Повсеместно отмечается рост заболеваемости острым панкреатитом и увеличение числа деструктивных форм заболевания [5]. Среди острых хирургических заболеваний органов брюшной полости ОП занимает третье место после острого холецистита и острого аппендицита и составляет 12% [3]. При явном прогрессе хирургических технологий результаты лечения панкреонекроза все же не могут считаться удовлетворительными, поскольку до настоящего времени летальность остается высокой, а сроки лечения - длительными. При стерильном панкреонекрозе летальность достигает 50%, при гнойном панкреонекрозе с явлениями панкреатогенного сепсиса - 80%. Социальная значимость проблемы обусловлена еще и тем, что 70% больных - лица трудоспособного возраста [6, 7].
Патогенез заболевания довольно сложен. Согласно существующим в настоящее время представлениям, острый панкреатит - это первично асептическое воспаление демаркационного типа, характеризующееся каскадной активацией ферментов поджелудочной железы и их аутоагрессией [8]. Морфологические исследования показали, что интегральным моментом, предопределяющим последующее развитие патофизиологических и биохимических нарушений в поджелудочной железе (ПЖ) и организме в целом, при ОП являются функциональные, а затем и структурные изменения клеточных мембран [9]. Поджелудочная железа очень чувствительна к недостатку кислорода и избытку углекислого газа в крови. При ОП наблюдаются значительные изменения кровообращения в сосудах бассейна чревного ствола и верхней брыжеечной артерии, что во многом определяет течение патологического процесса в ПЖ и его генерализацию. Многими исследователями признано участие липопероксидации в развитии патологических процессов в ПЖ. Антиоксидантная активность ПЖ слабая и при ОП создаются все условия для резкой активации липопероксидации [4].
Показано, что применение антиоксидантов при остром панкреатите обеспечивает защиту мембранных структур, препятствует прогрессированию морфофункциональных клеточных нарушений, снижает тяжесть эндогенной интоксикации и выраженность системных нарушений липидного обмена [1]. Одним из препаратов, обладающих антиоксидантными свойствами, является мексидол (2-этил-6-метил-3-оксипиридина сукцинат) - ингибитор свободнорадикальных процессов перекисного окисления липидов, активирующий супероксиддисмутазу и оказывающий влияние на физико-химические свойства клеточной мембраны. Механизм действия мексидола определяется прежде всего его способностью стабилизировать биологические мембраны клеток, активировать энергосинтезирующие функции митохондрий, модулировать работу рецепторных комплексов и прохождение ионных токов, усиливать связывание эндогенных веществ. Мексидол повышает резистентность организма к воздействию экстремальных факторов и кислородзависимым патологическим состояниям [2].
Материал и методы
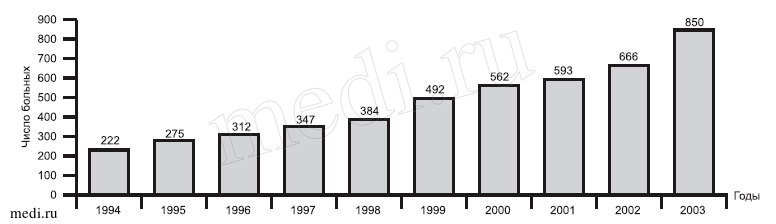
Тенденцию к увеличению числа больных с острым панкреатитом подтверждает статистика их госпитализации в хирургические отделения общего профиля ГКБ №13 Москвы (см. рисунок).
Рис. Рост числа больных с острым панкреатитом, находившихся на лечении в ГКБ №13.
Работа основана на результатах обследования и лечения 103 больных панкреонекрозом в период с 1997 по 2003 г. Мексидол в комплексе лечебных мероприятий был применен у 51 больного (основная группа), 52 пациента составили контрольную группу, в которой этот препарат не использовали. Основная и контрольная группы больных сопоставимы по полу, возрасту, времени, прошедшему с момента заболевания, форме панкреонекроза. Ведущим этиологическим фактором заболевания в обеих группах был алиментарный - соответственно 26 и 34%, билиарный фактор составил соответственно 74 и 66%, причем доминирующее место среди причин острого панкреатита занимал прием алкоголя.
Все больные в условиях хирургического и реанимационного отделений получали комплексное лечение, базисными компонентами которого являлись инфузионная терапия, внутривенное введение соматостатина или его аналогов, антиферментная, антисекреторная, кардиотоническая и антибактериальная терапия. При постановке диагноза панкреонекроза и его осложнений использовалась классификация, рекомендованная на IX Всероссийском съезде хирургов (2000 г.).
Стандартная схема обследования больных включала клиническую оценку их состояния, общий и биохимический анализы крови, определение уровня средне-молекулярных соединений плазмы крови и мочи, лапароскопическое и ультразвуковое исследование органов брюшной полости. Об уровне энзимной токсемии судили по показателям α-амилазы крови и α-амилазы мочи. Масштаб и характер поражения поджелудочной железы, забрюшинной клетчатки и органов брюшной полости оценивали на основании расчета индекса поражения брюшной полости (ИПБП) [5]. Необходимую дозу мексидола подбирали после оценки тяжести состояния пациента в соответствии со шкалой тяжести физиологического состояния (ТФС) [5]. В зависимости от величины суммарного балла ТФС в обеих группах было выделено по 4 подгруппы больных.
Первая подгруппа - ТФС 1-3 балла. Такие значения ТФС имели 13 пациентов основной группы (получали мексидол) и 13 пациентов контрольной группы (мексидол не получали). Летальных исходов не было. У больных этой подгруппы преобладали очаговое поражение поджелудочной железы и жировая форма ацинарной деструкции. Мексидол вводили по 100-200 мг 3 раза в сутки внутривенно и внутримышечно в течение 5 дней.
Вторая подгруппа - ТФС 4-7 баллов. Такие значения ТФС имели 15 пациентов основной группы и 15 пациентов контрольной группы. Различные формы ацинарной деструкции и масштабы поражения поджелудочной железы встречались одинаково часто. В этой подгруппе больным основной группы мексидол вводили по 200 мг 3 раза в сутки в течение 7-10 дней.
Третья подгруппа - ТФС 8-11 баллов. Такие значения ТФС имели 12 пациентов основной группы и 12 пациентов контрольной группы. Доминировали наблюдения смешанной и геморрагической ацинарной деструкции поджелудочной железы с преобладанием субтотально-тотальных форм некротического панкреатита. У больных этой подгруппы острый некротический панкреатит протекал в тяжелой форме, с явлениями панкреатогенного шока, распространенного панкреатогенного перитонита и гнойных парапанкреатических осложнений. Стартовую терапию мексидолом проводили с учетом тяжести состояния больных, манифестации панкреатогенного шока. При наличии последнего в первые сутки лечения суточная доза составляла 1000 мг за два приема. После стабилизации состояния больного мексидол вводили по 300 мг 3 раза в сутки в течение 8-10 дней с постепенным уменьшением дозы.
Четвертая подгруппа - ТФС 12 и более баллов. Такие значения ТФС имели 11 пациентов основной группы и 12 пациентов контрольной группы. Больные четвертой подгруппы характеризовались наиболее тяжелым течением заболевания с преобладанием геморрагической формы ацинарной деструкции и тотальным поражением поджелудочной железы. У всех наблюдалось развитие панкреатогенного шока и распространенного панкреатогенного перитонита, на следующей стадии заболевания развивались гнойные осложнения с прогрессированием эндогенной интоксикации и манифестацией синдрома полиорганной недостаточности. В этой подгруппе схема лечения мексидолом больных основной группы была следующей: стартовая доза 1000 мг в сутки до стойкого купирования явлений панкреатогенного шока в среднем до 5 дней, в дальнейшем по 300-400 мг 3 раза в сутки в течение 10-14 дней с постепенным снижением дозы.
Статистическую обработку полученных результатов проводили с использованием критериев Стьюдента.
Результаты и обсуждение
Первая подгруппа больных. У больных с наименьшей степенью тяжести состояния применение мексидола в комплексе лечения привело к более быстрому купированию явлений ферментемии, эндогенной интоксикации и улучшению субъективного состояния. Клиническая и лабораторная реконвалесценция наступала в среднем к 5-м суткам лечения (табл. 1).
Таблииа 1. Динамика лабораторных показателей у больных первой подгруппы
| Показатель | Основная группа | Контрольная группа | ||
| 1-е сутки | 5-е сутки | 1-е сутки | 5-е сутки | |
| МСМ плазмы, ед . опт. пл. | 0,49±0,04 | 0,24±0,02* | 0,56±0,08 | 0,48±0,07 |
| МСМ мочи, ед. опт . пл. | 1,09±0,19 | 0,35±0,06* | 1,19±0,33 | 0,79±0,11 |
| Лейкоциты, *109/л | 13,05±1,31 | 7,15±0,57* | 10,24±0,78 | 10,39±1,24 |
| α-амилаза мочи, ед/л | 11007±2553 | 434±72* | 2535±852 | 640±154* |
| АлАТ (аланинаминотрансфераза), ед/л | 156,3±34,7 | 60,2±18,9* | 204,9±40,4 | 148,4±26,5 |
| Альбумин, г/л | 39,2±2,8 | 53,1±2,7* | 42,7±3,1 | 35,8±2,7 |
В первой подгруппе у больных основной группы (получавших мексидол) к 5-м суткам лечения количество лейкоцитов достоверно снизилось в 1,8 раза, уровень МСМ плазмы - в 2 раза, МСМ мочи - в 3 раза, содержание α-амилазы мочи - в 13,3 раза, АлАТ - в 2,6 раза и концентрация сывороточного альбумина увеличилась в 1,3 раза. В этой погруппе у больных, не получавших мексидола (контрольная группа), достоверного изменения показателей лейкоцитов, МСМ и АлАТ не произошло, содержание α-амилазы мочи достоверно уменьшилось в 3,9 раза, содержание альбумина снизилось в 1,2 раза по сравнению с исходным уровнем. Применение мексидола не только улучшило динамику лабораторных показателей у больных первой подгруппы, но и оказало влияние на течение процесса в поджелудочной железе и брюшной полости, о чем свидетельствует достоверное снижение ИПБП в 4,5 раза. У больных первой подгруппы, не получавших мексидола, к 5-м суткам лечения динамика ИПБП отсутствовала. Осложненное течение острого панкреатита в первой подгруппе у получавших мексидол больных наблюдалось в 1,6 раза реже, чем у больных, в лечении которых мексидол не применялся (p<0,05).
Таким образом, анализ результатов лечения в этой подгруппе показал, что применение мексидола позволило добиться более быстрой нормализации общего состояния больных, лабораторных показателей и снизить вероятность осложнений, за счет чего произошло достоверное сокращение среднего срока пребывания в стационаре в 1,3 раза.
Вторая подгруппа больных. Клиническая и лабораторная реконвалесценция в этой подгруппе у получавших мексидол больных наступила в среднем к 7-м суткам лечения (табл. 2).
Таблица 2. Динамика лабораторных показателей у больных второй подгруппы
| Показатель | Основная группа | Контрольная группа | ||
| 1-е сутки | 7-е сутки | 1-е сутки | 7-е сутки | |
| МСМ плазмы, ед . опт. пл. | 0,46±0,04 | 0,26±0,02* | 0,63±0,1 | 0,53±0,1 |
| МСМ мочи, ед. опт . пл. | 1,05±0,16 | 0,33±0,04* | 0,96±0,22 | 0,75±0,161 |
| Сахар, ммоль/л | 6,49±0,69 | 4,8±0,25* | 7,23±0,91 | 6,51±0,7 |
| α-амилаза мочи, ед/л | 7464±4021 | 436±179 | 4986±823 | 515±179* |
| Альбумин, г/л | 38,6±0,5 | 47,5±0,6* | 41,1±0,5 | 29,6±0,6* |
В этой подгруппе у больных, леченных без мексидола, к 7-м суткам отсутствовало достоверное снижение уровней СМ и сахара крови, наблюдалось прогрессивное снижение содержания альбумина. Напротив, на фоне лечения мексидолом произошло достоверное снижение уровня МСМ плазмы в 1,8 раза, МСМ мочи в 3,2 раза, сахара крови в 1,4 раза, содержание сывороточного альбумина увеличилось в 1,2 раза. Отмечена также положительная динамика состояния поджелудочной железы: ИПБП на фоне применения мексидола достоверно снизился в 2 раза (p<0,05). У больных, леченных без мексидола, изменения ИПБП к 7-м суткам отсутствовали. Частота осложнений у получавших мексидол больных была в 6,7 раза ниже, чем без его применения (p<0,05).
Таким образом, анализ результатов лечения больных этой подгруппы показал, что применение мексидола позволило добиться более быстрой нормализации лабораторных показателей и значительно снизить вероятность осложнении, за счет чего произошло достоверное сокращение среднего срока пребывания в стационаре в 1,9 раза.
Третья подгруппа больных. Клиническая и лабораторная реконвалесценция в этой подгруппе у получавших мексидол больных наступала в среднем к 10-м суткам лечения (табл. 3).
Таблица 3. Динамика лабораторных показателей у больных третьей подгруппы
| Показатель | Основная группа | Контрольная группа | ||
| 1-е сутки | 10-е сутки | 1-е сутки | 10-е сутки | |
| МСМ плазмы, ед . опт. пл. | 0,93±0,19 | 0,41±0,08* | 1,13±0,29 | 0,89±0,14 |
| α-амилаза мочи, ед/л | 2307±671 | 350±89* | 856±171 | 473±88 |
| Альбумин, г/л | 36,4±2,9 | 48,1±3,4* | 36,0±2,8 | 27,1±2* |
Без применения мексидола к 10-м суткам лечения отсутствовало достоверное снижение содержания МСМ и амилазы мочи и наблюдалось прогрессивное снижение уровня альбумина, при лечении мексидолом произошло достоверное снижение уровня МСМ плазмы в 1,6 раза и α-амилазы мочи в 6,6 раза, а также повышение содержания альбумина в 1,3 раза. Кроме того, на фоне применения мексидола в третьей подгруппе отмечена тенденция к снижению количества лейкоцитов, содержания трансаминаз, билирубина и мочевины.
Достоверные изменения ИПБП отсутствовали, однако на фоне применения мексидола частота осложнений достоверно снизилась в 6,7 раза (p<0,05). В третьей подгруппе летальных исходов в группе больных, получавших мексидол, не было, в группе не получавших этого препарата они составили 8,3%.
При лечении мексидолом отмечено снижение продолжительности лечения в стационаре в 1,4 раза (p<0,05). Таким образом, применение мексидола в этой подгруппе больных привело к значительным положительным результатам.
Четвертая подгруппа больных. Отмечен выраженный противошоковый эффект мексидола с отчетливой стабилизацией основных физиологических параметров, характеризующих состояние больных. Это позволило в 3 наблюдениях выполнить необходимые оперативные вмешательства, в 2 - повторные. Частота гнойных осложнений снизилась в 1,3 раза. На фоне применения мексидола отмечено снижение летальности как на стадии панкреатогенного шока, так и на стадии гнойных осложнений панкреонекроза. В четвертой подгруппе летальный исход при использовании мексидола имел место в 55% наблюдений, без его применения - в 100%, т.е. данный показатель снизился в 1,8 раза.
Представленные данные свидетельствуют об отчетливом благоприятном влиянии мексидола на динамику местного патологического процесса не только в ткани поджелудочной железы, но и в парапанкреатической зоне и в брюшной полости с прогрессивным снижением величины ИПБП. Препарат позволяет эффективно снижать уровень ферментемии, тяжесть проявлений эндогенной интоксикации, оказывает выраженное неспецифическое противовоспалительное, антигипоксантное, гепатопротекторное действие. Очевидна благоприятная тенденция динамики клинико-лабораторных показателей заболевания у больных, получавших мексидол. Все основные показатели приобретали отчетливую тенденцию к нормализации в более ранние сроки, чем у больных контрольной группы, что является критерием стабилизации и купирования воспалительно-некротических процессов, восстановления функционального состояния поджелудочной железы и печени, коррекции нарушений гомеостаза.
Таким образом, использование ингибиторов перекисного окисления липидов позволяет замедлить деструктивные процессы в поджелудочной железе, способствует более быстрому отграничению воспалительных изменений, нормализации клинико-лабораторных показателей и снижению риска летального исхода при некротическом панкреатите.
ЛИТЕРАТУРА
- Власов А.П., Подеров В.Н., Саушев И.В. и др. Нарушения и коррекция гомеостаза при панкреонекрозе. Материалы IX Всероссийского съезда хирургов. Волгоград 2000; 20-22.
- Воронина Т.А. Информационные материалы НИИ фармакологии РАМН. 1999; 1-2: 2-6.
- Ермолов А.С., Иванов П.А., Гришин А.В. и др. Современное состояние диагностики и лечения острого панкреатита. Всероссийский съезд хирургов, 9-й: Материалы. Волгоград 2000; 45-46.
- Колесова О.Е., Маркин А.А., Федорова Т.Н. Перекисное окисление липидов и методы определения продуктов липопероксидации в биологических средах. Лаб дело 1984; 9: 540-546.
- Нестеренко Ю.А., Лаптев В.В., Михайлусов С.В. и др. Лечение панкреонекроза. Рос мед журн 2002; 1: 3-10.
- Савельев B.C., Филимонов М.И., Бурневич С.З. и др. Деструктивный панкреатит: комплексная диагностика и лечение. Новый мед журн 1997; 3: 10-13.
- Савельев B.C., Филимонов М.И., Гельфанд Б.Р. и др. Оценка эффективности современных методов лечения деструктивного панкреатита. Анналы хиргепатол 1996; 1: 58-61.
- Савельев B.C., Гельфанд Б.Р., Филимонов М.Й и др. Оптимизация лечения панкреонекроза: роль активной хирургической тактики и антибактериальной терапии. Анналы хир 2000; 2: 12-16.
- Филимонов М.И., Гельфанд Б.Р., Бурневич С.З. и др. Острый панкреатит 2000; 7-8: 13-14.
