Повышение эффективности релапаротомий в лечении больных перитонитом
СтатьиОпубликовано в журнале:
«Хирургия» №11, 2015.
Д.м.н., проф. А.П. Власов*, к.м.н. Е.К. Салахов, д.м.н., проф. О.Ю. Рубцов
ФГБОУ ВПО «Мордовский государственный университет им. Н.П. Огарева», Саранск
Ключевые слова: релапаротомия, перитонит, санация брюшной полости, энтеральный лаваж, мексидол.
Increase of relaparotomy efficacy in peritonitis manapement
A.P. Vlasov, E.K. Salakhov, O.YU. Rubtsov
N.P. Ogarev Mordovia State University
Keywords: relaparotomy, peritonitis, abdominal sanitation, enteral lavage, mexidol.
Проблема релапаротомии в современной хирургии не теряет своей актуальности в связи с ее достаточно частой встречаемостью и высокой летальностью, достигающей, по данным разных авторов, 40—50% [1, 5, 6]. Современный лечебный алгоритм при релапаротомии остается предметом споров и обсуждений [4, 7, 11]. Поэтому усилия хирургов направлены на поиск оптимальной тактики ведения таких тяжелых пациентов с тем, чтобы максимально снизить риск возможных осложнений и летальности [8, 10].
Цель работы — улучшение результатов релапаротомий путем совершенствования санации брюшной полости и энтерального лаважа.
Материал и методы
Проведен анализ результатов хирургического лечения 72 пациентов с послеоперационным перитонитом в возрасте от 19 до 76 лет, находившихся на лечении в ГБУЗ РМ «РКБ №3» (Саранск) и ГАУЗ «Менделеевская ЦРБ» в период с 2008 по 2015 г. Основную группу составили 42 пациента, которым в ходе релапаротомии брюшную полость санировали раствором антисептика, через назоинтестинальный зонд проводили энтеральный лаваж гипотоническим раствором хлорида натрия до «светлых вод» с последующим введением в просвет тонкой кишки 4 мл 5% раствора мексидола, разведенного в 400,0 мл изотонического раствора хлорида натрия (0,89%). Перед ушиванием брюшной стенки в брюшную полость вводили 4 мл 5% раствора мексидола, разведенного в 20,0 мл изотонического раствора хлорида натрия, и осуществляли ее ультразвуковую низкочастотную обработку при помощи аппарата УРСК-7Н-22. Группа сравнения (контрольная) состояла из 30 пациентов с острым перитонитом, которым проводились лишь промывание брюшной полости раствором антисептика и энтеральный лаваж гипотоническим раствором хлорида натрия.
В послеоперационном периоде оценивали сроки появления моторики кишечника (ультразвуковой контроль, аускультация), выраженность синдрома эндогенной интоксикации и функцию печени. Предметом анализа явились срок пребывания больного в стационаре, осложнения и летальность. Синдром эндогенной интоксикации определяли по содержанию молекул средней массы (МСМ) (254 и 280 нм), общей концентрации альбумина (ОКА) и эффективной концентрации альбумина (ЭКА). Функциональное состояние печени оценивали по рутинным показателям. Для статистической обработки полученных данных использовали программу Microsoft Excel 2007 и статистический пакет SPSS 11.5. При расчетах использовались выборочная средняя (М), средняя квадратическая ошибка (М±m), критерий хи-квадрат (χ2).
Результаты
Пациенты обеих групп по основным исследованным признакам были сопоставимы. При оценке гендерного распределения больных по группам оказалось, что в основной группе было 26 (61,9%) женщин и 16 (38,1%) мужчин. В группе сравнения (контрольной) также преобладали женщины — 18 (60,0%) человек (χ2=0,027, p=0,870). Отсутствовали достоверные различия и в среднем возрасте пациентов. В основной группе он составил 46,2±5,5 года, в контрольной — 42,3±4,8 года (p>0,05). Оценка тяжести перитонита с использованием перитонеального индекса Мангейма показала, что средний показатель в обеих группах практически не отличался и составлял 19,7±2,4 и 18,9±2,6 балла (p>0,05) соответственно.
Изучение причин, повлекших за собой повторное оперативное вмешательство, показало, что в обеих группах преобладала несостоятельность швов анастомозов или ран желудочно-кишечного тракта. Реже встречались ранняя спаечная кишечная непроходимость, абсцессы брюшной полости, прогрессирование вторичного перитонита, послеоперационные кровотечения, перфорация стресс-язв органов желудочно-кишечного тракта, эвентрация органов брюшной полости (табл. 1). Большинство послеоперационных осложнений, требующих выполнения релапаротомии, были обусловлены поздней госпитализацией больных, врачебными ошибками, а также низкой реактивностью организма больного и практически не зависели от лечебных действий при первой операции, в частности способов санации, что согласуется с данными других авторов [4, 7].
Таблица 1.
Причины релапаротомий у пациентов основной и контрольной групп
|
Причина релапаротомии |
Основная группа |
Контрольная группа |
||
|
n |
% |
n |
% |
|
|
Несостоятельность швов кишечника |
13 |
30,9 |
8 |
26,7 |
|
Ранняя спаечная кишечная непроходимость |
9 |
21,4 |
6 |
20,0 |
|
Абсцесс брюшной полости |
5 |
11,9 |
4 |
13,3 |
|
Прогрессирование перитонита |
6 |
14,3 |
5 |
16,6 |
|
Послеоперационное внутрибрюшное кровотечение |
3 |
7,1 |
2 |
6,7 |
|
Перфорация стресс-язв |
2 |
4,8 |
2 |
6,7 |
|
Эвентрация органов брюшной полости |
4 |
9,5 |
3 |
10,0 |
|
Всего |
42 |
100 |
30 |
100 |
При применении предложенной схемы терапии при релапаротомии у больных тяжелым перитонитом получен положительный лечебный эффект. Отмечено сравнительно быстрое купирование воспалительного процесса в брюшной полости. Подтверждением явились существенное уменьшение продукции экссудата, восстановление моторики кишечника, снижение температурной реакции. Так, через 1 сут после релапаротомии количество экссудата, оттекающего по дренажам, по сравнению с группой сравнения уменьшилось на 12,1% и составило 132,6±15,8 мл (p<0,05), через 2 сут — на 18,3% и составило 88,2±11,3 мл (p<0,05), через 3 сут — на 24,2% и составило 19,3±9,7 мл (p<0,05). Моторика кишечника в основной группе восстановилась через 58,2±6,1 ч, тогда как в группе сравнения — через 77,5±7,5 ч (p<0,05). Температурная реакция в основной группе больных острым перитонитом в раннем послеоперационном периоде регистрировалась в течение 3,1±0,53 дня, тогда как в группе сравнения — в течение 4,8±0,64 дня (p<0,05).
При использовании схем терапии с мексидолом констатировано существенное уменьшение в плазме крови токсических продуктов гидрофильной и гидрофобной природы (табл. 2). Так, уже через 1 сут после релапаротомии количество среднемолекулярных олигопептидов (МСМ при λ =254 и 280 нм) в плазме крови по сравнению с группой сравнения достоверно уменьшилось на 12,6 и 13,9% соответственно (p<0,05). Через 2 сут после повторной операции диагностировано существенное уменьшение и токсических продуктов гидрофобной природы. Резерв связывающей способности альбумина по сравнению с группой контроля увеличился на 24,5% (p<0,05), а индекс токсичности плазмы снизился на 24,1% (p<0,05). В этот срок уровень токсических продуктов гидрофильной природы был ниже на 25,8 и 15,5% соответственно (p<0,05). В последующие этапы периода наблюдения (3-и и 4-е сутки) в группе больных, которым применен комплекс лечебных процедур с мексидолом, в плазме крови также зарегистрировано заметное уменьшение содержания токсических продуктов.
Таблица 2.
Показатели эндогенной интоксикации у больных острым перитонитом в раннем послеоперационном периоде после релапаротомии (М±m)
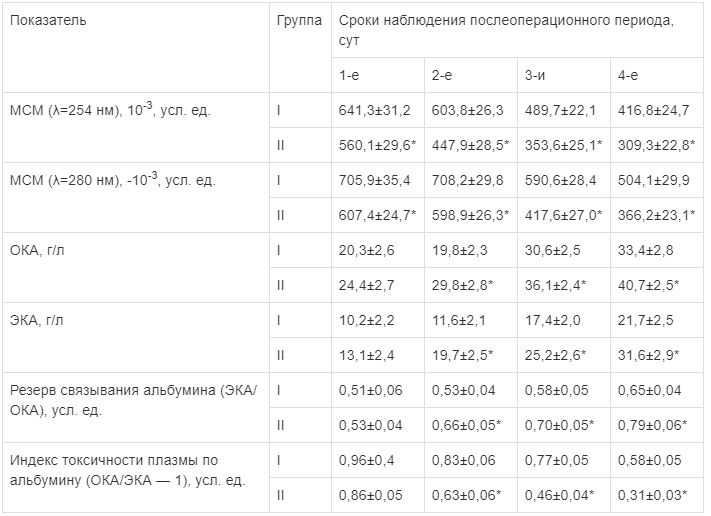 Примечание. I — группа сравнения (контроль); II — основная группа; * — достоверная разница между данными группы сравнения и основной группы при p<0,05.
Примечание. I — группа сравнения (контроль); II — основная группа; * — достоверная разница между данными группы сравнения и основной группы при p<0,05. Таким образом, применение мексидола в комплексной терапии острого перитонита существенно улучшает течение раннего послеоперационного периода. Безусловно, основной областью воздействия терапии является воспаленная брюшина. Ультразвуковая низкочастотная обработка брюшной полости в среде с препаратом мексидол решает двуединую задачу. Во-первых, происходит полноценная механическая обработка брюшины, что в условиях прогрессирующего перитонита зачастую с выраженными явлениями гнойно-фибринозного воспаления имеет важнейшее значение. Во-вторых, при помощи ультразвуковой низкочастотной обработки создаются благоприятные условия для полноценного контакта и максимального действия на брюшину фармакологических свойств мексидола, который обладает антиоксидантным и антигипоксантным эффектами. В результате в брюшине быстрым темпом происходит восстановление морфофункциональных свойств, в частности повышение защитной и пластической функций. Немаловажное значение в улучшении течения раннего послеоперационного периода у больных острым перитонитом после релапаротомии имеет использование мексидола и интестинального лаважа. Известно, что при остром воспалении брюшины, а тем более при затяжном его течении и повторных хирургических вмешательствах функция кишечника существенно нарушается вплоть до развития паралитической кишечной непроходимости. Кишечник становится дополнительным (не исключается, что и основным) источником эндогенной интоксикации вследствие нарушения барьерной функции слизистой оболочки, в патогенезе которой определяющую роль играют структурнофункциональные изменения фосфолипидного бислоя мембраны энтероцитов. Известно, что возникновение мембранодестабилизирующих явлений во многом связано с перекисным окислением липидов и гипоксией. Поэтому применение мексидола в этих условиях также патогенетически оправдано. Безусловно, его способность снижать явления перекисного окисления мембранных липидов и гипоксии тканей приводит к уменьшению энтеральной недостаточности и, как следствие, к снижению эндоинтоксикации. Подтверждение положительного действия препарата находим не только в уменьшении выраженности эндотоксикоза, но и в сравнительно быстром восстановлении моторики кишечника.
Следует отметить позитивный эффект предложенных схем применения препарата и по отношению к печени, функция которой при остром перитоните заметно ухудшается, особенно при тяжелых формах [3]. Установлены сравнительно лучшие характеристики функционального состояния печени у больных основной группы (табл. 3). Фактически почти все исследованные показатели функционального статуса органа уже через 2 сут после операции были заметно лучше, чем у больных группы сравнения.
Таблица 3.
Некоторые показатели функции печени у пациентов основной и контрольной групп через 2 сут после релапаротомии (М±m)
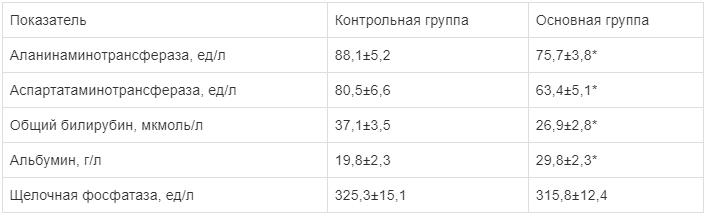 Примечание. * — достоверная разница между данными группы при p<0,05.
Примечание. * — достоверная разница между данными группы при p<0,05. Одним несомненным подтверждением преимущества предложенной схемы терапии явилось достоверное уменьшение повторных лапаросанаций по поводу прогрессирующего перитонита. У пациентов основной группы такая необходимость возникала у 6 (14,3%) человек, тогда как в группе сравнения — у 12 (40,1%) (χ2=6,171, p=0,013). Важнейшим критерием эффективности применения новых подходов в лечении тяжелого перитонита была послеоперационная летальность. У пациентов основной группы она составила 19,0% (n=8), тогда как в группе сравнения — 43,3% (n=13) (χ2=4,996, p=0,025). Достоверные различия числа повторных релапаротомий и показателей летальности у пациентов разных групп позволяют заключить, что применение предложенной схемы лечения больных острым перитонитом способствует существенному улучшению результатов лечения. Это подтверждает и оценка времени пребывания больных в стационаре. У больных основной группы оно составило 18,9±2,4 койко-дня, тогда как в группе сравнения — 25,3±1,9 койко-дня (χ2=4,835, p=0,027).
Обсуждение
На сегодняшний день предложены разнообразные варианты ведения пациентов при релапаротомии, в том числе использование различных схем лаважа брюшной полости, физических методов лечения (лазерного, ультрафиолетового облучения брюшной полости, обработка ультразвуком и др.) и способов коррекции энтеральной недостаточности. Однако, к сожалению, достичь хороших результатов лечения удается далеко не всегда [6, 9]. В целях улучшения результатов нами был предложен новый подход в терапии тяжелого перитонита, основанный на применении при ультразвуковой обработке брюшины и интестинальном лаваже мексидола, который обладает антиоксидантным и антигипоксантным эффектами [2].
Применение препарата в этих важнейших лечебных компонентах обусловливает ряд положительных эффектов, главным из которых является его способность снижать тяжесть синдрома эндогенной интоксикации. Препарат, оказывая антиоксидантное, антигипоксантное, неспецифическое противовоспалительное, гепатопротекторное действия, приводит к уменьшению воспалительных явлений в брюшной полости, заметно снижает явления энтеральной недостаточности, что в целом и обусловливает меньшую «продукцию» токсических субстанций. Очевидно применение и ультразвуковой обработки брюшной полости. Ультразвук оказывает бактерицидный, противовоспалительный и стимулирующий эффекты, а за счет фонофоретического действия увеличивает проникновение мексидола вглубь воспаленных тканей брюшной полости, а также в ткани кишечной стенки и со стороны слизистой оболочки.
Таким образом, при применении предложенной схемы терапии при релапаротомии у больных тяжелым перитонитом отмечается лечебное воздействие на два основных источника эндогенной интоксикации: воспаленную брюшину и кишечник с ухудшенными барьерными свойствами, что и обусловливает существенное уменьшение синдрома эндогенной интоксикации. Подчеркнем, что положительное действие новой схемы лечения определяется в самые ранние сроки после релапаротомии, тем самым препятствуя развитию (прогрессированию) полиорганной недостаточности, которая является основной причиной смерти больных перитонитом.
Выводы
1. Применение у больных перитонитом при релапаротомии ультразвуковой обработки брюшной полости и интестинального лаважа с раствором мексидола приводит к уменьшению повторных лапаросанаций на 25,8%, летальности — на 24,3%, сокращению срока пребывания больных в стационаре на 6,4±0,8 койко дня.
2. Важнейшим лечебным эффектом разработанной схемы, повышающей эффективность терапии тяжелого перитонита, является ее способность сравнительно быстро уменьшать явления воспаления в брюшной полости, восстанавливать функциональный статус кишечника и печени и в итоге существенно уменьшать выраженность синдрома эндогенной интоксикации.
Литература
1. Акилов Х.Д., Кахаров М.А., Сидиков А.У. Плановая релапаротомия в лечении терминальной стадии общего перитонита. Научно-практический журнал ТИППМК. 2011;2:14-19.
2. Батурин В.А., Фишер В.В., Сергеев С.А., Яцук И.В. Магний-кальциевое равновесие и эндотелиальная дисфункция при операционном стрессе. Медицинский вестник Северного Кавказа. 2015;10(1):22-25.
3. Плоткин Л.Л., Бордуновский В.Н., Базарова Е.Н., Смирнов Д.М. Защита печени у больных разлитым гнойным перитонитом, осложненным сепсисом. Анестезиология и реаниматология. 2008;4:39-40.
4. Рахов С.Б., Муканов М.У. Неотложная релапаротомия. Инновационные технологии в хирургии. 2010;1:10-12.
5. Салахов Е.К., Власов А.П. Способы санации брюшной полости при распространенных формах перитонита. Современные проблемы науки и образования. 2014;1.
6. Сандаков П.Я., Старикова А.И. Определение показаний к релапаротомии при распространенном перитоните. Хирургия. Журнал им. Н.И. Пирогова. 2014;4:16-19.
7. Томнюк Н.Д., Рябков И.А., Данилина Е.П. Понятие и классификация релапаротомий в неотложной хирургии. Успехи современного естествознания. 2014;12:18-19.
8. Харченко Д.А., Дубинский Н.В., Лысенко Б.Ф., Ксендз И.В., Туник Р.А., Коваленко Е.А., Толстой О.С., Белоногов А. В., Мокляк Е.В., Слюсарев Н.И., Чернуха Л.В. Ведение больных при программированной релапаротомии. Клиническая хирургия. 2011;8:36-38.
9. Das K, Ozdogan M, Karateke F, Uzun AS, Sozen S, Ozdas S. Comparison of APACHE II, P-POSSUM and SAPS II scoring systems in patients underwent planned laparotomies due to secondary peritonitis. Ann Ital Chir. 2014;85(1):16-21.
10. Kiewiet JJ van Ruler О, Boermeester MA, Reitsma JB. А decision rule to aid selection of patients with abdominal sepsis requiring a relaparotomy. BMC Surg. 2013;13:28.
11. Pauly S, Schulze FP, Horstman O, Becker H, Grade M, Ghadimi M. Value of one-stage surgical treatment of diffuse peritonitis (relaparotomy on demand): a single-center analysis. Zentralbl Chir.2013;138(3):289-294.
