Особенности влияния Мексидола на функциональное состояние центральной нервной системы у больных, перенесших инсульт
СтатьиОпубликовано в журнале:
«Неврологии и психиатрии» №6, 2012.
В.В. Кузнецов*, Ф.В. Юрченко
Институт геронтологии АМН Украины, Киев
Ключевые слова: мексидол, лечение, ЦНС, инсульт.
Effects of mexidol on the functional state of the central nervous system in post-stroke patients
V.V. Kuznetsov, F.V. Yurchenko
Institute of Gerontology, Ukrainian Academy of Medical Sciences, Kiev
Key words: mexidol, treatment, CNS, stroke.
В структуре цереброваскулярной патологии инсульт занимает ведущее место как одна из основных причин смертности и первичной инвалидизации населения [2]. В лечении инсульта в остром периоде на первый план выступают меры по коррекции нарушенных функций организма и поддержанию жизнеспособности нервной ткани. В восстановительном периоде используются препараты, оказывающие активизирующее воздействие на нейротрофические и репаративные процессы, и проводится вторичная профилактика инсульта [1, 8]. Известно, что ишемия головного мозга представляет собой мультифакторный патологический процесс, включающий снижение энергопродукции с нарушением активного транспорта ионов через мембраны клеток, избыточное накопление эксайтоксичных медиаторов возбуждения в структурах мозга, увеличение уровня ионизированного кальция в нейронах, гиперпродукцию свободных радикалов и активацию оксидантного стресса [4, 6, 9, 10]. Для коррекции данных изменений традиционно используются препараты с антигипоксантными и антиоксидантными свойствами, к которым относится и мексидол (2-этил-6-метил-3-гидроксипиридина сукцинат). Мексидол улучшает метаболизм нервной ткани, известно также, что он влияет на реологические свойства крови, снижает агрегацию тромбоцитов, обладает гиполипидемическим действием [5].
Цель настоящего исследования — изучение влияния мексидола на состояние церебральной гемодинамики, биоэлектрической активности головного мозга и липидный спектр крови у пациентов, перенесших инфаркт мозга (ИМ) в каротидном бассейне.
Материал и методы
Обследован 51 пациент в возрасте от 59 до 75 лет. Все включенные в исследование больные перенесли атеротромботический (по критериям TOAST) ИМ в каротидном бассейне (в сроки до 1 года после развития инсульта) и проходили стационарное лечение в отделении реабилитации.
Мексидол назначался в дозе по 200 мг (4 мл) препарата на 100 мл физиологического раствора внутривенно капельно 1 раз в сутки на протяжении 10 дней. Эффективность лечения по выбранным клиническим и параклиническим критериям оценивалась до и после окончания курса мексидола.
Пациентам проводилось клинико-неврологическое обследование с оценкой степени неврологического дефицита по шкале инсульта NIHSS и возможностей самообслуживания в быту по шкале Бартел, а также выполнялся комплекс лабораторно-инструментальных исследований. Исследовались состояние мозгового кровотока методом ультразвукового дуплексного сканирования экстра- и интракраниальных отделов магистральных артерий головы; биоэлектрическая активность мозга методом электроэнцефалографии (ЭЭГ); липидный спектр крови (общий холестерин, триглицериды, липопротеины высокой плотности (ЛПВП), липопротеины низкой плотности (ЛПНП), липопротеины очень низкой плотности (ЛПОНП), индекс атерогенности. Для верификации ИМ проводилась магнитно-резонансная томография (МРТ) головного мозга, при которой у всех больных выявлены очаги ишемии и признаки энцефалопатии сосудистого генеза.
На заключительном этапе исследования выполнялся статистический анализ полученных данных.
Результаты и обсуждение
Анализ клинических данных до и после курса мексидола показал позитивную динамику. У пациентов уменьшились жалобы на общую слабость (выявлялись у 88,2 и 46,5% больных до и после лечения соответственно), сонливость днем (52,4 и 41,2%), головные боли (72,4 и 56,1%), головокружение (42,6 и 33,7%), лабильность настроения (88,2 и 46,5%). Курсовой прием мексидола у больных, перенесших ИМ в правом и левом каротидном бассейне, привел к уменьшению неврологического дефицита по шкале NIHSS (до лечения — 6,9±2,7 балла, после лечения — 6,2±2,2 балла), а также росту индекса повседневной активности Бартел (66,1±13,2 и 73,8±10,5 балла соответственно).
По результатам дуплексного сканирования магистральных артерий головы (табл. 1) выявлено, что после курса приема мексидола у больных, перенесших ИМ в левом полушарии, достоверно (р<0,05) увеличивалась линейная систолическая скорость кровотока (ЛССК) как в ипсилатеральных очагу инфаркта, так и в контралатеральных сосудах. При локализации ИМ в левом полушарии ЛССК в ипсилатеральной общей сонной артерии до лечения препаратом составляла 68,07±1,12 см/с, после лечения — 74,87±1,21 см/с, а в контралатеральной общей сонной артерии — 64,03±1,12 и 69,82±1,31 см/с соответственно. ЛССК в ипсилатеральной внутренней сонной артерии составляла до лечения 64,95±1,12. см/с, после лечения — 71,09±1,1 см/с, в контралатеральной артерии — 58,93±1,12 и 65,28±1,21 см/с соответственно.
Таблица 1.
Динамика линейной систолической скорости кровотока (в см/с) в экстра- и интракраниальных артериях у пациентов после курса мексидола
 Примечание. Здесь и в табл. 2: *р<0,05 - достоверные различия показателя до и после лечения.
Примечание. Здесь и в табл. 2: *р<0,05 - достоверные различия показателя до и после лечения. Изменения состояния гемодинамики у больных с локализацией ИМ в правом полушарии после курсового приема мексидола характеризовались достоверным (р<0,05) увеличением ЛССК во внутренней сонной артерии и позвоночной артерии с двух сторон, в ипсилатеральных очагу передней, средней и задней мозговых артериях, а также в основной артерии (см. табл. 1). Так, после курса лечения у больных, перенесших ИМ в правом полушарии, ЛССК в ипсилатеральной внутренней сонной артерии увеличилась с 53,59±1,42 до 61,81±2,65 см/с, в контралатеральной — с 67,99±1,35 до 74,29±1,78 см/с; в позвоночной артерии ипсилатеральной — с 35,64±1,78 до 41,49±2,01 см/с, в контралатеральной — с 38,58±1,35 до 42,47±1,78 см/с.
Таким образом, после проведенного курса лечения мексидолом у перенесших ИМ пациентов по данным дуплексного сканирования выявлено увеличение ЛССК в экстра- и интракраниальных сосудах. Следует отметить, что влияние курса мексидола на церебральную гемодинамику различается в зависимости от локализации инфаркта в правом или левом полушарии: при локализации ИМ в левом полушарии ЛССК преимущественно увеличивается в обеих общих сонных и в контралатеральных передней и задней мозговых артериях, а при правополушарном ИМ — в обеих позвоночных и в ипсилатеральной передней мозговой артерии.
Принимая во внимание роль функционального состояния свободнорадикального окисления в определении уровня метаболизма нейронов и структуры биоэлектрической активности головного мозга [3, 7], был проведен анализ влияния курсового приема мексидола на частотно-амплитудный спектр ЭЭГ у больных, перенесших ИМ полушарной локализации.
Выявлено, что проведенный курс лечения приводил к достоверным изменениям интенсивности в диапазоне основных ритмов ЭЭГ. Тип этих изменений зависел от локализации ишемического очага. У больных с правополушарным ИМ в пораженном полушарии достоверно (р<0,05) увеличивалась интенсивность в диапазонах δ- и θ-ритма и снижалась интенсивность в этих диапазонах в интактном полушарии на фоне увеличения интенсивности α-1-ритма в центральных и затылочных областях обоих полушарий, а также наблюдалось достоверное (р<0,05) увеличение интенсивности в диапазонах β-1- и β-2-ритма во всех областях пораженного полушария и в отдельных областях интактного полушария. У больных с локализацией ИМ в левом полушарии после проведенного курса лечения отмечено снижение интенсивности в диапазоне медленных ритмов в пораженном полушарии и рост ее в интактном полушарии, а также снижение интенсивности в диапазонах быстрых ритмов в пораженном полушарии и ее рост в в интактном полушарии.
Таким образом, у больных при правополушарном ИМ под влиянием курсового приема мексидола статистически значимо увеличивается интенсивность ЭЭГ в диапазоне медленных и быстрых ритмов в пораженном полушарии, а в интактном полушарии снижается в диапазоне медленных ритмов и увеличивается в диапазоне быстрых ритмов. У больных с левополушарным ИМ под влиянием курсового приема мексидола в пораженном полушарии снижается интенсивность в диапазоне медленных и быстрых ритмов, в интактном — повышается интенсивность этих ритмов. При этом как при правополушарной, так и при левополушарной локализации ИМ курсовой прием мексидола увеличивал среднюю частоту α-ритма в обоих полушариях головного мозга. ;0,05 — достоверные различия показателя до и после лечения.
Для интегральной характеристики влияния курсового приема мексидола на функциональное состояние ЦНС у перенесших ИМ пациентов был проведен корреляционный анализ показателей состояния церебральной гемодинамики и биоэлектрической активности головного мозга. У больных с локализацией ИМ в левом полушарии головного мозга общее количество корреляционных связей между показателями ЛССК в сосудах каротидного и вертебрально-базиллярного бассейнов и интенсивностью основных ритмов ЭЭГ до лечения мексидолом составило 35, тогда как у больных, перенесших ИМ в правом полушарии, таких связей выявлено только 6, после проведенного курса лечения у больных с локализацией ИМ в левом полушарии общее количество корреляций уменьшилось до 24 и полностью нивелировалось у больных, перенесших ИМ в правом полушарии, что может свидетельствовать об усилении автономности биоэлектрической активности головного мозга, обусловленной повышением порога влияния церебральной гемодинамики на электрогенез мозга.
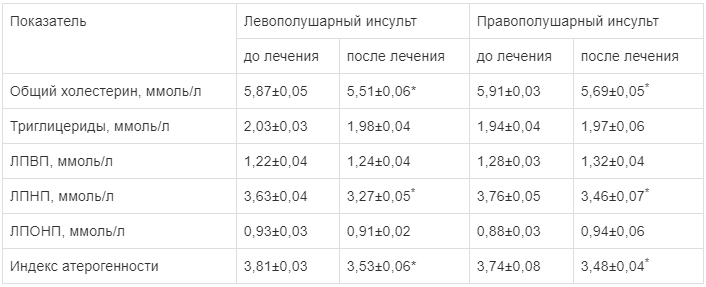
При оценке состояния липидного спектра крови до и после курса лечения мексидолом отмечено достоверное (р<0,05) снижение уровня общего холестерина, ЛПНП и индекса атерогенности (табл. 2).
Таблица 2.
Динамика липидного спектра крови на фоне курсового приема мексидола
 Таким образом, комплексный анализ влияния курсового приема мексидола на церебральную гемодинамику и биоэлектрическую активность головного мозга перенесших ИМ пациентов свидетельствует о гармонизирующем влиянии препарата на функциональное состояние ЦНС и дает основания для рекомендации включения мексидола в систему реабилитации подобных больных. На фоне приема препарата у пациентов отмечались улучшение самочувствия и уменьшение степени выраженности неврологического дефицита. При этом профиль изменений параметров церебральной гемодинамики и биоэлектрической активности мозга имел свои особенности в зависимости от локализации очага инфаркта.
Таким образом, комплексный анализ влияния курсового приема мексидола на церебральную гемодинамику и биоэлектрическую активность головного мозга перенесших ИМ пациентов свидетельствует о гармонизирующем влиянии препарата на функциональное состояние ЦНС и дает основания для рекомендации включения мексидола в систему реабилитации подобных больных. На фоне приема препарата у пациентов отмечались улучшение самочувствия и уменьшение степени выраженности неврологического дефицита. При этом профиль изменений параметров церебральной гемодинамики и биоэлектрической активности мозга имел свои особенности в зависимости от локализации очага инфаркта. Литература
1. Верещагин Н.В., Суслина З.А., Пирадов М.А. Принципы диагностики и лечения больных с острыми ишемическими нарушениями мозгового кровообращения. Мистетцтво лiкування 2006; 7: 26—32.
2. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. М: Медицина 2001; 586.
3. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. Болезни нервной системы. Руководство для врачей. М: Медицина 2005; 302.
4. Дюмаев К.М., Воронина Т.А., Смирнов Л.Д. Антиоксиданты в профилактике и терапии патологии ЦНС. М: Из-во Института биологии медицинской химии РАМН 1995; 4: 2: 73—85.
5. Кадин И.М. Применения препарата мексидол для лечения больных, перенесших инсульт. Бюл экспер биол и мед 2006; 1: 28—31.
6. Лукьянова Л.Д. Современные проблемы гипоксии. Вестник РАМН 2000; 9: 3—12.
7. Мамчур В.И., Дронов С.Н., Жилюк В.И. Церебропротекция: возможности медикаментозной защиты ишемизированного мозга. Рацiональна фармакотерапiя 2008; 3: 1—7.
8. Рябов Г.А. Гипоксия критических состояний. М: Медицина 1988; 288.
9. Geyer J.D., Gomes C.R. Stroke: a practical approach. LWW 2009; 361.
10. Nowinski W., Qian G., Kirgaval N. et al. Analysis of ischemic stroke MR images by means of brain atlases of anatomy and blood supply territories. Academic radiology 2006; 13: 1025—1034.
