Влияние применения мексидола в период «терапевтического окна» ишемического инсульта на эффективность внутривенной тромболитической терапии
СтатьиОпубликовано в журнале:
«Неврология, нейропсихиатрия, психосоматика» № 10(3), 2018
Кнни К.С., Демин Т.В., Адеева Л.Б.
ГАУЗ «Межрегиональный клинико-диагностический центр», Казань, Россия 420101, Республика Татарстан, Казань, ул. Карбышева, 12А
Цель исследования — оценка влияния внутривенного введения мексидола в период «терапевтического окна» на эффективность внутривенной тромболитической терапии (ТЛТ).
Пациенты и методы. В ретроспективное исследование включены 123 пациента с ишемическим инсультом (ИИ), которым была проведена внутривенная ТЛТ в условиях сосудистых центров Республики Татарстан. Для оценки динамики неврологического статуса использовали шкалу тяжести инсульта Национального института здоровья (National Institutes of Health Stroke Scale, NIHSS). В зависимости от исходной выраженности неврологического дефицита все пациенты были разделены на три подгруппы: с ИИ легкой степени тяжести (ЛИ) и оценкой по NIHSS при поступлении <8 баллов; с ИИ средней степени тяжести (СИ) — с оценкой >8 и <16 баллов; с тяжелым ИИ(ТИ) — с оценкой >16 баллов. Рентгеновскую компьютерную томографию выполняли всем пациентам в момент поступления, через 24 ч после проведения ТЛТ, а также при ухудшении состояния.
Результаты. Применение мексидола на догоспитальном этапе с последующим проведением ТЛТ у пациентов с ИИ положительно влияет на регресс неврологического дефицита независимо от тяжести заболевания. Выявлены достоверные различия в степени регресса неврологического дефицита по NIHSS через 24 ч и 10 сут после поступления у пациентов с ТИ, которым вводили мексидол на догоспитальном этапе и которые этот препарат до выполнения ТЛТ не получали. Применение мексидола до проведения ТЛТ способствует большему регрессу неврологического дефицита. Установлена меньшая частота развития геморрагических трансформаций у пациентов, получавших мексидол на догоспитальном этапе, в сравнении с пациентами, которые этот препарат не применяли.
Заключение. Полученные данные демонстрируют положительное влияние мексидола на эффективность и безопасность ТЛТ у пациентов с ИИ.
Ключевые слова: этилметилгидроксипиридина сукцинат; внутривенная тромболитическая терапия; ишемический инсульт; нейропротективная терапия.
Effect of mexidol on the efficiency of intravenous thrombolytic therapy for ischemic stroke during the therapeutic window
Knni K.S., Dyomin T.V., Adeeva L.B.
Interregional Clinical and Diagnostic Center, Kazan, Russia 12A, Karbyshev St., Kazan, Republic of Tatarstan 420101
Objective: to evaluate the effect of intravenous mexidol on the efficiency of intravenous thrombolytic therapy (TLT) during the therapeutic window.
Patients and methods. The retrospective study enrolled 123 patients with ischemic stroke (IS) who had undergone intravenous TLT in the vascular centers of the Republic of Tatarstan. The National Institutes of Health Stroke Scale (NIHSS) was used to assess the time course of changes in their neurological status. According to the baseline severity of a neurological deficit, all the patients were divided into three subgroups: 1) mild IS (<8 NIHSS scores at admission); 2) moderate IS (>8 scores); and 3) severe IS (<16 scores). All the patients underwent X-ray computed tomography at admission, at 24 hours after TLT, and in case of worsening of their health status.
Results. The prehospital use of mexidol followed by TLT in patients with IS had a positive effect on the regression of neurological deficit regardless of the severity of the disease. There were significant differences in the degree of regression of neurological deficit according to NIHSS at 24 hours and 10 days after hospital admission in patients with severe IS, who received intravenous mexidol at the prehospital stage and who did not take this drug before TLT. The pre-TLT use of mexidol contributed to higher regression of neurological deficit. There was a lower frequency of hemorrhagic transformations in the patients who used mexidol at the prehospital stage versus those who did not.
Conclusion. The findings demonstrate the positive effect of mexidol on the efficiency and safety of TLT in patients with IS.
Keywords: ethylmethylhydroxypyridine succinate; intravenous thrombolytic therapy; ischemic stroke; neuroprotective therapy.
Инсульт занимает 3-е место среди причин смертности и 1-е место среди причин инвалидизации взрослого населения в мире. Заболеваемость инсультом в разных странах составляет от 1 до 4 случаев на 1 тыс. населения в год, из них 70—85% — это пациенты с ишемическим инсультом (ИИ) [1—5].Формирование зоны ишемического повреждения мозговой ткани проходит несколько стадий. В первые 3 ч после острого нарушения мозгового кровообращения в ишемизированной ткани максимально представлены энергетический дефицит и лактат-ацидоз. На следующем этапе запускаются механизмы глутаматной эксайтотоксичности и нарушения кальциевого гомеостаза. В начале формирования зоны инфаркта в участках «нищей» перфузии (18—20 мл/100 г/мин) нейроны и клетки глии не функционируют, но сохраняют жизнеспособность в течение нескольких часов. Процесс образования зоны необратимых повреждений мозга завершается к концу 1-х суток. Своевременное оказание медицинской помощи, направленной на восстановление перфузии и энергетического баланса в клетках мозга, может в значительной степени уменьшить выраженность неврологических нарушений при ИИ [6].
Наиболее эффективным патогенетическим методом лечения ИИ в течение первых 4,5 ч после его развития является тромболитическая терапия (ТЛТ) [7—11]. Наряду с реперфузией предотвращению необратимых изменений в зоне инфаркта мозга способствует нейропротекция — применение препаратов, поддерживающих выживание клеток нервной ткани в условиях сниженной перфузии, в частности этилметилгидроксипиридина сукцината (Мексидол®). Этот отечественный препарат является наиболее эффективным и широко применяемым для мультимодальной нейропротекции, что подтверждено рядом клинических исследований [12—17]. Мексидол нормализует клеточный энергосинтез, нарушенный при ишемии, нейтрализует свободные радикалы, стабилизирует мембрану клеток, подавляя перекисное окисление липидов. Благодаря наличию в его структуре сукцината, препарат улучшает эндогенное дыхание митохондрий, активируя их энергосинтезирующие функции по сукцинатоксидазному пути, увеличивает содержание АТФ в мозге, проявляет свойства энергетического субстрата митохондрий. Таким образом, противоишемическое действие мексидола реализуется за счет его антиоксидантного, антигипоксантного и мембраностабилизирующего эффектов. Препарат оказывает дополнительное ноотропное, противосудорожное и анксиолитическое действие, повышает устойчивость организма к стрессу, обладает антиатерогенными и сахароснижающими свойствами, нормализует метаболические процессы.
Сочетание в структуре мексидола двух соединений — 2-этил-6-метил-3-гидроксипиридина и янтарной кислоты — обеспечивает его хорошую проходимость через гематоэнцефалический барьер, высокую биодоступность и воздействие на различные мишени, что определяет широкий спектр эффектов и высокий терапевтический потенциал препарата. Мексидол характеризуется благоприятным профилем безопасности и хорошей переносимостью, низким риском лекарственных взаимодействий. В ряде исследований показано, что раннее (на догоспитальном этапе) его применение при остром нарушении мозгового кровообращения в дозе 200—400 мг внутривенно позволяет существенно снизить выраженность развивающегося неврологического дефицита и достичь общего улучшения состояния пациента [18].
На основании этих данных нами было сделано предположение, что применение мексидола, оказывающего мультимодальное нейропротективное действие, до проведения ТЛТ повысит ее эффективность у пациентов с ИИ.
Цель исследования — оценка влияния внутривенного введения мексидола в период «терапевтического окна» на эффективность внутривенной ТЛТ.
Пациенты и методы. В ретроспективное исследование были включены 123 пациента с ИИ, которым была проведена внутривенная ТЛТ в условиях сосудистых центров Республики Татарстан. Возраст пациентов составил от 45 до 79 лет (средний возраст 58,7±12,8 года). В основную группу вошли 67 пациентов (36/54% женщин и 31/46% мужчина), которым на догоспитальном этапе внутривенно вводили мексидол в дозе 200 мг. Контрольную группу составили 56 пациентов (39/70% женщин и 17/30% мужчин), которые на догоспитальном этапе не получали этот препарат.
ТЛТ проводили в соответствии с «Клиническими рекомендациями по проведению тромболитической терапии при ишемическом инсульте (Национальные клинические рекомендации)».
Для оценки динамики неврологического статуса использовали шкалу тяжести инсульта Национального института здоровья (National Institutes of Health Stroke Scale, NIHSS). Неврологический дефицит по NIHSS определяли до проведения ТЛТ, после ее завершения, через 24 ч и 10 сут.
По исходной выраженности неврологического дефицита все пациенты были разделены на три подгруппы: с ИИ легкой степени тяжести (ЛИ) и оценкой по NIHSS при поступлении <8 баллов; с ИИ средней степени тяжести (СИ) — с оценкой >8 и <16 баллов; с тяжелым ИИ (ТИ) — с оценкой >16 баллов.
Рентгеновскую компьютерную томографию (КТ) выполняли всем пациентам при поступлении, через 24 ч после выполнения ТЛТ, а также при ухудшении состояния (нарастание неврологического дефицита, общемозговой симптоматики). На основании данных КТ выявляли развитие геморрагических трансформаций.
Статистическую обработку данных осуществляли с применением однофакторного дисперсионного анализа (ANOVA). Достоверность различий оценивали при уровне значимости, равном 0,05.
Результаты. До проведения ТЛТ неврологический дефицит по NIHSS у пациентов составлял от 4 до 23 баллов (11,4±5,3). У пациентов с ЛИ в основной группе средний балл по NIHSS равнялся 5,7±1,2 (n=14), в контрольной группе — 5,4±1,2 (n=17); у пациентов с СИ — соответственно 1,1±4,5 (n=25) и 10,8±5,3 (n=29); у пациентов с ТИ — соответственно 19,3±2,16 (n=28) и 18±0,81 (n=10; рис. 1).
 Рис. 1. Средний балл по NIHSS при поступлении у пациентов с ЛИ, СИ и ТИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б)
Рис. 1. Средний балл по NIHSS при поступлении у пациентов с ЛИ, СИ и ТИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б)После внутривенной ТЛТ у пациентов с ЛИ в основной и контрольной группах выявлен почти полный регресс неврологического дефицита: балл по NIHSS снизился до 3,35±1,33 и 3,5±1,6 соответственно. Достоверных различий между группами не выявлено (рис. 2).
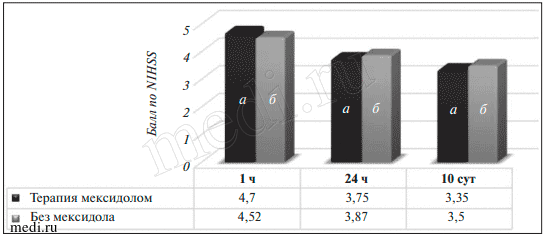 Рис. 2. Средний балл по NIHSS у пациентов с ЛИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТ
Рис. 2. Средний балл по NIHSS у пациентов с ЛИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТУ пациентов с СИ достоверных различий в регрессе неврологической симптоматики в 1-е сутки после проведения ТЛТ не выявлено: в основной группе среднее значение NIHSS через 24 ч составило 8±4,4 балла, а в контрольной группе — 8,17±5,7 балла. Однако на 10-е сутки после развития ИИ зафиксированы достоверные различия по этому показателю у пациентов основной и контрольной групп: 5,3±3,2 и 7±3,7 балла соответственно (р<0,05; рис. 3).
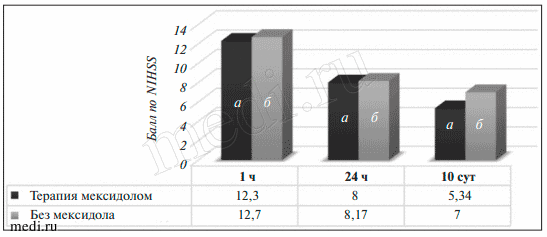 Рис. 3. Средний балл по NIHSS у пациентов с СИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТ
Рис. 3. Средний балл по NIHSS у пациентов с СИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТУ пациентов с ТИ зафиксированы достоверные различия в регрессе неврологического дефицита в основной и контрольной группах как через 24 ч, так и через 10 сут после начала заболевания. Среднее значение NIHSS через 24 ч в основной группе составило 14,2±5,47 балла, а в контрольной группе 16,8±8,9 балла (p<0,05). Спустя 10 сут после ТЛТ этот показатель в основной и контрольной группах достигал соответственно 11,5±6 и 14±6,7 балла (p<0,05; рис. 4).
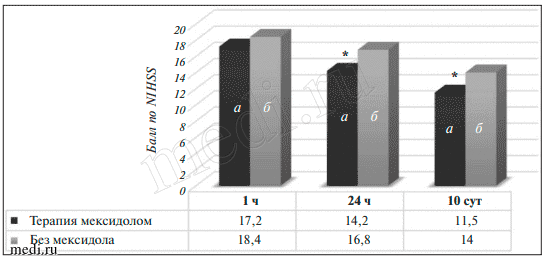 Рис. 4. Средний балл по NIHSS у пациентов с ТИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТ.
Рис. 4. Средний балл по NIHSS у пациентов с ТИ, получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и не использовавших такую терапию (б), через 1 ч, 24 ч и 10 сут после проведения внутривенной ТЛТ.* — достоверные различия показателей в группах (p<0,05)
По данным КТ, выполненной после ТЛТ у пациентов с ТИ и СИ, частота ранних геморрагических трансформаций в основной группе составила 7,5% (n=4), в группе сравнения — 17,9% (n=7; рис. 5).
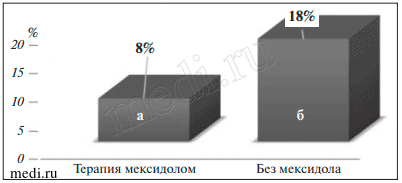 Рис. 5. Количество пациентов с осложнениями внутривенной ТЛТ в виде геморрагической трансформации среди получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и среди не использовавших такую терапию (б)
Рис. 5. Количество пациентов с осложнениями внутривенной ТЛТ в виде геморрагической трансформации среди получавших внутривенную терапию мексидолом на догоспитальном этапе (а) и среди не использовавших такую терапию (б)Обсуждение. Результаты нашего исследования показали эффективность и безопасность применения мексидола в период «терапевтического окна» при ИИ с последующей внутривенной ТЛТ. Выявлено также, что у пациентов, получавших этот препарат до ТЛТ, наблюдался больший регресс неврологического дефицита, а также меньшая частота развития геморрагических трансформаций в сравнении с больными, которым такое лечение не назначали.
В настоящее время опыт применения мексидола недостаточен для оценки его влияния на результаты внутривенной ТЛТ. Однако, по данным проведенного в нашей стране крупного рандомизированного двойного слепого мультицентрового плацебоконтролируемого исследования эффективности и безопасности мексидола при длительной последовательной терапии у 150 пациентов в остром и раннем восстановительном периодах полушарного ИИ, отмечен положительный эффект препарата в виде уменьшения выраженности неврологического дефицита в сравнении с плацебо [13].
Несомненно, эффективность Мексидола® при остром нарушении мозгового крообращения и последующей внутривенной ТЛТ требует дальнейшего изучения.
Заключение. Таким образом, применение мексидола на догоспитальном этапе с последующим проведением ТЛТ у пациентов с ИИ положительно влияет на динамику неврологического дефицита независимо от тяжести ИИ. Выявлены достоверные различия в степени регресса неврологического дефицита по NIHSS у пациентов с ТИ, которые получали и не получали мексидол на догоспитальном этапе, через 24 ч и 10 сут после поступления. В случаях применения мексидола до ТЛТ выявлен больший регресс неврологического дефицита. У пациентов с СИ отмечены аналогичные достоверные различия в степени регресса неврологического дефицита на 10-е сутки после развития ИИ. Установлена меньшая частота возникновения геморрагических трансформаций у пациентов, получавших мексидол на догоспитальном этапе, в сравнении с пациентами, которые его не применяли.
Полученные данные демонстрируют положительное влияние мексидола на эффективность и безопасность ТЛТ у пациентов с ИИ.
ЛИТЕРАТУРА
1. Дамулин ИВ, Парфенов ВА, Скоромец АА и др. Нарушения кровообращения в головном и спинном мозге. В кн.: Яхно НН, редактор. Болезни нервной системы. Руководство для врачей. Москва: Медицина; 2005. Том 1. С. 232—303. [Damulin IV, Parfenov VA, Skoromets AA, et al. Circulatory disorders in the brain and spinal cord. In: Yakhno NN, editor. Bolezni nervnoi sistemy. Rukovodstvo dlya vrachei. [Diseases of the nervous system. Guide for doctors] Moscow: Meditsina; 2005. Vol. 1. P. 232—303.]
2. Здравоохранение в России. Статистический сборник Федеральной службы государственной статистики (Росстат). Москва; 2007. [Healthcare in Russia. Statistical collection of the Federal state statistics service (Rosstat). Moscow; 2007.]
3. Суслина ЗА, Пирадов МА, редакторы. Инсульт: диагностика, лечение и профилактика. Москва: МЕДпресс-информ; 2008. 288 с. [Suslina ZA, Piradov MA, editors. Insult: diagnostika, lechenie i profilaktika [Stroke: diagnosis, treatment and prevention]. Moscow: MEDpress-inform; 2008. 288 p.]
4. Фейгин В, Виберс Д, Браун Р. Инсульт: клиническое руководство. Москва: Бином; 2005. 608 с. [Feigin V, Vibers D, Braun R. Insult: klinicheskoe rukovodstvo [Stoke: clinical guide]. Moscow: Binom; 2005. 608 p.]
5. European Stroke Organisation (ESO) Executive Committee; ESO Writing Committee. Guidelines for management of ischemic stroke and transient ischemic attack. Cerebrovasc Dis. 2008;25(5):457-507. doi: 10.1159/000131083. Epub 2008 May 6.
6. Гусев ЕИ, Скворцова ВИ. Нейропротективная терапия ишемического инсульта. Атмосфера. Нервные болезни. 2002;(1):3-7. [Gusev EI, Skvortsova VI. Neuroprotective therapy of ischemic stroke. Atmosfera. Nervnye bolezni. 2002;(1):3-7. (In Russ.)].
7. Gilligan AK, Thrift AG, Sturm JW, et al. Stroke units, tissue plasminogen activator, aspirin and neuroprotection: which stroke intervention could provide the greatest community benefit? Cerebrovasc Dis. 2005;20(4):239-44. Epub 2005 Aug 22.
8. Hacke W, Kaste M, Bluhmki E, et al. Trombolysis with alteplase 3 to 4,5 hours after acute ischemic stroke. N Engl J Med. 2008 Sep 25;359(13):1317-29. doi: 10.1056/NEJMoa 0804656.
9. Hand P, Kwan J, Lindley R, et al. Distinguishing between stroke and mimic at the bedside: The Brain Attack Study. Stroke. 2006 Mar;37(3):769-75. Epub 2006 Feb 16.
10. Libman RB, Wirkowski E, Alvir J, et al. Conditions that mimic stroke in the emergency department. Implications for acute stroke trials. Arch Neurol. 1995 Nov;52(11):1119-22.
11. Кулеш АА, Сыромятникова ЛИ, Голосова ЮА, Шестаков ВВ. Опыт проведения тромболитической терапии у больных с острыми нарушениями мозгового кровообращения: эффективность, безопасность, предикторы исхода и геморрагической трансформации. Журнал неврологии и психиатрии им. С.С. Корсакова. 2018;(7):18-24. [Kulesh AA, Syromyatnikova LI, Golosova YuA, Shestakov VV. Experience in thrombolytic therapy in patients with acute cerebral circulation disorders: efficacy, safety, predictors of outcome and hemorrhagic transformation. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2018;(7):18-24. (In Russ.)].
12. Эрлих АД, Грацианский НА. Изучение доказательной базы использования препаратов, содержащих этилметилгидроксипиридина сукцинат, у пациентов с инсультом и его последствиями. Реальная фармакотерапия в кардиологии. 2014;10(4):448-56. [Erlikh AD, Gratsianskii NA. Study of the evidence base of the use of drugs containing Ethylmethylhydroxypyridine succinate in patients with stroke and its consequences. Real'naya farmakoterapiya v kardiologii. 2014;10(4):448-56. (In Russ.)].
13. Стаховская ЛВ, Шамалов НА, Мельникова ЕВ и др. Результаты рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных группах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах полушарного ишемического инсульта (ЭПИКА). Журнал неврологии и психиатрии имени С.С.Корсакова. 2017;117(3):55-65. [Stakhovskaya LV, Shamalov NA, Mel'nikova EV, et al. The results of a randomized double-blind multicenter placebo-controlled parallel group study of the efficacy and safety of Mexidol in long-term sequential therapy in patients with acute and early recovery periods of hemispheric ischemic stroke (EPICA). Zhurnal nevrologii i psikhiatrii imeni S.S.Korsakova. 2017;117(3):55-65. (In Russ.)].
14. Куликов АЮ, Зинчук ИЮ. Фармакоэкономический анализ нейропротективных лекарственных средств в лечении острого нарушения мозгового кровообращения. Фармакоэкономика. 2013;6(3):17-21. [Kulikov AYu, Zinchuk IYu. Pharmacoeconomical analysis of neuroprotective drugs in the treatment of acute cerebral circulation disorders. Farmakoekonomika. 2013;6(3):17-21. (In Russ.)].
15. Маринич ЛИ, Степанюк ГИ, Черноиван НГ, Воскобойник АЮ. Влияние соединения мт-279 и мексидола на течение метаболических процессов при экспериментальной ишемии головного мозга. Тихоокеанский медицинский журнал. 2013;(2):21-4. [Marinich LI, Stepanyuk GI, Chernoivan NG, Voskoboinik AYu. Effect of MT-279 and Mexidol on metabolic processes in experimental cerebral ischemia. Tikhookeanskii meditsinskii zhurnal. 2013;(2):21-4. (In Russ.)].
16. Китаева ЭА, Сайхунов МВ, Хафизьянова РХ, Хасанова ДР. Нейропротективная терапия у больных с полушарным ишемическим инсультом. Казанский медицинский журнал. 2009;90(5):671-5. [Kitaeva EA, Saikhunov MV, Khafiz'yanova RKh, Khasanova DR. Neuroprotective therapy in patients with hemispheric ischemic stroke. Kazanskii meditsinskii zhurnal. 2009;90(5):671-5. (In Russ.)].
17. Киселева ОС, Фархутдинов РР. Исследование влияния препаратов, используемых в терапии ишемического инсульта, на генерацию активных форм кислорода и процессы перекисного окисления липидов в модельных системах. Медицинский вестник Башкортостана. 2011;6(3):124-6. [Kiseleva OS, Farkhutdinov RR. Study of the influence of drugs used in the treatment of ischemic stroke on the generation of reactive oxygen species and lipid peroxidation processes in model systems. Meditsinskii vestnik Bashkortastana. 2011;6(3): 124-6. (In Russ.)].
18. Солнцева ГА. Опыт применения препарата «Мексидол» выездными бригадами станции скорой медицинской помощи Великого Новгорода. Бюллетень экспериментальной биологии и медицины. 2005;(Прил 1): 201-4. [Solntseva GA. Opyt primeneniya preparata Meksidol vyezdnymi brigadami stantsii skoroi meditsinskoi pomoshchi Velikogo Novgoroda. Experience in the use of the drug Mexidol visiting teams ambulance station of Veliky Novgorod. Byulleten' eksperemental’noi biologii i meditsiny. 2005;(Suppl 1):201-4. (In Russ.)].
