Динамика изменений оксидативного стресса у пациентов с панкреонекрозом при лечении антиоксидантами
СтатьиСтолярчук А.В.
Украина, Винницкий национальный медицинский университет
Вступление
Острый панкреатит это полиэтиологическое и многофакторное заболевание, в патогенезе которого характерно попадание пищевых ферментов поджелудочной железы в ее интерстицию и в большой круг кровообращения, с увеличением продукции цитокинов, которые вызывают патологические местные и системные эффекты. Известно, что провоспалительные цитокины такие как IL-1p, TNF-a i IL-6 виступають в качестве посредников местных и системных воспалительных реакций острого панкреатита [Шалимов и др. 2006]. Активированные макрофаги выделяют IL-1p i TNF-a в ответ на местное повреждение тканей. Эти цитокины действуют локально, ухудшая течение острого панкреатита, и системно вместе с IL-6 увеличивая проницаемость капилляров, вызывает «капиллярную утечку», способствует адгезии и екстравазации лейкоцитов, что может перерасти в полиорганную недостаточность [Свиридов и др. 2005, Брискин 2005].
Оксидативный стресс следует рассматривать как основной фактор патогенеза при остром панкреатите. При остром панкреатите происходит повышение уровня липидной пероксидазы в желчи или ткани поджелудочной железы и низком уровней антиоксидантных витаминов в крови. Церулеин стимулирует большое количество активных форм кислорода (АФК) активирует окислительно-чувствительный фактора ядерного транскрипции NF-kB и, таким образом, индуцирует экспрессию цитокинов в свежевыделенных ацинарных клетках поджелудочной железы без воспалительных клеток in vitro.
Известно, что мексидол является производным 3 - оксипиридина, он регулирует функционально - метаболическую активность клеток и имеет широкий спектр воздействия, так он проявляет антиоксидантный, антигипоксический, мембранопротективний эффекты, подавляет ПОЛ, повышает активность супероксиддисмутазы и косвенно обладает противовоспалительным действием [Климов и др. 2007].
В условиях лавинообразного роста количества активных форм кислорода, повышения количества цитокинов, прямого и опосредованного повреждения клеточных структур, нарастание гипоксии становится критическим и катастрофическим для клеток поджелудочной железы. С другой стороны перечисленные эффекты мексидола являются спасательным кругом для энергетической системы клеток, а особенно свойство мексидола, обусловленное сукцинатом, одним из его компонентов, который способен на ранних стадиях гипоксии, в условиях недостатка кислорода, использоваться в качестве энергетического субстрата для дыхательной цепи, восстанавливая синтез и накопление АТФ в митохондриях, что положительно влияет на энергетический обмен и увеличивает степень енергизации клетки [Климов и др. 2007, Кузнецов и др. 2005].
Антиоксидантный эффект аскорбата проявляется при достаточном количестве других антиоксидантов, таких как а - токоферол и глутатион. Глутатион восстанавливает дегидроаскорбиновую кислоту прямым и неферментативным путем аскорбиновой кислоты. Эта реакция является одним из основных механизмов антиоксидантной системы, которая выглядит как восстановительные циклы - глутатион / глутатиондисульфид и аскорбиновая / дегидроаскорбиновая кислота. Также в организме при участии витамина С проходит регенерация а - токоферола с токофероксильного радикала [Павлинский 2004].
Цель исследования - исследовать изменения оксидативного стресса у больных панкреонекрозом хирургического отделения на протяжении лечения в сочетании с различными антиоксидантами и без них.
Материалы и методы
В исследование были включены 25 больных, среди которых 16 мужчин и 9 женщин в возрасте от 22 до 75 лет. Все больные поступали в отделение абдоминальной хирургии Винницкой областной клинической больницы им.Н.И. Пирогова в течение 2009-2011 годов. Диагноз устанавливался на основании клинических данных, результатов общелабораторных исследований, амилазурии, эндоскопических методов исследования желудка и двенадцатиперстной кишки, УЗИ и рентгенологических методов исследования органов брюшной полости, а в отдельных случаях лапароскопии. Больным проводилось соответствующее лечение, включавшее голод, декомпрессию желудка, спазмолитические и обезболивающие средства, ингибиторы протеаз, блокаторы секреции поджелудочной железы, пробиотики, инфузионную и дезинтоксикационную терапию с учетом диуреза, антибактериальную и симптоматическую терапию.
В зависимости от назначаемых антиоксидантов больные были разделены на группы: в первой группе 9 больных, которых лечили стандартизированными методиками в сочетании с мексидолом, во второй 8 больных - в сочетании с аскорбиновой кислотой, и контрольная группа составила 8 больных, где применялось только стандартизированное лечение без применения антиоксидантов. Назначение антиоксидантов проводилось по следующей схеме: мексидол применяли в дозе 200 мг 3 р/д последующим уменьшением суточной дозы для постепенной отмены препарата, аскорбиновая кислота вводилась внутривенно струйно на физиологическом растворе натрия хлорида в течение 2 - 3 мин. в дозе 200 мг 2 р / д. Также проводился забор крови для проведения лабораторных исследований оксидативного стресса - глутатионпероксидазы (ГП ), глутатионредуктазы (ГР ) и супероксиддисмутазы (СОД ).
Результаты. Обсуждение
Исследовано 25 больных, лечившихся в отделении абдоминальной хирургии ВОКБ им. Н.И. Пирогова.
В таблице 1 описана динамика изменений показателя ГП на протяжении лечения по группам. При поступлении показатель почти не отличался в группах и составил 28,09 ± 1,38, 26,64 ± 1,18 и 27,40 ± 1,42 мкмоль НАДФН2 ч / мг белка для группы мексидола, аскорбиновой кислоты и контроля соответственно. В дальнейшем, во время лечения на 3-6 день показатель начал снижаться и динамика изменений была разная по группам - самым низким показатель был в группе мексидола и составил 12,53 ± 0,40, низким оказался для группы аскорбиновой кислоты - 15,65 ± 0,49 и незначительно изменился в группе контроля - 22,22 ± 1,39. А на 8-12 день лечения тенденция в изменениях сохранилась, и наибольшего снижения ГП получил в группе мексидол и составил 9,42 ± 0,55, сравнительно большим оказался для группы аскорбиновой кислоты - 11,58 ± 0,83 и наибольшим был в контрольной группе - 17,16 ± 1,18.
Таблица 1.
Динамика показателя ГП у больных с панкреонекрозом на протяжении лечения (мкмоль НАДФН2 ч / мг белка)
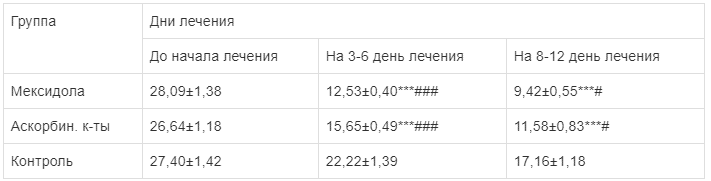 Примечание. * - вероятное отличие, по контролю, при этом: *** - p≤0,01, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1, ### - p≤0,01.
Примечание. * - вероятное отличие, по контролю, при этом: *** - p≤0,01, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1, ### - p≤0,01.
В таблице 2 описана динамика показателя ГР у больных на протяжении лечения по группам. При поступлении показатель почти не отличался в группах и составил для группы мексидол 8,16 ± 0,34 мкмоль НАДФН2 ч / мг белка, для группы аскорбиновой кислоты - 8,69 ± 0,46, а для контроля -8,91 ± 0,34. Во время лечения на 3 - 6 день показатель наиболее снизился в группе мексидола и составил 6,91 ± 0,35, несколько меньше снизился в группе аскорбиновой кислоты - 7,70 ± 0,35, и почти не изменился для группы контроля - 8,34 ± 0,37. На 8-12 день лечения показатель снизился в группе мексидол и составил 5,71 ± 0,50, а в группе аскорбиновой кислоты и контрольной изменился незначительно и составил 7,31 ± 0,51 и 7,26 ± 0,37 соответственно.
Таблица 2.
Динамика показателя ГР у больных с панкреонекрозом на протяжении лечения (мкмоль НАДФН2 ч/мг белка)
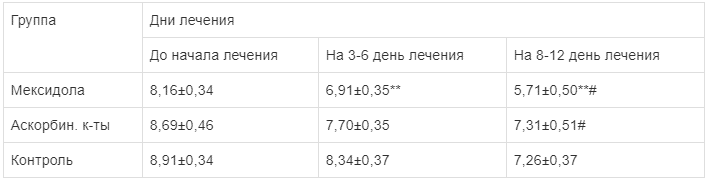 Примечание. * - вероятное отличие, по контролю, при этом: ** - p≤0,05, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1
Примечание. * - вероятное отличие, по контролю, при этом: ** - p≤0,05, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1 В таблице 3 описана динамика СОД у больных во время лечения по группам. При поступлении показатель составил 31,27 ± 2,64 торм\окисл\кврцт для группы мексидола, 30,30 ± 3,11 - для группы аскорбиновой кислоты и 29,97 ± 3,12 - для контрольной группы, и почти не отличалось друг от друга. На 3-6 день лечения уровень СОД увеличился в группе мексидола до 38,48 ± 3,51, а в группах аскорбиновой кислоты и контрольной наоборот снизился до 28,78 ± 3,05 и 25,71 ± 3,74 соответственно. На 8-12 день лечения в группе мексидола продолжалось рост и составил 49,63 ± 2,73, что выше по сравнению с другими группами, а в группах аскорбиновой кислоты и контрольной показатель тоже наблюдался рост до 41,22 ± 3,11 и 38,39 ± 3,37 соответственно.
Таблица 3.
Динамика показателя СОД у больных с панкреонекрозом во время лечения (торм\окисл\кврцт).
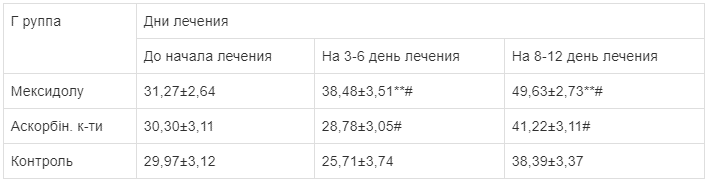 Примечание. * - вероятное отличие, по контролю, при этом: ** - p≤0,05, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1
Примечание. * - вероятное отличие, по контролю, при этом: ** - p≤0,05, # - вероятное отличие, по аскорбиновой кислоте, при этом: # - p≤0,1 Исследование лабораторных показателей оксидативного стресса глутатионпероксидазы и глутатионредуктазы и супероксиддисмутазы показало в динамике, что наиболее эффективной для торможения ПОЛ -оксидативного стресса, оказалась комбинация традиционного лечения с мексидолом, а при комбинации традиционного лечения с аскорбиновой кислотой эффективность торможения ПОЛ - оксидативного стресса была несколько ниже, хотя положительно отличался от контрольной группы.
Данные изменения характерны для панкреонекроза и описаны во многих работах [Климов и др. 2007, Кузнецов и др. 2005].
Мексидол благодаря непосредственному связыванию со свободными радикалами кислорода и элиминированию ионов железа, имеет влияния на активность супероксиддисмутазы, каталазы, ферментов системы глутатиона, повышает концентрацию восстановленной формы глутатиона, содержание биогенных аминов и влияет на энергетический обмен клеток. Его прямая мембраностабилизирующее действие проявляется реакцией с гидроксильными радикалами пептидов и белков, и он способен восстанавливать ультраструктурные изменения в клетках, при этом считается, что одной из основных мишеней для действия препарата выступают митохондрии, что и является компонентом антигипоксического влияния мексидола.
Таким образом, у больных с некротическим панкреатитом мексидол за счет данных механизмов тормозит оксидативный стресс снижая его показатели такие как, глутатион пероксидаза, глутатион рудуктаза и повышая супероксиддисмутазу.
Использование аскорбиновой кислоты компенсировало ее низкую плазматическую концентрацию, предупреждало нарушения тканевого дыхания по типу анаэробного гликолиза с накоплением недоокисленных продуктов обмена, которые обладают токсичными свойствами, а также способствовала усилению перекисного окисления липидов и цикла арахидоновой кислоты, предупреждала нарушения детоксикационной функции печени, снижение клеточного и гуморального иммунного ответа, и фагоцитарной активности нейтрофилов.
Выводы и перспективы дальнейших разработок
1. У больных с панкреонекрозом происходят значительные изменения показателей оксидативного стресса за счет глутатионпероксидазы, глутатионредуктазы и супероксиддисмутазы.
2. Быстрое увеличение на момент поступления и постепенное снижение во время лечения GSH peroxidase и GSH reductase, а также постепенное нарастание супероксиддисмутазы было характерно для больных с панкреонекрозом.
3. Применение антиоксидантов в сочетании со стандартизованным лечением дает положительный эффект в торможении оксидативного стресса по сравнению с группой без антиоксидантов.
4. Мексидол имеет преимущества по сравнению с аскорбиновой кислотой и эффективней подавляет оксидативный стресс и приводит к уменьшению показателей: так, глутатион пероксидаза от показателей при поступления снизилась в 2,98 раз при применении мексидола по сравнению с аскорбиновой кислотой - в 2,3 раза и группы контроля - в 1,59 раз на 8-12 день лечения, глутатион редуктаза снизилась при применении мексидола в 1,42 раза по сравнению с группой аскорбиновой кислоты - в 1,18 раза и в группе контроля в 1,23 раза на 8-12 день лечения. Рост супероксиддисмутазы в группе мексидола составило 1,58 раз, в группе аскорбиновой кислоты в 1,36 раз, а в контрольной группе в 1,28 раз на 8-12 дни лечения в сравнении с начальными показателями.
Список литературы:
1. Антиоксидантная и магнито-лазерная терапия в комплексном лечении больных панкреонекрозом /А.Е.Климов, А.Ю.Корольков, А.В.Рыков [и др.]//Российский медицинский журнал. - 2007. - №5. - С. 18-20
2. Брискин Б.С. Профилактика и лечение гнойно-некротических осложнений панкреонекроза /Б.С. Брискин // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2005. - Том15, №1. - С. 50-58
3. Значение продленной эпидуральной аналгезии местными анестетиками в комплексной терапии тяжелого острого панкреатита и панкреонекроза /С.В.Свиридов, А.М.Овечкин, Н.М.Федоровский [и др.] // Клиническая фармакология и терапия. - 2005. - №1. - С. 46-51
4. Кузнецов Н.А. Результаты применения синтетических антиоксидантов в лечении больных деструктивным панкреатитом /Н.А.Кузнецов, Г.В.Родоман, A.Т.Бронтвейн //Хирургия. Журнал имени Н.И. Пирогова. - 2005. - №3. - С. 36-39
5. Лiсничук Н.Є . Стан глутатioновоi ланки антиоксидантноi системи в умовах крiогенного панкреатиту рiзноi тривалостi /Н.Є .Лiсничук, I.Я.Демкiв, М.I.Кулiцька //Украiнський бiохiмiчний журнал: науково-теоретичний журнал. - 2011. - №4. -С .146
6. Павлинский С.Л. Роль антиоксидантов в лечении и профилактике заболеваний человека /С. Л.Павлинский // Российский семейный врач. - 2004. - Том8, №2. - С. 65-73
7. Хомерики С.Г. Фамотидин против окислительного стресса при некоторых заболеваниях пищеварительной системы /С.Г.Хомерики, Н.М.Хомерики, B. Г.Сафронов //Сучасна гастроентерологiя. - 2004. - №5. - С. 89-94
8. Чорномидз А.В. Роль вiльних радикалiв у прогресуваннi перебiгу гострого панкреатиту /А.В.Чорномидз //Украинский журнал хирургии. - 2013. - №1. С. 3843
9. Шалимов А. А. Современные тенденции в диагностике и лечении острого деструктивного панкреатита /А.А.Шалимов, М.Е.Ничитайло, А.Н.Литвиненко //Клiнiчна хiрургiя. - 2006. - №6. - С. 12-20
10. Early ascorbic acid depletion is related to the severity of acute pancreatitis /M.J.Bonham, F.M.Abu-Zidan, M.O.Simovic [et al.] //Br. J. Surg. - 1999. - Vol.86, №10. - Р. 1296-1301
11. Lee V.T. Infected pancreatic necrosis - an evaluation of the timing and technique of necrosectomy in a Southeast Asian population /V.T.Lee, A.Y.Chung, P.K.Chow [et al.] //Ann. Acad. Med. Singapore. - 2006. - №8. - Р. 523-530
