Патогенетическое обоснование включения таурина в лечение пациентов с сахарным диабетом типа 2
Статьи
Опубликовано в журнале:
« CONSILIUM MEDICUM » ТОМ 19 №4, 2017
М.Е.Стаценко, С.В.Туркина, И.А.Тыщенко, Е.Е.Горбачева
ФГБОУ ВО «Волгоградский государственный медицинский университет» Минздрава России. 400131, Россия, Волгоград, пл. Павших Борцов, д. 1
Обзор посвящен обоснованности применения препарата таурин у больных сахарным диабетом типа 2. Приведены данные многочисленных экспериментальных и клинических исследований, продемонстрировавших положительное влияние таурина как на течение сахарного диабета типа 2, так и на коморбидную патологию (заболевания сердца, почек).
Ключевые слова: сахарный диабет типа 2, таурин, хроническая сердечная недостаточность, липидный обмен, углеводный обмен, инсулинорезистентность.
Для цитирования: Стаценко М.Е., Туркина С.В., Тыщенко И.А., Горбачева Е.Е. Патогенетическое обоснование включения таурина в лечение пациентов с сахарным диабетом типа 2. Consilium Medicum. 2017; 19 (4):
Pathogenetic substantiation inclusion of taurine in the treatment of patients with diabetes mellitus type 2
M.E.Statsenko, S.V.Turkina, I.A.Tyshchenko, E.E.Gorbacheva
Volgograd State Medical University of Ministry of Health of the Russian Federation. 400131, Russian Federation, Volgograd, pl. Pavshikh Bortsov, d.1
The review is devoted to the validity of taurine in patients with diabetes mellitus type 2. The data of numerous experimental and clinical studies have shown the positive effect of taurine on both the course of diabetes mellitus type 2 and on the comorbid pathology (heart disease, kidney disease).
Key words: diabetes mellitus type 2, taurine, chronic heart failure, lipid metabolism, carbohydrate metabolism, insulin resistance.
For citation: Statsenko M.E., Turkina S.V., Tyshchenko I.A., Gorbacheva E. Pathogenetic substantiation inclusion of taurine in the treatment of patients with diabetes mellitus type 2. Consilium Medicum. 2017; 19 (4):
В настоящее время препараты, влияющие на обменные процессы на клеточном уровне, назначаются врачами общей практики, эндокринологами, кардиологами, невропатологами, что не случайно и связано с попыткой воздействовать на патогенетические механизмы возникновения нарушений функционирования разных органов в рамках их метаболического ремоделирования, возникающего при различных заболеваниях [1-3].
Одним из таких лекарственных средств является аминокислота таурин, которая играет важную роль в организме. Основными биологическими свойствами этой условно незаменимой аминокислоты являются: нейромодуляция (агонист g-аминомасляной кислоты и глицина); стабилизация нейрональных и синаптических мембран; влияние на распределение вне- и внутриклеточных потоков ионов кальция; осморегуляция; участие в конъюгации желчных кислот; конъюгация ретиноидов и ксенобиотиков; антиоксидантное и противовоспалительное действие [4]. Кроме того, таурин оказывает ингибирующее действие по отношению к ангиотензину (АТ) II [5], демонстрирует инсулиноподобный эффект, который опосредуется через взаимодействие с рецептором к инсулину при его конкурентном связывании с субъединицей рецептора инсулина с молекулярной массой 138 000 Да [6]. Предполагают, что тауринзависимое снижение уровня глюкозы в крови у больных сахарным диабетом (СД) типа 2 может быть связано с протективным действием таурина на b-клетки. E.Carneiro (2009 г.) и соавт. в рандомизированном плацебо-контролируемом исследовании показали, что 30-дневная диета здоровых мышей, обогащенная таурином, сопровождается, во-первых, регулирующим действием на гены, ответственные за глюкозостимулированную секрецию инсулина. В этом исследовании установлено, что островки Лангерганса у мышей, которые получали таурин, содержали большое количество инсулина; активно отвечали на глюкозостимулированную секрецию инсулина; повышалось содержание ионов Са2+ в митохондриях, экспрессия генов к инсулину, рецептору сульфомочевины-1, глюкокиназы, Glut-2, проконвертазе и PDX-1. Во-вторых, отмечена достоверно более высокая тирозинкиназная активность инсулиновых рецепторов на уровне скелетной мускулатуры как при базальной секреции, так и инсулиностимулированном ответе [7].
К настоящему времени накоплен значительный экспериментальный и клинический опыт, свидетельствующий о роли таурина в регуляции не только уровня глюкозы, но и его положительном влиянии на выраженность инсулино-резистентности и других нарушений обмена. В работе C.Xiao и соавт. (2008 г.) в ходе клинического исследования у пациентов без диабета, но имеющих ожирение или избыточную массу тела, перорально вводимый таурин снижал выраженность инсулинорезистентности и улучшал липидиндуцированную функциональную декомпенсацию функционирующих b-клеток за счет уменьшения оксидативного стресса [8].
Была обнаружена эффективность таурина, поступающего с продуктами питания, в отношении предотвращения гиперхолестеринемии и отложения жировых депо в мезентериальных артериях у крыс линии SHRSP на фоне диеты с высоким содержанием жира и холестерина (ХС). Согласно экспериментальным данным благоприятные эффекты таурина в отношении гиперхолестеринемии и отложения жировых депо в артериях таурина обусловлены усилением продукции желчных кислот и активацией 7α -гидроксилазы - фермента, регулирующего процесс метаболизации ХС и синтеза желчных кислот. Активация этого фермента, в свою очередь, обусловлена усилением экспрессии гена ХС-7α-гидроксилазы [9]. Снижению уровня ХС на фоне богатой таурином диеты соответствует усиление экспрессии этого гена. Кроме того, известно, что прием таурина эффективно повышает содержание рецепторов липопротеидов низкой плотности (ЛПНП) в печеночной ткани, что подтверждается ускорением распада I-125-меченых ЛПНП. Таким образом, гипохолестеринемическое действие таурина может быть обусловлено увеличением содержания рецепторов ЛПНП, ускорением метаболизации ХС в желчные кислоты, а также снижением активности кишечной ацил-КоА-холестерин-ацилтрансферазы [10]. В одном из последних обзоров, посвященных метаболической роли таурина в формировании метаболического синдрома (МС), обсуждаются и другие молекулярные механизмы, опосредующие его влияние на выраженность ожирения, дислипидемию, ренин-ангиотензин-альдостероновую (РААС) и почечную калликреинкининовую систему, ингибирование активности симпатической активности, вазодилатирующие свойства таурина. Предотвращение развития дефицита таурина рассматривается как мера профилактики развития МС [11].
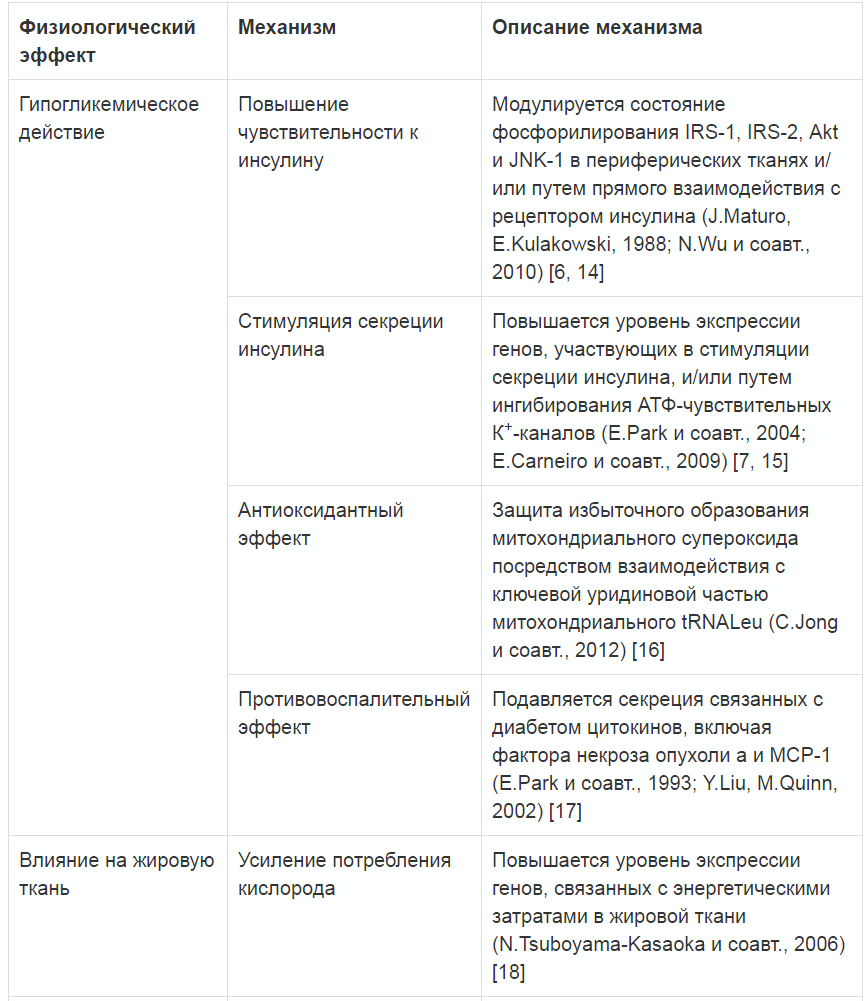
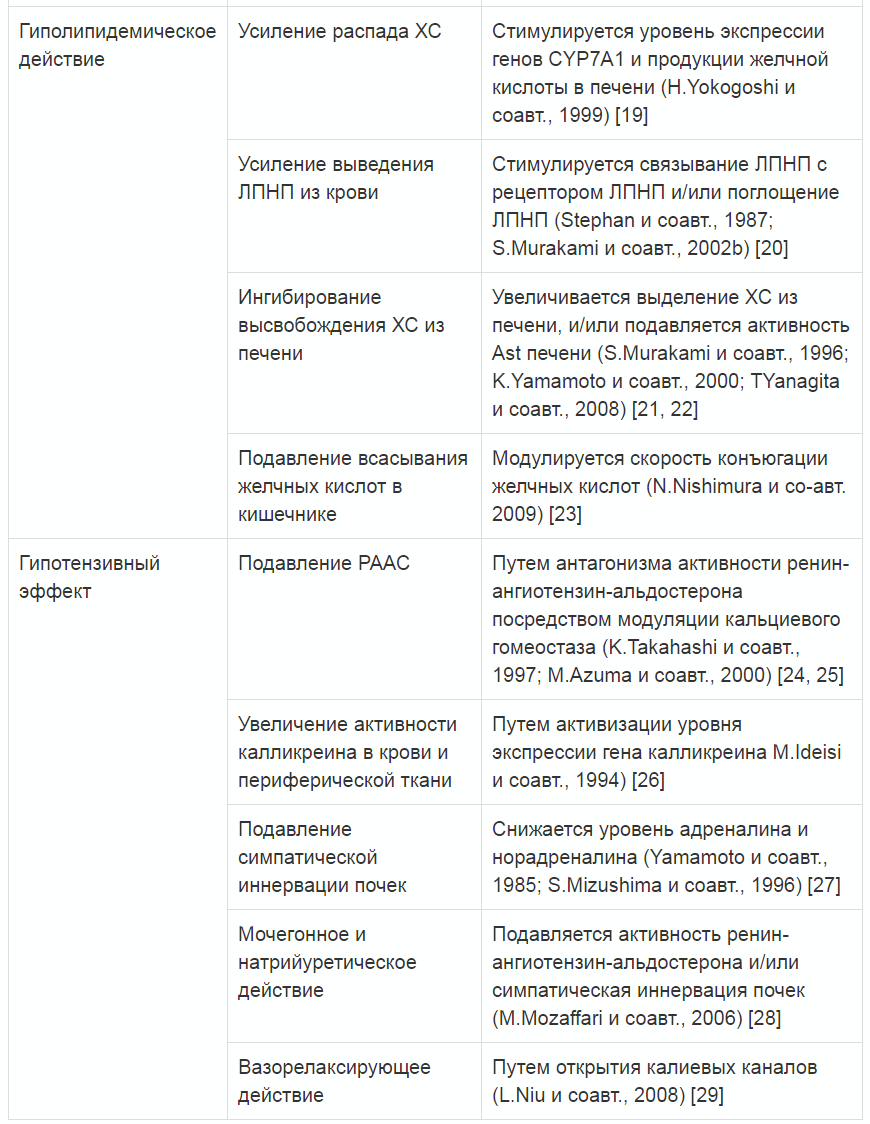
Отмеченные к настоящему времени физиологические эффекты таурина рассматриваются как потенциально клинически важные при его назначении больным СД. По мнению C. De la Puerta (2010 г.) и соавт. [12], как минимум четыре физиологических механизма влияния таурина определяют эффективность последнего при СД и его осложнениях: возможность влиять на выработку инсулина, чувствительность к нему, антиоксидантный и противовоспалительный потенциал, осморегулирующая активность. Суммарные положительные эффекты таурина у пациентов с ожирением, МС и СД представлены в табл. 1 [13].
Практически все эффекты таурина, отмеченные в экспериментальных моделях СД, получили подтверждение в клинических исследованиях, проведенных прежде всего в России, что связано с возможностью использования лекарственного препарата на основе таурина (Дибикор 250 и 500 мг, ПИК-ФАРМА). В исследованиях принимали участие пациенты с СД типа 1 и 2 обоих полов в возрасте от 18 до 65 лет. Препарат таурина применяли в суточной дозе 1 г перорально (0,5 г 2 раза в день) в сочетании с другими сахароснижающими средствами (инсулином или пероральными сахароснижающими препаратами - ПССП), а также в качестве монотерапии у пациентов с впервые выявленным СД типа 2. Длительность лечения составила от 1 до 6 мес. Таурин с высокой достоверностью снижал как тощаковую, так и постпрандиальную гипергликемию, а также уровень гликированного гемоглобина (НЬА1с). По данным А.С.Аметова (2007 г.), по результатам пяти медицинских центров через 3 мес лечения препаратом Дибикор уровень сахара крови натощак снизился на 1,0 ммоль/л, через 2 ч после еды ~ на 2 ммоль/л, НЬА1с - на 0,9% [30]. У пациентов, получающих инсулин, на фоне компенсации углеводного обмена при добавлении таурина отмечалось снижение потребности в инсулине на 2-17 ЕД/сут. Продемонстрирована возможность снижения НЬА1с более чем на 1%, что, безусловно, помогает снизить риск осложнений СД типа 2 [31]. У пациентов с СД типа 2 снижение гликемии и НЬА1с под влиянием таурина сочеталось с уменьшением инсулинорезистентности по индексу НОМА, причем, чем выше были исходные нарушения, тем отчетливее была положительная динамика.
Интерес представляют и исследования В.И.Петрова и В.В.Наумова (2014 г.) [32], которые показали, что гипогликемизирующий эффект у пациентов с СД типа 2 отмечается уже к 1-му часу от момента приема препарата таурина Дибикор в дозе 1 г, нарастая к 4 и 6-му часу от момента приема, не «проигрывая» при этом гипогликемизирующему эффекту глибенкламида в дозе 1,75 мг. Эпизодов гипогликемии зафиксировано не было. Терапия глибенкламидом чревата своими нежелательными эффектами на печень, почки и ß-клетки поджелудочной железы. Таурин уменьшал токсические проявления глибенкламида (повышение в крови креатинина и микроальбуминурию), что может быть связано с эффектами таурина на АТФ-зависимые К+-каналы. В эксперименте показано, что таурин ингибирует мышечные АТФ К+-каналы, взаимодействуя с местами связывания глибенкламида на рецепторах к сульфомочевине, или аллостерически меняет места связывания с рецептором. Во время ишемии и гипоксии скелетные и сердечные мышцы претерпевают ряд изменений, например активацию АТФ К+-каналов, и теряют внутриклеточный таурин. Истощение таурина во время ишемии будет способствовать ранней активации АТФ К+-каналов и падению внутриклеточного уровня АТФ [33].
Лечение таурином пациентов с СД типа 2 наряду с благоприятным влиянием на углеводный обмен приводило к улучшению показателей липидного обмена: достоверно снижался уровень общего ХС, триглицеридов (ТГ) и повышался показатель ХС липопротеидов высокой плотности (ЛПВП), наблюдалась тенденция к снижению ХС ЛПНП. Так, в исследованиях Г.И.Нечаевой и соавт. (2011 г.) [34], М.Е.Стаценко и соавт. (2014, 2015 г.) [35, 36] показано, что добавление препарата Дибикор в комплексную терапию СД типа 2 и хронической сердечной недостаточностью (ХСН) способствует более эффективному снижению общего ХС (ОХС), ТГ, более эффективному повышению ЛПВП.
Таблица 1. Суммарные положительные эффекты таурина у пациентов с ожирением, МС и СД
Таурин представляет 50% всех свободных аминокислот в сердце. Показано (по данным экспериментального исследования), что недостаточное поступление его может сопровождаться уменьшением толщины стенки левого желудочка (ЛЖ) и его сухого веса, площади поперечного сечения миоцитов, изменять толщину задней стенки ЛЖ и геометрию желудочков. Отмечено формирование диастолической и систолической дисфункции ЛЖ. Кроме того, у таурин-дефицитных моделей активизировались процессы окислительного повреждения клеток [37]. В исследовании I.Takashi и соавт. (2014 г.) показано, что мыши с дефицитом таурина (TauTKO) демонстрируют формирование структурных дефектов и непереносимость физических упражнений, что связанно с нарушениями энергетического обмена, опосредованными дефицитом таурина [38]. Доказано, что диабетическая кардиомиопатия, гипертрофия миокарда и миокардиодистодистрофия развиваются под влиянием АТ II и реализуются через увеличение экспрессии 2-го типа рецепторов к АТ на кардиомиоцитах и ускорение апоптоза. Таурин в эксперименте, уменьшая количества АТ2-рецепторов, предотвращает апоптоз кардио-миоцитов и защищает сердце от развития гипертрофии и миокардиодистрофии [39] Предполагаемое на основании экспериментальных исследований позитивное влияние таурина на деятельность сердца (модуляция активности транспортеров кальция и чувствительности кардио-миоцитов к кальцию; участие в клеточной осморегуляции, непрямая регуляция внутриклеточных окислительных процессов - механизм неизвестен, стабилизация клеточных мембран - прямое взаимодействие с фосфолипидами, модуляция активности протеинкиназ и фосфатаз кардио-миоцитов) [40] получило свое подтверждение при оценке его клинических эффектов у пациентов с ХСН и СД. Применение таурина на фоне приема сахароснижающих, гиполипидемических, гипотензивных препаратов, соблюдение рекомендаций, касающихся образа жизни (диета, физическая активность) у пациентов с СД типа 2, способствовали улучшению процесса реполяризации миокарда и диастолической функции (ДФ) ЛЖ, уменьшению числа пациентов с ДД, достоверному позитивному влиянию на показатели качества жизни больных при хорошей переносимости препарата [34]. Кроме того, по данным исследований, проведенных М.Е.Стаценко и соавт. (2014 г.), включение таурина в состав базисной терапии ХСН и СД типа 2 достоверно увеличивает толерантность к физическим нагрузкам и уменьшает функциональный класс ХСН, способствует снижению уровня Nt-proBNP и значимо увеличивает фракцию выброса ЛЖ у пациентов, перенесших инфаркт миокарда [35]. Кроме того, установлено вегетонормализующее действие его на синдром кардиальной симпатической дисрегуляции по данным оценки вариабельности ритма сердца. Отмеченные вегетонормализующие эффекты могут сопровождаться антиаритмическим эффектом таурина и возможностью достоверного снижения фатальных аритмий, которые продемонстрированы у пациентов с ХСН II—III функционального класса NYHA, обусловленной постинфарктным кардиосклерозом [41].
Эндотелиальная дисфункция является одним из важных механизмов формирования как микро-, так и макрососудистых осложнений при СД. По данным экспериментальных исследований включение таурина в пищевой режим положительно влияет на выраженность эндотелийзависимой релаксации сосудов при стрептозоцининдуцированном СД у крыс [42, 43]. В основе протективного действия таурина при дисфункции эндотелия при СД лежит целый ряд молекулярных механизмов. Так, таурин увеличивает биодоступность оксида азота, подавляет активность молекул адгезии сосудистого эндотелия 1 типа (VCAM-1) и молекул межклеточной адгезии 1 типа (ICAM-1), индуцированных высоким содержанием глюкозы в культивируемых эндотелиальных клетках [43]. В условиях хронической гипергликемиии в эксперименте таурин предотвращает индукцию экспрессии ICAM-1 и рецепторов LOX-1, отвечающих за включение окисленного ЛПНП в клетки аорты [42]. Клиническое изучение эндотелиотропных свойств таурина у пациентов с СД типа 2 и ХСН, проведенное М.Е.Стаценко и соавт. (2016 г.) [44], выявило, что на фоне приема таурина статистически значимо увеличивался уровень оксида азота в крови с одновременным снижением секреции эндотелина-1. Показано, что положительные эндотелио-протекторные свойства таурина в составе комбинированной терапии сопровождались достоверным уменьшением тяжести ХСН по данным оценки уровня Nt-proBNP.
Впервые в исследовании, проведенном М.Е.Стаценко и соавт. (2013 г.) [45], продемонстрированы вазопротективные эффекты таурина при его использовании в составе комбинированной терапии пациентов с ХСН и СД типа 2. Большинство больных с ХСН и СД типа 2, включенных в исследование, имели патологические гиперемический (43%) и спастический тип микроциркуляции (27%). Шестнадцатинедельный прием таурина в дополнение к базисной терапии ХСН и СД типа 2 статистически значимо сопровождался уменьшением числа больных со спастическим гемодинамическим типом микроциркуляции (ГТМ) на 17%, при этом возросло число пациентов с нормоциркуляторным ГТМ. При исследовании параметров жесткости магистральных артерий отмечены положительное влияние препарата на показатели скорости распространения пульсовой волны, снижение индекса артериальной жесткости и достоверное снижение числа парадоксальных проб при проведении пробы с реактивной гиперемией. Вазопротективные свойства таурина также отмечены в работах иностранных авторов, где установлена способность таурина снижать жесткость магистральных сосудов [46, 47] и улучшать эндотелиальную функцию [48].
СД типа 2 как эквивалент сердечно-сосудистого заболевания часто сочетается с артериальной гипертензией (АГ) которая вносит весомый вклад в кардиальный прогноз пациента и прогрессирование диабетической нефропатии. Выше обсуждались возможные механизмы гипотензивного действия препарата (см. табл. 1). В клинических исследованиях показано, что таурин (Дибикор) повышает эффективность гипотензивной терапии у больных СД типа 2. В исследовании, проведенном А.С.Адамчик и И.В.Крючковой (2009 г.), было показано, что использование препарата Дибикор способствует более эффективному снижению как систолического, так и диастолического артериального давления (АД) у пациентов, получающих регулярную гипотензивную терапию эналаприлом и индапамидом [49]. Авторы исследования отмечают, что практически все показатели суточного мониторирования АД достоверно положительно изменились, что может быть связано с тем, что таурин нормализует повышенный тонус симпатической нервной системы, являющийся одним из ведущих патогенетических звеньев стабилизации АГ на фоне инсулинорезистентности. Кроме того, можно предположить, что, уменьшая количество рецепторов к АТ II на мембранах эндотелиоцитов, таурин оказывает гипотензивный эффект, сходный с таковым у антагонистов рецепторов АТ II [39]. Продемонстрированы и вазорелаксирующие возможности таурина без участия АТ II [46].
Полученные экспериментальные данные свидетельствуют о нефропротективном потенциале таурина, связанном с его использованием при диабетической нефропатии: уменьшении выраженности альбуминурии и тубулоинтерстициального фиброза, что ассоциируют с подавлением экспансии мезенгиального матрикса, ТGF-ß-индуцированного окислительного стресса клубочков и проксимальных почечных канальцев [50]. В экспериментальном исследовании S.Lin и соавт. (2010 г.) [51] показано, что назначение высоких доз таурина в течение 10 нед при экспериментальной диабетической нефропатии сопровождалось снижением уровня экспрессии ламинин (LNB1)mRNA и улучшением метаболизма клубочковой базальной мембраны. Кроме того, таурин снижает нарушенный клеточный рост и гипертрофию клеток почечных канальцев, индуцируемых высоким уровнем глюкозы, что связано с подавлением активации таких сигнальных путей, как MAPK (митогенактивируемый протеинкиназный каскад) и STAT3 (преобразователь сигнала и активатор транскрипции-3) [52]; уменьшает клеточную гипертрофию и фиброз, индуцируемые конечными продуктами гликозилирования в клетках канальцевого эпителия почек [53]; подавляет индукцию генов, ассоциированных с фиброзом, в клетках канальцевого эпителия почек [54]. Несмотря на то что до настоящего времени нет подтверждающих исследований о том, что таурин взаимодействует с АТ II в почках, в сравнительном исследовании ренопротективного действия таурина с ингибиторами ангиотензинпревращающего фермента Cruz и соавт. (2000 г.) продемонстрировали, что как ингибиторы РААС, так и таурин уменьшают зависимое от возраста увеличение белков внеклеточного матрикса, таких как коллаген I, IV и трансформирующий ростовый фактор b (TGF-b) у крыс Fischer 344. Более того, они установили, что таурин ингибирует TGF-ßl-стимулированный синтез белков ECM в культивируемых клетках мезангеума человека, указывая на то, что данная аминокислота может служить альтернативой ингибиторам ангиотензинпревращающего фермента в профилактике фиброза почек у пожилых людей. В другом исследовании M.Mozaffari и соавт. (2003 г.) сравнили длительное лечение таурином, эналаприлом и комбинацией таурина и эналаприла при почечной дисфункции в модели АГ. Все три режима терапии уменьшали экскрецию белка с мочой и улучшали почечную экскреторную функцию. Примечательно, что комбинация таурина и эналаприла оказывала наибольшее положительное влияние на скорость клубочковой фильтрации (СКФ) [55].
Таблица 2. Исследования, посвященные изучению влияния таурина (Дибикор) на метаболические показатели и его органопротективные свойства у больных СД
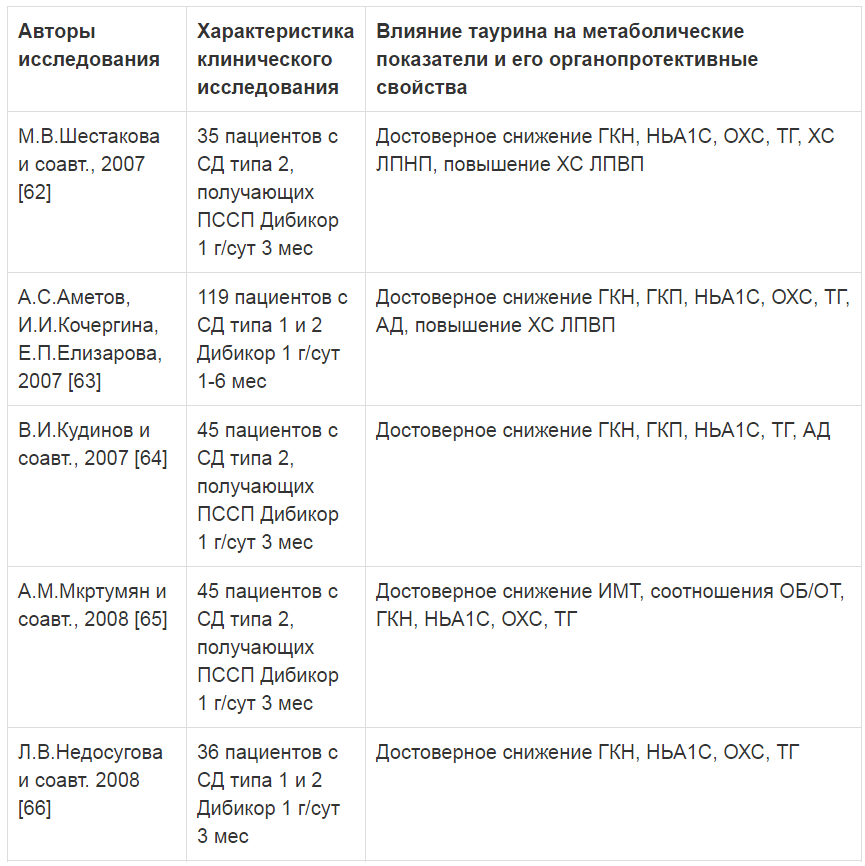
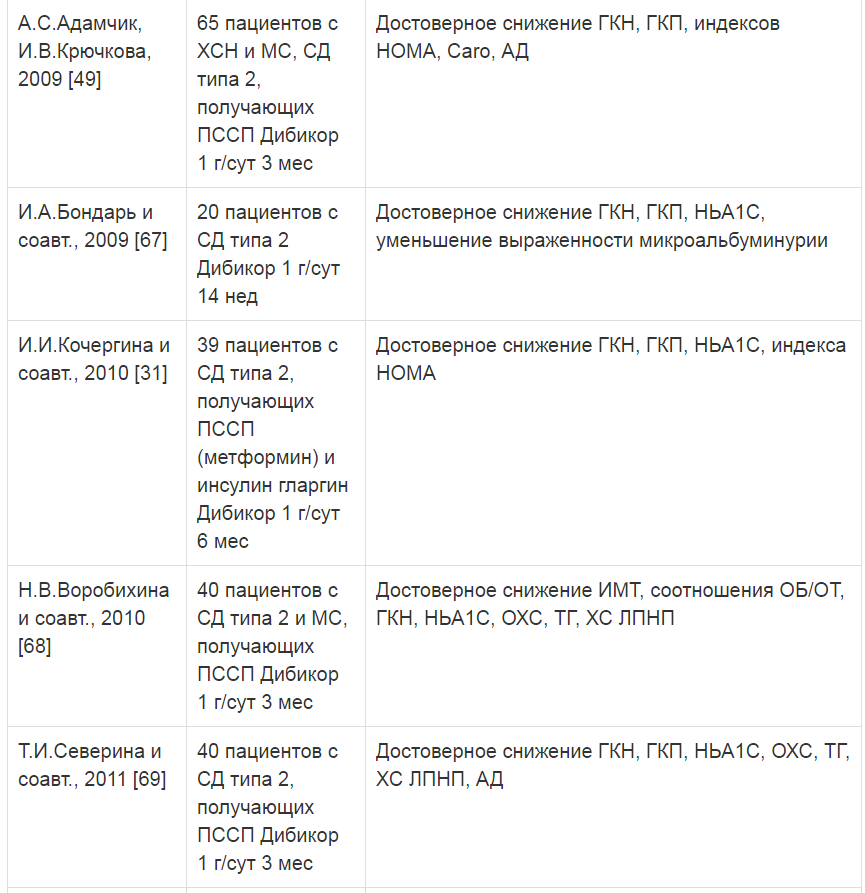
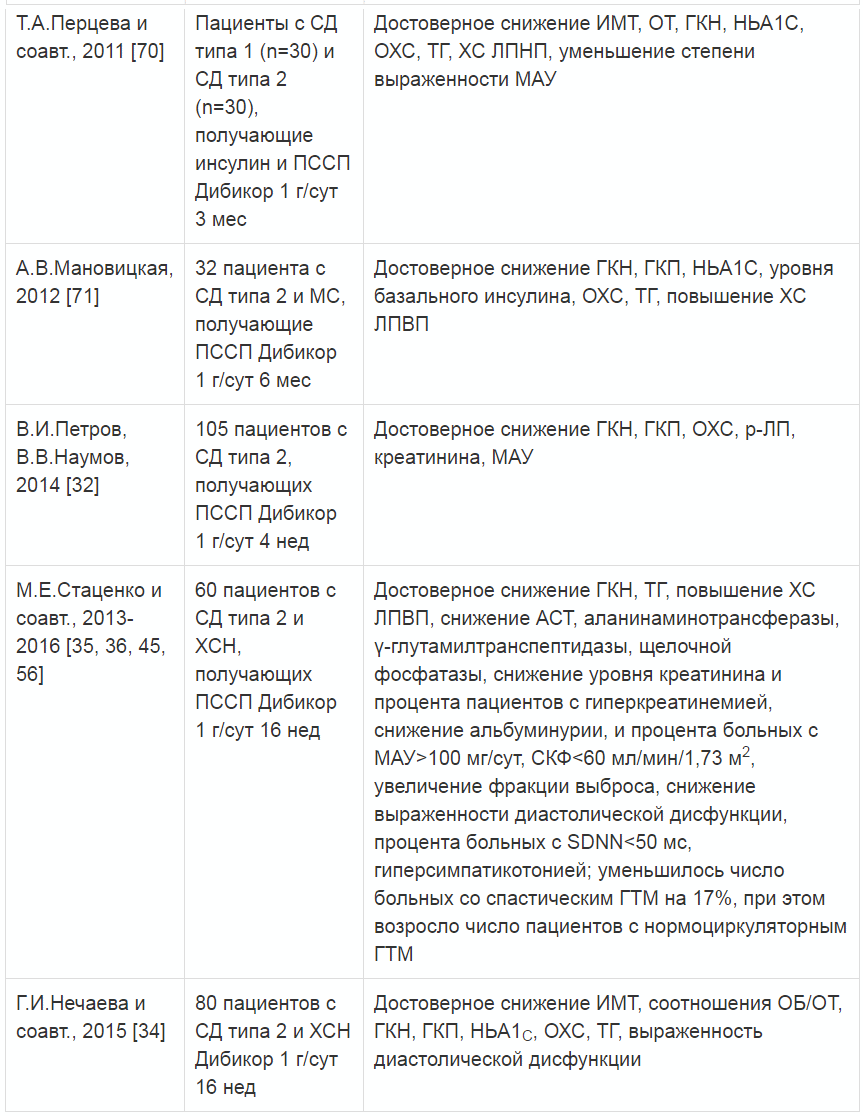
Примечание. ГКН - глюкоза крови натощак, ИМТ - индекс массы тела, ОБ - объем бедер, ОТ - объем талии, ГКП - глюкоза крови постпранди-альная, МАУ - микроальбуминурия, ß-ЛП - ß-липопротеиды.
Убедительно продемонстрирована возможность дополнительной нефропротекции таурином у пациентов с диабетической нефропатией при использовании в составе комбинированной терапии и клинических исследованиях. Так, в исследовании М.Е.Стаценко и соавт. [56] при анализе показателей, характеризующих функциональное состояние почек у пациентов с СД типа 2 и ХСН в ходе 16-недельного приема таурина в дозе 1 г/сут в составе комбинированной базисной терапии этих больных, к концу исследования обращало на себя внимание достоверное уменьшение средних значений креатинина крови, а также значимое снижение процента больных с повышенным содержанием креатинина в крови. Терапия таурином в течение 16 нед ассоциировалась с улучшением клубочковой функции почек: процент больных с исходно сниженной СКФ (менее 60 мл/мин/1,73 м2) в данной группе уменьшился на 11,2%, тогда как в группе контроля этот показатель увеличился на 4,9%. Назначение таурина сопровождалось выраженным антипротеинурическим эффектом: снижение альбуминурии составило 6,9% против 36,1% в 1 и 2-й группах соответственно (р<0,05). Различия между группами статистически значимо. Выявленные нефропротективные свойства таурина, вероятно, объясняются его способностью улучшать функцию эндотелия, вазоконстрикторными и вазодилататорными, антигипертензивными эффектами и возможностью его автономного контроля [47, 57]. В механизме снижения эндогенного креатинина вероятно прямое ренопротективное действие таурина [58].
Интерес представляют экспериментальные данные, свидетельствующие о гепатопротекторных свойствах таурина в лечении неалкогольной жировой болезни печени (НАЖБП). Результаты экспериментального исследования C.Gentile и соавт. (2011 г.) свидетельствуют о возможности таурина снижать выраженность стресса эндоплазматического ретикулума, окислительного стресса, подавлять активность каспазы-3 и апоптоз гепатоцитов, проявления хронического системного воспаления в гепатоцитах. Кроме того, таурин подавлял аккумуляцию ТГ в гепатоцитах, что позволяет рассматривать его как перспективный препарат для профилактики и лечения НАЖБП [59]. На модели неалкогольного стеатогепатита на крысах было показано, что при диете, обогащенной жирами, таурин существенно уменьшает массу печени, активность трансаминаз в сыворотке, уровень ТГ и глюкозы, окислительный стресс, количество экспрессируемой mRNA фактора некроза опухоли a, TGF-b и проколлагена-1; значительно увеличивает экспрессию адипонектина по сравнению с опытной группой.
Проведен ряд клинических исследований, демонстрирующих клиническую эффективность Дибикора при лечении НАЖБП у пациентов с СД типа 2. Так, в двойном слепом плацебо контролируемом сравнительном исследовании у пациентов с СД типа 2 с НАЖБП О.Н.Овсянниковой и Л.А.Звенигородской (2012 г.) [60] показано, что в группе пациентов комбинированной с таурином терапии (препарат назначался в дозе 0,5 г 2 раза в день за 20 мин до еды в течение 3 мес) отмечался достоверно более выраженный гиполипидемический эффект (снижение уровня ОХС), чем у больных, получавших плацебо. Проведенная терапия способствовала снижению уровня ферментов цитолиза, маркеров воспаления и атерогенных фракций липидов у больных с НАЖБП. По данным М.Е.Стаценко и соавт. (2014 г.), 4-месячная терапия препаратом Дибикор в составе комбинированной терапии у пациентов с СД типа 2 и ишемической болезнью сердца позволила не только дополнительно снизить уровень атерогенных липидов, но и способствовала снижению уровней ферментов цитолиза на фоне приема статинов. Через 16 нед приема таурина в составе комбинированной терапии СД типа 2 и ХСН отмечены не только достоверное снижение активности аспартата-минотрансферазы (АСТ) и аланинаминотрансферазы, но и исчезновение у пациентов гиперферментемии, тогда как в группе контроля в 10% случаев сохранилось повышение уровня активности АСТ, статистически значимо уменьшился процент больных с гиперферментемией γ-глутамил-транспептидазы. В исследовании Н.В.Лосевой и Е.Е.Моисеенко [61] таурин также продемонстрировал гепатопротекторное и дополнительное липидснижающее действие у пациентов с неалкогольным стеатогепатитом, ассоциированным с ожирением и СД, в виде положительного влияния на динамику маркеров повреждения у пациентов, принимающих статины.
Таким образом, физиологическая роль таурина, а также результаты доказательных исследований свидетельствуют о том, что эта аминокислота показана для коррекции метаболических нарушений и органопротекции в комплексной терапии больных СД типа 2.
Суммарные данные об органопротективных свойствах таурина при его использовании у пациентов с СД представлены в табл. 2.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru







