Возможности таурина в комплексной терапии больных хронической сердечной недостаточности и сахарного диабета второго типа
Статьи
Опубликовано в журнале:
« Медицинский алфавит » № 4 / 2015, том № 1 М. Е. Стаценко, д. м. н., проф., проректор по научной работе, зав. кафедрой
Н. Н. Шилина, к. м. н., ассистент кафедры
А. А. Винникова, аспирант кафедры
Кафедра внутренних болезней педиатрического и стоматологического факультетов ГБОУ ВПО «Волгоградский государственный медицинский университет» (ВолГМУ) Минздрава России, г. Волгоград
Резюме
В статье рассматривается влияния таурина в составе базисной терапии ХСН и СД второго типа на тяжесть сердечной недостаточности, структурно-функциональные параметры сердца, показатели микроциркуляции, функциональное состояние печени, инсулинорезистентность, углеводный и липидный обмены.
Ключевые слова: сердечная недостаточность, сахарный диабет второго типа, таурин.
В клинической практике сочетание хронической сердечной недостаточности (ХСН) и сахарного диабета (СД) встречается часто, так как ХСН и СД второго типа патогенетически являются взаимосвязанными заболеваниями [1]. Наличие ХСН удваивает риск развития СД из-за свойственной данному синдрому инсулинорезистентности [2]. В то же время наличие СД или наличие у пациента инсулинорезистентности предрасполагают к развитию ХСН [3].
Развитие и прогрессирование ХСН у больных СД второго типа ассоциировано с поражением органов-мишеней, значительными изменениями в углеводном и липидном обменах [4]. Отягощающее действие СД второго типа на развитие и прогноз ХСН обусловлено рядом тесно связанных между собой механизмов. Во-первых, это группа факторов сердечно-сосудистого риска, входящих в синдром инсулинорезистентности (ИР): дислипидемия, артериальная гипертензия (АГ), ожирение и воспаление [5]. Во-вторых, СД способствует развитию коронарного атеросклероза и реализует отрицательное влияние на ХСН через прогрессирование ишемической болезни сердца [6]. В третьих, СД второго типа предрасполагает к развитию ХСН через наличие специфической диабетической кардиомиопатии. Последнюю связывают с диабетической микроангиопатией, нейропатией, метаболическими нарушениями и фиброзом [7].
Самыми опасными последствия- ми СД являются его системные со- судистые осложнения: поражение магистральных сосудов, сердца, головного мозга, нефропатия, ретинопатия. Так, сердечно-сосудистые осложнения у больных СД встречаются в 3–4 раза чаще, чем в общей популяции [8]. Основной причиной смерти больных СД второго типа почти в 50 % случаев является инфаркт миокарда (ИМ) [9].
Кроме того, значительно увеличивает риск возникновения сердечно-сосудистых заболеваний неалкогольная жировая болезнь печени (НАЖБП) во всех ее проявлениях (стеатоз, стеатогепатит, фиброз) [10], являющаяся маркером поражения печени при СД второго типа [11].
Сочетание ХСН и СД второго типа ведет к росту печеночного липогенеза, гликонеогенеза и развитию НАЖБП [12].
Следует отметить, что сердце, почки, печень, сосудистое русло являются не столько пассивными органами мишенями при сочетании ХСН и СД второго типа, но и активными участниками дезадаптивного ремоделирования, так как при их поражении происходит дальнейшее нарастание риска сердечно-сосудистых осложнений, а их функциональное состояние оказывает значимое влияние на прогноз и исход [13].
Зачастую сердечно-сосудистые заболевания и СД второго типа развиваются параллельно [14], что значительно утяжеляет течение обоих заболеваний, ухудшает прогноз и диктует необходимость более активного поиска комплексной патогенетической стратегии предупреждения поражения органов-мишеней.
К настоящему времени выполнено достаточно много экспериментальных и клинических исследований, показывающих перспективность применения таурина в терапии пациентов с сердечно-сосудистой патологией и СД второго типа [15–21].
Однако пока не проведено ни одного крупного международного рандомизированного клинического исследования с включением таурина в базисную терапию ХСН или СД, позволяющего однозначно высказаться о целесообразности его назначения.
В доступной литературе нам также не встретились работы, посвящённые комплексному изучению влияния таурина на течение заболевания и поражение органов-мишеней у пациентов с ХСН и СД второго типа.
Целью исследования было изучение влияния таурина в составе базисной терапии ХСН и СД второго типа на тяжесть сердечной недостаточности, структурнo-функциональные параметры сердца, показатели микроциркуляции, функциональное состояние печени, инсулинорезистентность, углеводный и липидный обмены.
Материалы и методы
В исследование были включены 60 больных обоих полов в раннем постинфарктном периоде (3–4-я неделя от начала ИМ) с ХСН II–III функциональных классов (ФК) по классификации ОССН (2002) и сопутствующим СД второго типа.
Включённые в исследование пациенты имели клинико-ультразвуковые признаки неалкогольного стеатоза печени [22].
Протокол исследования одобрен Региональным этическим комитетом.
Все пациенты были распределены методом простой рандомизации в две группы по 30 человек: первая (контрольная) — пациенты, получающие базисную терапию сердечной недостаточности (бисопролол, периндоприл, ацетилсалициловая кислота, клопидогрел, симвастатин, диуретики (фуросемид или индапамид), спиронолактон, при необходимости нитраты) и базисную сахароснижающую терапию (метформин и [или] глибенкламид) и вторая (опытная) — пациенты, принимающие дополни- тельно к основному лечению ХСН и СД таурин (Дибикор, ПИК-ФАРМА, Россия) в дозе 500 мг два раза в сутки.
Средние дозы базисных препаратов, применяемых для лечения ХСН и СД второго типа, статистически достоверно не различались между группами
Больные в обеих группах при включении в исследование не имели достоверных различий по возрасту, полу, тяжести перенесенного инфаркта мио- карда, ХСН и СД второго типа (табл. 1).
Кроме того, пациенты не имели достоверных межгрупповых различий при включении в исследование по таким параметрам, как фракция выброса левого желудочка — ФВ ЛЖ (50,7 ± 6,1 vs 49,8 ± 5,9 %); индекс массы миокарда ЛЖ (145,5 ± 7,2 vs 146,9 ± 6,2 г/м 2); распределение типов диастолической дисфункции (ДД): рестриктивный тип ДД (3,3 vs 6,7 %), псевдонормальный тип ДД (13,3 vs 23,3 %), гипертрофический тип ДД (83,3 vs 70 %) соответственно в первой и второй группах.
Для решения поставленных задач проводили клиническое обследование пациентов с оценкой ФК ХСН пациента по тесту шестиминутной ходьбы (ТШХ). Для оценки выраженности проявлений ХСН определяли уровень мозгового натрийуретического пропептида (Nt-proBNP) методом иммуноферментного анализа (ИФА) на биохимическом анализаторе Liasys (AMS, Италия).
Эхокардиографическое (ЭхоКГ) исследование для изучения структурно-функционального состояния миокарда выполнено на аппарате Siemens SONOLINE G50 (Германия). Расcчитаны основные структурные и функциональные параметры сердца в соответствии с рекомендациями по количественной оценке структуры и функций камер сердца. Фракция выброса левого желудочка определялась по Симпсону.
Микроциркуляция (МЦ) изучалась методом лазерной допплеровской флоуметрии (ЛДФ) со спектральным анализом колебаний кровотока с помощью аппарата «ЛАКК-ОП» (Россия). Оценивали основные параметры микроциркуляторного русла [23].
С учетом показателя микроциркуляции на исходной ЛДФ-грамме и резервного капиллярного кровотока (РКК) при проведении окклюзионной пробы определяли гемодинамический тип микроциркуляции (ГТМ).
Были выделены следующие ГТМ: нормоциркуляторный, гиперемический, спастический. В тех случаях, когда указать конкретный ГТМ было затруднительно, решающим являлся показатель РКК, отражающий функциональные возможности сосудов МЦ.
Таблица 1.
Клинико-демографическая характеристика больных ХСН и СД второго типа
| Параметры | I группа | II группа |
|---|
| Число больных, человек | 30 | 30 |
| Возраст, лет | 54,3 ± 2,2 | 55,1 ± 2,8 |
| Мужчины, абс. число, % | 16 (53,3) | 13 (43,3) |
| Женщины, абс. число, % | 14 (46,7) | 17 (56,7) |
| ИМ с з. Q / без з. Q, человек, % | 23 (76,7) /7 (23,3) | 20 (66,7) / 10 (33,3) |
| ИМТ выше 25 кг/м2, человек, % | 13 (43,3 %) | 16 (53,3 %) |
| Ожирение I степени, человек, % | 9 (30 %) | 13 (43,3 %) |
| Курение, человек, % | 2 (6,7 %) | 6 (20 %) |
| Пациенты с АГ / без АГ в анамнезе, % | 28 (93,3) / 2 (6,7) | 29 (96,7) /1 (3,3) |
| Анамнез СД, годы | 4,5 ± 2,2 | 5,6 ± 3,1 |
| ФК ХСН, баллы | 2,1 ± 0,7 | 2,2 ± 0,7 |
| Nt-proBNP, пг/мл2 | 160,28 ± 430,6 | 1 940,29 ± 340,2 |
| Примечание: ИМ с з. Q — инфаркт миокарда с зубцами Q, ИМ без з. Q — инфаркт миокарда без зубцо Q, ИМТ — индекс массы тела, АГ — артериальная гипертензия, Nt-proBNP — мозговой натрийуретический пропептид. |
Для оценки функционального состояния печени определяли следующие показатели: активность аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT), активность щелочной фосфатазы (ЩФ) и γ-глутамилтранспептидазы (ГГТП), уровень общего белка и альбумина, общего билирубина, показатель тимоловой пробы и протромбиновый индекс (ПТИ) в сыворотке крови по общепринятым методикам на биохимическом анализаторе LIASYS-2 (AMS, Италия). Также определяли общий анализ крови с подсчётом количества тромбоцитов.
Состояние углеводного обмена оценивали по уровню глюкозы крови натощак (исследовали с помощью наборов фирмы Lachema, Чехия) унифицированным калориметрическим глюкозооксидазным методом), определяли базальный инсулин методом ИФА на иммуноферментном анализаторе «УНИПЛАН» («Пикон», Россия) и гликированный гемоглобин (HbA1c) методом боратного аффинного анализа на анализаторе NycoCard Reader II (Axis-Shield РоС AS, Норвегия). Рассчитан индекс инсулинорезистентности (ИР) — индекс HOMA-IR (Homeostasis Model of Assessment-Insulin Resistance).
Для оценки состояния липидного обмена крови определяли уровни общего холестерина (ОХС), ТГ, ЛПНП, липопротеидов высокой плотности (ЛПВП), индекс атерогенности (ИА) на биохимическом анализаторе Liasys (AMS, Италия).
Статистическая обработка результатов проведена с использованием функций Microsoft Excel 2010 и пакета статистических программ Statistica 6.0.
Применены методы параметрической и непараметрической статистики. Вычислено среднее значение исследуемых величин (М), ошибка средней величины (m) для каждого показателя. Оценка достоверности различий между данными, полученными в исследуемых группах, осуществлена с использованием t-критерия Стьюдента. Качественные величины сравнивали с помощью критерия Фишера.
Статистически значимыми считали отклонения при p Результаты и обсуждение
В конце 16-ти недель терапии по результатам ТШХ толерантность к физическим нагрузкам у пациентов достоверно увеличилась в обеих группах: на 38,5 % в основной и на 24,8 % в контрольной группах, в то время как ФК тяжести ХСН снизился на 18,2 и 16,1 % соответственно. Достоверного различия между группами не выявлено. В конце исследования во второой группе пациентов, принимавших таурин, выявлено достоверное снижение уровня Nt-proBNP, отражающего степень тяжести сердечной недостаточности у обследованных больных, — на 28,9 vs 13,7 % в группе сравнения. Различие между группами по данному показателю на уровне статистической тенденции (p = 0,07).
По данным ЭхоКГ, позитивные изменения наблюдались и в структурно-функциональных параметрах сердца на фоне приёма таурина [24].
Статистически значимым оказалось увеличение ФВ ЛЖ у больных, которым дополнительно назначали таурин: на 15 vs 2,4 % в группе сравнения по завершении исследования.
По-видимому, положительное влияние таурина на течение ХСН и систолическую функцию сердца обусловлено доказанными антиоксидантными [20] и противовоспалительными свойствами данной аминокислоты [18], способностью нивелировать эффекты ангиотензина II, а соответственно снижать скорость прогрессирования ремоделирования левого желудочка [25].
Исследование состояния МЦ показало, что большинство пациентов ХСН и СД второго типа, включённых в исследование, имели гиперемический тип МЦ: 43 % в основной группе и 37 % в контрольной. Спастический и нормоциркуляторный типы выявлены у 27 и 30 % больных во второй группе и у 27 и 33 % исследуемых в первой группе соответственно (см. рис.). Нарушение транспортной функции МЦ русла приводит к дистрофическим и атрофическим изменениям, а также актированию процессов перекисного окисления липидов, апоптоза клеток и фиброгенеза [26].
Отмечено перераспределение типов МЦ через 16 недель лечения среди пациентов второй группы, принимающих в дополнение к базисной терапии ХСН и СД второго типа таурин.
Статистически значимо уменьшилось количество больных со спастическим ГТМ на 17 %, при этом возросло ко- личество пациентов с нормоциркуляторным ГТМ (см. рис.).
Вазопротективные свойства таурина также отмечены в работах иностранных авторов, а именно способность таурина снижать жёсткость магистральных сосудов [19, 21] улучшать эндотелиальную функцию [16].
Под влиянием включения в состав комбинированной терапии таурина у пациентов с ХСН и СД второго типа наблюдалась благоприятная динамика показателей, отражающих функциональное состояние печени (табл. 2). Исходно повышение активности АСТ и АЛТ выше нормальных значений (но не более трёхкратного превышения верхней границы нормы) отмечалось в 20 % случаев во второй группе и в 23,3 % — в первой группе. Через 16 недель приема таурина в составе комбинированной терапии ХСН и СД второго типа ни у одного пациента во второй группе не регистрировалась гиперферментемия, тогда как в первой группе в 10 % случаев сохранилось повышение уровня активности АСТ. Различие между группами статистически значимо.
Таблица 2.
Динамика показателей функционального состояния печени у больных ХСН и СД второго типа
| Показатель | I группа (базисная терапия) | Δ,% | II группа (базисная терапия + таурин) | Δ, % | p’ |
|---|
| Исходно | 16 недель | Исходно | 16 недель |
|---|
| Билирубин общий, мкмоль/л | 13,6 ± 5,4 | 15,4 ± 4,9 | 13,7 | 13,8 ± 4,21 | 12,7 ± 4,37 | –8,05# | НД |
| Активность ГГТП, Ед/л | 28,6 ± 11,4 | 26,8 ± 9,12 | –6,9 | 33,8 ± 18,4 | 19,7 ± 8,1*# | –41,9 | р |
| Активность ЩФ, Ед/л | 2,9 ± 0,7 | 2,89 ± 0,63 | –0,34 | 2,2 ± 0,8 | 1,7 ± 0,36*# | –22,27 | р |
| АЛТ, Ед/л | 27,5 ± 11,54 | 26,4 ± 18,9 | –4,1 | 31,1 ± 5,3 | 18,92 ± 8,3*# | –39,06# | р |
| АСТ, Ед/л | 20,9 ± 8,4 | 20,45 ± 6,3 | –0,98 | 29,7 ± 11,9 | 21,67 ± 4,94*# | –26,93 | р |
| Тимоловая проба, Ед | 1,72 ± 0,35 | 1,91 ± 0,5 | 11,04 | 1,7 ± 0,98 | 1,79 ± 0,54 | 3,47 | НД |
| Общий белок, г/л | 66,9 ± 4,54 | 65,3 ± 5,12 | –2,39 | 70,6 ± 6,94 | 70,86 ± 7,8 | 0,35 | НД |
| Альбумин, г/л | 34,8 ± 5,96 | 35,13 ± 4,88 | 0,95 | 43,3 ± 7,7 | 45,16 ± 8,06 | 4,25 | НД |
| ПТИ, % | 83,13 ± 10,88 | 82,26 ± 9,92 | –1,04 | 84,0 ± 9,31 | 90,3 ± 4,3*# | 7,54 | НД |
| Примечание: * — достоверность различий между исходными и конечными результатами внутри группы при р |
Кроме того, отмечено достоверное снижение активности АСТ и АЛТ во второй группе пациентов, дополнительно принимающих таурин (Δ,% = –39,06 и Δ,% = –26,93 соответственно vs Δ ,% = –4,1 и Δ,% = –0,98 в первой группе).
Выявлено снижение активности как ЩФ, так и ГГТП у пациентов, получающих комбинированную терапию с включением таурина. Активность ЩФ снизилась на 22,7 % во второй vs 0,34 % в первой группе (р 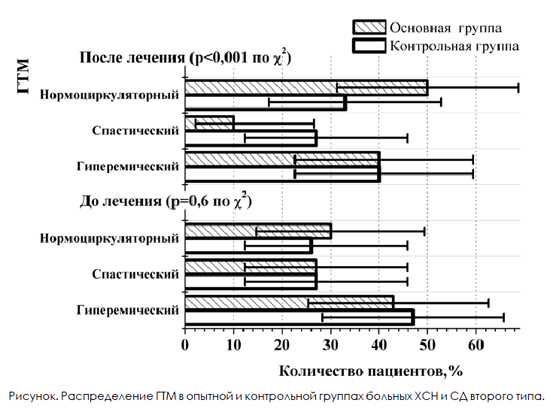
Результаты наших исследований согласуются с данными Лосева Н. В. и Моисеенко Е. Е., в которых таурин продемонстрировал гепатопротекторное действие у пациентов с неалкогольным стеатогепатитом, ассоциированным с ожирением и СД, в виде положительного влияния на динамику печеночных проб [27].
У больных второй группы на фоне включения в комбинированную терапию таурина также выявлено статистически значимое улучшение показателей углеводного обмена: снижение уровня глюкозы крови натощак и HbA1c, а достоверное снижение индекса HOMA свидетельствует о клинически значимом уменьшении ИР (табл. 3).
Таблица 3.
Динамика показателей углеводного и липидного обмена у больных ХСН и СД второго типа
| Показатель | I группа (базисная терапия) | Δ,% | II группа (базисная терапия + таурин) | Δ, % | p’ |
|---|
| Исходно | 16 недель | Исходно | 16 недель |
|---|
| Глюкоза натощак, ммоль/л | 8,7 ± 0,3 | 8,4 ± 0,3 | –3,4 | 9,25 ± 1,2 | 7,34 ± 0,9* | –20,6 | |
| HbA1c, % | 9,6 ± 1,2 | 8,7 ± 1,4 | –9,4 | 10,1 ± 1,8 | 8,20 ± 1,0* | –18,8 | НД |
| Индекс НОМА, у. е. | 5,05 ± 1,1 | 4,92 ± 0,8 | –2,6 | 5,62 ± 0,8 | 4,96 ± 0,6* | –11,7 | НД |
| ОХС, ммоль/л | 5,70 ± 1,0 | 5,5 ± 0,8 | –3,5 | 5,87 ± 0,9 | 5,63 ± 0,6 | –4,1 | НД |
| ХСЛПНП, ммоль/л | 4,33 ± 0,6 | 3,71 ± 0,4* | –14,3 | 4,26 ± 0,7 | 3,52 ± 0,4* | –17,4 | НД |
| ХСЛПВП, ммоль/л | 1,12 ± 0,3 | 0,96 ± 0,3 | –14,3 | 0,98 ± 0,3 | 1,11 ± 0,3 | 13,3 | НД |
| ТГ, ммоль/л | 2,96 ± 0,5 | 2,87 ± 0,6 | –3,0 | 3,20 ± 0,4 | 2,68 ± 0,4* | –16,3 | |
| ИА, у. е. | 3,18 ± 0,9 | 2,98 ± 0,7 | –6,3 | 3,65 ± 0,8 | 3,21 ± 0,6* | –12,1 | НД |
| Примечание: * — достоверность различий между исходными и конечными результатами внутри группы при р |
При изучении липидного обмена обнаружено статистически значимое снижение уровня ХСЛПНП (Δ17 %) и триглицеридов (Δ16 %) в группе пациентов, принимавших таурин в дополнение к базисной терапии ХСН и СД второго типа (табл. 3). Благоприятное влияние таурина на функциональное состояние печени и уровень триглицеридов и ХСЛПНП являются патогенетически важными, так как нарушение функционального состояния печени — один из наиболее важных факторов развития дислипопротеинемии, поскольку изменения липидного метаболизма начинаются на уровне гепатоцита, а печень является органом-мишенью при атерогенной дислипидемии [28].
В исследованиях, проведенных ранее, у пациентов с СД второго типа также показано благоприятное влияние таурина на углеводный и липидный обмены [29–30]. Гипогликемический и липидснижающий эффекты таурина объясняются снижением выраженности инсулинорезистентности, которая лежит в основе развития СД второго типа [31].
Выводы
1. Таурин в составе четырехмесячной базисной терапии ХСН и СД второго типа достоверно увеличивает толерантность к физическим нагрузкам и уменьшает ФК ХСН, способствует снижению уровня Nt-proBNP и значимо увеличивает ФВ ЛЖ.
2. На фоне приема таурина происходит статистически значимое увеличение доли нормоциркуляторного ГТМ у больных ХСН и СД второго типа за счет уменьшения встречаемости спастического типа.
3. Включение таурина в комплексную терапию больным с ХСН и СД второго типа оказывает гепатопротекторное действие, значимо снижая повышенную активность АСТ, АЛТ, ЩФ и ГГТП;
4. 16-недельная терапия таурином пациентов ХСН и СД второго типа оказывает благоприятные эффекты на углеводный и липидный обмен: достоверно снижает уровень глюкозы натощак, HbA1c, инсулинорезистентность, а также уменьшает уровни ЛПНП и ТГ.
Список литературы
1. Нарусов О. Ю., Лапина Ю. В., Мареев В. Ю. и соавт. Влияние тяжести хронической сердечной недостаточности на течение сопутствующего сахарного диабета 2-го типа. Результаты исследования «Рациональная Эффективная Многокопонентная терапия в Борьбе с Сахарным Диабетом у больных ХСН» (РЭМБО-СД ХСН). Терапевтический архив, 2009; 81 (9): 52–57.
2. Amato L., Paolisso G, Cacciotore F. et al1. Congestive hearts failure predicts the development of non-insulin-dependent diabetes mellitus in the elderly. The Osservatorio Geriatrico Regione Campania Group. Diabetes Metab. 1997; 23 (3): 213–218.
3. Мареев В. Ю., Беленков Ю. Н. Хрониче- ская сердечная недостаточность и ин- сулиннезависимый сахарный диабет: случайная связь или закономерность? Терапевтический архив, 2003; 75 (10): 5–10.
4. Стаценко М. Е., Фабрицкая С. В., Турки- на С. В. и др. Особенности поражения органов-мишеней, состояния углеводно- го и липидного обменов, качества жизни у пациентов с хронической сердечной недостаточнсотью и сахарным диабетом 2 типа. Журнал сердечная недостаточ- ность 2010; 11 (4): 206–212.
5. Bauters С, Lamblin N., Mc Fadden Е. P. et al1. Influence of diabetes mellitus on heart failure risk and outcome. Cardiovasc Diabetol. 2003;2 (1):1.
6. Стронгин Л. Г., Починка И. Г., Алейник Д. Я., Чарыкова И. Н. Предикторы выживаемости больных хронической сердечной недоста- точностью, страдающих сахарным диабе- том 2 типа. Сахарный диабет, 2004; 4: 14–18.
7. Bell D. S. Diabetic cardiomyopathy Diabetes Care. 2003; 26 (10): 2949–2951.
8. Петина М. М., Гороховская Г. Н., Марты- нов А. И. Эндотелиальная дисфункция у больных ишемической болезнью сердца с сахарным диабетом 2 типа. Российский кардиологический журнал. 2011; 2 (88): 32–36.
9. Мычка В. Б., Чазова И. Е. Сердечно-сосу- дистые осложнения сахарного диабета типа 2. Consilium medicum, 2003; 5 (9): 504–509.
10. Драпкина О. М. Неалкогольная жировая болезнь печени и метаболический син- дром. Справочник поликлинического врача, 2008; 3: 71–74.
11. Gupte P., Amarapurkar D. Agal S. et al. Non-alcoholic steatohepatitis in type 2 diabetes mellitus. Journal of Gastroenterology and Hepatology. 2004; 19 (8):854–858.
12. Targher G., Bertolini L., Padovani R., Rodella S., Tessari R., Zenari L. et al. Prevalence of non-alcoholic fatty liver disease and its association with cardiovascular disease among Type 2 diabetic patients. Diabetes Care. 2007; 30: 1212–1218.
13. Стаценко М. Е., Туркина С. В., Шилина Н. Н., Полетаева Л. В. и др. Поражение орга- нов — мишеней у больных с хронической сердечной недостаточнсотью и сахар- ным диабетом типа 2: есть ли особен- ности? Вестник Волгоградского государ- ственного медицинского университета 2014; 1 (49): 12–16.
14. Рекомендации по диабету, предиабету и сердечно-сосудистым заболеваниям. EASD/ESC. Российский кардиологический журнал 2014; 3 (107): 6–70
15. Стаценко М. Е., Винникова А. А., Шили- на Н. Н., Ронская А. М. Возможности ди- бикора в коррекции метаболических и сосудистых нарушений у больных хро- нический сердечной недостаточностью и сахарным диабетом 2 типа. Фармате- ка 2014; 5: 53–60.
16. El Idrissi A, Okeke E, Yan X, et al1. Taurine regulation of blood pressure and vasoactivity. Adv Exp Med Biol. 2013;775:407–425.
17. Покровская Е. М., Волов Н. А., Василье- ва И. С. Новые возможности лечения пациентов с сердечной недостаточ- ностью вследствие постинфарктного кардиосклероза. Медицинский совет. 2012;12:18–23.
18. Walczewska M, Marcinkiewicz J. Taurine chloramine and its potential therapeutical application. Przegl Lek. 2011;68 (6):334–338.
19. Abebe W, Mozaffari MS. Role of taurine in the vasculature: an overview of experimental and human studies. Am J Cardiovasc Dis. 2011;1 (3):293–311.
20. Schaffer SW, Azuma J, Mozaffari M. Role of antioxidant activity of taurine in diabetes. Can J Physiol Pharmacol. 2009;87 (2):91–99.
21. Satoh H, Kang J. Modulation by taurine of human arterial stiffness and wave reflection. Adv Exp Med Biol. 2009;643:47–55.
22. Ergün Y. The diagnostic role of ultrasonograhyy in liver streatosis. The Turkish Journal of Gastroenterology. 1999; 2: 96–100
23. Крупаткин А.И, Сидоров В. В. Лазерная допплеровская флоуметрия микроцир- куляции крови. Москва 2005. — 256 с.
24. Стаценко М. Е., Винникова А. А., Рон- ская А. М., Шилина Н. Н. Таурин в терапии хронической сердечной недостаточно- сти и сахарного диабета 2 типа: влияние на микроциркуляцию и эластические свойства магистральных сосудов. Жур- нал сердечная недостаточность 2013; том 14; № 6 (80): 347–353.
25. Schaffer SW, Lombardini JB, Azuma J. Interaction between the actions of taurine and angiotensin II. Amino Acids. 2000;18 (4):305–18
26. Драпкина О. М. РААС и фиброз. Гепато- кардиальные связи. Русский медицинси- кй журнал. 2011; 18: 1136–1139.
27. Лосева Н. В., Моисеенко Е. Е. Опыт при- менения препарата Дибикор в комплекс- ной терапии неалкогольной жировой бо- лезни печени. Фарматека 2010: 13; 63–67.
28. Балукова Е. В. Неалкогольная жировая болезнь печени и риск кардиоваскулярных событий. Русский медицинский журнал, 2013; 13:737–741.
29. Шестакова М. В., Чугунова Л. А., Шамхалова М. Ш. Опыт применения Дибикора при сахарном диабете 2 типа. Сахарный диабет 2007; 1:30–31.
30. Крючкова И. В., Адамчик А. С. Возможности коррекции нарушений углеводного обмена при метаболическом синдроме. Российский кардиологический журнал, 2009; 2: 38–42.
31. Аметов А. С., Кочергина И. И. Применение Дибикора при сахарном диабете и сердечно-сосудистой патологии. Эффективная фармакотерапия в эндокринологии 2007;2: 40–49.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru



