Применение препарата Дибикор у подростков с артериальной гипертензией
Статьи
Опубликовано в журнале:
«Системные гипертензии»; № 4; 2011; стр. 64-68.
М.Я.Ледяев, В.Б.Жукова, Я.А.Ананьева
ГБОУ ВПО Волгоградский государственный медицинский университет Минздравсоцразвития РФ
Резюме. В работе обсуждаются вопросы применения препарата Дибикор у подростков с артериальной гипертензией (АГ) 1-й степени. Показано, что Дибикор снижает величину среднего суточного артериального давления и индекс времени по данным суточного мониторирования артериального давления, а также снижает уровень реактивной тревожности у подростков с АГ 1 -й степени.
Ключевые слова: артериальная гипертензия, суточное мониторирование артериального давления, подростки, Дибикор, таурин.
Use Of Dibicorum In Adolescents With Arterial Hypertension
M.Ya.Ledyaev, V.B.Zhukova, Ya.A.Ananieva
Volgograd State Medical University, Ministry of Health and Social Development of the Russian Federation
Summary. This paper discusses the use of Dibicorum in adolescents with stage-1 hypertension. There are data of the influence of the Dibicorum on the value of the blood pressure and on the level of adolescent's anxiety. It was shown, that Dibicorum reduces the value of following ambulatory blood pressure monitoring parameters: the mean daily blood pressure and time-index, and also decreases the level of the reactive anxiety in adolescents with stage-1 hypertension.
Key words: hypertension, ambulatory blood pressure monitoring, adolescents, Dibicorum, taurine.
Актуальность
В последние десятилетия наблюдается тревожная тенденция к увеличению численности больных с артериальной гипертензией (АГ). Актуальность проблемы АГ в педиатрии обусловлена тем, что заболевание существенно «помолодело» и не является казуистической редкостью, а относится к распространенным заболеваниям, возникающим в период формирования нейрогенных и гуморальных механизмов регуляции сердечно-сосудистой системы и артериального давления (АД) [1—3].
Это подтверждают эпидемиологические исследования, проведенные за рубежом и в России методом случайного отбора с достаточной численностью обследуемых и едиными стандартизированными методиками измерения АД, позволившие получить объективные данные о распространенности АГ у детей и подростков, которая составляет от 2,4 до 18% [4-7].
Современным и перспективным направлением повышения качества диагностики АГ у подростков и контроля за антигипертензивной терапией является амбулаторное суточное мониторирование АД (СМАД) с использованием носимых портативных АД-мониторов [8-11].
Показаниями к фармакотерапии АГ служат стабилизация повышенного АД, отсутствие эффекта от немедикаментозной терапии, прогрессирование заболевания, поражение органов-мишеней [12, 13]. В настоящее время антигипертензивные препараты (β-адреноблокаторы, блокаторы ренин-ангиотензиновой системы, антагонисты ионов кальция и др.) широко применяются в терапевтической практике для лечения АГ у взрослых [14]. Однако остается много нерешенных вопросов о тактике ведения пациентов детского возраста с АГ.
Дибикор представляет собой нейроактивную аминокислоту таурин, который рассматривается как нейромодулятор [15-19]. Недавние исследования в клинической практике показали, что препарат обладает антигипертензивным действием у беременных с АГ [20, 21].
Однако его гемодинамические эффекты у подростков изучены недостаточно, а накопленный опыт его клинического применения, особенно в педиатрии, пока невелик.
Цель
Оценить терапевтический эффект препарата Дибикор у подростков с АГ 1-й степени на основе анализа его влияния на суточный профиль АД, суточный профиль артериального тонуса (АТ), а также на качество жизни пациентов.
Материалы и методы
Было проведено открытое контролируемое несравнительное исследование с выделением отдельной подгруппы с углубленным исследованием. Группу подростков с АГ 1-й степени, у которых изучалась эффективность терапии препаратом Дибикор, составили 65 подростков. Диагноз АГ 1-й степени верифицировался на основании рекомендаций по диагностике, лечению и профилактике АГ у детей и подростков, по величине систолического АД (САД) и/или диастолического АД (ДАД), превышающей значение 95 процентиля АД, но не более 99 процентиля плюс 5 мм рт. ст. [12, 13].
Критерии включения в исследование:
пациенты обоего пола от 12 до 18 лет;наличие АГ 1-й степени с уровнем САД, превышающем значение 95 процентиля АД, но не более 99 процентиля плюс 5 мм рт. ст.;уровень глюкозы крови натощак не более 5,5 ммоль/л по капиллярной крови;индекс массы тела (ИМТ) от 50 до 89 процентиля для соответствующего пола и возраста;пациенты, которые в течение не менее чем за 2 недели до 1 визита не принимали антигипертензивные препараты;наличие подписанного информированного согласия пациента на участие в исследовании.Критерии исключения из исследования:
повышенная чувствительность к исследуемому препарату;сердечная недостаточность в стадии декомпенсации;АГ тяжелой степени тяжести (более 99 процентиля плюс 5 мм рт. ст.);тяжелые сопутствующие заболевания, в.т. психические;острые состояния (инфекции, обострение хронических заболеваний, травмы, хирургические вмешательства);злоупотребление алкоголем;серьезные нарушения функции почек (креатинин в 2 раза выше нормы);серьезные нарушения функции печени (аспартатаминотрасфераза, аланинаминотрансфераза в 2 раза выше нормы);злокачественные новообразования;неспособность понять суть программы и дать обоснованного согласия на участие в ней.Дизайн исследования представлен на рис. 1.
Рис 1. Открытое исследование Дибикор при АГ.
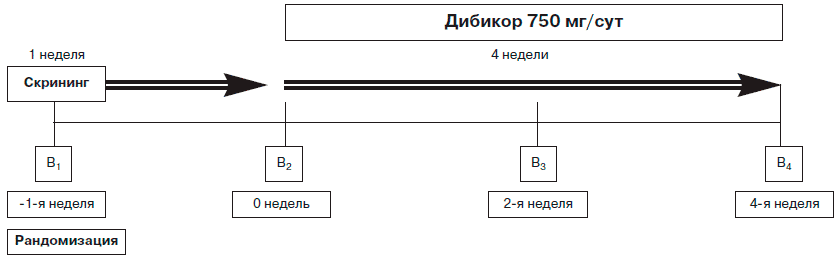
1 -й визит: скрининг, оценка соответствия критериям включения, взятие информированного согласия, рандомизация методом конвертов.
2-й визит: для основной группы исследования (65 подростков) -клинический осмотр, проведение обследования (заполнение опросников по уровню тревожности) и назначение препарата Дибикор® по 250 мг 3 раза в сутки.
2-й визит: для подгруппы с углубленным исследованием (20 подростков) - заполнение опросника по уровню тревожности, проведение обследования по определению уровня офисного АД, электрокардиография (ЭКГ), проведение СМАД, исследование по оценке АТ, эхокардиография (ЭхоКГ), назначение препарата Дибикор® по 250 мг 3 раза в сутки.
3-й визит: через 2 нед от начала терапии для всех групп исследования - контроль клинического состояния, учет побочных эффектов, контроль приверженности терапии, заполнение опросников по уровню тревожности, продолжение терапии препаратом исследования в прежней дозе. Для подгруппы углубленного исследования - проведение обследования по определению уровня офисного АД, ЭКГ, проведение СМАД, ЭхоКГ, исследование по оценке АТ.
4-й визит: через 4 нед от начала терапии для всех групп исследования - контроль клинического состояния, учет побочных эффектов, контроль приверженности терапии, заполнение опросников по уровню тревожности. Для подгруппы углубленного исследования -проведение обследования по определению уровня офисного АД, ЭКГ, проведение СМАД, ЭхоКГ, исследование по оценке АТ.
Средний возраст 14,3±0,4 года, давность заболевания от 2 до 3 лет.
Характеристика подростков представлена в табл. 1.
Таблица. 1.
Характеристика обследованных пациентов
| Показатель | Основная группа | Подгруппа с углубленным исследованием |
| Число пациентов | 65 | 20 |
| Средний возраст, лет | 14,3±0,4 | 14±0,3 |
| Длительность АГ, годы | 2,1±0,6 | 2,3±0,7 |
| Мальчики/девочки | 35/30 | 12/8 |
| ИМТ, кг/м2 | 20,1 ±1,4 | 20,6±1,8 |
Дибикор® (Dibicorum) относится к группе метаболических препаратов, действующим веществом является таурин (Taurine). Препарат Дибикор производится Российской фармацевтической компанией ООО «ПИК-ФАРМА». Номер регистрации -PN 001698/01.
В нашем исследовании СМАД и пульса проводилось прибором МнСДП-3 (ООО «Петр Телегин», Н.Новгород, Россия), зарегистрированным в Минздравсоцразвитии РФ за №29/02050901/3450-02. Манжету подбирали в соответствии с длиной окружности плеча ребенка.
Оценка АТ при проведении СМАД проводилась на основании анализа кривой осциллометрических амплитуд («колокола»). Во время проведения СМАД с использованием носимого монитора автоматического измерения АД и частоты пульса МнСДП-3 (ООО «Петр Телегин», Н.Новгород, Россия). Расчет АТ производился по формуле: АТ (ед.)=(САД-АДср.)/(Н2-Н1), где АДср. - среднее гемодинамическое АД в точке пересечения H2 с осью АД (мм. рт. ст.), САД в точке пересечения H1 с осью АД (мм рт. ст.), Н1 - средняя высота осциллометрических колебаний (условные единицы), соответствующая величине САД, Н2 - средняя высота осциллометрических колебаний (условные единицы), соответствующая величине АДср. (рис. 2).
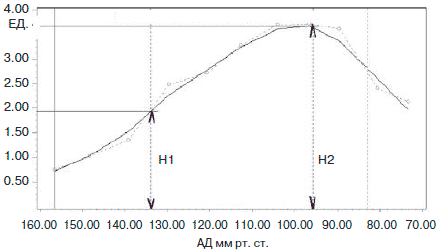
Рис. 2. Схема расчета АТ с использованием монитора АД МнСДП-3.
ЭхоКГ проводили по стандартной методике на аппарате Aloka 2000.
Для оценки уровня тревожности подростков в данный, определенный момент (реактивная тревожность) и личностной тревожности (как устойчивой характеристики человека) использовали тест, разработанный ЧД.Спилбергером (США) и модифицированный Ю.Л.Ханиным [22]. При интерпретации показателей, значения до 30 оценивали как низкую тревожность, 31-43 - как умеренную и 44 и более - как высокую тревожность.
Статистическую обработку данных проводили с использованием статистической программы INSTAT. Данные представлены в формате М± , достоверные изменения с p<0,05. Для графического анализа результатов исследования использовали приложение MS Excel, для сглаживания результатов использовали полиномиальный анализ - полином 6-й степени.
Результаты и обсуждение
В табл. 2 представлена динамика основных параметров гемодинамики у обследованных подростков. Офисное САД достоверно уменьшилось на 4-й неделе терапии на 7,4%, офисное ДАД, частота сердечных сокращений (ЧСС), ударный (УО) и минутный объем крови (МОК) не изменились на протяжении всего исследования.
Таблица 2
Динамика параметров гемодинамики у подростков с АГ 1-й степени на фоне терапии Дибикором (n=20, М±σ)
| Параметры | Офисное САД | Офисное ДАД | ЧСС, мин-1 | УО, мл | МОК, л |
| До лечения | 133,4±13,8 | 65±10,1 | 72,92±19,8 | 62±18,5 | 4,52±1,9 |
| 2-я неделя | 130,1 ±11,2 | 65±12,2 | 69,76±14,3 | 57,7±17,2 | 4,02±1,5 |
| 4-я неделя | 123,5±11,3* | 62±10 | 74,3±15,2 | 57,2±15,6 | 4,37±1,5 |
*достоверное различие с показателем до лечения с р<0,05.
Анализ СМАД (табл. 3) показал, что через 4 нед лечения достоверно снизилось среднее суточное САД на 8% (с 131,5±15,2 до 121±14,3 мм рт. ст.), причем более выражено было снижение среднего ночного САД - на 8,5% (с 122,5±16,4 до 112,2±12,2 мм рт. ст.), чем среднего дневного САД - на 6% (с 135,3± 13,6 до 127,2±15,3 мм рт. ст.).
Таблица 3
Динамика АД при проведении СМАД у подростков с АГ 1-й степени на фоне терапии Дибикором (n=20, М±σ)
| Параметры | САД сут | САД день | САД ночь | ДАД сут | ДАД день | ДАД ночь |
| До лечения | 131,5±15,2 | 135,3±13,6 | 122,5±16,4 | 65,2±8,43 | 69,7±9,8 | 61,3±10,6 |
| 2-я неделя | 127,2±13,2 | 131,1 ±15,1 | 119,3±12,6 | 61,3±9,34 | 63,8±8,2 | 59,1±9,5 |
| 4-я неделя | 121 ±14,3* | 127,2±15,3* | 112,2±12,2* | 60,17±8,34 | 62,9±10,2 | 57,3±7,2 |
*достоверное различие с показателем до лечения с р<0,05.
Средние значения ДАД (суточного, дневного и ночного) на фоне терапии дибикором имели тенденцию к уменьшению, но эти изменения были статистически недостоверны.
Проведенный анализ результатов СМАД (табл. 4), показал, что на фоне терапии дибикором на 2-й неделе достоверно снизился индекс времени (ИВ) для САД (с 54±8,1 до 35,2±7,6%). Таким образом, на 2-й неделе лечения уменьшилась систолическая нагрузка давлением. Через 4 нед лечения ИВ САД достоверно снизился до 15,4±4,9%.
Таблица 4
Динамика параметров СМАД у подростков с АГ 1-й степени на фоне терапии Дибикором (n=20, М±σ)
| Параметры | ИВ САД | ИВ ДАД | СИ САД | СИ ДАД | КВ САД |
| До лечения | 54±8,1 | 26,2±7,3 | 5,9±0,84 | 11,4±1,36 | 18,1±1,6 |
| 2-я неделя | 35,2±7,6* | 19,3±6,8 | 15,5±2,17* | 14,6±1,7 | 13,3±1,8* |
| 4-я неделя | 15,4±4,9* | 15,5±2,3 | 16,3±2,4* | 11,1±1,2 | 11,4±2,1* |
*достоверное различие с показателем до лечения с р<0,05.
Важным, на наш взгляд, является нормализация суточного профиля АД. Если до начала лечения большинство подростков были отнесены к группе non-dipper по величине суточного индекса - СИ (5,9%), то уже через 2 нед терапии дибикором степень ночного снижения АД превысила 10% для САД (15,5±2,17%) и сохранилась на 4-й неделе терапии (16,3±2,4%).
Под влиянием терапии дибикором наблюдалось достоверное снижение вариабельности АД. Коэффициент вариации (КВ) для САД уменьшился через 2 нед лечения на 26,5% по сравнению с исходным значением (с 18,1±1,6 до 13,3± 1,8%). Через 4 нед терапии вариабельность САД уменьшилась на 37% по сравнению с исходной величиной.
Достоверное снижение среднесуточной величины АТ (табл. 5) на 22% наблюдалось через 2 нед терапии (с65,2±16,2 до 50,8±15,7 ЕД.). Через 4 нед терапии дибикором АТ уменьшился на 29% по сравнению с исходными параметрами (до 46,2±13,8 ЕД.).
Таблица 5
Динамика величины АТ у подростков с АГ 1-й степени на фоне терапии Дибикором (n=20, М±σ)
| Параметры | АТ сут | АТ день | АТ ночь | СИ АТ |
| До лечения | 65,2±16,2 | 66,95±17,2 | 61,86±15,5 | 7,6±1,1 |
| 2-я неделя | 50,8±15,7* | 53±16,3* | 48±14,3* | 9,4±0,9 |
| 4-я неделя | 46,2±13,8* | 50,4±16,2* | 38,5±12,5* | 23,5±2,3* |
*достоверное различие с показателем до лечения с р<0,05.
Проводимая терапия не только уменьшила величину АТ, но и нормализовала суточный профиль АТ, который приобрел «двухфазный» вид (рис. 3). Кроме того, до лечения у подростков с АГ 1-й степени отмечалось снижение АТ в ночное время лишь на 7,6%, а после 4 недель терапии ночное снижение АТ достигло 23,5%.
Рис. 3. Суточный профиль АТ у подростков с АГ 1-й степени на фоне терапии Дибикором.
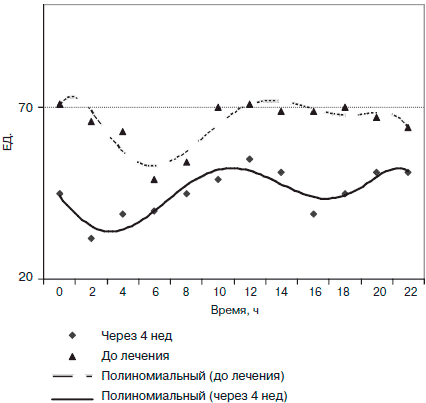
Оценка влияния дибикора на уровень тревожности подростков с 1-й степенью АГ показала (табл. 6), что через 2 нед терапии уровень реактивной тревожности уменьшился в среднем на 23% от исходного значения (с 44,2±7,5 до 34±6,35 ЕД.) и сохранялся на этом уровне до окончания терапии. Уровень личностной тревожности (по шкале Спилбергера) не изменился на протяжении всего курса фармакотерапии.
Таблица 6
Влияние терапии Дибикором на уровень тревожности подростков с АГ 1-й степени (n=65, М±σ)
| Параметры | До лечения | 2-я неделя | 4-я неделя |
| Личностная тревожность | 44,2±9,1 | 43,67±9,7 | 44,46±9,6 |
| Реактивная тревожность | 44,2±7,5 | 34±6,35* | 32,53±6,4* |
*достоверное различие с показателем до лечения с р<0,05.
Обсуждение результатов
Проведенное нами исследование подтвердило наличие гипотензивного эффекта у таурина (препарат Дибикор), как ранее было показано И.В.Захаровым у взрослых [20, 21]. 4-недельная терапия Дибикором АГ 1-й степени у подростков достоверно снизила величину среднего суточного, среднего дневного и среднего ночного САД.
Нами было показано, что раньше, чем произошло достоверное снижение АД (на 4-й неделе терапии), уже через 2 нед терапии дибикором наблюдалось достоверное снижение ИВ для САД. Таким образом, уже через 2 нед терапии дибикором уменьшилась систолическая нагрузка давлением. В это же время наблюдалась и нормализация суточного профиля АД. Если до начала лечения подростки были отнесены к группе non-dipper по величине СИ САД (5,9%), то уже через 2 нед терапии дибикором средняя степень ночного снижения САД составила 15,5%.
У подростков с АГ наблюдается повышенная вариабельность АД, в отличие от здоровых детей, что является неблагоприятным фактором [23]. В нашем исследовании под влиянием терапии дибикором наблюдалось снижение вариабельности АД. КВ для САД уменьшился через 2 нед лечения на 27,7% по сравнению с исходным значением.
Вероятнее всего, гемодинамической основой снижения АД у подростков с АГ 1-й степени на фоне терапии дибикором было уменьшение АТ, так как препарат не оказывал влияния на показатели УО и МОК. Снижение АТ на 22% наблюдалось уже через 2 нед терапии, а через 4 нед терапии дибикором АТ уменьшился на 29% по сравнению с исходными параметрами.
По данным И.ВЛеонтьевой (2002 г.) для подростков с АГ характерен высокий уровень как реактивной, так и личностной тревожности по тесту Спилбергера [24]. В нашем исследовании мы получили подобные результаты, а также показали, что уже через 2 нед терапии Дибикором уровень реактивной тревожности уменьшился в среднем на 23% от исходного значения. Это обстоятельство нам представляется важным: так как величина АД у подростков с АГ прямо коррелирует с уровнем тревожности [24], то уменьшение реактивной тревожности на фоне терапии дибикором может быть важным дополнительным вкладом в гипотензивный эффект препарата. Можно предположить, что применение дибикора будет особенно эффективным у подростков с АГ и высоким уровнем тревожности.
Выводы
4-недельная терапия АГ I у подростков Дибикором в дозе 750 мг в сутки внутрь в три приема привела к снижению среднего суточного, среднего дневного и среднего ночного САД.
Терапия Дибикором через 2 нед привела к снижению гипертонической нагрузки САД в течение суток (снижение ИВ САД), нормализовала суточный профиль САД (СИ САД) и уменьшила вариабельность САД по данным СМАД.
Дибикор уменьшает тонус артерий уже через 2 нед терапии.
Применение Дибикора у подростков с АГ 1-й степени снижает уровень реактивной тревожности.
Сведения об авторах
Ледяев Михаил Яковлевич - д-р мед. наук, проф., зав. каф. детских болезней ГБОУ ВПО ВГМУ Минздравсоцразвития РФ.
Жукова ВБ. - аспирант кафедры детских болезней ГБОУ ВПО ВГМУ Минздравсоцразвития РФ
Ананьева ЯА - аспирант кафедры детских болезней ГБОУ ВПО ВГМУ Минздравсоцразвития РФ
ЛИТЕРАТУРА
1. Бугун О.В., Рычкова Л.В., Долгих В.В. Двадцатичетырехчасовое мониторирование артериального давления в диагностике эссенциальной артериальной гипертензии в детском возрасте. Бюл. СО РАМН. 2003; 3 (108): 49-53.
2. Brady TM, Feld LG. Pediatric approach to hypertension. Semin Nephrol 2009; 29 (4): 3 79-88.
3. Flynn JT. Pediatric hypertension: recent trends and accomplishments, future challenges. Am J Hypertens 2008; 21 (6): 605-12.
4. Александров АА, Розанов ВБ. Профилактика артериальной гипертензии с детства: подходы, проблемы, перспективы. Кардиоваск. терапия и профилактика. 2004; 3:5-9.
5. Rosner B, Cook N, Portman R et al Blood Pressure Differences by Ethnic Group Among United States Children and Adolescents. Hypertension 2009; 54:502-8.
6. Harrabi I, Belarbia A, Gaha R et al. Epidemiology of hypertension among a population of school children in Sousse. Tunisia, Can J Cardiol 2006; 22 (3): 212-6.
7. Jackson LV, Thalange NKS, Cole TJ. Blood pressure centiles for Great Britain. Arch Dis Child 2007; 92:298-303.
8. Ледяев МЯ. Суточное мониторирование артериального давления в педиатрии. Метод. реком. Волгоград, 1998; 20.
9. Петров ВИ, Ледяев МЯ. Артериальная гипертензия у детей и подростков: Современные методы диагностики, фармакотерапии и профилактики. Волгоград, 1999; 146.
10. Петров ВИ., Ледяев МЯ. Оценка суточного ритма артериального давления у детей Н.Новгород, 2006; 78.
11. Soergel M, Kirschstein M, Busch C et al. Oscillometric twenty-four-hour ambulatory blood pressure values in healthy children and adolescents: a multicenter trial including 1141 subjects.J Pediatr 1997:130 (2): 178-84.
12. Диагностика, лечение и профилактика артериальной гипертензии у детей и подростков (второй пересмотр)
13. National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents. The fourth report on the diagnosis, evaluation, and treatment of high blood pressure in children and adolescents. Pediatrics 2004; 114 (Suppl 2): 555-76.
14. National Institutes of Health, National Heart, Lung and Blood Institute, National High Blood Pressure Program. The seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure. Report No. 04-5230. 2004.
15. Петров ВИ., Гурбанов КГ. Изучение кардио- и гемодинамических эффектов нейроактивных аминокислот. Фармакология и клиническое применение нейроактивных аминокислот и их аналогов: сб. науч. тр. Волгоград: ВгМИ, 1985; 37 (5): 21-8.
16. Serrano Ml, Serrano JS, Fernandez A et al. GABA (B) receptors and opioid mechanisms involved in homotaurine-induced analgesia. Gen Pharmacol 1998; 30 (3): 411 -5.
17. Huxtable R. Taurine in the central nervous system and the mammalian actions of taurine. Prog Neurobiol 1989; 32:471-533.
18. Paakkari P, Paakkari I, Karppanen H et al. Mechanisms of the inhibitory cardiovascular effects of taurine and homotaurine Acta Med Scand 1983; 214 (Suppl. 667): 134-7.
19. Bousquet P, Feldman f, Block R, Schwartz J TAG antagonises the central cardiovascular effects of taurine. European J Pharmacol 1984; 98 (2): 269-73.
20. Захаров ИВ. Артериальная гипертензия в акушерской практике: возможности коррекции психофармакологическими средствами. Вестн. ВолГМУ. 2006; 4 (20): 59-61.
21. Захаров ИВ. Эпидемиология и особенности терапии эссенциальной гипертензии у беременных. Вестн. ВолГМУ. 2006; 2 (18); 65-6.
22. Практикум по общей экспериментальной и прикладной психологии. Под ред. А.А.Крылова, С.А.Маничева. СПб. 2000; 560.
23. Лебедькова С.Е., Чулис Т.М., Суменко ВВ. и др. Суточный ритм артериального давления у подростков с артериальной гипертензией. Рос. педиатр. журн. 2003; 2:25-30.
24. Леонтьева И.В. Современное состояние проблем диагностики, лечения и профилактики первичной артериальной гипертонии у детей и подростков. Рос. вестн. перинатологии и педиатрии. 2002; 1:38-45.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru





