Применение Дибикора у больных с сахарным диабетом 2-го типа и метаболическим синдромом
Статьи
Опубликовано в журнале:
«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ»; ТОМ 18; № 28; 2010; стр. 1-4.
Профессор Н.В. Ворохобина, к.м.н. А.В. Кузнецова
ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования федерального агентства по здравоохранению и социальному развитию»
В 2000 г во всем мире насчитывалось более 171 млн больных с сахарным диабетом (СД) 2-го типа, что составляет 85-90% от общего количества больных с СД. Согласно прогнозам ВОЗ, к 2030 г число больных диабетом увеличится более чем вдвое и достигнет 350 млн человек. Эти прогнозы относятся к популяции взрослых лиц в возрасте от 35 до 64 лет. Однако в связи с глобальным старением населения большинства стран мира, ожидаемым в ближайшие десятилетия, доля взрослых лиц в возрасте 65 лет и старше значительно возрастет. Таким образом, реальное число больных СД 2-го типа в 2030 г. может быть намного больше [1].
В настоящее время жесткий гликемический контроль рассматривается как основная мера профилактики развития и прогрессирования микрососудистых осложнений у пациентов с СД 2-го типа. Крупное международное исследование UKPDS убедительно показало, что на каждый 1% снижения уровня гликозилированного гемоглобина (HbA1c) риск микрососудистых осложнений уменьшался на 25-30%. Тем не менее интенсивное лечение СД 2-го типа не приводило к снижению риска макрососудистых событий (инсульт, инфаркт миокарда, потребность в реваскуляризации) и к достоверному снижению общей смертности [2].
Известно, что фактором риска развития СД 2-го типа и независимым предиктором сердечно-сосудистых заболеваний является метаболический синдром (МС). В классическом варианте МС представляет собой сочетание артериальной гипертензии, абдоминального ожирения, атерогенной дислипидемии, нарушения углеводного обмена. Атерогенный липидный профиль, или «атерогенная триада», характеризуется высокой концентрацией триглицеридов (ТГ), незначительным повышением уровня холестерина липопротеидов низкой плотности (ХС ЛПНП), низким уровнем холестерина липопротеидов высокой плотности (ХС ЛПВП) [3].
Наряду с классическими компонентами при МС выявляются «вторичные» признаки: увеличение уровня С-реактивного белка (СРБ) и других воспалительных цитокинов, гиперурикемия и нарушение системы гемостаза [4].
Основой лечения СД 2-го типа в настоящее время являются диетотерапия в сочетании с оптимальной физической нагрузкой и коррекция гипергликемии пероральными сахароснижающими препаратами, обладающими широким спектром действия. Кроме того, в комплексной терапии СД 2-го типа представляется патогенетически обоснованным применение препаратов с антиоксидантными свойствами, способных замедлять прогрессирование сосудистых осложнений, оказывать протекторное действие на β-клетки поджелудочной железы и ослаблять инсулинорезистентность (ИР), обеспечивая лучшую компенсацию СД без риска развития гипогликемий [5]. В последнее время активно обсуждается вопрос использования в комбинированной терапии СД 2-го типа таурина (Дибикор®).
Таурин - аминоэтансульфоновая кислота, которая образуется в организме при ферментативном окислении метионина с участием цистеиндиоксигеназы до цистеинсульфиновой кислоты с последующим ее декарбоксилированием в гипотаурин и окислением гипотаурина в таурин. В организме человека таурин присутствует в больших количествах в мозге, сетчатке, лейкоцитах, миокарде и других органах и тканях. Содержание его в теле здорового человека составляет 0,1 г на 1 кг массы тела. При отсутствии патологии экзогенно вводимый таурин не проявляет своих биологических эффектов. При стрессовых ситуациях, ишемии, радиационном облучении концентрация таурина снижается, и только тогда можно наблюдать его эффекты [6,7].
Биологическое действие таурина, открытого в начале XIX в., долгое время оставалось неясным. В последнее время установлено, что в мозге таурин играет роль нейромедиаторной аминокислоты, тормозящей синаптическую передачу, обладает противосудорожной активностью, стимулирует репаративные процессы при дистрофических заболеваниях сетчатки, обладает кардиотропным эффектом.
К наиболее важным физиологическим эффектам таурина относятся образование желчных кислот, экскреция холестерина, влияние на внутриклеточное осмотическое давление и регуляцию клеточного объема, ингибирование фосфорилирования белков, регуляция натрий-кальциевого обмена. Кроме того, таурин оказывает антиоксидантное действие за счет удаления свободных радикалов, противовоспалительный эффект, связанный с образованием производного тауринмонохлорамина, под влиянием которого значительно снижается продукция многих цитокинов, вызывает ингибирование апоптоза [8-13,18,19].
Многочисленные данные о биологических эффектах таурина были получены в экспериментальных исследованиях с использованием высоких доз таурина (от 200 до 500 мг/кг) [5]. Гипогликемический эффект таурина впервые был выявлен в 1935 г. Askerman D. и Heisen H.A. [14,20]. Впоследствии разными исследователями показано, что таурин повышает поглощение глюкозы в лейкоцитах и накопление гликогена в печени и диафрагме крыс, потенцирует эффекты инсулина, влияя на активность фосфорилазы и гликогенсинтетазы [15,16,18].
Хорошо известно значение активации полиолового пути окисления глюкозы в патогенезе диабетической ретинопатии, нейропатии и нефропатии. Внутриклеточное накопление сорбитола ведет к осмотическому стрессу и усугублению окислительного стресса. Исходом избыточного образования сорбитола в условиях гипергликемии является снижение содержания таурина, что может усугублять клеточную и сосудистую дисфункцию при СД. Эти нарушения связаны с дисрегуляцией клеточного объема, недостаточным удалением свободных радикалов, усилением гликирования белков, что приводит к повышению агрегации тромбоцитов, нарушению иммунного ответа [5,20]. На сегодняшний день существует достаточное количество клинических исследований, отражающих возможности использования таурина у больных с разнообразной патологией, в том числе у больных с СД.
Целью настоящего исследования была оценка эффективности таурина (Дибикор®, ПИК-ФАРМА, Россия) в составе комплексной терапии у больных с СД 2-го типа и МС.
Критерии включения:
1. Мужчины и женщины с СД 2-го типа, получающие стабильную антидиабетическую терапию сахароснижающими пероральными препаратами, которая не менялась в течение 3 последних месяцев.
2. Индекс массы тела (ИМТ) ≥ 30 кг/м2.
3. Окружность талии (ОТ) >80 см у женщин и > 94 см у мужчин.
4. Желание пациента принять участие в клиническом исследовании и выполнять требования протокола.
Критерии исключения:
1. Известная повышенная чувствительность к таурину.
2. Сахарный диабет 1-го типа.
3. Неконтролируемая артериальная гипертензия.
4. Коронарная недостаточность: нарушения ритма сердца, хроническая стабильная стенокардия IV ФК, нестабильная стенокардия, острый инфаркт миокарда (менее чем 3 мес. назад).
5. Участие в исследовании любого нового лекарственного препарата в пределах последних 30 дней.
6. Психические расстройства, которые могут повлиять на комплайентность больного.
7. Клинически выраженная печеночная и почечная недостаточность.
8. Беременность, лактация.
9. Алкоголизм.
Материалы и методы
В открытое сравнительное рандомизированное исследование были включены 40 пациентов с СД 2-го типа и МС (13 мужчин и 27 женщин), средний возраст 60,2±1,3 года.
Для подтверждения диагноза МС использовали определение международной федерации по изучению СД (табл. 1).
Таблица 1
Определение метаболического синдрома Международной федерации по изучению сахарного диабета (IDF Consensus, 2005)
|
Абдоминальное ожирение
(Waist circumference) |
М > 94 см
Ж > 80 см |
|
Плюс 2 любых признака из приведенных ниже |
| ТГ (или факт лечения гипер-ТГ) | ≥ 1,7 ммоль/л |
| ХС ЛПВП | М < 0,9 ммоль/л
Ж < 1,1 ммоль/л |
| АД (или факт лечения АГ) | ≥ 130 ≥ 85 мм рт.ст. |
| Уровень гликемии натощак | ≥ 5,6 ммоль/л |
Все пациенты методом случайной выборки были распределены на 2 группы: основную (20 человек) и контрольную (20 человек). Пациенты основной группы получали Дибикор® в течение 3 мес. по 0,5 г 2 раза/сут. за 20 мин до еды.
Пациенты обеих групп принимали метформин от 850 до 2550 мг/сут. в сочетании с препаратами сульфонилмочевины (манинил, диабетон, амарил). Все пациенты продолжали принимать антигипертензивную (ингибиторы АПФ, селективные β-адреноблокаторы, блокаторы кальциевых каналов) и антиагрегантную терапию в предшествующих включению в исследование дозах, которые не менялись во время всего периода наблюдения.
В начале исследования и через 3 мес. наблюдения оценивались масса тела, ИМТ, ОТ, окружность бедер (ОБ), соотношение ОТ/ОБ, уровень систолического АД (САД) и диастолического АД (ДАД). Состояние углеводного обмена определяли по уровню HbA1c, гликемии натощак (ГН). Липидный спектр исследовали в динамике по уровню холестерина ХС, ТГ, ХС ЛПНП, ХС ЛПВП. Проводилась оценка параметров биохимического анализа крови: билирубина, АСТ, АЛТ, амилазы, липазы, щелочной фосфатазы (ЩФ), мочевой кислоты, креатинина, мочевины, калия, натрия.
Для обработки данных использовали непараметрические критерии Манна - Уитни и Вилкоксона.
Результаты исследования
Группы были сопоставимы по возрасту, длительности СД 2-го типа и артериальной гипертензии (АГ), ИМТ, уровню HbA1c (табл. 2).
Таблица 2
Характеристика больных
|
Группа |
Параметры | | |
| Возраст, лет | Длительность СД, лет | Длительность АГ, лет | ИМТ, кг/м2 | НЬА1с, % |
| Основная, n=20 | 58,4±1,79 | 7,2±1,06 | 8,2±1,02 | 33,3±0,69 | 8,4±0,22 |
| Контрольная, n=20 | 62,0±1,82 | 9,5±0,79 | 7,58±0,80 | 34,1±0,55 | 8,3±0,12 |
Через 3 мес. приема Дибикора® у больных основной группы выявлено статистически значимое снижение ИМТ, ОТ, ОБ и соотношения ОТ/ОБ. В контрольной группе через 3 мес. наблюдалось достоверное увеличение (p=0,027) ИМТ, при этом соотношение ОТ/ОБ не изменилось (табл. 3).
Таблица 3
Динамика антропометрических показателей у больных основной и контрольной групп
|
Показатель |
Основная группа, n=20 |
Контрольная группа, n=20 |
| До исследования | Через 3 мес. | p | До исследования | Через 3 мес. | p |
| ИМТ, кг/м2 | 33,3±0,69 | 32,6±0,69 | 0,0002 | 34,1±0,55 | 34,3±0,53 | 0,027 |
| ОТ, см | 97,9±1,50 | 96,2±1,46 | 0,0002 | 99,2±1,09 | 99,5±0,95 | 0,11 |
| ОБ, см | 103,3±1,93 | 102,6±1,90 | 0,041 | 103,7±1,10 | 100,8±2,6 | 0,37 |
| ОТ/ОБ | 0,95±0,01 | 0,93±0,01 | 0,001 | 0,96±0,01 | 0,96±0,01 | 1,0 |
Параллельно со снижением массы тела у больных, получавших Дибикор®, улучшились показатели углеводного обмена (ГН, HbA1c), отмечалась незначительная положительная динамика по уровню СП (С-пептида). У здоровых людей базальный уровень C-пептида в сыворотке (т. е. уровень C-пептида натощак) составляет 0,1-1,22 нмоль/л. Такое влияние Дибикора® на углеводный обмен может иметь позитивное прогностическое значение, поскольку имеются сведения об уменьшении под воздействием таурина процессов апоптоза эндотелиальных клеток, через уменьшение образования активных форм кислорода [21]. В группе контроля уровень HbA1c не изменился, а снижение уровня ГН и СП было недостоверным (табл. 4, рис. 1).
Таблица 4
Динамика показателей углеводного обмена у больных основной и контрольной групп
|
Показатель |
Основная группа, n=20 |
Контрольная группа, n=20 |
| До исследования | Через 3 мес. | p | До исследования | Через 3 мес. | p |
| Гликемия натощак, ммоль/л | 8,9±0,33 | 7,2±0,24 | 0,00004 | 8,7±0,16 | 8,2±0,20 | 0,169 |
| СП, нмоль/л | 0,7±0,01 | 1,2±0,39 | - | 0,8±0,02 | 0,7±0,03 | - |
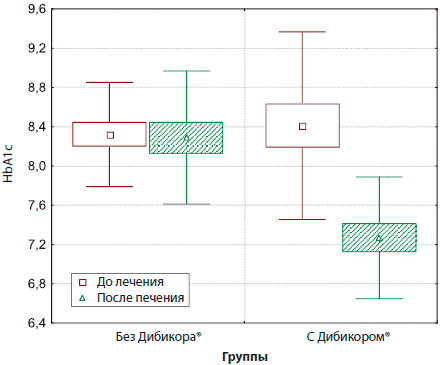
Рис. 1. Динамика уровня гликозилированного гемоглобина у больных основной и контрольной групп
Через 3 мес. приема Дибикора® у больных основной группы наблюдались изменения липидного спектра: достоверно понизился уровень ХС, ТГ, ХС ЛПНП (p=0,01). Изменений со стороны ХС ЛПВП не наблюдалось, но их уровень находился в пределах нормальных значений. У больных контрольной группы выявлено достоверное увеличение уровня ХС (p=0,024), другие показатели липидного спектра существенно не изменились (табл. 5).
Таблица 5
Динамика показателей липидного обмена у больных основной и контрольной групп
Показатель | Основная группа, n=20 | Контрольная группа, n=20 |
| До исследования | Через 3 мес. | p | До исследования | Через 3 мес. | p |
| ХС, ммоль/л | 5,6±0,22 | 5,0±0,21 | 0,01 | 6,1±0,08 | 6,3±0,04 | 0,024 |
| ТГ, ммоль/л | 2,67±0,28 | 2,26±0,22 | 0,01 | 3,3±0,20 | 3,4±0,18 | 0,48 |
| ХС ЛПНП, ммоль/л | 3,3±0,19 | 2,9±0,21 | 0,01 | 3,5±0,12 | 3,5±0,11 | 0,211 |
| ХС ЛПВП, ммоль/л | 1,2±0,06 | 1,3±0,06 | 0,181 | 1,0±0,05 | 1,1±0,05 | 1,186 |
В многочисленных исследованиях, посвященных влиянию Дибикора® на сердечно-сосудистую систему, выявлено его положительное воздействие на показатели сократимости миокарда и уровень АД. В нашем исследовании у больных основной группы после 3 мес. приема препарата наблюдалось статистически значимое (p=0,01) снижение уровня САД. Поскольку Дибикор® не является гипотензивным средством, постепенное развитие эффекта, по-видимому, есть результат глубоких изменений на уровне клеточных мембран и влияния на внутриклеточный кальций. В контрольной группе несмотря на то, что большинство больных находилось на гипотензивной терапии, уровень САД практически не изменился (табл. 6).
Таблица 6
Динамика систолического и диастолического АД у больных основной и контрольной групп
Показатель | Основная группа, n=20 | Контрольная группа, n=20 |
| До исследования | Через 3 мес. | p | До исследования | Через 3 мес. | p |
| САД, мм рт.ст. | 143,2±3,63 | 133,9±2,09 | 0,01 | 143,9±2,31 | 143,7±1,91 | 1,0 |
| ДАД, мм рт.ст. | 85,1±1,61 | 83,3±1,01 | 0,343 | 86,8±1,10 | 85,8±1,39 | 0,724 |
За период наблюдения большинство мониторируемых биохимических показателей существенно не изменилось (табл. 7). В основной группе выявлено статистически значимое (p=0,00004) снижение уровня мочевой кислоты (рис. 2). В группе контроля достоверного улучшения не было ни по одному представленному параметру.
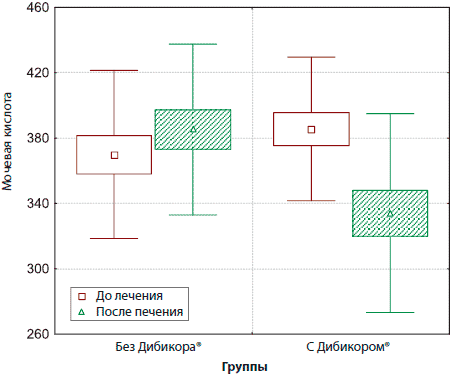
Рис. 2. Динамика уровня мочевой кислоты у больных основной и контрольной групп
Таблица 7
Динамика биохимических показателей у больных основной и контрольной групп
Показатель | Основная группа, n=20 | Контрольная группа, n=20 |
| Изменения | Достоверность | Изменения | Достоверность |
| Билирубин, мкмоль/л | -2,58 | 0,803 | -0,37 | 0,096 |
| АСТ, Е/л | -3,5 | 0,337 | 0,25 | 0,147 |
| АЛТ, Е/л | -6,25 | 0,06 | 0,5 | 0,258 |
| Амилаза, Е/л | 1,42 | 0,332 | -0,21 | 0,332 |
| Липаза, Е/л | 1,79 | 1 | -1 | 0,332 |
| ЩФ, Е/л | -2,26 | 0,359 | -1,6 | 0,579 |
| Мочевина, ммоль/л | -0,75 | 0,066 | -0,14 | 0,08 |
| Креатинин, мкмоль/л | -2,89 | 0,146 | -0,53 | 0,453 |
| Калий, моль/л | -0,23 | 0,239 | -0,05 | 1 |
| Натрий, моль/л | -0,84 | 0,480 | 1 | 0,803 |
Заключение
Таким образом, включение Дибикора® в комплексную терапию СД оказывает позитивное влияние на показатели углеводного и липидного обмена, сопровождается уменьшением массы тела, сопряжено с уменьшением уровня мочевой кислоты. Положительное действие Дибикора® на углеводный обмен у больных с СД 2-го типа и МС может быть связано с его мембрано-протективными и осморегуляторными свойствами, а также с нормализацией кальциевого и калиевого обменов в клетке, что повышает активность ферментов антиоксидантной защиты. Поскольку жесткий гликемический контроль не всегда приводит к снижению риска микро- и макрососудистых осложнений СД, присоединение к стандартной сахароснижающей терапии Дибикора®, обладающего антиоксидантными свойствами, может существенно улучшить прогноз у больных с СД 2-го типа и МС.
Выводы
1. У больных с СД 2-го типа и МС при включении в комплексную терапию Дибикора® по 0,5 г 2 раза/сут. отмечалось снижение ИМТ, уменьшение ОТ и ОБ, а также соотношения ОТ/ОБ.
2. У всех больных снижение массы тела, достигнутое через 3 мес. применения Дибикора®, сопровождалось улучшением показателей углеводного и липидного обмена: достоверным снижением уровня HbA1c, ГН, ХС, ТГ, ХС ЛПНП.
3. Всеми пациентами отмечена хорошая переносимость препарата.
ЛИТЕРАТУРА
1. Wild et al. Diabetes Care 2004;27:1047-53
2. UKPDS 33. Lancet 1998;352:837-53
3. American Diabetes Association. Diabetes Care 2003;26 (Suppl. 1):S83-86
4. Крючкова И.В., Адамчик АС. Возможности коррекции нарушений углеводного обмена при метаболическом синдроме // Российский кардиологический журнал. 2009. Т. 76. №2. С. 44-45.
5. Недосугова Л. В. Место дибикора в комплексной терапии сахарного диабета // ж. Фарматека. 2008. №17. С. 22-23.
6. Елизарова Е.П. Применение Дибикора в кардиологической практике: Пособие для врачей. - М., 2005.
7. Nakagawa K. // Effect of taurine on alteration in adrenal functions induced by stress // Jap. J. Pharmacol. - 1975. - V.25. - H. 737-746.
8. Stratton IM, Adler Al, Neil HA et al. Association of glycaemia with macrovascular and micro vascular complications of type 2 diabetes (UKPDS 35). BMJ 2000; 321:405-412.
9. Palmi M, Youmbi GT, Fusi F, Sgaragli GP, Dixon HB, Frosini M, Tipton KF. Potentiation of mitochondrial Ca2+ sequestration by taurine. Biochem Pharmacol. 1999 Oct 1;58(7):1123-31.
10. El Idrissi A, Trenkner E. Taurine as a modulator of excitatory and inhibitory neurotransmission. Neurochem Res. 2004 Jan;29(1):189-97.
11. Bustamante J, Lobo MV, Alonso FJ, Mukala NT, Gine E, Solis JM, Tamarit-Rodriguez J, Martin Del Rio R. An osmotic-sensitive taurine pool is localized in rat pancreatic islet cells containing glucagon and somatostatin. Am J Physiol Endocrinol Metab. 2001 Dec;281(6):E1275-85.
12. Huxtable RJ. Physiological actions of taurine. Physiol Rev. 1992 Jan;72(1):101-63.
13. Lampson WG, Kramer JH, Schaffer SW. Potentiation of the actions of insulin by taurine. Can J Physiol Pharmacol. 1983 May;61(5):457-63.).
14. Askerman D. И Heisen H.A. J Physiol Chem 1935; 235: 115-21.
15. Докшина ГА, Силаева Т.Ю., Ярцев ЕИ. Некоторые инсулиноподобные эффекты таурина // Вопросы Медицинской Химии. 1976. №22. С. 503-507.
16. Maturo J, Kulakowsky E.C. Insulin-like activeity of taurine. In; The biology of taurine:methods and mechanisms. Huxtable R.J.? Fanconi F., Giotti A. (eds). Plenum Press, New York 1987:217-26.
17. Lampson W.G, Kramer J.N.> Schafter S.W. Potemtiation of the actions of insulin by taurine. Can J Physiol Pharmacol 1983; 61: 457-63.
18. Franconi, et al. Plasma and platelet taurine are reduced in subjects with insulin- dependent diabetes mellitus: effects of taurine supplementation American Journal of Clinical Nutrition, 1995 Vol 61, 1115-1119.
19. Wu Q.D., Wang J.H., Fennessy F. Redmond H.P. Taurine prevents high-glucose-induced human vascular endothelial cell apoptosis. Am J Physiol. 1999 Dec; 277 (6 Pt 1): C 1229-38.
20. Hansen S.H., Andersen M.L, Birkedal H., Cornett C., Wibrand F. The impotant role of taurine in oxidative metabolism/ Adv Exp Med Biol. 2006; 583: 129-35.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru




