Дибикор – эффективное и безопасное средство для лечения сахарного диабета
Статьи
А.М. Мкртумян,
С.В. Подачина,
В.В. Петраченко
Сахарный диабет типа 2 (СД типа 2), составляющий 85-90% от общего количества больных с СД, является серьезной медико-социальной проблемой XXI века. Медицинская и социальная значимость СД типа 2 определяется, прежде всего, его тяжелыми сосудистыми и неврологическими осложнениями, которые приводят к ранней инвалидизации и высокой смертности, сокращением продолжительности и ухудшением качества жизни.
Распространенность заболевания во всем мире непрерывно повышается. Согласно эпидемиологическим прогнозам ожидается увеличение количества больных СД типа 2 со 150 млн (2000 г.) до 225 млн к 2010 году и до 300 млн к 2025 году. Эти данные касаются только случаев диагностированного СД типа 2, в то время как значительное количество случаев в течение длительного времени не диагностируется и не лечится.
Хорошо известно, что СД типа 2 является причиной преждевременной смерти и ранней инвалидизации больных. Вероятность неблагоприятного исхода у больных с СД типа 2 также высока, как у больных ишемической болезни сердца (ИБС) с постинфарктным кардиосклерозом. Главными причинами смерти и инвалидизации у больных СД типа 2 являются сердечнососудистые заболевания, при этом осложнения ИБС занимают среди причин смерти лидирующие позиции. СД типа 2 ускоряет развитие атеросклероза. Так, среди больных СД типа 2 сердечно-сосудистая заболеваемость и смертность в 3 раза выше, чем среди людей того же возраста, не страдающих диабетом. Известно, что примерно 60-75% смертельных исходов у больных СД типа 2 вызваны коронарным атеросклерозом, 10-25% – церебральным и периферическим атеросклерозом. Кроме того, СД типа 2 является важнейшей причиной потери зрения, развития терминальных стадий почечной недостаточности, нетравматических ампутаций. Сосудистые и неврологические осложнения СД, как правило, уже присутствуют у большинства больных к моменту постановки диагноза СД типа 2. Среди больных СД типа 2 распространенность ИБС в 2-4 раза, риск развития острого инфаркта миокарда в 6-10 раз, а мозговых инсультов в 4-7 раз выше, чем среди лиц без диабета. Возрастание сердечно-сосудистого риска у женщин с диабетом выше, чем у мужчин.
Диабет – заболевание, которое достаточно сложно по своей природе. Многообразие препаратов с различными механизмами действия позволяют выбирать оптимальную терапию (в пределах достижений современной науки) для профилактики СД, лечения больных с впервые выявленным заболеванием, ведения больных с большим стажем СД, для профилактики и лечения осложнений.
Современная фармакология предлагает множество препаратов, которые воздействуют на разные механизмы, способствующие снижению уровня глюкозы в крови.
- Препараты, влияющие на снижение абсорбции углеводов в желудочно-кишечном тракте (гуарем, акарбоза).
- Препараты сульфонилмочевины (глибенкламид, гликлазид, глипизид, гликвидон) относятся к секретогенам инсулина. Их действие связано со стимуляцией образования и высвобождения инсулина бетаклетками поджелудочной железы.
- Тиазолидиндионы или сенситайзеры (пиоглитазон, розиглитазон). Они повышают чувствительность периферических тканей к инсулину. Усиливают действие инсулина в скелетных мышцах, жировой ткани и в печени. Снижают уровень глюкозы, липидов и инсулина.
- Бигуанид – метформин (Глюкофаж, Сиофор). Не изменяют секрецию инсулина, не оказывают сахароснижающего эффекта при его отсутствии. В присутствии инсулина увеличивают периферическую утилизацию глюкозы кишечником, что проявляется снижением уровня глюкозы в крови, оттекающей от кишечника, подавляют в печени образование глюкозы путем глюконеогенеза, снижают повышенное содержание инсулина в сыворотке крови у больных с ожирением и с СД типа 2.
- Метаболические препараты:
- альфа-липоевая кислота (Тиогамма) не оказывает сахароснижающего действия;
- бенфотиамин (Мильгамма) не оказывает сахароснижающего действия;
- таурин (Дибикор) сульфоаминокислота обладает сахароснижающим эффектом.
В настоящее время предпочтение отдается комплексной терапии. Современная стратегия лечения СД предполагает достижение оптимального уровня глюкозы и показателей липидного обмена в кратчайшие сроки, т.к. глюкоза и липиды проявляют при повышенной концентрации токсичность, которая может необратимо приводить к макро- и микроангиопатиям, а также поражению самих β-клеток поджелудочной железы. В опубликованном в 2005 г. IDF «Общем руководстве по лечению сахарного диабета типа 2» подчеркивается необходимость поддержания HbA1c на уровне 6,5 или ниже, что сводит к минимуму опасность возникновения сосудистых осложнений диабета. Быстрая компенсация СД уменьшает в дальнейшем вероятность появления осложнений, позволяет иногда сократить дозу самих препаратов. А это желательно, т.к. лекарственные средства имеют побочные эффекты и противопоказания.
Так, например, длительное применение тиазолидиндионов ведет к задержке жидкости, увеличению массы тела за счет подкожного жира. Самые необходимые опробованные препараты последнего поколения сульфонилмочевины, от которых практически невозможно отказаться, при длительном применении приводят к истощению и апоптозу β-клеток. Метформин, способствующий уменьшению инсулинорезистентности, также имеет противопоказания и побочные эффекты. Существуют больные с индивидуальной непереносимостью к метформину. На повестке дня всегда стоял вопрос создания безопасных и эффективных средств многофакторного действия для лечения хронических заболеваний, в частности сахарного диабета. Дибикор (таурин) является продуктом окисления серусодержащих аминокислот. В его показаниях сахарный диабет типа 1 и 2, хроническая сердечная недостаточность и интоксикация, вызванная сердечными гликозидами. По своим эффектам препарат напоминает метформин, но он обладает действиями, не свойственными метформину. Дибикор уменьшает инсулинорезистентность, снижает уровень сахара в крови при гипергликемии и не влияет при нормальной концентрации глюкозы в крови. Дибикор нормализует обмен жиров: понижает общий холестерин и триглицериды (одиниз главных поражающих факторов при СД типа 2). Достоинством препарата Дибикор является отсутствие противопоказаний и побочных эффектов. Препарат совместим абсолютно со всеми средствами, которые используются для лечения СД. Его защитное действие направлено на сердце, сетчатку, печень и клетки крови. Добавление Дибикора к комплексной терапии способствует лучшей компенсации СД. В отечественной (11, 12, 13) и зарубежной (19) литературе уже появлялись сообщения об эффектах Дибикора и таурина при СД типа 2 и у пациентов с избыточной массой тела (14). Учитывая широкое применение метформина в клинической практике, наличие у части больных побочных эффектов препарата, уникальные свойства таурина, обладающего многофакторным влиянием на больной организм нами была поставлена цель: изучить эффективность и безопасность комбинированного применения Дибикора и метформина у больных сахарным диабетом типа 2, не получавших в прошлом бигуанид и таурин.
Дизайн исследования: открытое рандомизированное сравнительное исследование
Материалы и методы. В исследование было включено 45 пациентов с сахарным диабетом типа 2 (мужчины и женщины) в возрасте 42-70 лет, не получавших ранее Дибикор и препараты группы бигуанидов. В процессе рандомизации пациенты были разделены на три группы: в I группе к диетотерапии, либо получаемой сахароснижающей терапии (препараты сульфонилмочевины) был добавлен Дибикор («ПИК-ФАРМА», Россия) в дозе 500 мг 2 раза в сутки; во II группе был добавлен метформин (BAGO, Аргентина) в суточной дозе 1500 мг; в III группе к получаемой терапии была добавлена комбинация Дибикор 500 мг 2 раза в сутки и метформин 1500 мг в сутки. Пациенты всех трех групп были сопоставимы по возрасту, длительности диабета, индексу массы тела, компенсации углеводного обмена (таблица 1).
Таблица 1. Основные характеристики обследуемых пациентов до начала лечения
| Дибикор N = 15 | Метформин N = 15 | Дибикор + Метформин N = 15 | |
|---|
| Возраст (лет) | 56,8±7,39 | 55,0±7,07 | 56,47±7,63 |
| Длительность СД (лет) | 2,93±1,33 | 3,27±3,61 | 3,93±3,04 |
| Рост (см) | 162,07±5,09 | 164,07±9,63 | 164,13±8,25 |
| Вес (кг) | 101,24±15,40 | 103,22+19,78 | 101,52±15,90 |
| ИМТ (кг/м²) | 38,44±4,91 | 38,17±5,97 | 37,86±7,12 |
| HbA1c (%) | 8,55±0,92 | 8,76±1,48 | 8,75±1,25 |
| ИРИ, мкЕд/мл | 13,48±6,39 | 15,0±5,29 | 15,41±6,19 |
Кроме сахароснижающей терапии пациенты обеих групп получали антигипертензивную терапию при наличии показаний. Все пациенты получили рекомендации по коррекции диеты и расширению физической активности в рамках индивидуальных или групповых занятий по программе «Школа пациента с избыточной массой тела».
Пациенты всех групп были обследованы до начала лечения и через 3 месяца. Были оценены антропометрические показатели, компенсация углеводного обмена, липидный спектр, уровень лактата.
Результаты исследований. В результате лечения показатели индекса массы тела изменились достоверно (p 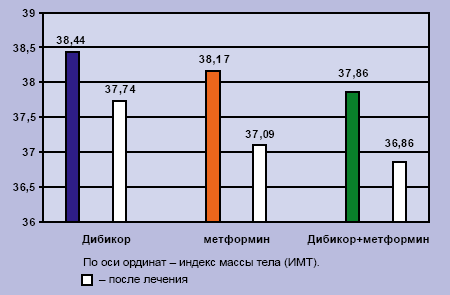
Рисунок 1. Динамика индекса массы тела (ИМТ) под влиянием терапии.
Через три месяца терапии достоверные изменения отношения окружности талии к окружности бедер (от/об) наблюдались только при лечении Дибикором (0,94 ± 0,08 – до лечения; 0,92 ± 0,08 – после, p = 0,02).
Во всех трех группах также улучшился углеводный обмен. Абсолютные изменения HbA1c (разница между показателями до лечения и после лечения) были: группа метформина – 0,71%, группа Дибикора – 0,32%, группа Дибикора + метформин – 0,85%, но достоверных различий между всеми группами при данной выборке (n = 15) не удалось выявить (таблица 2).
Таблица 2. Изменение показателей углеводного обмена
| показатели | Дибикор (n =15) | Метформин (n=15) | Дибикор + Метформин (n=15) |
|---|
| до | После исследования | Разница | р | до | После исследования | Разница | р | До | После исследования | Разница | р |
|---|
| HbA1c, % | 8,55±0,92 | 8,23±0,69 | -0,32 | |
В таблице 1 приведены значения иммунореактивного инсулина (ИРИ) до лечения. Средние цифры для каждой из групп были в пределах нормы (в норме уровень ИРИ сыворотки крови составляет 3-20 мкЕД/ мл). Они не изменились и после курса терапии.
Как видно из рисунка 2, терапия Дибикором, метформином и совместное лечение двумя препаратами уменьшает инсулинорезистентность, но статистически значимые результаты были получены у больных, получавших метформин (5,52±2,38 – до лечения, 3,91±1,30 – после лечения, p = 0,002).
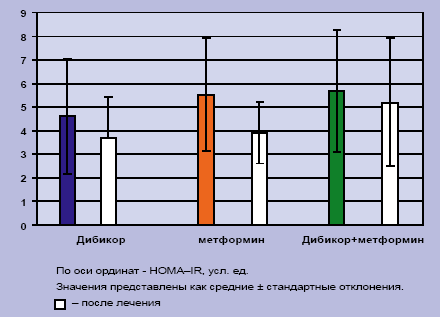
Рисунок 2. Изменение НОМА–IR.
После курса терапии Дибикором и метформином изменился липидный обмен (таблица 3), понизился общий холестерин, данные статистически значимые. На фоне Дибикора с большой степенью достоверности (p= 0,0002) уменьшились триглицериды, уровень их понизился и при метформине, но процесс был недостоверен. В то же самое время на фоне метформина понизился холестерин ЛПНП (p= 0,0025). Тенденция изменения на Дибикоре относительно этого показателя была положительной (3,42 – до лечения, 3,28 – после лечения), но недостоверной (p = 0,07). На метформине (достоверно) и Дибикоре (недостоверно) упал индекс атерогенности *(таблица 3).
Таблица 3. Изменение липидного обмена при лечении Дибикором и метформином
| Показатели | Дибикор n=15 | Метформин n=15 | Дибикор+Метформин n=15 |
|---|
| до | После исследования | Δ | р | До | После исследования | Δ | р | До | После исследования | Δ | р |
|---|
| Холестерин | 6,15±0,94 | 5,81±0,65 | -0,34 | 0,006 | 6,08±1,10 | 5,73±0,73 | -0,35 | 0,012 | 6,5±1,09 | 6,05±0,9 | -0,45 | 0,046 |
| Триглицериды | 2,3±0,76 | 2,09±0,54 | -0,21 | |
Изменений со стороны Хс-ЛПВП не наблюдалось, но надо отметить, что их уровень был в пределах нормальных значений. Совместное применение этих препаратов продемонстрировал еще более выраженный эффект. Общий холестерин снизился достоверно на 0,45 ммоль/л, холестерин ЛПНП – на 0,3 ммоль/л, достоверно повысился холестерин ЛПВП – на 0,15 (с 1,34±0,4 до 1,49±0,42, p = 0,009). Имелась тенденция к снижению уровня триглицеридов (с 2,61±0,77 до 2,45±0,88, p = 0,4). Уменьшился индекс атерогенности на 0,53.
Обсуждение. Дибикор (таурин) и метформин (рисунок 3) относятся к разным химическим соединениям. Таурин – это продукт окисления серусодержащих аминокислот. Метформин – производное гуанидина (относится к аминам).
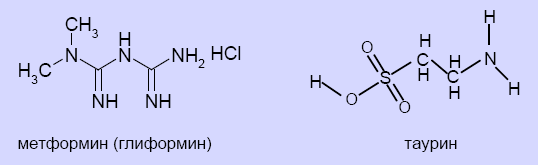
Рисунок 3. Формулы таурина и метформина.
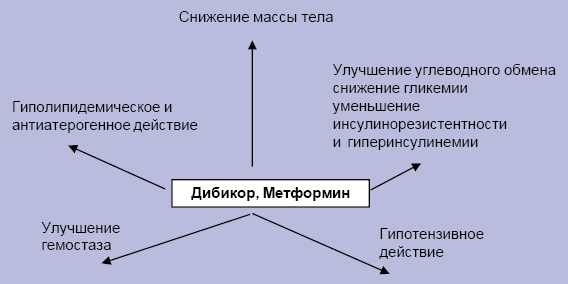
4. Эффекты Дибикора и метформина при лечении больных с СД и метаболическим синдромом.
По совокупности данных действие метформина при СД типа 2 представляет собой не как истинно гипогликемизирующее(сахароснижающее), а как антигипергликемическое средство, т.е. препятствующее повышению гликемии. Это подтверждается и тем, что применение бигуанидов практически не приводит к гипогликемии. В начале статьи о подобном свойстве Дибикора уже говорилось. Удивительно как эти два разных соединения имеют весьма схожие эффекты. Разница между этими двумя веществами состоит в том, что таурин представляет собой естественный метаболит.
В настоящее время метформин – единственный бигуанид, рекомендованный к применению Европейской Группой по разработке тактики ведения СД типа 2 (European NIDDM Policy Group, 1993 г). «Настольное руководство по сахарному диабету 2 типа», изданное Международной Федерацией диабета (IDF) в 1999 г, называет метформин первым в списке рекомендованных к применению пероральных сахароснижающих средств. Метформин признан препаратом первого ряда в консенсусе ADA\EASDЕ, принятый в декабре 2006 года. Если использование метформина при СД насчитывает более двух десятков лет, то таурин и его эффекты известны очень давно. Факты, которые приводятся ниже показывают, на сколько полезным может быть применение таурина с нарушенным обменом углеводов и жиров.
У взрослого человека весом 70 кг содержится около 70 г таурина. У больных сахарным диабетом концентрация таурина снижена (7,15), падает концентрация таурина у пожилых людей по отношению к молодым почти в два раза (8), при травме таурин теряется значительно. Уровень таурина необходимо восстанавливать. Известно, что недостаток его может приводить к кардиопатии, ретинопатии (16, 17, 18) и др. последствиям. При гестационном СД уровень таурина в крови женщин понижен. Таурин, по всей видимости, является ярким маркером измененного метаболизма глюкозы во время беременности у женщин с гестационным диабетом (9).
Таурин также как инсулин обладает гипогликемическими свойствами, участвует в развитии и защите инсулинового аппарата (1, 6), имеет сродство к рецепторам инсулина (5). Если говорить о клинической стороне действия таурина, то он благоприятно воздействует на гемостаз: на агрегацию тромбоцитов и эритроцитов (10, 12), проявляет защитные свойства при невропатии, кардиомиопатии, нефропатии и ретинопатии, защищает бетаклетки при гипергликемии от повреждающего действия супероксида (6). Недавние исследования показали роль таурина в развитии плода, а также в подавлении развития толерантности к глюкозе у ребенка, рожденного от диабетической матери (1, 2, 3, 4). В установленных механизмах таурина – это его эффектыосморегулятора и антиоксидантные свойства.
Не является неожиданным влияние Дибикора на липидный обмен. Участие таурина в метаболизме жиров также известно очень давно. Входя в состав желчных кислот, таурин участвует в дисмульгации и во всасывании жирорастворимых соединений, в том числе и витаминов.
При преимущественном потреблении глицина или таурина с пищей происходит изменение образования в сторону гликохолевой (G) или таурохолевой (T) кислоты. Так, например, если человеку добавлять таурин, соотношение G/T уменьшается. Надо отметить, что свойства кислот не совсем идентичны. При всех равных условиях в печени человека синтез идет с предпочтением таурохолевых кислот. При потреблении таурина значительно увеличивается скорость экскреции желчных кислот и их объем. Глицин не обладает таким эффектом (20). Таким образом, при недостаточности таурина будет страдать выделение желчных кислот. В эксперименте обнаружено, что на холестериновой диете образование холестериновых камней в желчном пузыре достигает 71-100% при дефиците таурина, не происходит образование камней при добавлении в рацион таурина (21).
Выше приведенные данные свидетельствуют о значительном вкладе таурина в обмен веществ и о роли препарата Дибикор в лечении пациентов с СД.
В заключении можно сказать, что присоединение Дибикора к стандартной сахароснижающей терапии и коррекции образа жизни у пациентов с сахарным диабетом типа 2 и ожирением приводит к улучшению показателей компенсации углеводного обмена, липидного спектра, снижению массы тела и к перераспределению жира. Дибикор не обладает побочными явлениями и не увеличивает их риск в сочетании с другими препаратами.
Выводы
- Во всех группах отмечено достоверное снижение массы тела в среднем от 0,7до 1,08 кг, что может быть обусловлено, как воздействием медикаментозных, так и немедикаментозных причин.
- Уровень гликированного гемоглобина достоверно снизился во всех группах, максимально – в группе метформин + Дибикор от 8,75 ±1,25% до 7,90 ± 1,18%, p = 0,05. Также во всех группах достоверно снизился уровень гликемии натощак.
- Достоверных изменений уровня иммунореактивного инсулина в ходе исследования не было выявлено, однако в группе метформина было выявлено достоверное уменьшение показателя HOMA IR с 5,52 ± 2,38 до 3,91 ± 1,30, p = 0,002.
- Во всех группах выявлено улучшение показателей липидного обмена, достигшее максимального в группе метформин + Дибикор (достоверное снижение общего холестерина, ЛПНП, индекса атерогенности и повышение уровня ЛПВП). Уровень холестерина достоверно снизился во всех группах. В группе пациентов, получавших Дибикор, выявлено достоверное снижение уровня триглицеридов с 2,3 ± 0,76 до 2,09 ± 0,54, p = 0,0002.
- В ходе исследования не было выявлено достоверных изменений уровня лактата.
- В группах получавших терапию метформином и метформином совместно с Дибикором отмечались жалобы на наличие побочных эффектов, характерных для метформина (метеоризм, вздутие живота, неустойчивость стула), однако эти жалобы не послужили причиной отказа от лечения, достоверных различий в частоте побочных эффектов в группах не выявлено. Переносимость Дибикора была хорошей, не было отмечено случаев непереносимости.
- Эффекты Дибикора и метформина при лечении больных с СД и метаболическим синдромом.
Список литературы:
- Remacle C., Dumortier O., Bol V., Goosse K., Romanus P., Theys N., Bouckenooghe T., Reusens B. Intrauterine programming of the endocrine pancreas. Diabetes Obes Metab. 2007 Nov; 9 Suppl 2: 196 – 209.
- Hultman K., Alexanderson C., Mannerеs L., Sandberg M., Holmдng A., Jansson T. Maternal taurine supplementation in the late pregnant rat stimulates postnatal growth and induces obesity and insulin resistance in adult offspring. J Physiol. 2007 Mar 15; 579 (Pt 3): 823-33. Epub 2007, Jan 4.
- Lee Y.Y., Park K.S., Pak Y.K., Lee H.K. The role of mitochondrial DNA in the development of type 2 diabetes caused by fetal malnutrition. J Nutr Biochem. 2005 – Apr; 16(4): 195 – 204.
- Aerts L., Van Assche F.A. Taurine and taurinedeficiency in the perinatal period. J Perinat Med. 2002; 30(4): 281 – 6.
- Maturo J., Kulakowski E.C. Taurine binding to the purified insulin receptor. Biochem Pharmacol. 1988 – Oct 1; 37(19): 3755 – 60.
- Tang C., Han P., Oprescu A.I., Lee S.C., Gyulkhandanyan A.V., Chan G.N., Wheeler M.B., Giacca A. Evidence for a role of superoxide generation in glucose-induced beta-cell dysfunction in vivo. Diabetes. 2007 – Nov; 56(11):2722 – 31. Epub 2007 – Aug 6.
- De Luca G., Calpona P.R., Caponetti A., Romano G., Di Benedetto A., Cucinotta D., Di Giorgio R.M. Taurine and osmoregulation: platelet taurine content, uptake, and release in type 2 diabetic patients. Metabolism. 2001 – Jan; 50(1): 60 – 4.
- Jeevanandam M , Young D H., Ramias L, Schiller W. R. Effect of major trauma on plasma free amino acid concentrations in geriatric patients. Am J Clin Nutr. 1990 – Jun; 51(6): 1040 – 5.
- Seghieri G., Tesi F., Bianchi L., Loizzo A., Saccomanni G., Ghirlanda G., Anichini R., Franconi F. Taurine in women with a history of gestational diabetes. Diabetes Res Clin Pract. 2006 – Sep 19.
- Кахновский И.М., Королева Е.В., Захарченко В.Н., Ларионов С.М.. ММА им. И.М.Сеченова. Таурин в лечении сахарного диабета. Клиническая фармакология и терапия, 1997; 6, 3. Опыт применения Дибикора при сахарном диабете 2 типа.
- М.В. Шестакова, Л.А. Чугунова, М.Ш. Шамхалова М.Ш.. Журнал «Сахарный диабет» – 2007 – № 1.
- Elizarova E.P., Nedosugova L.V. First experiments in taurine administration for diabetes mellitus. The effect on erythrocyte membranes. Adv Exp Med Biol. 1996; 403: 583 – 8.
- Кудинов В.И., Золотарева И.В., Корсун Н.А., Цхяева А.А., Шульга Ю.В., Волкова Т.В., Рудакова Ю.А. Изучение клинической эффективности Дибикора при сахарном диабете 2 типа. Тезисы XIV Конгресса «Человек и лекарство».
- Zhang M., Bi L.F., Fang J.H., Su X.L., Da G.L., Kuwamori T., Kagamimori S. Beneficial effects of taurine on serum lipids in overweight or obese non-diabetic subjects. Am J Clin Nutr. 1990 Jun; 51(6): 1040 – 5.
- Merheb M., Daher R.T., Nasrallah M., Sabra R., Ziyadeh F.N., Barada K., Pop-Busui R., Sullivan K.A., Van Huysen C., Bayer L., Cao X., Towns R., Stevens M.J. Taurine intestinal absorption and renal excretion test in diabetic patients: a pilot study. Diabetes Care. 2007 – Oct.;30(10): 2652 – 4.
- Pop-Busui R, Sullivan KA, Van Huysen C, Bayer L, Cao X, Towns R, Stevens MJ. Depletion of taurine in experimental diabetic neuropathy: implications for nerve metabolic, vascular, and functional deficits. Exp Neurol 168: 259 – 272, 2001.
- Ha H., Yu M.R., Kim K.H: Melatonin and taurine reduce early glomerulopathy in diabetic rats. Free Radic Biol Med 26: 944 – 950, 1999.
- Vilchis C., Salceda R.: Effect of diabetes on levels and uptake of putative amino acid neurotransmitters in rat retina and retinal pigment epithelium. Neurochem Res 21: 1167 – 1171, 1996.
- Chauncey K.B., Tenner T.E. Jr., Lombardini J.B., Jones B.G., Brooks M.L., Warner R.D., Davis R.L., Ragain R.M. The effect of taurine supplementation on patients with type 2 diabetes mellitus. Adv Exp Med Biol. 2003; 526: 91 – 6.
- E.R.L. O’Maille, Richards T.G., Short A.H. Acute taurine depletion and maximal rates of hepatic conjugation and secretion of cholic acid in the dog. J.Physiol. 1965180. 67 – 79.
- Chen W., Matuda K., Nishimura N., Yokogoshi H. The effect of taurine on cholesterol degradation in mice fed a high-cholesterol diet. Life Sci. 2004 – Feb 27; 74(15):1889 – 98.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru






