Лечение стенокардии: возможности никорандила в схеме антиангинальной терапии
Статьи
Юрий Александрович Карпов - докт. мед. наук, профессор, рук. отдела ангиологии ФГБУ “Национальный медицинский исследовательский центр кардиологии им. акад. Е.И. Чазова” Минздрава России, Москва.
Контактная информация: yuri_karpov@inbox.ru
Ишемическая болезнь сердца (ИБС) не только в значительной степени определяет продолжительность жизни, но и влияет на ее качество. Это обусловливает основную цель в лечении ИБС - снижение риска осложнений и улучшение качества жизни. На сегодняшний день с целью улучшения качества жизни, или устранения приступов стенокардии, применяются 7 классов антиангинальных (антиишемических) препаратов. Среди этих классов особое место занимает никорандил с двойным механизмом действия, являющийся активатором калиевых каналов, чувствительных к аденозинтрифосфату, и обладающий нитратоподобными свойствами. Никорандил рекомендуется при неуспешности применения препаратов первой линии, для лечения пациентов с микрососудистой стенокардией. Помимо антиангинального действия препарат вызывает ишемическое прекондиционирование, что позволяет снизить риск развития ишемического повреждения миокарда и инфаркта миокарда при плановом чрескожном коронарном вмешательстве или предупредить реперфузионный синдром при реваскуляризации у пациентов с острым коронарным синдромом. При длительном применении у пациентов со стабильной ИБС препарат снижает риск развития сердечно-сосудистых осложнений. Никорандил (Кординик, компания ПИК-ФАРМА) назначается для лечения стенокардии в дозе 10-20 мг 1-3 раза в день (наибольшая суточная доза 80 мг), чаще всего в составе комбинированной антиангинальной терапии с b-адреноблокаторами или блокаторами кальциевых каналов.
Ключевые слова: ишемическая болезнь сердца, антиангинальная терапия, никорандил, ишемическое прекондиционирование, чрескожное коронарное вмешательство.
Введение
В связи с большой распространенностью и существенным влиянием на качество и продолжительность жизни своевременная диагностика и эффективное лечение ишемической болезни сердца (ИБС) имеют огромное медицинское и социальное значение [1, 2]. В лечении ИБС важно изменить образ жизни пациента и назначить медикаментозную терапию, направленную на снижение риска сердечно-сосудистых осложнений и увеличение продолжительности жизни (болезньмодифицирующая), а также на улучшение качества жизни, или на уменьшение симптомов стенокардии и частоты возникновения ишемии [3-5]. В первое направление входит контроль артериального давления (АД), антитромбоцитарная терапия (при необходимости усиленная в виде двойной антитромбоцитарной или в комбинации с пероральным антикоагулянтом), липидснижающая терапия (также в виде комбинированной), по показаниям в-адреноблокаторы (БАБ) и ингибиторы ангиотензинпревращающего фермента.
При необходимости медикаментозная терапия дополняется инвазивными методами лечения: чрескожным коронарным вмешательством (ЧКВ) или операцией аортокоронарного шунтирования, которые не всегда улучшают прогноз при оптимальном медикаментозном лечении, но значительно снижают или полностью устраняют стенокардию [4, 6, 7].
В нашей стране для лечения стенокардии зарегистрировано 7 классов препаратов, оказывающих сопоставимое антиангинальное действие, которые на основании доказанности дополнительных эффектов, противопоказаний для назначения и переносимости традиционно делят на препараты первой линии (БАБ и блокаторы кальциевых каналов (БКК)) и препараты второй линии (нитраты длительного действия (НДД), ивабрадин, никорандил, ранолазин, триметазидин), а также выделяют группу препаратов, не влияющих на показатели гемодинамики (ранолазин, триметазидин) [3]. На рис. 1 представлен пошаговый алгоритм назначения антиишемической лекарственной терапии при стабильной ИБС в зависимости от клинической ситуации с учетом необходимости контроля частоты сердечных сокращений (ЧСС) и АД, индивидуальных особенностей пациентов, противопоказаний и нежелательных эффектов, а также приоритетов комбинированного лечения [3].
Среди антиангинальных препаратов особое место занимает никорандил. Никорандил, уникальный антиишемический препарат с двойным фармакологическим механизмом действия, являющийся активатором чувствительных к аденозинтрифосфату (АТФ) калиевых каналов и обладающий нитратоподобными свойствами, помогает эффективно вести пациентов со стенокардией и обеспечивает долгосрочную кардиопротекцию.
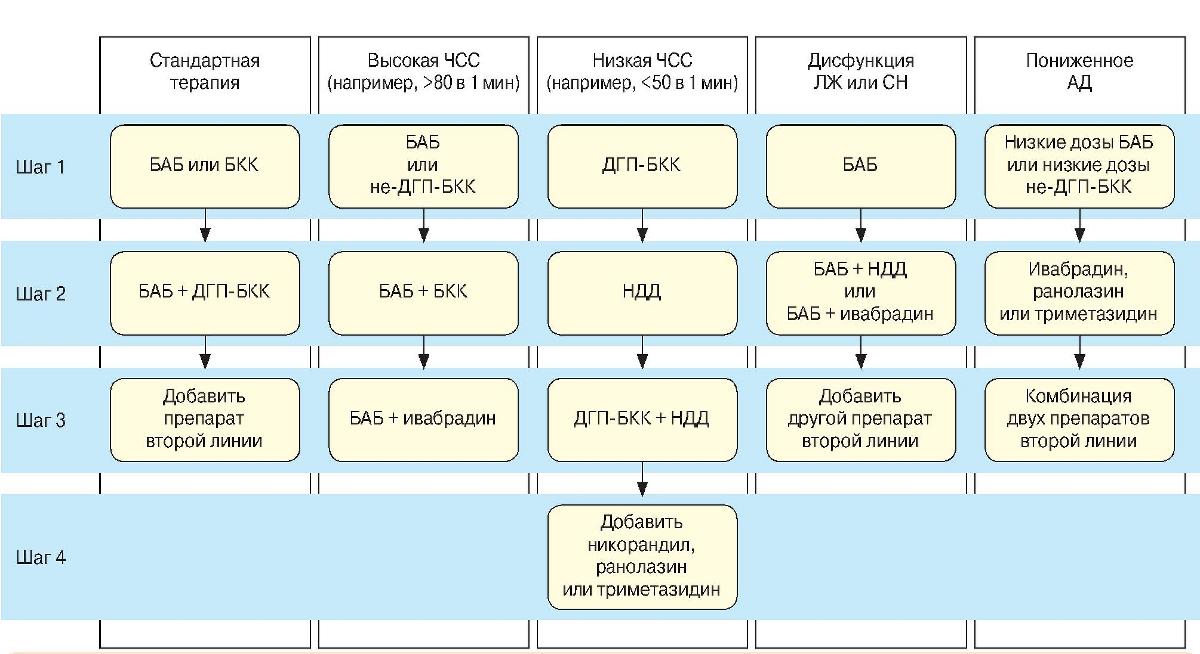
Рис. 1. Антиангинальная терапия в зависимости от клинической ситуации.
ДГП-БКК - дигидроприридиновые БКК, ЛЖ - левый желудочек, не-ДГП-БКК - недигидроприридиновые БКК, СН - сердечная недостаточность.
Механизм действия
Никорандил - производное никотинамида с двойным механизмом сосудорасширяющего действия. С одной стороны, он активирует АТФ-чувствительные калиевые каналы на мембранах гладкомышечных клеток сосудов, что приводит к оттоку ионов калия и гиперполяризации клеточной мембраны, закрытию потенциалзависимых кальциевых каналов, т.е. снижает приток ионов кальция (Ca2+) в клетку извне. При этом активация АТФ-чувствительных калиевых каналов саркоплазматической мембраны ингибирует поступление Ca2+ из саркоплазматического ретикулума, как показано на рис. 2 [8, 9]. Таким образом, активация АТФ-чувствительных калиевых каналов способствует снижению содержания Ca2+ в цитозоле, что продлевает время действия положительного заряда на наружной мембране гладкомышечной клетки, т.е. преобладает невозбужденное состояние последней. С другой стороны, никорандил осуществляет донацию оксида азота (NO) таким же образом, как и нитраты (нитроглицерин, динитрат изосорбида и мононитрат изосорбида) [10, 11]. Увеличение содержания свободных радикалов NO напрямую активирует гуанилат-циклазу, которая увеличивает образование циклического гуанозинмонофосфата (цГМФ) [9]. Последний активирует цГМФ-зависимую протеинкиназу. В итоге действие никорандила приводит к вазодилатации кровеносных сосудов.
Основные эффекты при применении никорандила следующие: уменьшение выраженности ишемии миокарда, меньшее влияние на гемодинамику и лучшая переносимость в сравнении с нитратами, улучшение прогноза. Это первый клинически доступный активатор АТФ-чувствительных калиевых каналов, дополненный эффектом нитратов. Пик гемодинамических эффектов никорандила достигается в течение 1-2 мин после внутривенного введения или в течение 30-60 мин после однократного перорального приема (20-40 мг), и они сохраняются до 12 ч (40-60 мг) [12].
Нитратоподобный эффект никорандила реализуется через расширение крупных артерий, в то время как активация АТФ-чувствительных калиевых каналов проявляется в расширении резистивных артерий диаметром менее 100 мм [13]. В исследовании было установлено, что внутрикоронарно введенный никорандил вызывает дозозависимое увеличение скорости коронарного кровотока и снижение коронарного сосудистого сопротивления [14]. Максимальный сосудорасширяющий эффект был достигнут при введении никорандила в дозе 1,5 мг в левую коронарную артерию и 1,0 мг в правую коронарную артерию. В этом эксперименте ни одна из доз никорандила не привела к клинически выраженным симптомам и его введение сопровождалось незначительными изменениями системной гемодинамики. Эти данные свидетельствуют о том, что болюсное введение никорандила внутрикоронарно может безопасно, быстро и надежно обеспечить максимальную коронарную гиперемию у человека.
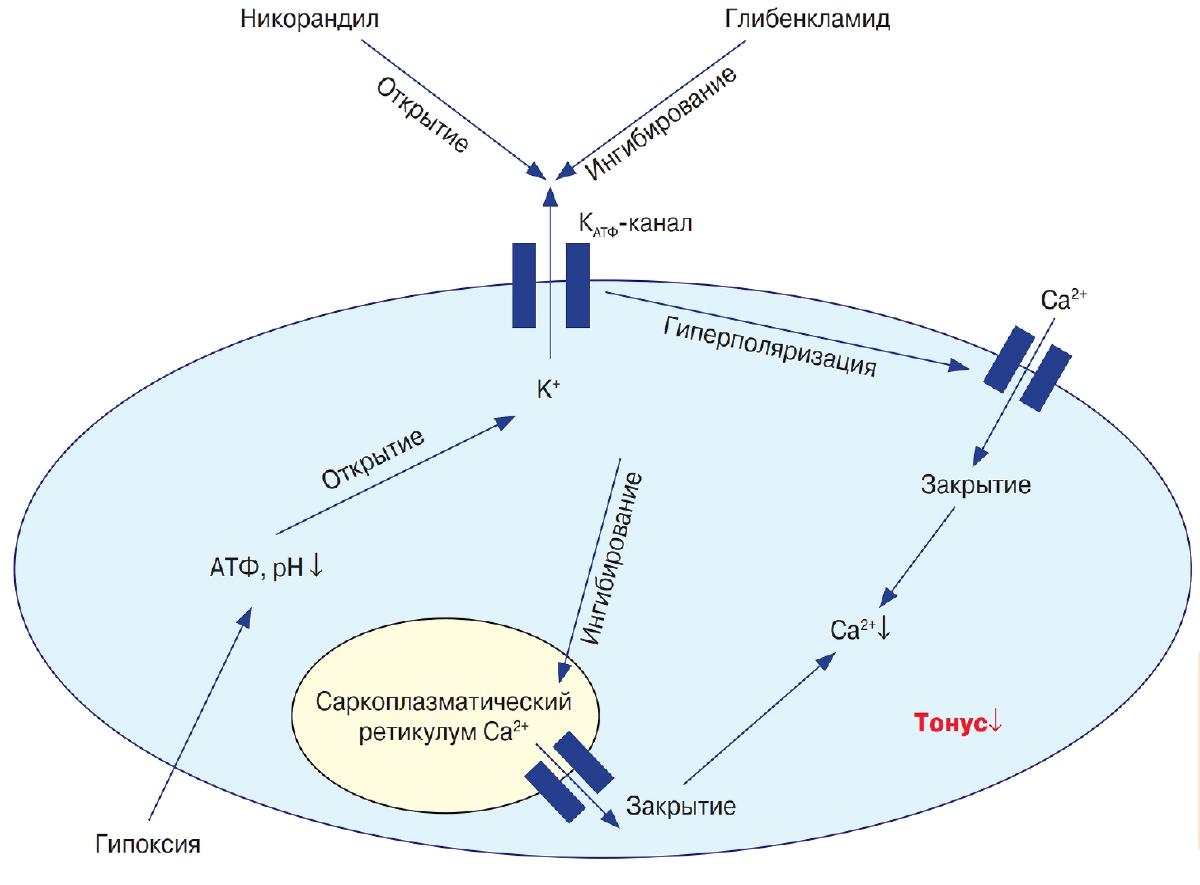 Рис. 2
Рис. 2. Возможная функция АТФ-чувствительных калиевых каналов (К
АТФ-канал) в гладкомышечных клетках артерий при введении никорандила и глибенкламида. Влияние никорандила на диаметр эпикардиальных коронарных артерий и коронарный кровоток человека исследовали с антагонистом АТФ-чувствительных калиевых каналов глибенкламидом и без него. Скорость увеличения диаметра коронарных артерий при введении никоранди-ла (0,2 мг/кг) у пациентов, получавших и не получавших глибенкламид, была схожей. Хотя никорандил увеличивает коронарный кровоток, а добавление глибенкламида препятствует этому увеличению, результаты исследования позволили предположить, что никорандилиндуцированная дилатация крупных коронарных артерий была связана с его нитратным эффектом, в то время как никорандилиндуцированная дилатация малых коронарных артерий тесно связана с его эффектами в качестве агониста АТФ-чувствительных калиевых каналов. Кроме того, первая реакция на никорандил возникала при низких концентрациях препарата, в то время как последняя реакция происходила при более высоких его концентрациях [15].
Таким образом, никорандил приводит к дилатации крупных коронарных сосудов вследствие нитратоподобного действия. Применение никорандила также сопровождается снижением сопротивления микрососудисто-го коронарного русла в отличие от нитратов и тем самым увеличивает коронарный кровоток за счет открытия АТФ-чувствительных калиевых каналов.
M. Hirose et al. продемонстрировали, что никорандил в дозах 10 и 30 ммоль/л: 1) в зависимости от дозы сокращал потенциал действия внутри стенки миокарда без увеличения разброса длительности потенциала действия; 2) уменьшал замедление проводимости внутри стенки миокарда; 3) ингибировал дисперсию локальной скорости проводимости [16]. Авторы пришли к выводу, что никорандил значительно снижает частоту возникновения желудочковой тахикардии во время глобальной ишемии. Сообщалось, что никорандил уменьшает дисперсию интервала QT на электрокардиограмме (ЭКГ), это указывает на неоднородность времени реполяризации, региональные различия в продолжительности потенциала действия и времени активации у пациентов с ЧКВ или острым инфарктом миокарда (ИМ) [17-20]. В экспериментах in vivo исследователи обнаружили, что никорандил снижает вероятность летального исхода: предотвращает ишемическую желудочковую тахиаритмию у находящихся в сознании крыс с острым ИМ и подавляет желудочковые аритмии во время и после ЧКВ у пациентов с ИМ [21].
В одном из исследований было отмечено, что внутривенное введение никорандила может уменьшать частоту фибрилляции желудочков и удлинения интервала QT у пациентов с ИМ, успешно перенесших ЧКВ [22]. В многоцентровом рандомизированном двойном слепом плацебоконтролируемом исследовании CESAR 2 также было выявлено, что пероральный прием никорандила в дозе 20 мг 2 раза в день в сочетании с другими антиангинальными препаратами при лечении нестабильной стенокардии снижает частоту возникновения желудочковой тахиаритмии в сравнении с плацебо [23]. Полученные данные свидетельствуют о том, что никорандил может проявлять антиаритмические свойства в случае аритмий, вызванных нарушением автоматизма и re-entry, особенно при ишемии миокарда.
Изучение клинической эффективности никорандила
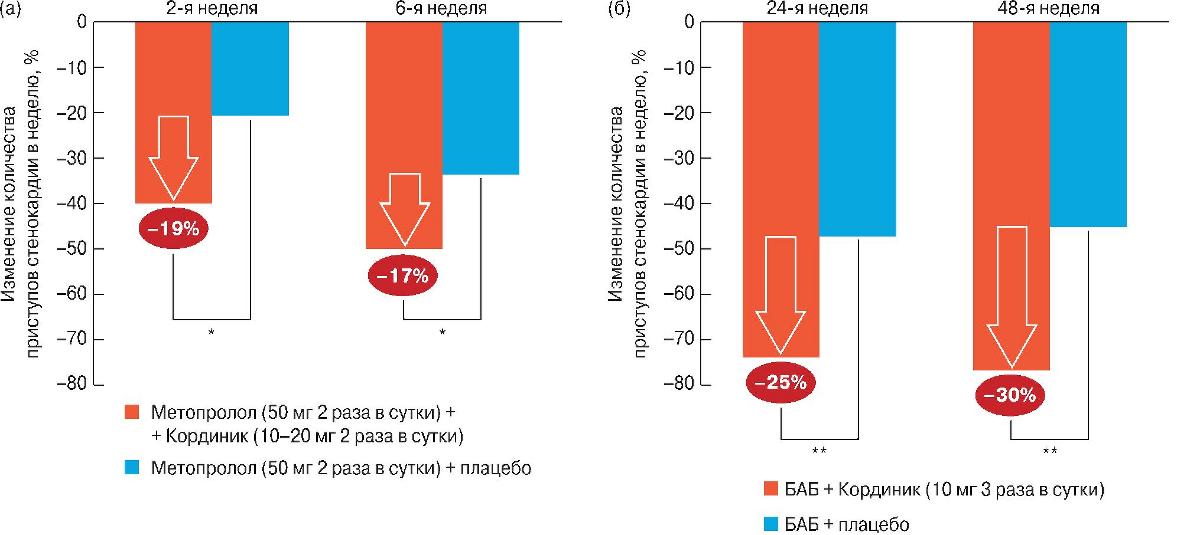 Рис. 3
Рис. 3. Антиангинальный эффект никорандила (Кординик) на фоне БАБ: а - исследование КВАЗАР (больные стабильной стенокардией напряжения II-III функционального класса (ФК); n = 120); б - двойное слепое плацебоконтролируемое исследование (больные стабильной стенокардией напряжения III ФК; n = 150) [25, 26]. * p = 0,02. ** p < 0,0001.
В клинических исследованиях было продемонстрировано, что никорандил эффективен при всех типах стенокардии, включая стенокардию напряжения, стенокардию покоя, стенокардию после перенесенного ИМ, нестабильную, вариантную и микрососудистую стенокардию (МСС) [9]. В контролируемых исследованиях было установлено, что антиангинальная эффективность, повышение толерантности к физической нагрузке и улучшение качества жизни у пациентов со стабильной стенокардией при лечении никорандилом в течение 6-12 нед сопоставимо с применением БАБ (атенолола, пропранолола, метопролола), НДД (изосорбида мононитрата и изосорбида динитрата) и БКК (дилтиазема, нифедипина, амлодипина) [24]. В среднем анти-ангинальный эффект достигается у 71% пациентов. Эти исследования показали, что никорандил обладает более благоприятным профилем переносимости, который включает в себя влияние на АД и ЧСС, что делает его особенно полезным для длительного лечения стенокардии.
 Рис. 4.
Рис. 4. Антиишемический эффект никорандила в исследовании КВАЗАР: влияние Кординика на время до достижения депрессии сегмента ST >1 мм при пробе на толерантность к физической нагрузке (тредмил) на 6-й неделе терапии по отношению к началу исследования у больных стабильной стенокардией напряжения II-III функционального класса (n = 120) (через 12 ч после приема препаратов) [27]. p < 0,0476.
В нашей стране также изучалось влияние добавления никорандила к стандартной терапии у больных стабильной ИБС на клинические проявления болезни, а также на безопасность проводимой терапии [25, 26]. Было проведено двойное слепое плацебоконтролируемое исследование КВАЗАР в параллельных группах, в которое было включено 120 пациентов с верифицированной ИБС и стабильной стенокардией напряжения. Все больные на протяжении наблюдения получали метопролол в дозе 100 мг/сут. Больным основной группы к лечению добавляли никорандил (Кординик, компания ПИК-ФАРМА) в дозе 10 мг 2 раза в сутки, через 2 нед дозу увеличивали до 20 мг 2 раза в сутки, больным контрольной группы к лечению добавляли плацебо, продолжительность исследования составила 6 нед. Назначение никорандила способствовало достоверному уменьшению количества приступов стенокардии (по сравнению с контрольным периодом и с больными, принимавшими плацебо) (рис. 3). Употребление нитратов короткого действия достоверно снизилось по сравнению с контрольным периодом при применении никорандила в обеих дозах. Нежелательные явления были отмечены у 10 (16,4%) из 61 пациента, принимавшего никорандил, и у 7 (11,9%) из 59 пациентов, принимавших плацебо, различия между группами статистически незначимые. В связи с развитием головной боли 3 пациента прекратили участие в исследовании: 2 пациента в группе никорандила и 1 пациент в группе плацебо. В этом же исследовании было показано, что прием никорандила в комбинации с метопрололом способствовал достоверному увеличению всех параметров нагрузочного тестирования в сравнении с группой плацебо (рис. 4) [27].
Рекомендованная фармакотерапия при МСС в зависимости от типа поражения коронарного русла [5]

Никорандил у пациентов с МСС
Несмотря на то что арсенал лекарственных средств для лечения стенокардии включает 7 классов антиангинальных препаратов, устранение стенокардии у пациентов с необструктивным поражением коронарных артерий с помощью стандартного антиишемического алгоритма нередко не дает положительного результата [28]. Это связано с тем, что пациенты представляют собой гетерогенную группу в плане происхождения ишемии миокарда, а также c отсутствием крупных рандомизированных исследований в этой клинической когорте. Например, БАБ или недигидропиридиновые БКК, с которых обычно начинают антиангинальную терапию, могут не давать желаемого результата [29]. Ранее клинические исследования с включением относительно небольшого количества пациентов показали, что никорандил может уменьшать выраженность болезни у пациентов с МСС [20, 30]. По мнению китайских экспертов, механизмы антиишемического действия никорандила соответствуют патофизиологии МСС, в связи с чем он был предложен в качестве препарата первого выбора для лечения этой формы стенокардии в Китае [31]. В клинических рекомендациях Американской ассоциации кардиологов/Американской коллегии кардиологов 2023 г. указывается, что у пациентов с МСС (необструктивная ИБС с доказанной коронарной микрососудистой дисфункцией) при неэффективности или непереносимости препаратов первой линии (БАБ) их заменяют на недигидропиридиновые БКК (например, верапамил 40 мг 2 раза в день, с титрованием дозы); при неэффективности к терапии БАБ можно присоединить дигидропиридиновые БКК (например, амлодипин), а затем никорандил (5 мг 2 раза в день, с титрованием дозы) или ранолазин (375 мг 2 раза в день, с титрованием дозы) (таблица) [5].
Преимущества никорандила помимо антиангинального действия
При изучении никорандила оказалось, что препарат может оказывать и другие благоприятные эффекты, в частности ишемическое прекондиционирование. Первое экспериментальное сообщение о феномене ишемического прекондиционирования было сделано еще в 1986 г. [32]. На сердце собаки было показано, что прекондиционирование миокарда путем четырех 5-минутных эпизодов ишемии приводило к развитию некроза меньшего размера (парадоксальному уменьшению размера ИМ до 25%) в результате длительной 40-минутной коронарной окклюзии по сравнению с группой без прекондиционирования. Однако этот защитный эффект исчезал, когда длительность ишемии увеличивалась до 3 ч. Этот феномен наблюдался у всех видов животных, даже если коллатеральный кровоток отсутствовал дистальнее закупоренных артерий. Ишемическое прекондиционирование - возможность с помощью повторной кратковременной ишемии повышать устойчивость миокарда к последующему длительному периоду ишемии.
Никорандил не только напрямую, но и косвенно, через активацию NO-протеинкиназы G, открывает митохондриальные АТФ-чувствительные калиевые каналы [33]. Было установлено, что ишемическое прекондиционирование, при котором кратковременный предварительный период ишемии обеспечивает надежную защиту от ишемически реперфузионного повреждения, уменьшает раскрытие митохондриальных пор проницаемости. С клинической точки зрения множественные приступы стенокардии, которые часто предшествуют ИМ у пациентов, могут отсрочить гибель клеток после коронарной окклюзии и, таким образом, обеспечить более эффективное восстановление миокарда с помощью реперфузионной терапии.
H. Matsuo et al. случайным образом распределили 44 пациента со стенокардией, которым было выполнено ЧКВ по поводу проксимального стеноза левой передней нисходящей артерии, в 2 группы, в одной из которых в течение 5 мин внутривенно вводили никорандил (80 мг/кг), а в другой - физиологический раствор [34]. Проводили запись ЭКГ и однофотонную эмиссионную компьютерную томографию с 99mTc тетрофосмином при 2-минутной инъекции во время проведения ЧКВ. Выраженность смещения сегмента ST была значительно меньше у пациентов, получавших никорандил. Однако при количественном анализе не было выявлено различий в степени выраженности окклюзии. Таким образом, предварительное введение никорандила вызывало прекондиционирование миокарда независимо от тяжести ишемии [34].
С целью предупреждения интраоперационного ишемического повреждения миокарда перспективным представляется формирование до проведения ЧКВ фармакологического прекондиционирования c применением никорандила. В исследовании изучали влияние использования никорандила перед плановым ЧКВ на предупреждение повреждений миокарда и ИМ 4а типа (первичная конечная точка) и развития сердечно-сосудистых событий в течение года после планового ЧКВ (вторичная конечная точка) у больных стабильной ИБС [35].
В исследование было включено 182 пациента со стабильной ИБС, которых рандомизировали в группы стандартного лечения (n = 92) и дополнительного назначения никорандила (n = 90). Никорандил (Кординик, компания ПИК-ФАРМА) назначался внутрь по следующей схеме: за 2 сут до ЧКВ - 30 мг/сут; в день ЧКВ - 20 мг за 2 ч до операции и 10 мг через 6-12 ч после ЧКВ; в последующие 30 дней - 30 мг/сут. Анализ высокочувствительного тропонина I (Вч-Тр) и креатинкиназы-МВ проводили до ЧКВ и спустя 24 и 72 ч после процедуры, диагноз ИМ 4а типа выставлялся согласно Четвертому универсальному определению ИМ. В качестве сердечно-сосудистых событий оценивали нефатальный ИМ, нефатальное нарушение мозгового кровообращения, смерть от сердечно-сосудистых причин, повторную реваскуляризацию коронарных артерий (ЧКВ, коронарное шунтирование в связи с ухудшением), госпитализации по поводу рецидива стенокардии (без вмешательств) и смерть от любых причин. Сбор информации о неблагоприятных событиях осуществляли за период пребывания пациентов в стационаре, и затем через 30, 180 и 365 дней после выписки. Инфаркт миокарда 4а типа был зарегистрирован у 14 пациентов (8%), среди мужчин - у 6%, среди женщин - у 12%.
В группе никорандила частота ИМ 4а типа была статистически значимо более низкой (n = 3; 3%), чем в группе контроля (n = 11; 12%; p = 0,05). Была установлена статистически значимая связь перенесенного ИМ 4а типа с частотой развития сердечно-сосудистых событий в течение года после ЧКВ (p = 0,0123). У пациентов с перенесенным ИМ 4а типа отношение шансов развития всех сердечно-сосудистых событий возрастало в 5,8 раза при доверительном интервале 1,5-21,6. По результатам логистического регрессионного анализа была выявлена статистически значимая взаимосвязь между приростом уровня Вч-Тр через 24 ч после ЧКВ и частотой развития ишемических событий в течение года после ЧКВ, с отрезным значением 389,8 пг/мл (AUC (area under the ROC curve - площадь под ROC-кривой) 0,641; p = 0,04). Прием никорандила в дозе 30 мг/сут до и в течение 30 дней после ЧКВ сопровождался снижением риска развития интраоперационного ишемического повреждения миокарда и сердечно-сосудистых осложнений в течение года после ЧКВ.
Влияние никорандила на клиническое течение заболевания у пациентов со стабильной ИБС
Влияние никорандила на прогноз изучалось в исследовании IONA, которое представляло собой крупномасштабное рандомизированное двойное слепое плацебоконтролируемое исследование никорандила в сравнении с плацебо [36]. Прием никорандила начинали с дозы 20-40 мг 2 раза в день. В исследование, проведенное в Великобритании, были включены только пациенты со стабильной стенокардией, получавшие регулярную антиангинальную терапию такими препаратами, как НДД, БАБ или БКК. Было отобрано около 5000 пациентов, которые были разделены на группу приема никорандила и группу плацебо. Средний период наблюдения составил 1,6 года (1-3 года). Первичной конечной точкой исследования была смерть от ИБС, нефатальный ИМ и незапланированная госпитализация по поводу подозрения на ИМ. В период наблюдения в общей сложности у 15,5% пациентов в группе плацебо были отмечены события первичной конечной точки по сравнению с 13,1% в группе никорандила (рис. 5). Никорандил снижал риск достижения событий первичной конечной точки на 17% (р = 0,014). Однако по вторичной конечной точке (смерть от ИБС или нефатального ИМ) статистически значимых различий не выявлено (р = 0,068), что, возможно, было связано с недостаточной мощностью исследования для выявления различий в риске развития более жесткой конечной точки, поскольку частота возникновения этих опасных осложнений ИБС в группе плацебо была существенно ниже, чем прогнозировалось. Вместе с тем исследование IONA стало первым долгосрочным наблюдением за пациентами со стабильной стенокардией, в ходе которого было установлено, что агонисты АТФ-чувствительных калиевых каналов, такие как никорандил, могут снижать вероятность клинически значимых исходов. Механизмы улучшения прогноза у пациентов с ИБС могут включать ишемическое прекондиционирование клеток миокарда путем открытия митохондриальных АТФ-чувствительных калиевых каналов и улучшение микрососудистого кровотока в коронарных артериях за счет открытия сарколеммальных АТФ-чувствительных калиевых каналов в гладкой мускулатуре сосудов.
В российской программе НИКЕЯ полученные в условиях реальной клинической практики данные по эффективности и безопасности никорандила у больных стабильной ИБС сопоставляли с данными исследования IONA [37, 38]. В эту многоцентровую программу было включено 590 пациентов со стабильной стенокардией напряжения. Участникам программы НИКЕЯ в дополнение к проводимой терапии ИБС назначался никорандил (Кординик, компания ПИК-ФАРМА) перорально по 10 мг 2 раза в день, с титрованием дозы через 1 мес до 20 мг 2 раза в день. Частота событий первичной комбинированной конечной точки оказалась выше в IONA. По данным программы НИКЕЯ, результаты применения никорандила в условиях реальной клинической практики продемонстрировали эффективность и безопасность препарата, а также его благоприятное влияние на прогноз у пациентов со стабильной ИБС, доказанные ранее в ходе рандомизированного клинического исследования IONA [38].
Уроки исследований ORBITA и ORBITA-2
В клинической практике пациенты часто не получают адекватной антиангинальной терапии до направления на ЧКВ. Важность такой терапии продемонстрировали результаты многоцентрового (5 центров в Великобритании) исследования ORBITA, включавшего 230 пациентов со стабильной стенокардией с однососудистым поражением коронарного русла [39]. Особенностью этого первого в истории ЧКВ плацебоконтролируемого исследования стала рандомизация в группы ЧКВ и имитации процедуры для исключения возможного плацебо-эффекта эндоваскулярного лечения ИБС. Оценивались клинически и инструментально (нагрузочное тестирование) преимущества процедуры ЧКВ на фоне оптимальной медикаментозной терапии (в среднем каждому пациенту назначались 2 антиангинальных препарата), коррекция которой проводилась в течение 6 нед до вмешательства. Через 6 нед после вмешательства (или его имитации) достоверные различия между группами эндоваскулярного лечения и плацебо были отмечены только при проведении стресс-эхокардиографии с добутамином: после ЧКВ индекс сократимости миокарда улучшился в значимо большей степени, чем при плацебо-вмешательстве, а изменения частоты приступов стенокардии, функционального класса стенокардии, а также показателей тредмил-теста были незначительными.
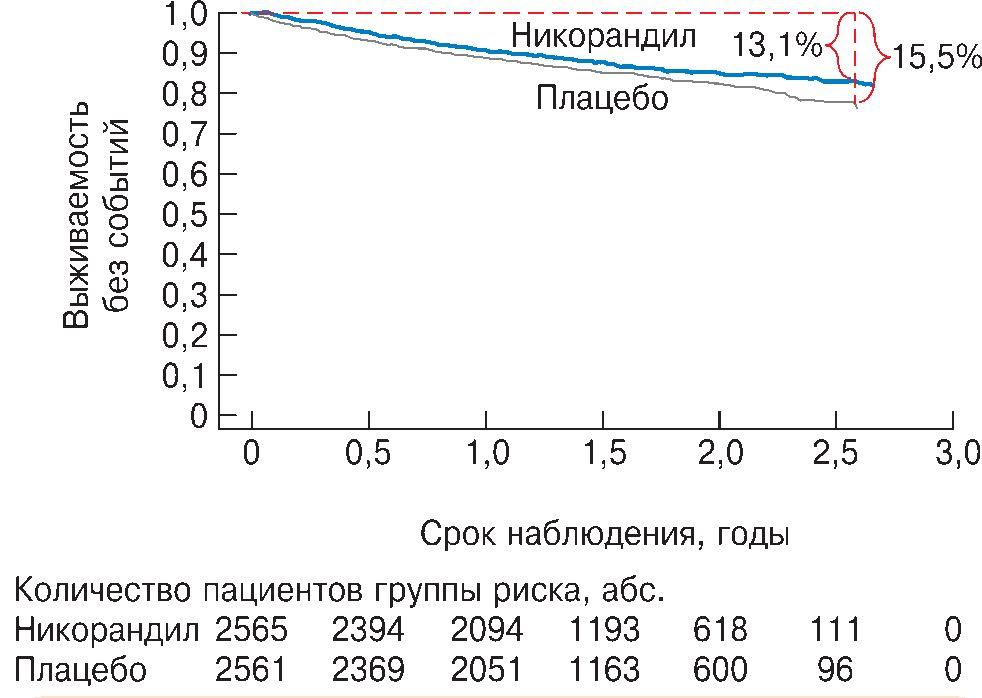
Рис. 5. График оценки Каплана-Мейера (кумулятивный) по частоте достижения первичной конечной точки в исследовании IONA (n = 5126; ИМ в анамнезе - у 66%, аортокоронарное шунтирование - у 22%, ЧКВ - у 14%; I-II класс стенокардии - у 89%; лечение: БАБ - 57%, БКК - 55%, нитраты -87%) [36]. р = 0,014.
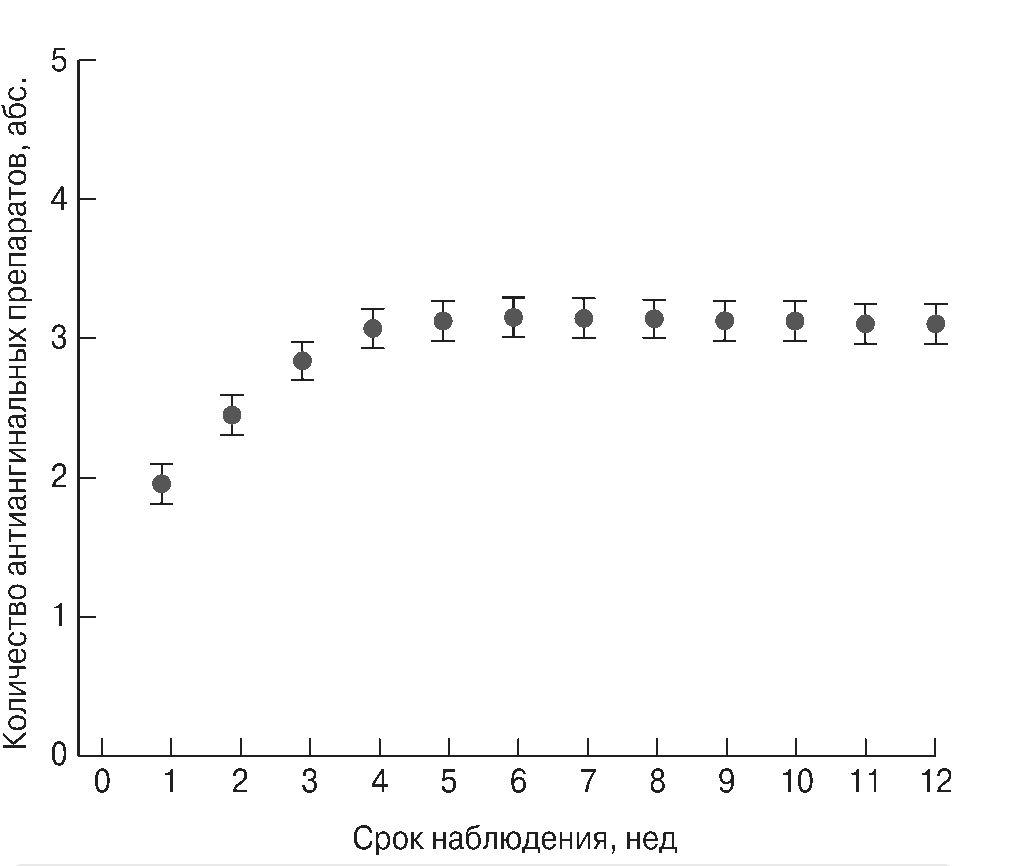
Рис. 6. Среднее количество антиангинальных препаратов у 1 пациента в ходе исследования ORBITA [39].
В ходе этого 12-недельного клинического исследования было продемонстрировано, что антиангинальная терапия в большинстве случаев хорошо переносится и что нежелательные эффекты, приводящие к отмене препарата, редки. Такой значительный клинический результат в группе медикаментозного лечения с имитацией ЧКВ был достигнут на фоне многокомпонентной антиангинальной терапии, в среднем 3 антиангинальных препарата на 1 больного (рис. 6). Надо отметить, что в этом исследовании никорандил показал свою эффективность у 72% пациентов, что соответствует ранее установленной антиангинальной эффективности никорандила, равной 71% [24]. Чаще никорандила в этом исследовании назначались только БАБ, БКК и НДД.
Проведенный анализ показал, что до направления на ЧКВ большинство пациентов принимали только 1 антиангинальный препарат, 32% пациентов - 2 антиангинальных препарата, а 9% пациентов, уже направленных на ЧКВ, вообще не получали такой терапии [40]. Отчасти это может быть вызвано опасениями по поводу переносимости такого лечения, полипрагмазии и возможных побочных эффектов. Следует отметить, что подбор и поиск оптимальной схемы антиангинальной терапии довольно трудоемкий и времязатратный процесс. В клинической практике пациенты могут не захотеть принимать >3 антиангинальных препаратов в течение длительного времени, предпочитая проведение ЧКВ. Это в итоге может склонить и пациента, и врача к выбору процедуры ЧКВ как более простого, доступного и предпочтительного метода антиангинального лечения. В этой ситуации следует напомнить, что в клинических рекомендациях перевод пациента со стабильной стенокардией на инвазивное лечение должен рассматриваться в большинстве случаев после исчерпания возможностей комбинированной антиангинальной терапии с назначением >2 препаратов с различным механизмом антиангиналь-ного действия [3-5].
В свете результатов исследования ORBITA необходимо было ответить на вопрос, помогает ли ЧКВ при стенокардии в большей степени, чем плацебо, у пациентов, не получающих антиангинальной терапии. Было организовано рандомизированное двойное слепое плацебоконтролируемое исследование по оценке эффективности ЧКВ у пациентов со стабильной стенокардией, прекративших прием всех антиангинальных препаратов и прошедших 2-недельный этап оценки выраженности стенокардии перед рандомизацией [41]. Затем пациенты были случайным образом распределены в соотношении 1 : 1 для прохождения процедуры ЧКВ или плацебо и находились под наблюдением в течение 12 нед. Первичной конечной точкой была оценка выраженности стенокардии, которая рассчитывалась ежедневно на основании количества приступов стенокардии, количества назначенных антиангинальных препаратов и числа клинических событий, включая возникновение осложнений из-за выраженной стенокардии, острого коронарного синдрома или смерть. Количество баллов варьировало от 0 до 79, причем более высокое их количество указывает на ухудшение состояния здоровья в связи со стенокардией.
В общей сложности 301 пациент (79% мужчин; средний возраст 64 года) был подвергнут рандомизации: 151 пациент - в группу ЧКВ и 150 пациентов - в группу имитации ЧКВ (плацебо). Ишемия до рандомизации визуализировалась в 1 области сердца у 242 пациентов (80%), в 2 областях - у 52 (17%) и в 3 областях - у 7 (2%). При 12-недельном наблюдении средняя оценка выраженности стенокардии составила 2,9 балла в группе ЧКВ и 5,6 балла в группе плацебо (отношение шансов 2,21; 95% доверительный интервал 1,41-3,47; р < 0,001). Острый коронарный синдром возник у 4 пациентов в группе ЧКВ и у 6 пациентов в группе плацебо. У пациентов со стабильной стенокардией, которые практически не получали антиангинальных препаратов и имели объективные признаки ишемии, ЧКВ приводило к меньшей выраженности стенокардии в сравнении с плацебо-процедурой, что указывало на улучшение качества жизни и несомненный антиангинальный эффект инвазивного лечения. Таким образом, результаты плацебоконтроли-руемого исследования ORBITA-2 доказали эффективность ЧКВ как метода антиангинальной монотерапии у пациентов со стабильной стенокардией.
Заключение
Никорандил - активатор АТФ-чувствительных калиевых каналов с нитратоподобным действием, который может облегчать симптомы в той же степени, что и НДД, БАБ и БКК, у пациентов со стабильной стенокардией напряжения. Двойной механизм действия препарата позволяет рекомендовать его для лечения пациентов с МСС на фоне необструктивного поражения коронарного русла. Препарат не только оказывает антиангинальное действие, но и улучшает прогноз пациентов с ИБС. Помимо антиангинального действия препарат обеспечивает ишемическое прекондиционирование, что позволяет снизить риск развития ишемического повреждения миокарда и ИМ при плановом ЧКВ или предупредить реперфузионный синдром при реваскуляризации у пациентов с острым коронарным синдромом. Таким образом, никорандил занимает важное место в современном алгоритме комбинированной антиангинальной терапии.
Конфликт интересов отсутствует.
Список литературы
1. Joseph P, Leong D, McKee M, Anand SS, Schwalm JD, Teo K, Mente A, Yusuf S. Reducing the global burden of cardiovascular disease, part 1: the epidemiology and risk factors. Circulation Research 2017 Sep;121(9):677-94.
2. РосИнфоСтат. Статистика и показатели. Статистика смертности по данным Росстат. 2023. Доступно по: rosinfostat. ru/ Ссылка активна на 24.06.2024.
3. Российское кардиологическое общество (РКО). Стабильная ишемическая болезнь сердца. Клинические рекомендации 2020. Российский кардиологический журнал 2020;25(11):201-50.
4. Knuuti J, Wijns W, Saraste A, Capodanno D, Barbato E, Funck-Bren-tano C, Prescott E, Storey RF, Deaton C, Cuisset T, Agewall S, Dickstein K, Edvardsen T, Escaned J, Gersh BJ, Svitil P, Gilard M, Hasdai D, Hatala R, Mahfoud F, Masip J, Muneretto C, Valgimigli M, Achenbach S, Bax JJ; ESC Scientific Document Group. 2019 ESC guidelines for the diagnosis and management of chronic coronary syndromes. European Heart Journal 2020 Jan;41(3):407-77.
5. Virani SS, Newby LK, Arnold SV, Bittner V, Brewer LC, Demeter SH, Dixon DL, Fearon WF, Hess B, Johnson HM, Kazi DS, Kolte D, Kumb-hani DJ, LoFaso J, Mahtta D, Mark DB, Minissian M, Navar AM, Patel AR, Piano MR, Rodriguez F, Talbot AW, Taqueti VR, Thomas RJ, van Diepen S, Wiggins B, Williams MS; Peer Review Committee Members. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA Guideline for the management of patients with chronic coronary disease: a report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation 2023 Aug;148(9):e9-e119.
6. Boden WE, O’Rourke RA, Teo KK, Hartigan PM, Maron DJ, Kos-tuk WJ, Knudtson M, Dada M, Casperson P, Harris CL, Chaitman BR, Shaw L, Gosselin G, Nawaz S, Title LM, Gau G, Blaustein AS, Booth DC, Bates ER, Spertus JA, Berman DS, Mancini GB, Weintraub WS; COURAGE Trial Research Group. Optimal medical therapy with or without PCI for stable coronary disease. The New England Journal of Medicine 2007 Apr;356(15):1503-614.
7. Maron DJ, Hochman JS, Reynolds HR, Bangalore S, O’Brien SM, Boden WE, Chaitman BR, Senior R, Lopez-Sendon J, Alexander KP, Lopes RD, Shaw LJ, Berger JS, Newman JD, Sidhu MS, Goodman SG, Ruzyllo W, Gosselin G, Maggioni AP, White HD, Bhargava B, Min JK, Mancini GBJ, Berman DS, Picard MH, Kwong RY, Ali ZA, Mark DB, Spertus JA, Krishnan MN, Elghamaz A, Moorthy N, Hueb WA, Demkow M, Mavromatis K, Bockeria O, Peteiro J, Miller TD, Szwed H, Doerr R, Keltai M, Selvanayagam JB, Steg PG, Held C, Kohsaka S, Mavromichalis S, Kirby R, Jeffries NO, Harrell FE Jr, Rockhold FW, Broderick S, Ferguson TB Jr, Williams DO, Harrington RA, Stone GW, Rosenberg Y; ISCHEMIA Research Group. Initial invasive or conservative strategy for stable coronary disease. The New England Journal of Medicine 2020 Apr;382(15):1395-407.
8. Escande D, Cavero I. K+ channel openers and ‘natural’ cardioprotection. Trends in Pharmacological Sciences 1992 Jul;13(7):269-72.
9. Horinaka S. Use of nicorandil in cardiovascular disease and its optimization. Drugs 2011 Jun;71(9):1105-19.
10. Taira N. Nicorandil as a hybrid between nitrates and potassium channel activators. The American Journal of Cardiology 1989 Jun;63(21):18J-24J.
11. KukovetzWR, Holzmann S, Braida C, Poch G. Dual mechanism of the relaxing effect of nicorandil by stimulation of cyclic GMP formation and by hyperpolarization. Journal of Cardiovascular Pharmacology 1991 Apr;17(4):627-33.
12. Frampton J, Buckley MM, Fitton A. Nicorandil. A review of its pharmacology and therapeutic efficacy in angina pectoris. Drugs 1992 Oct;44(4):625-55.
13. Akai K, Wang Y, Sato K, Sekiguchi N, Sugimura A, Kumagai T, Koma-ru T, Kanatsuka H, Shirato K. Vasodilatory effect of nicorandil on coronary arterial microvessels: its dependency on vessel size and the involvement of the ATP-sensitive potassium channels. Journal of Cardiovascular Pharmacology 1995 Oct;26(4):541-47.
14. Hongo M, Takenaka H, Uchikawa S, Nakatsuka T, Watanabe N, Sekiguchi M. Coronary microvascular response to intracoronary administration of nicorandil. American Journal of Cardiology 1995 Feb;75(4):246-50.
15. Nakae I, Quan L, Hashimoto K, Sugimoto Y, Tsutamoto T, Kinoshita M. Mechanism of the vasodilatory action of nicorandil on coronary circulation in dogs. Cardiovascular Drugs and Therapy 1994 Feb;8(1):137-45.
16. Hirose M, Tsujino N, Nakada T, Yano S, Imamura H, Yamada M. Mechanisms of preventive effect of nicorandil on ischaemia-induced ventricular tachyarrhythmia in isolated arterially perfused canine left ventricular wedges. Basic & Clinical Pharmacology & Toxicology 2008 Jun;102(6):504-14.
17. Kato T, Kamiyama T, Maruyama Y, Tanaka S, Yoshimoto N. Nicorandil, a potent cardioprotective agent, reduces QT dispersion during coronary angioplasty. American Heart Journal 2001 Jun;141(6):940-3.
18. Ashikaga T, Nishizaki M, Arita M, Yamawake N, Fujii H, Kishi Y, Isobe M, Hiraoka M. Opening of K(ATP) channel attenuates the increase in QT dispersion produced by the first balloon inflation during coronary angioplasty. Circulation Journal 2002 May;66(5):469-72.
19. Akagi T, Sarazawa K, Inai Y, Kitagawa M, Takahashi N, Hamanaka I, Yamazaki T, Takebe M, Hama N, Hiraoka Y, Ueda K, Nakazawa K, Matsumoto N. Continuous administration of nicorandil decreases QT dispersion during the chronic phase of acute myocardial infarction. International Heart Journal 2006 May;47(3):351-61.
20. Chen JW, Lee WL, Hsu NW, Lin SJ, Ting CT, Wang SP, Chang MS. Effects of short-term treatment of nicorandil on exercise-induced myocardial ischemia and abnormal cardiac autonomic activity in microvascular angina. The American Journal of Cardiology 1997 Jul;80(1):2-38.
21. Hara H, Horinaka S, Yabe A, Yagi H, Tsuboko Y, Yoshida K, Iemura T, Matsuoka H. [Suppressive effect of nicorandil in ventricular arrhythmias after reperfusion therapy in patients with acute myocardial infarction.] Journal of Cardiology 2007 Mar;49(3):135-41.
22. Ueda H, Nakayama Y, Tsumura K, Yoshimaru K, Hayashi T, Yoshikawa J. Intravenous nicorandil can reduce the occurrence of ventricular fibrillation and QT dispersion in patients with successful coronary angioplasty in acute myocardial infarction. Canadian Journal of Cardiology 2004 May;20(6):625-9.
23. Patel DJ, Purcell HJ, Fox KM. Cardioprotection by opening of the K(ATP) channel in unstable angina. Is this a clinical manifestation of myocardial preconditioning? Results of a randomized study with nicorandil. CESAR 2 investigation (Clinical European Studies in Angina and Revascularization). European Heart Journal 1999 Jan;20(1):51-7.
24. Hanai Y, Mita M, Hishinuma S, Shoji M. [Systematic review on the short-term efficacy and safety of nicorandil for stable angina pectoris in comparison with those of в-blockers, nitrates and calcium antagonists.] Yakugaku Zasshi 2010 Nov;130(11):1549-63.
25. Марцевич С.Ю., Кутишенко Н.П., Деев А.Д. от имени участников исследования КВАЗАР. Сравнительная оценка анти-ангинальной эффективности и безопасности препарата ни-корандил на фоне базисной терапии b-адреноблокаторами у больных ишемической болезнью сердца со стабильной стенокардией. Русский медицинский журнал. Кардиология 2016;19:1290-4.
26. Рябихин Е.А., Можейко М.Е., Красильникова Ю.А. Оценка влияния терапии никорандилом на показатели качества жизни и прогноза у больных стабильной стенокардией. Кардиология 2016;11:12-7.
27. Воронина В.П., Марцевич С.Ю., Кутишенко Н.П., Деев А.Д. от имени участников исследования КВАЗАР. Оценка анти-ишемического и антиангинального эффектов никорандила с помощью нагрузочных тестов на тредмиле в рамках исследования КВАЗАР. Российский кардиологический журнал 2017;3(143):97-103.
28. Crea F, Lanza GA. Treatment of microvascular angina: the need for precision medicine. European Heart Journal 2016 May;37(19):1514-6.
29. Russo G, Di Franco A, Lamendola P, Tarzia P, Nerla R, Stazi A, Vil-lano A, Sestito A, Lanza GA, Crea F. Lack of effect of nitrates on exercise stress test results in patients with microvascular angina. Cardiovascular Drugs and Therapy 2013 Jun;27(3):229-34.
30. Yamabe H, Namura H, Yano T, Fujita H, Kim S, Iwahashi M, Maeda K, Yokoyama M. Effect of nicorandil on abnormal coronary flow reserve assessed by exercise 201Tl scintigraphy in patients with angina pectoris and nearly normal coronary arteriograms. Cardiovascular Drugs and Therapy 1995 Dec;9(6):755-61.
31. Zhang Y, Chen Y, Fu X, Chen WQ, Li DD, Gu XS. Chinese expert consensus guidelines for diagnosis and management of coronary mic-rovascular disease. Chinese Circulation Journal 2017;32:421-30.
32. Murry CE, Jennings RB, Reimer KA. Preconditioning with ischemia: a delay of lethal cell injury in ischemic myocardium. Circulation 1986 Nov;74(5):1124-36.
33. Kuno A, Critz SD, Cohen MV, Downey JM. Nicorandil opens mitochondrial K(ATP) channels not only directly but also through a NO-PKG-dependent pathway. Basic Research in Cardiology 2007 Jan;102(1):73-9.
34. Matsuo H, Watanabe S, Segawa T, Yasuda S, Hirose T, Iwama M, Tanaka S, Yamaki T, Matsuno Y, Tomita M, Minatoguchi S, Fujiwara H. Evidence of pharmacologic preconditioning during PTCA by intravenous pretreatment with ATP-sensitive K+ channel opener nicorandil. European Heart Journal 2003 Jul;24(14):1296-303.
35. Соболева Г.Н., Гостищев Р.В., Рогоза А.Н., Коткина Т.И., Сам-ко А.И., Карпов Ю.А. Влияние фармакологического прекондиционирования никорандилом перед плановым чрескожным коронарным вмешательством на отдаленный прогноз больных стабильной ишемической болезнью сердца. Рациональная фармакотерапия в кардиологии 2020;16(2):191-8.
36. IONA Study Group. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA): randomized trial. The Lancet 2002 Apr;359(9314):1269-75.
37. Марцевич С.Ю., Лукина Ю.В., Кутишенко Н.П., Акимова А.В., Воронина В.П., Лерман О.В., Гайсенок О.В., Гомова Т.А., Ежов А.В., Куимов А.Д., Либис Р.А., Матюшин Г.В., Митрошина Т.Н., Нечаева Г.И., Резник И.И., Скибицкий В.В., Соколова Л.А., Чесникова А.И., Добрынина Н.В., Якушин С.С. Оценка приверженности к лечению и факторов, влияющих на нее, у пациентов со стабильной ишемической болезнью сердца при назначении никорандила. Рациональная фармакотерапия в кардиологии 2017;13(6):776-86.
38. Martsevich SY, Lukina YV, Kutishenko NP, Semenova YV. Comparison of the outcomes of the prolonged antianginal therapy use in stable coronary artery disease patients according to the data of randomized and observational studies. Contemporary Clinical Trials Communications 2021 Feb;21:100743.
39. Foley M, Rajkumar CA, Shun-Shin M, Ganesananthan S, Seligman H, Howard J, Nowbar AN, Keeble TR, Davies JR, Tang KH, Gerber R, O’Kane P, Sharp ASP, Petraco R, Malik IS, Nijjer S, Sen S, Francis DP, Al-Lamee R. Achieving optimal medical therapy: insights from the ORBITA trial. Journal of the American Heart Association 2021 Feb;10(3):e017381.
40. Al-Lamee R, Thompson D, Dehbi HM, Sen S, Tang K, Davies J, Keeble T, Mielewczik M, Kaprielian R, Malik IS, Njjer SS, Petraco R, Cook C, Ahmad Y, Howard J, Baker C, Sharp A, Gerber R, Talwar S, Assomull R, Mayet J, Wensel R, Collier D, Shun-Shin M, Thom SA, Davies JE, Francis DP; ORBITA investigators. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. The Lancet 2018 Jan;391(10115):31-40.
41. Rajkumar CA, Foley MJ, Ahmed-Jushuf F, Nowbar AN, Simader FA, Davies JR, O’Kane PD, Haworth P, Routledge H, Kotecha T, Gamma R, Clesham G, Williams R, Din J, Njjer SS, Curzen N, Rupare-lia N, Sinha M, Dungu JN, Ganesananthan S, Khamis R, Mughal L, Kinnaird T, Petraco R, Spratt JC, Sen S, Sehmi J, Collier DJ, So-haib A, Keeble TR, Cole GD, Howard JP, Francis DP, Shun-Shin MJ, Al-Lamee RK; ORBITA-2 Investigators. A placebo-controlled trial of percutaneous coronary intervention for stable angina. The New England Journal of Medicine 2023 Dec;389(25):2319-30. s
Treatment of Angina: Potential of Nicorandil in Antianginal Therapy
Yu.A. Karpov
Coronary artery disease (CAD) does not only determine the duration of life, but also affects its quality. It follows that the main goal of CAD treatment is to reduce the risks of complications and improve the quality of life. Today 7 classes of antianginal, or antiischemic, drugs are used to improve the quality of life or eliminate the attacks of angina. Nicorandil has a special place among these classes, as it has a dual mechanism of action, activating adenosine triphosphate-sensitive potassium channels and demonstrating nitrate-like properties. Nicorandil is recommended when the first-line treatment appears ineffective and for patients with coronary microvascular disease. In addition to antianginal effect, the drug causes ischemic preconditioning, which allows reducing the risk of development of ischemic myocardial damage and myocardial infarction during elective percutaneous coronary intervention or prevent from reperfusion injury during revascularization in patients with acute coronary syndrome. Long-term administration of nicorandil in patients with stable angina decreases the risk of cardiovascular complications. For treatment of angina nicorandil (Cordinic, Pik-Farma) is used at a dose of 10-20 mg 1-3 times a day, maximum daily dose of 80 mg, usually as part of combined antianginal therapy with в-blockers or calcium channel blockers.
Keywords: coronary artery disease, antianginal therapy, nicorandil, ischemic preconditioning, percutaneous coronary intervention.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)










