Влияние фармакологического прекондиционирования никорандилом перед плановым чрескожным коронарным вмешательством на отдаленный прогноз больных стабильной ишемической болезнью сердца
Статьи
Опубликовано в журнале:
Rational Pharmacotherapy in Cardiology 2020; 16(2) / Рациональная Фармакотерапия в Кардиологии 2020; 16(2)
Галина Николаевна Соболева1*, Роман Витальевич Гостищев2, Анатолий Николаевич Рогоза1, Татьяна Ивановна Коткина1, Анатолий Николаевич Самко1, Юрий Александрович Карпов1
1 Национальный медицинский исследовательский центр кардиологии
Россия, 121552, Москва, ул. 3-я Черепковская, 15А
2 Медицинский центр «Новомосковский»
Россия, 129301, Москва, пос. Коммунарка, ул. Сосенский стан, 8
Цель. Изучить влияние назначения никорандила перед плановым чрескожным коронарным вмешательством (ЧКВ) на предупреждение повреждений миокарда и инфаркта миокарда (ИМ) 4а типа (первичной конечной точки) и развития сердечно-сосудистых событий (ССС) в течение года после планового ЧКВ (вторичной конечной точки) у больных стабильной ишемической болезнью сердца (ИБС).
Материал и методы. В исследование включено 182 пациента со стабильной ИБС, которые рандомизированы в группу лечения никорандилом (n=90) и группу контроля, стандартного лечения (n=92). Никорандил назначался внутрь: за 2 суток до ЧКВ – 30 мг/сут; в день ЧКВ – 20 мг за 2 ч до операции и 1 0 мг через 6-12 ч после ЧКВ; в последующие 30 дней – 30 мг/сут. Анализ высокочувствительного тропонина I (Вч-Тр) и МВ-креатинкиназы (КК-МВ) проводили до ЧКВ и спустя 24, 72 ч после процедуры, диагноз ИМ 4а типа выставлялся согласно 4-му универсальному определению. В качестве ССС оценивали нефатальный ИМ, нефатальное нарушение мозгового кровообращения, смерть от CCC, повторную реваскуляризацию коронарных артерий (ЧКВ, коронарное шунтирование в связи с ухудшением), госпитализации по поводу рецидива стенокардии (без вмешательств) и смерть от любых причин. Сбор информации о неблагоприятных событиях осуществляли за время пребывания пациентов в стационаре, и затем – через 30, 180 и 365 дней после выписки.
Результаты. ИМ 4а типа зарегистрирован у 14 (8%) пациентов, среди мужчин – 6%, среди женщин – 12%. При оценке влияния никорандила на развитие ИМ 4а типа отмечалось достоверное снижение частоты развития ИМ 4а типа в группе никорандила (n=3; 3%) по сравнению с группой контроля (n=11; 12%, p=0,05). Вторичная конечная точка зафиксирована у 21% пациентов. Установлена статистически значимая связь перенесенного ИМ 4а типа с частотой развития ССС в течение года после ЧКВ (p=0,0123). У пациентов с перенесенным ИМ 4а типа относительные шансы (ОШ) развития ССС возрастают в 5,8 раза при доверительном интервале (ДИ) от 1,5426 до 21,6024. По результатам логистического регрессионного анализа выявлена статистически значимая взаимосвязь между уровнем прироста Вч-Тр через 24 ч после ЧКВ и частотой развития ССС в течение года после ЧКВ, с отрезным значением в 389,8 пг/мл, AUC=0,641 (p=0,04).
Заключение. Назначение никорандила в пероральной форме за 2 суток до ЧКВ в дозе 30 мг/сут, в день ЧКВ – 20 мг за 2 ч до операции и 10 мг через 6-12 ч после ЧКВ, и, начиная с со следующего дня после ЧКВ – в дозе 30 мг/сут в течение месяца, по данным нашего исследования снижает риск интраоперационного ишемического повреждения миокарда и риска развития ССС в течение года после ЧКВ.
Ключевые слова: никорандил, коронарная ангиопластика, ишемическая болезнь сердца, фармакологическое прекондиционирование.
Для цитирования: Соболева П.Н., Гостищев Р.В., Рогоза А.Н., Коткина Т.И., Самко А.И., Карпов Ю.А. Влияние фармакологического прекондиционирования никорандилом перед плановым чрескожным коронарным вмешательством на отдаленный прогноз больных стабильной ишемической болезнью сердца. Рациональная Фармакотерапия в Кардиологии 2020;1 6(2):191-198. DOI:10.20996/1819-6446-2020-04-05
The Effect of Pharmacological Preconditioning with Nicorandil before Elective Coronary Stenting on the Long-Term Prognosis of Patients with Stable Coronary Artery Disease
Galina N. Soboleva1*, Roman V. Gostishchev2, Anatoly N. Rogoza1, Tatyana I. Kotkina1, Anatoly N. Samko1, Yurii A. Karpov1
1 National Medical Research Centre of Cardiology. Tretya Cherepkovskaya ul. 15A, Moscow, 121552 Russia
1 "Novomoskovsky" Medical Center. Sosenskiy Stan ul. 8, pos. Kommunarka, Moscow, 129301 Russia
Aim. To study nicorandil prescription effects before elective percutaneous coronary intervention (PCI) to prevent myocardial injury and 4a type acute myocardial infarction (MI, primary endpoint) and cardiovascular events (CVE) in the first year after PCI (secondary endpoint) in patients with stable coronary artery disease.
Material and methods. 182 patients with stable coronary artery disease were included into the study and were randomized into two groups: nicorandil treatment group (n=90) and a control group with a standard medical treatment (n=92). Nicorandil was prescribed orally: 2 days before PCI – 30 mg/day; on the day of PCI – 20 mg 2 hours before intervention and 10 mg 6-12 hours after PCI; over the next 30 days – 30 mg/day. High sensitivity troponin I (hs-Tr) and creatine kinase-MB tests were carried out before PCI, 24 and 72 hours after the intervention; the 4a type MI was diagnosed according to the 4th Universal Definition. Non-fatal myocardial infarction, nonfatal stroke, death from cardiovascular diseases, repeat revascularization (PCI, coronary artery bypass surgery due to aggravation), hospital admissions for angina pectoris recurrence (without interventions) and death from any causes were considered as cardiovascular events. Data on adverse outcomes were collected over the hospital stay, and then 30, 1 80 and 365 days after the hospital discharge.
Results. 4a type MI was diagnosed in 1 4 patients (8%), in women – 12% and in men – 6%. There was a significant decrease in the incidence of type 4a MI in the nicorandil group (n=3; 3%) compared with the control group (n=11; 12%; p=0.05). Secondary endpoint was recorded in 21% of patients. The relationship was found between 4a type MI and the incidence of CVE the next year after the PCI (p=0.01). In patients with type 4a MI CVE odd ratio increases 5.8 times with confidence interval from 1.5426 to 21.6024. According to the logistic regression analysis the significant relationship between hs-Tr growth 24 hours after the PCI and CVE incidence next year after the PCI was found with cutting value 389.8 pg/ml, AUC=0.641 (p=0.04).
Conclusion. Peroral nicorandil 30 mg/day 2 days before PCI, 20 mg 2 hours before surgery and 10 mg 6-12 hours after PCI, and 30 mg/day next 30 days after PCI decreases the risk of intraoperative myocardial injury and CVE in the next year after PCI.
Keywords: nicorandil, elective coronary stenting; stable coronary artery disease, pharmacological preconditioning.
For citation: Soboleva G.N., Gostishchev R.V., Rogoza A.N., Kotkina T.I., Samko A.N., Karpov Y.A. The Effect of Pharmacological Preconditioning with Nicorandil before Elective Coronary Stenting on the Long-Term Prognosis of Patients with Stable Coronary Artery Disease. Rational Pharmacotherapy in Cardiology 2020;16(2):191-1 98. DOI: 1 0.20996/181 9-6446-2020-04-05
Интраоперационное ишемическое повреждение миокарда даже при условии успешного проведения чрескожного коронарного вмешательства (ЧКВ) и стандартного медикаментозного сопровождения отмечается до 40% случаев [1]. Среди возможных причин повышения специфических маркеров некроза кардиомиоцитов (высокочувствительного тропонина [Вч-Тр], МВ-фракции креатинкиназы [КК-МВ]) – дистальная эмболия фрагментами атеросклеротической бляшки, коронарный тромбоз, диссекция интимы, ишемия миокарда вследствие баллонной инфляции. Даже при условии асимптомного повреждения и умеренного повышения кардиоспецифичных ферментов после ЧКВ в этой группе пациентов отмечается повышение уровня смертности в долгосрочном прогнозе [2,3]. С целью предупреждения интраоперационного ишемического повреждения миокарда перспективным представляется формирование до ЧКВ фармакологического прекондиционирования c применением пероральной формы препарата никорандил. Никорандил – гибрид эфира никотинамида и нитратной группы, отличается уникальными свойствами: он не только создает антиангинальные эффект, но и оказывает влияние на прогноз больных ишемической болезнью сердца (ИБС) [4]. Целью нашего исследования явилось определение влияния назначения никорандила (Кординик, компания ПИК-ФАРМА) перед плановым ЧКВ на предупреждение повреждения и инфаркта миокарда (ИМ) 4а типа (первичной конечной точки) и развития сердечно-сосудистых событий (ССС) в течение года после планового ЧКВ у больных стабильной ИБС (вторичной конечной точки).
Материал и методы
Критерии включения: мужчины и женщины в возрасте от 18 лет, со стабильной ИБС, с показаниями для проведения ЧКВ, нормальные уровни Вч-Тр и КК-МВ до ЧКВ. Критерии исключения: менее 3 мес после острого инфаркта миокарда (ОИМ); хроническая сердечная недостаточность III или IV функционального класса по классификации NYHA; выраженная брадикардия (частота сердечных сокращений [ЧСС]<50 уд/мин); атривентрикулярная блокада II и III степени; левожелудочковая недостаточность с фракцией выброса (ФВ ЛЖ)< 40%; артериальная гипотензия (систолическое АД в покое <100 мм рт.ст.; выраженная анемия; рефрактерная гиперкалиемия; одновременный прием ингибиторов фосфодиэстеразы-5; противопоказания к проведению коронароангиографии и ЧКВ; коллагенозы и воспалительные заболевания, онкологические заболевания, печеночная недостаточность, беременность и лактация; прием глибенкламида и/или глимепирида для контроля гликемии до ЧКВ; осложнения процедуры (окклюзия боковой ветви, диссекция коронарной артерии, острый тромбоз коронарной артерии), устранить которые к окончанию ЧКВ не удалось; прием антикоагулянтов.
Дизайн исследовательской работы утвержден этическим комитетом при НМИЦ кардиологии. Исследование проведено согласно требованиям Хельсинкской декларации и надлежащей клинической практики (GCP – Good Clinical Practice). Всеми участниками исследования подписаны информированные согласия о включении в исследовательскую работу. Методом рандомизации (конвертов) с нивелированием отличий по полу и возрасту организованы две группы наблюдения: группа 1 – базовая антиангинальная терапии (группа контроля) и группа 2 – к базовой терапии был добавлен никорандил (Кординик, компания ПИК-ФАРМА). Базовая терапия бета-адреноблокаторами, антагонистами кальция, ингибиторами АПФ/блокаторами рецепторов ангиотензина II, статинами, ацетилсалициловой кислотой, тиенопиридинами назначалась в 1 и 2 группе, в группе контроля было возможно назначение нитратов. Обе группы больных сформированы из пациентов, поступивших в НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии для планового ЧКВ, давших информированное согласие на участие в данном исследовании. Никорандил за 2 сут до ЧКВ назначался в дозе 30 мг/сут, в день ЧКВ, за 2 ч до операции – 20 мг внутрь, 10 мг через 6-12 ч после ЧКВ и, начиная со следующего дня после ЧКВ – в дозе 30 мг/сут в течение 28 дней. Биомаркеры необратимого повреждения миокарда Вч-Тр и КК-МВ оценивались за сут до планового ЧКВ, через 24 и 72 ч после проведения ЧКВ. Изменения на электрокардиограмме (ЭКГ) оценивались до ЧКВ, во время ЧКВ и через 24 и 72 ч после ЧКВ. Дизайн исследования схематично представлен на рис. 1.
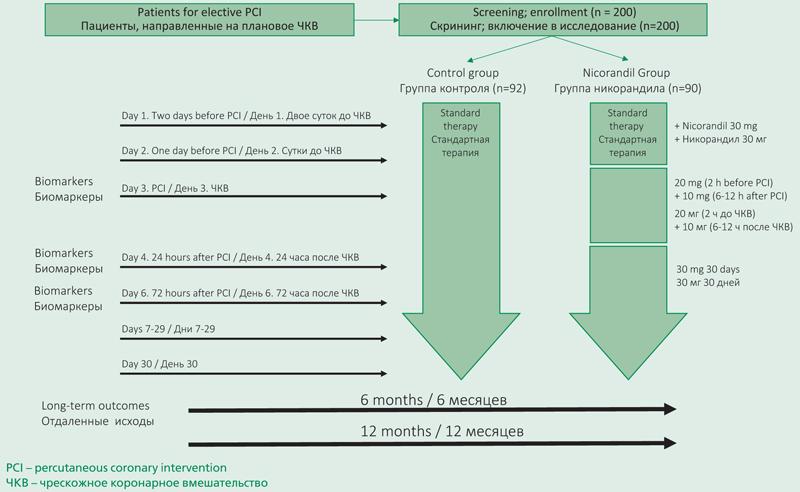 Figure 1. Study design
Figure 1. Study design
Рисунок 1. Дизайн исследования
Всем пациентам, включенным в данное исследование, выполнялось стентирование коронарных артерий с установкой стента с лекарственным покрытием, на фоне двойной антиагрегантной терапии.
Определение Вч-Тр проводили на диагностическом приборе ARCHITECT i1000SR с использованием специализированного теста STAT HS Trop-I. Превышение значения Вч-Тр выше 99 перцентиля от верхней границы нормы (ВГН) определяли как повышенное значение. Другой специфический кардиофермент, отражающий повреждение кардиомиоцитов, КК-МВ определяли на аналогичной системе ARCHITECT i1000SR.
В качестве первичной композитной конечной точки были приняты такие события как перипроцедурные повреждения и ИМ 4а типа. Перипроцедурным повреждением считали повышение Вч-Тр выше ВГН без клинических проявлений ишемии миокарда, ИМ 4а типа оценивали в соответствии с критериями IY универсального определения ИМ [5]. В качестве вторичной композитной точки оценивалась частота развития таких сердечно-сосудистых событий (ССС), как нефатальный ИМ, нефатальное НМК, смерть от CCC, повторная реваскуляризация коронарных артерий (ЧКВ, аорто-коронарное шунтирование [АКШ] в связи с ухудшением), случай госпитализации по поводу рецидива стенокардии (без вмешательств) и смерть от любых причин. Сбор информации о неблагоприятных событиях осуществляли за время пребывания пациентов в стационаре, и, затем через 30, 180 и 365 дней после выписки на очном приеме или посредством телефонного контакта.
Для количественных данных определяли среднее значение, среднеквадратическое отклонение, ошибку среднего, медиану, 25-й и 75-й процентили. Для анализа качественных переменных использовались показатели частоты в процентах. Для данных, лежащих в границах нормального распределения, выполняли статистический анализ с использованием критерия Пирсона и t-критерия Стьюдента. Для сравнения данных, не соответствующих нормальному распределению, использовался непараметрический тест Манна-Уитни. Статистически значимыми считались различия при p<0,05.
Ряд переменных описывался посредством RОС-анализа. Степень отклонения соответствует AUC (area under ROC curve, площадь под кривой) и увеличивается по мере влияния изучаемого фактора. Качество модели ROC определяли по шкале: 0,9-1,0 – отличное; 0,8-0,9 – очень хорошее; 0,7-0,8 – хорошее; 0,6-0,7 – среднее; до 0,6 – неудовлетворительное.
Статистическая обработка материала осуществлялась с использованием программного обеспечения Statistica (Statsoft Inc., США).
Результаты
После рандомизации 90 больных включено в группу лечения никорандилом и 92 больных – в группу контроля. У 167 человек имелись результаты анализов Вч-Тр и КК-МВ до и после вмешательства. Две группы, контроля и никорандила, сопоставимы по основным клиническим показателям (табл. 1). Различия в значениях клиренса креатинина, рассчитанного по разным методикам, не считали истинно достоверными, так как эти показатели находились в пределах нормальных значений.
Table 1. Clinical parameters of patients in the studied groups
Таблица 1. Клинические параметры пациентов изучаемых групп
| Параметр | Группа контроля (n=92) | Группа никорандила (n=90) | p
|
| Возраст, лет | 66 (58;73,5) | 64 (58;71) | 0,35 |
| Мужской пол, n (%) | 63 (68) | 58 (64) | 1 |
| ИМТ, кг/м² | 29 (26;32) | 29,5 (26;32) | 0,87 |
| Длительность анамнеза ИБС, годы | 5,5 (2;10) | 4 (2;10) | 0,22 |
| ИМ в анамнезе | 44 (48) | 41 (46) | 0,76 |
| Сахарный диабет, n (%) | 21 (23) | 24 (27) | 0,6 |
| Артериальная гипертония, n (%) | 85 (92) | 82 (91) | 0,79 |
| ФВЛЖ, % | 60 (55;60) | 60 (56;60) | 0,88 |
| Общий холестерин при поступлении, ммоль/л | 4,1 (3,5;5,1) | 4,0 (3,5;4,8) | 0,82 |
| ЛПНП при поступлении, ммоль/л | 2,1 (1,7;2,9) | 2,2 (1,8;3,7) | 0,73 |
| Вч-Тр при поступлении, пг/мл | 4,2 (2,6;7,6) | 5,1 (3,0;11,8) | 0,21 |
| КК-МВ при поступлении, нг/мл | 1,3 (0,8;1,8) | 1,2 (0,8;1,8) | 0,52 |
| СКФ (CKD-EPI), мл/мин | 82,8 (69,6;99,0) | 91,0 (76,8;103,1) | 0,03 |
ИМТ – индекс массы тела, ИБС – ишемическая болезнь сердца, ИМ – инфаркт миокарда, ФВЛЖ – фракция выброса левого желудочка, ЛПНП – липопротеины низкой плотности, Вч-Тр – высокочувствительный тропонин, КК-МВ – МВ креатинкиназа, СКФ – скорость клубочковой фильтрации
Развитие первичной конечной точки в виде повреждения миокарда зафиксировано у 146 (80%) пациентов. Обнаружена тенденция к более сдержанному повышению уровня среднего значения Вч-Тр через 24 ч в группе никорандила по сравнению с группой контроля: 364 пг/мл против 725 пг/мл (p=0,1). В группе контроля средний прирост Вч-Тр через 24 ч после ЧКВ составил 735,22 пг/мл, в группе никорандила – 260,31 пг/мл (p=0,21). В группе контроля статистически значимо чаще встречались случаи прироста Вч-Тр – более чем на 2000 пг/мл у 8 (10%) пациентов в группе контроля против 1 (1%) пациента в группе никорандила (p=0,038). При анализе прироста КК-МВ через 24 ч после ЧКВ выявлена тенденция: в группе контроля средняя величина прироста КК-МВ достигла 2,5 нг/мл против 0,5 нг/мл в группе никорандила (p=0,06). Более подробная характеристика динамики маркеров кардионекроза нами представлена в предыдущей публикации [6].
Первичная конечная точка в виде ИМ 4а типа зарегистрирована у 14 (8%) пациентов, среди мужчин – 6%, среди женщин – 12%. При оценке влияния никорандила на развитие ИМ 4а типа отмечалось статистически значимое снижение частоты развития ИМ4а типа в группе никорандила (3%) по сравнению с группой контроля (12%; p=0,05). При разделении пациентов на мужскую и женскую подгруппы установлено, что ИМ 4а типа развился у 8% мужчин в группе контроля и у 3% мужчин в группе никорандила, тогда как среди женщин ИМ 4а типа зарегистрирован у 21% в группе контроля и у 3% женщин в группе никорандила (Рис. 2).
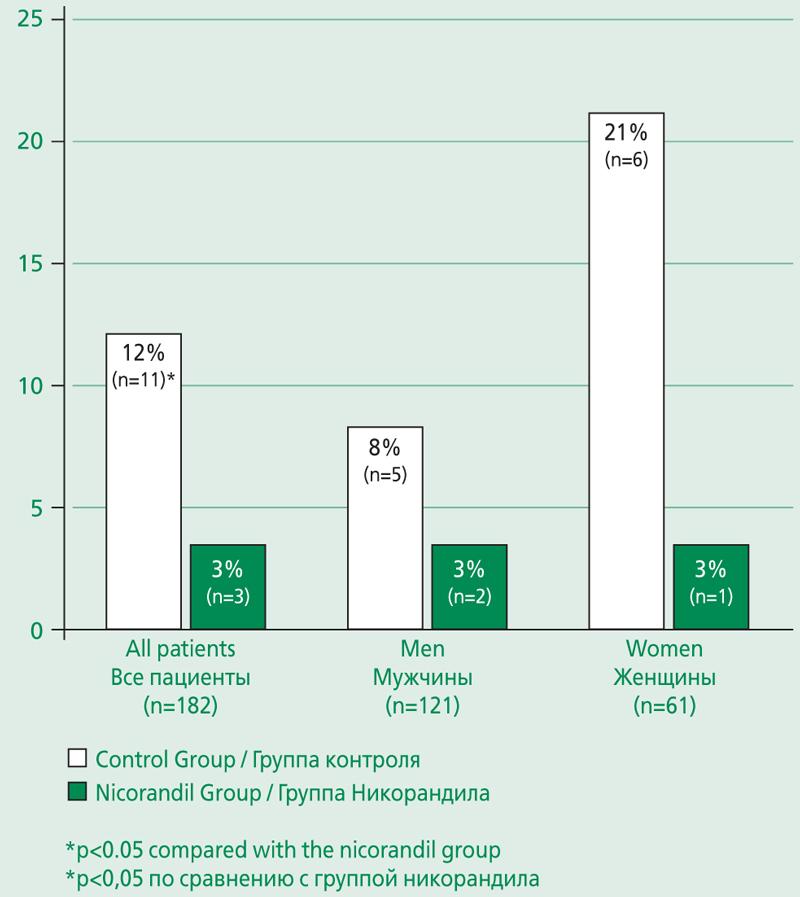 Figure 2. The incidence of type 4a myocardial infarction in the study groups
Figure 2. The incidence of type 4a myocardial infarction in the study groups
Рисунок 2. Частота встречаемости инфаркта миокарда 4а типа в изучаемых группах
Отдаленные результаты ЧКВ в группе контроля и в группе никорандила удалось собрать у 159 пациентов из 182, изначально включенных в исследование. Частота развития вторичной конечной точки – ССС (смерть от сердечно-сосудистых причин, ИМ, острое нарушение мозгового кровообращения, повторная коронарная реваскуляризация, госпитализация по поводу рецидива стенокардии, смерть от всех причин) – в течение года после ЧКВ составила 21% (табл. 2). За период наблюдения зафиксировано 3 смертельных исхода, один из которых – по причине прогрессирования сердечно-сосудистого заболевания. В двух других смертельных исходах выяснить причины не удалось.
Table 2. The incidence of cardiovascular events the next year after percutaneous coronary intervention
Таблица 2. Частота развития ССС в течение года после ЧКВ
| Вторичная конечная точка | n (%)
|
| Смерть от сердечно-сосудистых причин | 1 (0,6) |
| ИМ | 2 (1,3) |
| ОНМК | 1 (0,6) |
| Повторное ЧКВ | 7 (4,5) |
| Коронарное шунтирование | 1 (0,6) |
| Госпитализация в связи с рецидивом стенокардии | 19 (12) |
| Смерть от всех причин | 3 (1,9) |
| Всего | 33 (21) |
ССС – сердечно-сосудистые события, ИМ – инфаркт миокарда, ОНМК – острое нарушение мозгового кровообращения, ЧКВ – чрескожное коронарное вмешательство
Более детальный анализ факторов, ассоциированных с развитием ССС в течение года после ЧКВ, выполнялся с применением ROC-анализа. Для каждого возможного фактора-кандидата строилась ROC-кривая. Из нее оценивалась «диагностическая значимость показателя» и определялось оптимальное «отрезное» значение. Далее данный показатель кодировался «0» или «1» на основе отрезных значений. После этого проводилось построение логистической регрессии, которая оценивала снижение шансов.
Логистический регрессионный анализ не выявил статистически значимой связи числа пораженных сосудов с частотой развития ССС в течение года после ЧКВ (p=0,44). ROC анализ также не подтвердил прогностическую значимость данного показателя. Площадь под кривой (AUC) составила 0,558 при 95% ДИ от 0,478 до 0,637 (табл. 3). Также по результатам логистического регрессионного анализа не выявлено статистически значимой связи числа пораженных бассейнов коронарных артерий с ССС (p=0,30). Не удалось установить статистически значимой связи между наличием стенозов в артериях, не подвергнутых ЧКВ, после операции и частотой развития ССС в течение года после ЧКВ (p=0,22). Также не удалось получить статистически значимого результата при проведении логистического регрессионного анализа влияния приема никорандила на развитие ССС в течение года после ЧКВ, но установлено, что шансы развития ССС в группе контроля увеличиваются в 1,6 раз (p=0,27) (табл. 3).
Логистический регрессионный анализ выявил статистически значимую связь пола с частотой развития ССС в течение года после ЧКВ (p=0,0310), уровень статистической значимости для включения данного показателя в модель прогноза – 0,0304. У женщин ОШ развития ССС в течение года после ЧКВ возрастают в 2,5 раза при ДИ от 1,1 до 5,9. Логистический регрессионный анализ с дифференциацией пациентов по показателю пола установил тенденцию снижения частоты развития ССС в течение года после ЧКВ и приема никорандила в течение года после ЧКВ у женщин. Уровень статистической значимости модели составил p=0,1, отношение рисков 2,7 (табл. 3).
Table 3. Risk factors for cardiovascular events the next year after percutaneous coronary intervention (logistic regression analysis)
Таблица 3. Факторы, влияющие на развитие ССС в течение года после ЧКВ по результатам логистического регрессионного анализа
| Кандидаты на анализ влияния на ССС в течение года после ЧКВ | Уровень статистической значимости модели (p)
|
| Количество пораженных сосудов | 0,44 |
| Количество пораженных сосудистых бассейнов | 0,30 |
| Количество стенозов в артериях, не подвергнутых ЧКВ | 0,22 |
| Курение | 0,16 |
| Суммарная длина установленных стентов | 0,54 |
| Диаметр стентов | 0,50 |
| Давление предилатации | 0,57 |
| Суммарное время дилатации | 0,65 |
| Количество установленных стентов | 0,08 |
| Женский пол | 0,03 |
| Никорандил у женщин | 0,11 |
| Никорандил у мужчин | 0,85 |
| Прирост Вч-Тр через 24 ч после ЧКВ | 0,04 |
| ИМ 4а типа | 0,0123 |
ССС – сердечно-сосудистые события, Вч-Тр – высокочувствительный тропонин, ЧКВ – чрескожное коронарное вмешательство, ИМ – инфаркт миокарда
Установлена статистически значимая связь перенесенного ИМ 4а типа с частотой развития ССС в течение года после ЧКВ (p=0,0123). Таким образом, у пациентов с перенесенным ИМ 4а типа ОШ развития ССС возрастают в 5,8 раза при ДИ от 1,5426 до 21,6024 (табл. 3).
Также по результатам логистического регрессионного анализа выявлена статистически значимая взаимосвязь между уровнем прироста Вч-Тр через 24 ч после ЧКВ и частотой развития ССС в течение года после ЧКВ, с отрезным значением в 389,8 пг/мл, AUC=0,641 (p=0,04; рис. 3).
При этом логистический регрессионный анализ с дифференциацией пациентов по показателю пола установил тенденцию снижения частоты развития ССС в течение года после ЧКВ и приема никорандила в течение года после ЧКВ у женщин. Уровень статистической значимости модели составил p=0,1, отношение рисков 2,7 (табл. 3).
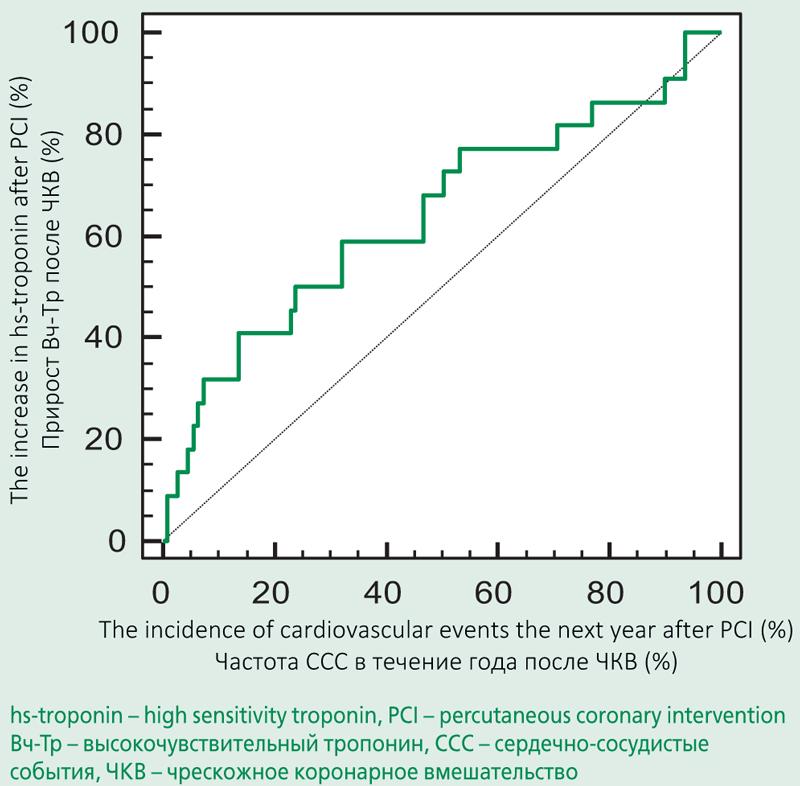 Figure 3. ROC-curve of the growth of hs-troponin after percutaneous coronary intervention and the incidence of cardiovascular events during the year after PCI
Figure 3. ROC-curve of the growth of hs-troponin after percutaneous coronary intervention and the incidence of cardiovascular events during the year after PCI
Рисунок 3. График ROC-кривой зависимости степени прироста Вч-Тр после ЧКВ и частоты развития ССС в течение года после ЧКВ
Обсуждение
Ишемическое повреждение миокарда, как и ИМ, может возникать на определенных этапах манипуляций, производимых на коронарных артериях во время ЧКВ. Повышенные уровни Вч-Тр и КК-МВ могут быть обусловлены ишемическим повреждением или некрозом миокарда вследствие диссекции и/или окклюзии коронарной артерии, феномена no-reflow или slow-reflow,, и др. Очевидно, что ограничение риска развития таких повреждений благоприятно для пациента, доказана связь между пиковыми концентрациями Вч-Тр и прогнозом жизни больных ИБС [7].
На сегодняшний день существует внушительная доказательная база по применению никорандила в пероральной и парентеральной формах у пациентов с ОИМ с целью предупреждения реперфузионного повреждения и снижения показателей летальности в ранние и отдаленные сроки после перенесенного ОИМ [8,9]. Также есть данные о снижении летальности после назначения пероральной формы никорандила больным с ОИМ [10]. Опираясь на результаты этих работ, мы предприняли попытку обеспечить эффект фармакологического прекондиционирования препаратом никорандил у больных стабильной ИБС перед плановым ЧКВ.
Временные интервалы назначения препарата перед ЧКВ были нами рассчитаны, исходя из параметров фармакокинетики препарата и доказанного в эксперименте времени наступления эффекта прекондиционирования [11]. Препарат назначали в минимальной суточной дозе (30 мг/сут) с целью повышения толерантности к терапии, перед ЧКВ назначали максимально допустимую разовую дозу – 20 мг за 2 ч до процедуры, так как именно в этом временном интервале достигается эффект фармакологического прекондиционирования. В дальнейшем в течение 28 дней после ЧКВ никорандил назначали 30 мг/сут для поддержания эффекта фармакологического прекондиционирования в послеоперационном периоде.
Результаты нашего исследования свидетельствуют о тенденции уменьшения средних уровней Вч-Тр через 24 ч после ЧКВ у пациентов, принимавших никорандил по предложенной схеме по сравнению с таковыми у пациентов, принимавших стандартную антиангинальную терапию (364 пг/мл в группе никорандила против 725 пг/мл в группе контроля, p=0,1).
Также в нашем исследовании было обнаружено, что превышение ВГН Вч-Тр более, чем на 2000 единиц статистически значимо чаще случалось в группе контроля по сравнению с группой никорандила (10% против 1%, p=0,038). При анализе превышения ВГН на 1000 единиц установлено, что подобные явления имели место в 3 раза чаще у пациентов из группы контроля по сравнению с группой никорандила (16% против 5%, однако степень доказательности установлена на уровне тенденции, p=0,07).
Анализ динамики КК-МВ выявил возможность никорандила нивелировать ишемическое повреждение миокарда при плановом ЧКВ. Так, медианный уровень КК-МВ через 24 ч после ЧКВ в группе никорандила составил 2,30 нг/мл против 2,05 нг/мл в группе контроля, p=0,08. При этом средняя степень прироста КК-МВ в группе никорандила была также ниже по сравнению с группой контроля (0,48 нг/мл против 1,05 нг/мл, p=0,06). Полученные данные соответствуют результатам других ранее опубликованных исследований никорандила [8,1 2].
По результатам нашего исследования установлено, что ИМ 4а типа встречался у 8% пациентов, при этом у женщин чаще, чем у мужчин (12% против 6%). Полученные данные соответствуют исследованиям, в которых частота развития ИМ 4а типа варьирует от 5 до 30% [1,13]. Установленный нами факт снижения первичной конечной точки (развитие ИМ 4а) в 4 раза в группе никорандила является непреложным доказательством эффекта фармакологического прекондиционирования этого препарата.
Существуют гендерные различия в оценке прогноза заболевания после перенесенного ЧКВ. В ряде работ продемонстрирован более высокий риск осложнений ЧКВ у женщин по сравнению с мужчинами [14,15]. По результатам нашего исследования у женщин вдвое чаще встречались превышения ВГН Вч-Тр (40% против 70%, p=0,048), также чаще развивался ИМ 4а типа (21% против 3%, p<0,05). Ухудшению исходов у женщин могут способствовать такие факторы, как меньший диаметр сосудов, чем у мужчин, что повышает сложность ЧКВ и риск повреждения сосудов, а также активация эстрогеном системы свертывания и воспаления [16,1 7].
Нами было продемонстрировано, что частота наступления вторичной конечной точки (ССС в течение года после ЧКВ) у женщин по сравнению с мужчинами была выше как в группе контроля (36% против 13%), так и в группе никорандила (17% против 12%). Установлена тенденция снижения частоты развития ССС в течение года после ЧКВ и приема никорандила в течение года после ЧКВ у женщин. Нами установлено, что никорандил способен нивелировать различия в исходах после ЧКВ между мужчинами и женщинами, и этот эффект может быть обеспечен уникальным свойством препарата корригировать дисфункцию микроциркуляции миокарда, столь значимой в становлении ишемии миокарда у женщин [18].
Результаты нашего исследования демонстрируют статистически значимое влияние ИМ 4а типа на повышение риска развития ССС в течение года после ЧКВ. Так, среди пациентов, имевших ССС в отдаленном периоде после ЧКВ, ИМ 4а типа был зарегистрирован в 19% случаев, в то время как пациенты без развития ССС в отдаленном периоде после ЧКВ имели частоту развития ИМ 4а типа в 4% случаев (p=0,024). Были определены и другие факторы, способствующие развитию ССС в течение года после ЧКВ: женский пол (p=0,03), количество установленных стентов (p=0,08). Этот факт подтверждается данными M. Zeitouni с соавт. [19], в котором установлено, что ИМ 4а типа и повреждение миокарда связаны с повышенной частотой сердечно-сосудистых событий в последующие 30 дней и 1 год наблюдения после ЧКВ.
Заключение
Назначение никорандила (Кординик, компания ПИК-ФАРМА) в пероральной форме за 2 суток до ЧКВ в дозе 30 мг/сут, в день ЧКВ – за 2 ч до операции – 20 мг и 10 мг через 6-12 ч после ЧКВ, и, начиная с со следующего дня после ЧКВ – в дозе 30 мг/сут в течение месяца – по данным нашего исследования снижает риск интраоперационного ишемического повреждения миокарда и риска развития ССС в течение года после ЧКВ.
Конфликт интересов. Публикация статьи поддержана компанией ПИК-ФАРМА, что никоим образом не повлияло на собственное мнение авторов.
Disclosures. The publication of the article is supported by the PIQ-PHARMA Group of Companies, but it did not affect own opinion of the authors.
References / Литература
- Califf R.M., Abdelmeguid A.E., Kuntz R.E., et al. Myonecrosis after revascularization procedures. J Am Coli Cardiol. 1998;31:241-51. DOI:10.1016/s0735-1097(97)00506-8.
- Lindsey J.B., Marso S.P., Pencina M., et al. Prognostic impact of periprocedural bleeding and myocardial infarction after percutaneous coronary intervention in unselected patients: results from the EVENT (evaluation of drug-eluting stents and ischemic events) registry. JACC Cardiovasc Interv. 2009;2:1074-82. DOI:10.1016/j.jcin.2009.09.002.
- Sakata Y., Nakatani D., Shimizu M., et al. Oral treatment with nicorandil at discharge is associated with reduced mortality after acute myocardial infarction. J Cardiol. 2012;59(1):14-21. DOI:10.1016/j.jjcc.2011.08.001.
- IONA Study Grup. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA): randomized trial. Lancet. 2002;359(9314):1269-75. DOI:10.1016/S0140-6736(02)08265-X.
- Thygesen K., Alpert J.S., Jaffe A.S., et al., ESC Scientific Document Group; Fourth universal definition of myocardial infarction. Eur Heart J. 2019;40(3):237-69. DOI:10.1093/eurheartj/ehy462.
- Soboleva G.N., Gostishchev R.V., Rogoza A.N., et al. Nicorandil in the prevention of damage and myocardial infarction of type 4A with planned percutaneous coronary intervention in patients with coronary artery atherosclerosis. Russian Journal of Cardiology. 2019;5:44-51 (In Russ.) [Соболева Г.Н., Гостищев Р.В., Рогоза А.Н., и др. Никорандил в предупреждении повреждения и инфаркта миокарда 4А типа при плановом чрескожном коронарном вмешательстве у больных с атеросклерозом коронарных артерий. Российский Кардиологический Журнал. 2019;5:44-51].
- Jansen H., Jaensch A., Schottker B., et al. Repeat Measurements of High Sensitivity Troponins for the Prediction of Recurrent Cardiovascular Events in Patients With Established Coronary Heart Disease: An Analysis From the KAROLA Study, J Am Heart Assoc. 2019;8(12):e011882. DOI:10.1161/JAHA.118.011882.
- Kawai Y., Hisamatsu K., Matsubara H. et al. Intravenous administration of nicorandil immediately before percutaneous coronary intervention can prevent slow coronary flow phenomenon. Eur Heart J. 2009;30(7):765-72. DOI:10.1093/eurheartj/ehp077.
- Lee H.C., An S.G., Choi J.H., et al. Effect of intra-coronary nicorandil administration prior to reperfusion in acute ST segment elevation myocardial infarction. Circ J. 2008;72(9):1 425-9, DOI:10.1253/circj, cj-08-0212.
- Sakata Y., Nakatani D., Shimizu M., et al. Oral treatment with nicorandil at discharge is associated with reduced mortality after acute myocardial infarction. J Cardiol. 2012;59(1):14-21. DOI:10.1016/j.jjcc.2011.08.001.
- Yang J., Zhang J., Cui W., et al. Cardioprotective effects of single oral dose of nicorandil before selective percutaneous coronary intervention. Anatolian J Cardiol. 2015;15:125-31. DOI:10.5152/akd.2014.5207.
- Zhao X.T., Zhang C.F., Liu Q.J. Meta-analysis of Nicorandil effectiveness on myocardial protection after percutaneous coronary intervention. BMC Cardiovasc Disord. 2019;19(1):144. DOI:10.1186/s12872-019-1071-x.
- Mironova O.Y. Myocardial infarction type 4a. Ter Arkchiv, 2014;9:102-7 (In Russ.) [Миронова О.Ю. Инфаркт миокарда типа 4а. Терапевтический Архив. 2014;9:102-7].
- Jackson E.A., Moscucci M., Smith D.E., et al. Tne association of sex with outcomes among patients undergoing primary percutaneous coronary intervention for ST elevation myocardial infarction in the contemporary era: insights from the Blue Cross Blue Shield of Michigan Cardiovascular Consortium (BMC2). Am Heart J. 2011;161:106-12e1. DOI:10.1016/j.ahj.2010.09.030.
- Chichareon P., Modolo R., Kerkmeijer L., et al. Association of Sex With Outcomes in Patients Undergoing Percutaneous Coronary Intervention: A Subgroup Analysis of the GLOBAL LEADERS Randomized Clinical Trial. JAMA Cardiol. 2019;6:1-10. DOI:10.1001/jamacardio.2019.4296.
- Cantor WJ., Miller J.M., Hellkamp A.S., et al. Role of target vessel size and body surface area on outcomes after percutaneous coronary interventions in women. Am Heart J. 2002;144:297-302. DOI:10.1067/mhj.2002.123318.
- Mahajan A.M., Claessen B.E., Chandrasekhar J., et al. Outcomes by Gender and Ethnicity After Percutaneous Coronary Intervention. Am J Cardiol. 2019;123(12):1941-8. DOI:10.1016/j.amj-card.2019.03.019.
- Hirohata A., Yamamoto K., Hirose E., et al. Nicorandil prevents microvascular dysfunction resulting from PCI in patients with stable angina pectoris: a randomised study EuroIntervention. 2014;9(9): 1050-6, DOI:10.4244/EJV9I9A178.
- Zeitouni M., Silvain J., Guedeney P., et al.; ACTION Study Group. Periprocedural myocardial infarction and injury in elective coronary stenting. Eur Heart J. 2018;39:1100-9. DOI:10.1093/eurheartj/ehx799.
About the Authors:
Galina N. Soboleva – MD, PhD, Leading Researcher, Angiology Department, Research Institute of Clinical Cardiology named after A.L. Myasnikov, National Medical Research Center of Cardiology
Roman V. Gostishchev – MD, Deputy Head Physician, "Novomoskovsky" Medical Center
Anatoly N. Rogoza – PhD (biology), Head of New Diagostic Methods Department, Research Institute of Clinical Cardiology named after A.L.Myasnikov, National Medical Research Center of Cardiology
Tatyana I. Kotkina – MD, PhD, Physician, Clinical Biochemistry Laboratory, Research Institute of Clinical Cardiology named after A.L. Myasnikov, National Medical Research Center of Cardiology
Anatoly N. Samko – MD, PhD, Head of Endovascular Diagnostic and Treatment Methods, Research Institute of Clinical Cardiology named after A.L. Myasnikov, National Medical Research Center of Cardiology
Yurii A. Karpov – MD, PhD, Head of Angiology Department, Research Institute of Clinical Cardiology named after A.L. Myasnikov, National Medical Research Center of Cardiology
Сведения об авторах:
Соболева Галина Николаевна – д.м.н., в.н.с., отдел ангиологии, НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии
Гостищев Роман Витальевич – зам. главного врача, медицинский центр «Новомосковский»
Рогоза Анатолий Николаевич – д.б.н, руководитель отдела новых методов диагностики, НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии
Коткина Татьяна Ивановна – к.м.н., врач, лаборатория клинической биохимии, НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии
Самко Анатолий Николаевич – д.м.н., профессор, руководитель отдела рентгенэндовскулярных методов лечения, НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии
Карпов Юрий Александрович – д.м.н., профессор, руководитель отдела ангиологии, НИИ клинической кардиологии им. А.Л. Мясникова, НМИЦ кардиологии
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)


 Figure 1. Study design
Figure 1. Study design  Figure 2. The incidence of type 4a myocardial infarction in the study groups
Figure 2. The incidence of type 4a myocardial infarction in the study groups  Figure 3. ROC-curve of the growth of hs-troponin after percutaneous coronary intervention and the incidence of cardiovascular events during the year after PCI
Figure 3. ROC-curve of the growth of hs-troponin after percutaneous coronary intervention and the incidence of cardiovascular events during the year after PCI 
