Возможности никорандила в коррекции коронарного резерва и эндотелиальной дисфункции у больных ишемической болезнью сердца
Статьи
Опубликовано в журнале:
«Сердце: журнал для практикующих врачей», 2013, Том 12, № 2 (70), с. 75-82
Сизова Ж. М.1, Захарова В. Л.1, Шамиева Е. С.2, Козлова Н. В.1
1 – ГБОУ ВПО «Первый МГМУ имени И. М. Сеченова» МЗ РФ, 119991, Москва, ул. Трубецкая, д. 8, стр. 2
2 – ГБУ «Кардиологический диспансер № 2» ДЗ г. Москвы, 117556, Москва, ул. Фруктовая, д. 12
Ишемическая болезнь сердца является важнейшей медико-социальной проблемой в связи с большой распространенностью, тяжестью осложнений, моральным и материальным ущербом, наносимым обществу. Несмотря на накопленный опыт применения лекарственных средств для лечения больных ИБС, ССЗ являются основной причиной инвалидизации и смертности в экономически развитых странах; при этом на долю ИБС и ИМ приходится примерно две трети случаев смерти от сердечно-сосудистой патологии [1]. Уровень ежегодной смертности больных стабильной стенокардией, самой многочисленной группы больных ИБС, составляет 2–3 % [2]. Однако качество жизни этих больных, как правило, низкое, со значительными ограничениями в повседневной жизни, главным образом, из-за возникающих приступов стенокардии. В связи с этим лечение больных стабильной стенокардией по-прежнему находится в центре внимания практических врачей.
Основной целью фармакотерапии таких больных является в первую очередь предотвращение возникновения ИМ и внезапной смерти (улучшение прогноза), а также полное купирование или, по крайней мере, уменьшение частоты приступов стенокардии и безболевой ишемии миокарда, т. е. улучшение качества жизни больных.
В современном арсенале кардиологов имеется три группы базисных антиангинальных лекарственных средств: нитропрепараты, блокаторы β-адрено-рецепторов и ACa2+, объективно влияющих на качество жизни больных ИБС. Однако влияние на клинические исходы ИБС доказано только для некоторых блокаторов β-адренорецепторов по отношению к больным ИБС с перенесенным ИМ и для верапамила по отношению к больным ИБС с АГ, к применению которых имеется целый ряд противопоказаний [3–6].
Традиционно для устранения и уменьшения частоты приступов стенокардии используются нитраты. Эти препараты, уже давно применяющиеся в клинической практике, повышают толерантность к физической нагрузке, увеличивают время до появления приступа стенокардии и уменьшают депрессию сегмента ST на ЭКГ при нагрузке [3].
В последние годы число нитропрепаратов увеличилось, появились новые лекарственные формы, расширился спектр их применения. Однако нитраты нередко дают побочные эффекты, наиболее частым из которых является появление головной боли. Другой причиной, лимитирующей назначение нитратов у больных со стабильной стенокардией, является развитие толерантности к ним. Степень развития привыкания к нитратам в значительной мере варьирует у разных больных, причем неизвестно какие индивидуальные особенности влияют на развитие этого явления. Показано, что при регулярном назначении изосорбида динитрата в дозе 10–20 мг 4 раза в сутки в течение 1 месяца полная потеря эффекта наступает у 10–15 % больных со стабильной стенокардией напряжения [3].
При назначении нитратов следует помнить о наличии противопоказаний к ним. Эти препараты следует назначать с осторожностью больным ИБС с пониженным АД. Нитраты противопоказаны при повышенном внутричерепном давлении, кровоизлиянии в головной мозг, они могут увеличить степень обструкции у больных с гипертрофической кардиомиопатией, степень регургитации при гемодинамически значимом пролапсе митрального клапана.
Это диктует необходимость дальнейшего поиска и совершенствования антиангинальной терапии. В этой связи значительный интерес представляет изучение антиангинальной эффективности препаратов достаточно перспективной группы модуляторов (активаторов) калиевых каналов, наиболее известным представителем которых является никорандил.
Никорандил-2-никотиноиламидоэтилнитрат (международное непатентованное название – никорандил) – принципиально новое антиангинальное лекарственное средство: помимо нитратной группы, содержит фрагмент витамина РР. Действие никорандила основано на сочетании нитратоподобных свойств и способности открывать АТФ-зависимые калиевые каналы. Нитратоподобный эффект заключается в увеличении внутриклеточного содержания циклического гуанилмонофосфата и, как следствие, приводит к увеличению продукции эндотелийзависимого фактора релаксации, что ведет к расслаблению гладких мышц кровеносных сосудов, особенно вен. Открывая АТФ-зависимые калиевые каналы клеточной мембраны, никорандил вызывает ее гиперполяризацию, что приводит к расслаблению гладких мышц сосудов артерий и артериол (снижение коронарного сопротивления), к закрытию потенциалзависимых кальциевых каналов (снижение влияния перегрузкой ионами кальция), к предотвращению гиперсокращения кардиомиоцитов во время реоксигенации – основного фактора повреждения миокарда при реперфузионном синдроме, к укорочению интервала действия и рефрактерного периода (действие на проаритмические факторы). Открытие никорандилом АТФ-зависимых калиевых каналов внутренней мембраны митохондрии активирует поступление ионов калия в митохондриальный матрикс, вызывая деполяризацию внутренней мембраны, ослабление влияния перегрузкой ионами кальция и набухание митохондрий во время ишемии, тогда как при отсутствии ишемии способствует образованию сублетальных уровней активных форм кислорода – одного из ключевых медиаторов механизма ишемического прекондиционирования, т. е. осуществляет фармакологическое прекондиционирование. Кроме того, открытие митохондриальных АТФ-зависимых калиевых каналов и образование сублетальных уровней активных форм кислорода ингибирует фатальное открытие митохондриальной поры с транзиторной проницаемостью, так называемой мегапоры или мегаканала, что также способствует кардиопротекции в первые минуты реперфузии. Эти фармакологические эффекты приводят к периферической вазодилатации, коронарорасширяющему действию и клеточной защите миокарда при ишемии [7–10].
Важно отметить, что влияние антиангинальных средств на клинические исходы у больных стабильной стенокардией, не перенесших ИМ или без АГ, не было доказано до опубликования результатов исследования IONA (Impact Of Nikorandil in Angina, Великобритания) [11]. В этом исследовании с длительностью наблюдения от 12 до 36 месяцев, включавшем 5 126 пациентов со стабильной стенокардией и высоким риском неблагоприятных исходов, никорандил в дозе 20 мг 2 раза в сутки на фоне стандартной терапии (β-адреноблокаторы, ACa2+, аспирин) приводил к снижению на 17 % риска достижения основной конечной точки – смерти от ИБС, нефатального ИМ и экстренной госпитализации в связи с загрудинной болью (р=0,014) и снижению на 21 % риска возникновения ОКС (р=0,028). Снижение риска по всем регистрируемым в данном исследовании сердечно-сосудистым событиям составило 14 % (р=0,027) [11]. В 2006 г. эксперты Европейского общества кардиологов включили в алгоритм медикаментозной терапии стабильной стенокардии активаторы калиевых каналов, в частности, никорандил [1]. В настоящее время никорандил включен в первые российские «Национальные рекомендации по кардиоваскулярной профилактике» (класс рекомендаций I, уровень доказательств B) [12].
В японском исследовании JCAD (Japanese Coronary Artery Disease) изучалось влияние никорандила на сердечно-сосудистые события у пациентов с ангиографически подтвержденной ИБС и органическим стенозом крупных коронарных артерий (не менее 75 %), включая больных острым ИМ – 21,4 % и нестабильной стенокардией – 14,8 %. Средний период наблюдения составил 2,7 года, средняя суточная доза никорандила – 15 мг, n=5116 [13, 14]. Для группы никорандила по сравнению с контрольной группой показано: снижение риска достижения первичной конечной точки (смерть от всех причин) на 35 % (р=0,0008); снижение рисков достижения вторичных конечных точек: сердечной смерти – на 56 % (р=0,0001), фатального ИМ – на 56 % (р=0,0022), цереброваскулярной или сосудистой смерти – на 71 % (р=0,0299), застойной СН – на 33 % (р=0,014), внебольничной остановки кровообращения и дыхания – на 64 % (р=0,0042), и это без увеличения числа смертей от других некардиоваскулярных причин.
Экспериментальные данные, результаты клинических исследований зарубежных авторов (Taira N., 1989; Meany T. В. с соавт., 1989; Kinoshita M., Sakai K., 1990) свидетельствуют о высокой антиангинальной и антигипертензивной эффективности модуляторов калиевых каналов, а также о некоторых преимуществах препаратов данной группы перед другими антиангинальными средствами. Так, например, в отличие от существующих антиангинальных средств нитратной структуры к действию никорандила не выявлено развития толерантности [15, 16]. Препарат улучшает доставку и увеличивает количество поступающего к сердцу кислорода без увеличения потребности сердца в нем [17, 18]. В отличие от блокаторов β-адренорецепторов, ACa2+ и нитратов никорандил практически не оказывает действия на ЧСС, систему проведения и сократительную способность миокарда. Кроме того, не отмечено существенного влияния никорандила на липидный обмен и метаболизм глюкозы.
В настоящее время в России отечественной инновационной фармацевтической компанией ПИК-ФАРМА зарегистрирован и запущен в производство препарат никорандил в таблетках по 10 мг.
Целью исследования явилась оценка антиангинальной эффективности и безопасности применения никорандила для профилактики и купирования приступов стенокардии у больных ИБС со стабильной стенокардией напряжения II–III ФК и возможностей его влияния на функцию эндотелия.
Материалы и методы
Под наблюдением находились 67 больных ИБС в возрасте от 45 до 78 лет (ср. возраст – 59,1±4,9 лет, мужчин 47 (70 %), женщин 20 (30 %)). Характеристика больных, включенных в исследование, представлена в таблице 1. Группы больных, получавших различную терапию, были сопоставимы по полу, возрасту, ФК стенокардии, анамнестической длительности заболевания.
Таблица 1. Демографическая и клиническая характеристика пациентов, включенных в исследование
Демографические и клинические
показатели |
Основная
группа
(n=30) |
Контрольная
группа
(n=37) |
| Число пациентов |
| Пол мужской / женский |
21 / 9 |
26 / 11 |
| Возраст (годы) |
| 45–50 |
3 |
8 |
| 51–60 |
17 |
18 |
| 61–70 |
8 |
7 |
| 71–80 |
2 |
4 |
| Индекс массы тела |
| <24,35 |
4 |
3 |
| 24,35< 25,96 |
14 |
15 |
| 25,96< 27,73 |
10 |
16 |
| >27,73 |
2 |
3 |
| Длительность ИБС (годы) |
| <3 |
6 |
10 |
| 3–6 |
12 |
17 |
| >6 |
12 |
10 |
| Стенокардия II ФК |
16 |
20 |
| Стенокардия III ФК |
14 |
17 |
| Наличие постинфарктного кардиосклероза с зубцом Q |
26 |
34 |
| ХСН I стадии по NYHA |
9 |
11 |
| ХСН II стадии по NYHA |
13 |
16 |
Верификация ИБС осуществлялась на основании типичной клинической картины заболевания, анамнестических указаний на перенесенный ИМ, результатов функциональных нагрузочных проб и ЭхоКГ–признаков локальной асинергии ЛЖ. Перенесенный ИМ в анамнезе, подтвержденный данными ЭКГ и ЭхоКГ, был следующей локализации: ИМ передне-перегородочной области – у 26 больных, задней стенки ЛЖ – у 20, у 14 – обширное поражение передней и задней стенок ЛЖ, у 7 – мелкоочаговый ИМ.
Более детальный анализ характеристик больных, включенных в исследование, показал, что стенокардия II ФК диагностирована у 36 (53,7 %) больных, III ФК – у 31 (46,3 %), у 12 – хроническая аневризма ЛЖ. У 20 (30 %) больных течение ИБС осложнилось развитием ХСН I ФК, у 29 (43,3 %) – ХСН II ФК.
В течение двух недель все пациенты, включенные в исследование, принимали амлодипин в виде монотерапии в дозе 10 мг / сут однократно. Для купирования приступа использовали препарат никорандил в дозе 10–20 мг, при неэффективности – нитроглицерин (НГ). Через 2 недели наблюдения все пациенты были рандомизированы на 2 группы. 1-я группа (30 больных) принимала никорандил в дозе 20 мг 3 раза в сут, 2-я группа (37 больных) – амлодипин в дозе 10 мг / сут. Возникающий приступ стенокардии купировался дополнительным приемом никорандила, в случае неэффективности использовался НГ. Длительность наблюдения составила 3 мес. В многочисленных клинических, в том числе мультицентровых, исследованиях (Roland E., 1993) установлено, что суточная доза никорандила 20–40 мг является наиболее эффективной. По данным большинства авторов, превышение вышеуказанных доз не приводит к дальнейшему повышению антиангинального и антигипертензивного действия, но способствует увеличению количества побочных реакций.
Методы оценки эффективности проводимой терапии включали анализ гемодинамических показателей (ЧСС, АД), ЭКГ, толерантность к физической нагрузке, суточное мониторирование ЭКГ по Холтеру, клинический и биохимический анализы крови. Интенсивность болевых ощущений определялась по шкале Борга, уровень качества жизни – по опроснику общего здоровья (General Health Questionnaire, GHQ-28).
Критериями оценки эффективности фармакотерапии являлось число эпизодов стенокардии в неделю. Хорошим клинический эффект считался в случае исчезновения приступов стенокардии или их урежения более чем на 50 %; удовлетворительным – при урежении приступов стенокардии менее чем на 50 %; при отсутствии антиангинального эффекта – неудовлетворительным.
Для оценки сосудодвигательной активности эндотелия использовали метод визуализации просвета плечевой артерии (ПА) с помощью ультразвука (УЗ) высокого разрешения. Через механическую стимуляцию эндотелия периферических артерий повышенным кровотоком после кратковременной артериальной окклюзии (фаза реактивной гиперемии – РГ) проводили оценку состояния зависимой от эндотелия вазодилатации (ЗЭВД) в сопоставлении с независимой от эндотелия вазодилатацией (НЭВД) под влиянием Н Г. Для получения увеличенного кровотока вокруг плеча накладывали манжету сфигмоманометра дистальнее по отношению к месту лоцирования артериального сегмента и накачивали ее до давления, на 50 мм рт. ст. превышавшего САД. Время окклюзии артерии составляло 4,5 мин. Отсутствие кровотока по ПА (фаза окклюзии) контролировали с помощью цветного допплеровского картирования потока. Через 15 мин отдыха после восстановления исходного диаметра ПА (ДПА) проводилась проба с экзогенным нитратом: пациент получал сублингвально 500 мкг Н Г. Изменения ДПА выражали в процентах по отношению к его исходной величине (D%).
Результаты и обсуждение
Через 2 недели лечения амлодипином у всех больных ИБС отмечено недостоверное снижение длительности приступов стенокардии, частоты приступов стенокардии на 17 % (р>0,05), количества эпизодов ишемии на 26 % (р>0,05) и увеличение средней продолжительности нагрузки до возникновения приступа стенокардии на 17 % (р>0,05).
При дальнейшей терапии амлодипином у больных 2-й группы отмечено снижение частоты приступов стенокардии к 4-й неделе на 31 % (р<0,05), к 12-й неделе – на 47 % (р<0,05). В 1-й группе частота приступов стенокардии уменьшилась на 39 и 60 % через 4 и 12 недель соответственно (р<0,05; р<0,05).
Длительность приступов стенокардии к 12-й неделе приема амлодипина достоверно уменьшалась на 37 % (р<0,05). На фоне приема никорандила длительность приступов стенокардии статистически достоверно уменьшилась к 4-й неделе на 37 % (р<0,05), к 12-й неделе – на 38 % (р<0,05). Максимальное уменьшение количества и длительности приступов стенокардии у больных обеих групп отмечалось к 4-й неделе лечения.
Через месяц терапии никорандилом средняя продолжительность нагрузки до возникновения приступа стенокардии достоверно увеличилась на 56 % (р<0,05), оставаясь примерно на таком же уровне до конца наблюдения. Через полтора месяца от начала терапии амлодипином этот показатель достоверно возрос на 38 % (р<0,05) и существенно не увеличился до конца исследования.
Динамика показателей Холтеровского мониторирования ЭКГ у больных ИБС на фоне проводимой терапии представлена в таблице 2. После завершения курсового приема амлодипина с купированием приступов стенокардии дополнительным приемом никорандила и НГ количество и длительность эпизодов ишемии миокарда уменьшились на 54 и 39 % соответственно (р<0,05; р<0,05), а в группе больных, принимавших курсовую терапию никорандилом – соответственно на 64 и 48 % (р<0,05; р<0,05).
Таблица 2. Динамика показателей Холтеровского мониторирования ЭКГ у больных ИБС на фоне проводимой терапии
| Показатели |
Исходно |
Через 2 недели |
Препарат |
Через 12 недель |
| Количество эпизодов ишемии миокарда (смещений сегмента ST) |
3,1±0,9 |
2,3±0,7 |
амлодипин |
1,4±0,3* |
| никорандил |
1,1±0,5* |
Средняя длительность эпизодов ишемии
(до приближения сегмента ST к изолинии <1 мм), сек. |
364±39 |
289±33 |
амлодипин |
221±28* |
| никорандил |
189± 25* |
| Интеграл смещения сегмента ST (мкВт × мин) (максимальный в эпизоде ишемии) |
6907±612 |
4769±612 |
амлодипин |
1571±129* |
| никорандил |
1273±146* |
* – статистически достоверные внутригрупповые различия (критерий Вилкоксона)
Антиангинальный и антиишемический эффекты никорандила можно объяснить наличием активной, мобильной нитратной группы и остатка амида никотиновой кислоты, которые определяют два механизма спазмолитического эффекта на основании объединения свойств органических нитратов и модуляторов калиевых каналов.
Первый механизм обусловлен активацией аденилатциклазы, что приводит к внутриклеточному накоплению гуанидилмонофосфата и, как следствие, к увеличению продукции эндотелийзависимого фактора релаксации; второй связан с открытием калиевых каналов, усилением проводимости ионов калия, что приводит к гиперполяризации мембран и, соответственно, к расслаблению гладких мышц сосудов. Следствием этого являются периферическая вазодилатация, коронарорасширяющее действие и незначительное снижение АД – от 5 до 15 % [7, 9].
При анализе динамики показателей опросника общего здоровья до начала лечения наибольшие изменения отмечались в субшкале «соматизация», наименьшие – в субшкале «депрессия». Статистически достоверные улучшения показателей опросника отмечались к 4-й неделе лечения – от 47 до 56 %, без существенной межгрупповой разницы. Общий средний балл шкалы у больных 1-й группы уменьшался на 54 % (р<0,05), во 2-й группе – на 44 % (р<0,05).
Анализ представленных результатов свидетельствует о том, что наибольшая эффективность курсового применения никорандила у больных со стенокардией напряжения отмечается через 1 месяц терапии, сохраняясь на этом уровне в дальнейшем, что указывает также на отсутствие эффекта привыкания к этому препарату. Курсовое применение амлодипина по эффективности несколько уступало никорандилу, но не столь существенно, т. к. по данным точного двустороннего критерия Фишера не было получено достоверной разницы по этому показателю.
Важным аспектом фармакотерапии любого заболевания является переносимость лекарственных препаратов. Переносимость никорандила у 24 (80 %) пациентов была хорошей, у 6 (20 %) – удовлетворительной. В качестве нежелательных явлений следует отметить возникновение головных болей, головокружения, тошноты. При этом необходимо отметить, что больные принимали никорандил практически в максимальной рекомендуемой терапевтической дозе.
Основным побочным эффектом, связанным с назначением никорандила, являлась головная боль, обусловленная дилатацией мозговых вен [2] Данный эффект объясняется наличием в формуле молекулы никорандила активной мобильной нитратной группы. У большинства пациентов отмечали нивелирование этого симптома через 1–3 дня регулярного приема препарата либо предупреждали его возникновение путем постепенного повышения дозы препарата. Согласно опубликованным данным международных исследований головная боль при приеме никорандила возникает в 3,5–9,5 % случаев [7]. Другие описанные побочные эффекты исчезали при регулярном приеме никорандила и не требовали отмены препарата.
Экспериментальные данные, результаты клинических исследований зарубежных авторов свидетельствуют как о высокой антиангинальной эффективности никорандила, так и об отсутствии развития толерантности и положительном влиянии на прогноз течения стабильной ИБС при его длительном приеме в отличие от существующих антиангинальных средств нитратной структуры [1, 5, 8, 9, 11].
Влияние никорандила на эндотелиальную дисфункцию больных ИБС по результатам допплерометрии плечевой артерии
Нормальной реакцией плечевой артерии (ПА) является ее дилатация на фоне реактивной гиперемии (РГ) более чем на 10 % от исходного диаметра. Меньшее ее значение или вазоконстрикция считаются патологическими [19]. В норме дилатация, вызываемая Н Г, составляет 17–19 %. Показатели дилатации плечевых артерий людей без ФР атеросклероза в ответ на увеличение кровотока остаются относительно стабильными у мужчин до 40 лет, затем снижаются приблизительно на 0,21 % в год, у женщин после 50 лет – на 0,49 % в год. Даже нормальный процесс старения вызывает ускорение регенерации эндотелиальных клеток, что приводит к нарушению ряда важных функций эндотелия [20]. Регенерированные эндотелиоциты утрачивают некоторые генетические свойства, в частности, снижается их способность к высвобождению фактора релаксации эндотелия – NO. При наличии таких ФР, как А Г, курение, стресс, ускоряется эндотелиальное старение и потенцируется регенерация эндотелия. По мере утолщения и повышения жесткости стенок артериальных сосудов NO все сложнее достигать гладко-мышечный слой, который способен к релаксации. Кроме того, в артериях, пораженных атеросклерозом, вырабатывается повышенное количество супероксидных радикалов кислорода. Эти свободные радикалы могут вырабатываться активированными макрофагами и компонентами артериальной стенки, что позволяет объяснить наблюдаемую резистентность к эндогенному и экзогенному NO. Взаимодействие NO с супероксидным радикалом с образованием менее активных метаболитов может объяснить резистентность к NO при атеросклерозе. Факторы риска, сниженное образование и повышенное разрушение NO, помимо нарушения вазореактивности артерий, также могут облегчать пролиферативные реакции и миграцию гладкомышечных клеток сосудов из мышечной оболочки в интиму.
Оценка вазодилатирующей функции эндотелия в динамике с помощью допплерометрии ПА в условиях пробы с РГ и НГ под влиянием лечения никорандилом проведена у 37 больных ИБС. Контрольную группу составили 10 здоровых добровольцев.
У 78,4 % больных ИБС до начала лечения никорандилом прирост диаметра ПА (ДПА) в фазу РГ был менее 10 %. Возможно, у больных ИБС усугубление дисфункции эндотелия происходит параллельно с прогрессированием заболевания и увеличением ФК стенокардии.
В испытуемой группе при острой пробе с 500 мкг Н Г, принятого сублингвально, ДПА увеличился на 14,6±1,5 %, что было сопоставимо с результатами, полученными в группе контроля – 17,5±5,3 %. 12-недельный непрерывный прием никорандила повлиял как на ДПА в покое, так и на параметры ЗЭВД и НЭВД. Отмечалось достоверное увеличение ДПА в покое в среднем на 5,2 %, что, вероятно, связано с вазодилатирующими свойствами никорандила (рис. 1).
Рисунок 1. Влияние никорандила на эндотелиальную функцию сосудов (по данным допплерометрии в условиях пробы с РГ и НГ)
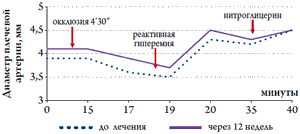
Как видно из таблицы 3, на фоне длительной терапии никорандилом происходило увеличение прироста ДПА при РГ (D% РГ) в среднем на 9,6 % (р<0,001) с одновременным снижением чувствительности эндотелия к экзогенному поступлению НГ на 25,7 % (р<0,001). Очевидно, снижение прироста диаметра плечевой артерии под влиянием НГ на фоне терапии никорандилом связано со снижением чувствительности гладкомышечных клеток сосудов к экзогенному NO в пробе с НГ на фоне предшествующего длительного приема никорандила.
Таблица 3. Динамика допплерометрических показателей в пробе с РГ и НГ до (W0) и после 12 недель лечения никорандилом (W12)
Допплерометрический
показатель ПА |
Больные ИБС (n=37) |
| W0 |
W12 |
Δ% |
| Д исх., мм |
3,84±0,4 |
4,05±0,4 |
5,2 %** |
| Д РГ, мм |
4,15±0,4 |
4,4±0,46 |
4,2 %** |
| Δ% Д РГ, % |
8,19±1,03 |
8,93±1 |
9,6 %** |
| Д НГ, мм |
4,45±0,46 |
4,45±0,7 |
–0,13 % |
| Δ% Д НГ, % |
15,9±1,6 |
11,8±1,4 |
–25,7 %** |
| Д окл., мм |
3,28±0,4 |
3,44±0,4 |
4,9 %** |
| Δ% Д окл., % |
–14, 09±5,3 |
–16±3,6 * |
7,1 % |
* – p<0,01; ** – p<0,001
Таким образом, полученные результаты позволяют предположить, что у больных ИБС имеет место нарушение эндотелийзависимой вазодилатации в виде снижения реакции эндотелия на увеличение «напряжения сдвига» во время пробы с Р Г. Абсолютное увеличение прироста диаметра плечевой артерии на 1 % у больных с эндотелиальной дисфункцией сопряжено со снижением риска сердечно-сосудистых осложнений на 10–25 % [21, 22].
Зависимая от эндотелия вазодилатация плечевой артерии под влиянием длительной терапии никорандилом нормализуется, что выражается в увеличении реакции (прироста диаметра плечевой артерии) на стимуляцию повышенным кровотоком после кратковременной окклюзии на 9,6 % (p<0,001). Таким образом, можно предположить, что одним из механизмов действия никорандила, влияющего на снижение риска сердечно-сосудистых осложнений у больных ИБС, является улучшение функции эндотелия.
Никорандил, производимый отечественной компанией ПИК-ФАРМА, при терапии больных ИБС со стенокардией II–III ФК в дозе по 20 мг 3 раза в сутки в течение 12 недель обладает хорошей переносимостью, не вызывает привыкания и приводит к существенному уменьшению частоты и длительности приступов стенокардии, частоты и длительности эпизодов ишемии миокарда, выраженности ангинозных болей, повышению толерантности к физической нагрузке, улучшению качества жизни пациентов по данным опросника общего здоровья и может применяться как с целью профилактики приступов стенокардии, так и для их купирования.
Побочные эффекты, возникшие при приеме препарата, относились к ожидаемым, были преходящими и не требовали отмены препарата.
Материал поступил в редакцию 17/09/2012
СПИСОК ЛИТЕРАТУРЫ
1. Fox K, Garcia MA, Ardissino D et al. Guidelines on the management of stable angina pectoris: executive summary: Te Task Force on the Management of Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J. 2006;27 (11):1341–1381.
2. Шевченко О. П., Мишнев О. Д., Шевченко А. О., Трусов О. А., Сластникова И. Д. Ишемическая болезнь сердца. – М. –Реафарм.2005. – 416 с.
3. Ольбинская Л . И., Морозова Т. е., Сизова Ж. М., Вартанова О. А. и др. Фармакотерапия хронических сердечно-сосудистых заболеваний: Руководство для врачей. – М.: «Медицина»,2006. – 386 с.
4. Рациональная фармакотерапия сердечно-сосудистых заболеваний: Рук. для практических врачей. Под общ. ред. е. И. Чазова, Ю. Н. Беленкова. – М.: «Литтерра», 2004. – 972.
5. Рациональная фармакотерапия сердечно-сосудистых заболеваний: Рук. для практических врачей. Под общ. ред. е. И. Чазова, Ю. Н. Беленкова. – М.: «Литтерра», 2005. – 972.
6. Эффективность и безопасность лекарственной терапии при первичной и вторичной профилактике сердечно-сосудистых заболеваний. Национальные рекомендации ВНОК. Рациональная фармакотерапия в кардиологии 2011; (Приложение 5):24–31
7. Horinaka S. Use of nicorandil in cardiovascular disease and its optimization. Drugs 2011;71 (9):1105–1119.
8. Kinoshita M, Sakai K. Pharmacology and therapeutic efects of nicorandil. Cardiovasc Drugs Ter. 1990;4 (4):1075–88.
9. Meany TB, Richardson P, Camm AJ et al. Exercise capacity afer single and twice-daily doses of nicorandil in chronic stable angina pectoris. Am J Cardiol. 1989;63 (21):66J-70J.
10. Rezkalla SH, Kloner R. Preconditioning in humans. Heart Fail Rev. 2007;12 (3-4):201–206.
11. Te IONA Study Grup.Efect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA): randomized trial. Lancet. 2002;359 (9314):1269–1275.
12. Национальные рекомендации ВНОК. Кардиоваскулярная терапия и профилактика 2011;10 (6); Приложение 2: 57
13. Japanese Coronary Artery Disease (JCAD) Study Investigators. Current status of the background of patients with coronary artery disease in Japan. Circ J. 2006;70 (10):1256–1262.
14. Horinaka S, Yabe A, Yagi H et al. Efects of nicorandil on cardiovascular events in patients with coronary artery disease in the Japanese Coronary Artery Disease (JCAD) study. Circ J. 2010;74 (3):503– 509.
15. Roland E. Safety profle of an anti-anginal agent with potassium channel opening activity: an overview. Eur Heart J. 1993;14 (Suppl B): 48–52.
16. Taira N. Nicorandil as a hybrid between nitrates and potassium channel activators. Am J Cardiol. 1989 Jun 20;63 (21):18J-24J.
17. Cokkinos DV, Pantos C. Myocardial protection in man – from research concept to clinical practice. Heart Fail Rev. 2007;12 (3-4):345–362.
18. Kitakaze M, Asakura M, Kim J et al. Human atrial natriuretic pep-tide and nicorandil as adjuncts to reperfusion treatment for acute myocardial infarction (J-WIND): two randomised trials. Lancet. 2007;370 (9597):1483–1493.
19. Затейщикова А. А., Затейщиков Д. А. Эндотелиальная регуляция сосудистого тонуса: методы исследования и клиническое значение. Кардиология. 1998;38 (9):69–80.
20. Ольбинская Л. И., Сизова Ж. М., Ушакова А. В. Эндотелиальная дисфункция у больных ишемической болезнью сердца, осложненной хронической сердечной недостаточность, и возможности коррекции изосорбид-5-мононитратом. Кардиология. 2001;41 (3):29–32.
21. Neunteuf T, Heher S, Katzenschlager R et al. Late prognostic value of fow-mediated dilation in the brachial artery of patients with chest pain. Am J Cardiol. 2000;86 (2):207–210.
22. Shimbo D, Grahame-Clarke C, Miyake Y et al. Te association between endothelial dysfunction and cardiovascular outcomes in a population-based multi-ethnic cohort. Atherosclerosis. 2007;192 (1):197–203.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)




