- общие рекомендации для больных и их родственников;
- немедикаментозные мероприятия;
- лекарственную терапию;
- вспомогательные устройства для кровообращения;
- электрокардиостимуляцию, в частности, ресинхронизацию;
- хирургические методы.
- отказ от курения;
- контроль массы тела;
- ограничение или отказ в приеме алкоголя;
- ограничение потребления соли;
- ограничение физических и эмоциональных нагрузок, соблюдение рекомендованного режима нагрузок, тренировок;
- исключение избыточного употребления жидкости;
- прием препаратов, которые необходимы для лечения заболеваний других органов, после консультации кардиолога.
- противовоспалительных нестероидных средств;
- антиаритмических препаратов I и IV групп;
- трициклических антидепрессантов;
- кортикостероидов;
- лития и препаратов из группы альфа-адреноблокаторов
- двусторонний стеноз почечных артерий;
- стеноз почечной артерии единственной почки;
- ангионевротический отек во время предшествовавшей терапии иАПФ;
- гиперкалиемия > 5,5 ммоль/л;
- креатинин крови > 250 ммоль/л;
- беременность.
- резкое снижение ОЦК;
- активация нейроэндокринной системы;
- задержка Na после снижения ОЦК;
- почечная недостаточность;
- снижение перфузии почек из-за снижения сердечного выброса;
- нарушение всасывания диуретиков;
- потребление большого количества соли;
- развитие алкалоза.
- ограничение соли;
- увеличение ОЦК;
- увеличение дозы диуретика и в/в его, включая инфузию фуросемида в дозе 5-40 мг в 1 час;
- комбинация диуретиков (фуросемида + гипотиазида, фуросемида + верошпирона) комбинация диуретиков с допамином (<3 мкг/кг/мин);
- уменьшение дозы иАПФ;
- устранение алкалоза;
- добутамин при сниженных сердечного выброса и артериального давления;
- ультрафильтрация воды.
- завершен выбор оптимальной (целевой) дозы ингибиторы АПФ/А2 рецепторов;
- состояние больного 2-4 функционального класса на терапии стабилизировано, и завершен подбор дозы диуретиков, периферические отеки и застой крови в легких контролируются;
- предпочтительнее подбор терапии начинать в стационаре, особенно большая осторожность требуется у больных с недавно возникшей и тяжелой формой сердечной недостаточности.
- Бета-блокатор - 1 А;
- Дигоксин - 1 В;
- Комбинация их - 1 В;
- У больных с непереносимостью бета-блокатора -амиодарон + дигоксин - Ив С;
- Аблация синусового узла и имплантация электрокардиостимулятора (двух-, трех-камерного) при непереносимости препаратов - Ив С.
- ультрафильтрация жидкости для устранения рефрактерных отеков;
- имплантация митрального клапана (при тяжелой митральной недостаточности);
- частые пароксизмы НЖТ, ЖТ (амиодарон);
- имплантация пейсмекера (брадикардия, АВ блокада);
- ресинхронизация систолы желудочков;
- устройства для вспомогательного кровообращения;
- искусственное сердце (на время ожидания трансплантации сердца).
- Ponikowski P, Anker SD, AlHabib KF et al. Heart failure: preventing disease and death worldwide. ESCHeart Failure. 2014;1:4-25. doi: 10.1002/ehf2.12005.
- Ceia F, Fonseca C, Mota T et al. EPICA Investigators. Prevalence of chronic heart failure Southwestern Europe: the EPICA study. Eur J Heart Fail. 2002;4:531-539.
- Ohlmeier C, Mikolajczyk R, Frick J et al. Incidence, prevalence and 1-year all-cause mortality of heart failure in Germany: a study based on electronic healthcare data of more than six million persons. Clin Res Cardiol. 2015;104:688-696. doi: 10.1007/s00392-015-0841-4.
- Taichman DB, Backus J, Baethge C, Bauchner H, de Leeuw PW, Drazen JM, Fletcher J, Frizelle FA, Groves T, Haileamlak A, James A, Laine C, Peiperl L, Pinborg A, Sahni P, Wu S. Sharing Clinical Trial Data--A Proposal from the International Committee of Medical Journal Editors. N Engl J Med. 2016;374(4):384-386.
- Мазур Н.А. Практическая кардиология. 2015, Москва. Медпрактика-М. 679 с.
- Ponikowski P (председатель). 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016 Jul 14;37(27):2129-200. doi: 10.1093/eurheartj/ehw128. Epub 2016 May 20.
- YANCY CW, Januzzi JL Jr, Allen LA, Butler J, et al 2017 ACC Expert Consensus Decision Pathway for Optimization of Heart Failure Treatment: Answers to 10 Pivotal Issues About Heart Failure With Reduced Ejection Fraction. J Am Coll Cardiol. 2017 Dec 13. pii: S0735-1097(17)41641.
- Wei Ping Sun, Hai Bin Zhang, Jin Cheng Guo et al. Comparison of the Efficacy and Safety of Different ACE Inhibitors in Patients With Chronic Heart Failure. A PRISMA-Compliant Network Meta-Analysis. Medicine (Baltimore). 2016 Feb; 95(6): e2554. Published online \2016 Feb 12. doi: 10.1097/MD.000 0000000002554 PMCID: PMC4753869D
- Hara M, Sakata Y, Nakatani D et al. OACIS Investigators. Comparison of5-year survival after acute myocardial infarction using angiotensin converting enzyme inhibitor versus angiotensin II receptor blocker. Am J Cardiol. 2014 Jul 1;114(1):18.doi:10.1016/j.amjcard.2014.03.055. Epub 2014 Apr 18
- McMurray J.J., Packer M., Desai A.S., et al. Angiotensin-Neprilysin Inhibition versus Enalapril in Heart Failure. N Engl J Med 2014;371:993-1004.
- Международный консорциум экспертов для защиты больных. NEJM, 2016; 375, 407-409)
- Digitalis Investigation Group. The effect of digoxin on mortality and morbidity in patients with heart failure. N Engl J Med. 1997 Feb 20;336(8):525-33.
- Faiez Zannad, John J.V. McMurray, Henry Krum, Dirk J. van Veldhuisen, Karl Swedberg, Harry Shi, John Vincent, Stuart J. Pocock, Bertram Pitt EMPHASIS-HF Study Grp Eplerenone inPatients with Systolic Heart Failure and Mild Symptoms. In: New England Journal of Medicine, 2011.Vol. 364, No. 1, p. 11-21.
- Karl Swedberg, MD, Michel Komajda, MD, Michael Bohm, MD,± Jeffrey Borer, MD,§ Michele Robertson, BSC, Luigi Tavazzi, MD,Tj Ian Ford, PHD, for the SHIFT Investigator. Effects on Outcomes ofHeartRateReduction by Ivabradine in Patients With Congestive Heart Failure: Is There an Influence ofBeta-Blocker Dose? Findings From the SHIFT (Systolic Heart failure treatment with the If inhibitor ivabradine Trial) Study. J Am Coll Cardiol 2012;59:1938-45.
- Fox K, Ford I, Steg PG, Tardif JC, Tendera M, Ferrari R; SIGNIFY Investigators. Ivabradine in stable coronary artery disease without clinical heart failure. N Engl J Med. 2014 Sep 18;371(12):1091-9.
- Tice FD, Binkley PF, Cody RJ, Moeschberger ML, Mohrland JS, Wolf DL, Leier CV. Hemodynamic effects of oral nicorandil in congestive heart failure. Am J Cardiol. 1990 Jun 1;65(20):1361-7.
- Zhao F, Chaugai S, Chen P, Wang Y, Wang DW. Effect of nicorandil in patients with heart failure: a systematic review and meta-analysis. Cardiovasc Ther. 2014 Dec;32(6):283-96. doi: 10.1111/1755-5922.12097.
- Рябихин Е. А., Можейко М. Е., Красильникова Ю. А, Савичева С. В., Потанина М. В. Дополнительные возможности в лечении ишемической болезни сердца, осложненной хронической сердечной недостаточностью с низкой фракцией выброса левого желудочка. Журнал Сердечная Недостаточность. 2016;17 (1): 3-9.
- Yoshihisa A., Sato Y, Watanabe S. et al. Decreased cardiac mortality with nicorandil in patients with ischemic heart failure. BMC Cardiovascular. Disorders. 2017; 17: 141-6.
- Nodari S ,Triggiani M, Campia U et al. Effects of n-3 polyunsaturated fatty acids on left ventricular function and functional capacity in patients with dilated cardiomyopathy. J Am Coll Cardiol. 2011 Feb 15;57(7):870-9. doi: 10.1016/j.jacc.2010.11.017. Epub 2011 Jan 6.
- Poole-Wilson PA, Lubsen J, Kirwan BA et al Effect of long-acting nifedipine on mortality and cardiovascular morbidity in patients with stable angina requiring treatment (ACTION trial): randomised controlled trial. Lancet. 2004 Sep 4-10;364(9437):849-57.
- Alikhan R, Cohen AT, Combe S et al. Prevention of venous thromboembolism in medical patients with enoxaparin: a subgroup analysis of the MEDENOX study. Blood Coagul Fibrinolysis. 2003.
- Jankowska EA, Tkaczyszyn M, Suchocki T et al. Effects of intravenous iron therapy in iron-deficient patients with systolic heart failure: a meta-analysis of ^ randomized controlled trials. Eur J Heart Fail. 2016 Jul;18(7):786-95. doi: 10.1002/ejhf.473. Epub 2016 Jan 28.
Хроническая сердечная недостаточность со сниженной сократительной способностью миокарда и терапия больных, получившая доказательства положительного влияния на их выживаемость с учетом новых требований
СтатьиОпубликовано в журнале:
« Поликлиника » 5, 2018
Н.А. Мазур, С.В. Миклишанская
Кафедра кардиологии ГБОУДПО РМАНПО Минздрава России
В обзорной статье представлены данные об актуальности данной проблемы для решения вопросов охраны здоровья населения страны. Показана важность, особенно в условиях наличия ограниченных средств, выделяемых медицинским учреждениям на бесплатное лечение заболевших, использования только тех средств, которые имеют доказательства положительного влияния на сохранение трудоспособности и продолжительность их жизни. Дана критическая оценка тому, как сегодня нерационально используются выделяемые средства и личные средства больных. В качестве доказательства наиболее рационального ведения таких больных используются и сравниваются полученные данные, представленные почти одновременно (в 2016 и 2017 гг) в США и Европе в Руководствах по лечению больных сердечной недостаточностью со сниженной сократительной способностью миокарда. Сравнительный анализ показывает насколько несовершенны сегодня имеющиеся представления о том, чем и как лечить таких больных. Этим демонстрируется важность договоренностей о необходимости выработки общих критериев оценки эффективности средств, используемых для лечения больных. Сегодня принципы, которые были заложены в основу «доказательной медицины», требуют существенного уточнения.
Сердечная недостаточность является осложнением многих заболеваний. Это сложный клинический синдром, который характеризуется наличием либо снижением насосной функции сердца, либо значительным уменьшением его кровенаполнения (иногда в сочетании со снижением сократительных свойств миокарда), что стимулирует повышение активности нейроэндокринной системы и приводит к задержке жидкости в кровеносном русле, к появлению застоя крови в малом и/или большом круге кровообращения, к снижению качества и продолжительности жизни больного. В последних рекомендациях (6, 7) стали выделять три варианта сердечной недостаточности: а) с сохраненной систолической функцией левого желудочка (>50%), б) со сниженной систолической функцией левого желудочка (<40%), б) с промежуточным ее нарушением (фракция выброса левого желудочка в пределах 41-49%). Проведенные пока в небольшом количестве исследования не показали каких-либо доказательств в необходимости различий в ведении либо лечении данной группы больных в сравнении с группой со сниженной фракцией выброса левого желудочка.
Сердечная недостаточность широко распространена в странах, среди населения которых наблюдается высокая заболеваемость артериальной гипертонией и ишемической болезнью сердца. Распространенность её значительно повышается с возрастом. Во всем мире сегодня насчитывается около 26 миллионов таких больных. В США на их лечение расходуется более 10% всех средств, выделяемых на здравоохранение. Заболеваемость (возникновение новых случаев) среди взрослого населения Европы достигает 1,6-1,8 случаев на 1000 жителей в 1 год, а среди населения в возрасте старше 70 лет - более 10 случаев. Показатель выживаемости больных в развитых странах, несмотря на современное лечение, составляет в течение 5 лет около 50%, а в группе с тяжелой формой сердечной недостаточности более половины умирает в течение 1 года (1,2,3).
В нашей стране подобные статистические данные Федеральной службой государственной статистики не предоставляются. Вместе с тем известно, что около половины, а в развитых странах - более половины умирают от сердечно-сосудистых заболеваний. Опираясь на приведенные ниже официальные данные, полученные в 2010 г. в странах с самой высокой смертностью (табл. №1 ), имеются основания считать, что в РФ сердечно-сосудистая смертность остается очень высокой, так как она вместе с Украиной и Болгарией находится среди именно этих стран (Африки и Азии). Кроме того, по данным Росстата в 2016 г. абсолютные показатели рождаемости, смертности повторяют прошлогодние, которые, в свою очередь, слабо изменяются уже четыре года подряд. Россия по-прежнему находится в состоянии «демографической бифуркации»: медленное улучшение текущих демографических показателей отягощается постепенным ухудшением общей демографической структуры (www.who.int/ gho/publications/world_health_statistics/ru/).
Таблица № 1. Страны с самой высокой смертностью в мире.
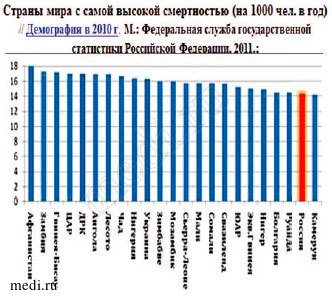
На 1 января 2016 года население России составило 146,520 млн человек, увеличившись за год на 252 тыс., из которых 33 тыс. - это естественный прирост, а почти 220 тыс. - миграционный, где более половины обеспечено Украиной. Естественный прирост, то есть превышение числа родившихся над умершими, фиксируется в России уже третий год подряд, однако по отношению к общему числу населения он является статистически незначительным. В этом смысле точнее считать, что в России четыре года подряд абсолютная рождаемость равна смертности. В Европейской части РФ население продолжает вымирать. По данным Росстата на 1 июля 2017 года: с начала года число жителей России уменьшилось на 17,0 тыс. человек или на 0,01% в результате сложившейся естественной убыли населения. Миграционный прирост на 85,7% компенсировал численные потери населения. Кроме того, произошло снижение рождаемости по сравнению с аналогичным периодом прошлого года, которое составило 107,4 тыс. человек (www.gks.ru/wps/wcm/connect/rosstat_main/rosstat/ ru/statistics/.../demography).
Ситуация осложняется еще и тем, что, как заявила глава Счетной палаты РФ Татьяна Голикова в ходе своего выступления на XVII съезде партии «Единая Россия» от 20.1 2. 201 7, более 20 млн граждан России находятся за чертой бедности. Приведенные данные диктуют врачам РФ необходимость максимально обоснованного использования для лечения больного только препаратов с безупречно доказанной эффективностью, а при длительном применении - увеличивающих продолжительность их жизни. Учитывая сложившуюся ситуацию в стране, решить эту проблему будет не просто, так как при этом будут затронуты интересы очень большого круга фирм, рекламодателей, врачей, профессоров и контролирующих органов. Ни в одной цивилизованной стране нет столь засоренного неэффективными и даже вредными веществами списка лекарственных средств, используемых не по назначению. Чего стоит только «метаболическая» терапия, процветающая в нашей стране около полувека. История начиналась с внутривенного введения витаминов, АТФ, рибоксина, креатинфосфата (некоторые из них вообще не проникали через мембрану клетки). Их сменили предуктал, милдронат, которые также широко используются и при других заболеваниях (в неврологии,гематологии, онкологии). А в неврологической клинике стали «течь реки» цербролизина, хотя начинались с 1 мл, а сейчас уже 50 мл, актовегина, ноотропов. Кстати, церебролизин в стране-производителе не используется, так как каких- либо значимых доказательств пользы до сих пор никто не представил. В 2010 году CochraneCollaboration, наиболее авторитетная международная организация, специализирующаяся на обобщении сведений о доказательных исследованиях, опубликовала обзор результатов рандомизированных клинических испытаний церебролизина. «Согласно результатам ни один из 146 обследуемых не показал улучшения состояния при приеме препарата. Нет никаких оснований для подтверждения эффективности применения церебролизина в лечении пациентов с ишемическим инсультом. В процентном соотношении не было никакой разницы между количеством летальных исходов - 6 человек из 78 в группе, получавших церебролизин, против 6 из 68 в группе, получавших плацебо. Состояние больных из первой группы не улучшилось в сравнении с больными из второй группы». (https:// esquire.ru/archive/1880-drugs). Актовегин, очень широко используемый в РФ, не прошёл полноценных, независимых исследований по правилам GCP. В странах западной Европы и США Актовегин не применяется. Препараты, содержащие компоненты животного происхождения, запрещены в развитых странах. В кокрановской библиотеке нет ни одного исследования Актовегина. И при этом у нас Актовегин назначается практически всем на любой стадии беременности, во время и после родов, для лечения ожогов, реабилитации после инфаркта миокарда и инсульта, при многих хронических заболеваниях. На англоязычном сайте корпорации-производителе указано, что вытяжка из крови телят продается только в страны СНГ, Китай и Южную Корею.
История с милдронатом, который в клинике не оказал у больных стенокардией никакого положительного влияния, и из-за чего вероятно было досрочно прекращено начатое многоцентровое исследование, вдруг у спортсменов неизвестно по какой причине приобрел название «допинга», что может служить ярким примером вреда не только для спорта!
В кардиологии, в качестве примера бесполезных затрат, следует привести данные ЗАО «Группа ДСМ» (pharmvestnik.ru/.../dsm-group). Продажа вещества триметазидина в 2016 г. (без данных из льготных списков ) составила сумму почти 4 миллиарда руб. Для сравнения продажа высокоэффективного метопролола, положительно влияющего на выживаемость больных со многими тяжелыми заболеваниями (перенесшими инфаркт миокарда, страдающими сердечной недостачностью) достигает лишь 2,6 млрд рубл. Кроме того, огромные бесполезные затраты общество несет на самолечение с помощью БАД. По данным аудита фармацевтического рынка России, проводимого DSMGroup, за 2016 год через аптечную сеть было реализовано 268 млн. упаковок БАД на сумму 31,5 млрд. рублей (в ценах закупки аптек).
В течение почти 30 лет при организации научных исследований и в практической работе при осуществлении профилактической и лечебной работы врачам было рекомендовано перейти от оказания помощи больным с основными кардиологическими заболеваниями не исходя из исторически накопленного опыта, а учитывая новые данные, полученные в специально организованных исследованиях на принципах (правилах) доказательной медицины. Этот термин был предложен сотрудниками Университета Мак Мастера в 1990 г. В течение этого времени, кроме очень важных данных, существенно изменивших наши представления об обоснованности и даже о вреде ранее использовавшихся методов и средств лечения, были установлены отклонения в организации и в полноте предоставляемых данных, отклонения в отборе данных для публикаций и, особенно, в предоставлении множества незаплнированных вторичных анализов, что увеличило риск обнаружения ложных результатов. Поэтому был организован международный консорциум экспертов для непрерывной оценки научных исследований в области сердечнососудистых заболеваний (4). Цель создания консорциума - разработать рекомендации для международного комитета редакторов медицинских журналов и институтов медицины для оценки качества предоставляемых результатов клинических исследований. Кроме того, будет организовано проведение повторного анализа данных независимой группой специалистов с учетом более строгих требований. Этот консорциум назван «международный консорциум экспертов для защиты больных». В связи с представленной не очень высокой оценкой эры доказательной медицины, указанный Консорциум рекомендует при организации исследований и обеспечении лечения больных переходить в «эру точной (с устранением обнаруженных проблем, включая рандомизацию больных с учетом величины риска плохого исхода), персонофицированной медицины». Последняя должна основываться на данных, полученных при генетических исследованиях больных, включаемых под наблюдение. Круг таких генетических мутаций, на основании которых можно осуществлять выбор терапии больного, пока очень ограниченный.
Тяжесть сердечной недостаточности. После постановки диагноза сердечной недостаточности необходимо определить степень её выраженности. Известны различные подходы к оценке тяжести состояния больного. Но сегодня наиболее широкое распространение получила Нью-Йоркская классификация в связи с простотой, возможностью применения её у больных с различной этиологией сердечной недостаточности, включая оценку эффективности проводимой терапии. В основе классификации находится определение переносимости физических нагрузок, которые ежедневно выполняются больными. Очень важно, что в ней представлена группа больных, находящихся под угрозой возникновения сердечной недостаточности. К этой группе больных относятся те, кто имеет объективные данные, свидетельствующие о наличии кардиальной дисфункции (сниженная фракция выброса, увеличенные объемы камер сердца, увеличенный кардиоторакальный индекс), но у которых обычная нагрузка не вызывает появления слабости, одышки, сердцебиения. Эти больные составляют группу с сердечной недостаточностью функционального класса I. Сегодня таким больным рекомендуется проведение профилактической терапии, включая медикаментозную, которая имеет доказательства положительного влияния на отдаленные исходы.
Функциональные классы II, III и IV отличаются между собой по величине нагрузки, которая провоцирует появление симптомов сердечной недостаточности.
В нашей стране ранее использовалась классификация хронической сердечной недостаточности, которая была предложена Г.Ф. Лангом, В.Х. Василенко и Н.Д. Стражеско. В 2013 г. Американское общество кардиологов (ACCF) и Ассоциация сердца (AHA) опубликовали новое руководство по лечению больных сердечной недостаточностью, в котором предложили, наряду с существующей Нью-йоркской классификацией (NYHA) по классам, выделять еще и 4 ее стадии (А, В, С, D) в соответствии задачами, которые должны определять подходы к выбору лечения. На стадии А обеспечивается модификация факторов риска, обуславливающих в последующем формирование сердечной недостаточности; на стадии В - лечение заболеваний, вызвавших структурные изменения сердца, на стадии С - уменьшение проявлений заболеваний и летальности, на стадии D (рефрактерная форма) продолжается терапия с целью уменьшения повторных госпитализаций, проявлений сердечной недостаточности в покое и улучшения качества жизни. Терапия может включать трансплантацию сердца. Допускается возможность использования экспериментальных вмешательств. В этих рекомендациях впервые также было сформулировано предположение о возможности паллиативного лечения таких больных в хосписе после того, как будут исчерпаны все возможности терапии, включая трансплантацию сердца, и высказанного собственного желания больного, а также согласия родственников. На поздних стадиях тяжелой сердечной недостаточности возможно избыточное снижение веса у некоторых больных и появление т.н. сердечной кахексии. Наличие избыточной потери веса определяется в следующих случаях: 1) при индексе массы менее 22 кг/м2, 2) при снижении массы в течение 6 мес. на 5 кг или на 7,5% по сравнению с предшествующей массой, имевшейся во время компенсации, достигнутой с помощью терапии; 3) при снижении массы до уровня менее 90% по сравнению с идеальной массой.
Лечение больных с хронической систолической сердечной недостаточностью
Терапевтические мероприятия у данной группы больных включают:
Немедикаментозные мероприятия
Их выполнение больным может способствовать длительному сохранению компенсации на правильно подобранном лечении. Эти мероприятия включают:
Для своевременного выявления ухудшения состояния больному рекомендуется регулярно (не менее двух раз в неделю) определять свой вес. В случае его увеличения на 2 кг и более в течение 3 дней при сохранении обычного режима питания, необходимо обратиться к лечащему врачу в ближайшие дни или больной может самостоятельно (в согласованных заблаговременно с врачом пределах) увеличить дозу диуретика и ограничить прием соли.
Соль и жидкость. Рекомендуется всем больным значительно ограничить прием соли: при I-II функциональном классе сердечной недостаточности целесообразно принимать в сутки до 3 грамм, а в случае наличия III-IV функционального класса - не более 1-2 грамм в сутки.
У очень тяжелых больных с трудно контролируемой сердечной недостаточностью необходимо исключить прием всех продуктов, при приготовлении которых использовалась соль. Важность представленных рекомендаций была подтверждена в исследовании, результаты которого были сообщены во время конгресса Европейского общества кардиологов в 2014 году. В данном исследовании учитывалось количество NaCl, выделяемого c мочой в течение суток, а не его поступление с пищей, что определить точно у большого количества больных практически невозможно. Полученные в длительных наблюдениях результаты позволили прийти к следующим выводам: а) чем меньше соли выделяется с мочой, тем меньше летальность, б) выделение в течение 24 ч. с мочой 3.0-6.0 грамм NaCl ассоциируется с достоверно более высокой летальностью.
Прием жидкости, включая продукты её содержащие, при наличии гипонатриемии значительно ограничивается (менее 1 л в сутки); в обычных условиях больной может употреблять до 1,5-2 л в день.
Алкоголь не рекомендуется больным с подозрением на алкогольную кардиомиопатию. В других случаях разрешается, но не поощряется, прием весьма умеренного количества. Прием большого количества спиртных напитков может вызвать ухудшение состояния больного.
Масса тела. У многих больных с сердечной недостаточностью, обусловленной ИБС и артериальной гипертонией, имеется избыточная масса тела или ожирение (индекс массы более 30 кг/м2), у которых не менее важной задачей, чем медикаментозная терапия, является обеспечение её снижения до нормальной величины (индекс массы менее 25 кг/м2).
У больных, длительно страдающих тяжелой сердечной недостаточностью, наблюдается избыточное снижение массы тела или кахексия сердечного генеза. Подозрение на наличие избыточной потери веса должно возникать у больных, у которых вес меньше идеального более, чем на 10% или индекс массы тела менее 22 кг/м2. В этих случаях рекомендуется принимать пищу малыми порциями и часто.
Окружающая среда. Больному рекомендуется избегать пребывания в очень жаркой с большой влажностью среде, а также перемещаться на большую высоту (более 1,5-2 км). При необходимости переезда в другое место следует избегать длительных поездок. Поэтому предпочтительнее использовать воздушный транспорт, но полет также должен быть непродолжительным. В противном случае возникает риск дегидратации, венозного тромбоза, избыточного отека нижних конечностей.
Сексуальная активность. Не рекомендуется запрещать или, наоборот, стимулировать. Больной должен понимать, что избыточные нагрузки, особенно у больных с III-IV ф.кл., могут провоцировать ухудшение состояния.
Физическая активность. У больных с острой сердечной недостаточностью или при дестабилизации состояния больного с хронической сердечной недостаточностью необходимо обеспечить соблюдение покоя (пребывание в постели).
При очень тяжелом состоянии показан полный физический покой, но при этом необходимо выполнение пассивных упражнений с целью профилактики венозного тромбоза. После улучшения состояния больному следует постепенно увеличивать объем нагрузок, которые начинают с проведения дыхательных упражнений.
Больным, находящимся в стабильном состоянии, показаны такие дневные нагрузки, которые не провоцируют появление симптомов (одышки, сердцебиения, усталости). Не рекомендуются спортивные нагрузки, участие в спортивных соревнованиях, играх, тяжелый физический труд, а также нагрузки, связанные с изометрическим напряжением.
Физические тренировки по специальной программе показаны больным с сердечной недостаточностью II-III ф.кл., у которых достигнута стабилизация состояния на фоне проводимой терапии. Результаты, полученные в небольших рандомизированных наблюдениях, свидетельствуют, что у таких больных удается существенно улучшить переносимость физических нагрузок (на 15-25%), улучшить самочувствие больных. Поэтому под эгидой Европейского кардиологического общества были разработаны рекомендации по методике осуществления реабилитации таких больных (2001 г.), в которых указаны величина нагрузки, их продолжительность и частота выполнения на различных этапах тренировки.
Начальный этап. На этом этапе больным, исходно имевшим сердечную недостаточность III-IV ф. кл., рекомендуется медленная ходьба со скоростью менее 50 метров в 1 мин и продолжительностью 5-10 мин несколько раз в течение дня, что определяется на основании учета переносимости больным такой нагрузки. Величина этой нагрузки не превышает 40-50% максимального потребления кислорода (VO2). Улучшение переносимости нагрузок происходит медленно (до 4 недель).
Больным, находящимся в более удовлетворительном состоянии, можно рекомендовать ходьбу со скоростью 50 метров в 1 мин один-два раза в день в течение 15 мин.
Этап увеличения нагрузок. Улучшение состояния больных позволяет постепенно увеличивать скорость ходьбы и её продолжительность до 1 5-20-30 мин 3-5 раз в течение недели. Проведение таких тренировок обеспечивает достижение максимального результата в течение 16-26 недель.
Этап поддержания физического состояния больных обычно начинается спустя 6 мес. от начала реабилитации и должен соблюдаться постоянно. Ограничение выполнявшихся физических нагрузок на протяжении 3 недель приводит к потере достигнутого результата.
Больным, находящимся в относительно удовлетворительном состоянии, возможно выполнение тренировок на велотренажере с последующей ездой на велосипеде. Начинаются тренировки с вращения педалей без сопротивления в течение 3 мин, далее для тренировок назначается нагрузка, составляющая 50% от уровня, который был достигнут при максимальной величине потребления кислорода (VO2). В восстановительном периоде больной вращает педали при сопротивлении 10 W.
Препараты, используемые для лечения и профилактики других заболеваний
У больных с тяжелой сердечной недостаточностью особенно важно учитывать взаимодействие между препаратами, которые могут быть назначены другими специалистами для лечения соответствующих заболеваний. Такая терапия может усиливать или резко снижать эффективность препаратов, используемых для контроля застоя крови. Требуют осторожности или следует избегать назначения следующих препаратов:
Медикаментозное лечение больных с систолической формой сердечной недостаточности
В 2016 и 2017 гг были опубликованы Европейские и Американские руководства по лечению больных хронической сердечной недостаточностью, т.е. почти одновременно, что позволяет сравнивать их содержание (6, 7). Большинство рекомендаций близки или повторяют друг друга. Но, к большому сожалению, имеется немало принципиальных расхождений, чему нет научных обоснований, а различия привносятся, как правило, специалистами, представляющими чью-то заинтересованность. Врачу самому надо быть высокограмотным специалистом, чтобы сразу отказаться от «навязываемых представлений». Поэтому в зарубежных медицинских журналах прозвучала достаточно нелицеприяная критика: «We hope that physicians will understand what the guidelines are, and more importantly, what they are not. Specifically, this paper describes the emergence of a new non-existent disease; the strange battle between two bradycardic drugs (digoxin and ivabradine); the confusion that reigns over the positioning and dosing ofinhibitors of the renin-angiotensin system; and the special recommendations that have been issued for certain special populations. As Otto von Bismarck remarked, guideline deliberations are like sausages». [Наш перевод: Мы надеемся, что врачи понимают, что наличие руководств более важно, чем их отсутствие. Именно в этом документе описывается экстренная помощь новой несуществующей болезни, идет странная борьба между двумя пульсурежающими препаратами (дигоксином и ивабрадином), путаница по применению, которая царит над позиционированием и дозами ингибиторов АПФ и их специальными рекомендациями. Как Отто вон Бисмарк заметил, что руководство надо обдуманно выбирать, подобно сосиске»]. Данная ситуация дополнительно оправдывает создание Международного Консорциума специалистов в защиту больных.
Ингибиторы АПФ. Данные, полученные во многих рандомизированных и плацебо контролируемых исследованиях, свидетельствует об эффективности и безопасности ингибиторов ангиотензин превращающего фермента (АПФ) при их использовании у больных систолической формой сердечной недостаточности (СН), включая её бессимптомную стадию, которая распознается при наличии фракции выброса (ФВ) левого желудочка менее 40-45%. Кроме положительного влияния на выживаемость, эти препараты улучшают функциональное состояние больных, хотя при этом оказывают малое влияние на их физические возможности (8). Ингибиторы АПФ тормозят дальнейшее расширение камер сердца и снижение фракции выброса левого желудочка. Терапия иАПФ больных, перенесших инфаркт миокарда, снижает также риск реинфаркта.
Обеспечивает достижение перечисленных эффектов только использование целевых доз препаратов, для чего необходимо их постепенное повышение, начиная с малых. Целевая доза - это максимальная доза, при использовании которой были получены доказательства положительного влияния на общую летальность.
Препараты и их целевые дозы, установленные в контролируемых исследованиях и приняты в обоих Руководствах, представлены в таблице 2.
Таблица 2. Ингибиторы АПФ, получившие доказательства положительного влияния на выживаемость больных
| Препарат | Начальная доза | Дозы, снижающие летальность | |
| Целевая | Максимальная | ||
| Каптоприл | 6,25 мг | 50 мг 3 раза в сутки | 150 мг |
| Эналаприл | 2,5 мг | 10 мг 2 раза в сутки | 40 мг |
| Лизиноприл | 2,5 мг | 20-25 мг в день | 35 мг |
| Рамиприл | 1,25-мг 2,5 мг |
5 мг 2 раза в день | - |
| Трандолаприл | 1 мг | 4 мг в день | - |
У больных с систолическим артериальным давлением ниже 100 мм рт.ст. начальная доза иАПФ должна быть в 2 раза меньше указанной в таблице. Доза препарата в стационаре может увеличиваться спустя несколько дней, в амбулаторных условиях - спустя 7-14 дней. У больных АГ рекомендуется поддерживать его уровень ниже 130/80 мм рт. ст. (6, 7).
Другие иАПФ (беназеприл, квинаприл, периндоприл, цилазаприл, фозиноприл) в длительных контролируемых исследованиях у больных с сердечной недостаточностью не изучались и поэтому их целевые дозы пока не определены. Эти препараты не рекомендованы Европейским и Американским обществами кардиологов для применения (201 6, 201 7 гг.) у больных сердечной недостаточностью.Абсолютные противопоказания для назначения иАПФ:
Выбор дозы иАПФ. Впервые терапию начинают с назначения минимальной дозы. После первого приема даже минимальной дозы во избежание избыточного снижения артериального давления в вертикальном положении рекомендуется больному находиться в постели в течение нескольких часов или принять препарат перед сном. Риск гипотонии увеличивается у больных, принимающих большие дозы диуретиков, у больных с гипонатримией или с нарушенной функцией почек, а также у пожилых. Поэтому важно избегать их назначения в течение 24-48 часов после использования больших доз диуретиков, после обильного диуреза. До начала терапии иАПФ следует отменить калийсберегающие препараты и нестероидные противовоспалительные средства.
Систолическое артериальное давление ниже 90 мм рт.ст. на фоне терапии иАПФ и при сохранении удовлетворительного самочувствия больного (отсутствие головокружения, слабости, тахикардии в вертикальном положении) не служит показанием для отмены препарата.
Антагонисты рецепторов ангиотензина II. Данная группа препаратов рекомендуется для лечения больных, как альтернативная ингибиторам АПФ, в тех случаях, когда последние вызывают побочные реакции (кашель, ангионевротический отек). В проведенных исследованиях они оказали положительное влияние на выживаемость больных с сердечной недостаточностью. Впервые в 2014 г. в работе (9) приведены результаты сравнительной оценки ингибиторов АПФ, антагонистов А2 рецепторов и плацебо у сопоставимых (score - matchedpopulation) групп больных (всего 4 425 чел). Терапия продолжалась 5 лет. Результаты: 1) терапия иАПФ или антаг. А2 рецепторов при сравнении с плацебо снизила летальность (р = 0,03), 2) терапия иАПФ в сроки от 2 до 5 лет обеспечила более высокую выживаемость (р<0,001). Следовательно, в используемых сегодня дозах антагонсты А2 рецепторов не могут быть препаратами первого выбора в лечении больных с сердечной недостаточностью. Наибольшее количество доказательств пользы получили валсартан (начальная доза 40 мг 2 раза, максимальная - 160 мг 2раза в сутки), кандасартан (начальная 4-8 мг и максимальная - 32 мг 1 раз в сутки). Лосартан даже в суточной дозе 150 мг мало повлиял на смертность. Его включили только в последние Европейские рекомендации (до этого считали препаратом, не имеющим доказательств пользы). Дозы 25-50 мг, широко назначаемые в нашей стране, малоэффективны или бесполезны.
Выбор дозы антагониста А2 рецепторов осуществляется подобно иАПФ, т.е. начинают с малой и постепенно увеличивают до целевой. Переносимость этих препаратов очень хорошая. Однако при подборе дозы необходимо оценивать состояние функции почек (содержание в крови калия и креатинина) в такие же сроки, как и при терапии иАПФ.
Недавно были опубликованы результаты исследования нового комбинированного препарата для лечения больных с систолической формой сердечной недостаточности - блокатора РААС и стимулятора сннтеза эндогенного натрийуретического пептида (10 ). У 8 442 больных с СН II-IV функционального класса (ФК) новый препарат LCZ696 (валсартан + ингибитор неприлизина (сакубитрил)) сравнили с эналаприлом. Дозы LCZ696 составили 200 мг 2 раза, эналаприла -10 мг 2 раза в день. Результаты оказались следующими: а) общая смертность была ниже в 1-ой группе (17% VS 19,8%, р<0,001), б) кардиоваскулярная летальность также снизилась (на 20%, р<0,000...), в) толерантность к нагрузкам выросла. Авторы сделали вывод, что препарат должен заменить иАПФ и антагонисты А2 рецепторов, которые сегодня используются для лечения многих больных. В этом исследовании новое вещество использовалось в максимально разрешенной дозе, а эналаприл только в половинной (20 мг в сутки, а не 40 мг.) И если исходить из требований точной медицины, то это пример некачественного протокола исследования (11). Требуется проведение повторного исследования с использованием сопоставимых дозировок. Поэтому вывод, что этот препарат должен заменить эналаприл, более чем преждевременен.
Диуретики. Показанием для назначения данной группы препаратов у больных с сердечной недостаточностью является наличие застоя крови (застойные хрипы в легких, увеличение печени в связи с застоем крови в большом круге кровообращения, а также появление жидкости в подкожной клетчатке на ногах, иногда в области поясницы, а также в плевральной или брюшной полостях). Такая терапия уменьшает выраженность симптомов сердечной недостаточности и увеличивает толерантность к нагрузкам. До настоящего времени остается неясным какой режим назначения диуретиков является наиболее оптимальным для длительного лечения больных с сердечной недостаточностью. В американском руководстве по лечению больных сердечной недостаточностью (7) для выбора оптимальной длительной терапии диуретиком и обеспечения эуволемического состояния больного было рекомендовано регулярное определение содержания в крови натрийуретического пептида.
В рандомизированном, в сравнении с плацебо DIG исследовании (12) при ретроспективном анализе результатов, полученных в специально отобранных группах больных - «двойников» (2782 чел.), у которых на терапии не было симптомов или имелись минимальные проявления сердечной недостаточности (ф.кл. I-II), было установлено достоверное увеличение летальности (на 25%, р<0,002) при продолжении терапии диуретиками, по сравнению с теми, кто её не получал. Другая проводившаяся терапия была одинаковой (иАПФ у 92%, дигоксин у 51-52% больных).
Несмотря на то, что больные в эти группы были подобраны ретроспективно, полученные данные не могут быть проигнорированы. Вероятно, они свидетельствуют о том, что терапия диуретиками должна быть строго обоснованной (только при наличии клинически значимых проявлений застоя крови), а также, по-видимому, не у всех больных с умеренными отеками на голенях необходима активная терапия с помощью диуретиков.
В рекомендациях Европейского общества у больного, с впервые выявленной сердечной недостаточностью с явлениями застоя крови и не получавшего диуретика, терапию начинают с малой его дозы и постепенно увеличивают до той, которая обеспечивает прирост суточного диуреза на 200-600 мл. Не рекомендуется провоцировать избыточный (форсированный) диурез (на 800 мл и более выделенной мочи по сравнению с принятым количеством жидкости).
У больных с умеренно выраженной сердечной недостаточностью терапию начинают с назначения диуретиков из группы умеренных диуретиков. Но у больных с тяжелой формой недостаточности или у больных с ухудшением состояния на фоне приема умеренных диуретиков показано использование петлевых диуретиков. Отсутствие диуретического эффекта после приема перорально большой дозы петлевого диуретика может свидетельствовать о наличии нарушения всасывания препарата в кишечнике или о наличии почечной недостаточности. В этих случаях показано продолжительное внутривенное инфузионное их введение (например, фуросемид 5-40 мг в 1 час.).
Умеренные (тиазидовые) диуретики характеризуются малой эффективностью у больных со сниженной скоростью гломерулярной фильтрации (менее 30 мл/ мин), что достаточно часто наблюдается у больных пожилого возраста. В этих случаях, также как и в случае наличия почечной недостаточности, показано применение петлевых диуретиков.
В последнем Американском Руководстве (7) тиазидовые диуретики в отдельности не рекомендованы для лечения больных с систолической сердечной недостаточностью и только могут быть назначены в случае недостаточного эффекта на терапии петлевыми мочегонными препаратами. Известно, что тиазидовые и петлевые диуретики обладают синергизмом действия. Поэтому при отсутствии достаточного диуреза на терапии петлевыми назначали их комбинацию давно, не прибегая к использованию очень высоких доз петлевых диуретиков, что часто сопровождается увеличением риска побочных эффектов.
Диуретики оказывают положительное влияние на состояние больного с хронической застойной сердечной недостаточностью благодаря уменьшению объема циркулирующей жидкости (крови), снижению давления наполнения сердца, что сочетается с уменьшением напряжения стенок желудочков сердца, застоя крови в легких и периферических отеков. Однако избыточное уменьшение объема плазмы вызывает увеличение продукции ренина, ангиотензина, альдостерона и катехоламинов, что приводит к возникновению парадоксального эффекта, т.е. к задержке натрия, воды, что обусловливает прогрессирование болезни.
В настоящее время после ликвидации застоя крови диуретики должны назначаться в минимальной поддерживающей дозе, которая обеспечивает предупреждение задержки жидкости и увеличения веса тела при условии сохранения стабильного режима питания. Это достигается при наличии адекватного наблюдения врачом за состоянием больного и строгого выполнения больным советов врача-специалиста. Научных доказательств по режиму приема поддерживающей дозы диуретиков пока не получено. Но в настоящее время наиболее часто рекомендуется принимать диуретик в индивидуально подобранной дозе регулярно, не прибегая к так называемой прерывистой терапии. Бесконтрольное продолжение регулярного приема диуретика после исчезновения отеков может сопровождаться увеличением летальности таких больных, очень важно контролировать ОЦК с целью предупреждения развития гиповолемии. С этой целью рекомендуют определение содержания в крови натрийуретических пептидов, в частности, промозгового пептида.
Тиазидовые и петлевые диуретики оказывают диуретическое действие в условиях наличия сниженного рН крови (в кислой среде). Но в ходе лечения кислотно-щелочное равновесие может измениться и рН увеличиться (стать щелочной). В этих условиях диуретическое действие может оказать только ингибитор карбоангидразы - диакарб (фонурит). Его назначают в течение нескольких дней (до 5 дней) 1 раз в день в дозе 0,25-0,5 г.
Причины рефрактерности к диуретикам:
Наиболее часто встречающимся нежелательным их действием является гипокалиемия, которая даже на фоне терапии иАПФ выявляется у каждого 3-4 больного с III-IV ф.кл. сердечной недостаточности, что требует проведения заместительной терапии препаратами калия в дозе 3 грамма и более в сутки с последующим назначением калийсберегающего препарата (триамтерена или амилорида). Но в настоящее время таким больным в первую очередь рекомендуется назначить спиролактон (альдактон) в индивидуально подобранной дозе (12,5-50 мг в день). Альдактон, как было показано в длительном плацебо-контролируемом исследовании RALES, значимо (на 30%) снижает летальность среди тяжелых больных, что вероятно обусловлено не только устранением гипокалиемии, но также и подавлением синтеза альдостерона, уменьшением отрицательного воздействия диуретиков на ренин-ангиотензин-альдостероновую систему.
В соответствии с рекомендациями Европейского общества кардиологов (6) всем больным сердечной недостаточностью II-IV ф.кл. показана, наряду с ингибитором АПФ, терапия альдактоном в малых дозах. Противопоказанием для его назначения является наличие нарушения функции почек (креатинин более 250 микромоль/л и содержание калия в сыворотке более 5 ммоль/л). Тактика его применения следующая: первая доза не должна превышать 2 5 мг в сутки, спустя 4-6 дней повторно определяют содержание креатинина и калия и в случае повышения содержания калия в пределах 5,0-6,0 ммоль/л дозу альдактона уменьшают до 12,5 мг в сутки. Уровень содержания калия более 6,0 ммоль/л служит показанием для отмены препарата. У больных с нормокалиемией при сохранении симптомов сердечной недостаточности, несмотря на проводимую в течение 1 мес. терапию, дозу альдактона увеличивают до 50 мг. После этого через 5-7 дней определяют содержание калия, креатинина и, если уровень калия превышает 5 ммоль/л, то возвращаются к прежней дозе. Сохранение сниженного содержания калия в сыворотке крови служит показанием для назначения калийсберегающих препаратов (амилорид или триамтерен), начиная с малой дозы. После контрольных исследований на содержание в крови калия их доза постепенно повышается до ликвидации гипокалиемии или достижения их максимальной дозы.
Антагонисты синтеза альдостерона (альдактон, эплеренон), назначенные дополнительно к иАПФ и другим препаратам, достоверно улучшают отдаленные исходы. В определенной степени такой эффект обусловлен торможением действия альдостерона, содержание которого в крови многих больных с сердечно-сосудистыми заболеваниями повышено и оказывает отрицательное влияние на прогноз их жизни. Об этом свидетельствуют данные, полученные в исследовании LURIC, в котором наблюдались 3 153 больных с ИБС, АГ, СН, получавших терапию ингибитором АПФ или ингибиторами рецепторов А2 (62%), бета-блокаторами (70%), антагонистами кальция (11%) и диуретиками (24%). Повышенное содержание альдостерона у больных ИБС, АГ достоверно ассоциировалось с риском смерти, а при возникновении ОКС - с риском внезапной смерти. У больных с систолической формой сердечной недостаточности ее тяжесть имела достоверную связь с уровнем содержания альдостерона, а у больных с диастолической ее формой в группе с высоким содержанием альдостерона отмечено также наличие связи с риском смерти.
При терапии альдактоном у некоторых больных развивается гинекомастия. Значительное увеличение грудных желез и появление боли является показанием для отмены альдактона. При наличии эплеренона такого больного можно перевести на его прием (13). В исследовании EMPHASIS, включавшем 2 584 больных с СН I-II ф.кл. NYHA после перенесенного инфаркта миокарда (ФВ 30-35%), медиана наблюдения составила 21 мес. Результаты длительного лечения подтвердили целесообразность использования препаратов из этой группы не только при лечении сердечной недостаточности III-IV функционального класса:
а) летальность от любых причин в группе на эплереноне составила 19,8%, в контрольной - 27,4% (р<0,001);
б) летальность от кардиоваскулярных причин -10,8% и 13,5% (р=0,01) соответственно по группам;
в) госпитализировано по всем причинам 29,9% и 35,8%, соответственно;
г) госпитализировано в связи с СН 12% и 18,4% (р<0,001), соответственно;
д) содержание К+ в сыворотке более 5,5 моль/л было у 11,8% и 7,2% (р<0,001), а менее 4 моль/л -у 38,8% и 48,4% (р<0,001), соответственно.
Не только гипокалиемия, но и относительно невысокие показатели содержания калия в сыворотке крови больного сердечной недостаточностью ассоциируются с увеличением риска общей и кардиоваскулярной летальности, а также риска прогрессирования тяжести застойных явлений. Кроме давно известного факта, что гипонатриемия ассоциируется с плохим прогнозом, в последних работах показано, что и гипохлоремия также обладает прогностически неблагоприяным влиянием.
Антагонисты рецепторов AII являются препаратами выбора для лечения больных, у которых возникли побочные действия во время приема ингибиторов АПФ (кашель, ангионевротический отек).
Сердечные гликозиды. Это единственная группа препаратов с положительным инотропным и отрицательным хронотропным действием, которая в терапевтических дозах используется для длительного лечения больных с систолической формой сердечной недостаточности во всех странах мира. Но в последнем руководстве, принятом в США (2017 г), эта группа не рекомендована для лечения больных сердечной недостаточностью, что является вероятно следствием конкурентной борьбы с ивабрадином (объяснения не представлено). В Европейском руководстве сердечные гликозиды остаются в составе средств для лечения данной группы больных. Дигоксин и дигитоксин являются наиболее часто назначаемыми сердечными гликозидами. Дигитоксин метаболизируется в печени, выделяется с желчью и поэтому его применение наиболее оправдано у больных с нарушенной функцией почек.
Показания для назначения сердечных гликозидов следующие: 1) необходимость замедления ритма желудочков у больных с фибрилляцией предсердий при любой степени выраженности симптомов сердечной недостаточности, особенно в комбинации с блокатором бета-адренорецепторов, которая в наибольшей степени обеспечивает урежение частоты сердечных сокращений в покое и во время стресса; 2) улучшения состояния больного с систолической формой сердечной недостаточности III-IV ф.кл., особенно при наличии синусовой тахикардии.
В рандомизированном и плацебо контролируемом исследовании DIG (12) было показано, что средняя суточная доза дигоксина составляет 0,375 мг. Эта доза обеспечивает достижение терапевтической концентрации препарата в крови почти у 90% больных и достоверно улучшает качество жизни больных, особенно у имеющих очень низкую фракцию выброса левого желудочка. В группе лечения по сравнению с плацебо летальность в целом не уменьшилась. Однако дополнительный анализ результатов в подгруппах с различной тяжестью состояния больных выявил наличие достоверного снижения риска летального исхода в группе более молодого возраста, требовавших меньшее количество диуретиков, с меньшим кардиоторакальным индексом, с меньшим уровнем содержания креатинина крови и с более успешным контролем застоя крови в легких, что сочеталось, по-видимому, с необходимостью использования меньших доз дигоксина (концентрация его в крови у этих больных была менее 1 нг/мл).
В группе, которая на основании перечисленных показателей, характеризовалась как состоящая из более тяжелых больных (различия высоко достоверны, р<0,001), концентрация дигоксина также оказалась выше (более 1 нг/мл). Очевидно, что врачи для достижения терапевтического эффекта были вынуждены назначать более высокую дозу дигоксина. В этой группе летальность изменилась недостоверно, но была выше и была сопоставимой с летальностью в контрольной группе, состоявшей из таких же больных «двойников» (р=0,08).
Противопоказаниями для назначения сердечных гликозидов являются: наличие у больных сердечной недостаточностью: синусовой брадикардии, слабости синусового узла, синдрома Wolff - Parkinson - White, обструктивной кардиомиопатии, атриовентрикулярной блокады II-III ст., гипокалиемии, гиперкальциемии.
До назначения гликозидов следует определить уровень содержания креатинина и калия в сыворотке крови больного. При наличии нормальных показателей и относительно стабильного состояния больному в течение нескольких дней рекомендуется в амбулаторных условиях принимать дигоксин по 2 таблетки в день; поддерживающая доза у большинства больных составляет 0,25 мг в день. У больных с повышенным содержанием креатинина индивидуальная доза должна быть уменьшена в соответствии со степенью снижения клубочковой фильтрации (клиренс креатинина рассчитывается по формуле Cockroft, Gault). Но, по-видимому, для лечения таких больных более оправдано использование дигитоксина. В рекомендациях Европейского общества кардиологов от 2008 г. при длительном лечении предлагается обеспечивать концентрацию дигоксина в крови в пределах 0,6-1,2 нг/мл.
У лиц старческого возраста доза дигоксина также должна быть уменьшена (0,0625-0,1 25 мг и редко - 0,25 мг).
Блокаторы бета-адренорецепторов. В проведенных контролируемых исследованиях было доказано, что терапия кардиоселективными бета-блокаторами (метопрололом сукцинатом, бисопрололом) значительно увеличивают выживаемость, улучшают инотропную функцию миокарда и качество жизни больных. Терапия больных старческого возраста бета-блокатором с вазодилятирующими свойствами - небивалолом - лишь улучшила качество жизни и не повлияла на летальность. Сегодня следует учитывать, что кардиоселективные бета-адреноблокаторы, получившие доказательства положительного влияния на выживаемость, разрешено применять у больных любого возраста. Сравнительная оценка карведилола и метопролола резината (исследование СОМЕТ) является примером некорретно организованного исследования и его результаты нельзя оценивать положительно с позиции точной медицины. Кроме того, общая частота избранной конечной точки на максимальной дозе карведилола была абсолютно одинаковой, что и на мало эффективной дозе метопролола тартрата. В итоге, только метопролол и бисопролол в адекватно подобранных дозах можно рекомендовать для лечения, как имеющие доказательства положительного влияния на выживаемость больных с систолической формой сердечной недостаточности.
Общие требования, которые должны быть учтены перед началом терапии больных с систолической формой сердечной недостаточности с помощью бета-блокатора:
При анализе полученных результатов в исследовании SHIFT (14) пришли к заключению, что эффективность бета-блокатора ассоциируется с урежением ритма сердца. У больных из группы плацебо увеличение ЧСС на каждый удар сочеталось с ростом числа комбинированной конечной точки (к.к.т.) на 3% (р<0,0001). Исходная ЧСС выше 87 уд. в 1 мин ассоциировалась с увеличением к.к.т. в 2 и более раза (р<0,0001) .
Терапия бисопрололом в индивидуально подобранных дозах (от 1,2 5 мг до 10 мг) также обеспечила снижение общей летальности на 32% (р<0,0001). Суточная доза препарата почти у половины больных составила 10 мг и только лишь у трети - менее 5 мг.
Для обеспечения оптимальной частоты сердечного ритма у больных сердечной недостаточностью (около 60 в 1 мин при ее хорошей переносимости) в руководстве АККФ/ААС (2013 г.) рекомендована следующая тактика выбора препарата(ов) и уровень их доказательности:
Вазодилятаторы. Эта группа препаратов рассматривается как дополнительная или как терапия второго или третьего выбора. Из этой группы доказательства наличия пользы были получены при длительной терапии комбинацией изосорбида динитрата и гидралазина (апрессина) в дозах соответственно 20-40 мг 4 раза в сутки (или в ретардной форме 2 раза в сутки) и 25-75 мг 3-4 раза в сутки. Прием препаратов в данной комбинации оказывает более выраженное инотропное действие, чем ингибиторы АПФ.
В исследовании A. L. Taylor с соавт. (2004 г.) было показано, что присоединение к стандартной терапии (иАПФ, бета-блокатор, диуретик, дигоксин) комбинации изосорбида динитрата и апрессина (1050 больных с III-IV ф.кл.) привело к достоверному, по сравнению с плацебо, снижению летальности (6,2% и 10,2% соответственно). Эти результаты могут служить основанием для такого лечения больных, у которых невозможно использование ингибиторов АПФ в комбинации с альдактоном или с антагонистами рецепторов АН (например, из-за возникающей гиперкалиемии), а также в случае недостаточной эффективности терапии препаратами из всех четырех групп. В руководстве ACCF|AHA (2013, 2017 г.) рекомендовано использовать комбинацию гидралазина и изосорбида-динитрата у African-American больных с систолической формой сердечной недостаточности III-IV функциональных классов и вероятно у больных с наличием протвопоказаний или с непереносмостью иАПФ и антагонистов А2 рецепторов.
К сожалению, данная комбинация вазодиллятаторов в нашей стране отсутствует, а больных с противопоказаниями для терапии иАПФ и атагонистами А2 рецепторов много. Но, сегодня мы располагаем другим вазодилля-татором с двойным механизмом действия - никорандилом, который достаточно широко используется в странах Европы и Азии. В нашей стране он производится под наименованием Кординик (компания ПИК-ФАРМА) и применяется при лечении больных стенокардией, преимущественно, вместо пролонгированных нитратов. Сегодня имеются доказательства его положительного влияния на показатели гемодинамики у больных с систолической формой сердечной недостаточности. Например, в двойном слепом, рандомизированном исследовании у 25 больных с застойной сердечной недостаточностью оценили острый гемодинамический эффект никорандила после приема внутрь в дозах от 10 мг до 60 мг (16). Последняя доза статистически значимо снизила общее систолическое и диастолическое АД, давление в правом предсердии, давление заклинивания в легочных капиллярах,системное и легочное сосудистое сопротивление, систолическое и диастолическое АД в легочной артерии. Доза препарата 40 мг вызывала подобные гемодинамические изменения результатов при оценке сердечного индекса, а также системного и легочного сопротивления. Другие гемодинамические показатели также изменялись в меньшей степени. Все показатели вернулись к исходному состоянию в пределах 3 час. На дозах 10 и 20 мг все показатели не изменялись в значительной степени. Определение содержания препарата показало, что эти изменения ассоциировались с быстрым уменьшением его концентрации в крови.
В другом исследовании результаты проведенного мета-анализа данных, полученных при наблюдении за 1 222 больными с сердечной недостаточностью на терапии никорандилом (17). Из них в 5 рандомизированных исследованиях продемонстрировано снижение общей летальности (р<0,001), улучшение насосной функции сердца (р=0,02). А в 15 наблюдательных исследованиях терапия не только улучшила функциональный класс больных с сердечной недостаточностью, но также снизила давление заклинивания в легочных капиллярах в среднем на 6,86 мм рт.ст. (р<0,01) и общее артериальное давление в легочной артерии (р<0,001). Дозы препарата колебались в пределах 1 5-30-40-60 мг в день. В контролируемых исследованиях показано, что на терапии наблюдается достоверное сижение систолического и диастолического АД (в среднем на 6 мм и 6,6 мм рт.ст., соответственно (р=0,006). При этом не отмечено существенного изменения ЧСС (р=0,7). В пилотном исследовании с изучением эффективности никорандила (Кординик, компания ПИК-ФАРМА) у больных со стабильно протекающей ИБС, осложненной ХСН с низкой ФВ ЛЖ прием препарата по 10 мг 3 раза в сутки к 48-й неделе снизил КСО ЛЖ на 12,3 % (р<0,05), ФВ ЛЖ возросла на 14,5 % (р<0,05), отношение пиковых скоростей трансмитральных диастолических потоков Е / А увеличилось на 12,5 % (р<0,05) (18). В группе плацебо достоверных изменений не было. Кординик не вызвал серьезных нежелательных явлений. В недавно опубликованном ретроспективном исследовании изучали смертность больных с СН ишемической этиологии в зависимости от влияния перорального приема никорандила (средний период наблюдения - 963 дня, n=334) (19). В анализе выживаемости Каплана-Мейера сердечная смертность была ниже в группе никорандила, чем в контрольной: 11,2% VS 19,7% (p=0,032). Никорандил снижал относительный риск сердечной смерти на 48,8% (p=0,035).
Длительный и положительный опыт применения препарата у больных стенокардией, а также данные о положительных изменениях гемодинамики в большом и малом круге кровообращения у больных с систолической сердечной недостаточностью, позволяют полагать, что в случае наличия противопоказаний для терапии ингибитором АПФ и антагонистом А2 рецепторов, препарат может быть использован, как минимум, для улучшения качества жизни, а также выживаемости этих больных при индивидуальном подборе его дозы.
В течение многих десятилетий в нашей стране у больных сердечной недостаточностью врачи широкой практики считали обязательным назначение препаратов, которые «улучшают метаболизм миокарда». В 60-е годы ХХ века это были витамины, кокарбоксилаза, АТФ, креатинфосфат, которые были вытеснены рибоксином, а затем предукталом, милдронатом. Эти вещества не имеют доказательств пользы для больных и поэтому не включены в принятые в странах Европы и Америки рекомендации по лечению любых заболеваний.
В настоящее время в качестве «цитопротектора» для этих больных следует рекомендовать омега-3 ненасыщенные жирные кислоты в суточной дозе около 1 г., получившие доказательства положительного влияния на их выживаемость (кл. II B).
Положительное действие омакора у этих больных можно частично объяснить положительным влиянием на инотропную функцию миокарда. В исследовании (20) наблюдалось 133 больных, имевших умеренные проявления сердечной недостаточности на фоне стандартной терапии. Через 12 мес. терапии были выявлены значимые различия (р<0,001) в изменении фракции выброса левого желудочка (увеличение на 10,4% при приеме омакора и снижение ее на 5% при приеме плацебо).
Альфа-адреноблокаторы (празозин, доксазозин) могут увеличить летальность, что было продемонстрировано 1986 г в исследовании V HeFT-1. Поэтому их не следует применять у больных со сниженной фракцией выброса (5).
Антагонисты кальция. Пульсурежающие препараты (верапамил, дилтиазем), изучавшиеся у больных после инфаркта миокарда, увеличивали летальность в группе, которая имела признаки застоя крови в легких (рентгенологические данные) или в острой стадии инфаркта миокарда была сердечная недостаточность. Поэтому у больных с систолической формой сердечной недостаточности их применение противопоказано.
Дигидропиридиновая группа антагонистов кальция в длительных наблюдениях при их применении у больных с сердечной патологией не оказала какого-либо эффекта на отдаленные исходы и поэтому могут быть использованы в качестве дополнительной терапии при необходимости, например, контроля стенокардии или артериальной гипертонии (21).
Левосимендан, незиретид также являются вазодилятаторами с положительным инотропным действием. Их инфузионное введение у больных с острой сердечной недостаточностью, по сравнению с добутамином, лучше переносится больными. Но убедительных данных, свидетельствующих об их положительном влиянии на отдаленные исходы, пока не получено.
Нарушения ритма и проводимости. Показаниями для антиаритмической терапии является наличие у больного фибрилляции предсердий или других над-желудочковых пароксизмальных форм тахикардии, а также пароксизмальной желудочковой тахикардии.
Антиаритмические препараты I класса не должны применяться из-за их отрицательного влияния на сократимость миокарда и увеличения риска летального исхода в результате их проаритмического (профибрилляторного) действия.
Препараты II класса (кардиоселективные блокаторы бета-адренорецепторов) показаны для лечения сердечной недостаточности и хотя их антиаритмическая эффективность невелика, но они обладают антифибрилляторным действием, что обеспечивает уменьшение летальности, в первую очередь, благодаря снижению количества случаев внезапной смерти. Их также используют в комбинации с амиодароном для лечения желудочковой тахикардии.
У больных с сердечной недостаточностью, имеющих приступы желудочковой тахикардии, единственным препаратом, который может оказаться полезным, является амиодарон в индивидуально подобранной дозе, обеспечивающей достаточное снижение частоты синусового ритма (около 60 ударов в 1 мин) и умеренное удлинение коррегированного интервала QT (около 0,50 с). Омега-3 ПНЖК (омакор) обычно в рекомендациях представлен как дополнительная терапия у тяжелой группы больных (кл. II B).
В настоящее время не получено доказательств пользы от имплантации кардиовертера-дефибриллятора больным с умеренными проявлениями хронической застойной сердечной недостаточности и с короткими пробежками желудочковой тахикардии по сравнению с оптимальной медикаментозной терапией.
Сердечная недостаточность предрасполагает также к возникновению других желудочковых нарушений ритма сердца и фибрилляции предсердий. Для уменьшения риска их возникновения целесообразно обеспечить применение целевых доз ингибиторов АПФ и кардио-селективных блокаторов бета-адренорецепторов (метопролол сукцинат, бисопролол). Крайне важно также обеспечить предупреждение гипокалиемии. Её наличие устраняется с помощью верошпирона или калийсберегающих препаратов (например, триамтерена). Калий-заместительная терапия является менее эффективной, так как не снижает риска летального исхода.
Для купирования и профилактики пароксизмов фибрилляции предсердий следует также использовать амиодарон, так как это единственный препарат, который не оказывает клинически значимого отрицательного влияния на сократимость миокарда и может оказать положительное влияние на выживаемость. При индивидуальном подборе эффективной дозы частота опасных побочных действий (альвеолит, гепатит) невелика.
Дофетилид, новый препарат из III класса антиаритмических средств, в проведенном исследовании не оказал положительного влияния на выживаемость больных сердечной недостаточностью. Поэтому его можно рекомендовать лишь как препарат второго выбора (после амиодарона) для улучшения качества жизни больных с сердечной недостаточностью и пароксизмами тахикардии.
У больных с нарушением функции проводящей системы сердца целесообразна имплантация двухкамерного электрокардиостимулятора.
Уширение комплекса QRS (0,12 сек и более) у больных сердечной недостаточностью ухудшает прогноз. Имплантация электрокардиостимулятора/кардиовертера-дефибриллятора с возможностью обеспечения бивентрикулярной стимуляции существенно увеличивает фракцию выброса левого желудочка, а также улучшает прогноз жизни.
Нарушения ритма сердца. Нет доказательств необходимости регистрации у всех больных Холтер ЭКГ для выявления нарушений ритма сердца. Исследование показано при наличии симптомов, вероятно обусловленных аритмией. Холтер мониторирование ЭКГ выявляет у всех больных наличие желудочковых экстрасистол и достаточно часто - короткие пробежки желудочковой тахикардии. Брадикардия и паузы также очень часто регистрируются, особенно в ночное время. Их триггером вероятно является апноэ сна. Остановки функции синусового узла, брадикардия ассоциируются с плохим прогнозом. Фибрилляция предсердий является наиболее частой формой тахиаритмии у больных с сердечной недостаточностью и не зависит от величины ФВ левого желудочка.
Таблица 3. Контроль частоты ритма жедудочков при ФП у больных с СН (Реком. ЕОК, 2016 г)
| Рекомендации | Класс доказательства | Уровень согласия |
| Ургентная электрокардиоверсия | I | C |
| У больных с СН IY ф.к. внутривенно амиодарон + болюсно дигоксин (если они не использовались и нет непереносимости) |
IIa | B |
| У больных с СН I—III кл. бета-блокатор внутрь (важно наличие эуволемии) |
I | A |
| У б-х с СН I - III кл. дигоксин, а при сохранении частого ритма добавляется бета — блокатор, а также при наличии противопоказаний для бета-блокаторов |
IIa | B |
| Аблация АВ узла при не эффективности препаратов или противопоказаниях к ним |
IIb | B |
| Дронедарон абсолютно противопоказан | III | A |
У больных с впервые выявленной ФП в первую очередь следует исключить наличие нарушения функции щитовидной железы, электролитного дисбаланса, порока сердца и т.п. Все препараты, которые используются для лечения больных сердечной недостаточностью, уменьшают риск ее развития. За исключением «нового средства» -ивабрадина, который достоверно увеличивает его. Кроме того, у этих больных он снижает сократительную способность миокарда левого жедудочка.
Оптимальной частотой ритма при лечении больных с СН, если исходить из данных, полученных в доказательных исследованиях на терапии метопрололом и бисопрололом, является ЧСС около 60 в 1 мин. (5). Это, в определенной степени, подтверждается данными, полученными в исследовании SHIFT в контрольной в группе больных, получавших плацебо. У больных из данной группы увеличение ЧСС на каждый удар сочеталось с ростом числа комбинированной конечной точки (к.к.т.) на 3% (р<0,0001). Исходная ЧСС выше 87 уд. в 1 мин ассоциировалась с увеличением числа к.к.т. в 2 и более раза (р<0,0001).
Для профилактики рецидивов ФП используется амиодорон, возможно в течение длительного времени при обеспечении контроля функции щитовидной железы. В случае развития первого приступа ФП у больного со слабо выраженными симптомами СН назначают для контроля ритма бета-блокатор, а при выраженной СН предпочтение отдается гликозиду (с учетом функции почек).
Внутрисосудистое тромбообразование и его профилактика. У больных с сердечной недостаточностью резко увеличивается риск образования тромбов в венах нижних конечностей и внутри камер сердца, особенно в предсердиях при их фибрилляции. У больных с тяжелой сердечной недостаточностью неожиданная смерть чаще обусловлена тромбоэмболией, чем аритмией. Данные о частоте выявления тромбоза вен у больных, госпитализированных в связи с сердечной недостаточностью, весьма противоречивы, также как и частота возникновения тромбоэмболии легочной артерии. Вместе с тем, проведенные исследования (22) с целью оценки роли гепаринов (например, эноксипарина 40 мг/сут) продемонстрировали снижение риска развития тромбоза вен и тромбоэмболии с 14,9% (на плацебо) до 5,5%.
К группе высокого риска развития венозного тромбоза следует относить больных с патологией вен нижних конечностей, длительно находящихся на постельном режиме, больных с тяжелой сердечной недостаточностью, требующих активной терапии диуретиками, а также ведущих малоподвижный образ жизни в связи с различными заболеваниями (после инсульта, болезни опорно-двигательного аппарата, особенно принимающих нестероидные противовоспалительные препараты). В этих случаях представляется целесообразным использовать для профилактики тромбоза и тромбоэмболии один из низкомолекулярных гепаринов в достаточной дозе с учетом возраста и функции почек.
У большинства больных с тяжелой формой сердечной недостаточности при длительном пребывании в постели развивается тромбоз глубоких вен нижних конечностей, что сопровождается возникновением большого риска тромбоэмболии легочной артерии. Результаты контролируемых исследований, в которых оценивалась эффективность низкомолекулярных гепаринов, демонстрируют наличие снижения частоты возникновения периферических тромбозов при использовании этих препаратов в достаточно больших дозах. Поэтому при длительном пребывании больного в постели показано проведение антикоагулянтной терапии с целью профилактики тромбообразования и тромбоэмболии.
Показаниями для восстановления ритма сердца у больных является недостаточная эффективность оптимальной терапии хронической сердечной недостаточности. Восстановление ритма может быть достигнуто с помощью введения амиодарона или электрошоковой терапии. Предварительное насыщение амиодароном может повысить эффективность электроразряда, а ее продолжение обеспечить профилактику рецидива аритмии. Препараты I класса и дронедарон (мультак) противопоказаны, так как увеличивают риск смерти .
Наличие у больных сердечной недостаточностью нарушения функции почек и анемии по сравнению с группой больных, не имевших указанных нарушений, достоверно ухудшает прогноз (р<0,0001), в частности, каждое уменьшение гемоглобина на 1 г/дл сочетается с увеличением частоты конечных точек на 17% (р=0,0001). У таких больных резко возрастает необходимость трансплантации сердца, которая в течение 3-х летнего наблюдения может возникнуть у 14 %-53% случаев (5).
| Рекомендации ЕОК (2016 г) по профилактике тромбоэмболии у больных СН и ФП | Доказательства (класс) | Согласие (уровень) |
| У больных с риском тромбоэмболии 2 и более назначают оральный антикоагулянт | I | B |
| Новые оральные антикоагулянты не назначают больным с искусственными клапанами, больным с митральным стенозом | II | B |
| У больных с неизвестной давностью или с давностью ФП более 48 ч перед кардиоверсией в течение более 3 недель проводится пероральная терапия терапевтическими дозами антикоагулянт | I | B |
| У больных с жизнеопасной аритмией под контролем ЧП ЭхоКГ проводится терапия гепарином или низкомолекулярным гепарином | I | C |
| У больных на терапии дезагрегантами кардиоверсия не проводится и только после ее завершения назначается терапия антикоагулянтом и после чего она может производиться | III | C |
| У больных с СН и неклапанной этиологией ФП предпочтительнее использовать вместо варфарина новые оральные антикоагулянты | IIa | B |
| Шкалы риска тромбоза и кровотечения используют для оценки величины риска и у больных с СН и ФП | I | B |
Анемия у больных хронической сердечной недостаточностью регистрируется у 10-20% (6). Критерии ее диагностики: у мужчин - Hb<13 г %, у женщин<12 г %. Причинами ее являются увеличение ОЦК; подавление функции костного мозга, дефицит железа, повышение активности иммунной системы под влиянием иАПФ, почечная недостаточность. Лечение: 1) в/в препараты железа, 2) эритропоэтин (данные противоречивы). Данные последнего мета-анализа (23) , включившем в основную группу 509 больных на терапии железом и в контрольную - 342 больных. Терапия осуществлялась с помощью внутривенного введения препаратов железа. Результаты: в основной группе снизился риск комбинированной конечной точки (общая летальность или кардиоваскулярная госпитализация, а также другой к.к.т. - кардиоваскулярная летальность или госпитализация в связи с ухудшением сердечной недостаточности (P<0,0001).
У части больных лекарственная терапия со временем становится малоэффективной и требует другого лечения. Терапия рефрактерной формы сердечной недостаточности:
ЛИТЕРАТУРА
Комментарии
ПРАКТИКА ПЕДИАТРА



