Профилактика кардиальных осложнений у больных с ишемической болезнью сердца при сосудистых операциях: возможности никорандила
Статьи
Ю.А. Кудаев1, Т.Ф. Субботина2, Н.Л. Лоховинина1, М.З. Алугишвили1, И.Т. Абесадзе1, И.В. Титенков1, А.А. Жлоба2, М.А. Чернявский1, А.В. Панов1
1ФГБУ «Национальный медицинский исследовательский центр им. В.А. Алмазова» Минздрава России, Санкт-Петербург, Россия;
2ФГБОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Резюме
Цель исследования. Оценить влияние никорандила на концентрацию оксидов азота, уровни участников и модуляторов NO-синтазных реакций и взаимосвязанных участников трансметилирования в плазме крови через 2 ч после его приема, а также исходы артериальных реконструкций в раннем послеоперационном периоде у пациентов с ишемической болезнью сердца (ИБС).
Материал и методы. В исследование включены 60 больных со стенокардией напряжения II-III класса, направленных на плановое аутовенозное бедренно-подколенное шунтирование (БПШ). Все пациенты после компьютерной рандомизации были разделены на две группы: группа контроля (n=30) и основная группа (п=30). В последней группе дополнительно к базовой терапии за 2 ч до операции назначали никорандил (Кординик, компания ПИК-ФАРМА) в максимальной разовой дозе 20 мг. До и через 2 ч после приема препарата, непосредственно перед премедикацией осуществляли забор крови для определения концентрации сумма окислов азота, уровней участников и модуляторов NO-синтазных реакций (аргинина и цитруллина) и взаимосвязанных участников трансметилирования (общего гомоцистеина и метионина). В послеоперационном периоде оценивали частоту и структуру сердечно-сосудистых осложнений (CCO).
Результаты. Пациенты обеих групп были сопоставимы по клиническим характеристикам, проводимой медикаментозной терапии и продолжительности артериальной реконструкции. При оценке метаболических показателей через 2 ч после приема никорандила достоверного изменения концентрации суммы окислов азота не зарегистрировано. Отмечено повышение содержания субстрата NO-синтазных реакций — аргинина (Арг) (р=0,018), уменьшение содержания продукта этих реакций — цитруллина (Цит) (р=0,038) и убедительное увеличение соотношения Арг/Цит (р=0,00037). Уровни общего гомоцистеина, метионина и их соотношения достоверно не изменялись. Выявлено статистически значимое межгрупповое различие при анализе случаев повреждения миокарда. Так, в контрольной группе в 5 случаях уровень высокочувствительного сердечного тропонина через 24 ч после операции превысил пороговые значения, что свидетельствовало об интраоперационном повреждении миокарда. В группе никорандила динамика повышения отсутствовала (16,7% против 0%, р=0,002). В основной группе пациентов, получавших никорандил, отмечено статистически значимое снижение общей частоты ССО (повреждение и инфаркт миокарда, нарушения ритма, сердечная недостаточность, острое нарушение мозгового кровообращения) в раннем послеоперационном периоде (6,7% против 33,3%, р=0,001).
Вывод. Отсутствие достоверного изменения концентрации суммы окислов азота после приема никорандила свидетельствует о его прямом воздействии без опосредованного превращения в оксид азота. Прямое влияние препарата на К-транспортер приводит к активации внутриклеточных метаболических функций, включая эффект увеличения соотношения Арг/Цит, вероятно, за счет ресинтеза Арг из Цит в тканях, что способствует увеличению пула Арг и, соответственно, увеличению биодоступности субстрата NO-синтазных реакций. Применение никорандила (Кординик, компания ПИК-ФАРМА) перед сосудистыми вмешательствами способствует снижению частоты ССО в раннем послеоперационном периоде.
Ключевые слова: никорандил, ишемическая болезнь сердца, сосудистая операция, участники NO-синтазных реакций.
Источник: Профилактика кардиальных осложнений у больных с ишемической болезнью сердца при сосудистых операциях: возможности никорандила / Ю. А. Кудаев, Т. Ф. Субботина, Н. Л. Лоховинина [и др.] // Кардиология и сердечно-сосудистая хирургия. – 2022. – Т. 15. – № 4. – С. 402-411. – DOI 10.17116/kardio202215041402. – EDN OXSBIB.
Prevention of cardiac complications in patients with coronary artery disease undergoing vascular surgery: possibilities of nicorandil
YU.A. Kudaev1, T.F. Subbotina2, N.L. Lokhovinina1, M.Z. Alugishvili1, I.T. Abesadze1, I.V. Titenkov1, A.A. Zhloba2, M.A. Chernyavsky1, A.V. Panov1
1Almazov National Medical Research Center, St. Petersburg, Russia;
2Pavlov First St. Petersburg State Medical University, St. Petersburg, Russia
Abstract
Objective. To assess the effect of nicorandil on serum concentration of nitrogen oxides, participants and modulators of NO-synthase reactions and interrelated participants of transmethylation in 2 hours after administration, as well as to analyze early postoperative outcomes of arterial reconstructions in patients with coronary artery disease (CAD).
Material and methods. The study included 60 patients with class II-III angina pectoris who underwent femoropopliteal bypass surgery. All patients were randomized into two equal groups: control group (n=30) and main group (n=30). In the last group, nicorandil (Cordinic, PIQ-Pharma) was prescribed 2 hours before surgery in addition to basic therapy with a maximum single dose of 20 mg. Blood samples were taken before and 2 hours after taking pills, as well as immediately before sedation. The main goal was to determine the concentration of nitrogen oxides, participants and modulators of NO-synthase reactions (arginine and citrulline) and interrelated participants in transmethylation (total homocysteine and methionine). We assessed the incidence and structure of cardiovascular complications (CVC) in postoperative period.
Results. Both groups were comparable by clinical characteristics, drug therapy and duration of arterial reconstruction. There were no significant changes in serum concentration of total nitrogen oxides according to metabolic analysis in 2 hours after nicorandil taking. We observed an increase in the content of arginine (Arg) as a substrate of NO-synthase reactions (p=0.018), decrease of citrulline (Cyt) as a product of these reactions (p=0.038) and increase of Arg/Cyt ratio (p=0.00037). The levels of total homocysteine, methionine and their ratios were not significantly changed. We found significant between-group difference in myocardial injury. In the control group, high-sensitivity cardiac troponin was increased in 24 hours after surgery in 5 cases that indicated intraoperative myocardial damage. At the same time, no increase of troponin was observed in the main group (16.7% vs. 0%, p=0.002). Incidence of early postoperative CVC (myocardial infarction and injury, rhythm disturbances, heart failure, stroke) was significantly less in the main group (6.7% vs. 33.3%, p=0.001).
Conclusion. No significant changes in serum concentration of nitrogen oxides after taking nicorandil indicate its direct exposure without indirect conversion to nitric oxide. Direct effect on K-transporter activates intracellular metabolic functions including increase of Arg/Cyt ratio. Probably, it happens due to resynthesis of Arg from Cyt in tissues that contributes to increase of Arg pool and, accordingly, bioavailability of substrate for NO-synthase reactions. Application of nicorandil (Cordinic, PIQ-Pharma) before vascular interventions reduces the incidence of CVC in early postoperative period.
Keywords: nicorandil, coronary artery disease, vascular surgery, participants of NO-synthase reactions.
Введение
В 2018 г. в Российской Федерации были выполнены 130109 сосудистых операций, при этом рост количества артериальных реконструкций за последние пять лет составил 8,4% [1]. Хирургические вмешательства на аорте и периферических артериях согласно рекомендациям Европейского общества кардиологов (ESC) относятся к внесердечным операциям среднего и высокого кардиального риска, при которых риск инфаркта миокарда (ИМ) либо смерти от сердечно-сосудистой патологии в течение 30 дней после операции вне зависимости от наличия сопутствующей патологии составляет 1—5% и более 5%, соответственно [2]. Частота фатальных исходов вследствие сердечно-сосудистых причин при внекардиальных вмешательствах достигает 1,5%, а кардиальных осложнений — 3,5% [3]. Основным периоперационным осложнением является ИМ, летальность при котором составляет 15—25% [4]. Отмечено, что у 20% пациентов после операции верифицируется повреждение миокарда, определяемое как диагностически значимое повышение уровня тропонина [5]. Несомненно, сосудистые операции — триггер кардиальных событий, так как приводят к нарушению гемодинамики, гиперкоагуляции, воспалению, симпатической стимуляции и кровотечениям, что предрасполагает к ишемическому повреждению кардиомиоцитов [6]. Ишемия миокарда является ведущей причиной 30-дневной летальности после сосудистых вмешательств, а ее диагностика затруднительна на фоне применения анальгетиков и отсутствия систематического скрининга маркеров повреждения кардиомиоцитов [5, 7]. В связи с этим крайне актуальной представляется проблема своевременной диагностики повреждения миокарда после внекариальных хирургических вмешательств (myocardial injury after non-cardiac surgery, MINS), которое объединяет ИМ и ишемическое повреждение миокарда, не подпадающее под определение ИМ [8]. Таким образом, MINS — это обусловленное ишемией повреждение кардиомиоцитов, возникающее во время или в течение 30 дней после операции и способное привести к некрозу миокарда, что имеет крайне важное прогностическое значение [7]. Исключением из MINS является периоперационное повреждение миокарда, обусловленное документально подтвержденной неишемической причиной (пароксизм фибрилляции предсердий, сепсис, тромбоэмболия легочной артерии). MINS следует считать любое повышение значения тропонина выше верхнего референтного предела 99 процентиля [9].
Данные New York University School of Medicine показали, что у 48,2% больных в возрасте старше 45 лет, перенесших некардиальные операции, встречаются множественные сердечно-сосудистые факторы риска, такие как гипертоническая болезнь (ГБ), гиперхолестеринемия, ожирение, сахарный диабет (СД), хроническая болезнь почек, а у 25% имеется анамнез сосудистого заболевания атеросклеротического генеза, что значительно повышает риск послеоперационных кардиальных осложнений [10]. Следует учитывать, что большая часть оперируемых пациентов страдает мультифокальным атеросклерозом. Так, при гемодинамически значимых стенозах каротидных артерий вероятность ИБС составляет 39—61%, а у пациентов с поражением артерий нижних конечностей частота сочетанного поражения коронарного русла достигает 70% [11]. Установлено, что у больных с ИБС после сосудистых реконструкций частота кардиальных событий возрастает с 3 до 8,5% [12].
Распространенность ИБС и факторов риска атеросклеротических заболеваний сердечно-сосудистой системы среди населения РФ, увеличение доли лиц пожилого возраста определяют профилактику кардиальных осложнений при сосудистых операциях как чрезвычайно актуальную задачу. Тем более, что превентивная реваскуляризация миокарда не улучшает исходы плановых артериальных реконструкций [13]. Современным трендом снижения риска кардиальных событий при сосудистых операциях являются изучение и разработка медикаментозных способов их профилактики.
Особое внимание привлекает применение в предоперационном периоде лекарственных средств с непосредственным влиянием на метаболические процессы в кардиомиоцитах и моделирующих феномен ишемического прекондиционирования. Одним из их представителей является никорандил, обладающий двойным механизмом действия. Он приводит к вазодилатации и снижению постнагрузки путем активации открытия АТФ-зависимых калиевых каналов, вызывая гиперполяризацию мембран гладкомышечных клеток (ГМК) сосудистой стенки и уменьшение поступления Са2+ внутрь клетки. Моделирование феномена ишемического прекондиционирования происходит за счет активации АТФ-зависимых калиевых каналов митохондрий. Никорандил способствует уменьшению и преднагрузки за счет наличия в составе нитратной группы, обуславливающей нитратоподобный эффект посредством повышения уровня внутриклеточного циклического гуанозинмонофосфата и расслабления ГМК, особенно венозной системы [14].
Известно, что на образование оксида азота влияет уровень субстрата NO-синтаз — аргинина (Арг), биосинтез которого осуществляется из цитруллина (Цит) под действием аргининсукцинатсинтазы и аргининсукцинатлиазы [15]. Соотношение субстрата Арг и продукта синтазных реакций Цит при применении никорандила до настоящего времени не изучено. Оценка влияния фармакотерапии на эти важнейшие метаболические функции является основным направлением изучения действия никорандила на внутриклеточный метаболизм в нашем исследовании. Поскольку от уровня общего гомоцистеина (оГци) зависит биодоступность окислов азота с одной стороны, а с другой никорандил определенно влияет на вазомоторную функцию, изучение суммы окислов азота и изменений в соотношениях участников указанных реакций представляет весомый интерес. В связи с влиянием препарата на трансмембранный транспорт важным моментом является изучение перераспределения гомоцистеина (Гци) между плазмой крови и клетками. Известно, что Гци способствует ослаблению эндотелий-зависимой релаксации сосудов. В свою очередь, Гци в клетках находится в форме S-аденозилгомоцистеина (АдоГци), который при транспорте во внеклеточную среду переходит в свободный Гци, образующий смешанные дисульфиды как с белковыми тиоловыми остатками, так и с другими аминотиолами плазмы крови [16]. Гци плазмы в свободном состоянии и определяемый в виде различных дисульфидов суммарно обозначается как оГци [16]. АдоГци оказывает ингибирующее действие на процессы трансметилирования, т.е. переноса метильной группы аминокислоты метионина (Мет) к различным внутриклеточным субстратам, включая белки и нуклеиновые кислоты, тем самым оказывая влияние на эпигенетические процессы регуляции метаболизма и стабилизацию генома. Таким образом, от соотношения Мет/Гци напрямую зависят функциональное состояние клеток и их способность к репарации. Их влияние на эндотелий-зависимую релаксацию при назначении никорандила также остается неизученным.
Цель исследования — оценка влияния никорандила на концентрацию окислов азота, уровни участников и модуляторов NO-синтазных реакций и взаимосвязанных участников трансметилирования в плазме крови через 2 ч после его приема, а также анализ исходов артериальных реконструкций в раннем послеоперационном периоде у пациентов с ИБС.
Материал и методы
В исследование включали пациентов со стенокардией напряжения II-III функционального класса (ФК), направленных в клинику сосудистой хирургии ФГБУ «НМИЦ им. В.А. Алмазова» для реваскуляризации нижних конечностей. Отобраны 60 больных с показаниями к аутовенозному бедренно-подколенному шунтированию (БПШ). Средний возраст пациентов составил 64±8 лет, всего включено 46 мужчин и 14 женщин. Критериями исключения являлись острый ИМ, декомпенсация хронической сердечной недостаточности, брадикардия с частотой сердечных сокращений (ЧСС) менее 50 уд/мин, систолическое АД ниже 100 мм рт.ст., атриовентрикулярная блокада II и III ст., анемия и повышенная чувствительность к никорандилу.
Все больные после компьютерной рандомизации были разделены на две группы: 1-я группа (основная) с назначением никорандила и 2-я группа (контроля) стандартной терапии. В 1-й группе (п=30) к медикаментозной терапии, получаемой больными на госпитальном этапе, назначали никорандил (Кординик, компания ПИК-ФАРМА) в разовой дозе 20 мг за 2 ч до операции. В контрольной группе (n=30) никорандил в предоперационном периоде не использовали.
Перед операцией проводили лабораторное и клинико-инструментальное обследование, включавшее клинический и биохимический анализы крови, общий анализ мочи, электрокардиографию (ЭКГ) и эхокардиографию (ЭхоКГ). До и через 2 ч после приема никорандила, непосредственно перед премедикацией осуществляли забор крови для определения концентрации окислов азота, уровней участников и модуляторов NO-синтазных реакций (Арг и Цит) и взаимосвязанных участников трансметилирования (оГци и Мет). С целью оценки метаболических показателей использован современный энзиматический способ определения суммы окислов азота (NO2-/NO3-) с использованием нитратредуктазы. Концентрации окислов азота предварительно анализировали в двух группах здоровых лиц и данные референтного интервала представляли в виде медианы, 5 и 95 перцентилей [17]. Определение оГци осуществляли с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) [18]. Определение аминокислот Мет, Арг и Цит осуществляли в рамках единой процедуры ВЭЖХ анализа. До и через 24 ч после операции контролировали уровень тропонина с помощью анализатора Architect i2000 (Abbott Laboratories, США). Верхняя граница нормы (ВГН) тропонина составляла 0,034 нг/ мл. Периоперационным повреждением миокарда, согласно четвертому универсальному определению ИМ, считали повышение уровня тропонина в динамике, превышающее 99 перцентиль ВГН, при отсутствии болевого синдрома в грудной клетке, ишемических изменений на ЭКГ и новых зон асинергии по данным ЭхоКГ. ФК стенокардии оценивали на основании классификации Канадского сердечно-сосудистого общества.
Всем больным выполнено аутовенозное БПШ. Под общей анестезией разрезами в нижней и верхней третях бедра выделяли подколенную (ПКА) и общую бедренную артерию (ОБА), соответственно. Из отдельных кожных разрезов выделяли ствол большой подкожной вены. Формировали дистальный анастомоз между аутовеной и ПКА, проксимальный анастомоз между аутовеной и ОБА. После пуска кровотока и определения отчетливой пульсации зоны реконструкции выполняли послойный шов ран в местах артериальных доступов с наложением асептической повязки. В послеоперационном периоде оценивали частоту и структуру ССО, уровень тропонина. Учитывали наиболее неблагоприятные ССО, такие как повреждение миокарда, ИМ, декомпенсация или развитие сердечной недостаточности, нарушения ритма, острое нарушение мозгового кровообращения (ОНМК). Период наблюдения в раннем послеоперационном периоде составил 9,7±2,5 сут.
Полученные первичные данные подвергали математической обработке с использованием статистического пакета Statistica 10.0 (StatSoft Inc., США). Степень соответствия распределения данных нормальному распределению оценивали с помощью критериев Шапиро—Уилка и Колмогорова-Смирнова. Данные представлены в виде медианы и межквартильного интервала, если не указано иное. Статистическая обработка результатов проведена с использованием параметрических методов после теста на характер распределения выборки. В случае несоответствия вариант нормальному распределению использовали непараметрические методы обработки данных. Для оценки межгрупповых различий использован непараметрический критерий Манна-Уитни для независимых и парный критерий Вилкоксона для зависимых выборок. Корреляционный анализ проведен с применением критерия Спирмена. Критический уровень достоверности нулевой статистической гипотезы принимали равным 0,05.
Результаты
Среди госпитализированных для реваскуляризации нижних конечностей мужчины составили 76,7%, женщины — 23,3%. Возраст пациентов варьировал от 43 до 89 лет. Большинство больных имели избыточный вес или ожирение (75%), страдали ГБ (90%). Частота СД составила 26,7%. ОНМК перенесли 14 (23,3%) пациентов. У 10 (16,7%) больных ранее выполнялись операции на брахиоцефальных артериях (6 (20%) в основной группе и 4 (13,3%) в контрольной). Мультифокальный атеросклероз с вовлечением трех сосудистых бассейнов (коронарные, каротидные артерии и артерии нижних конечностей) верифицирован у 9 (30%) пациентов основной группы и 10 (33,3%) больных группы контроля. на догоспитальном этапе целевой уровень холестерина липопротеинов низкой плотности (ХС ЛПНП) (менее 1,4 ммоль/л) был достигнут в 7 (11,7%) случаях. Таким образом, у всех больных с заболеваниями артерий нижних конечностей (ЗАНК), направленных для хирургического лечения, выявляли факторы риска в разных сочетаниях.
Пациенты обеих группы были сопоставимы по основным клиническим характеристикам, характеру и длительности операций (табл. 1).
Таблица 1.
Клиническая характеристика и периоперационные параметры пациентов основной и контрольной групп
Table 1.
Clinical characteristics and perioperative features in both groups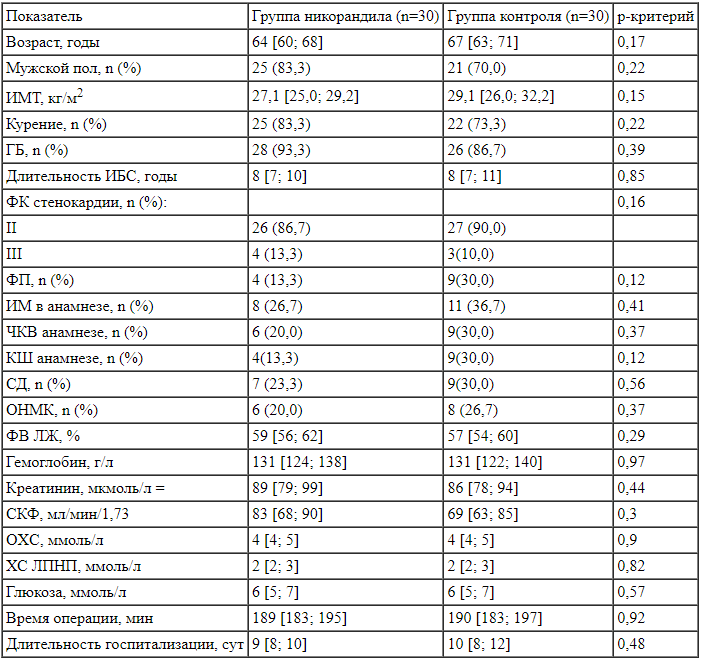 Примечание. ИМТ — индекс массы тела, ЧКВ — чрескожное коронарное вмешательство, КШ — коронарное шунтирование, ФВ ЛЖ — фракция выброса левого желудочка, СКФ — скорость клубочковой фильтрации, ОХС — общий холестерин.
Примечание. ИМТ — индекс массы тела, ЧКВ — чрескожное коронарное вмешательство, КШ — коронарное шунтирование, ФВ ЛЖ — фракция выброса левого желудочка, СКФ — скорость клубочковой фильтрации, ОХС — общий холестерин.
При поступлении в группе никорандила у 86,7% пациентов присутствовала клиника стенокардии II ФК, у 13,3% — III ФК. В контрольной группе эти значения составили 90 и 10% соответственно. Фибрилляцией предсердий (ФП) страдали 4 (13,3%) пациента группы никорандила и 9 (30%) больных группы контроля (p=0,12). ИМ перенесли 8 (26,7%) и 11 (36,7%) больных, соответственно (p=0,41). Реваскуляризация миокарда, не связанная с предстоящей сосудистой реконструкцией, выполнена 10 (33,3%) пациентам основной группы и 18 (60%) больным группы контроля. В группе никорандила в 6 (20%) случаях проведено ЧКВ, у 4 (13,3%) больных — КШ. В контрольной группе аналогичные процедуры выполнены у 9 (30%) и 9 (30%) пациентов, соответственно.
Обе группы также были сопоставимы по характеру медикаментозной терапии в предоперационном периоде (табл. 2).
Таблица 2.
Предоперационная медикаментозная терапия в обеих группах
Table 2.
Preoperative drug therapy in both groups Примечание. АСК — ацетилсалициловая кислота, ББ — бета-адреноблокаторы, БМКК — блокаторы медленных кальциевых каналов, БРА — блокаторы рецепторов ангиотензина, иАПФ — ингибиторы ангиотензинпревращающего фермента.
Примечание. АСК — ацетилсалициловая кислота, ББ — бета-адреноблокаторы, БМКК — блокаторы медленных кальциевых каналов, БРА — блокаторы рецепторов ангиотензина, иАПФ — ингибиторы ангиотензинпревращающего фермента.
Прием никорандила в основной группе в дозе 20 мг за 2 ч до операции хорошо переносился, не зафиксировано случаев выраженной гипотензии. После применения никорандила достоверного изменения концентрации суммы окислов азота не зарегистрировано (табл. 3), что означает прямое воздействие препарата без его опосредованного превращения в оксид азота. При этом уровни тропонина и окислов азота положительно коррелировали по отношению друг к другу, указывая на возможную связь образования окислов азота за счет активации именно индуцибельной NO-синтазы. Эти энзимы активируются закономерно вслед за повреждением тканей, в том числе, сердечной мышцы, вызывая возрастание уровней тропонинов и других маркеров нестабильности мембран клеток.
Как следует из данных табл. 3, уровни оГци, Мет и их соотношения достоверно не изменяются. Наоборот, уровни Арг возрастают, а уровень Цит понижается. Соответственно, их соотношение (Арг/Цит) повышается с еще более убедительной достоверностью в условиях применения никорандила (табл. 3, рис. 1).
Таблица 3.
Метаболические маркеры до и через 2 ч после приема никорандила до хирургического вмешательства
Table 3.
Preoperative metabolic markers before and 2 hours after taking nicorandill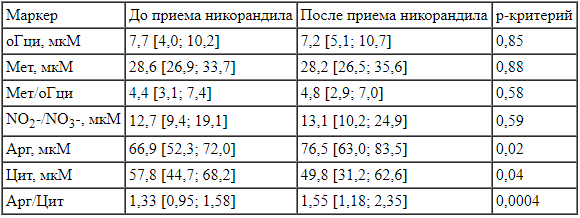 Примечание. Достоверность различий оценивали с помощью теста Вилкоксона для парных наблюдений.
Примечание. Достоверность различий оценивали с помощью теста Вилкоксона для парных наблюдений.
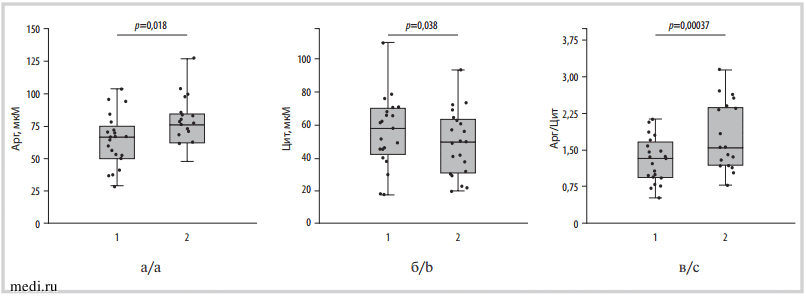 Рис. 1. Уровни участников NO-синтазных реакций аргинина (а), цитруллина (б) и их соотношения (в) в плазме крови пациентов до (1) и через 2 ч после (2) приема никорандила.
Рис. 1. Уровни участников NO-синтазных реакций аргинина (а), цитруллина (б) и их соотношения (в) в плазме крови пациентов до (1) и через 2 ч после (2) приема никорандила.
Fig 1. Serum levels of NO-synthase reaction participants — arginine (a), citrulline (b) and their ratio (c) prior (1) and 2 hours after taking nicorandil (2).
При этом содержание Арг или Цит не коррелирует с экскреторной функцией почек (рис. 2, а, б), тогда как их соотношение достоверно зависит от скорости клубочковой фильтрации (СКФ) только до применения никорандила (рис. 2, в), а после его приема соотношение Арг/Цит теряет зависимость от СКФ.
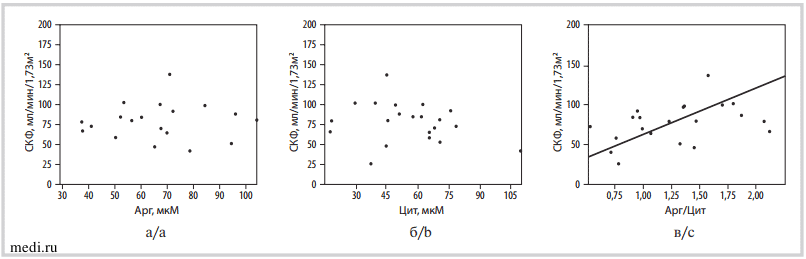 Рис. 2. Разброс данных в зависимости от скорости клубочковой фильтрации: аргинин (а) — корреляция недостоверна, цитруллин (б) — корреляция недостоверна, соотношение Арг/Цит (в) — RS=0,482, р=0,046.
Рис. 2. Разброс данных в зависимости от скорости клубочковой фильтрации: аргинин (а) — корреляция недостоверна, цитруллин (б) — корреляция недостоверна, соотношение Арг/Цит (в) — RS=0,482, р=0,046.
Fig 2. Scatter plot depending on glomerular filtration rate: arginine (a) — correlation is not significant, citrulline (b) — correlation is not significant, Arg/Cit ratio (c) — RS=0.482, p=0.046.
Влияние никорандила на уровни суммы окислов азота, высвобождающихся за счет NO-синтазных реакций, менее заметно, так как механизм действия препарата реализуется на уровне клеток за счет прямого воздействия на К-транспортер, что приводит к активации внутриклеточных метаболических функций, включая показанный нами эффект увеличения соотношения Арг/Цит, по-видимому, за счет ресинтеза Арг из Цит в тканях. Это способствует увеличению пула Арг и, соответственно, увеличению биодоступности субстрата NO-синтазных реакций. Другая возможная причина увеличения уровня Арг может заключаться в ингибировании внутриклеточных аргиназ второго типа, однако действия никорандила в качестве ингибитора аргиназ в литературе не описано. Поэтому его влияние на внутриклеточные метаболические процессы, включая реакции ресинтеза Арг из Цит, представляется более вероятным.
Всем больным выполнили БПШ. Длительность операции в среднем составила 189 мин в группе никорандила и 190 мин в контрольной группе (р=0,92). Осложнения в раннем послеоперационном периоде выявлены у 12 (20%) пациентов. Летальных исходов, ОНМК и ИМ в обеих группах не зарегистрировано. Выявлено статистически значимое межгрупповое различие при анализе случаев повреждения миокарда. Так, в контрольной группе в 5 случаях уровень тропонина через 24 ч после операции превысил пороговые значения, что свидетельствовало об интраоперационном повреждении миокарда. В группе никорандила динамика повышения отсутствовала (16,7% против 0%, р=0,002). Статистически значимого различия средних значений тропонина после операции в обеих группах получено не было. Нарушения ритма зарегистрированы у 2 пациентов основной группы (пароксизмы ФП) и у 3 больных в контрольной группе (пароксизмы ФП в двух случаях и пароксизм неустойчивой желудочковой тахикардии в одном случае) (6,7% против 10%, р=0,64). Явления декомпенсации сердечной недостаточности в раннем послеоперационном периоде выявлены у 2 больных контрольной группы при отсутствии таковых в группе никорандила (6,7% против 0%, р=0,15). В основной группе отмечено статистически значимое снижение общей частоты ССО (повреждение миокарда, ИМ, нарушения ритма, сердечная недостаточность, ОНМК) в раннем послеоперационном периоде (6,7% против 33,3%, р=0,001) (табл. 4).
Таблица 4.
Госпитальные послеоперационные осложнения
Table 4.
In-hospital postoperative complications Обсуждение
Обсуждение
Сосудистые операции представляют особый интерес, так как сопровождаются крайне высоким риском ССО. Известно, что у пациентов с атеросклерозом периферических артерий после реваскуляризации пораженного бассейна 30-дневная частота неблагоприятных кардиальных событий достигает 21% [19]. Таким образом, расчетный показатель случаев повреждения миокарда в РФ при операциях на периферических артериях превышает 27 000 ежегодно. Это обуславливает актуальность проблемы профилактики ССО при сосудистых вмешательствах.
Предоперационная инвазивная коронарная ангиография (КАГ) не рекомендуется перед сосудистыми операциями и может рассматриваться лишь у пациентов с высоким риском ИБС по данным стресс-теста, но только в том случае, если ее результаты повлияют на тактику лечения [20]. Тем более, что рутинная реваскуляризация миокарда перед плановым вмешательством не улучшает периоперационные исходы и не должна выполняться с превентивной целью за исключением случаев тяжелого многососудистого поражения или поражения ствола левой коронарной артерии [13]. Реваскуляризация миокарда оправдана только при наличии показаний к ее проведению вне зависимости от факта планируемой сосудистой операции.
Учитывая этот факт, медикаментозная терапия — главный инструмент снижения периоперационного сердечно-сосудистого риска. Согласно рекомендациям ESC перед хирургическим вмешательством все пациенты с заболеваниями периферических артерий должны получать статины, бета-адреноблокаторы, блокаторы ренин-ангиотензиновой системы при наличии высокого риска, а также контролируемую антитромботическую терапию при необходимости.
Гиполипидемическая терапия, по данным ряда исследований, приводит к снижению периоперационного кардиального риска. При ретроспективном анализе более 200 000 пациентов, перенесших внекардиальные операции, назначение гиполипидемической терапии во время госпитализации было ассоциировано с более низкой летальностью (2,1% против 3,1%) [21]. Подтверждение этому получено и в наблюдательном исследовании Noncardiac Surgery Patients Cohort Evaluation, а также при анализе когорты из 180 478 пациентов (1,8% против 2,3%) [22, 23]. Кроме того, среди больных, которым выполняли реваскуляризацию нижних конечностей, частота сохранения конечности через 1 год была выше у тех, кто получал статины [24]. Эксперты Американской ассоциации кардиологов (AHA) считают предоперационную терапию статинами целесообразной у пациентов высокого риска, страдающих атеросклеротическим сердечно-сосудистым заболеванием или СД. По их мнению, лечение статинами должно быть продолжено или инициировано перед планируемыми вне-сердечными сосудистыми операциями [13].
Применение бета-адреноблокаторов способствует пролонгации диастолы и уменьшению потребления кислорода кардиомиоцитами вследствие уменьшения ЧСС. Снижение числа периоперационных кардиальных событий на фоне использования пролонгированного метопролола сукцината (5,8% против 6,9%; p=0,04) отмечено в рандомизированном исследовании Perioperative Ischemic Evaluation trial, включавшем 8351 пациента [25]. Считается, что длительный период приема бета-адреноблокаторов до операции с титрацией дозы по ЧСС является более полезным. В наблюдательном исследовании 940 пациентов, которым проводили артериальные реконструкции, отмечено снижение частоты комбинированной конечной точки, включавшей повреждение миокарда, ИМ, инсульт и смерть, в том случае, когда прием бета-адреноблокаторов начинали более чем за 1 нед до предстоящей операции (15% против 27%, p<001) [26]. Эксперты ESC рекомендуют больным, принимающим бета-адреноблокаторы, продолжить лечение в периоперационном периоде при отсутствии брадикардии или гипотензии. Инициация терапии бета-адреноблокаторами перед операцией может быть оправдана у пациентов с ИБС, множественными факторами риска или высоким риском ССО. При этом начинать прием препаратов необходимо не позднее чем за 1 нед до предстоящей операции [2]. Кроме того, целесообразно использовать кардиоселективные бета-адреноблокаторы без внутренней симпатомиметической активности с длительным периодом полувыведения [27].
Весьма дискутабельным остается вопрос эффективности и безопасности применения иАПФ или АРА при вне-кардиальных вмешательствах. Несмотря на то, что они обладают органопротективными свойствами, их применение не ведет к снижению смертности и частоты кардиальных событий после сосудистых операций у больных высокого риска, но связано с риском тяжелой гипотензии во время анестезиологического пособия [2]. Так, при анализе рандомизированных исследований продолжение приема иАПФ или АРА ассоциировалось с повышением частоты интраоперационной гипотензии (57,8% против 23,5) [28, 29]. В крупном международном проспективном когортном исследовании, включавшем 14 687 пациентов, предоперационное прекращение приема иАПФ или АРА приводило к снижению частоты интраоперационной гипотензии (23,3% против 28,6%) и комбинированной конечной точки (повреждение миокарда, инсульт и смерть) через 30 дней после операции (12,0% против 12,9%) [30]. Эксперты AHA рекомендуют не прекращать терапию блокаторами ренин-ангиотензиновой системы в предоперационном периоде, а в случае показаний к их отмене возобновлять прием как можно раньше [13]. Эксперты ESC рекомендуют временно прекратить прием иАПФ или АРА до вмешательства при назначении их по поводу артериальной гипертензии и продолжить прием у пациентов с сердечной недостаточностью или систолической дисфункцией левого желудочка [2].
Ацетилсалициловая кислота является обратимым ингибитором циклооксигеназы-1, снижающим агрегацию тромбоцитов, уменьшая выработку тромбоксана А2. С одной стороны, это способствует снижению риска тромботических осложнений, а с другой повышает риск кровотечений. Целесообразность рутинного применения аспирина перед внекардиальными операциями изучена в исследовании Perioperative Ischemic Evaluation-2, включавшем 10 010 пациентов. Частота ИМ и летальность не отличались в группе с аспирином и без него (7,0% против 7,1%, p=0,92), но наблюдали повышение числа больших кровотечений (4,6% против 3,8%, p=0,04) [31]. Рутинное применение аспирина при внесердечных операциях не рекомендуется, хотя может назначаться пациентам, у которых ишемический риск превышает риск кровотечения.
Никорандил — нитратное производное никотинамида, обладающее феноменом ишемического прекондиционирования, которое позволяет повышать устойчивость миокарда к повторным эпизодам гипоксии, приводя к снижению числа кардиальных событий в периоперацинном периоде [32].
Применение никорандила в дозе 20 мг за 2 ч до артериальной реконструкции у больных с ИБС в ходе нашего исследования позволило улучшить исходы открытых сосудистых операций. Отсутствовали нежелательные явления при приеме препарата, отмечено снижение числа госпитальных ССО (рис. 3).
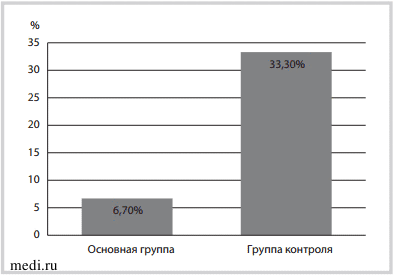 Рис. 3. Частота кардиальных осложнений при открытой артериальной реконструкции в обеих группах.
Рис. 3. Частота кардиальных осложнений при открытой артериальной реконструкции в обеих группах.
Fig. 3. Incidence of cardiac complications in open arterial reconstruction in both groups.
Согласно полученным данным устойчивость к нарушениям гемодинамики за счет влияния никорандила может в значительной мере объясняться показанным нами увеличением содержания субстрата NO-синтазных реакций — аргинина. Так как это происходит при одновременном уменьшении содержания продукта этих реакций (цитруллина) и убедительном увеличении соотношения Арг/Цит, изменение соотношений следует объяснить, скорее всего, ресинтезом аргинина из цитруллина (табл. 3, рис. 1).
В данной работе получено подтверждение широко известного наблюдения о том, что с нарушением экскреторной функции почек при сердечно-сосудистых заболеваниях связано повышение уровня оГци. На фоне приема никорандила экскреторная функция почек улучшается, по-видимому, за счет улучшения местного кровотока, что прослеживается в усилении независимости корреляции соотношения Арг/Цит и скорости клубочковой фильтрации (рис. 2).
Все более широкое применение никорандила в настоящее время наблюдается при коронарных вмешательствах у больных с ИБС. По данным метаанализа 24 исследований с участием 2965 пациентов установлено, что использование никорандила при чрескожных коронарных вмешательствах у больных с ИМ снижало частоту реперфузионного синдрома и неблагоприятных ССО [33]. Внутривенное введение препарата пациентам с ИМ с подъемом сегмента ST (ИМпST) во время ЧКВ эффективно уменьшало зону ИМ без увеличения частоты реперфузионных аритмий и эпизодов гипотензии [34]. Кроме того, дальнейший прием больными с ИМ, перенесшими первичное ЧКВ, никорандила в течение 6 мес приводил к улучшению систолической функции левого желудочка и повышению толерантности к физическим нагрузкам [35]. Интракоронарное введение 2 мг никорандила при ЧКВ у больных с ИМпST приводило к значительному улучшению перфузии миокарда и снижению частоты феномена no-reflow [36]. Назначение препарата после планового ЧКВ, по данным метаанализа 14 рандомизированных клинических исследований, включавших 1864 пациента, способствовало улучшению сократительной функции миокарда и снижению количества ССО [37].
Таким образом, результаты нашего исследования подтверждают эффективность назначения никорандила перед хирургическими вмешательствами, связанными с ишемией миокарда, который в дополнение к известным механизмам воздействия на клеточный метаболизм вызывает усиление использования Цит для ресинтеза Арг с увеличением содержания субстрата NO-синтаз (аргинина) и, соответственно, соотношения Арг/Цит. Этот механизм поддержки функций NO-синтаз открывает новые перспективы для изучения препарата и новый взгляд на возможности его использования в повседневной клинической практике.
Вывод
Периоперационная медикаментозная терапия должна назначаться с учетом специфического риска для пациента. Использование никорандила (Кординик, компания ПИК-ФАРМА) в дозе 20 мг за 2 ч до реваскуляризации нижних конечностей у больных с ИБС снижает количество неблагоприятных кардиальных осложнений. Учитывая непрерывный рост числа операций сосудистого профиля и высокую частоту ССО, особенно у пациентов с мультифокальным атеросклерозом, соблюдение существующих и разработка новых способов предупреждения сердечно-сосудистых событий при данных вмешательствах имеет важное социально-экономическое значение.
ЛИТЕРАТУРА/REFERENCES
1. Российский статистический ежегодник. М. 2019;708. Russian statistical yearbook. M. 2019;708. (In Russ.).
2. Kristensen SD, Knuuti J, Saraste A, et al. The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesthesiology (ESA). Eur Heart J. 2014;35(35):2383-2431.
3. Poldermans D, Bax JJ, Boersma E, et al. Guidelines for preoperative cardiac risk assessment and perioperative cardiac management in non-cardiac surgery. The Task Force for Preoperative Cardiac Risk Assessment and Perioperative Cardiac Management in Non-cardiac Surgery of the European Society of Cardiology (ESC) and endorsed by the European Society of Anaesthesiology (ESA). European Heart Journal. 2009;30(22):2769-2812.
4. Devereaux PJ, Goldman L, Cook DJ, et al. Perioperative cardiac events in patients undergoing noncardiac surgery: a review of the magnitude of the problem, the pathophysiology of the events and methods to estimate and communicate risk. CMAJ. 2005;173(6):627-634.
5. Devereaux PJ, Biccard BM, Sigamani A, et al. Writing Committee for the VISION Study Investigators. Association of postoperative high-sensitivity troponin levels with myocardial injury and 30day mortality among patients undergoing noncardiac surgery. J Am Med Assoc. 2017;317(16):1642-1651.
6. Devereaux PJ, Sessler DI. Cardiac complications in patients undergoing major noncardiac surgery. N Engl J Med. 2015;373:2258-2269.
7. Botto F, Alonso-Coello P, Chan MTV, et al. Myocardial injury after non-cardiac surgery: a large, international, prospective cohort study establishing diagnostic criteria, characteristics, predictors, and 30-day outcomes. Anesthesiology. 2014;120:564-578.
8. Devereaux PJ, Szczeklik W. Myocardial injury after non-cardiac surgery: diagnosis and management. Eur Heart J. 2020;41(32):3083-3091.
9. Thygesen K, Alpert JS, Jaffe AS, et al. ESC Scientific Document Group. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019;40:237-269.
10. Smilowitz NR, Gupta N, Guo Y, et al. Trends in cardiovascular risk factor and disease prevalence in patients undergoing non-cardiac surgery. Heart. 2018;104(14):1180-1186.
11. Aboyans V, Ricco JB, Bartelink MLE, et al. 2017 ESC guidelines on the diagnosis and treatment of peripheral arterial diseases. European heart journal. 2017;39(9):763-816.
12. Mangano DT. Adverse outcomes after surgery in the year 2001 — a continuing odyssey. Anesthesiology. 1998;88(3):561-564.
13. Fleisher LA, Fleischmann KE, Auerbach AD, et al. 2014 ACC/ AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol. 2014;64(22):77-137.
14. Goldschmidt M, Landzberg BR, Frishman WH. Nicorandil: a potassium channel opening drug for treatment of ischemic heart disease. Clin J Pharmacol. 1996;36:559-572.
15. Жлоба А.А. Роль АДМА в качестве эндогенного ингибитора eNOS и одного из медиаторов развития вазомоторной эндотелиальной дисфункции. Регионарное кровообращение и микроциркуляция. 2007;6(3):4-14.
Zhloba AA. The role of ADMA as an endogenous inhibitor of eNOS and one of the mediators of vasomotor endothelial dysfunction. Regional circulation and microcirculation. 2007;6(3):4-14. (In Russ.).
16. Жлоба А.А., Субботина Т.Ф. Оценка связывания гомоцистеина с фракцией белков плазмы, ассоциированных с ремоделированием сосудистой стенки. Артериальная гипертензия. 2013;19(2):184-188.
Zhloba A.A., Subbotina T.F. evaluation of homocysteine binding with a fraction of serum proteins associated with vascular remodeling. Arterial Hypertension. 2013;19(2):184-188. (In Russ.).
17. Жлоба А.А., Субботина Т.Ф., Алексеевская Е.С. Содержание окислов азота в плазме крови здоровых лиц в зависимости от возраста. Клиническая лабораторная диагностика. 2016;61(11):760-765.
Zhloba AA, Subbotina TF, Alekseevskaya ES. Serum content of nitric oxide in healthy persons depending on age. Russian Clinical Laboratory Diagnostics. 2016;61(11):760-765. (In Russ.).
18. Zhloba AA, Subbotina TF. Homocysteinylation score of high-molecular weight plasma proteins. Amino Acids. 2014;46(4):893-899.
19. Sazgary L, Puelacher C, Lurati Buse G, et al. Incidence of major adverse cardiac events following non-cardiac surgery. Eur Heart J Acute Cardiovasc Care. 2020;10(5):550-558.
20. Schulman-Marcus J, Feldman DN, Rao SV, et al. Characteristics of patients undergoing cardiac catheterization before non-cardiac surgery: a report from the national cardiovascular data registry Cath PCI Registry. JAMA Intern Med. 2016;176(5):611-618.
21. Lindenauer PK, Pekow P, Wang K, et al. Lipid-lowering therapy and in-hospital mortality following major noncardiac surgery. J Am Med Assoc. 2004;291(17):2092-2099.
22. London MJ, Schwartz GG, Hur K, Henderson WG. Association of perioperative statin use with mortality and morbidity after major non-cardiac surgery. JAMA Intern Med. 2017;177(2):231-242.
23. Berwanger O, Le Manach Y, Suzumura EA, et al. VISION Investigators. Association between pre-operative statin use and major cardiovascular complications among patients undergoing non-cardiac surgery: the VISION study. Eur Heart J. 2016;37(2):177-185.
24. Vogel TR, Dombrovskiy VY, Galinanes EL, Kruse RL. Preoperative statins and limb salvage after lower extremity revascularization in the Medicare population. Circ Cardiovasc Interv. 2013;6(6):694-700.
25. Devereaux PJ, Yang H, Yusuf S, et al. POISE Study Group. Effects of extended-release metoprolol succinate in patients under going non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet. 2008;371(9627):1839-1847.
26. Flu WJ, van Kuijk JP, Chonchol M, et al. Timing of pre-operative beta-blocker treatment in vascular surgery patients: influence on postoperative outcome. J Am Coll Cardiol. 2010;56(23):1922-1929.
27. Mangano D. Peri-operative cardiovascular morbidity: new developments. Bailliere’s Clin Anaesthesiol. 1999;13:335-348.
28. Bertrand M, Godet G, Meersschaert K, et al. Should the angiotensin II antagonists be discontinued before surgery? Anesth Analg. 2001;92(1):26-30.
29. Schirmer U, Schurmann W. Preoperative administration of angiotensin-converting enzyme inhibitors. Article in German. Anaesthesist. 2007;56(6):557-561.
30. Roshanov PS, Rochwerg B, Patel A, et al. Withholding versus continuing angiotensin converting enzyme inhibitors or angiotensin II receptor blockers before non-cardiac surgery: an analysis of the vascular events in non-cardiac surgery patients cohort evaluation prospective cohort. Anesthesiology. 2017;126(1):16-27.
31. Devereaux PJ, Mrkobrada M, Sessler DI, et al. Aspirin in patients undergoing non-cardiac surgery. N Engl J Med. 2014;370(16):1494-1503.
32. Lenz M, Kaun C, Krychtiuk KA, et al. Effects of Nicorandil on Inflammation, Apoptosis and Atherosclerotic Plaque Progression. Biomedicines. 2021;9(2):120.
33. Zhou J, Xu J, Cheng A, et al. Effect ofnicorandil treatment adjunctive to percutaneous coronary intervention in patients with acute myocardial infarction: a systematic review and meta-analysis. J Int Med Res. 2020;48(11):1-21.
34. Wang ZD, Li H, Liu M, Li P, et al. Effect of intravenous application of nicorandil on area of myocardial infarction in patients with STEMI during the perioperative stage of PCI. Clin Hemorheol Microcirc. 2021;77(4):411-423.
35. Wang S, Duan Y, Feng X, et al. Sustained nicorandil administration reduces the infarct size in ST-segment elevation myocardial infarction patients with primary percutaneous coronary intervention. Anatol J Cardiol. 2019;21(3):163-171.
36. Qi Q, Niu J, Chen T, Yin H, et al. Intracoronary Nicorandil and the Prevention of the No-Reflow Phenomenon During Primary Percutaneous Coronary Intervention in Patients with Acute ST-Segment Elevation Myocardial Infarction. Med Sci Monit. 2018;24:2767-2776.
37. Zhao XT, Zhang CF, Liu QJ. Meta-analysis of Nicorandil effectiveness on myocardial protection after percutaneous coronary intervention. BMC Cardiovascular Disorders. 2019;19:144.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)


 Примечание. ИМТ — индекс массы тела, ЧКВ — чрескожное коронарное вмешательство, КШ — коронарное шунтирование, ФВ ЛЖ — фракция выброса левого желудочка, СКФ — скорость клубочковой фильтрации, ОХС — общий холестерин.
Примечание. ИМТ — индекс массы тела, ЧКВ — чрескожное коронарное вмешательство, КШ — коронарное шунтирование, ФВ ЛЖ — фракция выброса левого желудочка, СКФ — скорость клубочковой фильтрации, ОХС — общий холестерин. Примечание. АСК — ацетилсалициловая кислота, ББ — бета-адреноблокаторы, БМКК — блокаторы медленных кальциевых каналов, БРА — блокаторы рецепторов ангиотензина, иАПФ — ингибиторы ангиотензинпревращающего фермента.
Примечание. АСК — ацетилсалициловая кислота, ББ — бета-адреноблокаторы, БМКК — блокаторы медленных кальциевых каналов, БРА — блокаторы рецепторов ангиотензина, иАПФ — ингибиторы ангиотензинпревращающего фермента. Примечание. Достоверность различий оценивали с помощью теста Вилкоксона для парных наблюдений.
Примечание. Достоверность различий оценивали с помощью теста Вилкоксона для парных наблюдений. Рис. 1. Уровни участников NO-синтазных реакций аргинина (а), цитруллина (б) и их соотношения (в) в плазме крови пациентов до (1) и через 2 ч после (2) приема никорандила.
Рис. 1. Уровни участников NO-синтазных реакций аргинина (а), цитруллина (б) и их соотношения (в) в плазме крови пациентов до (1) и через 2 ч после (2) приема никорандила. Рис. 2. Разброс данных в зависимости от скорости клубочковой фильтрации: аргинин (а) — корреляция недостоверна, цитруллин (б) — корреляция недостоверна, соотношение Арг/Цит (в) — RS=0,482, р=0,046.
Рис. 2. Разброс данных в зависимости от скорости клубочковой фильтрации: аргинин (а) — корреляция недостоверна, цитруллин (б) — корреляция недостоверна, соотношение Арг/Цит (в) — RS=0,482, р=0,046. Обсуждение
Обсуждение Рис. 3. Частота кардиальных осложнений при открытой артериальной реконструкции в обеих группах.
Рис. 3. Частота кардиальных осложнений при открытой артериальной реконструкции в обеих группах.
