Терапия никорандилом при сердечнососудистых заболеваниях и ее оптимизация
Статьи
Опубликовано в журнале:
Consilium Medicum | 2012 | ТОМ 14 | № 10
Shigeo Horinaka (Шигео Хоринака)
Департамент гипертензии и кардиоренальной медицины. Медицинский университет Dokkyo, Tochigi, Japan
"Первоначальная публикация: Drugs 2011; 71 (9): 1106-19. Публикуется с разрешения правообладателя: Springer Science and Business Media.
В профилактике сердечно-сосудистых заболеваний важную роль играет изменение образа жизни. Для лечения стабильной стенокардии напряжения существуют три варианта ведения больных. Первый - терапевтические меры, включающие a, b, c, d, e:
- а - это ацетилсалициловая кислота и антиангинальные средства;
b - b-адреноблокаторы и артериальное давление (АД);
c - холестерин и сигареты;
d - диета и диабет;
e - образование и физические упражнения.
Второй - это чрескожное коронарное вмешательство (ЧКВ). И третий вариант - это операция аортокоронарного шунтирования. Однако в последних исследованиях ЧКВ не всегда приводило к улучшению клинических исходов в долгосрочной перспективе пациентов со стабильной стенокардией на фоне оптимальной терапии [1-4]. Вот почему возникла необходимость пересмотреть важность медикаментозной терапии.
Согласно рекомендациям Американской коллегии кардиологов и Американской ассоциации сердца [5], а также рекомендациям Европейского общества кардиологов (ЕОК) [6], терапия стабильной стенокардии решает две задачи. Во-первых, это уменьшение симптомов и повторных эпизодов ишемии, а во-вторых, изменение течения заболевания с целью профилактики развития острого инфаркта миокарда (ОИМ) и летальных исходов.
Нитраты, b-адреноблокаторы, антагонисты кальция считаются антиангинальными препаратами, в то время как антитромбоцитарные средства, ингибиторы редуктазы гидроксиметилглютарового кофермента А (статины), ингибиторы ангиотензинпревращающего фермента и антагонисты рецепторов ангиотензина II так же, как и b-адреноблокаторы, являются лекарствами, влияющими на течение заболевания. Никорандил обладает как антиангинальным эффектом, так и способностью улучшать прогноз заболевания.
Никорандил - уникальный антиангинальный препарат с двойным механизмом действия, обладающий свойствами активаторов аденозинтрифосфатзависимых калиевых (КАТФ) каналов и нитратов. Он дает новые возможности кардиологам эффективно убирать симптомы стенокардии и обеспечивает долгосрочную кардиопротекцию [7-11].
1. Фармакологические свойства
Никорандил - производное никотинамида. Он индуцирует продукцию оксида азота (NO) так же, как и нитраты, включая нитроглицерин (глицерина тринитрат), изосорбида динитрат (ИСДН) и изосорбида мононитрат [7-11]. Основными преимуществами никорандила являются уменьшение ишемии миокарда, менее выраженное влияние на гемодинамику, более низкая частота развития нитратной толерантности и улучшение прогноза. Это первый доступный в клинической практике активатор (открыватель) КАТф-каналов с эффектом нитратов. Максимум гемодинамических эффектов никорандила наблюдается через 1-2 мин после внутривенного введения или через 30-60 мин после однократного приема внутрь 20-40 мг и продолжается в течение 12 ч после приема 40-60 мг [12, 13].
1.1. Обоснование применения и фармакологическое действие на гладкомышечные клетки сосудистой стенки
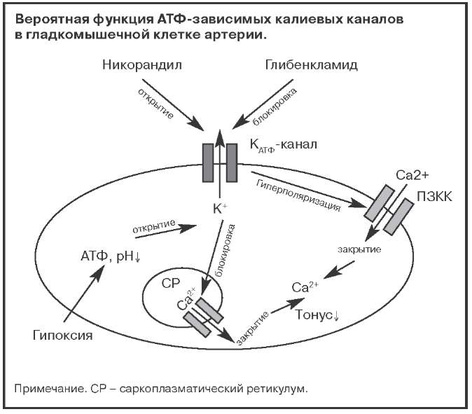
Сперва рассмотрим ионные токи в момент деполяризации и реполяризации клеточной мембраны. Процесс деполяризации индуцирует открытие потенциалзависимых кальциевых каналов (ПЗКК), вследствие чего увеличивается содержание внутриклеточного Ca2+. Затем открываются активируемые кальцием большие калиевые каналы (ВК-каналы), что приводит к реполяризации клеточной мембраны. Содержание внутриклеточного калия падает, что индуцирует закрытие ПЗКК [14, 15].
Никорандил открывает КАТф-каналы в мембранах гладкомышечных клеток сосудов, приводя к выходу калия из клетки и гиперполяризации мембраны, что приводит к снижению поступления Ca2+ внутрь клетки, включая закрытие ПЗКК. Воздействие никорандила на КАТФ-каналы приводит также к ингибированию выхода Ca2+ через саркоплазматическую мембрану. Концентрация внутриклеточного свободного Ca2+ падает [16] (см. рисунок) и в результате преобладает артериальная вазодилатация.
Более того, считается, что нитратподобный эффект никорандила приводит к нарастанию содержания свободных радикалов NO, которые напрямую активируют гуанилатциклазу. Активированная гуанилатциклаза усиливает синтез циклического гуанозинмонофосфата (цГМФ) [17, 18], который активирует цГМФ-зависимую протеинкиназу.
Вследствие этого происходит изменение фосфориляционного статуса различных белков, что запускает следующий каскад событий: активирование ВК-каналов (выход K+ из клетки), вызывающее гиперполяризацию клеточной мембраны и закрытие ПЗКК [19], ингибирование активности семейства протеинов Rho [20], что приводит к активации фосфатазы легких миозиновых цепей, ответственной за дефосфориляцию последних, закрытию рецептор-управляемых кальциевых каналов [21], активации кальциевого насоса сарколеммы и ингибированию инозитолтрифосфатного рецептора на сарколемме [22]. В результате происходит снижение сосудистого сопротивления и вазодилатация, причем доминирует венозная дилатация. Венозная и артериальная дилатация, опосредованные никорандилом, уменьшают как постнагрузку и тонус коронарных артерий, так и преднагрузку и тонус коронарных вен и, соответственно, уменьшают ишемию миокарда. Как было продемонстрировано в условиях эксперимента in vitro, никорандил обладает как нитратподобным действием, так и способностью активировать КАТФ-каналы. Никорандил приводит к дозозависимому расслаблению изолированных коронарных артерий крысы. Кривая релаксации артерии сдвигается вправо не только при использовании метиленового синего - ингибитора образования цГМФ, но и на фоне применения глибенкламида, являющегося блокатором КАТФ-каналов. Таким образом, никорандил расслабляет артерии крысы посредством двойного механизма [9].
Нитратподобный эффект никорандила расширяет крупные артерии, в то время как эффект активирования КАТФ-каналов приводит к дилатации артерий сопротивления диаметром менее 100 мкм [23]. Внутрикоронарное введение никорандила приводит к дозозависимому повышению скорости кровотока и снижению коронарного сосудистого сопротивления. Максимальный вазодилатирующий эффект развивается при введении 1,5 мг никорандила в левую коронарную артерию и 1 мг - в правую. В этом эксперименте ни одна из доз не вызывала клиническую симптоматику и лишь немного изменялась системная гемодинамика. Представленные данные свидетельствуют о том, что болюсное интракоронарное введение никорандила безопасно, быстро и уверенно вызывает максимальную коронарную вазодилатацию у людей [24].
Влияние никорандила на диаметр человеческой эпикардиальной коронарной артерии и на коронарный кровоток изучались как в присутствии глибенкламида -антагониста КАТФ-каналов, так и без него. Степень увеличения диаметра коронарной артерии после болюса никорандила (0,2 мг/кг) не отличалась от такового показателя в присутствии глибенкламида. Введение только никорандила приводило к увеличению коронарного кровотока, а добавление глибенкламида блокировало этот процесс. Это различие в результатах предполагает, что никорандилиндуцированная дилатация крупных коронарных артерий обусловлена нитратподобным эффектом, в то время как дилатация мелких артерий тесно связана с эффектом активирования КАТФ-каналов. Кроме того, первый эффект никорандила проявляется при низких концентрациях, а второй - при более высоких [25].
Таким образом, никорандил вызывает расширение крупных коронарных артерий посредством нитратподобного эффекта. Только в отличие от нитратов никорандил, открывая КАТФ-каналы, способен расширять мелкие коронарные артерии, создающие коронарное сопротивление, и тем самым увеличивает коронарный кровоток.
1.2. Фармакологическое действие на электрофизиологию сердца и антиаритмические эффекты
Никорандил в высокой концентрации в сердечной мышце действует в основном в качестве активатора КАТФ-каналов, укорачивает потенциал действия и рефрактерный период [26, 27], что может давать проаритмические эффекты. Однако M.Hirose и соавт. [28] продемонстрировали, что никорандил в концентрациях 10 и 30 мкмоль/л обладает следующими эффектами:
1) укорачивает потенциал действия в сердечной мышце дозозависимым образом трансмурально, без увеличения дисперсии длительности потенциала действия и без инактивации эпикардиальных слоев;
2) нивелирует замедление трансмуральной проводимости;
3) ингибирует дисперсию скорости локальной проводимости.
Авторы сделали вывод, что никорандил достоверно снижает вероятность появления желудочковой тахикардии во время обширной ишемии в основном за счет усиления инактивации эпикарда опосредованной, по всей видимости, КАТФ-каналами сарколеммы в артериально перфузируемом клиновидном препарате стенки левого желудочка (ЛЖ) собаки. Имеются сообщения о том, что никорандил уменьшает дисперсию интервала QT на электрокардиограмме (ЭКГ) в 12 отведениях [29], тем самым способствуя формированию гетерогенности времени реполяризации, локальных различий длительности потенциала действия и времени активации у пациентов после ЧКВ [30, 31] или при ОИМ [32]. В экспериментах in vivo мы обнаружили, что никорандил предотвращает летальные желудочковые тахиаритмии на фоне ишемии у крыс с ОИМ [33] и блокирует желудочковые аритмии во время и после ЧКВ у пациентов с ОИМ [34]. H.Ueda и соавт. [35] также сообщали, что внутривенное введение никорандила может уменьшать вероятность развития фибрилляции желудочков и дисперсию интервала QT у пациентов с ОИМ, перенесшим успешное ЧКВ. Многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование CESAR (Clinical European Studies in Angina and Revascularization - Клинические европейские исследования стенокардии и реваскуляризации) 2 показало, что никорандил в дозе 20 мг 2 раза в день при приеме внутрь, добавляемый к активной антиангинальной терапии при нестабильной стенокардии, снижает частоту неустойчивых желудочковых аритмий по сравнению с плацебо [36]. Эти результаты предполагают, что никорандил обладает антиаритмическими свойствами в случае нарушений ритма, вызванных автоматизмом или по механизму re-entry, особенно в условиях ишемии миокарда.
2. Клиническая эффективность никорандила
2.1. Пациенты с хронической стабильной стенокардией
При приеме внутрь никорандил эффективен для всех типов стенокардии, включая стенокардию напряжения, покоя, постинфарктную, смешанную, вазоспастическую и нестабильную. В целом эффективность никорандила составляет 71% [37].
В проспективных контролируемых исследованиях краткосрочное (6-12 нед) лечение никорандилом оказалось сопоставимым с b-блокаторами (атенолол [38], пропранолол [39], метопролол [40]), нитратами (изосорбид мононитрат [41, 42], ИСДН [43]) и антагонистами кальция (дилтиазем [44, 45], нифедипин [46], амлодипин [47]) по безопасности и эффективности в отношении подавления симптомов стенокардии, переносимости физических нагрузок и улучшения качества жизни у пациентов с симптоматической стабильной стенокардией. Представленные исследования дали основание полагать, что никорандил обладает более благоприятным профилем переносимости, включая действие на АД и частоту сердечных сокращений (ЧСС), что делает преимущество и при длительной терапии стенокардии.
В рекомендациях ЕОК (2006 г.) использование никорандила (в качестве одной из альтернатив) при непереносимости b-блокаторов или их низкой эффективности соответствует классу рекомендаций I [6].
Другие исследования продемонстрировали эффективность никорандила при вазоспастической стенокардии [48-50].
Внутривенное введение 4-12 мг никорандила приводило к несколько меньшему (от 8 до 27%) увеличению диаметра крупных коронарных артерий по сравнению с сублингвальным приемом 0,3 мг нитроглицерина (от 16 до 32%), к достоверному снижению коронарного сосудистого сопротивления (от -9 до -53%) и к достоверному увеличениинию кровотока в коронарном синусе (от 6 до 81%) у пациентов с ишемической болезнью сердца (ИБС). Эффективность внутривенного применения никорандила (2-6 мг/ч) у пациентов с нестабильной стенокардией была изучена в сравнении с ИСДН (2-5 мг/ч) в двойном слепом многоцентровом исследова. За время лечения в течение 3-9 дней применение никорандила выявило тенденцию к большей эффективности в отношении снижения частоты приступов стенокардии и уменьшению потребления нитроглицерина [51].
2.2. Пациенты с застойной сердечной недостаточностью (ЗСН)
Внутривенное применение никорандила (4-12 мг) у пациентов с ЗСН достоверно снижает среднее АД (от -5 до -15%), системное сосудистое сопротивление -ССС (от -8 до -27%), давление заклинивания в легочной артерии - ДЗЛА (от -15 до -41%), конечное диастолическое давление в ЛЖ (от -8 до -18%) и увеличивает сердечный выброс (от +3 до +19%). Гемодинамические эффекты внутривенного введения 4-8 мг ни-корандила сопоставимы с действием 0,3 мг нитроглицерина. Однако нитроглицерин в большей степени снижает преднагрузку [48].
В исследовании у пациентов с острой сердечной недостаточностью болюсное введение никорандила в дозе 0,2 мг/кг и дальнейшая инфузия 0,2 мг/кг/ч приводила к быстрому и существенному снижению ДЗЛА (-26,5%) и ССС (-13,8%), а также к выраженному увеличению сердечного индекса (15,8%) без избыточного снижения АД и без значимых отклонений ЧСС [52]. Эти результаты и другие исследования [53] дают основание полагать, что никорандил можно безопасно назначать внутривенно пациентам с острой сердечной недостаточностью с низким систолическим АД.
У пациентов с ЗСН через 12 ч непрерывной инфузии нитроглицерина развивается гемодинамическая толерантность. Этого не происходит при использовании никорандила, который сохраняет свою гемодинамическую эффективность и через 24 ч инфузии [54]. Отсутствие развития проявлений гемодинамической толерантности у никорандила, вероятно, является следствием его действия как активатора КАТФ-каналов, а не как нитратподобного агента [55].
A.Larsen и соавт. [56] сравнивали степень гемодинамической толерантности при применении нитроглицерина и никорандила у пациентов с ЗСН. В двойном слепом перекрестном исследовании 20 пациентов с ЗСН были рандомизированы к внутривенному введению нитроглицерина или никорандила. Доза препаратов титровалась до достижения снижения ДЗЛА не менее чем на 30% и в дальнейшем поддерживалась на этом уровне. Оба препарата достоверно снизили ДЗЛА, однако на фоне инфузии нитроглицерина за 24 ч этот показатель постепенно нарастал. Напротив, на фоне инфузии никорандила этот показатель оставался сниженным и через 24 ч. В результате в группе нитроглицерина по сравнению с группой никорандила ДЗЛА через 24 ч оказалось достоверно выше. Исследователи сделали вывод, что внутривенное введение никорандила приводит к гораздо меньшей гемодинамической толерантности за 24 ч, чем введение нитроглицерина. Представленные данные показывают клиническое преимущество никорандила при краткосрочном лечении пациентов с ЗСН.
3. Преимущества никорандила, лежащие за пределами антиангинального действия
3.1. Феномен ишемического прекондиционирования
Первое сообщение о феномене ишемического прекондиционирования в эксперименте было сделано C.Murry и соавт. [57]. В экспериментальной модели на сердце собаки миокард, подвергшийся четырем последовательным 5-минутным эпизодам ишемии/реперфузии, в дальнейшем в меньшей степени испытал некротическое поражение (парадоксальное ограничение размера инфаркта на 25%) на фоне длительной ишемии в виде 40-минутной окклюзии коронарной артерии по сравнению с миокардом, подвергшимся только окклюзии. Однако этот защитный эффект пропадал, когда длительность ишемии доводили до 3 ч. Этот феномен наблюдался у всех видов животных, даже в тех случаях, когда коллатеральный кровоток отсутствовал дистальнее места окклюзии. Ишемическое прекондиционирование описывается как способность кратковременной ишемии сделать миокард более устойчивым к последующей длительной ишемии. Эта «процедура» индуцирует две фазы кардиопротекции - немедленную и отсроченную. Немедленное действие проявляется сразу и длится 2-3 ч, отсроченное - развивается в период от 24 до 48 ч после воздействия коротких периодов ишемии/реперфузии [58].
При продолжительной ишемии и дальнейшей реперфузии перегрузка ионами Ca2+ играет ведущую роль в гиперсократимости мышечных волокон. Это ведет к разрывам сарколеммы [59] и открытию митохондриальных пор с транзиторной проницаемостью (mPTP) [60] в первые минуты после восстановления кровотока.
В механизм ишемического прекондиционирования вовлечено несколько ключевых медиаторов, включая аденозин, сублетальные активные формы кислорода (ROS) и NO. Вероятно, что ишемическое прекондиционирование защищает миокард, снижая оксидативный стресс во время ишемии и реперфузии за счет уменьшения открытия mPTP [61, 62]. В нормальных условиях mPTP закрыты и на митохондриальной мембране поддерживается определенный потенциал и градиент pH. Когда в ответ на ишемию резко увеличивается образование ROS, ухудшаются митохондриальные функции [63], происходит открытие mPTP и различные молекулы, включая протоны, беспрепятственно поступают внутрь митохондрии, что в сочетании с нагрузкой Ca2+, развившейся за время ишемии и реперфузии, ведет к некрозу и апоптозу клеток [61, 64, 65]. A.Costa и соавт. [66] показали, что сигнальный путь открытия КАТФ-каналов приводит к образованию сублетальных уровней ROS и ингибированию открытия mPTP. Кроме того, никорандил открывает митохондриальные КАТФ-каналы не только прямым воздействием, но и опосредованно, через активацию пути NO - цГМФ-зависимой протеинкиназы [67]. Как было показано, ишемическое прекондиционирование, которое достигается короткими эпизодами ишемии и приводит к защите от ишемического и реперфузионного повреждения, сопровождается уменьшением открытия mPTP. С клинической точки зрения, многократные эпизоды стенокардии, которые часто предшествуют ОИМ, способны отсрочить гибель клеток после окклюзии коронарной артерии и обеспечить сохранение миокарда в ходе реперфузионной терапии.
3.2. Ишемическое прекондиционирование в клинической практике
Прединфарктная стенокардия - вариант ишемического прекондиционирования, возникающего у пациентов с ОИМ.
Из 3002 пациентов, рандомизированных в исследование TIMI-9b (Thrombolysis In Myocardial Infarction -Тромболизис при ИМ) стенокардия до ОИМ была у 452 больных. Оказалось, что у пациентов, имеющих приступы стенокардии в течение 24 ч до развития ОИМ, риск развития осложнений, возникающих в ближайшие 30 дней с частотой 4% (смерть, повторный инфаркт, сердечная недостаточность или шок), снизился на 17% по отношению к больным, которые испытывали приступы стенокардии более, чем за 24 ч до ОИМ(р=0,03). Пиковые уровни повышения креатинкиназы также имели тенденцию к более низким значениям в группе больных с приступами стенокардии в ближайшие 24 ч перед ОИМ [68]. Более того, предшествовавшая инфаркту стенокардия в пределах 24 ч ассоциировалась с более низкой госпитальной смертностью (6% против 14%; p=0,02) и меньшей смертностью в ближайшие 5 лет (p=0,009). Пациенты со стенокардией в анамнезе достоверно не отличались по уровню выживаемости от тех, у кого ее раньше не было. Многофакторный анализ показал, что предынфарктная стенокардия, предшествующая ОИМ в пределах 24 ч, является независимым предиктором лучшей выживаемости в течение 5 лет после ОИМ (относительный риск - ОР 0,49;p=0,04) [69].
Как было продемонстрировано E.Deutsch и соавт. [70], ЧКВ - это точная клиническая модель ишемического прекондиционирования. При сравнении первичной окклюзии, вызванной раздуванием баллона с повторной манипуляцией, оказалось, что последняя сопровождается меньшим субъективным ангинальным дискомфортом, меньшим смещением сегмента ST (0,44±0,13 против 0,21+0,07 мВ; p=0,01) и более низким средним давлением в легочной артерии (25±1,0 против 20±1,7 мм рт. ст.; p=0,005). В то же время во время повторной окклюзии кровоток по магистральным венам сердца (96+1,4 против 83+2,4 мл/мин; p=0,005) и произведение ЧСС и АД были достоверно ниже, чем при первой. Также во время второй процедуры была меньше продукция лактата в миокарде (индекс экстракции лактата: первая окклюзия -0,11±0,03; вторая окклюзия -0,03+0,02; p=0,04). Авторы работы сделали вывод, что уменьшение клинических, электрокардиографических, гемодинамических и метаболических признаков ишемии во время повторной окклюзии коронарной артерии во время ЧКВ поддерживает концепцию ишемического прекондиционирования [70].
3.3. Фармакологическое прекондиционирование
Действие активаторов митохондриальных КАТФ-ка-налов препятствует гиперсокращению кардиомиоцитов, обусловленному реоксигенацией - ключевым свойством реперфузионного повреждения [71]. Активаторы митохондриальных КАТФ-каналов, например никорандил, индуцируют вход ионов K+ в митохондриальный матрикс, что вызывает деполяризацию внутренней митохондриальной мембраны. Это, в свою очередь, способствует снижению перегрузки митохондрий ионами Ca2+ во время ишемии, уменьшению их набухания и ведет к продукции сублетальных уровней ROS. Воздействие последних имитирует ишемическое прекондиционирование в отсутствии ишемии [72, 73].
Более того, применение активаторов КАТФ-каналов даже на этапе реоксигенации может обеспечить существенную защиту миокарда [74].
Был проведен эксперимент с использованием культуры изолированных миоцитов желудочка сердца новозеландского белого кролика. Никорандил (100 мкмоль/л) увеличивал окисление флавопротеинов через митохондриальные КАТФ-каналы, но не увеличивал ток через КАТФ-каналы сарколеммы. Для открытия обоих типов каналов требовалось 10-кратное увеличение концентрации. Дозозависимая кривая указывает на то, что концентрации никорандила в пределах 10 мкмоль/л открывают только митохондриальные КАТФ-каналы, в то время как для открытия КАТФ-каналов сарколеммы требуются на порядок более высокие концентрации (ммоль/л). В экспериментальной модели ишемии никорандил уменьшал число погибших клеток (через 60 и 120 мин). Это кардиопротективное действие блокировалось при добавлении блокатора митохондриальных
КАТФ-каналов, тогда как при добавлении блокатора КАТФ-каналов сарколеммы кардиопротективное действие не наблюдалось. Таким образом, небольшие концентрации никорандила оказывают прямой кардиопротективный эффект на сердечную мышцу, который обусловлен селективной активацией митохондриальных КАТФ-каналов [75]. Представленные результаты исследований указывают на наличие у никорандила эффекта фармакологического прекондиционирования посредством активации митохондриальных КАТФ-каналов.
В исследовании, выполненном T.Matsubara и соавт. [76], 46 пациентов со стабильной стенокардией были рандомизированы в 4 группы. В первых двух длительность первой окклюзии в качестве прекондиционирования в ходе ЧКВ составляла 60 и 180 с. В двух других группах никорандил (80 мкг/кг) или ИСДН (40 мкг/кг) назначались внутривенно в течение 1 мин без окклюзии артерии баллоном. Во всех группах через 5 мин после первой окклюзии или после назначения лекарств проводили окклюзию артерии, раздувая баллон на 120 с. Вторая окклюзия вызвала достоверно меньшее смещение сегментов ST на ЭКГ в группе 180 с ишемического прекондиционирования и в группе, получавшей никорандил, по сравнению с двумя другими. Таким образом, в клинической модели при ЧКВ в ответ на окклюзию в течение 180 с (но не при 60-секундной ишемии) развивалось ишемическое прекондиционирование, а после введения никорандила (но не после введения ИСДН) -фармакологическое прекондиционирование [76].
Несмотря на то, что защитный эффект никорандила может быть отчасти обусловлен защитой сосудистой сети во время реперфузии, он также может вовлекать потенцирование ишемического прекондиционирования кардиомиоцитов и артериол через коллатеральный кровоток, индуцированный посредством внутривенного или внутрикоронарного введения никорандила, назначаемого перед ЧКВ даже тогда, когда имеет место полная окклюзия коронарной артерии.
В исследование, выполненное H.Matsuo и соавт. [77], были включены 44 пациента со стенокардией и стенозом в проксимальной части левой передней нисходящей артерии, которым была проведена ЧКВ. Больные были в случайном порядке разделены на 2 группы: первым назначался никорандил внутривенно (80 мкг/кг), вторым - физиологический раствор в течение 5 мин. Во время ЧКВ в момент раздувания баллона длительностью 2 мин регистрировали ЭКГ и проводили однопротонную эмиссионную компьютерную томографию с технецием (99mTc). В группе получавших перед ЧКВ никорандил отмечалось достоверное уменьшение смещений ST-сегмента в сравнении с пациентами, получавшими физраствор. Тем не менее при количественном сравнении ангиограмм, полученных во время окклюзии, различий по дефектам наполнения не наблюдалось. Таким образом, предшествовавшее окклюзии введение никорандила вызывало прекондиционирование миокарда независимо от тяжести ишемии [77].
4. Клиническое действие никорандила при лечении пациентов с ИБС
Предшествующие исследования с активаторами КАТФ-каналов дали основание предполагать, что вероятный механизм их действия - это индукция состояния, сопоставимого с ишемическим прекондиционированием [74-77]. Ишемическое прекондиционирование, например в виде предынфарктной стенокардии, при длительном наблюдении уменьшает смертность у пациентов с успешной реперфузией при ОИМ [68, 69]. Однако предынфарктная стенокардия в ближайшие 24 ч перед ОИМ развивается не всегда. Исследование IONA (the Impact of Nicorandil in Angina) было проведено для того, чтобы изучить возможность использования активаторов КАТФ-каналов для индуцирования состояния прекондиционирования миокарда, похожего на то, которое возникает при предынфарктной стенокардии.
Исследование IONA было крупномасштабным рандомизированным двойным слепым и плацебоконтролируемым [78]. Никорандил назначался в дозе 20-40 мг 2 раза в день. Включались только пациенты со стабильной стенокардией, получающие регулярную антиангинальную терапию, такую, как нитраты длительного действия, b-блокаторы или антагонисты кальция. Исследование проводилось в Великобритании. Около 5 тыс. пациентов были рандомизированы к приему никорандила или плацебо. Средний период наблюдения составил 1,6 года (от 1 до 3 лет). Критериями исключения были острый коронарный синдром (ОКС) и прием препаратов сульфонилмочевины, которые ингибируют КАТФ-каналы.
Первичной конечной точкой этого исследования было одно из следующих событий: смерть от ИБС, нефатальный ИМ или незапланированная госпитализация в связи с ангинозным приступом. В группе плацебо конечная точка была зарегистрирована в 15,5% случаев, а в группе никорандила - у 13,1%. Никорандил снизил риск развития первичной конечной точки на 17% (p=0,014). Однако вторичные конечные точки - смерть от ИБС и нефатальный ИМ достоверно не различались (p=0,068). Вероятно, в исследовании не было достаточной статистической мощности, чтобы продемонстрировать различие по твердым конечным точкам, поскольку частота событий в группе контроля была существенно ниже, чем ожидалось.
Исследование IONA стало первым длительным исследованием у пациентов со стабильной стенокардией, где была показана способность активаторов КАТФ-каналов, таких как никорандил, уменьшать число клинически значимых исходов. Однако в исследовании IONA снижение событий первичной конечной точки произошло в основном за счет «мягких» исходов [79], что говорит о необходимости дальнейшего изучения влияния препаратов на твердые клинические исходы.
После завершения исследования IONA осталось несколько нерешенных вопросов. Результаты могут варьировать в различных этнических группах. Из исследования исключались пациенты высокого риска с ОКС. Кроме того, неясно, какая доза никорандила наиболее подходит для лечения ИБС.
JCAD (the Japanese Coronary Artery Disease) - многоцентровое (217 госпиталей) кооперативное проспективное наблюдательное исследование большой когорты больных с ИБС, проводившееся для изучения факторов риска, текущей терапии и проверки различий в исходах ИБС. Оно включало около 36% больных с ОКС [80].
Из 13 812 пациентов, зарегистрированных в JCAD, были отобраны по 2558 больных, принимавших никорандил и подобранных им в пару по индексу соответствия больных контрольной группы. Среднее время наблюдения составило 2,7 года. Частота достижения первичной конечной точки (смерть от любых причин) в группе никорандила была достоверно на 35% ниже, чем в контрольной группе (ОР 0,65; р=0,0008). В группе никорандила отмечено также достоверное снижение частоты достижения вторичных конечных точек, включая сердечную смерть (56%), фатальный ИМ (56%), церебральную или сосудистую смерть (71%) и ЗСН (33%) без увеличения числа смертей от других некардиоваскулярных причин. Это исследование продемонстрировало, что пероральный прием никорандила (по 5 мг 3 раза в день) улучшает клинические исходы при ИБС и останавливает развитие хронической сердечной недостаточности (ХСН) при ИБС. Однако оно было описательным и нерандомизированным, без плацебоконтроля [81]. Тем не менее снижение сердечнососудистой смертности при применении никорандила у больных с ИБС было значительным, что имеет большое значение для применения в терапии этого заболевания.
В отличие от предыдущего в проспективное одинарное слепое исследование J-WIND (the Japan Working Group Studies on Acute Myocardial Infarction for the Reduction of Necrotic Damage) [82] были включены 1216 пациентов с ОИМ после успешной реперфузии. В общей сложности 276 пациентов были рандомизированы к получению внутривенной инфузии никорандила (0,067 мг/кг болюсно, затем инфузия 1,67 мкг/кг/мин в течение 1 сут) с кардиопротективной целью [83] и 269 пациентов составили группу контроля. Первичными конечными точками были размер инфаркта (по уровню креатинкиназы) и фракция выброса (ФВ) ЛЖ (по данным вентрикулографии). Общий показатель креатинкиназы составил в группе никорандила 70520,5 МЕ/мл/ч и в группе контроля 70852,7 МЕ/мл/ч (отношение геометрических средних составило 0,995; p=0,94). Внутривенное введение никорандила не повлияло на ФВЛЖ, в то время как дальнейший пероральный прием привел к увеличению ФВ на 2,2% по сравнению с острым периодом (3,66% при пероральном применении никорандила против 1,47% без него; p=0,0338).
Причина, по которой внутривенное введение никорандила не повлияло на размер инфаркта, могла быть маленькая доза, что было обсуждено M.Kitakaze и соавт. [82]. Действительно, однократная внутривенная инъекция никорандила (12 мг) перед реперфузией, которая в 3 раза превышала дозировку в J-WIND, улучшала состояние не только в острой фазе, но и приводила к уменьшению клинических событий в отдаленном периоде (сердечно-сосудистая смерть или госпитализация в связи с ХСН; ОР 0,39; p=0,0058) у пациентов с первым ОИМ с подъемом сегмента ST [84]. Существует вероятность, что сывороточные концентрации никорандила в этом исследовании были достаточны для дилатации сосудов сопротивления в местах ишемических поражений. Однако этот результат может отражать и усиление ишемического прекондиционирования кардиомиоцитов перед реперфузией.
В исследовании H.Ito и соавт. [83] 81 пациент с первым ОИМ передней локализации был рандомизирован в 2 группы: получавшие никорандил (4 мг болюс, затем инфузия 6 мг/ч в течение 24 ч, затем пероральный прием 15 мг/день) или плацебо. В результате при проведении контрастной эхокардиографии после успешной ЧКВ феномен no-reflow в группе никорандила встречался достоверно реже, чем в группе плацебо (15% против 33% соответственно; p<0,05). Улучшение микрососудистой функции на фоне никорандила может быть также обусловлено лучшими исходами после ЧКВ [83]. В исследовании YKawai и соавт. [85] 408 пациентам с ОКС и стабильной стенокардией назначали болюсно 6 мг никорандила или плацебо непосредственно перед ЧКВ. В результате на основании ангиографических данных число случаев феномена slow-flow в группе никорандила было достоверно меньше, чем в группе плацебо (4,4% против 17,8%; p<0,0001). Более того, у исследуемых пациентов с ОКС частота реваскуляризации «целевой» артерии была достоверно ниже в группе никорандила по сравнению с группой плацебо.
Другой возможной причиной отрицательных результатов в J-WIND может являться тот факт, что 45% пациентов имели предынфарктную стенокардию, которая может уменьшать эффект от фармакологического прекондиционирования [59-62], поскольку она сама приводит к возникновению ишемического прекондиционирования [68-70]. С другой стороны, метаанализ публикаций по никорандилу с 1998 по 2007 г. также выявил, что терапия этим препаратом в качестве дополнительной к реперфузии терапии приводит к существенному уменьшению случаев пост-ЧКВ феномена no-reflow и к увеличению ФВЛЖ в постинфарктном периоде [86].
Интересно, что в исследовании J-WIND также было показано, что пероральный прием никорандила в хроническую фазу ИМ приводит к повышению ФВЛЖ [82]. Микрососудистая обструкция, возникающая через 6-10 дней после ОИМ, ведет к формированию рубца,
нежелательному ремоделированию ЛЖ и к ухудшению прогноза [87, 88]. Открытие КАТФ-каналов в этот период времени может улучшить коронарное кровоснабжение за счет дилатации микрососудов [18].
В исследованиях у пациентов с ОИМ [89] и ишемической кардиомиопатией [90] по данным сцинтиграфии с 123I-MIBG (общий дефект наполнения, сердечномедиастинальное соотношение и скорость вымывания) применение никорандила в течение 6 мес (по 5 мг 3 раза в день) приводило к существенному улучшению по сравнению с 3-недельным курсом терапии. Длительный пероральный прием никорандила был более эффективен, чем прием нитратов в отношении симпатической нервной активности сердца и ремоделирования ЛЖ после реперфузионной терапии у пациентов с ОИМ или постинфарктным кардиосклерозом, как и в экспериментальной модели [91]. Таким образом, действие активаторов КАТФ-каналов на микрососудистую циркуляцию и/или на симпатическую нервную активность в сердце приводило к улучшению функции ЛЖ.
S.Sanada и соавт. [92] сообщали, что никорандил уменьшал ремоделирование сердца, ингибируя активность S6 (70 кДа) при длительном ингибировании NO-синтазы (NOS) в модели на крысах, получавших метиловый эфир Nw-нитро-L-аргинина. S.Horinaka и соавт. [93] также сообщали, что никорандил предотвращает ремоделирование ЛЖ и ухудшение сердечной функции у гипертензивных чувствительных к соли крыс Dahl с сердечной недостаточностью. Эти эффекты отчасти опосредованы усилением экспрессии эндотелиальной NOS через активацию КАТФ-каналов в сердце.
В исследовании JCAD [80] частота развития ЗСН была значительно ниже в группе никорандила в сравнении с контрольной группой, возможно, за счет улучшения эндотелиальной функции [94, 95] и функции ЛЖ, за счет улучшения микрососудистого кровообращения [18] и/или симпатической активности сердечных нервов [89-91].
Эти механизмы также вовлечены в процесс увеличения ФВЛЖ при длительном пероральном приеме никорандила в терапии постинфарктного кардиосклероза.
Недавно при ретроспективном анализе исследований были получены свидетельства улучшения прогноза на фоне перорального приема никорандила у пациентов с ИБС и находящихся на плановом гемодиализе [96, 97]. В исследовании M.Nishimura и соавт. [98] при проспективном анализе 129 пациентов, подвергшихся ЧКВ и получавших плановый гемодиализ, были распределены на 2 группы: группу никорандила (по 5 мг 3 раза в день) и в контрольную группу. В группе никорандила выживаемость через 3 года оказалась достоверно (p=0,009) выше (86,6%), чем в контрольной группе (70,7%). R.Dikow и соавт. [99] продемонстрировали, что размер зоны инфаркта после лигирования коронарной артерии у крыс с умеренной почечной недостаточностью больше, чем без нее, что предполагает уменьшение толерантности к ишемии в условиях почечной дисфункции. Известно, что смертность среди пациентов после ОИМ на фоне выраженной почечной недостаточности выше [100-102]. D.Hodgson и соавт. [103] продемонстрировали, что собственные свойства КАТФ-каналов предполагают наличие места терапевтического приложения для повышения толерантности клеток при различных заболеваниях. Таким образом, ожидается, что никорандил проявит защитные свойства против ишемии посредством активации КАТФ-каналов и у пациентов с тяжелой почечной недостаточностью.
Механизмы улучшения прогноза у пациентов с ИБС могут включать ишемическое прекондиционирование кардиомиоцитов посредством открытия митохондриальных КАТФ-каналов и улучшения микрососудистой циркуляции крови в коронарных артериях посредством открытия КАТФ-каналов сарколеммы в гладкомышечных клетках сосудистой стенки.
Недавно Y.Izumiya и соавт. [104] показали, что пероральное лечение никорандилом (15 мг в день в течение
6 и более месяцев) приводит к большему проценту фиброзной ткани и меньшему объему некротического ядра атеросклеротической бляшки по данным прединтервенционного внутрисосудистого ультразвукового исследования (УЗИ) и виртуальной гистологии (специальный анализ внутрисосудистого УЗИ), чем лечение другим агентом у пациентов со стабильной стенокардией. Таким образом, никорандил обладает эффектом стабилизации атеросклеротической бляшки.
Такие механизмы, как нормализация функции эндотелия [94, 95], ингибирование активности симпатических нервов в сердце [89-91], антитромботический эффект [105] и, как уже упоминалось, стабилизация атеросклеротической бляшки, также могут быть вовлечены в улучшение прогноза у пациентов с ИБС.
Рекомендуемые в Европе и Океании дозы при назначении никорандила - 10-40 мг/сут, разделенных на 2 приема. В Азии рекомендуется принимать никорандил 7,5-30 мг/сут, разделенных на 3 приема [106]. Как было показано, пероральный прием никорандила (по 5 мг 3 раза в день) обладает эффектом прекондиционирования у пациентов с ИБС. Никорандил в дозе 40 мг/сут, разделенных на 2 приема, которая применялась в исследовании IONA, улучшает клинические исходы. Таким образом, 3-кратный пероральный прием можно считать идеальным, но для пациентов с низким комплаенсом как вариант можно использовать 2-кратную схему [13].
5. Переносимость
Суммарный анализ данных показывает, что никорандил хорошо переносился в клинических исследованиях длительностью 3 и более лет [78, 107-109]. В сравнительных исследованиях никорандила с другими антиангинальными препаратами (пропранололом [107], дилтиаземом [45], амлодипином [47]), частота нежелательных эффектов не различалась между группами (30-36%). Нежелательные эффекты чаще развивались в начале лечения, а в дальнейшем их частота снижалась [107, 108]. Наиболее частым нежелательным эффектом, связанным с приемом препарата, была головная боль (частота отмены 3,5-9,5%) [108, 109]. Однако в недавнем исследовании при сравнении никорандила с изосорбидом мононитратом не было выявлено достоверных различий по частоте развития головной боли [42]. Для того чтобы избежать отмен никорандила из-за этого побочного эффекта, необходимо начинать лечение с низких доз с постепенной дальнейшей титрацией [107, 108]. Изредка развиваются такие нежелательные эффекты:, как головокружение, желудочно-кишечные симптомы, недомогание и утомляемость [78, 107, 108].
6. Заключение
Никорандил - активатор КАТФ-каналов с нитратоподобным действием, который устранаяет симптомы стенокардии не только у пациентов со стабильной стенокардией напряжения подобно нитратам, b-блокаторам и антагонистам кальция, но и у пациентов с вазоспастической стенокардией. Открытие митохондиальных КАТФ-каналов никорандилом может защищать кардиомиоциты и уменьшать частоту возникновения сердечно-сосудистых осложнений. Таким образом, никорандил является идеальным антиангинальным препаратом. Для обеспечения максимальной эффективности при ОИМ очень важно назначить никорандил внутривенно как можно раньше, а затем переходить к пероральному приему.
Конфликт интересов
При подготовке рукописи сторонние источники финансирования не использовались. У автора отсутствует конфликт интересов, непосредственно связанный с содержанием обзора.
Списоклитературы находится на сайте журнала Consilium Medicum: www.consilium-medicum.com
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)