Микрососудистая стенокардия: вопросы диагностики и лечения 2019 г.
Статьи
Опубликовано в журнале:
«Атмосфера. Новости кардиологии», 2018, 4, с. 16-27
Ю.А. Карпов, Г.Н. Соболева, Е.А. Ерпылова
В обзоре рассматриваются вопросы микрососудистой стенокардии: распространенность, влияние пола, патофизиология и подходы к лечению. Выделена группа риска развития этой патологии - женщины со стабильной стенокардией, положительными результатами нагрузочных тестов и ангиографически нормальными или малоизмененными коронарными артериями. Проводится анализ данных, позволяющих улучшить понимание дисфункции коронарных сосудов и результирующей ишемии миокарда, которые характеризуют микрососудистую дисфункцию у пациентов с микрососудистой стенокардией. Даются рекомендации по изменению образа жизни пациентов, применению препаратов, направленных на улучшение микрососудистой функции, антиангинальной терапии, а также лекарств и процедур, связанных с восприятием боли.
Ключевые слова: ишемическая болезнь сердца, микрососудистая стенокардия, нарушение эндотелиальной функции, коронарный кровоток, диагностика, подходы к лечению, активаторы калиевых каналов, никорандил.
На сегодняшний день сердечно-сосудистые заболевания, особенно ишемическая болезнь сердца (ИБС), относятся к числу основных причин инвалидизации и смертности взрослого населения [1,2]. Согласно данным Росстата, количество смертей от ИБС в 2016 г. составило 328,5 на 100 000 населения [3]. Наиболее распространенной причиной развития ИБС и, соответственно, ишемии миокарда считается коронарный атеросклероз с различной степенью обструкции, вплоть до окклюзий, питающих миокард сосудов, имеющий грозные осложнения (коронарный тромбоз, сердечная недостаточность, внезапная смерть). Тем не менее, по разным данным, примерно у половины пациентов со стабильной стенокардией, которым проводится диагностическая коронарная ангиография (КАГ), и у 10-20% пациентов с острым коронарным синдромом выявляются неизмененные или малоизмененные (менее 50% сужения просвета сосуда) коронарные артерии [2, 4].
В одном из исследований у 44,5% из 925 пациентов, направленных на плановую диагностическую КАГ, были выявлены неизмененные или малоизмененные коронарные артерии [5]. Согласно данным W.L. Proudfit et al., у 20% пациентов, которым была выполнена КАГ при болях в груди, обнаруживались нормальные коронарные артерии [6]. Еще в одном исследовании у 14,6% пациентов, которым была выполнена КАГ при наличии болевого синдрома в груди и подозрении на поражение коронарных артерий, также не было выявлено их изменений [7]. Следует отметить, что у пациентов с болями в груди и без предварительного установления ишемии миокарда обнаруженные при КАГ неизмененные коронарные артерии исключают диагноз микрососудистой стенокардии (МСС), а само инвазивное обследование может оказаться малообоснованным в отсутствие других данных и факторов риска.
Указанное состояние впервые было описано примерно 40 лет назад H.G. Kemp et al. и получило название “кардиальный синдром Х” (КСХ) [8]. Наряду с этим термином в последующем использовались и многие другие определения, такие как синдром Х, болезнь малых сосудов, стенокардия с поражением сосудов малого диаметра, синдром Джорлина-Лайкоффа, необструктивная болезнь коронарных артерий, а в последние годы наибольшее распространение получил термин МСС. Следует напомнить, что термин МСС был первоначально предложен R.O. Cannon, S.E. Epstein еще в 1988 г. для обозначения миокардиальной ишемии, возникшей не вследствие обструктивных изменений коронарного русла, а в связи с микрососудистыми аномалиями [9]. В российских и европейских рекомендациях по стабильной ИБС предлагается в подобных случаях использовать термин МСС [1,2], который и употребляется наиболее часто в последнее время, в том числе в клинической практике. Его популяризация, возможно, связана еще и с тем, что у многих из таких пациентов клинические симптомы могут быть, как предполагают эксперты, следствием микрососудистой дисфункции (МСД) коронарного русла, которая чаще всего и описывается в указанных случаях [10-12].
Также предполагается, что МСС может возникать в результате функциональной или структурной дисфункции коронарной микроциркуляции при специфических заболеваниях сердца и сосудов, например при кардиомиопатии, сочетаться с ИБС на фоне коронарного атеросклероза или при системных заболеваниях, например в связи с аутоиммунными заболеваниями, коллагеновыми заболеваниями, артериальной гипертонией, и в таких случаях она определяется как вторичная МСС [13-15]. Однако в большинстве случаев MCC развивается вследствие изолированной коронарной МСД, которая является единственным или преобладающим механизмом, ответственным за возникновение эпизодов стенокардии или ишемии миокарда. Такая МСС определяется как первичная [13, 14].
Совсем недавно группа COVADIS предложила диагностические критерии для определения МСС в виде триады признаков [10, 14]:
1) боль в груди (стенокардия), в основном при нагрузке (иногда также в состоянии покоя);
2) ишемические изменения на электрокардиограмме (ЭКГ) (депрессия сегмента ST) во время нагрузочного теста или других неинвазивных тестов на выявление ишемии миокарда;
3) нормальные или малоизмененные коронарные артерии при КАГ.
Не всегда МCC клинически представляет собой стабильную стенокардию, возникающую при напряжении. У некоторых пациентов заболевание может манифестировать в форме острого коронарного синдрома с выраженными и длительными болями в грудной клетке и изменениями реполяризации на ЭКГ, иногда также с повышенными уровнями сывороточных маркеров некроза миокарда, что обусловливает определение этого конкретного состояния как нестабильной (или острой) МCC с развитием инфаркта миокарда (ИМ) [13, 14].
Распространенность заболевания, влияние пола
У женщин, обращающихся к врачу с болевым синдромом с подозрением на стенокардию, при проведении КАГ в 5 раз чаще, чем у мужчин, выявлялись нормальные или малоизмененные коронарные артерии [4]. В исследованиях также указывается на значительное преобладание женщин в этой группе больных [5]. У женщин с КСХ симптомы появляются, как правило, в перименопаузе или менопаузе, между 40 и 50 годами [16]. По данным одного из исследований, пациенты, у которых отмечалась меньшая выраженность коронарного стеноза, были моложе и среди них было больше женщин. У них наблюдалась меньшая распространенность периферического и цереброваскулярного атеросклеротического поражения и факторов риска развития ИБС [5, 14]. Между этими пациентами не было статистически значимых различий по выраженности стеноза при нестабильной и стабильной стенокардии [5].
Патофизиология
Понимание причин развития, патогенеза и сопутствующих факторов, лежащих в основе болей в грудной клетке, которые манифестируют ишемическими изменениями на ЭКГ при нормальных или малоизмененных коронарных артериях по данным КАГ, имеет большое значение для правильного ведения больных с МСС [1,2, 11, 15].
На сегодняшний день нет сомнений в том, что МСС является гетерогенным синдромом, в основе развития которого могут лежать различные патогенетические механизмы. К предполагаемым механизмам относятся МСД, измененная регуляция коронарной микроциркуляции вегетативной нервной системой, генерализованные сосудистые нарушения и изменения субэндокардиальной перфузии (рисунок) [10, 11, 14, 17, 18]. Основной причиной развития МСС может служить дисфункция коронарных микрососудов как аномальный ответ коронарной микроциркуляции на различные вазоконстрикторные и вазодилатирующие стимулы [11, 12]. Кроме того, к числу факторов, способствующих возникновению МСС, относят воспаление, гипер-инсулинемию, повышение активности натрий-водородного обмена, гормональный дефицит, нарушение восприятия внутрисердечной боли и, наконец, врожденные патогенетические механизмы [11].
Механизмы миокардиальной ишемии
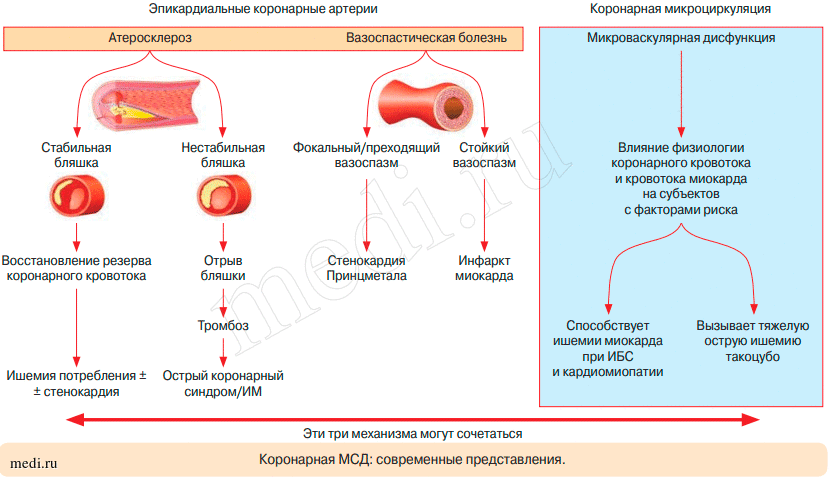
Диагностика
Среди пациентов со стенокардией невозможно с уверенностью выделить лиц с MCC и обструктивными поражениями коронарных артерий при использовании только клинических данных и неинвазивной диагностики, без проведения КАГ [1, 2]. Тем не менее некоторые особенности болевого синдрома в груди позволяют заподозрить диагноз МСС. В частности, типичными для МСС являются большая длительность болевого синдрома после нагрузки и неустойчивый эффект при приеме сублингвальных нитратов. Наблюдая подобную клиническую картину, особенно у женщин, врач может сделать предположение о микрососудистом происхождении симптомов [1,2, 11].
Неинвазивные диагностические исследования также редко способствуют установлению дифференциального диагноза с ИБС на фоне стенозирующего поражения коронарных артерий. Результаты нагрузочных проб не различаются у пациентов с МСС и пациентов с обструктивным поражением коронарных артерий; при нагрузочной сцин-тиграфии миокарда у 50% пациентов с МСС выявляются дефекты перфузии, неотличимые от таковых у пациентов со стенозирующим коронарным атеросклерозом [2, 11].
Вместе с тем, если при стресс-эхокардиографии (с физической нагрузкой или фармакологической пробой) отсутствуют глобальные или региональные нарушения сократимости стенки левого желудочка при наличии у пациента клинической картины стенокардии и изменений сегмента ST на ЭКГ, то это скорее указывает на микрососудистое происхождение симптомов, хотя и умеренные обструктивные изменения коронарных артерий при ИБС не могут быть полностью исключены [10, 11, 14].
Повторение нагрузочного теста после приема сублингвальных нитратов может облегчить диагностику у пациентов с МСС. У больных ИБС на фоне обструктивных изменений отрицательная динамика сегмента ST уменьшается, в то время как у больных с МСС действие сублингвальных нитратов является переменным и непостоянным, а в некоторых случаях у них отмечается более раннее возникновение ишемических изменений, таких как депрессия сегмента ST во время нагрузки [2, 10, 14].
Основополагающими методиками верификации ишемии миокарда у больных с МСС являются (табл. 1) [2, 10, 11, 14]:
- однофотонная эмиссионная компьютерная томография (ОФЭКТ) сердца, совмещенная с нагрузочным или фармакологическим тестом;
- интракоронарное введение аденозина с оценкой скорости коронарного кровотока методом внутрисосудистого ультразвукового исследования;
- аномальное соотношение фосфокреатина/аденозин-трифосфата (АТФ) в миокарде у больных с МСС по данным магнитно-резонансной спектрографии (МРС);
- субэндокардиальные дефекты перфузии по данным магнитно-резонансной томографии сердца.
Таблица 1.
Обследование пациентов с подозрением на МСС [2]

Группой COVADIS было предложено выставлять окончательный диагноз МСС после верификации МСД при помощи определения резерва коронарного кровотока (РКК) [10]. Исследование коронарной микрососудистой функции можно проводить как инвазивными, так и неинвазивными методами.
Наиболее широко применяемый инвазивный метод для оценки коронарной микрососудистой функции - это запись скорости коронарного кровотока с использованием интракоронарной допплерографии в сочетании с устройством давления/термодилюции, позволяющим измерять как коронарный кровоток, так и коронарное микрососудистое сопротивление [19, 20]. Ранее в ФГБУ “РКНПК” МЗ РФ проводились исследования с введением ацетилхолина интра-коронарно и 99mTc-МИБИ внутривенно с целью провокации ишемии миокарда, обусловленной дисфункцией эндотелия [12]. Указанный метод продемонстрировал высокую информативность, но не нашел широкого применения из-за инвазивного характера [2].
Среди наиболее надежных и точных методов неинвазивной оценки МСД - позитронная эмиссионная томография (ПЭТ), которая позволяет определять неоднородное распределение дефектов перфузии, не ограничивающихся распространением в области одной коронарной артерии [21,22]. Эти нарушения расслабления гладких мышц, а также снижение коронарного кровотока у больных с гемодинамически незначимыми стенозами на КАГ подтверждают гипотезу о том, что клинические симптомы имеют в основе нарушение микроциркуляции [18, 23]. Однако ограниченная доступность ПЭТ в клинической практике и высокая стоимость исключают его широкое применение для рутинного обследования пациентов с МСС [2, 22].
Магнитно-резонансная томография с гадолинием также является перспективным инструментом для неинвазивной оценки коронарного кровотока [2, 5, 19].
В настоящее время исследования, проведенные в ФГБУ “НМИЦ кардиологии” МЗ РФ, позволяют рекомендовать к применению в широкой клинической практике такой способ верификации ишемии миокарда у больных с МСС, как ОФЭКТ миокарда, совмещенную с введением доступного на российском фармрынке АТФ [24]. С появлением метода объемной компьютерной томографии (КТ) сердца, сочетающего проведение КТ-КАГ, изучение перфузии миокарда и выполнение фармакологической пробы с АТФ, выявление ишемии миокарда при необструктивном поражении коронарных артерий стало возможным при проведении только одного этого неинвазивного метода [24].
Подходы к лечению
Как и при лечении пациентов со стабильной ИБС на фоне обструктивного атеросклеротического поражения, комплекс мероприятий при МСС должен включать несколько основных направлений.
Общие терапевтические подходы (изменение образа жизни)
1. Прекращение курения и снижение избыточной массы тела для улучшения микроциркуляции [25, 26].
2. Использование средиземноморской диеты и проведение регулярных умеренных физических тренировок, направленных на улучшение эндотелиальной функции [27].
3. Адренергическая модуляция, связанная с физическими тренировками, которая способствует уменьшению выраженности загрудинных болей [28].
4. Обязательный контроль артериального давления при его повышении и нормализация нарушенного углеводного обмена.
Применение препаратов, направленных на улучшение микрососудистой функции
С учетом патофизиологических механизмов, лежащих в основе развития коронарной МСД, предлагается целый ряд препаратов, которые могут восстановить нарушенную функцию. К ним относятся ингибиторы ангиотензинпревращающего фермента (АПФ), статины, бигуаниды, ингибиторы ксантиноксидазы и препараты гормональной заместительной терапии [11,29].
Ингибиторы АПФ. Препараты, блокирующие активность ренин-ангиотензиновой системы, могут улучшать микрососудистую функцию за счет устранения вазоконстрикторных эффектов ангиотензина II. В небольших исследованиях было показано, что ингибиторы АПФ улучшают симптомы, уменьшая выраженность и частоту болевых ощущений, увеличивают продолжительность нагрузочных проб и могут быть полезными в лечении МСС [10].
Также было установлено, что ингибиторы АПФ улучшают эндотелиальную функцию и могут оказывать положительное влияние при КСХ. Например, в рандомизированном двойном слепом плацебоконтролируемом исследовании наблюдалось уменьшение депрессии сегмента ST при лечении ингибиторами АПФ, улучшение показателей при пробе с физической нагрузкой у пациентов с КСХ и сниженным коронарным кровотоком [30].
Еще в одном плацебоконтролируемом исследовании также продемонстрировано, что при лечении эналаприлом на протяжении 8 нед значительно улучшились не только показатели проб с физической нагрузкой, но и РКК, а также увеличился уровень эндотелиального оксида азота у пациентов с КСХ [31].
Статины. Следует отметить, что у пациентов с МСС было проведено несколько исследований по оценке влияния статинов на течение этой формы ИБС. Статины наряду с липидснижающими эффектами оказывают и так называемые плейотропные эффекты. К ним относятся активация синтазы оксида азота (NOS) для улучшения функции эндотелия, снижение уровня эндотелина-1 в плазме (вазоконстриктор), асимметричного диметиларгинина (эндогенного ингибитора NOS) и ингибирование воспаления, а также различные антитромботические и антиоксидантные эффекты, способствующие стабилизации атеросклеротической бляшки [2].
В плацебоконтролируемом исследовании в условиях двойного слепого метода у 20 пациентов с МСС было продемонстрировано увеличение эндотелийзависимой вазодилатации вследствие улучшения эндотелиальной функции на фоне приема правастатина 40 мг в течение 3 мес [32]. Еще в одном исследовании было отмечено значительное улучшение потокзависимой вазодилатации (ПЗВД) и увеличение времени до появления депрессии сегмента ST на ЭКГ более 1 мм во время нагрузочного теста (р < 0,0001) у пациентов с гиперхолестеринемией, стенокардией напряжения и неизмененными коронарными артериями, получавших симвастатин 20 мг/сут, в сравнении с группой плацебо [33].
D. Baller et al. сообщили об улучшении РКК у пациентов с нормальной или малоизмененной КАГ и умеренно повышенными уровнями холестерина (ХС) липопротеидов низкой плотности (ЛПНП) после 6-месячной липидснижающей терапии симвастатином [34]. В двойном слепом плаце-боконтролируемом рандомизированном исследовании у пациентов с МСС, получавших 20 мг аторвастатина, значительно улучшилась эндотелиальная функция [35].
Метформин. Согласно одной из гипотез, резистентность к инсулину, вызывая эндотелиальную дисфункцию, может приводить к ишемии миокарда и повышение чувствительности к инсулину при терапии метформином может способствовать уменьшению выраженности ишемии миокарда [36]. В плацебоконтролируемом исследовании было показано, что метформин улучшает эндотелийзави-симую сосудистую функцию и уменьшает выраженность ишемии по результатам нагрузочного тестирования у женщин с МСС без сахарного диабета [37]. Следует отметить, что улучшение сосудистой функции произошло, несмотря на отсутствие значительных изменений в уровне гликемии или маркеров воспаления [37].
В соответствии с рекомендациями базовое лечение больных стабильной ИБС, к которым относятся и пациенты с МСС, включает назначение антиагрегантов (ацетилсалициловая кислота или клопидогрел), статинов с достижением целевого уровня ХС ЛПНП, а также препаратов, блокирующих активность ренин-ангиотензиновой системы, - ингибиторов АПФ, а при их непереносимости - блокаторов ангиотензиновых рецепторов [1, 2]. Эти же основополагающие принципы профилактики осложнений стабильной ИБС в полной мере относятся и к пациентам с МСС. Однако по сравнению с предыдущими европейскими рекомендациями пациентам с МСС теперь рекомендуют назначать ацетилсалициловую кислоту и статины в обязательном порядке, а не только при гиперлипидемии, как это было ранее [38].
Антиангинальная терапия
При лечении больных с МСС применяются те же принципы, что и в отношении пациентов со стабильной стенокардией, однако следует отметить, что устранение стенокардии и улучшение состояния больных достигаются с большими трудностями, поэтому далеко не всегда удается обеспечить пациентам хорошее качество жизни [2, 14].
Терапия, направленная на устранение ишемических проявлений стенокардии и/или безболевой ишемии миокарда, включает p-блокаторы (ББ), блокаторы кальциевых каналов (БКК), пролонгированные нитраты, ингибитор If-каналов клеток синусового узла (ивабрадин), цитопро-тективные препараты (триметазидин), ингибитор позднего тока ионов натрия (ранолазин) и активатор калиевых каналов (никорандил). Все эти препараты оказывают антиангинальное (антиишемическое) действие, которое было доказано в контролируемых клинических исследованиях, и входят в клинические рекомендации [1,2].
P-блокаторы. Для профилактики приступов стенокардии у пациентов с МСС в качестве препаратов первой линии рекомендуются ББ, а БКК назначают в тех случаях, если ББ недостаточно эффективны, плохо переносятся или противопоказаны.
Р-блокаторы следует включать в стартовую терапию стенокардии, особенно в тех случаях, когда имеются признаки повышенной адренергической активности (повышенная частота сердечных сокращений в покое, быстрый сердечный ритм и/или повышение артериального давления при физической нагрузке). Ранее было показано, что у пациентов с КСХ атенолол и пропранолол снижают частоту ангинальных эпизодов и уменьшают ишемию более эффективно, чем нитраты и БКК [39, 40]. В исследованиях было обнаружено, что небиволол увеличивает высвобождение оксида азота из сосудистого эндотелия и значительно улучшает РКК. Однако антиангинальная эффективность ББ неустойчивая и колеблется от 19 до 60%, что потребовало поиска дополнительных терапевтических вариантов [41].
Блокаторы кальциевых каналов. Результаты применения БКК, таких как верапамил и дилтиазем, в целом противоречивые, и обычно БКК назначаются в качестве альтернативы ББ, особенно у пациентов с сильно изменяющимся болевым порогом стенокардии и/или болью в покое или у пациентов, у которых ББ неэффективны или плохо переносятся. Однако в одном из исследований была отмечена высокая эффективность БКК, связанная с вазодилатацией микрососудов и снижением потребления кислорода миокардом, особенно в тех случаях, когда спазм мелких сосудов являлся одной из причин развития МСС [42]. Предполагается, что выраженное антиспастическое действие БКК в разрешении коронарного спазма объясняет их эффективность при таком варианте течения МСС [43].
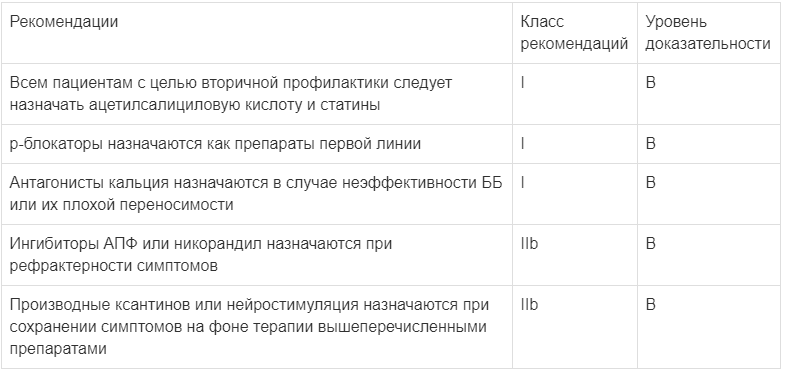
Никорандил - активатор калиевых каналов, который обладает сосудорасширяющими свойствами. Никорандил используется как для купирования, так и для профилактики приступов стенокардии. Недавно был уточнен механизм антиангинального действия этого препарата, который, кроме того, что обладает свойствами, присущими органическим нитратам, также активирует АТФ-зависимые калиевые каналы [44, 45]. Никорандил расширяет коронарные артериолы и вены, воспроизводит защитный эффект ишемического прекондиционирования, уменьшает агрегацию тромбоцитов. Никорандил не вызывает развития толерантности, не влияет на артериальное давление, частоту сердечных сокращений, на проводимость и сократимость миокарда. Следует также отметить, что назначение никорандила пациентам с МСС рекомендуется при недостаточном эффекте ББ, БКК и нитратов длительного действия для предотвращения приступов стенокардии (табл. 2).
Таблица 2.
Алгоритм лечения пациентов с МСС [2]
Эффективность никорандила при длительном применении изучалась в нескольких крупных наблюдательных исследованиях у пациентов с разными формами ИБС. В многоцентровом исследовании JCAD (Japanese Coronary Artery Disease) (средний период наблюдения 2,7 года) изучалось влияние никорандила на отдаленные исходы у 5116 больных стабильной ИБС [46]. В группе никорандила, добавленного к стандартной терапии, в сравнении с группой, получавшей только стандартную терапию, частота всех регистрируемых событий была статистически значимо меньшей, в частности, частота смерти от любых причин была меньше на 35%, смерти от сердечно-сосудистых причин - на 56%, фатального ИМ - на 56%, застойной сердечной недостаточности - на 33% [46].
В исследовании OACIS (Osaka Acute Coronary Insufficiency Study) (n = 1846) у пациентов с острым ИМ с выполненным чрескожным коронарным вмешательством (ЧКВ), которым при выписке из стационара дополнительно назначали никорандил перорально (длительность лечения в среднем 709 дней), риск смерти от любых причин был ниже на 50,5% в сравнении с группой стандартного лечения (р = 0,04) вне зависимости от исхода ЧКВ [47].
Недавно в нашей стране было проведено клиническое исследование КВАЗАР - многоцентровое рандомизированное двойное слепое исследование в параллельных группах по оценке антиангинальной эффективности и безопасности перорального применения препарата никоран-дил под торговым наименованием Кординик (компания ПИК-ФАРМА, Россия) в сравнении с плацебо на фоне базисной терапии ББ метопролола тартратом у пациентов со стабильной стенокардией [48]. Длительность наблюдения составила 6 нед. Половине из 120 пациентов со стабильной стенокардией, рандомизированных в группу никорандила, препарат назначался дополнительно к ранее назначенному метопролола тартрату (50 мг 2 раза в день) вначале в дозе 10 мг 2 раза в сутки, а через 2 нед (визит В2) дозу увеличивали до 20 мг 2 раза в сутки. Визит В6 проводился через 4 нед после визита В2. На этом визите пациент выполнял 2 пробы с дозированной физической нагрузкой - до приема никорандила и через 1,5 ч после его приема.
Переносимость терапии оказалась хорошей. Частота приступов стенокардии у пациентов, принимавших нико-рандил, значимо снизилась к моменту проведения визитов В2 и В6 по отношению к показателям в группе плацебо (р = 0,02), а в группе плацебо она снизилась только к моменту проведения визита В6 по отношению к исходным данным на визите В0 [48]. Частота приема нитратов короткого действия для купирования приступов уменьшилась в обеих группах, но у пациентов, принимавших никорандил, потребность в этих препаратах снизилась в большей степени, а различие с исходным показателем было статистически значимым как на визите В2, так и на визите В6 (р < 0,001).
Через 6 нед приема никорандила наблюдалось статистически значимое увеличение времени до начала приступа стенокардии (р < 0,0001), времени до появления депрессии сегмента ST 1,0 мм (р < 0,005) и времени до развития приступа стенокардии средней интенсивности (р < 0,005). В группе плацебо увеличилось только время до начала приступа стенокардии (р < 0,01), при этом продолжительность нагрузки до появления депрессии сегмента ST 1,0 мм и до развития приступа стенокардии средней интенсивности статистически значимо не изменилась. В подгруппе пациентов, у которых при проведении пробы с дозированной физической нагрузкой регистрировались ишемические изменения сегмента ST на фоне приема исследуемого препарата, при выполнении пробы непосредственно перед очередным его приемом отмечался существенный прирост продолжительности нагрузки до появления ишемических изменений на ЭКГ в сравнении с группой плацебо (р < 0,05), что подтверждает антиишемическое действие никорандила в течение суток при двукратном режиме дозирования [49]. Препарат оказал заметное влияние на качество жизни. В группе никорандила в сравнении с группой плацебо к концу исследования наблюдалась четкая положительная динамика качества жизни и функциональных возможностей [50].
В работе H. Yamabe et al. внутривенное введение ни-корандила во время исследования перфузии миокарда приводило к значительному уменьшению степени тяжести нарушения перфузии у пациентов со стенокардией и почти нормальной КАГ [51]. В рандомизированном контролируемом исследовании 2-недельная терапия никорандилом у пациентов с МСС способствовала значительному улучшению индуцированной физической нагрузкой ишемии миокарда в сравнении с плацебо [52]. Таким образом, отмечен потенциальный эффект никорандила в лечении пациентов с первичной стабильной МСС, но данные о его эффективности при этом синдроме ограничены и требуются дальнейшие исследования.
В последние годы изучаются также дополнительные эффекты никорандила. Недавно было выявлено влияние никорандила на воспроизведение эффекта фармакологического прекондиционирования у больных стабильной ИБС во время проведения планового ЧКВ. В исследование было включено 88 пациентов со стабильной формой ИБС, направленных на плановое ЧКВ. Пациентов разделили на 2 группы - основную (n = 45), в которой назначали нико-рандил (Кординик, компания ПИК-ФАРМА), и группу сравнения (n = 43), в которой проводили стандартную терапию. Никорандил назначался за 2 сут до ЧКВ в дозе 30 мг/сут, за 2 ч до ЧКВ - дополнительно 20 мг внутрь, спустя 6 ч после ЧКВ - 10 мг. Высокочувствительный тропонин как биомаркер необратимого повреждения миокарда оценивался до ЧКВ и через 24 ч после проведения ЧКВ.
Полученные данные свидетельствовали о более выраженном повышении уровня высокочувствительного тропо-нина через 24 ч у пациентов, не принимавших никорандил (117 нг/л), по сравнению с таковым в группе никорандила (73 нг/л) (р = 0,04). Выявлены статистически значимые различия в приросте уровня высокочувствительного тро-понина через 24 ч: в группе сравнения он оказался выше (112 нг/л), чем в группе никорандила (67 нг/л) (р = 0,03). Также в группе никорандила статистически значимо реже наблюдалось повышение уровня тропонина выше верхней границы нормы - в 62% случаев против 85% случаев в группе сравнения (р = 0,03). Изученная схема применения никорандила позволит расширить показания к его назначению в стратегии медикаментозного сопровождения ЧКВ у больных стабильной ИБС [53].
Ивабрадин является специфическим ингибитором If-канала, который действует путем прямого ингибирования активности синоатриального узла. В исследовании A. Villano et al. прием ивабрадина в течение 4 нед в дополнение к обычной антиангинальной терапии способствовал улучшению симптомов у пациентов с МСС, не влияя на РКК и функцию эндотелия [54]. Эти результаты свидетельствуют о клинической пользе ивабрадина независимо от какого-либо положительного влияния на коронарную микрососудистую функцию [54].
Триметазидин является ингибитором фермента 3-кетоацил-коэнзим-А-тиолазы, который ингибирует окислительное фосфорилирование, увеличивает утилизацию глюкозы и выработку АТФ, тем самым ограничивая образование и внеклеточное высвобождение аденозина [55]. В двух небольших исследованиях, в которых изучалось влияние триметазидина у пациентов с ишемией, вызванной физической нагрузкой, и с нормальными коронарными артериями, было показано, что при лечении триметазидином увеличивалась физическая работоспособность и уменьшались частота и продолжительность ангинозных эпизодов [56, 57]. Хотя триметазидин может оказывать благоприятное действие у пациентов с первичной МСС, необходимы дальнейшие исследования [21].
Ранолазин является относительно новым лекарственным средством для лечения стенокардии. Препарат ингибирует поздний ток ионов натрия и таким образом улучшает диастолическую функцию левого желудочка. В одном из исследований при 4-недельном лечении ранолазином улучшались ангинальные симптомы и ишемия миокарда у женщин с МСС [58]. В другом исследовании 4-недельный прием ранолазина в дополнение к обычной антиангиналь-ной терапии способствовал улучшению симптомов у пациентов без влияния на РКК и функцию эндотелия. Хотя механизм этого действия не ясен, ранолазин, по-видимому, может улучшать самочувствие и уменьшать симптоматику у пациентов с МСС [54].
Лекарства и процедуры, связанные с восприятием боли
В качестве патогенетического механизма, лежащего в основе резистентной к терапии МСС, было указано и повышенное восприятие боли. Следовательно, назначение лекарственных средств, влияющих на механизмы, связанные с восприятием или переносимостью боли, может быть еще одним вариантом лечения первичной стабильной МСС (см. табл. 2) [2].
Производные ксантина. Аденозин является одним из основных медиаторов сердечной боли, и предполагают, что его повышенное высвобождение участвует в усилении восприятия боли у пациентов с МСС. Производные ксантина (аминофиллин) оказывают противоболевое воздействие, связанное с блокадой аденозиновых рецепторов. Отмечено, что 3-недельное лечение пероральным аминофилли-ном положительно влияет на порог боли в грудной клетке, вызванной физической нагрузкой. Также продемонстрировано, что аминофиллин оказывает благоприятное влияние на состояние пациентов с МСС, возможно связанное с его способностью перераспределять коронарный кровоток в ишемизированных областях [59].
Имипрамин - один из наиболее широко используемых антидепрессантов, его влияние основано на ингибировании поглощения серотонина и норадреналина. Он также является ингибитором висцеральной боли и поэтому может оказаться полезным в лечении рефрактерной МСС. В проведенных исследованиях имипрамин уменьшал симптомы у пациентов с болью в груди и нормальной КАГ, возможно благодаря висцеральному обезболивающему эффекту [60]. Таким образом, имипрамин в низких дозах может быть препаратом выбора у пациентов с рефрактерной к лечению МСС, но следует учитывать его значительные нежелательные эффекты [60].
Стимуляция спинного мозга использовалась у больных с рефрактерной МСС и приводила к значительному уменьшению боли в груди и улучшению качества жизни у пациентов, нечувствительных ко всем другим видам лечения. Применение устройств для электрической нейромодуляции, таких как аппарат для чрескожной электрической стимуляции нервов, оказалось умеренно успешным в лечении КСХ. Точный механизм действия процедуры не ясен, но существует гипотеза о прямом влиянии стимуляции спинного мозга на тонус сосудов коронарного микроциркуляторного русла, что приводит к усилению коронарного кровотока и нормализации аномальной обработки кортикальной боли [61, 62]. Осложнения, связанные с процедурой, включают образование эпидурального абсцесса, кровотечение и неврологическое повреждение. Это лечение значительно дороже, чем обычные методы, но можно рассматривать его проведение для контроля симптомов и уменьшения частоты госпитализаций у пациентов с множественной лекарственной устойчивостью.
Выше отмечалось, что при лечении МСС, так же как и при лечении других вариантов течения ИБС, необходимо обеспечить оптимальный контроль факторов коронарного риска [1, 2]. Целый ряд направлений терапии, обсуждавшихся в настоящей статье, подразумевают симптоматическое лечение и являются эмпирическими в связи с недостаточным знанием причин рассматриваемого состояния. Результаты клинических исследований сложно обобщить в связи с отсутствием единых критериев включения и немногочисленностью выборок больных, несовершенным дизайном исследований и другими сложностями оценки эффективности лечения МСС [6]. У пациентов с МСС чувствительность симптомов к медикаментозному лечению чрезвычайно вариабельна, поэтому приходится экспериментальным путем, нередко очень долго, подбирать различные комбинации антиангинальной терапии, прежде чем будет получен удовлетворяющий пациента контроль имеющихся симптомов заболевания.
Прогноз
Результаты длительного наблюдения за пациентами со стенокардией на фоне непораженных крупных коронарных артерий оказались противоречивыми. Ранее, по данным проведенных исследований, предполагалось, что у пациентов с МСС средний срок жизни, коронарная заболеваемость и смертность в целом близки к таковым в общей популяции [63, 64]. Например, в исследовании WISE (Women’s Ischemia Syndrome Evaluation) в этой группе больных был зарегистрирован 2,5% ежегодный риск развития неблагоприятных сердечно-сосудистых событий, включая смерть, ИМ, инсульт и сердечную недостаточность [65]. Следует отметить, что в изучавшуюся когорту входили только женщины, и риск повторных госпитализаций, КАГ и затраты были выше в группе с аномальной МРС в сравнении с женщинами с болями, но без ИБС.
По результатам 20-летнего наблюдения, проведенного в Дании и включавшего 17 435 больных с неизмененными коронарными артериями и с необструктивным диффузным поражением коронарных артерий со стенокардией, в этих группах было выявлено 52 и 85% повышение риска крупных сердечно-сосудистых событий (сердечно-сосудистая смертность, госпитализация по поводу ИМ, сердечной недостаточности, инсульта) соответственно и 29 и 52% повышение риска общей смертности соответственно без существенных различий по половому признаку [66]. Ухудшение сердечной функции в исследованиях описывалось довольно редко [63]. Следует отметить, что, хотя коронарные артерии остаются “чистыми”, с клинической точки зрения самочувствие пациентов из-за болевого синдрома является неудовлетворительным, а качество жизни низким [67]. Повышенный риск развития коронарных событий был описан в основном у пациентов с другими многочисленными факторами сердечно-сосудистого риска [68].
Вместе с тем в последнее время МСС уже не рассматривается как абсолютно доброкачественное состояние. Было установлено, что частота сердечно-сосудистых событий близка или даже сопоставима с прогнозом при обструктивных изменениях коронарного русла. В одном из исследований в группе пациентов с МСС и исходной ПЗВД плечевой артерии <4,7% был отмечен достоверно более высокий риск сердечно-сосудистых осложнений в сравнении с группой с ПЗВД >4,7% (р < 0,05) на протяжении 9-18 лет наблюдения [69].
Перспективные исследования
Как отмечалось выше, имеется значительный дефицит клинических контролируемых исследований, посвященных изучению проблемы МСС, что не позволяет дать рекомендации по повышению эффективности лечения этой большой группы пациентов. Для устранения этого пробела недавно было организовано клиническое исследование WARRIOR (Women’s ischemiA tRial to Reduce events In non-ObstRuctive CAD) [70]. В него планируется включить 4422 женщины с признаками и симптомами ишемии миокарда (стабильная стенокардия или ее эквиваленты), но без обструктивных изменений коронарных артерий (т.е. стеноз <50%). Работа финансируется Министерством обороны США, по дизайну это рандомизированное клиническое проспективное слепое исследование в параллельных группах, которое будет проводиться в 50 центрах в США. Предполагается (гипотеза исследования), что интенсивная медицинская терапия снизит риск развития коронарных событий на 20% в сравнении с обычным клиническим лечением.
В качестве первичных конечных точек выбраны: смерть от всех причин; нефатальный ИМ; инсульт/транзиторная ишемическая атака; госпитализация в связи со стенокардией или сердечной недостаточностью. Планируются следующие вторичные точки: качество жизни; сроки возвращения на работу или возобновления выполнения других обязанностей; расходы на диагностику и лечение; стенокардия; сердечно-сосудистая смерть и отдельные компоненты первичной конечной точки.
В основной группе будет проводиться интенсивное медикаментозное вмешательство (высокие дозы аторваста-тина или розувастатина; умеренные дозы лизиноприла или лозартана; ацетилсалициловая кислота, если не противопоказана; применение ингибиторов PCSK9 у пациентов с непереносимостью статинов), консультирование по образу жизни, заполнение опросников по качеству жизни. В группе сравнения будет продолжаться ранее проводимая терапия; будут проводиться консультации по образу жизни и заполнение опросников по качеству жизни. Запланированная длительность исследования 3 года. Исследование WARRIOR должно дать новую информацию по ведению пациентов со стенокардией на фоне необструктивного поражения коронарного русла.
Фокус на повышение осведомленности
В последние годы необструктивной ИБС уделяется всё больше внимания, и для практического кардиолога важно уметь распознать и правильно квалифицировать таких пациентов, даже в отсутствие стенозирующих просвет коронарных артерий атером, и проводить лечение на основе имеющихся симптомов. Эксперты считают, что прекращение или минимизация лечения у таких больных может приводить к развитию неблагоприятных сердечно-сосудистых событий, включая смертельный исход.
Заключение
Когорта больных с первичной стабильной МСС - это пациенты в основном женского пола, со стабильной стенокардией, с положительными результатами нагрузочных тестов и ангиографически нормальными или малоизмененными коронарными артериями. В развитии заболевания могут принимать участие самые разные патофизиологические механизмы. Новые данные способствовали улучшению понимания дисфункции коронарных сосудов и результирующей ишемии миокарда, которые характеризуют МСД у пациентов с МСС. Несмотря на то что ряд препаратов, включая антиангинальные, могут облегчать симптомы, у многих пациентов сохраняется клиническая симптоматика, плохое качество жизни, и лечение остается сложной задачей. Прогноз у больных с МСС, по последним данным, не такой благоприятный, как считалось ранее, что делает актуальным поиск новых методов диагностики и лечения.
Отдел ангиологии Института клинической кардиологии им. А.Л. Мясникова ФГБУ “НМИЦ кардиологии” МЗ РФ, Москва.
Юрий Александрович Карпов - профессор, рук. отдела.
Галина Николаевна Соболева - докт. мед. наук, вед. науч. сотр.
Елена Александровна Ерпылова - аспирант.
Список литературы
1. Российское кардиологическое общество; Национальное общество по изучению атеросклероза; Национальное общество по атеротромбозу. Клинические рекомендации. Стабильная ишемическая болезнь сердца 2016. МКБ 10: I20.1/I20.8/I20.9/ I25.0/I25.1/I25.2/I25.5/I25.6/I25.8/I25.9. Год утверждения: 2016 (пересмотр каждые 3 года).
2. Task Force Members; Montalescot G, Sechtem U, Achenbach S, Andreotti F, Arden C, Budaj A, Bugiardini R, Crea F, Cuisset T, Di Mario C, Ferreira JR, Gersh BJ, Gitt AK, Hulot JS, Marx N, Opie LH, Pfisterer M, Prescott E, Ruschitzka F, Sabate M, Senior R, Taggart DP, van der Wall EE, Vrints CJ; ESC Committee for Practice Guidelines; Zamorano JL, Achenbach S, Baumgartner H, Bax JJ, Bueno H, Dean V, Deaton C, Erol C, Fagard R, Ferrari R, Hasdai D, Hoes AW, Kirchhof P, Knuuti J, Kolh P, Lancellotti P, Lin-hart A, Nihoyannopoulos P, Piepoli MF, Ponikowski P, Sirnes PA, Tamargo JL, Tendera M, Torbicki A, Wijns W, Windecker S; Document Reviewers; Knuuti J, Valgimigli M, Bueno H, Claeys MJ, Don-ner-Banzhoff N, Erol C, Frank H, Funck-Brentano C, Gaemperli O, Gonzalez-Juanatey JR, Hamilos M, Hasdai D, Husted S, James SK, Kervinen K, Kolh P, Kristensen SD, Lancellotti P, Maggioni AP, Piepoli MF, Pries AR, Romeo F, Ryden L, Simoons ML, Sirnes PA, Steg PG, Timmis A, Wijns W, Windecker S, Yildirir A, Zamorano JL. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. European Heart Journal 2013 Oct;34(38):2949-3003.
3. Федеральная служба государственной статистики. Здравоохранение в России. Статистический сборник 2017. М., 2017.
4. Humphries KH, Pu A, Gao M, Carere RG, Pilote L. Angina with “normal” coronary arteries: sex differences in outcomes. American Heart Journal 2008 Feb;155(2):375-81.
5. Ouellette M, Loftier AI, Beller GA, Workman VK, Holland E, Bourque JM. Clinical characteristics, sex differences, and outcomes in patients with normal or near normal coronary arteries, non obstructive or obstructive coronary artery disease. Journal of American Heart Association 2018 May;7(10). pii: e007965. doi: 10.1161/JAHA.117.007965.
6. Proudfit WL, Shirey EK, Sones FM Jr. Selective cine coronary arteriography. Correlation with clinical findings in 1,000 patients. Circulation 1966 Jun;33(6):901-10.
7. Sandler KM, McNaughton CD, Presley MA, Williams JR. Incidence and management of mild coronary atherosclerotic disease diagnosed with coronary CTA in the emergency department. Emergency Medicine (Los Angeles) 2015;5:6.
8. Kemp HG, Kronmal RA, Vliestra RE, Frye RL. Seven year survival of patients with normal or near normal coronary arteriograms. A CASS registry study. Journal of the American College of Cardiology 1986;7:479-83.
9. Cannon RO 3rd, Epstein SE. ‘Microvascular angina’ as a cause of chest pain with angiographically normal coronary arteries. The American Journal of Cardiology 1988 Jun;61(15):1338-43.
10. Lanza GA, De Vita A, Kaski JC. ‘Primary’ microvascular angina: clinical characteristics, pathogenesis and management. Journal of Interventional Cardiology 2018 Sep;13(3):108-11.
11. Crea F, Camici PG, Bairey Merz CN. Coronary microvascular dysfunction: an update. European Heart Journal 2014 May;35(17):1101-11.
12. Сергиенко В.Б., Саютина Е.В., Самойленко Л.Е., Самко А.Н., Першуков И.В., Левицкий И.В., Соболева Г.Н., Карпов Ю.А. Роль дисфункции эндотелия в развитии ишемии миокарда у больных ишемической болезнью сердца с неизмененными и малоизмененными коронарными артериями. Кардиология 1999;39(1):25-30.
13. Lanza GA, Crea F. Primary coronary microvascular dysfunction clinical presentation, pathophysiology, and management. Circulation 2010 Jun;121(21):2317-25.
14. Villano A, Lanza GA, Crea F. Microvascular angina: prevalence, pathophysiology and therapy. Journal of Cardiovascular Medicine (Hagerstown, Md) 2018 Feb;19(Suppl 1):e36-9.
15. Camici PG, Crea F. Coronary microvascular dysfunction. The New England Journal of Medicine 2007 Feb;356(8):830-40.
16. Patel MB, Bui LP, Kirkeeide RL, Gould KL. Imaging microvascular dysfunction and mechanisms for female-male differences in CAD. JACC. Cardiovascular Imaging 2016 Apr;9(4):465-82.
17. Cannon RO, Watson RM, Rosing DR, Epstein SE. Angina caused by reduced vasodilator reserve of the small coronary arteries. Journal of the American College of Cardiology 1983 Jun;1(6):1359-73.
18. Kaski JC, Valenzuela Garcia LF. Therapeutic options for the management of patients with cardiac syndrome X. European Heart Journal 2001 Feb;22(4):283-93.
19. Lanza GA, Buffon A, Sestito A, Natale L, Sgueglia GA, Galiuto L, Infusino F, Mariani L, Centola A, Crea F. Relation between stress-induced myocardial perfusion defects on cardiovascular magnetic resonance and coronary microvascular dysfunction in patients with cardiac syndrome X. Journal of the American College of Cardiology 2008 Jan;51(4):466-72.
20. Rodes-Cabau J, Gutierrez M, Courtis J, Larose E, Dery JP, Cote M, Nguyen CM, Gleeton O, Proulx G, Roy L, Noёl B, Barbeau G, De La-rochelliere R, Rinfret S, Bertrand OF. Importance of diffuse atherosclerosis in the functional evaluation of coronary stenosis in the proximal-mid segment of a coronary artery by myocardial fractional flow reserve measurements. The American Journal of Cardiology 2011 Aug;108(4):483-90.
21. Ziadi MC, Dekemp RA, Williams KA, Guo A, Chow BJ, Renaud JM, Ruddy TD, Sarveswaran N, Tee RE, Beanlands RS. Impaired myocardial flow reserve on rubidium-82 positron emission tomography imaging predicts adverse outcomes in patients assessed for myocardial ischemia. Journal of the American College of Cardiology 2011 Aug;58(7):740-8.
22. Schelbert HR. Positron emission tomography measurements of myocardial blood flow: assessing coronary circulatory function and clinical implications. Heart 2012 Apr;98(7):592-600.
23. Marinescu MA, Loffler AI, Ouellette M, Smith L, Kramer CM, Bourque JM. Coronary microvascular dysfunction, microvascular angina, and treatment strategies. JACC. Cardiovascular Imaging 2015 Feb;8(2):210-20.
24. Соболева Г.Н., Гаман С.А., Терновой С.К., Шария М.А., Карпова И.Е., Карпов Ю.А. Нарушение перфузии миокарда левого желудочка при неизмененных коронарных артериях по данным объемной компьютерной томографии, совмещенной с фармакологической пробой аденозинтрифосфатом. Russian Electronic Journal of Radiology 2018;8(3):273-8.
25. Raitakari OT, Adams MR, McCredie RJ, Griffiths KA, Celermajer DS. Arterial endothelial dysfunction related to passive smoking is potentially reversible in healthy young adults. Annals of Internal Medicine 1999 Apr;130(7):578-81.
26. Gokce N, Vita JA, McDonnell M, Forse AR, Istfan N, Stoeckl M, Li-pinska I, Keaney JF Jr, Apovian CM. Effect of medical and surgical weight loss on endothelial vasomotor function in obese patients. The American Journal of Cardiology 2005 Jan;95(2):266-8.
27. Klonizakis M, Alkhatib A, Middleton G, Smith MF. Mediterranean diet- and exercise-induced improvement in age-dependent vascular activity. Clinical Science (London, England 1979) 2013 May;124(9):579-87.
28. Eriksson BE, Tyni-Lenne R, Svedenhag J, Hallin R, Jensen-Ur-stad K, Jensen-Urstad M, Bergman K, Selven C. Physical training in syndrome X: physical training counteracts deconditioning and pain in syndrome X. Journal of the American College of Cardiology 2000 Nov;36(5):1619-25.
29. Lim TK, Choy AJ, Khan F, Belch JJ, Struthers AD, Lang CC. Therapeutic development in cardiac syndrome X: a need to target the underlying pathophysiology. Cardiovascular Therapeutic 2009 Spring;27(1):49-8.
30. Kaski JC, Rosano G, Gavrielides S, Chen L. Effects of angiotensin-converting enzyme inhibition on exercise-induced angina and ST segment depression in patients with microvascular angina. Journal of the American College of Cardiology 1994 Mar;23(3):652-7.
31. Chen JW, Hsu NW, Wu TC, Lin SJ, Chang MS. Long-term angiotensin-converting enzyme inhibition reduces plasma asymmetric di-methylarginine and improves endothelial nitric oxide bioavailability and coronary microvascular function in patients with syndrome X. The American Journal of Cardiology 2002 Nov 1;90(9):974-82.
32. Kayikcioglu M, Paysin A, Yavuzgil O, Kultursay H, Can LH, Soydan I. Benefits of statin treatment in cardiac syndrome X. European Heart Journal 2003 Nov;24(22):1999-2005.
33. Fabian E, Varga A, Picano E, Vajo Z, Ronaszeki A, Csanady M. Effect of simvastatin on endothelial function in cardiac syndrome X patients. The American Journal of Cardiology 2004 Sep;94(5):652-55.
34. Baller D, Notohamiprodjo G, Gleichmann U, Holzinger J, Weise R, Lehmann J. Improvement in coronary flow reserve determined by positron emission tomography after 6 months of cholesterol-lowering therapy in patients with early stages of coronary atherosclerosis. Circulation 1999 Jun 8;99(22):2871-5.
35. Pizzi C, Manfrini O, Fontana F, Bugiardini R. Angiotensin-converting enzyme inhibitors and 3-hydroxy-3-methylglutaryl coenzyme A reductase in cardiac syndrome X: role of superoxide dismutase activity. Circulation 2004 Jan;109(1):53-8.
36. Mather KJ, Verma S, Anderson TJ. Improved endothelial function with metformin in type 2 diabetes mellitus. Journal of the American College of Cardiology 2001 Apr;37(5):1344-50.
37. Jadhav S, Ferrell W, Greer IA, Petrie JR, Cobbe SM, Sattar N. Effects of metformin on microvascular function and exercise tolerance in women with angina and normal coronary arteries: a randomized, double-blind, placebo-controlled study. Journal of the American College of Cardiology 2006 Sep;48(3):956-63.
38. Fox K, Garcia MA, Ardissino D, Buszman P, Camici PG, Crea F, Daly C, De Backer G, Hjemdahl P, Lopez-Sendon J, Marco J, Mo-rais J, Pepper J, Sechtem U, Simoons M, Thygesen K, Priori SG, Blanc JJ, Budaj A, Camm J, Dean V, Deckers J, Dickstein K, Le-kakis J, McGregor K, Metra M, Morais J, Osterspey A, Tamargo J, Zamorano JL; Task Force on the Management of Stable Angina Pectoris of the European Society of Cardiology; ESC Committee for Practice Guidelines (CPG). Guidelines on the management of stable angina pectoris: executive summary. The Task Force on the Management of Stable Angina Pectoris of the European Society of Cardiology. European Heart Journal 2006 Jun;27(11):1341-81.
39. Lanza GA, Colonna G, Pasceri V, Maseri A. Atenolol versus am-lodipine versus isosorbide-5-mononitrate on anginal symptoms in syndrome X. The American Journal of Cardiology 1999 Oct;84(7):854-6, A8.
40. Bugiardini R, Borghi A, Biagetti L, Puddu P Comparison of verapamil versus propranolol therapy in syndrome X. The American Journal of Cardiology 1989 Feb;63(5):286-90.
41. Togni M, Vigorito F, Windecker S, Abrecht L, Wenaweser P, Cook S, Billinger M, Meier B, Hess OM. Does the beta-blocker nebivolol increase coronary flow reserve? Cardiovascular Drugs and Therapy 2007 Apr;21(2):99-108.
42. Suzuki H, Matsubara H, Koba S, Murakami M, Takeyama Y, Katagi-ri T. Clinical characteristics and follow-up in patients with microvascular angina. Circulation Journal 2002 Jul;66(7):691-5.
43. Masumoto A, Mohri M, Takeshita A. Three-year follow-up of the Japanese patients with microvascular angina attributable to coronary microvascular spasm. International Journal of Cardiology 2001 Dec;81(2-3):151-6.
44. Kinoshita M, Sakai K. Pharmacology and therapeutic effects of nico-randil. Cardiovascular Drugs and Therapy 1990 Aug;4(4):1075-88.
45. Карпов Ю.А. Хроническая ишемическая болезнь сердца: новости лечения. Consilium Medicum 2016;18(1):38-44.
46. Horinaka S, Yabe A, Yagi H, Ishimitsu T, Yamazaki T, Suzuki S, Kohro T, Nagai R; JCAD Study Investigators. Effects of nicorandil on cardiovascular events in patients with coronary artery disease in the Japanese Coronary Artery Disease (JCAD) study. Circulation Journal 2010 Mar;74(3):503-9.
47. Sakata Y Nakatani D, Shimizu M, Suna S, Usami M, Matsumoto S, Hara M, Sumitsuji S, Kawano S, Iwakura K, Hamasaki T, Sato H, Nanto S, Hori M, Komuro I. Oral treatment with nicorandil at discharge is associated with reduced mortality after acute myocardial infarction. Journal of Cardiology 2012 Jan;59(1):14-21.
48. Марцевич С.Ю., Кутишенко Н.П., Деев А.Д. от имени участников исследования КВАЗАР Сравнительная оценка анти-ангинальной эффективности и безопасности препарата ни-корандил на фоне базисной терапии Р-адреноблокаторами у больных ишемической болезнью сердца со стабильной стенокардией. Кардиология 2016;56(10):30-4.
49. Воронина В.П., Марцевич С.Ю., Кутишенко Н.П., Деев А.Д. от имени участников исследования КВАЗАР. Оценка антиишемического и антиангинального эффектов никорандила с помощью нагрузочных тестов на тредмиле в рамках исследования КВАЗАР Российский кардиологический журнал 2017;22(3):97-103.
50. Марцевич С.Ю., Кутишенко Н.П., Деев А.Д. от имени участников исследования КВАЗАР Изучение влияния никорандила на качество жизни пациентов со стабильной стенокардией в рамках исследования “КВАЗАР”. Рациональная фармакотерапия в кардиологии 2016;12(6):654-60.
51. Yamabe H, Namura H, Yano T, Fujita H, Kim S, Iwahashi M, Mae-da K, Yokoyama M. Effect of nicorandil on abnormal coronary flow reserve assessed by exercise 201Tl scintigraphy in patients with angina pectoris and nearly normal coronary arteriograms. Cardiovascular Drugs and Therapy 1995 Dec;9(6):755-61.
52. Chen JW, Lee WL, Hsu NW, Lin SJ, Ting CT, Wang SP, Chang MS. Effects of short-term treatment of nicorandil on exercise-induced myocardial ischemia and abnormal cardiac autonomic activity in microvascular angina. The American Journal of Cardiology 1997;80:32-8.
53. Гостищев РВ., Соболева Г.Н., Самко А.Н., Минасян А.А. Реализация кардиопротекции никорандилом от перипроцедурного повреждения у больных стабильной ишемической болезнью сердца при плановых чрескожных коронарных вмешательствах. Consilium Medicum 2018;20(5):61-5.
54. Villano A, Di Franco A, Nerla R, Sestito A, Tarzia P, Lamendola P, Di Monaco A, Sarullo FM, Lanza GA, Crea F. Effects of ivabradine and ranolazine in patients with microvascular angina pectoris. The American Journal of Cardiology 2013 Jul;112(1):8-13.
55. Allibardi S, Chierchia SL, Margonato V, Merati G, Neri G, DellAnto-nio G, Samaja M. Effects of trimetazidine on metabolic and functional recovery of postischemic rat hearts. Cardiovascular Drugs and Therapy 1998 Dec;12(6):543-9.
56. Rogacka D, Guzik P, Wykretowicz A, Rzezniczak J, Dziarmaga M, Wysocki H. Effects of trimetazidine on clinical symptoms and tolerance of exercise of patients with syndrome X: a preliminary study. Coronary Artery Disease 2000 Mar;11(2):171-7.
57. Nalbantgil S, Altintiğ A, Yilmaz H, Nalbantgil I I, Onder R. The effect of trimetazidine in the treatment of microvascular angina. The International Journal of Angiology 1999 Jan;8(1):40-3.
58. Mehta PK, Goykhman P, Thomson LE, Shufelt C, Wei J, Yang Y Gill E, Minissian M, Shaw LJ, Slomka PJ, Slivka M, Berman DS, Bairey Merz CN. Ranolazine improves angina in women with evidence of myocardial ischemia but no obstructive coronary artery disease. JACC. Cardiovascular Imaging 2011 May;4(5):514-22.
59. Elliott PM, Krzyzowska-Dickinson K, Calvino R, Hann C, Kaski JC. Effect of oral aminophylline in patients with angina and normal coronary arteriograms (cardiac syndrome X). Heart 1997 Jun;77(6):523-6.
60. Cox ID, Hann CM, Kaski JC. Low dose imipramine improves chest pain but not quality of life in patients with angina and normal coronary angiograms. European Heart Journal 1998 Feb;19(2):250-4.
61. Latif OA, Nedeljkovic SS, Stevenson LW. Spinal cord stimulation for chronic intractable angina pectoris: a unified theory on its mechanism. Clinical Cardiology 2001 Aug;24(8):533-41.
62. Sestito A, Lanza GA, Le Pera D, De Armas L, Sgueglia GA, Infusi-no F, Miliucci R, Tonali PA, Crea F, Valeriani M. Spinal cord stimulation normalizes abnormal cortical pain processing in patients with cardiac syndrome X. Pain 2008 Sep;139(1):82-9.
63. Kaski JC, Elliott PM. Angina pectoris and normal coronary arteriograms: clinical presentation and hemodynamic characteristics. The American Journal of Cardiology 1995 Nov;76(13):35D-42D.
64. Schroeder JS. Emerging therapies for angina: new modalities may offer additional clinical options. Managed Care Interface 2004 Apr;17(4):45-52.
65. Johnson BD, Shaw LJ, Buchthal SD, Bairey Merz CN, Kim HW, Scott KN, Doyle M, Olson MB, Pepine CJ, den Hollander J, Sharaf B, Rogers WJ, Mankad S, Forder JR, Kelsey SF, Pohost GM; National Institutes of Health-National Heart, Lung, and Blood Institute. Prognosis in women with myocardial ischemia in the absence of obstructive coronary disease: results from the National Institutes of Health-National Heart, Lung, and Blood Institute-sponsored Women’s Ischemia Syndrome Evaluation (WISE). Circulation 2004 Jun;109(24):2993-9.
66. Jespersen L, Hvelplund A, Abildstrom SZ, Pedersen F, Galatius S, Madsen JK, J0rgensen E, Kelbӕk H, Prescott E. Stable angina pectoris with no obstructive coronary artery disease is associated with increased risks of major adverse cardiovascular events. European Heart Journal 2012 Mar;33(6):734-44.
67. Tavella R, Cutri N, Tucker G, Adams R, Spertus J, Beltrame JF. Natural history of patients with insignificant coronary artery disease. European Heart Journal. Quality of Care & Clinical Outcomes 2016 Apr 1;2(2):117-24.
68. Lichtlen PR, Bargheer K, Wenzlaff P Long-term prognosis of patients with anginalike chest pain and normal coronary angiographic findings. Journal of the American College of Cardiology 1995 Apr;25(5):1013-8.
69. Соболева Г.Н., Федулов В.К., Самко А.Н., Левицкий И.В., Рогоза А.Н., Балахонова Т.В., Карпов Ю.А. Прогностическое значение дисфункции эндотелия коронарных и плечевой артерии, традиционных факторов риска в развитии сердечно-сосудистых осложнений у пациентов с микрососудистой стенокардией. Российский кардиологический журнал 2017;22(3):54-8.
70. Women’s ischemiA tRial to Reduce events In non-ObstRuctive CAD (WARRIOR).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)



 Группой COVADIS было предложено выставлять окончательный диагноз МСС после верификации МСД при помощи определения резерва коронарного кровотока (РКК) [10]. Исследование коронарной микрососудистой функции можно проводить как инвазивными, так и неинвазивными методами.
Группой COVADIS было предложено выставлять окончательный диагноз МСС после верификации МСД при помощи определения резерва коронарного кровотока (РКК) [10]. Исследование коронарной микрососудистой функции можно проводить как инвазивными, так и неинвазивными методами.  Эффективность никорандила при длительном применении изучалась в нескольких крупных наблюдательных исследованиях у пациентов с разными формами ИБС. В многоцентровом исследовании JCAD (Japanese Coronary Artery Disease) (средний период наблюдения 2,7 года) изучалось влияние никорандила на отдаленные исходы у 5116 больных стабильной ИБС [46]. В группе никорандила, добавленного к стандартной терапии, в сравнении с группой, получавшей только стандартную терапию, частота всех регистрируемых событий была статистически значимо меньшей, в частности, частота смерти от любых причин была меньше на 35%, смерти от сердечно-сосудистых причин - на 56%, фатального ИМ - на 56%, застойной сердечной недостаточности - на 33% [46].
Эффективность никорандила при длительном применении изучалась в нескольких крупных наблюдательных исследованиях у пациентов с разными формами ИБС. В многоцентровом исследовании JCAD (Japanese Coronary Artery Disease) (средний период наблюдения 2,7 года) изучалось влияние никорандила на отдаленные исходы у 5116 больных стабильной ИБС [46]. В группе никорандила, добавленного к стандартной терапии, в сравнении с группой, получавшей только стандартную терапию, частота всех регистрируемых событий была статистически значимо меньшей, в частности, частота смерти от любых причин была меньше на 35%, смерти от сердечно-сосудистых причин - на 56%, фатального ИМ - на 56%, застойной сердечной недостаточности - на 33% [46]. 
