Возможности «ремаксола» для профилактики токсических гепатитов при химиотерапии онкологических больных
Статьи
Опубликовано в журнале:
« Вопросы онкологии » 2013, Том 59, №3
ВТ. Черенков, А.Б. Петров, Т.М. Васильева, ММ. Строженков
ФГБОУ ВПО «Новгородский государственный университет им. Ярослава Мудрого»,
ГОБУЗ «Областной клинический онкологический диспансер», Великий Новгород
Эффективность планируемой полихимиотерапии (ПХТ) онкологических больных зависит от функционального состояния печени. Изучено применение ремаксола у 100 больных с распространенными формами рака (включая рак молочной железы) в профилактическом режиме в сравнении с контрольной группой (100 больных, группой эссенциале (40 больных) и в процессе ПХТ.
Показано, что ремаксол в сравнении с контрольной группой позволяет уменьшить частоту лекарственного токсического гепатита на 30±3,7% и на 6,5±2,9% в сравнении с группой больных, получавших эссенциале.
Ключевые слова: полихимиотерапия, ремаксол, снижение частоты токсических гепатитов
Больные с распространенными формами рака, как правило, имеют значительное угнетение иммунного статуса, анемию, интоксикацию и снижение функций печени. Страдает перекисное окисление липидов, развивается тканевая гипоксия [1]. В результате, проведение ПХТ с высокой интоксикацией остается во многих аспектах нерешенной проблемой. Требуется поиск препаратов, направленных на восстановление органов и систем, участвующих в детоксикации.
Одной из основных причин структурно-функциональных нарушений гепатоцитов является синдром эндотоксикоза, развивающийся в результате опухолевой интоксикации, присоединяющихся бактериальных и вирусных инфекций, а также массивного лизиса опухолевой ткани в ответ на введение противоопухолевых препаратов. Цитостатики могут во много раз уменьшать возможность выведения вредных для печени веществ. В этих условиях противоопухолевые агенты могут оказать кумулятивное токсическое действие на её функциональное состояние: по сборной статистике, в 15% [5,6]. Более того, повышение активности трансаминаз I-II степени в зависимости от типа химиопрепаратов констатируется чаще, чем в 20% случаев. [4]. Существенно, что повышение уровня билирубина (общего и непрямого) может наблюдаться без повышения активности трансаминаз. По мнению многих авторов, почти все химиопрепараты вызывают токсическую нагрузку на печень. Цисплатин приводит к возникновению тяжелых осложнений функции печени и почек [2], лечение которых занимает до 2-3 мес.
Одним из перспективных препаратов, улучшающих энергетическое обеспечение печени и оказывающих антиоксидантный эффект и детоксикацию, является ремаксол, что доказано в ряде доклинических и клинических исследований [3, 8].
Напомним, что ремаксол - это инфузионный раствор, ускоряющий переход анаэробных процессов в аэробные, улучшающий энергетическое обеспечение гепатоцитов (синтез макроэргов), повышающий устойчивость мембран гепатоцитов к перекисному окислению липидов и активность ферментов антиоксидантной защиты. Препарат снижает цитолиз, что проявляется в снижении индикаторных ферментов: аспартатаминотрансфераз, аланинаминотрансфераз. Ремаксол способствует снижению билирубина и его фракций, улучшает экскрецию прямого билирубина в желчь. Снижает активность экскреторных ферментов гепатоцитов - щелочной фосфатазы и гамма-глютамилтранспептидазы, способствует окислению холестерина в желчные кислоты.
Состав ремаксола: янтарная кислота, рибоксин, никотинамид, метионин, N-метилглюкамин, натрия хлорид, магния хлорид, калия хлорид, гидроокись натрия.
Янтарная кислота, ее соли и эфиры являются универсальными внутриклеточными метаболитами, выполняя по отношению к циклу Кребса каталитическую функцию, снижая содержание других медиаторов цикла, накапливающихся на ранних стадиях гипоксии. Никотинамид (НА) активирует NAD-зависимые ферменты клеток, в том числе, антиоксидантные системы убихиноновых оксиредуктаз, защищающие мембраны клеток от разрушения радикальными частицами. Свойством усиления синтеза макроэргических молекул обладает активный компонент ремаксола - рибоксин, представляющий собой производное пурина—предшественника АТФ. Антиоксидантное действие инозина (рибоксина) реализуется за счет активации синтеза NAD в митохондриях из никотинамида, где рибоксин выступает в качестве донора рибозы. Липотропный эффект метионина способствует синтезу холина, с недостаточным образованием которого связано нарушение синтеза фосфолипидов. Путем метилирования метионин обезвреживает токсичные продукты.
Цель настоящего исследования—провести оценку клинической и экономической эффективности ремаксола для профилактики токсических гепатитов в сравнении с контрольной группой и эссенциале в процессе ПХТ у онкологических больных.
Методы и дизайн клинического исследования
В ходе исследования сформированы три группы пациентов: первая (основная) группа получала «Ремаксол» до введения химиопрепаратов (100 пациентов); вторая группа (контрольная)—ретроспективная, не получающая гепатопротекторы (100 пациентов); третья группа (сравнения) получала эссенциале до введения химиопрепаратов (40 человек).
Пациенты включались в исследование после установленного диагноза злокачественного новообразования (морфологической верификации) и планирования курса химиотерапии. Для профилактики токсического поражения печени пациент получали либо ремаксол, либо эссенциале; в контрольной группе пациентам гепатопротекторы не назначались.
Схемы и дозы применения препарата для профилатики токсического гепатита.
Курс лечения:
1 группа (основная)—ремаксол в/в капельно по 400 мл х 1 раз в сутки в течение 5 дней до введения химиотерапев-тических препаратов и ежедневно вместе с курсом ПХТ;
2 группа (сравнения)—эссенциале в/в капельно по 2 ампулы (10 мл) или в тяжелых случаях — 2-4 ампулы (10-20 мл) в день в течение 5 дней до введения химио-терапевтических препаратов и ежедневно вместе с курсом ПХТ;
3 группа—курс химиотерапии без гепатопротектора.
Критерии включения:
1. Планируемый курс ПХТ при установленном диагнозе злокачественного новообразования (подтвержденный мор фологическим исследованием) следующих локализаций:
а) Колоректальный рак (стадия IIIa-IV),
б) Рак молочной железы (стадия IIb-IV),
с) Рак яичников (II-IV стадия),
д) Рак легкого (IIb-IIIb стадии).
2. Возраст от 40 до 75 лет.
3. Пол любой.
4. Пациенты, которые могли, по мнению исследователя, соблюдать протокол в течение необходимого времени.
Критерии исключения:
1 Общее тяжелое состояние больных (менее 60% по Карновскому);
2 Сосудистые поражения мозга при синдроме полиорганной недостаточности;
3 Острые и подострые формы инфаркта миокарда, нарушение функций сердца, аритмия;
4 Острые вирусные и респираторные заболевания;
5 Тяжелые системные заболевания: декомпенсированный сахарный диабет, гипотиреоз, хроническая сердечная, легочная, почечная недостаточности, цирроз печени;
7 Беременность, лактация;
8 Наличие у больных ВИЧ-инфекции, сифилиса, вирусных гепатитов, туберкулеза;
9 Пациенты, получающие другие гепатопротекторы, должны были завершить прием данных препаратов не ме нее чем за три дня до включения в исследование;
10.Пациенты, имеющие алкогольную или наркотическую зависимость в анамнезе;
11.Реакция гиперчувствительности на исследуемый препарат или его составляющие в анамнезе;
12.Психические и аутоиммунные заболевания.
За шесть дней до проведения химиотерапии оценивалось общее состояние пациента по критериям включения и исключения;
а) Клинический анализ крови (гемоглобин, эритроци ты, цветной показатель, гематокрит, тромбоциты, лейко циты, миелоциты, палочкоядерные нейтрофилы, сегменто- ядерные нейтрофилы, эозинофилы, базофилы, лимфоциты, моноциты, СОЭ);
б) Биохимический анализ крови (общий белок, альбумин, холестерин, билирубин общий, билирубин прямой, билирубин непрямой, аспартатаминотрансфераза (ACT), аланинаминотрансфераза (АЛТ), общая лактатдегидрогеназа (ЛДГ), щелочная фосфатаза (ЩФ), гамма-глутамилтранспептидаза (ГГТП));
в) Показатели эндотоксикоза: лейкоцитарная формула крови, лейкоцитарный индекс интоксикации.
Полихимиотерапия рака легкого проводилось по схеме ЕР (1,3,5 дни):
Этопозид 120 мг/ м2
Цисплатин 60 мг/м2
Полихимиотерапия рака яичников проводилось по схеме САР (вариант 1)
Циклофосфан 800-1000 мг/м2 Введение всех препаратов
Адриабластин 40-50 мг/м2 в один день
Платидиам 80 мг/м2
В случае противопоказаний для варианта 1—лечение по схеме СР (вариант 2)
Циклофосфан 1000 мг/м2 Введение всех препаратов
Платидиам 100 мг/м2 в один день
Полихимиотерапия рака кишечника проводилась по схеме Мейо (вариант 1)
Лейковорин 20 мг/м2 5 дней 5ФУ 425 мг/м2
Полихимиотерапия рака кишечника проводилась по схеме FOLFOX4 (вариант 2)
Оксалиплатин 85 мг/м2 1 день
Лейковорин 200 мг/м2 1,2 день
5ФУ 200 мг/м2 в/в струйно1,2 день + 5ФУ 600 мг/м2 в/в кап в течение 22 часов 1,2 день
Полихимиотерапия рака молочной железы (РМЖ) проводилась по схеме CAF введение всех препаратов в один день
Циклофосфан 500 мг/м2
Адриабластин 50 мг/м2
5ФУ 500 мг/м2
Оценка эффективности терапии
Степень выраженности токсичности химиотерапии оценивали по рекомендациям ВОЗ и Международного противоракового союза для учета токсичности на фоне введения исследуемого препарата с оценкой таких параметров, как:
а) динамика показателей ферментемии (ACT, АЛТ, ще лочная фосфатаза, ГГТП, ЛДГ);
б) динамика показателей пигментного обмена (общий билирубин, прямой и непрямой билирубин);
в) наличие/отсутствие холестаза (ГГТП, щелочная фосфотаза, холестерин);
г) наличие/отсутствие нарушения белково-синтетической функции печени (альбумин, общий белок);
д)динамика показателей эндотоксикоза: лейкоцитарная формула крови, лейкоцитарный индекс интоксикации, уровень С-реактивного белка.
Оценку параметров эффективности проводили:
На 6-й день исследования:
Клинический, биохимический анализ крови, анализ крови на эндотоксикоз;
Наличие или отсутствие нежелательных реакций;
Степень выраженности токсичности химиотерапии (рекомендации ВОЗ и Международного противоракового союза);
На 11-й день исследования:
Клинический, биохимический анализ крови, анализ крови на эндотоксикоз;
Степень выраженности токсичности химиотерапии (рекомендации ВОЗ и Международного противоракового союза).
Результаты исследования и их обсуждение
Всего, как отмечалось, в исследование включено 240 пациентов: 100 пациентов в основной группе (ремаксол), 100 человек в контрольной группе и 40 пациентов в группе сравнения (эссенциале). Сравнительный анализ клинико-лабораторных показателей в 1 группе показал, что у 89 больных все клинико-лабораторные показатели в процессе ПХТ находились в пределах нормы (у 9 пациентов, бывшие высокими показатели: ЛИИ, билирубина, холестерина и/ или АЛТ/ACT, нормализовались). У 11 больных (11,0±2,6%) показатели АЛТ/ACT или билирубина после ПХТ несколько повысились (I степень). Однако, во всех этих случаях лечение удалось провести без снижения дозы химиопрепа-ратов и перерыва в терапии. Оценка результатов представлена в табл. 1.
Таблица 1.
Результаты оценки эффективности и безопасности терапии ремаксол ом на завершающем этапе (11 день исследования)
| Эффективность | Переносимость |
|---|
| Оценка | Число б-х | Оценка | Число б-х |
|---|
| Отличная | 44 | Отличная | 52 |
| Хорошая | 45 | Хорошая | 48 |
| Удовлетворительная | 9 | Удовлетворительная | - |
| Неудовлетворительная | 2 | Неудовлетворительная | - |
| Затрудняется ответить | - | Затрудняется ответить | - |
Детальный анализ отдельных случаев показал, что у большинства больных РМЖ и раком яичников IV стадии (получавших доксору-бицин и цисплатин) с генерализацией опухолевого процесса, поступивших с интоксикацией, ЛИИ выше нормы, высокой СОЭ (более 50 мм/ час), но сохраняющейся в норме АЛТ/АСТ до начала лечения после терапии активность АЛТ повысилась выше допустимого критерия максимально в 1,4 раза. В одном случае лечение проводилось на фоне рожистого воспаления послеоперационного рубца после радикальной мастэк-томии, что, естественно, привело к повышению показателей АЛТ/АСТ. В то же время, в контрольной группе (2-я группа) токсический гепатит (1 степени—у 39 больных и у двух—2 степени) развился у 41 из 100 больных (41,0±3,7%), леченных по аналогичным схемам ПХТ без ремаксола (табл. 2). Наибольшая частота повышения печеночных показателей констатирована при РМЖ IIb-IV стадии (46,8%) и раке яичников IIb-IV стадии (42,8%), получающих платину и доксорубицин. ПХТ удалось провести с кратковременным перерывом у 12 больных (3-4 дня).
Эффективность терапии ремаксолом оценивалась, по динамике показателей АЛТ/АСТ, билирубина, ЛИИ и других показателей, свидетельствующих о проявлении токсического гепатита (ТГ).
В одном случае, в связи с сохраняющимися высокими показателями ALT/ACT, билирубина и креатинина от проведения ПХТ решено отказаться (пациент исключен из общей группы).
Таблица 2.
Общие сведения о результатах исследования: частота токсического гепатита (ТГ)
| Локализация и стадия рака | 1 группа
(с ремаксолом) | 2 группа | 3 группа
(с эссенциале) |
|---|
| Число б-х | в т.ч. ТГ | Число б-х | в т.ч. ТГ | Число б-х | в т.ч. ТГ |
|---|
| колоректальный рак IIIa-IV ст. | 35 | 1
(8,5%) | 22 | 8
(36,3%) | 14 | 2
(14,2%) |
| РМЖ IIb-IV ст. | 27 | 5
(18,5%) | 32 | 15
(46,8%) | 18 | 3
(16,6%) |
| рак яичников IIb-IV ст. | 13 | 2
(15,3%) | 14 | 6
(42,8%) | 3 | 1 |
| рак легкого IIb- IIIb ст. | 25 | 3
(12%) | 32 | 12
(37,5%) | 5 | 1 |
| Всего | 100 | 11
{11,0+2,6%) | 100 | 41
(41,0±3,7%) | 40 | 7
(17,5±2,9%) |
Таблица 3.
Сравнительные результаты работы в зависимости от применяемых гепатопротекторов и этапов исследования (М±σ)
Показатели
ммоль/л | Этап исследования/группы |
|---|
| исход | 6-е сутки | 11-е сутки |
|---|
| ремаксол | эссенциале | контроль | ремаксол | эссенциале | контроль | ремаксол | эссенциале | контроль |
|---|
| Общий белок | 71,25 ±5,53 | 72,46 ±4,7 | 72,27 ±5,21 | 71,11 ±5,23 | 73,41 ±4,86 | 71,48 ±6,35 | 73,70 ±5,2 | 72,04 ±5,16 | 70,60 ±5,28 |
| Альбумины | 38,09 ±3,89 | 39,97 ±2,83 | 29,84 ±6,00 | 38,91 ±3,58 | 21,84 ±9,8 | 26,1 ±17,2 | 38,51 ±4,00 | 27,57 ±13,13 | 21,58 ±18,28 |
| Общий билирубин | 11,49 ±4,02 | 12,34 ±3,98 | 12,05 ±4,48 | 12,36 ±3,77 | 15,88 ±6,88 | 16,1 ±9,08 | 13,63 ±4,52 | 14,01 ±5,36 | 15,81 ±7,06 |
| Прямой билирубин | 2,15 ±1,69 | 2,35 ±1,44 | 2,30 ±1,49 | 2,28 ±1,70 | 3,10 ±2,25 | 3,26 ±2,25 | 2,48 ±1,71 | 2,72 ±1,73 | 3,15 ±2,50 |
| Непрямой билирубин | 9,40 ±3,81 | 9,99 ±3,31 | 10,06 ±4,40 | 10,11 ±3,89 | 12,78 ±5,39 | 12,84±6,92 | 11,1 4 ±4,20 | 11,15 ±4,48 | 13,39 ±8,26 |
| АЛТ | 22,99 ±17,34 | 21,7 ±12,1 | 20,84 ±12,00 | 19,84 ±11,78 | 21,31 ±10,93 | 26,13 ±17,25 | 18,35 ±9,28 | 19,57 ±13,13 | 27,58 ±18,28 |
| ACT | 23,71 ±10,53 | 23,50 ±8,9 | 23,30 ±12,87 | 21,50 ±7,27 | 22,40 ±9,47 | 27,93 ±14,57 | 21,59 ±6,78 | 25,18 ±19,89 | 29,03 ±15,07 |
| ЩФ | 137,48 ±61,5 | 133,3 ±52,4 | 121,9 ±35,36 | 133,1 ±44,46 | 125,3 ±45,27 | 133,6 ±45,78 | 134,2 ±42,64 | 219,95 ±42,43 | 233,45 ±47,67 |
| ГГТП | 34,07 ±15,57 | 47,18 ±20,8 | 47,18 ±21,81 | 32,02 ±11,86 | 47,31 ±20,25 | 47,31 ±22,25 | 31,03 ±10,51 | 50,40 ±24,14 | 51,40 ±25,34 |
| Холестерин | 4,95 ±0,87 | 4,88 ±0,73 | 5,42 ±0,79 | 5,00 ±0,89 | 4,85 ±0,88 | 5,04 ±0,87 | 4,84 ±0,91 | 4,67 ±0,79 | 5,01 ±0,84 |
| ЛДГ | 324,8 ±109,0 | 311,9 ±112,7 | 301,4 ±111,8 | 311,1 ±106,5 | 309,4 ±111,6 | 323,7 ±121,6 | 292,25 ±96,81 | 304,9 ±124,1 | 309,4 ±132,5 |
В группе 3 проведение курса ПХТ осуществлялось на фоне эссенциале: несмотря на это, повышение показателей АЛТ и/или ACT, в одном случае—билирубина и ЛДГ констатировано у 17,5±2,9% больных (рис.1).
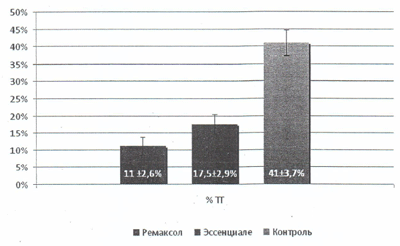
Рис.1 Сравнительная характеристика частоты токсических гепатитов (ТГ) после ПХТ; все локализации.
Следует отметить, что по отдельным локализациям в зависимости от схем ПХТ и применения гепатопротекторов констатированы заметные колебания средней арифметической и квадратических отклонений данных лабораторных анализов, особенно на 6-е и 11-е сутки (табл. 3, рис. 2) Статистический анализ результатов исследования проводился в системе SAS (Statistical Analisis System, SAS Institute Inc.,США) с применением стандартных алгоритмов вариационной статистики, а также программы STATISTIC А, версия 10.0.
Анализ показал, что различия большинства лабораторных показателей в 1-ой группе в сравнении с контрольной на 11-е сутки ПХТ значимы на уровне рРациональное использование средств в онкологии всегда рассматривалось как наиболее важная цель совершенствования системы здравоохранения. В этом плане, анализ всех затрат в денежном выражении безусловно, заслуживает внимания, хотя это и сложная задача. Часто требуется проанализировать в этом отношении результаты, эффективность которых не может быть оценена прямо [5]. В стоимость следует включать лабораторные анализы и стоимость препаратов, используемых для лечения осложнений.
Таблица 4.
Сравнительная стоимость профилактики токсического гепатита при ПХТ.
| Препараты | Средняя стоимость | Стоимость 1 профилактического курса |
|---|
| Ремаксол, 400 мл 1 флакон | 300 руб | 300 руб х 10 = 3000 руб |
| Эссенциале, 5 мл амп № 5 (1 упак.) | 630 руб | (126 руб х 2) х 10 = 2520 руб |
Таблица 5.
Расходы на лечение токсического гепатита, возникшего на фоне или после ПХТ (на 1 пациента).
| Дополнительные медицинские расходы | Стоимость 10-дневного лечения |
|---|
| Увеличение пребывания на онкологической койке на 10 дней, диета №5 | 427руб х 10 суток = 4270 руб |
| Комплекс биохимических исследований (ACT, АЛТ, щелочная фосфатаза, ГГТП, ЛДГ, общий билирубин, прямой и непрямой билирубин, общий белок, альбумин)— 2 раза | 647 руб х 2 = 1294 руб |
| УЗИ печени и поджелудочной железы —2 раза | 450руб х 2= 900 руб |
| КТ печени и поджелудочной железы— 1 раз | 6100 руб х 1=6100 руб |
| Лекарственные средства (витамины С, В1, В6.В12, раствор Рингера, холензим)+эссенциале | (27+18+19+19+90+99)=272 руб х 10 =2720 руб + 2520 руб= 5240 руб |
| Всего | 18 076 руб |
Так, хотя стоимость 10-дневного курса профилактики токсического гепатита ремаксолом выше курса эссенциале на 480 руб, однако, проявление токсических осложнений при профилактике ремаксолом оказалось выражено в 1,6 раза меньше, чем при использовании эссенциале и в 3,7 раза ниже, чем при отсутствии профилактических мероприятий (табл. 4, 5). Если к этому добавить, что лечение ТГ, занимающего в среднем в стационаре дополнительно 10 дней, например, эссенциале требует 3000 руб (1 пациент), то стоимость лечения эссенциале 30 пациентов будет равна 9000руб. Кроме того, возникает необходимость в применении и других лекарственных средств, дополнительных лабораторных анализов и визуализирующих методов исследования, удорожающих ПХТ, приведенных ниже.
Таким образом, стоимость дополнительного лечения 30 пациентов в стационаре, получающих ПХТ без профилактической терапии ремаксолом, составляет 542 280 руб. (18076 х 30), а с гепатропными препаратами дополнительно 90000 руб, Иными словами, поскольку расходы на лечение при отсутствии профилактики токсических гепатитов весьма велики, то понятно, что профилактическое назначение ремаксола следует рекомендовать для сопроводительного лечения химиотерапии распространенных форм онкологических заболеваний.
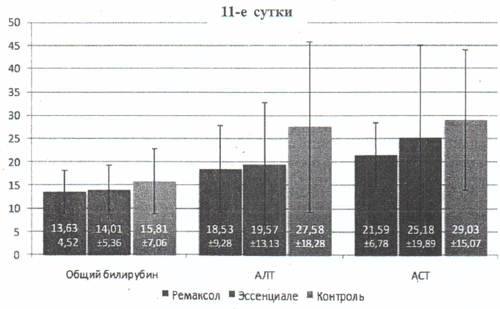
Рис.2. Сравнительные лабораторные данные (М±σ): общий билирубин, АЛТ и ACT на 11-е сутки.
Выводы
Профилактическое введение ремаксола за 5 дней до ПХТ и в процессе химиотерапии подтверждает данные литературы об отсутствии влияния препарата на снижение эффективности противоопухолевых средств.
Ремаксол в сравнению контрольной группой позволяет уменьшить частоту лекарственного токсического гепатита на 30±3,7% в сравнении с контрольной группой и на 6,5±2,9% в сравнении с группой, получавших эссенциале.
Проведение профилактики токсического гепатита, при сохраняющейся возможности его развития у 11±2,6% больных, позволяет снизить себестоимость ПХТ у пациентов с распространенными формами рака (за счет снижения затрат на лечение побочных эффектов химиопрепара-тов) в денежном эквиваленте более, чем на 0,6 млн руб. Профилактическое назначение препарата ремаксол следует рекомендовать для дальнейшего изучения эффективности и введения в стандарт в качестве средства сопровождения лечения ПХТ больных с распространенными формами злокачественных новообразований. ЛИТЕРАТУРА
1. Антонеева И.И. Перекисное окисление липидов и ферментативное звено антиоксидантной системы крови при раке яичников // Казан, мед. журнал.—2006. -№ З.-С. 158-166.
2. Безбородова О.А., Немцова Е.Р., Александрова Л.Н. и др. Оценка детоксирующего действия препарата «ремаксол» на экспериментальной модели токсикоза индуцированного цисплатином // Эксперимент, клин. фармакол. —2011. —№ 3. —С. 26-31.
3. КоваленкоА.Л., Петров А.Ю, Суханов Д.С. и др. Ремаксол—препарат для восстановления системы антиоксидантной защиты при поражении печени циклофос-фаном в эксперименте // Эксперимент, и клин, фармакол. 2011. —№ 1.- С. 32-35.
4. Мамедов Ф.Ф., Нариманов М.Н., Базин И.С. и др. Три режима химиотерапии диссеминированного коло-ректального рака // Consilium Med. 2001,—Т.З (2).— С. 12-16.
5. Поддубная И.В., Аркадьева ТВ. Фармоэкономика в онкологии (методология и особенности применения. Краснодар. 2000. —75 с.
6. Поддубная И.В., Орел Н.Ф., Егорова Г.Н. Осложнения противоопухолевой химиотерапии, терапия неотложных состояний // Рук. по химиотерапии опухолевых заболеваний / Под ред. Переводчиковой Н.И. М., 2005.
7. Поддубная И.В., Орел Н.Ф. Осложнения противоопухолевой химиотерапии, терапия неотложных состояний // Рук. по химиотерапии опухолевых заболеваний / Под ред. Переводчиковой Н.И. М., 2011. — С. 423-445.
8. Скопин П.П., Скопина Ю.А., Зорькина А.В. Влияние эмоксипинана на фоне экспериментальной химиотерапии на показатели свободнорадикального окисления и эндотоксикоза в организме опухоленосителя // Мат. VI Всероссийского съезда онкологов. —2005.— Т. 2-С.170-171.
9. Суханов Д.С, Коваленко А.Л., Романцев М.Г. и др. Цитопротекторная активность сукцинатсодержащих препаратов на функциональную активность печени в эксперименте // Эксперимент, и клин, фармакол. 20Ю.-№ 8.-С. 35-38.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru



