Эффективность инфузионного гепатопротектора ремаксола в патогенетической терапии хронических диффузных заболеваний печени на цирротической стадии
Статьи
Опубликовано в журнале Экспериментальная и клиническая гастроэнтерология | выпуск 128 | №4 2016
Стельмах В. В., Козлов В. К.
ГБОУ ВПО ДПО СЗГМУ им. И.И. Мечникова, Санкт-Петербург
Стельмах Виктория Валерьевна — к.м.н., доцент кафедры внутренних болезней и нефрологии, сотрудник отделения гепатологии и нефрологии, Северо-Западный государственный медицинский университет им. И.И. Мечникова (СЗГМУ им. И.И. Мечникова).
Козлов Виктор Константинович - д.м.н., профессор кафедры внутренних болезней и нефрологии, кафедры клинической лабораторной диагностики, Северо-Западный государственный медицинский университет им. И.И. Мечникова (СЗГМУ им. И.И. Мечникова).
Резюме
Целью настоящего исследования явилось изучение влияния терапии инфузионным гепатопротектором ремаксолом на функциональное состояние печени при циррозах печени в исходе хронических гепатитов (вирусного (В, С), алкогольного, токсического, аутоиммунного, метаболического генеза) на протяжении 11 дневного лечения.
Для этого обследовано 130 пациентов от 25 до 80 лет с диагнозом: хронический (вирусный (В, С), аутоиммунный, токсический, алкогольный, неалкогольный) гепатит, цирротическая стадия, Child-Pugh A-С. Пациенты основной группы (п=80) в составе комплексной терапии получали ремаксол ежедневно внутривенно капельно по 400,0 мл 1 раз в сутки, в течение 10-11 дней. Пациенты группы сравнения (n=50) на фоне инфузионной терапии кристаллоидами получали адеметионин 400 мг в сутки, (лиофилизат для приготовления раствора для внутривенного и внутримышечного ведения, разведенный в оригинальном растворителе) в течение 10-11 дней.
Выявлено, что включение в схему комплексного лечения ремаксола в больных циррозом печени различной этиологии (вирусной (В, С), алкогольной, токсической, аутоиммунной, метаболической) способствует улучшению функционального состояния печени: снижению выраженности синдрома цитолиза, холестаза, уменьшению проявлений печеночно-клеточной недостаточности, уменьшению выраженности печеночной энцефалопатии, оказывает цитопротекторный эффект по отношению к клеткам периферической крови (лейкоцитам, лимфоцитам, тромбоцитам) за счет мембраностабилизирующего, антихолестатического, цитопротективного эффектов препарата. Полученные результаты свидетельствуют о положительном влиянии терапии ремаксолом при циррозах печени различной этиологии с проявлениями печеночно-клеточной недостаточности и печеночной энцефалопатии.
Ключевые слова: цирроз печени, вирусный, алкогольный, токсический, аутоиммунный, метаболический гепатит, печеночно-клеточная недостаточность, печеночная энцефалопатия, патогенетическая терапия, гепатопротектор, Ремаксол.
Экспериментальная и клиническая гастроэнтерология 2016; 128 (4): 72-79
Efficiency infusion hepatoprotectors remaxol the pathogenetic therapy of chronic diffuse liver diseases cirrhotic on stage
Stelmach V. V., Kozlov V. K.
North-Western State Medical University named after I.I. Mechnicov, S-Petersburg
Summary
The purpose of this study was to investigate the effect of infusion therapy hepatoprotector remaxol on the functional state of the liver in liver cirrhosis in the outcome of chronic hepatitis (HBV, HCV), alcoholic, toxic, autoimmune, metabolic origin) for 11 days care.
To do this, we examined 130 patients from 25 to 80 years with a diagnosis of chronic (viral (В, C), autoimmune, toxic, alcoholic, non-alcoholic) Hepatitis, cirrhotic stage, Child-Pugh A-С. Patients of the main group (n = 80) in the complex therapy received remaxol daily intravenously at 400,0 ml of 1 times a day, for 10-11 days. Patients comparison group (n = 50) on the background of crystalloid infusion therapy ademetionine received 400 mg per day, (lyophilisates for solution for intravenous and intramuscular reference, diluted in the original solvent) for 10-11 days.
It was found that the inclusion in the scheme of complex treatment remaxol in patients with liver cirrhosis of various etiologies (HBV, HCV), alcohol, toxic, autoimmune, metabolic) improves the functional state of the liver: decrease the severity cytolysis syndrome, cholestasis, reduced manifestations of hepatocellular insufficiency, reduce the severity of hepatic encephalopathy, providing cytoprotective effect relative to peripheral blood cells (leukocytes, lymphocytes, platelets) due to membrane stabilizing, antiholestaticheskogo, cytoprotective effects of the drug. The results show the positive effect of therapy remaxoi with cirrhosis of the liver of different etiology manifestations of hepatocellular insufficiency and hepatic encephalopathy.
Keywords: cirrhosis, viral, alcoholic, toxic, autoimmune, metabolic hepatitis, hepatocellular failure, hepatic encephalopathy, pathogenetic therapy, hepatoprotector, Remaxol.
Eksperimental'naya i Klinicheskaya Gastroenterologiya 2016; 128 (4): 72-79
Введение
Цирроз печени (ЦП), впервые описанный R. Lаеnек (1819) является финальной стадией хронических гепатитов различной этиологии и представляет собой актуальную проблему здравоохранения в виду лидирующего места среди неонкологических причин смертности от болезней пищеварительной системы [1,2,3]. При этом в возрастной группе 20-40 лет летальность от ЦП превосходит таковую от ишемической болезни сердца [4,5].
По данным эпидемиологических исследований, проведенных в различных регионах мира, наиболее частыми причинами развития цирроза печени являются хроническая интоксикация алкоголем и вирусные гепатиты наряду с аутоиммунными болезнями печени, болезнями обмена веществ и др. (К.П. Майер, 2004). Прогрессирование фиброза при хронических гепатитах различной этиологии в итоге приводит к нарушению дольковой архитектоники печени и обусловливает развитие цирроза печени и портальной гипертензии [8]. Клиническая картина цирроза печени определяется не столько его этиологией, сколько характером и тяжестью морфологических изменений [6,10,11].
Важная роль в развитии гепатоцеллюлярного повреждения печени отводится процессу оксидативного стресса и индуцированных им апоптозу и некробиозу гепатоцитов [12,13], что способствует прогрессии фибротических процессов в печени [14,15,16]. Высокий риск летального исхода от осложнений портальной гипертензии, гепаторенального синдрома, печеночной энцефалопатии и комы, существенное ограничение в ряде случаев этиотропного лечения обуславливает поиск оптимальных методов патогенетической терапии [7].
В этой связи одним из эффективных патогенетических подходов в гепатологии является использование сукцинатсодержащих препаратов (Реамберин, Ремаксол (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург)), корригирующих тканевую гипоксию, а также модифицирующих клеточный обмен и оказывающих гепатопротективное действие [17-20]. За рубежом имеется позитивный опыт применения антиоксидантных ферментов и витаминов-антиоксидантов (вит. Е, С) при заболеваниях печени [21].
Ремаксол — многокомпонентный инфузионный гепатопротектор, состоит из естественных метаболитов (янтарная кислота, рибоксин, никотинамид, метионин), оказывает антиоксидантное, антигипоксантное, гепатотропное действие, стимулирует синтез эндогенного адеметионина, повышает показатели системы глутатиона, усиливает регенеративные процессы в печени [22]. Согласно опубликованным данным клинические эффекты ремаксола при гепатопатиях различного генеза превосходят эффекты традиционной фармакотерапии [23-27].
Целью настоящего исследования явилось изучение влияния терапии инфузионным гепатопротектором ремаксолом на функциональное состояние печени при циррозах печени в исходе хронических гепатитов (вирусного (В, С), алкогольного, токсического, аутоиммунного, метаболического генеза) на протяжении 11 дневного лечения.
Материал и методы исследования
Обследовано 130 пациентов от 25 до 80 лет с диагнозом: хронический гепатит (вирусный (В, С), аутоиммунный, токсический, алкогольный, неалкогольный), цирротическая стадия, Сhild-Рugh А-С. Этиология цирроза печени пациентов, включенных в исследовании представлена на рис. 1.
Рисунок 1.
Этиология цирроза печени исследуемых пациентов.
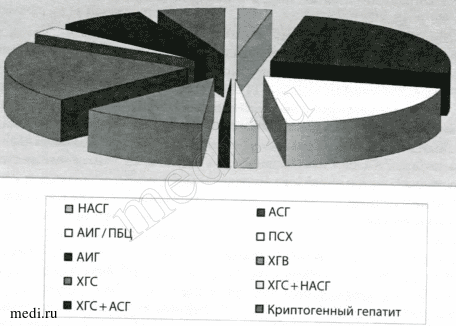
Примечания:
НАСГ — неалкогольный стеатогепатит
АИГ/ПБЦ — аутоиммунный гепатит/первичный билиарный цирроз печени
АИГ — аутоиммунный гепатит ХГС — хронический гепатит С
ХГС+АСГ — микст-гепатит (хронический гепатит С + алкогольный стеатогепатит)
АСГ — алкогольный стеатогепатит
ПСХ — первичносклерозирующий холангит
ХГВ — хронический гепатит В
ХГС+НАСГ — ХГС+АСГ — микст-гепатит (хронический гепатит С + неалкогольный стеатогепатит)
Пациенты основной группы (п=80) в составе комплексной терапии получали инфузионный гепатопротектор ремаксол ежедневно внутривенно капельно по 400,0 мл 1 раз в сутки, в течение 10-11 дней. Пациенты группы сравнения (п=50) в составе комплексной терапии получали лиофилизат для приготовления раствора для внутривенного и внутримышечного ведения адеметионин 400 мг, разведенный в оригинальном растворителе. В сутки вводилось 400 мг адеметионина, на фоне инфузионной терапии кристаллоидами (400 мл NaCL 0,9%) в течение 10-11 дней. Диагноз ставился на основании совокупности клинико-лабораторных данных в соответствии с классификацией МКБ-10.
Критерии включения пациентов в исследование: мужчины и женщины в возрасте от 25 до 80 лет, с диагнозом: хронический (вирусный (В, С), аутоиммунный, токсический, алкогольный, неалкогольный) гепатит, цирротическая стадия, Child-Pugh А-С.
Портальная гипертензия: асцит и/или варикозное расширение вен пищевода и/или гиперспленизм и/или расширение воротной вены более 15 мм; АсТ и/или АлТ >1,5 N; 4. ГГТП > 1,5 N.
Критерии невключения пациентов в исследование: индивидуальная непереносимость компонентов препарата ремаксол, недавние случаи (менее трех месяцев назад) одного из следующих состояний: острый инфаркт миокарда, аорто-коронарное шунтирование, чрескожное коронарное вмешательство, реконструктивные вмешательства на сосудах нижних конечностей или сонных артериях, инсульт, травмы головного и спинного мозга, пациенты со злокачественными новообразованиями, туберкулезная инфекция, сердечная недостаточность IV степени по классификации NYHA, дыхательная недостаточность III степени на момент включения в исследование, хроническая почечная недостаточность, требующая проведения гемодиализа, беременность и период лактации.
Гематологические исследования выполнялись с использованием автоматического гематологического анализатора «BECMAN-COULTER5-diff» (Германия). Биохимические методы исследования с определением уровней билирубина, аланинаминотрансферазы (АлТ), аспартатаминотрансферазы (АсТ), гаммаглютамилтранспептидазы (ГГТП), щелочной фосфатазы (ЩФ), глюкозы проводились на автоматическом биохимическом анализаторе «Cobas Integra — 400 Plus» фирмы «Roshe-Diagnostics» с помощью коммерческого набора реактивов фирмы «Roshe-Diagnostics» (Швейцария). Серологическая диагностика хронических вирусных гепатитов (HBsAg, анти-HCV антитела) проводилась методом иммуноферментного анализа с помощью тест-системы ЗАО «Вектор-Бест» III поколения.
Скрининг аутоиммунного поражения печени и системных заболеваний соединительной ткани выполнялись на базе НМЦ по Молекулярной медицине М3 и СР РФ при СПбГМУ им. акад. И.П. Павлова.
Инструментальное исследование предусматривало ультразвуковое исследование (УЗИ) органов брюшной полости; фиброгастродуоденоскопию (ФГДС) с определением состояния слизистой оболочки пищевода, желудка и 12-перстной кишки, исключения варикозных вен в пищеводе и антральном отделе желудка.
Указанием на цирротическую стадию хронического гепатита служили изменение структуры печени, а также наличие признаков портальной гипертензии, выявляемых по данным УЗИ (увеличение диаметра воротной вены более 15 мм и/или наличие асцита), наличие варикозного расширения вен пищевода по данным ФГДС, а также клинически выраженный отечно-асцитический синдром, не связанный с патологией других органов и систем организма.
Всем пациентам проводился психометрический тест связи чисел, характеризующий степень выраженности печеночной энцефалопатии, а также тестирование Gage для выявления алкогольной зависимости.
Для обработки полученных данных были использованы пакеты программ Office Std. 2010 (Excel 2010) и Statistica 7.0. Оценка значимости различия проводилась непараметрическими методами: между независимыми группами (Контроль-Ремаксол) проводилась при помощи U-критерия Манна-Уитни, между связанными выборками (до и после, на 6-й день) — при помощи теста Вилкоксона и Sign теста. Для сравнения качественных признаков использовались х2 критерий — для оценки частоты появления признака, который работает при п>5, противном случае использовался точный критерий Фишера. Проверка статистических гипотез проводилась при критическом уровне значимости Р = 0,05, т.е. различие считалось статистически значимым, если р<0,05.
Результаты исследования и их обсуждение
Распределение больных по группам с учетом этиологических и демографических данных представлено на рис. 1, табл. 1.
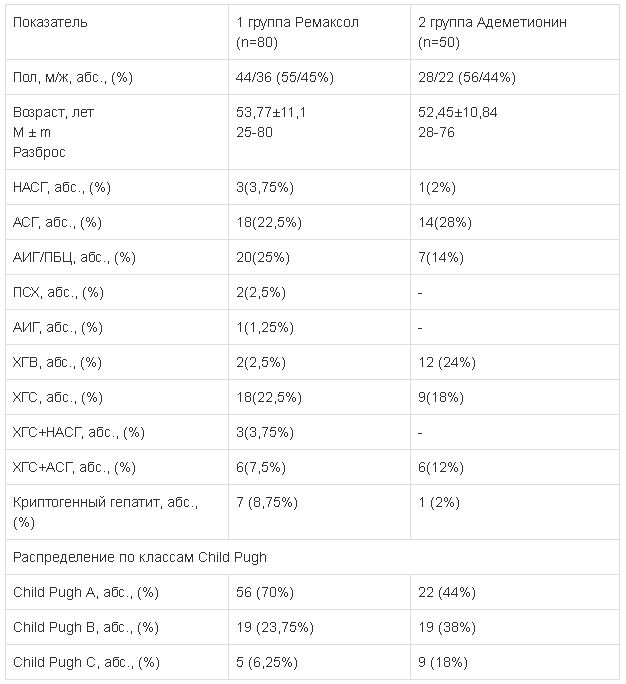
Таблица 1.
Демографические характеристики исследуемых больных
Жалобы диспепсического характера исходно отмечали 84% больных основной группы и 78% больных группы сравнения (р>0,05). Боли в области правого подреберья беспокоили 84% больных основной группы и 76% больных группы сравнения (р<0,001). Кожный зуд исходно беспокоил 54% больных основной группы и 60% больных группы сравнения. Исходно желтуха наблюдалась у 27% больных основной группы и у 30% больных группы сравнения (Табл. 2).
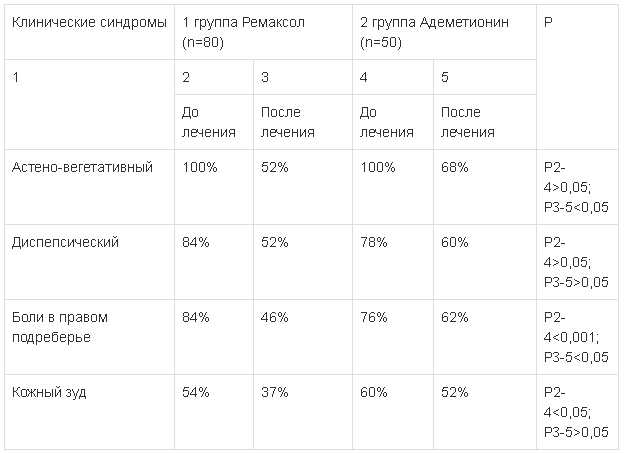
Таблица 2
Клинические синдромы исследуемых больных
Признаки портальной гипертензии (варикозно-расширенные вены пищевода) выявлены у 72% больных основной группы и у 63% больных группы сравнения. Отечно-асцитический синдром исходно наблюдался у 45% больных основной группы и у 60% больных группы сравнения.
Исходно у 65 (50%) исследуемых пациентов с циррозами печени выявлялась (с помощью теста на цифровую последовательность) латентная печеночная энцефалопатия (ЛПЭ), у 51 (39%) пациентов выявлялась клинически выраженная печеночная энцефалопатия I стадии (ПЭ I ст.), у 9 (7%) пациентов выявлялась клинически выраженная печеночная энцефалопатия II стадии (ПЭ II ст.), у 5 (4%) пациентов определялась клинически выраженная печеночная энцефалопатия III стадии (ПЭ III ст.).
У пациентов обеих групп исходно было выявлено нарушение функции печени в виде синдромов цитолиза, холестаза, печеночно-клеточной недостаточности (табл. 3).
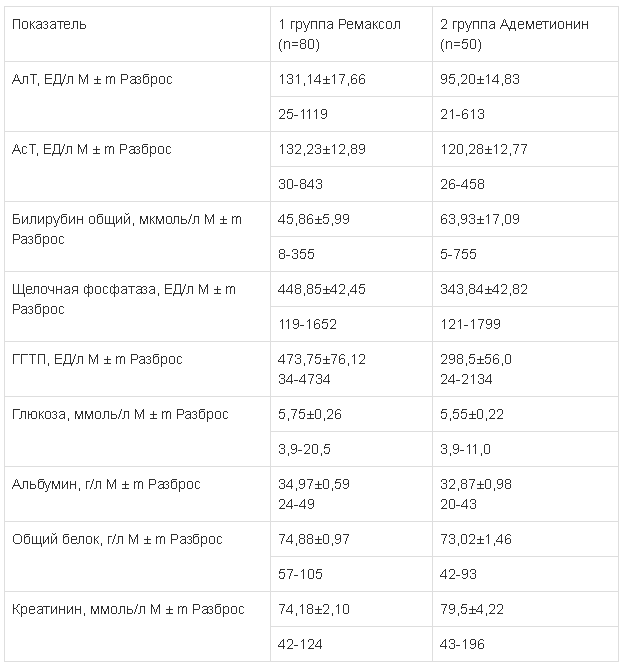
Таблица 3.
Биохимический анализ крови (исходные данные)
Изучение липидного обмена у исследуемых больных выявило исходно повышенные значения общего холестерина у 44% больных основной группы и 27% больных группы сравнения (7,57±0,37 и 6,93±0,44 ммоль/л соответственно, р>0,05); повышение уровня триглицеридов у 23% больных основной группы и 18% больных группы сравнения (2,32±0,12 и 2,13±0,17 ммоль/л соответственно, р>0,05). Наиболее часто нарушения в липидном обмене наблюдались у больных с циррозом печени в исходе хронического алкогольного гепатита и перекрестного аутоиммунного синдромы, реже при вирусной этиологии заболевания.
При назначении дезинтоксикационной терапии в обеих группах регистрировалось уменьшение жалоб и частоты патологических симптомов. При этом у пациентов, получавших ремаксол, более быстро уменьшались проявления астенического, диспепсического и болевого абдоминального синдромов по сравнению с группой сравнения (р<0,05). Инфузионная терапия ремаксолом способствовала более существенному уменьшению кожного зуда к концу лечения по сравнению с группой контроля. (Табл. 2, рис. 2-3).
Рисунок 2.
Динамика выраженности основных клинических синдромов в основной группе (Ремаксол, п=80) до лечения (0 день) и после лечения (12 день).
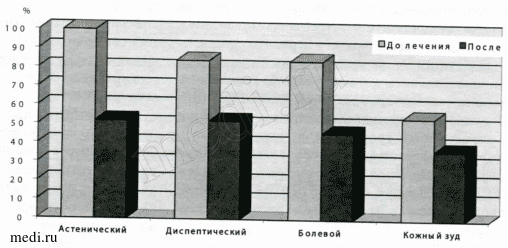
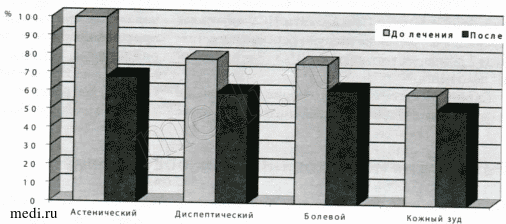
Рисунок 3.
Динамика выраженности основных клинических синдромов в группе сравнения (Адеметионин, п=50) до лечения (0 день) и после лечения (12 день).
Доказана важная роль процессов свободно-радикального окисления липидов клеточных мембран в развитии гепатоцеллюлярного повреждения, биохимическим отражением которого является синдром цитолиза [Ляшенко В. А. 1995, Мазо В. К. 1998]. Выраженный гепатотропный эффект ремаксола подтверждался темпами снижения средних показателей АлТ и АсТ. Относительные величины снижения уровней этих ферментов у больных циррозом печени Child Pugh А, получавших ремаксол, составили 59% и 42% против 32% и 42% у пациентов группы сравнения; у больных циррозом печени Child Pugh В, получавших ремаксол, составили 30% и 40% против 33% и 26% у пациентов группы сравнения; у больных циррозом печени Child Pugh С, получавших ремаксол, составили 24% и 23% против 15% и 25% у пациентов группы сравнения (рис. 4-6.).
Рисунок 4.
Относительные изменения (среднее) показателей АлТ, АсТ, ГГТП и билирубина у больных с циррозом печени Child Pugh А на фоне инфузионной терапии.
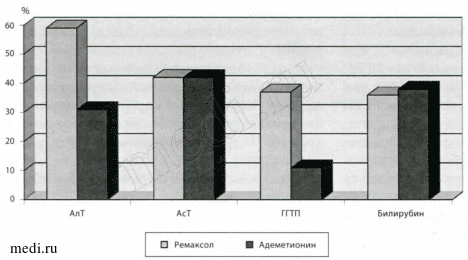
Рисунок 5.
Относительные изменения (среднее) показателей АлТ, АсТ, ГГТП и билирубина у больных с циррозом печени Child Pugh В на фоне инфузионной терапии.
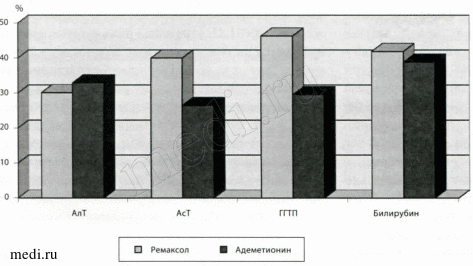
Рисунок 6.
Относительные изменения (среднее) показателей АлТ, АсТ, ГГТП и билирубина у больных с циррозом печени Child Pugh С на фоне инфузионной терапии.
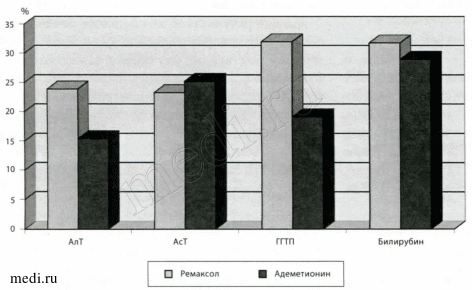
Динамика снижения выраженности средних значений параметров синдрома цитолиза на фоне инфузионной терапии ремаксолом: при циррозах печени Child Pugh А снижение АлТ с 214,0±16,7 до 88,6±15,19 ЕД/л, р<0,01, АсТ с 146,63±27,47 до 85,34±8,93 ЕД/л, (р<0,05); при циррозах печени Child Pugh В снижение АлТ с 108,14±12,61 до 75,57±16,14 ЕД/л, (р<0,05), АсТ с 138,78± 15,27 до 83,21±12,27 ЕД/л, (р<0,05); при циррозах печени Child Pugh С снижение АлТ с 74,0±2,3 до 56,33±6,3 ЕД/л, (р<0,05), АсТ с 108,25±8,79 до 83,00±9,25 ЕД/л, (р<0,05).
Механизмы развития синдрома холестаза при хронических диффузных заболеваниях печени многофакторны. У исследуемых больных с циррозом печени различной этиологии синдром холестаза и клинически и биохимически исходно был более выражен в основной группе (по частоте регистрации кожного зуда и уровню ГГТП (Табл. 2,3).
Установлено статистически значимое различие в динамике показателей холестаза по изменению величины ГГТП (р=0,03) между группами. Относительные величины снижения уровней ГГТП у больных, получавших инфузионную терапию в основной группе составили 37%, 46% и 32% против 11%, 29% и 19% у пациентов группы сравнения (рис. 4-6.), что свидетельствует о выраженном антихолестатическом эффекте ремаксола.
Динамика снижения выраженности средних значений параметров синдрома холестаза (ГГТП) на фоне инфузионной терапии ремаксолом: при циррозах печени Child Pugh А снижение ГГТП с 532,97±83,57 до 336,04±51,29 ЕД/л, (р<0,05); при циррозах печени Child Pugh В снижение ГГТП с 646,40±54,72 до 347,42±74,03 ЕД/л, (р<0,05); при циррозах печени Child Pugh С снижение ГГТП с 233,40±19,14 до 158,86±17,81 ЕД/л, (р<0,001).
Печеночно-клеточная недостаточность осложняет течение цирротической стадии заболеваний печени вне зависимости от этиологии, проявляется желтухой, асцитом, печеночной энцефалопатией, низким уровнем альбумина в сыворотке, недостаточностью протромбина. Содержание в крови этих белков позволяет оценить синтетическую функцию печени [21].
На фоне терапии ремаксолом у пациентов с циррозом печени наблюдалось улучшение белковосинтетической функции печени при циррозах печени Child Pugh А: повышение синтеза альбумина (с 38,22±0,42 до 40,75±0,46 г/л, р<0,05; при циррозах печени Child Pugh В: повышение синтеза альбумина (с 30,69±0,64 до 34,25±0,97 г/л, р<0,05; при циррозах печени Child Pugh С: повышение синтеза альбумина (с 25,66±0,88 до 28,25±1,7 г/л, р<0,05. Повышение уровня альбуминов наблюдалось у 68% пациентов основной группы и только у 36% больных группы сравнения, (р<0,05). У пациентов с печеночно-клеточной недостаточностью Child Pugh В в группе ремаксола выявлено более существенное повышение относительных величин уровней альбумина сыворотки крови, по сравнению с группой контроля: 11,6% против 7,8% соответственно (р<0,05).
Применение ремаксола способствовало развитию цитопротективного эффекта по отношению к клеткам периферической крови при циррозах печени Child Pugh А: повышение абсолютного количества лимфоцитов (с 1,22±0,05 до 1,83±0,19 109/л, р<0,05); повышение абсолютного количества лейкоцитов (с 3,38±0,12 до 4,53±0,36 109/л, р<0,01); при циррозах печени Child Pugh В, С: повышение абсолютного количества лимфоцитов (с 0,94±0,09 до 1,4±0,13 109/л, р<0,05); повышение абсолютного количества лейкоцитов (с 3,33±0,37 до 4,20±0,98 109/л, р<0,05).
Инфузионная терапия ремаксолом способствовала уменьшению проявлений гиперспленизма: при циррозах печени Child Pugh А: повышение абсолютного количества тромбоцитов периферической крови (с 111,40±7,31 до 150,93±16,29 109/л, р<0,05); при циррозах печени Child Pugh В, С: повышение абсолютного количества тромбоцитов периферической крови (с 94,33±9,33 до 121,75±10,03 109/л, р<0,05).
Патогенез печеночной энцефалопатии (ПЭ) до сих пор остается предметом научных гипотез и представляется многофакторным процессом, протекающего параллельно в печени и в головном мозге (Надинская М. Ю„ 2006; Ивашкин В. Т. и соавт., 2007). Центральная роль в патогенезе ПЭ отводится гипераммониемии возникающей главным образом вследствие гепатоцеллюлярной недостаточности и связанному с этим токсическому воздействию на центральную нервную систему (ЦНС) [28, 29]. С этих позиций представляется перспективным применение препаратов на основе янтарной кислоты в комплексной терапии больных ЦП с проявлениями ПЭ. Янтарная кислота, обладает прямым модифицирующим воздействием на клеточный метаболизм, активирует аэробный гликолиз, в условиях гипоксии увеличивает интенсивность окислительных процессов в цикле Кребса, повышает внутриклеточный фонд макроэргических соединений (АТФ и креатинфосфата) [30].
Анализ результатов выполнения психометрических тестов через 10 дней на фоне проводимой терапии подтвердил улучшение психомоторных функций в большей степени у пациентов основной группы по сравнению с группой сравнения. Инфузионная терапия Ремаксолом способствовала уменьшению выраженности ПЭ: к концу курса инфузионной терапии у больных ЦП в основной группе не наблюдалась ПЭ III ст., гораздо реже диагностировалась ПЭ I и II ст. по сравнению с группой сравнения.
Выводы
Выявлено, что 11-дневный курс инфузионным гепатопротектором ремаксолом при циррозах печени различной этиологии (вирусной (В, С), алкогольной, токсической, аутоиммунной, метаболической):
- существенно уменьшает выраженность основных клинических синдромов (астеновегетативного, диспепсического, холестатического);
- способствует редукции основных биохимических синдромов гепатоцеллюлярного повреждения — синдрома цитолиза и холестаза;
- способствует уменьшению проявлений печеночно-клеточной недостаточности: улучшению белково-синтетической функции печени, уменьшению выраженности печеночной энцефалопатии;
- оказывает цитопротективный эффект: повышение абсолютного количества лейкоцитов, лимфоцитов, тромбоцитов периферической крови.
Заключение
Учитывая наличие серьезных структурных изменений в печени с наступлением цирротической стадии заболевания, проявляющихся развитием печеночно-клеточной недостаточности, печеночной энцефалопатии, признаков портальной гипертензии, диктуется необходимость осмысленного назначения патогенетически значимых лекарственных средств с гепатопротективной и цитопротективной направленностью.
Исследование эффективности инфузионного гепатопротектора ремаксола в лечении больных с циррозами печени различной этиологии (вирусного (В, С), алкогольного, токсического, аутоиммунного, метаболического генеза) выявило наличие мембраностабилизирующего, антихолестатического, цитопротективного эффектов. Полученные результаты свидетельствуют о положительном влиянии терапии ремаксолом при циррозах печени различной этиологии с проявлениями печеночно-клеточной недостаточности и печеночной энцефалопатии.
В этой связи, ремаксол является эффективным препаратом в комплексной терапии больных с циррозами печени различной этиологии (вирусной (В, С), алкогольной, токсической, аутоиммунной, метаболической).
Литература
1. Маевская М.В., Федосьина Е.А. Лечение осложнений цирроза печени./ Метод. Рекомендации для врачей под ред.. акад. РАМН, Ивашкина В.Т. Москва, «МЕД-пресс-информ» 2012. —56 с.
2. Khan М. N„ Farrell G. C., Byth К. et al. Which patients with hepatitis С develop liver complication? Hepatology 2000;31:513-520.
3. Юргель Л. А. Выживаемость больных циррозом печени неуточненной этиологии при различных показателях стандартной шкалы тяжести Чайлд-Пью /Л. А. Юргель, В.И. Козловский, М.Л. Доценко // Медицинская панорама. — 2008. — № 9. — С. 57-59.
4. Садовникова И. И. Циррозы печени. Вопросы этиологии, патогенеза, клиники, диагностики, лечения // РМЖ. - 2003. - Т. 5. — № 2.
5. Резистентный асцит у больных циррозом печени. Метод. рекоменд. для врачей под ред. Ивашкина В. Т., 2013, М., МедПресс-Информ, 80 с.
6. Тинсли Р. Харрисон Внутренние болезни. Пер. с англ. Под ред. Алипова H.H., Тимофеевой Е.Р. Практика. Москва. 2002 Т. 23176 с.
7. Заривчацкий М. Ф„ Каменских Е. Д., Мугатаров И. Н. Оценка эффективности ремаксола у больных циррозом печени. /Хирургия. Журнал им. Н.И. Пирогова. 2013. № 3 -С.79-82.
8. Шерлок Ш„ Дули Дж. Заболевания печени и желчных путей. Пер. с англ. Под ред. Апросиной З.Г., Мухина H.A. Москва, ГЭОТАР-МЕД, 2002:860 с.
9. Лобзин Ю. В., Гусев Д. А., Чирский В. С. и др. Морфологическая характеристика естественного течения хронической HCV-инфекции при различных темпах прогрессирования заболевания. Вестник Санкт-Петербургского университета 2008. Сер. 11. Вып. 4. С. 91-101.
10. Учайкин В.Ф, Чуелов С. Б., Россина А. Л., Смирнов А. В. и др. Циррозы печени у детей. Педиатрия. 2008: Т. 87; №5:52-58.
11. Акопян В. Г. Хирургическая гепатология детского возраста. М.: Медицина, 1982:384.
12. Шифф Ю.Р., Соррел М.Ф., Мэдрей У.С. Алкогольные, лекарственные, генетические и метаболические заболевания. Пер. с англ. Под ред. H.A. Мухина. М. ГЭОТАР-Медиа 2011; 480.
13. Радченко В. Г., Шабров А. В., Зиновьева E. Н. и др. Заболевания печени и желчевыводящих путей: руководство для врачей. СПб: СпецЛит 2011:241-269.
14. Koruk М., Aksoy H., Akcay F., Onuk M. D. Ann Clin Lab Sci, 2002,32:252-256.
15. Liaw K. Y., Lee P. H., Wu F. C. et al., Am J Gastroenterol, 1997,92:2260-2263.
16. Yasa H. M., Kacmaz M., Ozturk S. Durak I., Hepatogastro-enterology, 1999,46: 2460-2463.
17. Суханов Д. C., Петров A. Ю„ Романцов M. Г., Александрова Л. Н. и др. Фармакологическая активность сукцинат-содержащих препаратов при хроническом поражении печени различными инициирующими агентами. Фундаментальные исследования. 2011. № 5 — С. 159-169.
18. Стельмах В. В., Козлов В. К. Метаболические корректоры на основе янтарной кислоты и их использование при неалкогольном стеатогепатите. Профилактическая и клиническая медицина/ СПб., 2010 № 3-4. — С. 224-225.
19. Стельмах В. В., Радченко В. Г., Козлов В. К. Метаболические корректоры на основе янтарной кислоты как средства патогенетической терапии при хронических вирусных гепатитах. Терапевтический архив/ СПб., 2011 №2. —С. 67-71.
20. Суханов Д. С. Эффективность гепатопротекторного действия и оценка риска при использовании реамберина, ремаксола и адеметионина у больных туберкулезом органов дыхания с лекарственными поражениями печени. Терапевтический архив/ СПб., 2012 № 11 Т 84. — С. 26-29.
21. American Association for the study of liver disease. 2005, available at: http:// hepar-sfgh-ucsf. edu.]. JE Lavine, J. Pediatr, 2000,136,734-738.
22. Романцов М. Г., Суханов Д. С., Петров А. Ю. и др. Применение субстратов энергетического обмена при хроническом поражении печени для коррекции метаболических нарушений (экспериментально-клинические исследования). Фундаментал. исслед.2011.; 3:131-142.
23. Радченко В. Г., Стельмах В. В. Применение реамберина в комплексной терапии хронических гепатитов. Метод. Рекомендации для врачей. СПб.; — 2001. — С. 16.
24. Козлов В. К., Стельмах В. В. Оксидативный стресс в патогенезе дисфункции иммунной системы при инфекционной патологии. Модификаторы энергетического обмена клеток как средства патогенетической иммуноориентированной терапии. Материалы международного Евро-Азиатского конгресса по инфекционным болезням. Беларусь, Витебск — 2008: 106-109.
25. Сологуб Т. В., Горячева Л. Г., Суханов Д. С., Романцов М. Г. и др. Гепатопротективная активность ремаксола при хронических поражениях печени. Клиническая медицина / СПб., 2010 № 1. — С. 62-66.
26. Стельмах В. В., Козлов В. К. Метаболическая коррекция при дислипидемии у больных с неалкогольной жировой болезнью печени как новая стратегия терапии. Терапевтический архив. —2013. —Т. 85. — № 4. — С. 71-76.
27. Стельмах В. В., Козлов В. К., Радченко В. Г., Некрасова А. С. Патогенетическая терапия метаболического синдрома на стадии органных поражений Клиническая медицина/ СПб., 2012 № 6. — С. 61-65.
28. RiordanSM, Williams R. Treatment of hepatic encephalopathy. N Engl J Med 1997;337:473-479.
29. Blei AT, Cordoba J, Practice Parameters Committee of the American College of Gastroenterology. Hepatic encephalopathy. Am J Gastroenterol 2001;96:1968-1976.
30. Козлов В. К., Стельмах В. В. Применение корректоров клеточного метаболизма и регуляторов энергетического обмена клеток в комплексной этиопатогенетической терапии больных хроническим вирусным гепатитом.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru









