Коррекция функциональных расстройств печени в раннем послеоперационном периоде у пациентов после холецистэктомии
Статьи
Опубликовано в журнале:
"Экспериментальная и клиническая фармакология" 2017 Том 80 №9 С. 52-57
А. П. Власов, Н. С. Шейранов, О. Ю. Рубцов, П. А. Власов, П. П. Зайцев, Т. И. Власова, Н. Ю. Лещанкина, Ю. Г. Курочка
1 - ФГБОУ ВО "Национальный исследовательский Мордовский государственный университет им. Н. П. Огарева", Россия, Республика Мордовия, 430005, Саранск, ул. Большевистская, д. 68.
Целью настоящей работы явилась оценка эффективности ремаксола в коррекции функционального состояния печени в раннем послеоперационном периоде после холе-цистэктомии у больных с повышенным риском поражения печени. Полученные результаты и их анализ свидетельствуют о существенном уменьшении нарушений функционального состояния печени, мембраностабилизирующем эффекте ремаксола на печеночные клетки. Применение ремаксола у больных в послеоперационном периоде позволило уменьшить количество билирубина относительно группы больных, получавших стандартное лечение, через 1 сутпосле операции на 11,22 % (р < 0,05), на2 сут — на 12,71 % (р < 0,05), на 3 сут — на 22*14 % (р < 0,05), на 4 сут — на 20,11 % (р < 0,05) и на 5 сут — на 14,15 % (р < 0,05). Также отмечено уменьшение активности сывороточных аминотрансфераз: аланиновой — на 16,17 - 28,21 % (р < 0,05), аспарагиновой — на 7,25 - 12,02 % (р < 0,05). В свою очередь включение в комплексную послеоперационную терапию ремаксола позволило на 5 сут после операции нормализовать процессы перекисного окисления липидов, что не наблюдалось у больных в группе сравнения.
Ключевые слова: ремаксол; холецистэктомия; острый холецистит; ранний послеоперационный период.
ВВЕДЕНИЕ
Лечение острого холецистита — одна из немногих проблем в абдоминальной хирургии, которая решается успешно [11, 13, 14]. Безусловно, одним из важнейших путей ее реализации является использование малотравматичных оперативных технологий [4, 12, 16]. Их широкое применение позволяет существенно расширить показания к хирургическому своевременному лечению, благодаря чему появилась возможность профи-лактировать осложнения этой патологии [5, 10, 15]. Однако еще нередки случаи, когда из-за продолжительности и/или тяжести болезни в патологический процесс активно вовлекаются органы, структурно и функционально связанные с желчным пузырем. Одним из значимых негативных проявлений острого воспалительного процесса в желчном пузыре является поражение печени [6, 7]. Вовлечение этого органа обусловлено многими взаимосвязанными факторами, главными из которых являются распространение патологического процесса контактным путем, а также возможные содружественные дисфункциональные нарушения желчевыводящих путей.
Важнейшей причиной поражения печени при остром холецистите в случаях его деструктивного состояния является и эндотоксемия. Определенный вклад в поражение печени вносит и сама операция, какой бы она не была. Здесь речь идет не только о хирургической травме, но и о последствиях для организма в целом, связанных с удалением желчного пузыря. Подчеркнем, что от степени поражения печени, которая является одним из важнейших органов, участвующих в процессах пищеварения и метаболизма, зависит течение не только раннего, но и отдаленного послеоперационного периода. В этой связи вполне очевидным является такой состав комбинированной терапии, вектор которой направлен не только на орган поражения, но и на коррекцию патологии органов-мишеней, особенно печени [3].
Современная хирургия не должна игнорировать этот тезис, ибо ее уровень развития позволяет рассматривать успешность хирургической терапии не только в разрезе непосредственного оперативного воздействия на основной очаг, но и на лечение (предупреждение прогрессирования) содружественной патологии. Поэтому становится очевидным назначение при остром холецистите гепато-протекторной терапии в случаях с высокой вероятностью поражения печени. Большой интерес в этой связи к ремаксолу (ООО "НТФФ "ПОЛИСАН", Санкт-Петербург) проявляется как к отечественному инфузионному средству, обладающему антиоксидантным и антигипоксантным действием [1,2].
Целью работы было определение эффективности терапии ремаксолом в коррекции функционального состояния печени в раннем послеоперационном периоде после холецистэктомии у больных с повышенным риском поражения печени.
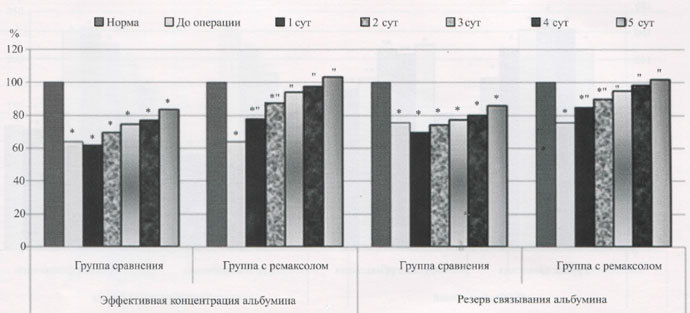
Рис. 1. Влияние ремаксола на эффективную концентрацию и резерв связывания альбумина у больных острым окклюзионным деструктивным холециститом в раннем послеоперационном периоде.
* Данные, изменение которых достоверно по отношению к норме при р< 0,05;"-достоверность разницы между данными 2 групп при р < 0,05.
МЕТОДЫ ИССЛЕДОВАНИЯ
Клинико-лабораторные исследования проведены у 65 больных острым холециститом. Всем пациентам выполнена лапароскопическая холецистэктомия, после которой выделены 2 группы. В первой группе, принятой за группу сравнения, у 34 больных интрао-перационно (затем морфологически) диагностирован острый окклюзионный флегмонозный или гангренозный холецистит с эмпиемой желчного пузыря (эти пациенты получали стандартное лечение), во второй (основной) группе у 31 пациента — аналогичная патология, а в раннем послеоперационном периоде проводилась дополнительная терапия с ремаксолом (ООО НТФФ "ПОЛИСАН", Санкт-Петербург), раствор для нфузий. Ремаксол представляет собой сбалансированный полиионный комплекс, содержащий янтарную кислоту, метионин, инозин, никотинамид, N-метилг-люкамин, а также электролиты (натрия хлорид, магния хлорид, калия хлорид).
Всем больным в раннем послеоперационном периоде проводилась стандартизированная терапия, включающая инфузионный, детоксикационный, антибактериальный, обезболивающий и другие компоненты. У ациентов основной группы терапия дополнительно содержала инфузии ремаксола (ежедневные внутривенные вливания 400 мл в течение 5 сут). При этом общий объем инфузионной терапии не увеличивали, что достигалось уменьшением инфузии других растворов. Больным проведено клинико-инструментальное обследование, выполнены общие и биохимические исследования крови и мочи, позволяющие судить и о функциональном состоянии печени. Кроме того, проводилась оценка детоксикационной, альбуминсинтези-рующей, альбумин- и липидметаболизирующей функции печени. С этой целью выраженность эндогенной интоксикации определяли по уровню токсических продуктов гидрофильной природы (по содержанию молекул средней массы) спектрофотометрическим методом при длинах волн 254 и 280 нм и гидрофобной природы (по общей (ОКА) и эффективной (ЭКА) концентрации альбумина) флюоресцентным методом на специализированном анализаторе АКЛ-01 "Зонд" (резерв связывания альбумина (РСА) рассчитывали по формуле: РСА = ЭКА/ОКА; индекс токсичности (ИТ) плазмы — по формуле: ИТ = ОКА/ЭКА-1) [8]. Показатели интенсивности перекисного окисления липидов — диеновые и триеновые конъюгаты — определяли спектрофотометрическим методом на спектрофотометре СФ-46, уровень малонового диальдегида — в реакции с тиобарбитуровой кислотой, активность су-пероксиддисмутазы (СОД) оценивали в реакции с нитросиним тетразолем, фосфолипазы А2 — по каталитической деятельности фермента потенциометрическим методом [9].
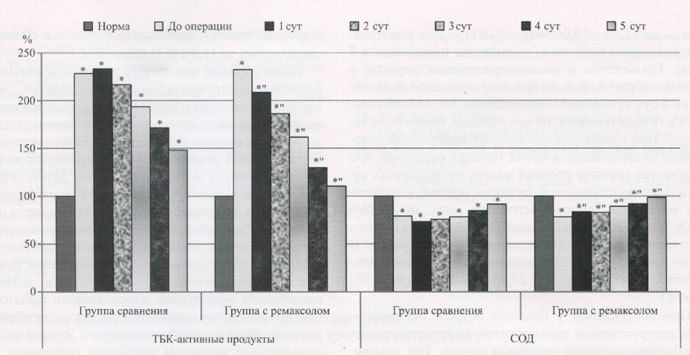
Рис. 2. Влияние ремаксола на уровень общего билирубина и коэффициент де Ритиса (АсАТ/АлАТ) у больных острым окклюзионным деструктивным холециститом в раннем послеоперационном периоде
* Данные, изменение которых достоверно по отношению к норме при р < 0,05;" достоверность разницы между данными 2 групп при р < 0,05.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Клинико-лабораторные исследования у 65 больных острым холециститом, из них у 154 (93,3 %) — калькулезным, показали, что наиболее значимые функциональные изменения печени возникают при окклюзионном деструктивном холецистите с эмпиемой желчногопузыря (65 пациентов). Эта категория больных и взята в качестве объекта исследования с выделением 2 групп. Существенных различий по возрасту, полу, давности заболевания, общему состоянию, данным ультразвукового и эндоскопического обследования, показателям общего и биохимического анализа крови в обеих группах не было, что позволило провести сравнение результатов лечения больных, получавшими в послеоперационном периоде стандартизированную терапию и таковую с включением ремаксола.
Исследованиями установлено, что у больных в обеих группах при госпитализации в хирургическую клинику диагностирован синдром эндогенной интоксикации (табл. 1).
Таблица 1. Некоторые показатели эндогенной интоксикации у больных острым окклюзионным деструктивным холециститом на фоне применения ремаксола (М ± т)
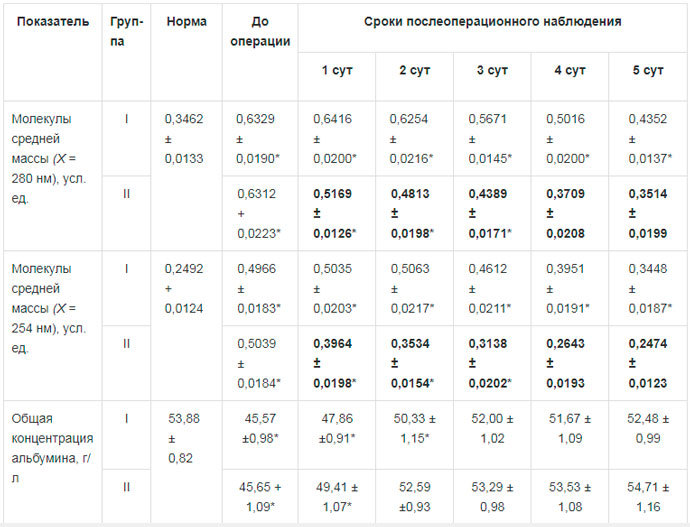
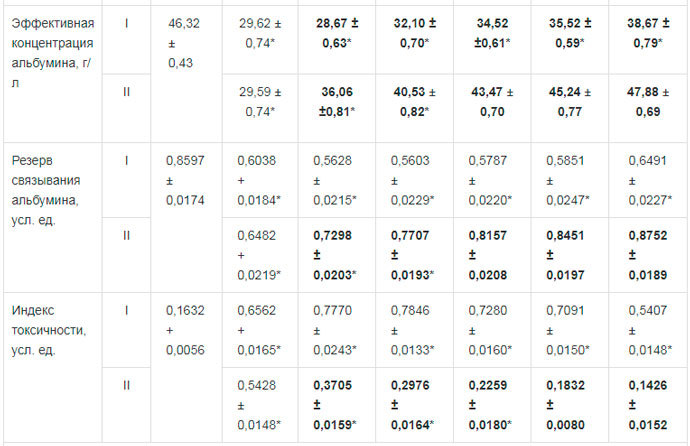
Примечание: I — группа сравнения; II — основная группа; * достоверность изменений по отношению к норме при р < 0,05; жирный шрифт — достоверность разницы между данными группы I и II при р < 0,05.
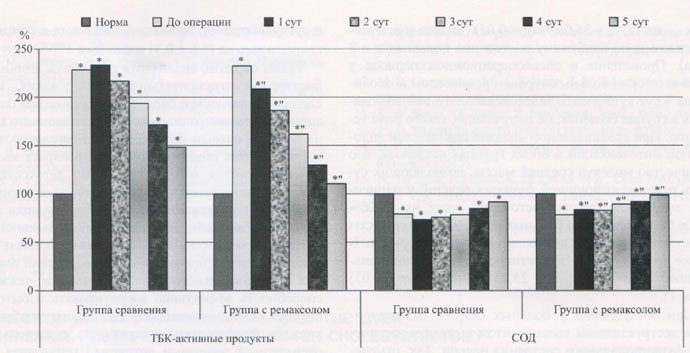
Рис. 3. Относительное количество ТБК-активных продуктов (малоновый диальдегид) и активность СОД в крови у больных острым окклюзионным деструктивным холециститом в раннем послеоперационном периоде.
* Данные, изменение которых достоверно по отношению к норме при p < 0,05; "достоверность разницы между данными 2 групп при p< 0,05.
Таблица 2. Некоторые показатели перекисного окисления л и пило в в крови у больных острым окклюзионным деструктивным холециститом на фоне применения ремаксола (М± т)
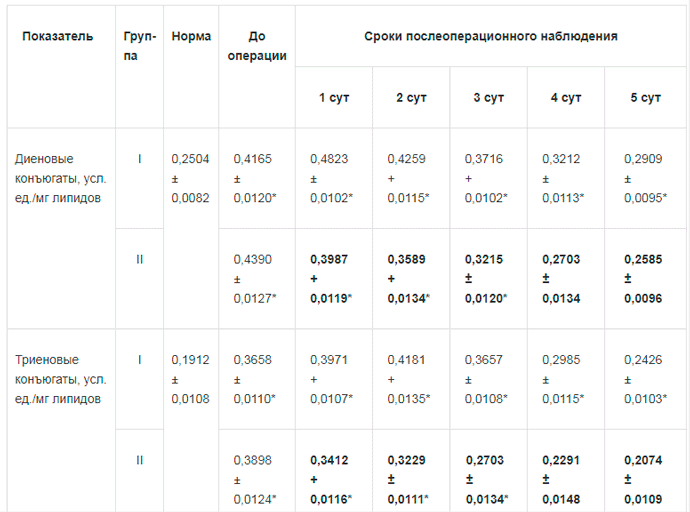
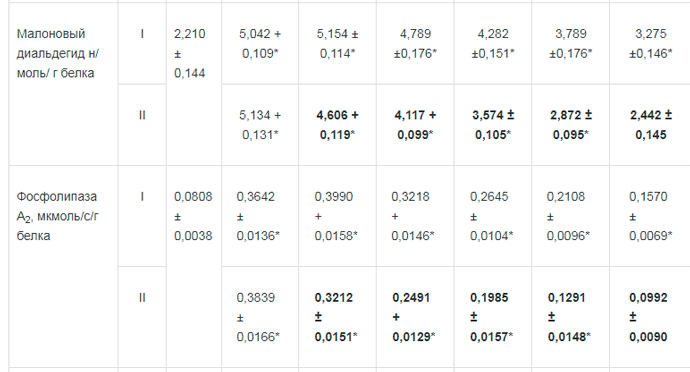
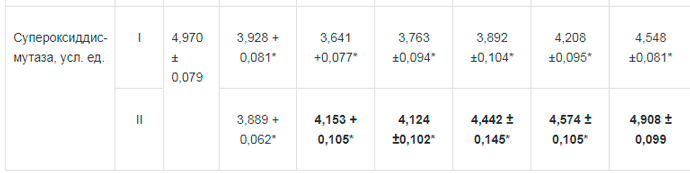
Примечание: I — группа сравнения; II— основная группа; * достоверность изменений по отношению к норме при р < 0,05; жирный шрифт - достоверность разницы между данными группы I и II при р < 0,05.
Содержание гидрофильных токсических продуктов увеличивалось в 1,83 - 2,02 раза (р < 0,05), гидрофильных — на 15,42 - 36,06 % (р < 0,05) (индекс токсичности плазмы по альбумину достоверно повышался в 3 раза). Проведение в послеоперационном периоде у этой категории больных терапии ремаксолом позволило на 4 сут купировать эндотоксикоз, что не наблюдалось в группе больных, не получавших такого рода терапию. При сравнительном анализе показателей эндогенной интоксикации в обеих группах оказалось, что количество молекул средней массы, позволяющих судить о детоксикационной функции печени, у пациентов во второй группе достоверно ниже на 19,26-26,06 % относительно больных первой группы на всем протяжении раннего послеоперационного периода. В то же время уровень эффективной концентрации альбумина был выше на 23,83-27,34% (р<0,05) (рис. 1).
При поступлении у больных острым окклюзион-ным деструктивным холециститом выявляли нарушения функционального состояния печени. Так, отмечено увеличение, по сравнению с нормой, содержания общего билирубина на 47,62 - 50,54 % (р < 0,05), активности сывороточных аминотрансфераз — на 30,01-109,02% (р<0,05). Применение ремаксола у больных в послеоперационном периоде позволило уменьшить количество билирубина относительно первой группы больных через 1 сут после операции на 11,22 % (р < 0,05), на 2 сут — на 12,71 % (р < 0,05), на 3 сут — на 22,14 % (р < 0,05), на 4 сут — на 20,11 % (р < 0,05) и на 5 сут — на 14,15 % (р < 0,05). Также отмечено уменьшение активности сывороточных аминотрансфераз — аланиновой (АлАТ) — на 16,17 - 28,21 % (р < 0,05), аспарагиновой (АсАТ) — на 7,25 - 12,02 % (р < 0,05) (рис. 2).
До операции у больных острым окклюзионным деструктивным холециститом обнаруживалось достоверное нарастание, по сравнению с нормой, интенсивности свободно-радикальных процессов липопере-окисления в 1,66 - 2,32 раза и активности фосфолипазы А2 — в 4,51 раза, снижение активности СОД — на 21,74%. Включение в комплексную послеоперационную терапию ремаксола позволило на 5 сут после операции нормализовать процессы перекисного окисления липидов, что не наблюдалось у больных в группе сравнения. Количество молекулярных продуктов липопереокисления во второй группе относительно первой группы было ниже на 11,13-26,09% (р < 0,05), активность фосфолипазы А2 — на 19,49-38,77%) (р < 0,05), активность СОД — выше на 7,91 - 14,13 % (р < 0,05) (табл. 2, рис. 3).
Отметим и другие клинико-лабораторные эффекты терапии ремаксолом. У больных основной группы, по сравнению с группой контроля, уменьшалась продолжительность температурной реакции на (1,4 ± 0,4) сут, уменьшалась продукция экссудата в подпеченочном пространстве на 17,2-29,3 % (оценка его уровня по дренажным трубкам), быстрее восстанавливалась функция кишечника на (10,3 ± 0,6) ч (по данным УЗИ и аускультативно), пребывание больных в стационаре сокращалось на (1,6 ± 0,3) койко-дня.
Таким образом, анализируя результаты клинико-ла-бораторно-инструментального исследования, можно сделать заключение о способности ремаксола оптимизировать течение раннего послеоперационного периода больных острым холециститом. Безусловно, одним из важнейших объектов влияния препарата является печень, функция которой, особенно детоксикацион-ная, при окклюзионном холецистите существенно нарушается, в патогенезе чего, как показали наши исследования, лежат избыточная интенсивность липопероксидации и активизация фосфолипазных систем. Важнейшее значение препарата в осуществлении повышения функционального статуса печени и лежит его способность эффективно корригировать избыточную интенсивность перекисного окисления мембранных липидов, фосфолипазную активность, повышать анти-оксидантный энзимный потенциал гепатоцита. Подчеркнем, что особенностью терапии с ремаксолом является ее быстрый положительный эффект. Существенное гепатопротекторное действие регистрируется уже через 1 сут после операции и введения препарата, когда нарушения печени манифестированы хирургической агрессией. Отметим еще и то, что в эффекте коррекции функционального состояния печени ремаксолом лежит не только его прямое гепатопротекторное действие, но и способность уменьшать воспалительный процесс в области пораженного органа.
ВЫВОДЫ
1. Добавление ремаксола (ежедневные внутривенные вливания 400 мл в течение 5 сут) к стандартной терапии в раннем послеоперационном периоде больным острым окклюзионным деструктивным холециститом с эмпиемой желчного пузыря приводит к существенному уменьшению нарушений функционального состояния печени: уменьшению количества билирубина на 2 - 5 сут на 11 - 20 % (р < 0,05), уменьшению активности сывороточных аминотрансфераз — аланиновой — на 16,17 - 28,21 % (р < 0,05), аспарагиновой на 7,25 - 12,02 % (р < 0,05) относительно показателей больных, получавших стандартное лечение.
2. Введение ремаксола в схему лечения сопровождалось сокращением продолжительности температурной реакции пациентов на (1,4 ± 0,4) сут, уменьшением продукция экссудата в подпеченочном пространстве на (17,2 - 29,3) %, ускорением восстановления I функции кишечника на (10,3 ± 0,6) ч, сокращением] пребывания больных в стационаре на (1,6 ±0,3) кой-ко-дней (р < 0,05).
ЛИТЕРАТУРА
1. Т. И. Виноградова, Д. С. Суханов, Н. В. Заболотных и др., Эксперим. и клин, фармакол., 74(2), 34 - 38 (2011).
2. В. А. Доровских, О. Н. Ли, Н. В. Симонова и др., Якутский мед. ж., 4(52), 21 -24 (2015).
3. М. В. Кукош, А. П. Власов, Острый холецистит, Наука, Москва (2009), с. 308.
4. Д. М. Курбанов, Н. И. Расулов, А. С. Ашуров, Новости хирургии, 22(3), 366 - 373 (2014).
5. Ф. И. Махмадов, К. М. Курбонов, Ф. X. Кузратов, С. Р. Рафиков, Вестник педагог, универ., 60(5), 152 - 156 (2014).
6. Г. Г. Мелконян, Р. Б. Мумладзе, А. В. Гейниц и др., Лазерная медицина, 18(3), 37 - 43 (2014).
7. Е. Д. Хворостов, Н. В. Черкова, С. А. Бычков, М. С. Томин, Хирургия Украины, 2(18), 062 - 066 (2006).
8. Ю. А. Грызунов, Альбумин сыворотки крови в клинической медицине, ГЭОТАР, Москва (1998).
9. В. А. Трофимов, Р. 3. Аширов, А. П. Власов, Биохимические методы исследования липидов в клинике, Учеб. Пособие, Крас. Окт., Саранск (2001).
10. Т. Acar, Е. Kamer, N. Acar, et al., Pan. Afr. Med. J., Jan., 31(26), 49 (2017); doi: 10.11604/pamj.2017.26.49.8359.
11. J. Ackerman, R. Abegglen, M. Scaife, et al., J. Trauma Acute Care Surg., Jul, 83(1), 55-60 (2017); doi: 10.1097 / TA.0000000000001515.
12. M. R. Gurgenidze, M. A. Kiladze, T. U. Tabucadze, Ann. Ital. Chir, 88 (2017); pii: S0003469X17021662.
13. S. de Sousa, O. Tobler, P. Iranmanesh, et al., Surg., Apr 17, 17(1), 39 (2017); doi: 10.1186 / sl2893 - 017 - 0232-z.
14. D. Papis, E. Khalifa, R. Bhogal, et al., Am Surg., Jun 1, 83(6), 623-627(2017).
15. N. Tartaglia, P. Cianci, A. Di Lascia, et al., Open Med. {Wars), Nov 13, 11(1), 429-432 (2016); doi: 10.1515 / med-2016-0078.
16. S. Tran, V. Choi, K. Hepburn, et al., ANZ J. Surg., May 16, (2017); doi: 10.1111/ans.l3986.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru








