Профилактика печеночной недостаточности при обширных резекциях печени
Статьи
Опубликовано в журнале:
« АНЕСТЕЗИОЛОГИЯ И РЕАНИМАТОЛОГИЯ » № 4, 2014
Хороненко В.Э., Донскова Ю.С., Баскаков Д.С., Дрожжина О.В., Сидоров Д.В., Ложкин М.В., Петров Л.О., Немцова Е.Р., Якубовская Р.И.
ФГБУ Московский научно-исследовательский онкологический институт им. П.А. Герцена МЗ РФ, 125284, Москва
Статья посвящена актуальной проблеме — профилактике пострезекционной печеночной недостаточности у онкологических больных. Представлены данные, полученные авторами при проведении контрольно-сравнительного исследования эффективности и безопасности применения отечественного препарата ремаксола у онкологических больных с метастазами колоректального рака в печень. Проведен сравнительный анализ динамики показателей цитолитического и холестатического синдромов, белоксинтетнческой функции печени, пигментного обмена, состояния про- и антиоксидантной систем и уровня эндогенной интоксикации в послеоперационном периоде.
Включение в схему анестезиологического пособия и интенсивной послеоперационной терапии раствора ремаксола позволило сократить сроки послеоперационной реабилитации, время пребывания пациентов в отделении интенсивной терапии и в стационаре.
Ключевые слова: пострезекционная печеночная дисфункция, ремаксол.
PROPHYLAXIS OF HEPATIC INSUFFICIENCY AFTER MAJOR HEPATIC RESECTIONS
Khoronenko V.E., Donskova Yu.S., BaskakovD.S., Drozhzhina O.V., Sidorov D.V., Lozhkin M.V., PetrovL.O., Nemtsova E.R., Yakubovskaya R.I.
Gertsen Moscow Research Oncological Institute, 125284, Moscow, Russian Federation
The article deals with a problem of prophylaxis of hepatic insufficiency in oncological patients after liver resections. Materials and methods: We analyzed data of effectiveness and safety of the use ofRemax ol in oncological patients with hepatic metastasis of colorectal cancer - dynamics of indicators of cytolysis and cholestasis, hepatic protein synthesis. exchange of pigments, pro- and antioxidant system and the level of endogen intoxication in postoperative period. Results: Use of Remaxol allows decreasing the duration of postoperative rehabilitation and intensive care unit staying.
Key words: hepatic dysfunction, hepatic resection, remaxol.
Введение.
В структуре онкологических заболеваний в России первичный рак ободочной кишки занимает 7-е место, а рак прямой кишки — 5-е место, уступая только новообразованиям легкого и предстательной железы у мужчин и молочной железы у женщин [1]. Синхронное метастатическое поражение печени диагностируется у 25% больных, еще у 35—45% метастазы выявляются при динамическом наблюдении (преимущественно в течение первых трех лет после удаления первичного очага) [2, 3]. При отсутствии лечения средняя продолжительность жизни этой категории больных редко достигает 1 года, варьируя от 6 до 18 мес [4].
Стандартом лечения метастазов колоректального рака в печень признается комбинированное лечение с проведением после- или периоперационной системной полихимиотерапии, основным условием успеха которого является выполнение операции в объеме R0 (макро- и микроскопическое отсутствие резидуальной опухоли). Резекция печени с последующим проведением системной химиотерапии позволяет достичь 5-летней выживаемости у 35—60%, что доказано значительным числом клинических наблюдений [2, 3, 5, 6].
Несмотря на совершенствование хирургических технологий, активное внедрение современной аппаратуры и накопление опыта, оперативные вмешательства в гепато-билиарной зоне по-прежнему остаются в группе высокого риска. Причиной смерти больных после расширенной гемигепатэктомии в 56—77% случаев является пострезекционная острая печеночная недостаточность (ОПН), развивающаяся в послеоперационном периоде [8]. Она же служит ограничением к проведению специфического противоопухолевого лечения.
Риск развития ОПН обусловлен несколькими факторами. Прежде всего это функциональная недостаточность остающегося объема паренхимы печени, часто обусловленная исходными дистрофическими или цирротическими изменениями. Вторым, не менее важным фактором риска является гипоксия, которая может носить циркуляторный (вследствие ишемии при пережатии гепатодуоденальной связки — прием Прингла), гемический (вследствие массивной кровопотери) или смешанный характер [8].
Летальность при развитии ОПН достигает 59%, стоимость комплексного лечения очень высока и определяется значительными расходами на растворы белков, трансфузионные среды, экстракорпоральные методы детоксикации, антибактериальные препараты, трудозатраты медицинского персонала. Поэтому поиск методов прогнозирования, эффективной профилактики и лечения пострезекционной ОПН является актуальным.
Методы профилактики развития ОПН можно условно разделить на две группы — хирургические и анестезиологические. К хирургическим методам относится комплексная предоперационная оценка функциональных резервов печени и прецизионный подход к рациональному выбору объема операции; применение кровесберегающих методик на интраоперационном этапе.
Анестезиологические методы можно условно разделить на общие и специфические. К первым относится тщательная предоперационная подготовка, включающая максимально возможное устранение нутритивной недостаточности, сердечно-сосудистых и бронхолегочных расстройств, компенсацию нарушений в системе гемостаза. Специфическим методом профилактики ОПН можно считать выбор компонентов анестезии, интра- и послеоперационной интенсивной терапии с минимальным гепатотоксическим эффектом и максимальными гепатопротекторными свойствами.
По данным литературы, на настоящий момент "золотым стандартом" анестезиологического обеспечения считают мультимодальную сочетанную анестезию на основе ингаляционного анестетика севофлурана и опиоидного анальгетика фентанила с эпидуральным компонентом (ропивакаин или ропивакаин + фентанил) и продленной эпидуральной анальгезией [9, 10]. Мультимодальный подход обеспечивает уменьшение доз всех компонентов анестезии до безопасных, эффективность и непрерывность антиноцицептивной защиты, стабильность гемодинами-ческих показателей, раннюю посленаркозную реабилитацию, быстрое восстановление моторики ЖКТ [11].
Тактика инфузионной терапии при выполнении расширенных операций на печени также имеет свои особенности. Для достижения "хирургического комфорта", уменьшения темпа и объема кровопотери на мобилизационном и резекционном этапах желательно поддерживать относительную гиповолемию. Наиболее часто в литературе описывают метод "сухого" резекционного этапа, когда темп и объем внутривенной инфузии существенно уменьшают, контролируя ЦВД на уровне 3—4 см вод. ст. Это наряду с использованием современных хирургических технологий позволяет снизить объем кровопотери (по данным ряда авторов, в 1,5 раза) даже без применения приема Прингла [12].
Наконец, в целях профилактики и лечения ОПН в схеме инфузионной терапии широко применяют различные препараты, обладающие гепатопротекторными свойствами. В связи с этим представляет большой интерес отечественный раствор для инфузий ремаксол (ООО ПО-ЛИСАН, СПб.), в состав которого входят соль янтарной кислоты, метионин, N-метилглюкамин и рибоксин.
Каждый компонент ремаксола обладает антиоксидантными, антигипоксантными и иммуномодулирующими свойствами, осуществляющимися посредством различных механизмов действия и выраженными в разной степени. Янтарная кислота, являющаяся центральным субстратом цикла Кребса, интенсифицирует клеточное дыхание, обеспечивает утилизацию кислорода тканями, повышает устойчивость мембран гепатоцитов к гипоксии.
Метионин способствует синтезу холина, с недостаточным образованием которого связаны нарушение синтеза фос-фолипидов из жиров и отложение в печени нейтрального жира, путем метилирования и транссульфирования обезвреживает токсичные продукты. Рибоксин повышает активность ряда ферментов цикла Кребса, стимулирует синтез нуклеотидов, обменные процессы в клетках и повышает их энергетический баланс. Никотинамид активирует NAD-зависимые ферменты клеток, в том числе антиоксидантные системы убихиноновых оксиредуктаз, защищающие мембраны клеток от разрушения свободно-радикальными частицами [13, 14].
Таким образом, ремаксол обладает многообразными гепатопротекторными свойствами, подтвержденными в экспериментальных [15, 16] и клинических [17, 18] исследованиях, и его применение в схеме профилактики/лечения ОПН представляется патогенетически оправданным.
Цель данного исследования — изучить эффективность применения ремаксола для профилактики развития пострезекционной ОПН при выполнении расширенных гемигепатэктомии по поводу метастазов колоректального рака.
Материал и методы.
В рамках научного протокола проведено рандомизированное контрольно-сравнительное исследование эффективности и безопасности применения препарата ремаксол у онкологических больных с метастазами колоректального рака в печень (состояние после хирургического удаления первичного очага), которым выполнены обширные резекции печени. Обследованы две группы больных, сопоставимых по полу, возрасту, функциональному состоянию печени и объему операции. Рандомизацию пациентов проводили с помощью программы случайных чисел. В основной группе (n = 40, мужчин 14, средний возраст 54,5 ± 4,7 года; женщин 26. средний возраст 57.3 ± 5,1 года) в схему интра- и послеоперационной инфузионной терапии включали ремаксол 800 мл в сутки, в контрольной группе (и = 35, мужчин 15. средний возраст 56,3 ± 2,8 года; женщин 20. средний возраст 55,9 ± 3,4 года; в качестве гепатопротекто-ра использовали адеметионин (Гептрал, Hospira S.p.A., Италия) 800 мг(10 мл). Инфузию препаратов начинали интраоперацион-но и продолжали в ОРИТ в течение 5 сут после операции. Наблюдение за клиническим состоянием больных и динамикой показателей метаболизма осуществляли до выписки из стационара (в среднем в течение 12 сут после операции).
Оценивали динамику объективных и субъективных показателей состояния пациентов: жалоб, температурной реакции, физической активности, физиологических отправлений; фиксировали сроки перевода из ОРИТ и выписки из стационара.
Всем пациентам проводили сочетанную мультимодальную общую анестезию с эпидуральной анальгезией и ИВЛ на основе фентанила (средняя общая доза 0.0008 ± 0,00002 мг/кг × ч), пропофола (средняя общая доза 1,1 ±0,4 мг/кг × ч), ингаляционного анестетика севофлурана (0,7 ± 0,2 МАК) [8]. По общим правилам проводили катетеризацию эпидурального пространства на уровне
VIII-
X, с продвижением катетера краниально до уровня
VI-
VII. После введения тест-дозы 2% раствора лидокаина — 2,0, осуществляли постоянную инфузию 0,33% раствора ропивакаина гидрохлорида (наропин 0,75%, AstraZeneca) при помощи инфузионного шприцевого насоса.
Начальная скорость инфузии ропивакаина составляла 10—12 мл/ч, далее после распределения раствора анестетика в эпидуральном пространстве, скорость уменьшали до 4—6 мл/ч. Средняя общая доза составила 0,28 ± 0,03 мг/кг × ч. Внутривенную инфузию начинали с введения кристаллоидного раствора (раствор Рингера 500 мл) и гепатопротектора ремаксол 400 мл или гептрал 400 мг согласно программе рандомизации. Учитывая большую поверхность операционной раны и значительную продолжительность операции (среднее время 327 ±113 мин) для предотвращения избыточной потери тепла использовали прибор конвекционного обогрева пациента (Bair Hugger, Frizant International, США).
На этапах мобилизации и резекции печени с целью снижения кровопотери и обеспечения комфортных условий для работы хирургов ограничивали скорость внутривенной инфузии (в среднем 5,6 ± 0,6 мл/кг × ч), во время последующих хирургических этапов ее увеличивали (в среднем до 18,75 ± 2,9 мл/кг × ч), достигая компенсации жидкостных потерь. Темп диуреза на всех этапах оставался стабильным, не ниже 80—90 мл/ч, ЦВД на резекционном этапе поддерживали на уровне 3—5 см вод. ст., на последующих этапах — 7—9 см вод. ст.
Средняя продолжительность операций составила 327 ± 113 мин, кровопотеря — 630 ± 197 мл. Прием Принта во время хирургического вмешательства не применяли.
По окончании операции осуществляли перевод больных в отделение реанимации и интенсивной терапии (ОРИТ), где продолжали ИВЛ, инфузию и мониторирование основных жизненно важных показателей.
В ОРИТ всем пациентам проводили продленную эпидураль-ную анальгезию ропивакаином (наропин 0,2%) со скоростью 4—8 мл/ч при помощи волюметрического инфузомата или микро-инфузионной помпы. Согласно принятой в институте методике ведения больных, оперированных в гепатобилиарной зоне, пациенты получали в виде постоянной инфузии лорноксикам (ксефокам, Dr. Madaus GmbH, Германия) со скоростью 16 мг/сут и каль-цитонин (миакальцик, Novartis Pharma, Швейцария) 350 мг/сут для предупреждения чрезмерной системной воспалительной реакции и снижения секреторной активности поджелудочной железы [18]. По согласованию с хирургами, учитывая возможное развитие явлений гепатоцеллюлярной недостаточности и связанной с ней гипокоагуляции, профилактику тромбоэмболических осложнений низкомолекулярными гепаринами в 1-е сутки не проводили, начиная ее под контролем гемостазиограммы на 2—3-й сутки после операции.
Пациенты основной группы получали ремаксол 800 мл/сут, а пациенты контрольной группы — гептрал 800 мг/сут в течение следующих после операции 4-х суток. Общий объем внутривенной инфузии назначали из расчета 40 мл/кг/сут, трансфузию эритроцитов осуществляли при уровне Нb Перевод больных из ОРИТ в профильное отделение осуществляли при условии стабильной гемодинамики, тенденции к нормализации показателей лабораторных тестов, отсутствии клинико-лабораторных признаков наличия системной воспалительной реакции, явлений токсической или дисциркуляторнои энцефалопатии, удовлетворительного самочувствия.
Исследование крови осуществляли на следующих этапах: исходно до операции, в 1, 5 и 12-е сутки после операции. Анализировали общие клинические показатели, показатели биохимического состава (общий белок, альбумин, мочевина, креатинин, билирубин общий и фракции, аспартатаминотрансфераза (ACT), аланинаминотрансфераза (АЛТ), щелочная фосфатаза (ЩФ), гамма-глутамилтранспептидаза (ГГТП), С-реактивный протеин), показатели гемостаза (протромбиновое время, протромбин по Квику, активированное частичное тромбиновое время — АЧТВ, международное нормализованное отношение — MHO, показатели окислительно-антиокислительного статуса (концентрация малонового диальдегида (МДА), лактоферрина (ЛФ), активность церулоплазмина(ЦП), каталазы (КАТ), коэффициент окислительно-антиокислительного баланса (К0АС)). К0АС рассчитывали по формуле: КОАС = ЦПб/ЦПн × КАТб/КАТн × ЛФ/ЛФн × МДДб/МДАн,
где б — показатели больного, н — значение нормы, полученное при исследовании крови здоровых доноров нашего региона.
Выраженность дисфункции печени оценивали по динамике биохимических показателей цитолиза (ACT, АЛТ), холестаза (ЩФ), белоксинтетической функции (уровень альбумина, протромбиновый индекс). Дополнительно проводили оценку степени тяжести печеночной недостаточности по шкале Child—Pugh [20].
Шкала Child—Pugh впервые была опубликована в 1964 г и с тех пор почти не претерпела изменений. Разработанная для прогноза осложнений и летальности при циррозах печени, шкала позволяет оценить степень гепатоцеллюлярной недостаточности: суммируются балльные эквиваленты признаков, выявляемых у больного; степени А соответствует 5—6 баллов, степени В — 7—9, степени С — 10—15. Таким образом, общее количество баллов возрастает в зависимости от тяжести печеночно-клеточной недостаточности, при степени С вероятность летального исхода составляет 70% (табл. 1).
Таблица 1.
Критерии оценки функционального состояния печени по шкале Child—Pugh
| Клинические и биохимические показатели | Оценка, баллы |
|---|
| 1 | 2 | 3 |
|---|
| Асцит | Нет | Транзиторный | Стабильный |
| Энцефалопатия | Нет | 1—2 | 3—4 |
| Билирубин | | 35—50 | > 50 |
| Билирубин при первичном билиарном циррозе | | 68—171 | > 171 |
| Альбумины | >35 | 28—35 | | Протромбиновый индекс/МНО, % | 90—75 | 75—62,5 | | Сумма баллов | 5—6 — А | 7—9 — В | 10—15 — С |
В последние годы оценку тяжести пострезекционной гепатоцеллюлярной недостаточности и прогнозирование летальности чаще проводят по критерию fifty-fifty, который основан на количественном определении уровня билирубина и протромбинового индекса: при снижении протромбинового индекса 50 мкмоль/л на 5-й день после операции риск летального исхода достигает 59% [21].
Обе эти шкалы эффективны при прогнозировании риска осложнений и летальности после резекций печени, но не учитывают показателей, характеризующих степень цитолиза и холестаза, рутинно используемых в клинической практике.
Динамика печеночных аминотрансфераз и ЩФ отражает процессы, происходящие в печени после расширенных резекций.
Использование современных хирургических инструментов позволяет значительно снизить интраоперационную кровопотерю, но при этом формируется обширная ожоговая поверхность остающейся паренхимы печени и может повышаться внутрипеченочное давление, приводящее к дополнительной потере гепатоцитов. Повышение уровня аминотрансфераз до 300—400 усл. ед/л указывает на прямое повреждение печени и некроз гепатоцитов [22].
Результаты исследования и их обсуждение.
Всем обследованным больным выполнены оперативные вмешательства запланированного объема. Осложнений, связанных с общей анестезией или инфузией растворов гепатопротекторов, не отмечено. Время продленной ИВЛ после окончания операции составило в среднем 1,6 ± 0,3 ч в обеих группах наблюдения, без достоверных отличий.
Исходно в биохимических показателях функции печени у пациентов обеих групп отклонений не было. По шкале Child—Pugh они соответствовали 5 баллам (группа А), что свидетельствует об отсутствии нарушений [18]. Уровни билирубина, аминотрансфераз и показатели гемостаза находились в пределах нормальных значений.
На протяжении всего периода исследования после расширенных гемигепатэктомий у пациентов обеих групп регистрировали лабораторные признаки транзиторной печеночной дисфункции, соответствующие синдромам гепа-тоцеллюлярной недостаточности и цитолиза: снизились уровни общего белка, альбумина, протромбина, выросли уровни печеночных аминотрансфераз, общего билирубина. Динамика основных лабораторных показателей представлена в табл 2.
Проведена сравнительная оценка функциональной способности печени по шкале Child—Pugh между группами: в 1-е сутки после операции у больных основной группы соответствовала 9 баллам (группа В), что свидетельствовало о субкомпенсированном состоянии нарушений, а у больных контрольной группы — 11 баллам (группа С), т.е. имела место декомпенсация расстройств. К 5-м суткам послеоперационного периода степень тяжести печеночной дисфункции в основной группе имела тенденцию к снижению — 8 баллов, тогда как в контрольной группе сохранялся прежний уровень нарушений — 11 баллов. К 12-м суткам после операции функциональные показатели печени в обеих группах выравнивались. Степень тяжести печеночной дисфункции соответствовала группе В и составила 7 и 8 баллов соответственно.
Важным аспектом биохимической активности гепатоцитов является синтез белков, относящихся к факторам свертывания крови. Анализ белоксинтезирующей функции печени после обширных резекций показал, что в 1-е сутки после операции у пациентов обеих групп имело место резкое снижение альбумина и протромбина и увеличение АЧТВ при нормальном уровне тромбоцитов. Эти показатели имели тенденцию к нормализации в последующие сутки, однако у пациентов контрольной группы на всех этапах послеоперационного исследования восстановление шло медленнее и исследуемые показатели достоверно отличались от основной группы (см. таблицу). Ни в основной, ни в контрольной группах уровни альбумина, протромбина и АЧТВ не достигали исходных значений к 12-м суткам.
Анализ объемов заместительной инфузионно-трансфузионной терапии, проводимой в обеих группах, выявил достоверное (р Таким образом, из вышесказанного следует, что периоперационное применение ремаксола способствовало более раннему восстановлению белоксинтезирующей функции оперированной печени.
В результате лизиса печеночных клеток вследствие коагуляции и воспаления в 1-е сутки происходило многократное повышение уровней аминотрансфераз в обеих группах. В основной группе кратность повышения составила 1:14,5, а в контрольной 1:20 (см. рисунок). К 5-м суткам в обеих группах регистрировали выраженную положительную динамику, но кратность снижения уровней ACT и АЛТ была примерно в 2 раза выше в основной группе. К 5-м суткам в основной группе она составила 1:3, в контрольной — 1:6, а к 12-м суткам — 1:1,6 и 1:3 соответственно. Такая динамика снижения уровней печеночных ферментов, по нашему мнению, свидетельствует о положительном влиянии ремаксола на скорость элиминации продуктов цитолиза из плазмы крови (см. рисунок).
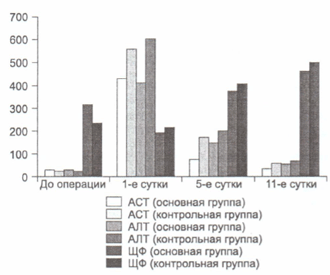
Рис. Динамика биохимических показателей на этапах лечения.
Интерпретация динамики ЩФ представляет большие трудности. Высокое содержание ЩФ отмечается преимущественно в печени и костях, 20% находится в стенке кишечника. Активность фермента растет, когда в соответствующих тканях имеется метаболическая стимуляция. Так, в пубертатном периоде уровень ЩФ возрастает в 2 раза по сравнению с нормой для взрослых за счет костного изофермента, активность которого ассоциирована с бурным ростом костной ткани. В клинической практике фракционное определение изоферментов ЩФ обычно не проводят, поэтому повышение уровня ЩФ при болезнях печени традиционно связывают с синдромом холестаза (в совокупности с гипербилирубинемией и повышением уровня ГГТП).
Активность ЩФ в 1-е сутки после операции снизилась в сравнении с исходной у пациентов обеих групп (достоверность отличий получена только в основной группе, р Таблица 2.
Динамика клинико-лабораторных показателей на этапах хирургического лечения
| Показатель | Значения показателей на этапах исследования в группах |
|---|
| до операции | 1-е сутки | 5-е сутки | 11 — 12-е сутки |
|---|
основная,
n = 40 | контроль,
n = 35 | основная,
n = 40 | контроль,
n =35 | основная,
n = 40 | контроль,
n = 35 | основная,
n = 40 | контроль,
n = 35 |
|---|
| Основные пабораторные показатели |
|---|
| ACT, усл. ед/л | 30.8 ±7,1 | 25,1 ±8,3 | 434,2 ± 78,2*, ** | 560,3 ± 100.1* | 74.2 ± 19,4*. ** | 171,0 ±14,6*.** | 34,28 ± 9,3 | 59.42 ± 9,8 |
| АЛТ, усл. ед/л | 32,9 ± 11,4 | 22,9 ± 13,7 | 415,7± 81,3*,** | 593,4 ± 77,4* | 148,6 ± 16,9*, ** | 203,4 ± 19,1*,** | 54,66 ± 8,6 | 63,22 ± 7.8 |
| ЩФ, усл. ед | 317.5 ±38,9 | 233,8 ±45,5 | 194 ± 33,1* | 216,9 ±57,2 | 375,9 ±64,3 | 409,3 ± 49.9 | 463.8 ±57.3* | 502.1 ±48.9* |
| Общий билирубин, ммоль/л | 11,82 ±7,4 | 14,7 ±6.1 | 34,56 ± 11,3 | 52,17 ± 10,8 | 17,85 ±6,8** | 47,51 ± 14,7 | 13,25 ±7,7** | 24.84 ± 9,8 |
| Общий белок, г/л | 72,3 ± 5,5 | 72,9 ± 4.4 | 54,8 ±6,9 | 50,9 ±8.6 | 53,2 ±4.1 | 50,0 ±5,3 | 58,5 ±4,2** | 52.0 ±3,4 |
| Альбумин, г/л | 32,9 ±2,1 | 33,0 ±2,3 | 27,8 ±2.4 | 21,2 ± 3,0*,** | 28, 4 ± 2,9 | 20,0 ± 2 2* ** | 28,82 ±3.6 | 22,47 ± 3,1* ,** |
| Протромбин, % | 92,3 ± 10,8 | 91,9± 11,6 | 52,87 ± 12,4* | 50,41 ± 10,8* | 63,8 ± 11,7* .** | 51,7 ± 12,9 | 70,4 ± 11,8*,** | 65.1 ± 12,9 |
| Child—Pugh, баллы | 5 | 5 | 9 | 11 | 8 | 11 | 7 | 8 |
| Показатели окислительно-антиокислительной системы |
|---|
МДА 2,8—3,3,
мкмоль/л | 4,45 ± 0,3 | 4,42 ± 0,2 | 4,3 ±0,2* | 5,3 ± 0,3 | 4,0 ±0,1* | 5,1 ±0,1 | 3,5 ± 0,2* | 4,4 ± 0,3 |
ЦП 0,49— 0,57,
мг/л | 0.61 ±0,001 | 0.63 ±0,001 | 0,54 ± 0.002* | 0.50 ±0,001* | 0,51 ±0,001* | 0,46 ± 0,001*. ** | 0,55 ± 0,002*. ** | 0,49 ±0,001 |
КАТ 500— 600,
усл. ед | 647,8 ± 101 | 671.34 ± 104 | 851,45 ± 135*,** | 573,37 ± 114 | 722.54 ± 98*, ** | 517,98 ± 100 | 725,75 ± 103*,** | 578.19± 117 |
| К0АС 0,8-1,1 | 0,6 | 0,7 | 0,7* ,** | 0.4 | 0,6*, ** | 0,3 | 0.8*,** | 0.4 |
| Примечание. * —р |
Подобная динамика активности ЩФ может быть обусловлена инициацией викарной гипертрофии печеночной ткани (по аналогии с повышением активности ЩФ при бурном росте остеобластов). Однако это смелое предположение, безусловно, нуждается в подтверждении на основании дальнейшего исследования и анализа клинического материала, который проводится в институте.
Известно, что в основе физиологических и патофизиологических процессов в организме лежат окислительно-восстановительные реакции. Среди них важное место занимают реакции перекисного окисления липидов (ПОЛ). Нарушение баланса между активностью окислительных и антиокислительных процессов ведет к развитию так называемого окислительного стресса, с возникновением эндотоксикоза и иммуносупрессии, которые могут благоприятствовать манифестации онкологических заболеваний.
Для онкологических пациентов, особенно на поздних стадиях развития опухоли, характерно повышение активности окислительных процессов при одновременном угнетении антиокислительных [23]. В нашем исследовании у пациентов обеих групп исходно отмечали возрастание уровня МДА и некоторое напряжение системы детоксикации организма — повышение активности ЦП, снижение активности каталазы, умеренное снижение К В 1-е сутки после операции активность процессов ПОЛ в обеих группах возрастала, показатели антиоксидантного звена ОАС снижались (табл. 2). Регистрировали дальнейшее снижение К0АС, что свидетельствовало о наличии окислительного стресса, более выраженное в контрольной группе. К 5-м суткам у пациентов основной группы появлялась тенденция к нормализации показателей антиоксидантного статуса, которая проявлялась в снижении уровня МДА. У пациентов контрольной группы сохранялся высокий уровень ПОЛ и депрессия антиокислительных процессов (дальнейшее снижение КОАС).
Для хирургических пациентов с печеночной недостаточностью характерно падение активности эндогенного антиоксиданта ЦП [23]. Динамика ЦП у пациентов обеих групп была одинаковой. В 1-е и 5-е сутки после операции отмечалось снижение активности ЦП, более выраженное в контрольной группе, однако без значимых отличий (см. табл. 1). К окончанию исследования активность ЦП восстановилась до нормальных значений, хотя у пациентов контрольной группы оставалась на нижней границе нормы. КОАС у пациентов основной группы к 12-м суткам также достиг нормы, в контрольной группе оставался вдвое ниже нормальных значений, что свидетельствовало о сохраняющемся глубоком дисбалансе между звеньями окислительно-антиокислительной системы и высоком риске возникновения воспалительных осложнений.
Пациенты основной группы наблюдались в ОРИТ 1,9 ± 0,7 сут, контрольной — 2,6 ± 1,1 сут, выписаны из стационара соответственно на 11 ± 0,5 и 13 ± 0,9-е сут после хирургического лечения.
Заключение
Комплексный мультимодальный подход к предоперационной подготовке, интра- и послеоперационному ведению онкологических пациентов с метастатическим поражением печени с включением в схему поддерживающей терапии препаратов гепатопротективного действия позволяет достичь хороших непосредственных результатов хирургического лечения при выполнении обширных резекций печени. Включение в схему инфузионной терапии раствора ремаксола представляется целесообразным. Компоненты ремаксола способствуют быстрому регрессу лабораторных проявлений печеночной дисфункции, восстановлению баланса окислительно-антиокислительных процессов и сокращению сроков послеоперационной реабилитации.
Проведенное исследование показало, что патогенетически обоснованная инфузионная терапия растворами ремаксол и адеметионин способствует коррекции дисфункции печени. При сравнительном анализе показателей интенсивности цитолитического и холестатического синдромов, белоксинтетической функции печени, пигментного обмена, состояния про- и антиоксидантной систем и уровня эндогенной интоксикации оптимальные значения, наиболее близкие к исходным, были получены в группе пациентов, получавших ремаксол.
На основании полученных результатов следует признать целесообразным включение инфузионного гепато-протектора ремаксол в схему инфузионной терапии онкологических пациентов в периоперационном периоде.
REFERENCES * ЛИТЕРАТУРА
1. Chissov V.I., Starinskiy V.V., PetrovaG.V. Malignant Neoplasms in Russia in 2009. Moscow; 2010 (in Russian).
2. Adam R., Pascal G., Azoulay D. et al. Liver resection for colorectal metastases: the third hepatectomy. Ann. Surg. 2003; 238: 871—83.
3. Bengtsson G., Carlsson G., Hafstro M.L., Jonsson P.E. Natural history of patients with untreated liver metastases from colorectal cancer. Am. J. Surg. 1981; 141:586—9.
4. Kanas G.P., Taylor A., Primrose J.N., Langeberg W.J., Kelsh M.A., Mowat F.S. et al. Survival after liver resection in metastatic colorectal cancer: review and meta-analysis of prognostic factors. Clin. Epidemiol. 2012; 4: 283—301.
5. Gallagher D.J., Kemeny N. Metastatic colorectal cancer: from improved survival to potential cure. Oncology. 2010; 78 (3—4): 237—248.
6. Simmonds PC, Primrose J.N., Colquitt J.L. et al. Surgical resection of hepatic metastases from colorectal cancer: A systematic review of published studies. Br. J. Cancer 2006; 94: 982—99. 7. Blumgart L.H. Surgery of the Liver and Biliary Tract. New York: Churchill Livingstone; 2006.
8. Kotiv B.N., Dzidzava 1.1., Alent'ev S.A., Kashkin D.P. Slobody-anik A.V. Extensive resection in the treatment of malignant liver tumors. Sovremennye tekhnologii meditsine. 2010: 1: 34—5 (in Russian).
9. Osipova N.A., Petrova V.V., Mitrofanov S.V., Beresnev V.A.. Don-skova Yu.S. et al. Systemic and regional patient pain protection in surgery. The problem of choice. Anestheziologiya i reanimatologi-ya, 2006; 4: 12—6 (in Russian).
10. Ovezov A.M. Anesthetic management of liver resections. Al'manakh anesthesiologii i reanimatologii. 2005; 5: 34—5 (in Russian).
11. Osipova N.A., Khoronenko V.E., Shemetova M.M. Anesthetic management of geriatric patients with coexisting cardiovascular disease in oncology. Sevoflurane as a component of multimodal general anesthesia. Klinicheskaya gerontologiya. 4—5: 39—50 (in Russian).
12. Maartje A„ Steven W.M., Cornells H.C. Liver failure after partial hepatic resection: definition, pathophysiology, risk factors and treatment. Liver Int. 2008; 26 (8): 767—80.
13. Khazanov B.A. Pharmacological regulation of energy metabolism. Exsperimental'naya i klinicheskaya farmakologiya. 2009; 34: 61— 4 (in Russian).
14. De Groot H. Reactive oxygen species in tissue injury. Hepatogas-troenterology. 1994; 41: 328—32.
15. Bezborodova O.A., Nemtsova E.R., Aleksandrova L.N., Sukha-nov D.S., Kovalenko A.L., Yakubovskaya R.I. Evaluation detoxifying action of "Remaksol" on the model of toxicity induced by cisplatin. Experimental'nay a farmakologiya. 2011; 74 (3): 26—31 (in Russian).
16. Sukhanov D.S., Vinogradova Т.1., Zabolotnykh N.V., Kovalenko A.L., Vasil'eva S.N.. Romantsov M.G. Comparative study of hepatoprotective action of remaksol, reamberin and ademetionine liver damage when anti-TB drugs. (Experimental study) Antibiotiki i khimioterapiya. 2011; 56(1— 2): 12—6.
17. Yakovlev A.Yu., Semenov V.B., EmePyanov N.V., Mokrov K.V., Zubeev N.S., Akulenko S.V., Zarechenkova N.V. Infusion in correction of bile outflow and endotoxemia in patients with mechanical icterus. Vestnik khirurgii im. I.I. Grekova. 2011; 170 (3): 23—6 (in Russian).
18. Koval'chuk L.V., Ovanesyan E.R., Gorskiy V.A., Leonenko I.V., Khoreva M.V., Agapov M.A. et al. Cytokine-antagonist therapy in complex treatment of destructive pancreatitis: possibilities and prospects. Consilium Medicum. Khirurgiya. 2011; 1: 43—6 (in Russian).
19. Tolpinets A.V., Khoronenko V.E., Donskova Yu.S., Edeleva N.V., Petrova V.V.. Kudryavtsev S.B., Pankratova M.A. Perioperative management of cancer patients with extended hemihepateclomy complicated by supermassive hemorrhage (case). Anestheziologiya i reanimatologiya. 2012; 5: 47—50 (in Russian).
20. Pugh R.N., Murray-Lyon I.M., Dawson J.L., Pietroni M.C., Williams R. Transection of the oesophagus for bleeding oesophageal varices. Br. J. Surg. 1973; 60 (8): 646—9.
21. Schroeder R.A.. Marroquin C.E., Bute B.P. Predictive indices of morbidity and mortality after liver resection. Ann. Surg. 2006; 243: 373—9.
22. Podymova S.D. Liver Disease. Guidance for Doctors. 4th ed. Moscow: Meditsina; 2006 (in Russian).
23. Edeleva N.V., Sergeeva TV., Nemtsova E.R., Osipova N.A. Antioxidants ceruloplasmin and lactoferrin in the prevention and treatment of postoperative complications in patients with cancer. Anes-thesiologiya i reanimatologiya. 2001; 5: 61—4 (in Russian).
* * *
1. Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2009 г. М.; 2010.
9. Осипова Н.А.. Петрова В.В., Митрофанов СВ.. Береснев В.А.. Донскова ЮС. и др. Системная и регионарная антиноцицеп-тивная защита пациента в хирургии. Проблема выбора. Анестезиология и реаниматология. 2006; 4: 12—6.
10. Овезов A.M. Анестезиологическое обеспечение резекций печени. Альманах анестезиологии и реаниматологии. 2005; 5: 34—5.
11. Осипова Н.А., Хороненко В.Э.. Шеметова М.М. Анестезиологическое обеспечение гериатрических пациентов с сопутствующими сердечно-сосудистыми заболеваниями в онкохи-рургии. Севофлуран как компонент мультимодальной общей анестезии. Клиническая геронтология. № 4—5: 39—50.
13. Хазанов Б.А. Фармакологическая регуляция энергетического обмена. Экспериментальная и клиническая фармакология. 2009:34: 61—4.
15. Безбородова О.А., Немцова Е.Р., Александрова Л.Н., Суханов Д.С, Коваленко А.Л., Якубовская Р.И. Оценка детоксици-рующего действия препарата "Ремаксол" на модели токсикоза, индуцированного цисплатином. Экспериментальная фармакология. 2011; 74 (3): 26—31.
16. Суханов Д.С, Виноградова Т.Н., Заболотных Н.В., Коваленко А.Л., Васильева С.Н., Романцов М.Г. Сравнительное изучение гепатопротективного действия ремаксола, реамберина и адеметионина при повреждении печени противотуберкулезными препаратами (Экспериментальное исследование). Антибиотики и химиотерапия. 2011; 56 (1—2): 12—16.
17. Яковлев А.Ю., Семенов В.Б., Емельянов Н.В., Мокрое КВ.. Зубеев Н.С, Акуленко СВ., Зареченкова Н.В. Инфузионная коррекция желчеоттока и эндотоксикоза у больных с механической желтухой. Вестник хирургии им. И.И. Грекова. 2011: 170(3): 23—6.
18. Ковальчук Л.В., Ованесян Э.Р., Горский В.А., Леоненко И.В., Хорева М.В., Агапов М.А. и др. Цитокинантагонистическая терапия в комплексном лечении деструктивного панкреатита: возможности и перспективы. Consilium Medicum. Хирургия. 2011; 1:43—6.
19. Толпинец А.В., Хороненко В.Э., Донскова ЮС, Эделева Н.В., Петрова В.В., Кудрявцев СБ., Панкратова М.А. Периопераци-онное ведение онкологического больного с расширенной геми-гепатэктомией, осложнившейся сверхмассивной кровопотерей (клинический случай). Анестезиология и реаниматология. 2012;5:47-50.
22. Подымова С.Д. Болезни печени. Руководство для врачей. 4-е изд. М.: Медицина; 2006.
23. Эделева Н.В., Сергеева ТВ., Немцова Е.Р., Осипова Н.А. Антиоксиданты церулоплазмин и лактоферрин в профилактике и лечении послеоперационных осложнений у онкологических больных. Анестезиология и реаниматология. 2001; 5: 61—4. Received. Поступила 20.05.14
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru

