Эффективность инфузионного гепатотропного препарата ремаксол в патогенетической терапии хронических вирусных гепатитов на цирротической стадии
Статьи
Опубликовано в журнале:
«ТЕРАПЕВТИЧЕСКИЙ АРХИВ», 2015, № 8, с. 67-72
В.В. Стельмах1, В.К. Козлов1-3, В.Ф. Иванова1, И.А. Самусенко4
1ФБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия;
2ГБОУ ВПО «Новгородский государственный университет им. Ярослава Мудрого», Великий Новгород, Россия;
3ФГБОУ ВПО «Санкт-Петербургский государственный университет», Санкт-Петербург, Россия;
4ФГУЗ «Всероссийский центр экстренной и радиационной медицины им. А.М. Никифорова» МЧС России, Санкт-Петербург, Россия
Резюме
Цель исследования. Изучение влияния терапии инфузионным гепатопротектором ремаксолом на функциональное состояние печени при циррозах в исходе хронических вирусных гепатитов (ХВГ) HCV, HBV, HCV+HBV, HBV+HDV.
Материалы и методы. Обследовали 65 пациентов в возрасте от 26 до 76 лет с диагнозом цирроз печени (ЦП) в исходе ХВГ HCV, HBV, HCV+HBV, HBV+HDV. Пациенты с ЦП в исходе ХВГ В, С (n=32) при проведении инфузионной терапии ежедневно внутривенно капельно получали ремаксол по 400 мл 1 раз в сутки в течение 11 дней. Группу сравнения составили 33 пациента с аналогичной патологией, которым внутривенно струйно вводили адеметионин 400 мг на фоне инфузионной терапии кристаллоидами (400 мл изотонического раствора натрия хлорида, раствор Рингера) в течение 11 дней.
Результаты. После окончания курса инфузионной терапии в основной группе больных зарегистрировано более существенное уменьшение показателей цитолиза, холестаза. Выраженный гепатотропный эффект препарата подтверждался темпами снижения средних концентраций аланинаминотрансферазы, аспартатаминотрансферазы и общего билирубина. Относительные величины снижения уровней этих биохимических показателей у больных основной группы составили 29, 29 и 40% против 15, 20 и 9% у пациентов контрольной группы.
Заключение. Использование инфузионной терапии ремаксолом в комплексном лечении больных ЦП вирусной этиологии способствует не только улучшению функционального состояния печени (снижению выраженности синдрома цитолиза, холестаза), но и оказывает цитопротекторный эффект по отношению к клеткам периферической крови (лейкоцитам, лимфоцитам, тромбоцитам). Ключевые слова: вирусный гепатит С, В, цирроз печени, патогенетическая терапия, ремаксол, гепатотропный эффект.
Efficacy of the infusion hepatotropic drug remaxol in the pathogenetic therapy for cirrhotic stage chronic viral hepatitides
V.V. STELMAKH1, V.K. KOZLOV1-3, V.F. IVANOVA1, I.A. SAMUSENKO4.
1Mechnikov North-Western State Medical University, Ministry of Health of Russia, Saint Petersburg, Russia;
2Yaroslavl-the-Wise Novgorod State University, Veliky Novgorod, Russia;
3Saint Petersburg State University, Saint Petersburg, Russia;
4A.M. Nikiforov All-Russian Center of Emergency and Radiation Medicine, Russian Ministry for Civil Defense, Emergencies and Elimination of Consequences of Natural Disasters, Saint Petersburg, Russia
Aim. To investigate the impact of therapy with the infusion hepatoprotector remaxol on liver function in cirrhosis in the outcome of chronic viral hepatitides (CVH): HCV, HBV, HCV+HBV, and HBV+HDV.
Subjects and methods. Sixty-five patients aged 26 to 76 years, who had been diagnosed as having liver cirrhosis (LC) in the out-come of CVH: HCV, HBV, HCV+HBV, and HBV+HDV were examined. During infusion therapy, every day 32 cirrhotic patients in the outcome of CVH B or C received intravenous remaxol 400 ml in a jetwise manner once daily for 11 days. A comparison group comprised 33 patients with the similar condition who had intravenous ademetionine 400 mg in a jetwise fashion during infusion therapy with crystalloids (400 ml of isotonic sodium chloride solution, Ringer's solution) for 11 days.
Results. After an infusion therapy cycle, the study group patients were recorded to have more significantly reduced cytolytic and cholestatic parameters. The pronounced hepatotropic effect of the drug was confirmed by the rate of a decline in the average concentrations of alanine aminotransferase, aspartate aminotransferase, and total bilirubin. In the study group patients, the relative values of a decrease in the levels of these biochemical parameters were 29, 29, and 40% versus 15, 20, and 9% in the control patients.
Conclusion. Infusion therapy with remaxol in the combination treatment of the patients with viral LC not only improves liver function (reduces the degree of cytolysis, cholestasis), but also exerts a cytoprotective effect on peripheral blood cells (leukocytes, lymphocytes, platelets).
Keywords: viral hepatitis C, B, liver cirrhosis, pathogenetic therapy, remaxol, hepatotropic effect.
АлАТ — аланинаминотрансфераза
АсАТ — аспартатаминотрансфераза
ГГТП — γ-глутамилтранспептидаза
ФГДС — фиброгастродуоденоскопия
ХВГ — хронические вирусные гепатиты
ЦП — цирроз печени
HBV — вирус гепатита В
HCV — вирус гепатита С
Цирроз печени (ЦП), являясь финальной стадией хронических гепатитов различной этиологии, представляет собой актуальную проблему здравоохранения. С наступлением цирротической стадии заболевания увеличивается инвалидизация, ухудшается качество жизни больных, возрастает риск смерти от осложнений портальной гипертензии, риск развития спонтанного бактериального перитонита, гепаторенального синдрома, кровотечения из варикознорасширенных вен пищевода, печеночной энцефалопатии и комы [1]. Частота развития декомпенсированного ЦП, по данным ряда авторов, составляет 3,6—6% в год, а гепатоцеллюлярного рака — 1,4—3,3% [2].
Важная роль в развитии гепатоцеллюлярного повреждения печени при хронических вирусных гепатитах (ХВГ) отводится окислительному стрессу и индуцированных им апоптозу и некробиозу гепатоцитов [3, 4]. В условиях продолжающейся репликации вирусов гепатита С (HCV), гепатита В (HBV) и окислительного стресса развиваются дефицит выработки и утилизации АТФ клетки, повреждение мембран гепатоцитов (цитоплазматических и митохондриальных) [5].
Следствием персистирующей виремии является опосредованная цитокинами активация клеток Купфера (резидентных макрофагов печени), приводящая к паракринной активации звездчатых клеток и прогрессированию фиброза [6—8]. Накопление субэндотелиального матрикса приводит к аваскуляризации пространства Диссе, что препятствует транспорту питательных веществ из синусоида к гепатоциту, способствуя прогрессированию дистрофии, апоптоза и некробиоза гепатоцитов (рис. 1).
Рис. 1. Гепатобиоптат.
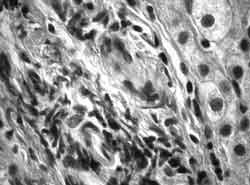 |
а — световая микроскопия (данные совместно с И.А. Самусенко) ХГС (ИГА 12 F4): капилляризация синусоидов, дистрофические изменения печеночных балок, окраска гематоксилином и эозином; |
|
a |
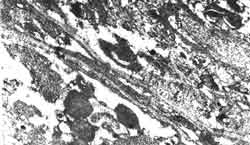 |
б, в — электронная микроскопия (данные совместно с Ивановой В.Ф.) ХГС (ИГА 10 F4): дегенеративные изменения цитоплазмы, пучки коллагеновых волокон, замещающих разрушенные участки цитоплазмы, коллагенизация пространства Диссе, разрушение пограничной пластинки (б); дегенеративные изменения ядра и цитоплазмы гепатоцита, пучки коллагеновых волокон, замещающих разрушенные участки цитоплазмы (в). ХГС — хронический гепатит С; ИГА — индекс гистологической активности. |
|
б |
 |
|
в |
Существенное ограничение проведения этиологической противовирусной терапии ХВГ на цирротической стадии обусловливает необходимость оптимизации патогенетической терапии [9]. Эффективным патогенетическим подходом в гепатологии является использование сукцинатсодержащих препаратов реамберин, ремаксол (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург), восстанавливающих митохондриальную мембрану и окислительное фосфорилирование, корригирующих тканевую гипоксию, а также модифицирующих клеточный обмен и оказывающих гепатопротективное действие [10—14]. Ремаксол — многокомпонентный инфузионный гепатопротектор, состоит из естественных метаболитов (янтарная кислота, рибоксин, никотинамид, метионин), оказывает антиоксидантное, антигипоксантное, гепатотропное действие, стимулирует синтез эндогенного адеметионина, повышает показатели системы глютатиона, усиливает регенеративные процессы в печени [15—17].
In vivo клинические эффекты ремаксола при гепатитах различной этиологии превосходят эффекты традиционной фармакотерапии: сопровождаются восстановлением функционального состояния печени (по уменьшению выраженности синдромов цитолиза, холестаза, восстановлению синтетической функции печени), нормализацией липидного и пигментного обменов, уменьшению выраженности основных клинических синдромов при ХВГ, неалкогольной жировой болезни печени [18—20].
В этой связи, комплекс физиологически активных компонентов препарата ремаксол, оказывающий антиоксидантное/антигипоксантное и гепатопротекторное действие, можно рассматривать как перспективный инфузионный гепатопротектор при ЦП вирусной этиологии.
Целью настоящего исследования явилось изучение влияния инфузионной терапии метаболическим корректором ремаксолом на функциональное состояние печени при ЦП в исходе ХВГ HCV, HBV, HCV+HBV, HBV+HDV.
Материалы и методы
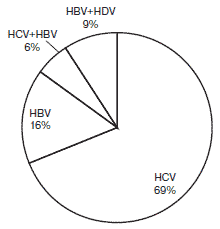
В исследование включили 65 пациентов (39 мужчин и 26 женщин) с ЦП в исходе ХВГ (HCV, HBV, HCV+HBV, HBV+HDV) в возрасте от 28 до 76 лет. Этиология ЦП пациентов, включенных в исследовании представлена на рис. 2. Диагноз устанавливали на основании совокупности клинико-лабораторных данных в соответствии с Международной классификацией болезней десятого пересмотра.
Рис. 2. Этиологические факторы ЦП обследованных пациентов.
Пациенты 1-й, или основной, группы (n=32) в составе комплексной терапии получали ремаксол ежедневно внутривенно капельно по 400 мл 1 раз в сутки в течение 11 дней. Пациенты 2-й, или группы сравнения (n=33), в составе комплексной терапии получали лиофилизат для приготовления раствора для внутривенного и внутримышечного введения гептрал 400 мг, вводимый аналогично на фоне инфузионной терапии в изотоническом растворе натрия хлорида 400 мл в течение 11 дней.
Демографические характеристики исследуемых больных представлены в табл. 1. В исследовании включены пациенты с цирротической стадией ХВГ (HCV, HBV, HCV+HBV, HBV+HDV).
Таблица 1. Демографические, этиологические и прогностические факторы исследуемых больных
| Показатель |
1-я группа (ремаксол; n=32) |
2-я группа (адеметионин; n=33) |
| Пол, м/ж |
21/11(66/34) |
18/15 (55/45) |
| Возраст, годы: |
| M±m |
51,32±12,0 |
54,35±10,56 |
| Разброс |
26—71 |
28—76 |
| Этиология ЦП: |
| HBV |
3 (9) |
7 (21) |
| HCV |
28 (88) |
17 (52) |
| HCV+HBV |
1 (3) |
3 (9) |
| HBV+HDV |
— |
6 (18) |
| Распределение по классам Child—Pugh: |
| A |
21 (66) |
21 (64) |
| B |
11 (34) |
12 (36) |
Примечание. Данные представлены в виде абсолютного числа больных (%), если не указано другое.
Среди обследованных больных большинство составили мужчины (55 и 66% в основной и контрольной группах соответственно), что не противоречит данным других исследователей, указывающих на более высокую распространенность цирротической стадии хронических диффузных заболеваний печени у мужчин. Сравнительный анализ показал, что по возрасту, росту и массе тела группы статистически значимо не различались (критерий Манна-Уитни, p>0,05).
Критериями включения пациентов в исследование служили: возраст от 28 до 76 лет; диагноз ХВГ (В, С, В+С, В+D), цирротическая стадия, Child-Pugh A— В; обязательные проявления портальной гипертензии (асцит и/или варикозное расширение вен пищевода и/или гиперспленизм и/или расширение воротной вены более 15 мм); концентрация аспартатаминотрансферазы (АсАТ) и/или аланинаминотрансферазы (АлАТ) выше нормы более чем в 1,5 раза; концентрации γ-глутамилтранспептидазы (ГГТП) выше нормы более чем в 1,5 раза; наличие антигенов (антител) вирусов гепатита В, С, D.
Методы исследования. Гематологические исследования выполняли с использованием автоматического гематологического анализатора BECMAN-COULTER 5-diff (Германия). Аппаратное клиническое исследование крови дополняли мануальными методиками с определением скорости оседания эритроцитов, подсчетом лейкоцитарной формулы. Биохимические методы исследования c определением уровней билирубина, АлАТ, АсАТ, ГГТП, щелочной фосфатазы, глюкозы проводили на автоматическом биохимическом анализаторе Cobas Integra-400 Plus фирмы «Roshe-Diagnostics» с помощью коммерческого набора реактивов фирмы «Roshe-Diagnostics» (Швейцария). Белковые фракции определяли на аппарате Paragon. HBsAg и антитела к HCV исследовали методом иммуноферментного анализа с помощью тестсистемы ЗАО «Вектор-Бест» третьего поколения. Инструментальное исследование предусматривало ультразвуковое исследование органов брюшной полости (сканер Siemens Sonoline Antares с 2 мультичастотными датчиками — конвексным 3,0-6,0 МГц, и линейным 6,0—11,0 МГц; фиброгастродуоденоскопию (ФГДС) с помощью волоконного эндоскопа GIF Q10 («Olympus», Япония) с определением состояния слизистой оболочки пищевода, желудка и двенадцатиперстной кишки, исключения варикозно-расширенные вены в пищеводе и антральном отделе желудка.
Статистический анализ. Для обработки полученных данных использовали пакеты программ Office Std. 2007 (Excel 2007) и Statistica 6.0. Перед началом анализа эмпирические распределения переменных были испытаны на согласие с законом нормального распределения по критерию Шапиро-Уилка (используется для выборок с 5 5, в противном случае использовали точный критерий Фишера. Проверку статистических гипотез проводили при критическом уровне значимости р=0,05, т.е. различие считали статистически значимым при pРезультаты
Распределение больных по группам с учетом этиологических и демографических данных представлено на рис. 2 и в табл. 1.
Наиболее частыми были жалобы астеновегетативного характера (слабость, быстрая утомляемость) у 100% больных основной группы и группы сравнения; p>0,05) (табл. 2). Диспепсический синдром исходно наблюдался у 86% больных основной группы и 84% больных группы сравнения (р>0,05). Боли в области правого подреберья до лечения отмечали 78% больных основной группы и 73% больных группы сравнения (р>0,05). Исходно жаловались на кожный зуд 54% больных основной группы и 56% больных группы сравнения.
Таблица 2. Динамика выраженности клинических синдромов у больных с ЦП Child—Pugh A, В на фоне инфузионной терапии, %
| Клинический синдром |
1-я группа (ремаксол; n=32) |
2-я группа (адеметионин; n=33) |
р |
| до лечения |
после лечения |
до лечения |
после лечения |
| Астенический |
100 |
43 |
100 |
65 |
р1—3>0,05; р2—4<0,05 |
| Диспепсический |
86 |
42 |
84 |
48 |
р1—3>0,05; р2—4>0,05 |
| Боли в правом подреберье |
78 |
29 |
73 |
45 |
р1—3>0,05; р2—4<0,05 |
| Кожный зуд |
54 |
34 |
56 |
42 |
р1—3>0,05; р2—4>0,05 |
Следует отметить, что печеночно-клеточная дисфункция Child—Pugh A выявлена у 66% больных основной группы и у 64% больных группы сравнения, Child—Pugh В — у 34 и 36% больных соответственно (см. табл. 1). У пациентов с ЦП класса В по шкале Child—Pugh выявлялась классическая картина с типичными печеночными знаками («сосудистые звездочки», «лакированный язык», «печеночные ладони») и сосудистыми анастомозами. Исходно желтуха наблюдалась у 20% больных основной группы и у 24% больных группы сравнения.
Наличие признаков портальной гипертензии по данным ФГДС (наличие варикознорасширенных вен пищевода) регистрировалось у 48% больных основной группы и у 52% больных группы сравнения. Отечно-асцитический синдром выявлялся у 34% больных основной группы и у 36% больных группы сравнения. Исходно у 22% исследуемых пациентов выявлялась клинически выраженная печеночная энцефалопатия I стадии, у 11% — клинически выраженная печеночная энцефалопатия II стадии.
У пациентов обеих групп исходно выявлено нарушение функции печени в виде синдромов цитолиза и холестаза (табл. 3). Синдром холестаза наблюдался у большинства пациентов, при этом исходно в группе больных, получавших ремаксол, наблюдались более высокие концентрации ГГТП как основного маркера холестаза. Средние уровни ГГТП превышали норму в 5,3—3,3 раза, составляя 363,50±31,82 ед/л у больных основной группы и 226,11±45,26 ед/л у больных группы сравнения (рТаблица 3. Динамика показателей цитолитического и холестатического синдромов у больных с ЦП Child—Pugh A, В на фоне инфузионной терапии, M±m
| Показатель |
1-я группа (ремаксол; n=32) |
2-я группа (адеметионин; n=33) |
р |
| до лечения |
после лечения |
до лечения |
после лечения |
| АлАТ, ед/л |
147,32±19,58 |
104,78±16,39 |
121,38±23,32 |
103,57±20,49 |
р1—2>0,05; р3—4>0,05 |
| АсАТ, ед/л |
132,88±10,46 |
94,82±13,44* |
126,53±15,96 |
100,63±9,73 |
р1—2<0,05; р3—4>0,05 |
| Билирубин, мкмоль/л |
61,73±6,62 |
37,07±6,01* |
46,04±5,14 |
37,54±4,44 |
р1—2<0,05; р3—4>0,05 |
| ГГТП, ед/л |
363,50±31,82 |
268,36±24,78* |
226,11±45,26 |
204,00±37,22 |
р1—2<0,05; р3—4>0,05 |
| Альбумин, г/л |
31,31±1,23 |
33,00±1,33 |
29,50±1,07 |
30,66±1,08 |
р1—2>0,05; р3—4>0,05 |
У пациентов основной группы после курса инфузионной терапии наблюдалось более выраженное снижение уровня общего билирубина: с 61,73±6,62 до 37,07±6,01 мкмоль/л (д0,05) (см. табл. 3).
При проведении инфузионной терапии ремаксолом со скоростью инфузии 40—60 капель в минуту не зафиксировано ни одного случая нежелательных эффектов. В обеих группах регистрировалось уменьшение числа жалоб и патологических симптомов. При этом у пациентов, получавших ремаксол, астеновегетативный синдром нивелировался быстрее, чем в группе сравнения (рПосле окончания курса инфузионной терапии в основной группе больных зарегистрировано более существенное уменьшение показателей цитолиза, холестаза (см. табл. 3). Выраженный гепатотропный эффект препарата подтверждался темпами снижения средних концентраций АлАТ, АсАТ и общего билирубина. Относительные величины снижения уровней этих биохимических показателей у больных основной группы составили 29, 29 и 40% против 15, 20 и 9% у пациентов контрольной группы (рис. 3).
Рис. 3. Относительные изменения (средние) концентрации АлАТ, ГГТП и билирубина у больных с ЦП Child—Pugh A, B на фоне инфузионной терапии.
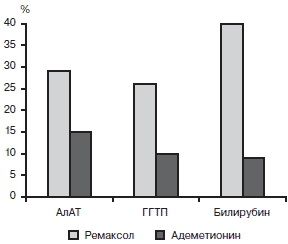
Снижение уровней ГГТП наблюдалось у 75% больных основной группы и у 73% больных группы сравнения, что в относительных величинах составило 26 и 10% соответственно (см. рис. 3). Эффективность препарата подтверждала и кратность снижения уровня ГГТП, составив 1,4 в основной группе и 1,1 раза в группе сравнения соответственно, что доказывает большую эффективность ремаксола по сравнению с адеметионином в отношении терапии внутрипеченочного холестаза при ЦП вирусной этиологии (см. табл. 3).
Печеночно-клеточная недостаточность осложняет течение цирротической стадии заболеваний печени вне зависимости от этиологии. Печеночно-клеточная недостаточность проявляется желтухой, асцитом, печеночной энцефалопатией, низким уровнем альбумина в сыворотке, недостаточностью протромбина. Содержание в крови этих белков позволяет оценить синтетическую функцию печени [21].
В данном исследовании исходно нарушение синтетической функции печени у больных ЦП выявлено у 44% больных основной группы и у 54% больных группы сравнения по уровню альбумина сыворотки крови, средние значения которого составили 31,31±1,23 г/л у пациентов основной группы и 29,50±1,07 г/л в группе сравнения (p>0,05). На фоне инфузионной терапии у обследуемых пациентов с ЦП и печеночно-клеточной недостаточностью Child—Pugh А и Child—Pugh В наблюдалась тенденция к улучшению синтетической функции печени (по увеличению синтеза альбумина гепатоцитами с 31,31±1,23 до 33,00±1,33 г/л и с 29,50±1,07 до 30,66±1,08 г/л соответственно; р>0,05) (см. табл. 3).
Применение ремаксола оказывало цитопротективный эффект в отношении количества лейкоцитов, лимфоцитов и тромбоцитов периферической крови. Абсолютная лимфопения (снижение количества лимфоцитов менее 1,5-109/л) на фоне лейкопении исходно выявлена у 28% больных в основной группе и у 30% больных группы сравнения. Снижение абсолютного количества лимфоцитов в периферической крови является признаком депрессии иммунной системы [22]. По завершению инфузионной терапии установлен иммунокорригирующий эффект у пациентов основной группы на основании повышения абсолютного количества лимфоцитов с 0,99±0,11 до 1,44±0,21х109/л (р9/л; рУ 80% обследованных больных ЦП исходно наблюдалась тромбоцитопения. Инфузионная терапия ремаксолом способствовала повышению уровня тромбоцитов на 43% (с 119±14,2 до 144±12,6х109/л; рВыводы: 1) инфузионная терапия ремаксолом положительно влияет на клиническое течение ЦП вирусной этиологии (HBV, HCV), существенно уменьшает выраженность основных клинических синдромов (астеновегетативного, диспепсического, холестатического) 2) 11-дневный курс инфузионным гепатопротектором ремаксолом при ЦП вирусной этиологии (HBV, HCV) способствует улучшению функционального состояния печени на основании уменьшения выраженности основных биохимических синдромов гепатоцеллюлярного повреждения — синдрома цитолиза и холестаза. Применение препарата способствует развитию дезинтоксикационного, мембраностабилизирующего, а также выраженного антихолестатического эффектов; 3) инфузионная терапия ремаксолом способствует улучшению белковосинтетической функции печени (по увеличению синтеза альбумина гепатоцитами) у пациентов с печеночно-клеточной недостаточностью; 4) 11-дневный курс инфузионным гепатопротектором ремаксолом способствует достижению иммунокорригирующего эффекта у пациентов с ЦП вирусной этиологии (HBV, HCV) и исходными признаками иммунодепрессии на основании повышения абсолютного количества лимфоцитов в периферической крови; 5) 11-дневный курс инфузионным гепатопротектором ремаксолом оказывает цитопротекторный эффект по отношению к клеткам периферической крови (лейкоцитам, лимфоцитам, тромбоцитам).
Заключение
Исследование эффективности инфузионного гепатопротектора ремаксола в лечении больных ЦП в исходе ХВГ (В, С) выявило наличие мембраностабилизирующего, антихолестатического, иммунокорригирующего, цитопротективного эффектов. Полученные результаты свидетельствуют о положительном влиянии терапии инфузионным гепатопротектором ремаксолом на функциональное состояние печени, а также цитопротекторный эффект по отношению к клеткам периферической крови (лимфоцитам, лейкоцитам, тромбоцитам) у больных с ХВГ В, С на цирротической стадии.
Эффективная коррекция синдрома внутрипеченочного холестаза наряду с эффективной гепатопротекцией, а также достижением цитопротекции, наблюдаемая при инфузионной терапии ремаксолом, открывает новые перспективы комплексной терапии многоплановых нарушений, сопровождающих развитие ЦП вирусной этиологии.
ЛИТЕРАТУРА
1. Маевская М.В., Федосьина Е.А. Лечение осложнений цирроза печени. Методические рекомендации для врачей. Под ред. Ивашкина В.Т. М.: МЕДпресс-информ; 2012.
2. Khan MN, Farrell GC, Byth K, Lin R, Weltman M, George J, Samarasinghe D, Kench J, Kaba S, Crewe E, Liddle C. Which patients with hepatitis C develop liver complication? Hepatology. 2000;31:513-520.
3. Poli G. Pathogenesis of liver fibrosis: role of oxidative stress. Mol Aspects Med. 2000;21(3):49-98.
4. Козлов В.К., Стельмах В.В. Оксидативный стресс в патогенезе дисфункции иммунной системы при инфекционной патологии. Модификаторы энергетического обмена клеток как средства патогенетической иммуноориентированной те-рапии. В кн.: Актуальные вопросы гепатологии: Материалы 7-го Международного симпозиума гепатологов Беларуси. Под ред. Цыркунова В.М. Витебск, 5—6 июня 2008 г.: в 2 т. Гродно: ГрГМУ; 2008.
5. Шифф Ю.Р., Соррел М.Ф., Мэдрей У.С. Алкогольные, лекар-ственные, генетические и метаболические заболевания. Пер. с англ. Под ред. Мухина Н.А. М.: ГЭОТАР-Медиа; 2011.
6. Friedman SL. Molecular regulation of hepatic fibrosis, an inte-grated cellular response to tissue injury. J Biol Chem. 2000;275: 2247-2250.
7. Schulze-Krebs A, Preimel D, Popov Y., Bartenschlager R, Loh- mann V, Pinzani M, Schuppan D. Hepatitis C virus-replicating hepatocytes induce fibrogenic activation of hepatic stellate cells. Gastroenterology. 2005;129:246-258.
8. Радченко В.Г., Стельмах В.В., Козлов В.К. Оптимизация этиопатогенетической терапии хронического гепатита С: пособие для врачей-терапевтов, гастроэнтерологов, гепатоло- гов, инфекционистов. СПб.: СПбГМА; 2004.
9. Heathcote EJ. Treatment considerations in patients with hepatitis C and cirrhosis. J Clin Gastroenterol. 2003;37:395-398.
10. Суханов Д.С., Петров А.Ю., Романцов М.Г., Александрова Л.Н. и др. Фармакологическая активность сукцинатсодержащих препаратов при хроническом поражении печени различными инициирующими агентами. Фундаментальные исследования. 2011;5:159-169.
11. Стельмах В.В., Козлов В.К. Метаболические корректоры на основе янтарной кислоты и их использование при неалкогольном стеатогепатите. Профилактическая и клиническая медицина. 2010;3-4:224-225.
12. Стельмах В.В., Радченко В.Г., Козлов В.К. Метаболические корректоры на основе янтарной кислоты как средства патогенетической терапии при хронических вирусных гепатитах. Терапевтический архив. 2011;2:67-71.
13. Суханов Д.С. Эффективность гепатопротекторного действия и оценка риска при использовании реамберина, ремаксола и адеметионина у больных туберкулезом органов дыхания с лекарственными поражениями печени. Терапевтический архив. 2012;11:26-29.
14. Заривчацкий М.Ф., Каменских Е.Д., Мугатаров И.Н. Оценка эффективности ремаксола у больных циррозом печени. Хирургия. Журнал им. Н.И. Пирогова. 2013;3:79-82.
15. Суханов Д.С., Петров А.Ю., Коваленко А.Л., Романцов М.Г. Индукция S-аденозил-L-метионина в гепатоцитах при фармакотерапии токсических и лекарственных поражений печени в эксперименте. Экспериментальная и клиническая фармакология. 2011;10:34-38.
16. Коваленко А.Л., Петров А.Ю., Суханов Д.С., Саватеева Т.Н. и др. Ремаксол — препарат для восстановления системы антиоксидантной защиты при поражении печени циклофосфаном в эксперименте. Экспериментальная и клиническая фармакология. 2011;1:32-35.
17. Смирнова Н.Г., Чефу С.Г., Коваленко А.Л., Грашин Р.А., Власов Т.Д. Состояние свободнорадикального окисления и антиоксидантной защиты при экспериментальном холестазе. Хирургия. Журнал им. Н.И. Пирогова. 2011;3:50-55.
18. Сологуб Т.В., Горячева Л.Г., Суханов Д.С., Романцов М.Г., Антонова Т.В., Яковлев А.А., Радченко В.Г., Шульдяков А.А., Речник В.Н., Суздальцев А.А., Есауленко Е.В., Максимов С.Л., Баранова И.П. Гепатопротективная активность ремаксола при хронических поражениях печени. Клиниче-ская медицина. 2010;1:62-66.
19. Стельмах В.В., Козлов В.К. Метаболическая коррекция при дислипидемии у больных с неалкогольной жировой болезнью печени как новая стратегия терапии. Терапевтический архив. 2013;85(4):71-76.
20. Стельмах В.В., Козлов В.К., Радченко В.Г., Некрасова А.С. Патогенетическая терапия метаболического синдрома на стадии органных поражений. Клиническая медицина. 2012;6:61-65.
21. Внутренние болезни по Тинсли Р Харрисону. Под ред. Фаучи Э., Браунвальда Ю., Иссельбахера К. М.; 2002.
22. Козлов В.К., Стельмах В.В., Радченко В.Г. Хронический гепатит С: иммунопатогенез, аспекты диагностики и современная стратегия комплексного лечения. Руководство для врачей. СПб.; 2009.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru





