Энерготропная патогенетически ориентированная терапия сукцинатсодержащими препаратами при неалкогольной жировой болезни печени: перспективы клинического применения
Статьи
Опубликовано в журнале:
Медицинский алфавит. Гастроэнтерология №1 2/2013, стр. 3-8
В. В. Стельмах1, к. м. н., доцент
В. К. Козлов 2,3,4д. м. н. профессор
В. Л. Баранов 5, д. м. н. профессор
Э. Л. Латария 5, к. м. н., доцент
А. С. Некрасова 1, сотрудник кафедры
1 Северо-Западный государственный медицинский университет им. И. И. Мечникова, кафедра внутренних болезней и нефрологии, отделение гепатологии и нефрологии СЗГМУ им. И. И. Мечникова, Санкт-Петербург
2 Институт высоких медицинских технологий при СПбГМУ, Санкт-Петербург
3 Северо-Западный государственный медицинский университет им. И. И. Мечникова, кафедра клинической лабораторной диагностики, Санкт-Петербург
4 Университет им. Ярослава Мудрого, кафедра микробиологии, иммунологии и инфекционных болезней, В. Новгород
5 Северо-Западный государственный медицинский университет им. И. И. Мечникова, управление клиниками, Санкт-Петербург
Работа выполнялась на кафедре внутренних болезней и нефрологии, отделении гепатологии и нефрологии СЗГМУ им. И. И. Мечникова, Санкт-Петербург.
Резюме
Целью настоящего исследования явилось изучение фармакотерапевтической эффективности и безопасности инфузионного метаболического корректора ремаксол в терапии больных с неалкогольной жировой болезнью печени на стадии стеатогепатита в комплексной терапии метаболического синдрома.
Материалы и методы
В исследование было включено 108 пациентов возрастом от 21 до 77 лет (64 мужчин и 44 женщин) с неалкогольным стеатогепатитом на фоне метаболического синдрома (IDF, 2005). Пациенты основной группы (62 чел.) в составе комплексной терапии получали метаболический корректор с гепатопротективными свойствами ремаксол ежедневно внутривенно капельно по 400,0 мл 1 раз в сутки, пациенты группы сравнения (46 чел.) в составе комплексной терапии получали лиофилизат для приготовления раствора для внутривенного и внутримышечного ведения адеметионин 400 мг, разведенный в растворе NaCL 0,9 % 400 мл. Длительность инфузионной терапии составила 11 дней.
Результаты
Применение ремаксола у пациентов с НАСГ способствовало: регрессии основных клинических синдромов НАСГ; улучшению функционального состояния печени; улучшению показателей липидного обмена; уменьшению выраженности процессов ПОЛ мононуклеаров периферической крови.
Заключение
Инфузионная терапия ремаксолом пациентов с НАСГ в рамках метаболического синдрома способствует достижению мембраностабилизирующего, антиоксидантного, антихолестатического, гиполипидемического эффекта.
Ключевые слова: неалкогольный стеатогепатит, метаболический синдром, дислипидемия, перекисное окисление липидов, ремаксол, янтарная кислота, патогенетическая терапия
Summary
The purpose of this study was to evaluate the efficacy and safety pharmacotherapeutic metabolic corrector Remaksol infusion in the treatment of patients with nonalcoholic fatty liver disease at the stage of steatohepatitis in the treatment of metabolic syndrome.
Materials and methods
The study included 108 patients aged 21 to 77 years (64 men and 44 women) with nonalcoholic steatohepatitis in the metabolic syndrome (IDF, 2005). Treatment group (62 pers.) in the adjuvant therapy received metabolic corrector with hepatoprotective properties remaksol daily intravenous drip for 400.0 ml 1 per day, (46 pers.) in the adjuvant therapy received lyophilisate for solution for intravenous and intramuscular geptral of 400 mg, dissolved in a solution of NaCL 0,9 % 400 ml. infusion. Duration of therapy was 11 days.
Results of using Remaksol patients with NASH contributed: regression of major clinical syndromes NASH, improve liver function, improve lipid metabolism, reduces the severity of lipid peroxidation peripheral blood mononuclear cells.
Conclusion
Infusion therapy with Remaksol patients with NASH in the metabolic syndrome contributes to the achievement of antioxidant, antiholestatic, lipid-lowering effects.
Keywords: non-alcoholic steatohepatitis, metabolic syndrome, dyslipidemia, lipid peroxidation, remaksol, succinic acid, pathogenetic therapy.
Список сокращений
АЛТ — аланинаминотрансфераза.
АСТ — аспартатаминотрансфераза.
Y-ГТП — гамма-глютамилтранспептидаза.
ИБС — ишемическая болезнь сердца. ИМТ — индекс массы тела.
ЛПВП — липопротеиды высокой плотности.
МС — метаболический синдром.
НАЖБП — неалкогольная жировая болезнь печени.
НАСГ — неалкогольный стеатогепатит.
СД 2-го типа — сахарный диабет II типа.
СКФ — скорость клубочковой фильтрации.
ХПН — хроническая почечная недостаточность.
ЩФ — щелочная фосфатаза.
Введение
Неалкогольная жировая болезнь печени (НАЖБП) является одним из широко распространенных заболеваний печени в мире, что обусловливает непрекращающийся поиск оптимальных методов патогенетической терапии. Популяционные и клинические исследования убедительно доказали, что НАЖБП является печеночной манифестацией метаболического синдрома (МС) [12, 17]. Такие компоненты МС, как: дислипидемия, инсулино-резистентность, ожирение являются факторами риска развития НАЖБП и ее прогрессии [11, 15]. В ряде случаев НАЖБП является первым органным поражением при МС, являясь серьезным предиктором развития и прогрессирования сахарного диабета, кардиоваскулярной патологии, смертность от которых занимает лидирующее положение в мире [18].
Понятие неалкогольной жировой болезни печени (НАЖБП) охватывает спектр поражений печени, включающий жировую дистрофию или жировой гепатоз, жировую дистрофию с воспалением и повреждением гепатоцитов — неалкогольный стеатогепатит (НАСГ), развитие фиброза с возможностью прогрессии с исходом в цирроз печени [13, 16]. У 30 % пациентов с диагностированной НАЖБП на стадии стеатоза и стеатогепатита в течение 5-10 лет наблюдается прогрессия до стеатофиброза и стеатоцирроза. У 25 % больных на цирротической стадии в течение ближайших трех лет развиваются фатальные осложнения портальной гипертензии [14].
Инсулинорезистентность и окислительный стресс играют большую роль в патогенезе НАЖБП. Важнейшим универсальным патогенетическим механизмом развития НАСГ на фоне жировой инфильтрации печени является перекисное окисление липидов (ПОЛ), эффектами которого объясняется основная часть наблюдаемых гистологических изменений в ткани печени. Инфильтрация жирными кислотами гепатоцитов, а также избыточное образование продуктов ПОЛ способствуют прогрессированию фибротических процессов в печени [19].
В условиях стеатоза гепатоцитов развиваются проявления липотоксичности. Свободные жирные кислоты оказывают как прямое детергентное, так и опосредованное (продуктами перекисного окисления липидов) повреждающее действие на клеточные структуры, сопровождающееся деструкцией митохондрий, угнетением ферментов гликолиза, разобщением окислительного фосфорилирования, активизацией пероксисомного пути утилизации избытка свободных жирных кислот. В результате доминирования процессов окислительного стресса и повреждения митохондрий наблюдается гибель гепатоцитов путем апоптоза или некроза [1, 2].
По этой причине лекарственные средства метаболического типа действия, способные эффективно ко рректировать метаболизм клеток и их энергетический обмен, всё шире используются при различных заболеваниях как полноценный компонент комплексной патогенетической терапии [3, 5, 6, 15].
Современные подходы к лечению НАЖБП направлены главным образом на устранение или ослабление факторов, ведущих к развитию НАЖБП (похудание, коррекция гиперлипидемии и гипергликемии, отмена потенциально гепатотоксических препаратов). Перспективной является гепатопротекция, блокирующая второй толчок патогенеза НАСГ — окислительный стресс. Эффекты производных янтарной кислоты — сукцинатов — направлены на коррекцию митохондриальной дисфункции и восстановление утраченной при гипоксии и оксидативном стрессе энергосинтезирующей функции клеток, поэтому подобные препараты относят к энерготропным антигипоксантам. Коррекция нарушений в функционировании антиоксидантных систем организма с помощью препаратов антиоксидантного типа действия является одним из перспективных направлений нормализации клеточного метаболизма и способствует восстановлению функциональной активности различных клеток, включая клетки системы мононуклеарных фагоцитов [4, 5, 7].
В этой связи, метаболическую композицию ремаксол, обладающую антиоксидантным/антигипоксантным и цитопротекторным действием, можно рассматривать как перспективный гепатопротекторный метаболический корректор [8, 10].
Ремаксол представляет собой уникальную метаболическую композицию благодаря входящему в его состав, наряду с янтарной кислотой, метионину (0,75 г), а также инозину и никотинамиду. Благодаря этой комбинации в организме происходит синтез эндогенного аденозилметионина, который участвует в трех типах биохимических реакций:
1. реакции трансметилирования (важный этапом синтеза фосфолипидов — фосфатидилхолина, обеспечивающего текучесть мембран и их поляризацию, которая играет заметную роль в синтезе желчи);
2. реакции транссульфурирования (синтез глутатиона — важнейшего клеточного антиоксиданта);
3. синтезе полиаминов (предшественников других тиоловых соединений, таких как цистеин, таурин, коэнзим А).
Активным веществом препарата является янтарная кислота, обладающая прямым модифицирующим воздействием на клеточный метаболизм: происходит активирование аэробного гликолиза, а в условиях гипоксии увеличивается интенсивность окислительных процессов в цикле Кребса, возрастает внутриклеточный фонд макроэргических соединений (АТФ и креатинфосфата), обеспечивается переход глюкозы в гликоген, стабилизируется липидный обмен, повышается активность ферментов первой линии свободнорадикальной защиты (супероксиддисмутаза [СОД] и каталаза [КАТ]), стабилизируется уровень восстановленной части тиолдисульфидой антиоксидантной системы. Потенцирующие эффекты других биологически активных компонентов способствует восстановлению дыхательной цепи митохондрий (никотинамид), усиление синтеза макроэргических молекул (инозин).
Цель исследования — оценка фармакотерапевтической эффективности и безопасности инфузионного метаболического корректора ремаксол в терапии больных с неалкогольной жировой болезнью печени на стадии стеатогепатита в комплексной терапии метаболического синдрома.
Материалы и методы
В исследование было включено 108 пациентов возрастом от 21 до 77 лет (64 мужчины и 44 женщины) с неалкогольным стеатогепатитом на фоне метаболического синдрома (IDF, 2005).
Схемы и дозы введения препарата
Исследуемые больные были рандомизированы методом конвертов и таблиц случайных чисел на две сравнимые по всем показателям группы. Пациенты основной группы (62 чел.)в составе комплексной терапии получали метаболический корректор с гепатопротективными свойствами ремаксол ежедневно внутривенно капельно по 400 мл один раз в сутки в течение 11 дней. Пациенты группы сравнения (46 чел.) в составе комплексной терапии получали лиофилизат для приготовления раствора для внутривенного и внутримышечного ведения адеметионин 400 мг, разведенный в растворе NaCL 0,9 % 400 мл в течение 11 дней. Терапия назначалась на фоне базисной, максимально унифицированной терапии (спазмолитики, ферменты, гипотензивные препараты).
Всем больным проводилось комплексное обследование, включающее общий осмотр, антропометрические показатели (определение массы тела, роста, индекса массы тела), оценку клинических признаков заболевания, лабораторных и инструментальных методов исследования (ультразвуковое исследование органов брюшной полости, электрокардиограмма, измерение артериального давления).
Оценка эффективности препаратов проводилась на основании изучения динамики клинического течения заболевания с учетом основных симптомов и синдромов (астено-вегетативного, диспепсического, холе статического синдромов, выраженности гепатомегалии), динамики лабораторных методов исследования, характеризующих функциональное состояние печени (выраженность синдромов цитолиза и холестаза, белоксинтетической функции печени), состояние липидного и углеводного обменов, выраженность процессов ПОЛ (ПОЛ мононуклеаров периферической крови).
Критерии включения пациентов в исследование
1. Мужчины и женщины в возрасте от 18 до 80 лет с диагнозом «неалкогольная жировая болезнь печени».
2. Обязательные сопутствующие диагнозы: «гипертоническая болезнь I—III стадии» и/или «ишемическая болезнь сердца» (стенокардия напряжения 1-3 ф. к.).
3. Нарушение толерантности к глюкозе или сахарный диабет II типа.
4. Избыточная масса тела (ИМТ > 25,0 кг/м).
5. АСТ и/или АЛТ > 1,5 N.
6. Уровень холестерина выше 6 ммоль/л и/или коэффициент атерогенности более 3,5.
Критерии исключения пациентов из исследования
1. Индивидуальная непереносимость компонентов препарата ремаксол.
2. Положительные маркеры вирусньгх гепатитов (HBsAg, анти-HCV антитела).
3. Анамнестическое указание на регулярное употребление алкоголя, наркотических веществ.
4. Аутоиммунные заболевания печени.
5. Недавние случаи (менее трех месяцев назад) одного из следующих состояний: острый инфаркт миокарда, аортокоронарное шунтирование, чрескожное коронарное вмешательство, реконструктивные вмешательства на сосудах нижних конечностей или сонных артериях, инсульт, травмы головного и спинного мозга.
6. Злокачественные новообразования.
7. Туберкулезная инфекция.
8. Сердечная недостаточность IV степени по классификации NYHA, дыхательная недостаточность III степени на момент включения в исследование.
9. Цирроз печени с явлениями портальной гипертензии.
10. Любой из перечисленных параметров: исходная анемия Hb < 80 г/л, тромбоцитопения < 80 х 10 9/л, лейкоцитоз > 20 х 10 9/л.
11. Хроническая почечная недостаточность, требующая проведения гемодиализа.
12. Беременность и период лактации.
Статистические методы
Для обработки полученных данных были использованы пакеты программ Office Std. 2007 (Excel 2007) и Statistica 6.0. Проверка статистических гипотез проводилась при критическом уровне значимости Р = 0,05, т. е. различие считалось статистически значимым, если p < 0,05.
Результаты исследования и их обсуждение
Исходные характеристики пациентов
В исследование включались пациенты с первичной формой НАЖБП, связанной с развитием инсулиноре-зистентности и МС (табл. 1.). Все пациенты имели выраженный избыток массы тела с преимущественным распределением жировой ткани по висцерально-абдоминальному типу. Индекс массы тела (ИМТ) составил 32,34 ± 3,62 кг/м 2 в основной группе и 32,75 ± 1,37 кг/м 2 в группе сравнения, p > 0,05. Отобранные в исследование пациенты характеризовались наличием инсулинорезистентности, о чем свидетельствовало повышение индекса HOMA-IR (табл. 1).
Таблица 1
|
Показатель
|
I группа (ремаксол)
|
II группа (адеметионин)
|
|
(n = 62)
|
(n = 46)
|
|
Пол, м/ж, абс.,
|
32/30
|
32/14
|
|
(%)
|
(52/48 %)
|
(69/31%)
|
|
Возраст, лет
M ± m
Разброс
|
|
|
|
50,18 ± 2,38
|
49,27 ± 2,16
|
|
30-77
|
18-77
|
|
Вес, кг
M ± m
Разброс
|
|
|
|
93,69 ± 2,96
|
95,36 ± 3,14
|
|
68-129
|
64-144
|
|
ИМТ, кг/м 2
|
32,34 ± 3,62
|
32,75 ± 1,37
|
|
HOMA-IR
|
8,94 ± 0,12
|
9,32 ± 0,18
|
|
СД II типа, абс., ( %)
|
32 (52 %)
|
24 (52 %)
|
|
Нарушение толерантности к глюкозе, абс., ( %)
|
30 (48 %)
|
22 (48 %)
|
|
Гиперхолестеринемия, абс., ( %)
|
48 (77 %)
|
39 (85 %)
|
|
Гипертриглицеридемия, абс., ( %)
|
28 (45 %)
|
18 (39 %)
|
|
Артериальная гипертензия, абс., ( %)
|
61 (98 %)
|
46 (100 %)
|
|
ИБС, абс., ( %)
|
36 (58 %)
|
23 (50 %)
|
У исследуемых больных НАСГ наблюдался в рамках МС (IDF, 2005): артериальная гипертензия (у 98 % больных основной группы и у 100 % больных группы сравнения, р > 0,05), нарушение липидного обмена (гиперхолестеринемия у 77 % больных основной группы и у 85 % больных группы сравнения, р > 0,05; гипертриглицеридемия у 45 % больных основной группы и у 39 % больных группы сравнения, р > 0,05). Сочетание НАСГ с сахарным диабетом II типа было зарегистрировано более чем у половины больных основной группы и группы сравнения; нарушение толерантности к глюкозе у 48 % больных основной группы и группы сравнения, р > 0,05 (табл. 1).
Следует отметить, что особенностью течения стеатогепатита при НАЖБП является скудная клиническая симптоматика со стороны органов гепатобилиарной системы. Наиболее частыми жалобами больных были проявления астено-вегетативного характера (слабость, быстрая утомляемость) у 96 % больных основной группы и 95 % больных группы сравнения. Чувство тяжести, боли в правом подреберье и снижение аппетита исходно отмечали 62 % больных основной группы и 54 % больных группы сравнения; 10 % больных основной группы беспокоил незначительный кожный зуд. Гепатомегалия исходно выявлялась у 50 % больных в основной и контрольной группах.
Влияние инфузионной терапии на клиническую картину заболевания
При назначении инфузионной терапии в обеих группах регистрировалось уменьшение жалоб и частоты патологических симптомов. Несмотря на более частое выявление диспепсического, болевого абдоминального и холестатического синдромов у больных основной группы, на фоне лечения отмечалось существенное снижение их частоты регистрации: проявления диспепсического синдрома к концу терапии сохранялись лишь у 3 % больных основной группы, боли в области правого подреберья к 7 суткам регистрировались лишь у 4 % больных, на кожный зуд к концу лечения не жаловался ни один пациент.
Влияние инфузионной терапии на показатели цитолитического и холестатического синдромов
Исходно у больных основной группы наблюдались более высокие показатели синдрома цитолиза (АЛТ, АСТ) по сравнению с таковыми группы сравнения (табл. 2). Частота нормализации уровня АЛТ и АСТ к 12-му дню терапии у пациентов, получавших ремаксол, составила соответственно 35 и 68 %, в то время как у больных контрольной группы, получавших адеметионин — 22 и 53 °/о (p < 0,05). Относительные величины снижения уровней этих ферментов у больных основной группы составили 33 и 39 % против 18 и 30 % у пациентов контрольной группы.
Таблица 2Динамика показателей цитолитического и холестатического синдромов у пациентов с НАСГ M ± m
|
Показатель
|
I группа (ремаксол) (n = 62)
|
II группа (адеметионин) (n = 46)
|
Р
|
|
До лечения
|
После лечения
|
До лечения
|
После лечения
|
|
1
|
2
|
3
|
4
|
|
АЛТ, ЕД/л
|
104,82 ± 7,53
|
70,66 ± 6,35*
|
76,32 ± 6,48
|
62,44 ± 7,23
|
Р1-2 < 0,01
|
|
АСТ, ЕД/л
|
76,18 ± 8,34
|
46,11 ± 4,02*
|
60,12 ± 6,38
|
42,15 ± 3,18*
|
Р1-2 < 0,05 Р3-4 < 0,05
|
|
Билирубин, мкмоль/л
|
27,32 ± 2,64
|
14,22 ± 1,38*
|
25,47 ± 1,85
|
13,21 ± 2,81*
|
Р1-2 < 0,05 Р3-4 < 0,05
|
|
Y-ГТП, ЕД/л
|
310,74 ± 18,25
|
192,18 ± 19,12*
|
214,64 ± 22,66
|
171,16 ± 20,35
|
Р1-2 < 0,05 Р3-4 > 0,05
|
Примечание: * — достоверность отличий р < 0,05.
У исследуемых больных синдром холестаза и клинически и биохимически исходно был более выражен в основной группе (по частоте регистрации кожного зуда и уровню у-ГТП (табл. 2). Синдром холестаза наблюдался более чем у половины исследуемых пациентов, при этом средние значения у-ГТП превышали норму в 4,5-3,1 раза, составляя 310,74 ± 18,25 ЕД/л и 214,64 ± 22,66 ЕД/л у больных основной группы и группы сравнения соответственно (табл. 2). У пациентов обеих групп после проведения курса инфузионной терапии наблюдалась нормализация уровня общего билирубина у 76 % больных в основной группе и у 64 % больных в группе сравнения (p < 0,05).
Анализ полученных результатов после завершения курса терапии выявил более интенсивное влияние инфузионной терапии на показатели синдрома холестаза в основной группе: установлено статистически значимое различие в динамике показателей холестаза по изменению величины у-ГТП (р = 0,03) между группами (табл. 2). Снижение уровней у-ГТП наблюдалось у 74 % больных основной группы и у 73 % больных группы сравнения, что в относительных величинах составило 38 против 20 % соответственно, что доказывает большую эффективность ремаксола по сравнению с адеметионином в отношении терапии внутрипеченочного холестаза при НАСГ.
Влияние инфузионной терапии на липидный обмен
У пациентов обеих групп исходно было установлено наличие нарушений углеводного, липидного обменов (табл. 1, 3). Частота встречаемости гиперхолестеринемии составила 77 % в основной группе и 85 % в группе сравнения; гипертриглицеридемии — 45 % в основной группе и 39 % в группе сравнения.
Применение ремаксола оказывало существенное положительное влияние на профиль липидов (табл. 3). У 76 % больных основной группы и у 82 % больных группы сравнения наблюдалось достоверное снижение концентрации общего холестерина, причем в группе ремаксола существенное снижение уровня общего холестерина достигалось уже к шестым суткам терапии, чего не наблюдалось у больных контрольной группы (р < 0,001). В относительных величинах снижение уровня общего холестерина составило 17 % против 13 % в исследуемых группах соответственно.
Таблица 3
Частота повышенных значений показателей липидного обмена (холестерин общий, холестерин ЛПВП, триглицериды, коэффициент атерогенности), %
|
Показатель
|
1 группа (ремаксол) (n = 62)
|
2 группа (адеметионин) (n = 46)
|
|
До лечения
|
После лечения
|
До лечения
|
После лечения
|
Р
|
|
1
|
2
|
3
|
4
|
|
|
Холестерин общий, мкмоль/л
|
Частота повышенных значений
|
77 %
|
|
85 %
|
|
Р1-3 > 0,05
|
|
Значения
|
6,96 ± 0,18
|
5,80 ± 0,23*
|
6,73 ± 0,20
|
5,82 ± 0,26*
|
Р1-2 < 0,05 Р3-4 < 0,05
|
|
Триглицериды, мкмоль/л
|
Частота повышенных значений
|
45 %
|
|
39 %
|
|
Р1-3 > 0,05
|
|
Значения
|
4,28 ± 0,36
|
2,64 ± 0,42*
|
4,19 ± 0,47
|
4,43 ± 0,63
|
Р1-2 < 0,05 Р3-4 > 0,05
|
|
Коэффициент атерогенности
|
Частота повышенных значений
|
87 %
|
|
91%
|
|
Р1-3 > 0,05
|
|
Значения
|
6,42 ± 0,14
|
4,25 ± 0,16**
|
5,14 ± 0,22
|
4,94 ± 0,28
|
Р1-2 < 0,005 Р3-4 > 0,05
|
Примечание: * — достоверность отличий р < 0,05; ** — достоверность отличий р < 0,005.
После курса инфузионной терапии ремаксолом у 76 % больных основной группы с исходной гипертриглицеридемией наблюдалось существенное снижение уровня триглицеридов (на 38 %), тогда как препарат группы сравнения не оказывал никакого влияния на данный показатель липидного обмена, играющий важную роль в прогрессировании процессов жировой дегенерации печени при развитии НАСГ.
Таким образом, в ходе исследования установлено более интенсивное влияние ремаксола по сравнению с адеметионином на показатели липидного обмена, заключающееся в снижении уровней основных атерогенных липидов: общего холестерина, триглицеридов, что свидетельствует о положительном влиянии инфузионной терапии метаболическим корректором ремаксолом на один из основных метаболических дефектов при метаболическом синдроме за счет устранения липотоксичности.
Влияние инфузионной терапии на процессы ПОЛ мононуклеаров периферической крови
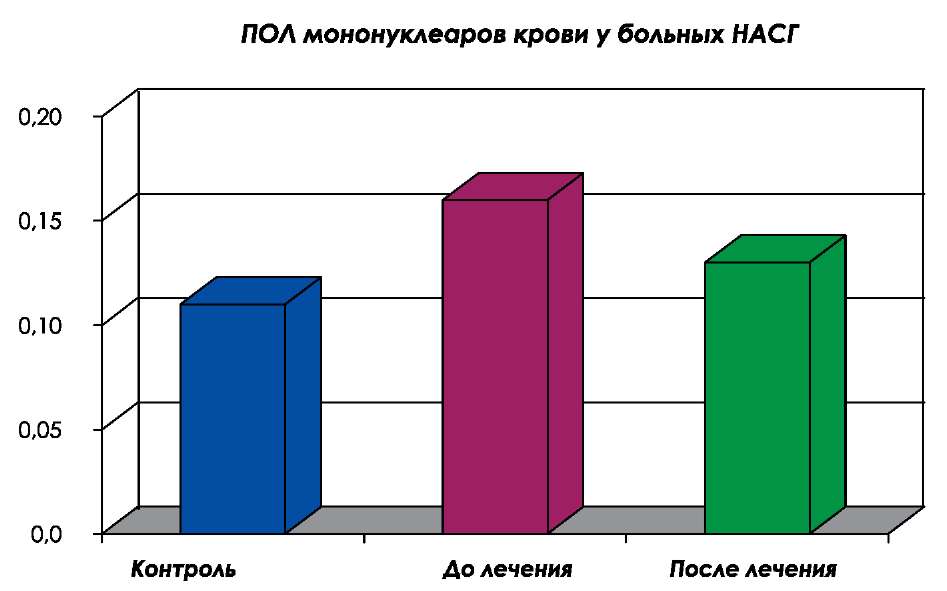
Исходно у пациентов обеих групп было установлено избыточная активация процессов ПОЛ мононуклеаров периферической крови (рис. 1). Частота повышенных показателей ПОЛ мононуклеаров периферической крови составила 99 0% в основной группе и 98 % в группе сравнения, что указывает на наличие дисфункции клеток системы мононуклеарных фагоцитов, превалирование процессов оксидативного стресса у данной категории больных, что объективизирует актуальность назначения антиоксидантных, энергокорригирующих препаратов [9]. В этой связи применение метаболического корректора ремаксола способствовало снижению интенсивности процессов ПОЛ мононуклеаров периферической крови (рис. 1).
Рис. 1. Динамика выраженности процессов ПОЛ мононуклеаров периферической крови у исследуемых больных на фоне инфузионной терапии ремаксолом.
Влияние инфузионной терапии на ультразвуковые признаки стеатоза печени
При оценке выраженности гепатомегалии, дистального затухания сигнала и степени стеатоза печени в группе больных, получавших ремаксол, наблюдалась тенденция к более значительному изменению ультразвуковой картины печени на фоне проводимого лечения. Положительная динамика в уменьшении степени стеатоза печени выражалась в уменьшении количества пациентов с 3-4 степенью стеатоза и увеличении числа больных с 1-2 степенью стеатоза.
Заключение
Таким образом, применение ремаксола у пациентов с НАСГ способствовало: регрессии основных клинических синдромов НАСГ (болевого абдоминального, диспепсического, астеновегетативного); улучшению функционального состояния печени (снижение выраженности синдрома цитолиза, холестаза, уменьшению выраженности гепатомегалии, снижению степени стеатоза печени [по данным УЗИ]); улучшению показателей липидного обмена (снижение уровня общего холестерина, триглицеридемии, уменьшение коэффициента атерогенности); уменьшению выраженности процессов ПОЛ мононуклеаров периферической крови.
Выводы
Ремаксол, прошедший полный этап доклинического изучения и клинического исследования, рекомендованный к применению в практическом здравоохранении при нарушении функциональной активности печени [15], при исследовании эффективности в лечении НАСГ в рамках метаболического синдрома проявил себя как препарат, обладающий мембраностабилизирующим, антиоксидантным, антихолестатическим, гиполипидемическим действием. Эффективность применения ремаксола у пациентов с НАСГ при метаболическом синдроме указывает на роль гепатопротекторного липидрегулирующего влияния антиоксидантной терапии в восстановлении функционального статуса печени как органамишени при указанной патологии. Проблема нарушений нескольких видов обмена при метаболическом синдроме, превалирование проявлений оксидативного стресса как типового патологического процесса, поражение ключевого обменного органа — печени — диктуют необходимость осмысленного назначения патогенетически значимых лекарственных средств из группы метаболических корректоров с гепатопротективной и антиоксидантной направленностью пациентам с НАСГ.
Список литературы
1. Буеверов А. О. Жирная печень: причины и последствия. Практикующий врач. 2002; 1: 36-38.
2. Зайчик А. Ш., Чурилов Л. П. Основы общей патологии. Часть 1. СПб.: Элби. 1999.
3. Ивницкий Ю. Ю., Софронов А. И. Янтарная кислота в системе средств метаболической коррекции функционального состояния и резистентности организма: СПб. 1998.
4. Козлов В. К., Стельмах ВВ. Применение корректоров клеточного метаболизма и регуляторов энергетического обмена клеток в комплексной этиопатогенети-ческой терапии больных хроническим вирусным гепатитом С. Медицинские новости. 2004; 4: 5-9.
5. Радченко В. Г., Баскович Г. А., Стельмах ВВ.. Реамберин в комплексной терапии хронических гепатитов. Мир медицины. 2001;9-10: 19-22.
6. Радченко В. Г., Стельмах ВВ. Применение реамберина в комплексной терапии хронических гепатитов. 2001.
7. Радченко В. Г., Стельмах ВВ. Способ лечения больных хроническим гепатитом С. Бюл. 2004, № 1.
8. Сологуб Т. В., Горячева Л. Г. и др. Гепа-топротективная активность ремаксола при хронических поражениях печени (материалы многоцентрового рандомизированного плацебо-контролируемого исследования). Вестник СПбГМА им. И. И. Мечникова. 2009; 2 (31): 1-8.
9. Козлов В. К., Стельмах ВВ. Оксидативный стресс в патогенезе дисфункции иммунной системы при инфекционной патологии. Модификаторы энергетического обмена клеток как средства патогенетической иммуноориентированной терапии. Материалы международного Евро-Азиатского конгресса по инфекционным болезням. Беларусь, Витебск — 2008: 106-109.
10. Стельмах ВВ., Радченко В. Г., Козлов В. К. Метаболические корректоры на основе янтарной кислоты как средства патогенетической терапии при хронических вирусных гепатитах. Терапевтический архив. 2011; 2: 67-71.
11. Angulo P., Keach J. С., Batts K. P., Lin-dor K. D. Independent predictors of liver fibrosis in patients with nonalcoholic steatohepatitis. Hepatology. 1999; 30: 1356-1362.
12. Angulo P. Nonalcoholic fatty liver disease. J Gastroenterol Hepatol. 2002; 17 (Suppl):S186-S190.
13. Belentani S., Scaglioni F., Marino M., et. al. Epidemiology of non-alcoholic fatty liver disease. Dig Dis. 2010; 28:155-161.
14. Caldwell S., Argo C. The natural history of nonalcoholic fatty liver disease. Dig Dis.2010; 28: 162-168.
15. Dixon J. B., Bhathal P. S., O'Brien P. E. Nonalcoholic fatty liver dsease: predictors of nonalcoholic steatohepatifs and liver fibros's in the severely obese. Gastroenterology. 2001; 121: 91-100.
16. Guzman G., Brunt E. M., Petrovic L. M. et al. Does nonalcoholic fatty liver disease predispose patients to hepatocellular carcinoma in the absence of cirrhosis? Arch
Pathol Lab Med. 2008; 132: 1761-1766.
17. Marchesini G., Bugianesi E., Forlani G. et al. Nonalcoholic fatty liver, steatohepatitis and the metabolic syndrome. Hepatology. 2003; 37:917-923.
18. Ong J. P., Pitts A., Younossi Z. M., Increased overall mortality and liver-related mortality in nonalcoholic fatty liver disease. J. Hepatol. 2008; 49: 608-612.
19. Poli G. Pathogenesis of liver fibrosis: role of oxidative stress. Mol Aspects Med.—2000. — 21 (3): 49-98.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru

