Патогенетически обоснованная, с оценкой качества жизни, расчетом риска исхода заболевания, терапия больных вирусным гепатитом С
Статьи
Опубликовано в журнале:
«АНТИБИОТИКИ И ХИМИОТЕРАПИЯ» 2010, ТОМ №55, № 3-4, с. 3-13
М. Г. РОМАНЦОВ1, Т. В. СОЛОГУБ1, Л. Г. ГОРЯЧЕВА6, С. Н. КОВАЛЕНКО4, Д. С. СУХАНОВ1, А. А .ШУЛЬДЯКОВ2, А. Н. БОНДАРЕНКО3, А. Л. КОВАЛЕНКО5, А. Ю. ПЕТРОВ5
1 Санкт-Петербургская государственная медицинская академия им. И. И. Мечникова
2 Саратовский государственный медицинский университет
3 Центр диагностики и лечения инфекционных болезней, Кривой Рог, Украина
4 Санкт-Петербургский филиал Современной гуманитарной академии
5 Научно-технологическая фармацевтическая фирма «ПОЛИСАН», Санкт-Петербург
6 НИИ детских инфекций ФМБА, Санкт-Петербург
Pathogenetically Substantiated Therapy of Patients with Virus Hepatitis C, the Life Quality and the Disease Outcome Risk (Clinical Survey)
M. G. ROMANTSOV, T. V. SOLOGUB, L. G. GORYACHEVA, S. N. KOVALENKO, D. S. SUKHANOV,
A. A. SHULDYAKOV, A. N. BONDARENKO, A. L. KOVALENKO, A. YU. PETROV
I. I. Mechnikov St. Petersburg State Medical Academy, St. Petersburg Saratov State Medical University, Saratov
Centre for Diagnosis and Treatment of Infectious Diseases, Krivoi Rog, Ukraine St. Petersburg Branch of Contemporary Humanitarian Academy, St. Petersburg Scientific and Technological Pharmaceutical Company POLISAN, St. Petersburg Research Institute of Children Infections, St. Petersburg
Обсуждаются вопросы иммунопатогенеза вирусного гепатита С, акцентируется внимание на повышенной продукции Th1 цитокинов, обеспечивающих активную защиту организма от HCV-инфекции. Представлены современные подходы к терапии хронического гепатита С, описанные в литературе, а также собственные данные авторов, включающие проведение пациентам «тройной терапии», с использованием иммуномодуляторов (циклоферона в инъекционной и таблетированной форме, галавита и дерината) различного механизма действия. Проведена сравнительная оценка эффективности терапии. Показано, что циклоферон у наркопотребителей на фоне вирусного гепатита является препаратом выбора. Описана клинико-лабораторная эффективность метаболического гепатопротектора ремаксола с антиоксидантной активностью. Высокая его эффективность в сочетании с хорошей переносимостью (побочные эффекты, требующие отмены препарата встречались только в 0,3% случаев) и минимальным риском отсутствия биохимической ремиссии позволяет расценивать ремаксол как высокоэффективный метаболический гепатопротектор для патогенетической терапии хронических гепатитов.
Ключевые слова: гепатит С, лечение, иммунопатогенез, благоприятный исход заболевания, риск неблагоприятных исходов, биоптат печени.
The aspects of virus hepatitis C immunopathogenesis are discussed. The main attention is paid to higher production of Th1 cytokines providing active protection of the host from HCV. The up-to-date approaches to the therapy of chronic hepatitis C, described in the literature and the original ones, including the triple therapy with immunomodulators of various mechanisms of action, i.e. cycloferon (injections and tablets), galavit and derinat are presented. The comparative efficacy of the therapy is estimated. Cycloferon is shown to be the drug of choice in the treatment of patients with virus hepatitis addicted to narcotics. The clinical and laboratory efficacy of the metabolic hepatoprotector remaxol with antioxidant activity is described. Its high effictivity and satisfactory tolerability (side effects requiring discontinuation of the drug use were recorded only in 0.3% of the cases), as well as the minimal risk of no biochemical remission after its use allow to conseder remaxol as a highly efficient metabolic hepatoprotec-tor for pathogenetic therapy of chronic hepatitis.
Key words: hepatitis С, therapy, immunopathogenesis, favourable outcome, unfavourable outcome risk, liver bioptat.
Хронический гепатит С (ХГС) является прогрессирующим заболеванием с переходом в цирроз и карциному печени, распространённость которого колеблется от 3 (0,3—14,5%) до 5% в популяции. В России заболеваемость гепатитом С составляет приблизительно 12 человек на 100000 населения [1—4]. Для лечения больных в качестве стандарта терапии широко используется интерферон-альфа-2а. Лучше поддаются лечению больные, инфицированные вирусами с генотипами 1а и 2а, чем больные, инфицированные вирусом с генотипом 1b. Максимальные результаты терапии достигаются при лечении больных с невысоким уровнем виремии и гиперферментемии. Эффективность терапии HCV-инфекции не велика и связана с высокой частотой развития нежелательных побочных эффектов [5—11]. «Золотым стандартом» лечения ХГС считается терапия, предусматривающая введение альфа-интерферона 3 раза в неделю в комбинации с ежедневным введением рибавирина в дозе 800—1200 мг (в зависимости от массы тела больного) в течение 6—12 месяцев [12—14].
Терапия хронического гепатита С постоянно совершенствуется, предлагаются новые лекарственные препараты и комбинации лекарственных средств, принадлежащих к разным фармакологическим группам [15—20]. С целью повышения эффективности лечения ХГC рекомендуется применение пегилированных интерферонов в комбинации с рибавирином [21—23]. Однако, наряду с улучшением эффективности лечения ХГС, применение пегилированных интерферонов приводит к резкому увеличению осложнений, уменьшая приверженность пациентов к лечению [24—28].
Цитолиз гепатоцитов связан не с активной репродукцией вируса или действием его белков на клеточные функции, а с характером иммунного ответа. Развитие воспалительного процесса в печени и презентация вирусных антигенов на поверхности гепатоцитов приводят к активации иммунных реакций, направленных на лизис заражённых клеток, а элиминация вируса определяется типом иммунного ответа. Именно дисбаланс между Th1-и Th2-ответом на HCV-инфекцию ответственен за течение заболевания. Повышенная продукция Th1 цитокинов (ИФН-γ и ФНО) необходима для активной защиты от HCV, а Th2 цитокины, подавляя иммунные реакции, обеспечивают хронизацию инфекционного процесса. Мутационная изменчивость вируса в период развития инфекционного процесса связана с рецидивами заболевания, когда идёт активная репликация вируса и приводит к тому, что продуцируемые антитела не способствуют остановке вирусной репродукции, препятствуя эффективной презентации вирусных антигенов [29—35].
Становится совершенно очевидно, что эффективность терапии больных ХГС можно повысить включением в стандартную терапию иммунотропных препаратов, модулирующих иммунный ответ. Улучшение эффективности лечения достигается стимулированием выработки цитокинов Th1 иммунного ответа, минимизируя при этом побочные реакции противовирусной терапии. Дополнительные возможности эффективной терапии связывают с индивидуальным подбором дозы препарата для каждого конкретного больного [1, 3, 30, 36—40].
Особенностью противовирусного иммунитета при ХГС является защита организма от внутриклеточного патогена, что реализуется уничтожением инфицированных вирусом клеток и/или нарушением репликации вируса в клетке [32, 33, 41, 42]. В первом случае IL-2 и гамма-ИФН активируют NK-клетки и цитотоксические лимфоциты, которые, определив клетку как чужеродную, вводят в неё растворимые белки (протеолитические и липолитические ферменты), приводящие к гибели клетки. Во втором случае активируются интерфероны, взаимодействуя со своим рецептором, передают сигнал ядру клетки. Включаются гены, кодирующие белки, ингибирующие репликацию вируса, блокируя через соответствующие клеточные рецепторы, синтез вируса в клетке [20, 29, 33, 42].
Регуляторный фактор интерферона фосфорилируется и перемещается в ядро, инициируя транскрипцию интерферона через образование интерферон-стимулирующего ген фактора 3. Связываясь с дсРНК, интерферон инициирует активность геликаз, активирующих цитоплазматические киназы, индуцируя антивирусные гены, ингибирующие репликацию вируса, трансляцию, индуцируя апоптоз, а связываясь промотором гена интерферона, стимулируют его транскрипцию [5, 16, 32, 35]. Таким образом, индуцируется «противовирусное состояние», характеризующееся не только подавлением вирусной репликации, но и способностью лизировать инфицированные вирусом клетки. Множественность механизмов инактивации противовирусных эффектов интерферонов и продуктов его индукции в инфицированных клетках свидетельствует о том, что HCV высоко адаптирован к реакциям неспецифического иммунного ответа. В условиях различного уровня экспрессии вирусспецифических белков вирус может подавлять систему клеточной защиты или «ускользать» от действия реакций иммунного ответа. Важную роль, как в устойчивости к интерферонотерапии, так и в хронизации инфекционного процесса, играет ИЛ-8: он как антагонист α-ИФН способен подавлять противовирусную защиту [7, 14, 32, 43].
Интерферон II типа (γ-ИФН) влияет на процессы клеточного иммунитета, как неспецифического, так и специфического, поэтому он и получил название «иммунный интерферон». Его ген локализован в 12-й хромосоме и обнаружен на СД4+ и СД8+ лимфоцитах. Под влиянием γ-интерферона Т-лимфоциты синтезируют ИЛ-2, ИЛ-12, другие цитокины, потенцирующие Thl-клеточный иммунный ответ [20, 29, 31, 33, 38].
Знание иммунопатогенеза ХГС позволяет проводить коррекцию цитокинового статуса, что может быть весьма эффективным в отношении снижения частоты рецидивов и усиления фармакологического эффекта препаратов α-ИФН [16, 30, 31, 34, 35, 38].
В рандомизированных клинических исследованиях [3, 36, 37] показан синергидный эффект α-интерферона и иммуномодулятора с противовирусной активностью — циклоферона, позволяющего поддерживать у пациента постоянный уровень эндогенного интерферона в крови при лечении не только ХГВ, но и ХГС.
Обследовано 86 мужчин в возрасте 16—30 (22,6±0,8 лет) лет с верифицированным диагнозом: хронический вирусный гепатит С; 1b генотип, в фазе репликации (RNA HCV +) с длительностью заболевания от 6 месяцев до 5 лет при уровне АлАТ в 1,5—5 раз больше нормы. В соответствии с методикой рандомизации (метод «конвертов») сформированы две группы пациентов. В первой группе пациентов (n=43) проводилась стандартная терапия: α2-интерферон (3 млн МЕ/м2 1 раз в сутки подкожно 3 раза в неделю) и рибавирин (800—1200 мг в сутки ежедневно) в течение 48 недель. Во второй группе (n=43) дополнительно к стандартной терапии (α2-интерферон + рибавирин) пациенты получали циклоферон (перорально 1 раз в сутки по 600 мг два дня подряд, а затем 3 раза в неделю) в течение 48 недель. Клиническая картина репликативной фазы ХГС характеризовалась мягким течением и неярко выраженной симптоматикой. Пациенты активно не предъявляли жалоб, они выявлялись только при целенаправленном опросе у 87% больных.
По окончании 3-месячного курса лечения 15,4% больных, получавших стандартную противовирусную терапию (первая группа), обращали внимание на улучшение самочувствия и исчезновение астеновегетативных симптомов, однако 36 (42,8%) пациентов предъявляли жалобы на снижение физической активности и 7 (8,3%) больных отмечали ухудшение самочувствия со снижением трудоспособности. Пациенты второй группы (69,2%), получавшие «тройную» терапию, чувствовали себя лучше, а 42,0% больных отмечали повышение работоспособности. Больным c отрицательным эффектом терапии (на этапе 3-месячного наблюдения) проводилась коррекция лечения (назначался 12,5% раствор циклоферона и пэгинтерферон).
Антивирусный ответ в этот же срок отсутствовал у 11 (27,5%) пациентов первой группы, получавших стандартную терапию, и у 14 (34,1%) больных второй группы, получавших тройную терапию. Устойчивый вирусологический ответ (стабильная ремиссия) через 24 недели терапии наблюдался у 56,3% больных, получавших стандартную комбинацию (а-интерферон+рибавирин) и у 68,3% больных второй группы, получавших дополнительно к стандартной терапии таблетки циклоферона (табл. 1), который повысил эффект терапии на 12,0%.
Таблица 1. Эффективность шестимесячной противовирусной терапии больных ХГС
| Наблюдаемые группы больных (получаемые ими препараты) |
Число пациентов |
Выход больных в ремиссию абс. (%) |
| первичная |
полная |
стабильная |
| Первая (α-интерферон+рибавирин) |
32 |
30 (93,8) |
21 (65,6) |
18 (56,3) |
| Вторая (α-интерферон+рибавирин+циклоферон) |
41 |
39 (95,1) |
30 (73,2) |
28 (68,3) |
Необходимо отметить, что в период с 3 до 6 месяцев отказались продолжать лечение 14 пациентов первой группы. Причиной отказа от продолжения терапии явилось появление побочных эффектов: депрессивная симптоматика, снижение уровня качества жизни в виде астенической усталости, болевых ощущений, трудности в выполнении обычных повседневных дел, невозможности функционировать в привычном для пациентов режиме.
Нейтропения (менее 0,75х 109/л) отмечалась у 1 пациента первой группы, что потребовало временного снижения дозы рибавирина. Уровень тиреотропного гормона повысился у 4 больных первой группы (12,5%), у 1 (3,1%) пациента выявлен аутоиммунный тиреоидит, потребовавший отмены противовирусной терапии. Лечение прекращено у 14 (32,6%) пациентов первой группы (у 1 больного аутоиммунный тиреоидит), у 2 — цитопенический синдром, а 6 человек самостоятельно прекратили лечение раньше срока (2 — из-за выраженного снижения веса; 1 — из-за выпадения волос, а 3 пациента из-за усиления депрессивной симптоматики, не приводящей к улучшению качества жизни на фоне проводимого лечения), а во второй группе пациентов, дополнительно получавших циклоферон, все завершили полный курс лечения. Среди больных 2-й группы у 5 (11,6%) человек отмечено обострение сопутствующей гастродуоденальной патологии, у 1 — выявлен аутоиммунный тиреоидит. Этим больным противовирусная терапия была продолжена. Снижение массы тела колебалось от 5 до 12 кг. Выпадение волос регистрировалось у 45,5% больных, получавших стандартную терапию, и лишь у 22,8%, получавших терапию с циклофероном. Этот симптом купировался применением шампуней с цинком. У больных со стойким вирусологическим и биохимическим ответом (стабильная ремиссия) признаков рецидива HCV-инфекции не отмечено в течение 12 месяцев после окончания терапии.
Морфологическое исследование биоптатов печени проведено у 40 больных (у 18 из первой группы и у 22 больных второй группы). По данным пункционной биопсии печени, нами подтверждено антифибротическое действие проводимой терапии, а также высокая противовирусная активность препаратов даже у тех больных, у которых полная ремиссия (биохимическая и вирусологическая) не была достигнута. Минимальная степень активности (ИГА=1—3 балла) установлена у 3 (16,6%) и 4 (19%) больных, низкая (ИГА= 4—8 баллов) у 11 (61,1%) и 12 (57,1%), умеренная (ИГА=9—12 баллов) — у 4 (22,2%) и 5 (23,8%) больных соответственно в обеих группах. У 35 из 40 (87,5%) больных выявлен слабый фиброз (ГИС=1 балл), а у 4 — выраженный фиброз (ГИС=3 балла). Гистологическое улучшение (снижение активности по шкале Knodell на 2 балла) отмечалось у 12 (37,5%) человек, получавших стандартную терапию, и у 24 (58,5%) больных, получавших тройную терапию с циклофероном; на 3—4 балла — у 7 (21,9%) человек и у 12 (29,3%) больных соответственно при отсутствии прогрессирования фиброза.
Лечение больных ХГС с помощью лекарственных средств, включённых в стандарт лечения, сопряжено с множеством нежелательных эффектов [3, 8, 24, 25, 27, 37]. В связи с этим раннее выявление пациентов, у которых лечение может оказаться неэффективным, позволит избежать нежелательных реакций, повысить эффективность лечения, улучшив качество жизни больных. Для повышения эффективности противовирусной терапии необходимым условием является разработка новых этиотропных препаратов, либо включение в схему лечения дополнительных препаратов, обеспечивающих больший терапевтический эффект и улучшающих переносимость стандартных схем лечения, а индивидуальный подбор препарата, персонализированные схемы лечения, оптимальный курс и длительность терапии позволят добиться максимального вирусологического ответа в каждом отдельном случае [1, 3, 44, 45].
Методом амперометрического титрования, в зависимости от изменения величины SH-групп и коэффициента SH/SS, проведён подбор доз препаратов каждому больному [3]. Под наблюдением находились 180 пациентов с верифицированным диагнозом «хронический гепатит С», из них — 112 мужчин и 68 женщин. Средний возраст 33,08±2,34 лет.
Способ индивидуального подбора лекарственных препаратов включает культивирование цельной гепаринизированной крови в течение 1 часа при 37°С с тестируемыми препаратами, вводимыми в кровь в дозе, соответствующей 1:5000 от терапевтической. Определение соотношения SH/SS-групп в крови больного после культивирования, количества SH-групп — амперометрическим титрованием раствора нитрата серебра, SS-групп — на основании падения тока после внесения гипосульфита натрия и выбор оптимального препарата — по определению наибольшего соотношения SH/SS-групп в пределах 2,6—4.
Увеличение содержания SH-групп (на 10% и более) и увеличение коэффициента SH/SS (в 1,5—2 раза), в сравнении с контрольными значениями, квалифицировалось нами как высокая чувствительность пациентов к препарату. Снижение содержания SH-групп более чем на 10% с уменьшением коэффициента SH/SS расценивалось как отсутствие чувствительности пациента к данной дозе препарата.
У больных ХГС имеются существенные изменения в системе антиоксидантной защиты (АОС). Так, у 153 (85,0%) пациентов выявлено повышение более чем в 4 раза уровня небелковых SS-групп в крови по сравнению со здоровыми лицами. У 82,22% обследованных больных наблюдали повышение содержания небелковых SH-групп (до 2,64 мМ/л), при среднем значении показателя — 2,24±0,4 мМ/л. Изменения, выявленные в тиолдисульфидной системе, свидетельствуют о нарастании процессов окисления в клетке на фоне повышения (в 1,5 раза) перекисного окисления липидов при среднем значении показателя 0,12±0,02 М/л. Изменения наблюдались и в ферментном звене антирадикальной защиты. Так, наблюдалось повышение (от 42,35 ед/г•сек. до 75,22 ед/г•сек) активности СОД у 80,56% обследованных, снижение активности каталазы — у 74,44% больных ХГС. Выявленные изменения показателей АОС указывают на усиление интенсивности окислительных процессов и повышение активности ферментного звена АОС у больных ХГС.
Повышение содержания SH-групп на 10% и более, по сравнению с контрольными значениями, после инкубации крови с циклофероном в дозе 500 мг (4,0 мл 12,5% раствора) отмечено у 35,7% больных, с галавитом — у 37,1%, с деринатом — у 40,71% обследованных.
Рандомизацию больных проводили, применяя «метод конвертов» с разделением больных на 4 группы. Первую группу составили 50 больных ХГС, которым кроме стандартной терапии α-ИФН (альфароном) и рибавирином был назначен циклоферон в оптимально подобранной дозе — 500 мг (4,0 мл 12,5% раствора). Вторую группу составили 45 больных ХГС, которым наряду с α-ИФН и рибавирином назначался галавит в дозе 100 мг через день. В третью группу вошли 45 больных, которым наряду с α-ИФН и рибавирином назначался деринат в дозе 5 мл 1,5% раствора. Четвёртую контрольную группу составили 40 больных ХГС, получавших только стандартную терапию α-ИФН и рибавирин без добавления третьего препарата. Эффективность терапии оценивалась по достижению «быстрого» (через 1 месяц от начала терапии), «раннего» (через 3 мес. от начала терапии) и «стойкого» вирусологического ответа (через 6 мес. от начала терапии при 2-м и 3-м генотипе HCV-инфекции и через 12 мес. от начала терапии при 1-м генотипе HCV-инфекции). В последующем продолжалось наблюдение за пациентами для оценки устойчивого вирусологического ответа через 6—12 мес. после окончания терапии.
Оценивая динамику цитолитического синдрома больных ХГС 1-го генотипа НCV, получавших различные препараты, установлено, что к окончанию терапии у всех больных, получавших галавит, отмечены нормальные показатели АЛТ; в группе больных, получавших деринат — в 91,30% случаев; у получавших циклоферон — в 92,59% случаев, а у пациентов контрольной группы — в 83,33% случаев.
При сравнении эффективности терапии (рис. 1) больных ХГС (1b генотип HCV) отмечены ее особенности. У больных, получавших в качестве третьего препарата циклоферон (первая группа), полный ответ на терапию наблюдался в 70,0% случаев, у получавших в качестве третьего препарата галавит (вторая группа) — в 64,4%, получавших деринат (третья группа) — в 73,3%, а у пациентов контрольной четвёртой группы полный ответ на терапию был зафиксирован только в 50,0% случаев.
Рис. 1. Эффективность противовирусной терапии больных HCV-инфекцией, получавших иммуномодуляторы.

Для суждения об эффективности лекарственного препарата одним из способов является оценка его влияния на риск возникновения благоприятного/неблагоприятного исхода заболевания. Одними из наиболее распространенных показателей, как считает T. L. Chap, являются относительный риск и снижение риска1. Относительный риск (RR) определяется как отношение риска наступления исхода в группе применения изучаемого лекарственного средства к риску наступления исхода у больных контрольной группы или группы сравнения. Вероятность наступления благоприятного исхода у больных, получавших циклоферон (RR=0,384), выше по сравнению с пациентами, получавшими стандартную терапию (интерферон+рибавирин) (RR=0,247), при этом величина относительного риска составила 1,55 (>1/0), указывая на достоверное преобладание благоприятного исхода заболевания у больных в исследуемой группе.
Наступление стабильной ремиссии (благоприятный исход заболевания), рассчитанное у больных, получавших в качестве третьего препарата один из иммуномодуляторов (циклоферон, галавит, деринат), показало, что благоприятный исход заболевания более вероятен у пациентов, получавших циклоферон (RR1—2=1,2, RR1—3 =1,06), в сравнении с галавитом и деринатом, поскольку у больных контрольной группы показатель RR1—4=1,74.
Интерферонотерапия сопровождается известными нежелательными побочными эффектами. Реже регистрировались гриппоподобный и депрессивный синдромы у пациентов, получавших циклоферон, а их проявления были менее выражены, чем у больных контрольной группы. У больных, получавших деринат, реже регистрировалась анемия, лейкопения и тромбоцитопения.
Традиционно принято обращать внимание на клинические, лабораторные и метаболические параметры, характеризующие состояние больного, отражая результаты лечения. Оценка уровня здоровья проводится с учетом медицинского состояния, находя свое выражение в клиническом диагнозе. Хроническое заболевание ограничивает социальную адаптацию пациента за счёт нарушения личностно-средового воздействия. Исследования психологических особенностей пациентов, инфицированных НСV, выявили психогенные нарушения, связанные с реакцией на факт выявления заболевания, а сам факт установления диагноза «гепатит С», явился психологическим и эмоциональным «срывом», а некоторые пациенты, инфицирование НСV, рассматривают это как «социальный позор». Патопсихологические изменения в структуре личности пациентов с ХГС развиваются и на фоне течения хронического вирусного процесса, т. е. при длительном персистировании в организме вируса гепатита С ухудшается уровень качества жизни пациентов, особенно в параметрах ментальных функций. Относительный вклад психологических, поведенческих и клинических факторов в уровень качества жизни пациентов, страдающих ХГС, мало исследован. Демографические, клинические и вирусологические факторы не коррелируются с показателями качества жизни больных ХГС. Основными симптомами пациентов при ХГС являются физическое утомление (у 86%), раздражительность (у 75%,) депрессия и когнитивные нарушения (у 70%), абдоминальная боль (у 68% пациентов). Регрессионный анализ факторов показывает, что депрессия, курение, алкоголь являются наиболее существенными маркерами, влияющими на качество жизни при ХГС, а употребление наркотиков, отсутствие семьи у больных ХГС резко снижают его уровень. Важнейшим фактором, влияющим на уровень качества жизни мужчин, инфицированных НСV, является сексуальная дисфункция, не зависящая от уровня депрессии пациента [7, 10, 24, 27, 28, 46, 47].
Влияние лечения на параметры качества жизни при проведении стандартной терапии ХГС (интерферон+рибавирин) оценивается неоднозначно (74% пациентов указывают на физическую слабость, гриппоподобный синдром встречается в 32%, а депрессия — в 38% случаев). У 24% опрошенных отмечаются осложнения при общении с членами семьи и друзьями, а 31% пациентов сообщают о трудностях во взаимоотношении с коллегами по работе. Наличие депрессии или состояния, близкого к ней, является стимулирующим фактором прогрессирования заболевания на фоне отсутствия приверженности к терапии [7, 24, 46].
У больных, получавших дополнительно к стандартной терапии циклоферон, положительная динамика качества жизни наблюдалась уже к концу 3-го месяца наблюдения от начала терапии. Особенно четко это прослеживалось по увеличению (на 30 баллов) физической активности, а социальная активность возросла на 24 балла. Показатель общего восприятия здоровья оценивался больными в 34 балла. К окончанию курса лечения удовлетворенность качеством жизни, как по физическим, так и по психологическим параметрам, достигла 90 баллов и более. Оценка общего восприятия здоровья, уровня жизнеспособности, психического состояния и эмоционального статуса превысила 97 баллов [37, 48].
Повышает уровень качества жизни больных и лечение наркотической зависимости на фоне гепатита С, за исключением пациентов, имеющих большой стаж употребления наркотиков при низких когнитивных функциях.
В проведённом А. Н. Бондаренко исследовании 324 наркопотребителей с вирусным гепатитом [44, 45] показан клинический эффект циклоферона (применение по 4,0 мл на 1-, 2-, 4-, 6-, 8-, 11-, 14-, 17-, 20- и 23-й дни, затем препарат вводили в поддерживающем режиме по 2,0 мл 2 раза в неделю) у 80% больных. Сопоставление чувствительности пациентов к циклоферону с клинической эффективностью препарата у больных, ответивших на индуктор, выявило повышение индекса сдвига и индекса чувствительности к циклоферону соответственно в 1,7 и 1,5 раза, чем у больных с низкой эффективностью препарата.
Синтез сывороточного α-ИФН в крови у больных вирусным гепатитом, не ответивших на индуктор, был в 2 раза выше (72,8 пкг/мл), чем у пациентов, ответивших на введение препарата (19,7±3,85 пкг/мл). Введение циклоферона больным, ответившим на терапию, повышало уровень α-ИФН в крови до 118,4±3,91пкг/мл, а у больных вирусным гепатитом, не ответивших на индуктор, синтез сывороточного α-ИФН снижался до 25,8 пкг/мл (рис. 2).
Рис. 2. Динамика уровня сывороточного α-интерферона у больных, получавших циклоферон.
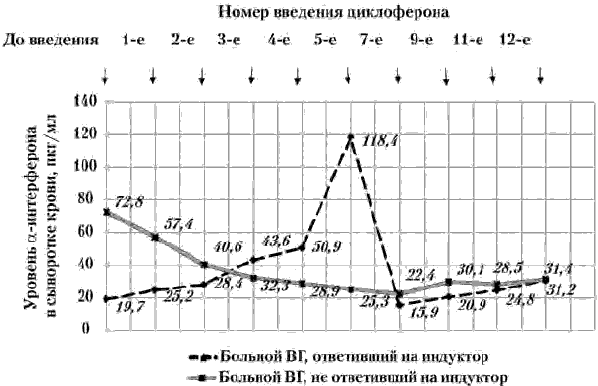
Информативным, в плане прогноза эффективности терапии, является уровень синтеза сывороточного α-ИФН после первых введений циклоферона. Повышение (более чем на 20%) уровня сывороточного α-ИФН в крови указывает на высокую вероятность эффективности препарата. Если в результате применения циклоферона, уровень интерферона снижается или не повышается, то его эффективность будет низкой. Коэффициент корреляции (r) чувствительности к циклоферону с индукцией синтеза α-ИФН и клинической эффективностью препарата составили 0,81 и 0,89, свидетельствуя о выраженной прямой положительной связи между чувствительностью к индуктору, индукцией синтеза α-ИФН и клиническим эффектом его применения. У 7% наркопотребителей с тяжёлым и длительным течением вирусного гепатита (микст-ВГ) применение циклоферона после глюкокортикоидной терапии оказалось единственным средством, позволившим достичь нормализации состояния и длительной ремиссии. Применение циклоферона у наркопотребителей на фоне вирусного гепатита может сопровождаться серьёзными осложнениями в случае его использования на фоне введения опиатов (резкое ухудшение течения гепатита с развитием печёночной энцефалопатии), особенно при употреблении больными опиатов во временном интервале 12—24 ч до или после введения индуктора. Оценку вероятности осложнений при применении индуктора интерферона у наркопотребителей на фоне вирусного гепатита с высокой вероятностью (80% и более) можно проводить, определяя чувствительность пациента к препарату в тесте Е-РОК. Высокий (более 30%) индекс чувствительности у наркопотребителей с вирусным гепатитом свидетельствует о высоком риске развития осложнений. При невозможности отказа больных от приёма наркотиков применение циклоферона возможно только в режиме, обеспечивающем временной интервал, превышающий 24 ч, между введением опиатов и назначением индуктора.
Повреждения печени вызывают серьезные нарушения метаболизма, иммунного ответа, детоксикации, которые реализуются через химические и иммунологические механизмы. В соответствии с современными принципами лечения хронических заболеваний печени программа комплексной терапии включает два основных направления. Первое, описанное выше, этиотропное лечение, направленное на элиминацию возбудителя и санацию организма. Второе — патогенетическое, осуществляющее адекватную фармакологическую коррекцию универсальных мультифакторных звеньев патогенеза. Универсализм звеньев патогенеза поражений печени позволяет использовать патогенетическую терапию, основу которой составляют лекарственные средства с направленным действием на печеночные клетки.
Патогенетическим подходом является использование препаратов, способных не только восстанавливать митохондриальную мембрану, липидный биослой мембраны клетки, окислительное фосфорилирование, но и модифицировать клеточный обмен. Это возможно за счёт применения гепатопротекторов, обладающих антигипоксическим/антиоксидантным эффектом, поскольку печень является основным местом метаболизма и мишенью токсического действия с первичным нарушением функции мембран. При хронических поражениях печени развивается тканевая гипоксия, приводящая к нарушению функций митохондрий, истощаются запасы АТФ, в результате чего образуются свободные радикалы и активизируется перекисное окисление липидов (ПОЛ). При этом повреждаются клеточные мембраны (цитоплазматическая, митохондриальная) [49, 50]. Т. Г. Кожока [51] выделяет антигипоксанты/антиоксиданты в отдельную группу препаратов — «энергообеспечивающие средства — антигипоксанты», куда включает и сукцинатсодержащие препараты, разработанные на основе янтарной кислоты и/или её солей, в подгруппу «регуляторы энергетического обмена/субстраты энергетического обмена». Их активным компонентом является янтарная кислота (ЯК) — универсальный энергообеспечивающий интермедиат — продукт пятой и субстрат шестой реакций цикла трикарбоновых кислот Кребса. Мощность системы энергопродукции, использующей сукцинат, в сотни раз превосходит другие системы энергообразования организма [51].
К таким препаратам относится «гепатопротекторный метаболит» ремаксол. Нами проведено изучение его эффективности у 494 больных хроническим гепатитом, которые методом рандомизации разделены на 2 группы. Первая группа больных — «исследуемая», получавшая раствор ремаксола, в нее вошло 294 человека. Вторая группа больных — «контрольная», получавшая «активное плацебо», в нее вошло 200 человек. Препараты вводились внутривенно, ежедневно в течение 12 дней по 400 мл. У больных с хроническим поражением печени регистрировался астено-вегетативный и диспептический синдромы соответственно у 58—48% и 43—45% больных. Гепатомегалия отмечена у 88—84% пациентов. Синдром интоксикации, клинически проявляющийся слабостью и утомляемостью, выявлен соответственно у 75—59,9% и 53,7—64,0% больных. Диспептический синдром, проявляющийся снижением аппетита, тяжестью в правом подреберье, тошнотой, болезненностью живота при пальпации, регистрировался соответственно в 18—31% случаев. Нарушение пигментного обмена установлено лишь у 14% больных, а спленомегалия отмечена у 7—8,5%. Артралгический синдром выявлен не более чем у 8% больных, проявляясь болью в мышцах и суставах. У больных в 18% случаев отмечена высокая активность патологического процесса в печени, но у 45% пациентов преобладала умеренно выраженная активность. Концентрация общего билирубина незначительно повышена, превышая уровень нормальных значений в 1,8—1,3 раза, составив 36,0—25,3 мкмоль/л, гипербилирубинемия установлена лишь у 24—18% больных. Выраженный синдром цитолиза, превышающий уровень в норме в 6—4 раза (соответственно по АлАТ и АсАТ), составил 281 и 186 ед/л, при сниженном до 0,6 коэффициенте де Ритиса. ЛДГ характеризует степень окислительно-восстановительных процессов и гликолиза, свидетельствуя о нарушении энергетического обеспечения гепатоцитов и наличии анаэробных процессов окисления, поддерживая гипоксическое состояние, подтверждением чего явился уровень ЛДГ, который у пациентов превышал показатель нормы в 1,3—1,1 раза, составив соответственно 581,1 и 507,5 МЕ. Проявление цитолитического синдрома (катаболизм нуклеиновых кислот за счёт распада ядер гепатоцитов) характеризует и уровень мочевой кислоты в сыворотке крови. У наблюдаемых больных уровень мочевой кислоты соответствовал средним значениям нормы (214—458 мкмоль/л), составив 341,2 мкмоль/л, но в динамике наблюдения (первые 6 суток терапии) отмечался рост показателя в 1,1 раза, составив 374,4 мкмоль/л, не превышая при этом значений нормы. Рост мочевой кислоты в крови отмечен у 5—13% больных и связан с процессом окисления пуриновых азотистых оснований на микросомах (цитохром Р450, НАДФ-зависимые дегидрогеназы), а также с активацией ферментов дыхательной цепи, увеличением синтеза и потребления макроэргов (АТФ), конечным продуктом которого является образование в гепатоците мочевой кислоты. Оценивая средние значения тимоловой пробы, которые незначительно превышали (в 1,6—1,3 раза) уровень нормы, необходимо сказать о её повышенных значениях, которые выявлены у 55,8—40,3% больных, что указывало на нарушение антитоксической функции печени.
Под влиянием проводимой терапии наблюдалось снижение астеновегетативного (-51,2%), диспептического (-39,3%) синдромов, желтухи (-8,9%), гепатомегалии (-12,8%), в сравнении с пациентами, получавшими плацебо. Астеновегетативный синдром у пациентов, получавших плацебо, после окончании терапии регистрировался у 15,3% больных, а у получавших ремаксол, лишь в 7,2% случаев (ðПри оценке эффективности ремаксола взят неблагоприятный исход — риск (R1) ненаступления биохимической ремиссии (снижение и/или его отсутствие) и отсутствие её нормализации (табл. 2). Далее определен относительный риск (RR), представляющий отношение рисков различных исходов у больных наблюдаемых групп и абсолютное снижение риска (Absolute risk reduction, ARR), определяемое как разность рисков анализируемых исходов у больных наблюдаемых групп. Важно учесть, что при величине относительного риска менее 1 риск наступления исхода в исследуемой группе ниже, чем в группе контроля.
Таблица 2. Риск исходов терапии ремаксолом больных хроническим вирусным гепатитом гепатитом
| Основная группа больных, получавших ремаксол |
Риск отсутствия снижения активности процесса (R1) |
100/294 |
0,3401 |
| Риск отсутствия биохимической ремиссии (R2) |
229/294 |
0,7789 |
| Контрольная группа больных, получавших активное плацебо |
Риск отсутствия снижения активности процесса(R1) |
126/200 |
0,6300 |
| Риск отсутствия биохимической ремиссии(R2) |
176/200 |
0,8800 |
| Относительный риск (RR) |
Отсутствие снижения активности процесса |
0,3401/0,6300 |
0,5398 |
| Отсутствие биохимической ремиссии |
0,7789/0,8800 |
0,8851 |
В обоих анализируемых случаях исходов терапии величина относительного риска меньше 1. Относительный риск составил 0,54 и 0,89 при абсолютном снижении риска от 0,29 до 0,10, что свидетельствует о минимальной возможности наступления неблагоприятного исхода заболевания у больных, получавших лечение ремаксолом, в сравнении с пациентами, получавшими активное плацебо. При анализе финансовых затрат (в рублях) на курсовое лечение с использованием раствора ремаксола и активного плацебо, получены следующие результаты2: стоимость единицы действующего вещества в случае ремаксола составила 5,56, для плацебо — 0,625; стоимость суточной дозы для ремаксола составила 16,68, для плацебо — 2,5; стоимость фармакотерапии для ремаксола составила 200,16, для плацебо — 30,0 рублей.
Таким образом, стоимость курсового применения ремаксола оказалась в 6,7 раза выше стоимости применения активного плацебо. Однако, с учетом достоверного снижения относительного риска (RR=0,5—0,8), высокой эффективности терапии (66,2 против 37,0% в группе контроля), финансовые затраты являются вполне оправданными.
Нежелательные реакции (НР) в ходе исследования выявлены в 5,5% случаев при лечении ремаксолом и в 7,0% при использовании активного плацебо. НР отмечались на 1—2 сутки инфузионной терапии, лишь у 2 больных, получавших ремаксол, и у 3 пациентов, пролеченных активным плацебо — на 4—6-е и 11-е сутки. Их длительность не превышала 5 дней, в среднем составляя 2—3 дня, оценивалась в 1 балл и только у одного пациента в 2 балла. Наиболее часто, в 56,3% (9 человек) случаев, при введении ремаксола отмечалось першение в горле, чувство жара и выраженная гиперемия лица, туловища, конечностей. Эта была реакция на компоненты, входящие в состав раствора (в первую очередь, на никотинамид рибоксин). Они не требовали отмены препарата и купировались антигистаминными средствами. Аллергическая реакция в виде сыпи отмечена у 1 пациента, получавшего ремаксол, и у 2 больных, получавших активное плацебо. Частота аллергических реакций среди всех НР в наблюдаемых группах составила 6,7 и 14,3%. Отмена ремаксола понадобилась у 1 из 294 больных, у которого НР оценивалась в 2 балла и проявлялась головной болью, тошнотой как при первой, так и при повторной попытке введения лекарственного средства.
У больных, получавших активное плацебо, в 73,3% случаев реакции были невротического характера (плацебо-эффект) и не требовали медикаментозного лечения, при 18,7% подобных реакций, отмеченных у больных, получавших ремаксол [52].
Таким образом, частота нежелательных реакций на ремаксол составила 5,5 против 7,0% в группе больных, получавших активное плацебо. Ремаксол хорошо переносился больными, а частота его отмены, в связи с индивидуальной непереносимостью, не превысила 0,3%.
Заключение
Стабильная ремиссия в ответ на противовирусную терапию больных ХГС с добавлением циклоферона установлена у 68,3% больных против 56,3% у пациентов, получавших стандартную терапию, т. е. циклоферон повышал на 12,0% эффективность проводимого лечения. Гистологическое улучшение (снижение активности по шкале Knodell на 2 балла) отмечено у 37,5% человек, получавших стандартную терапию, и у 58,5% (+21%), получавших тройную терапию с циклофероном, т. е. на 3—4 балла у 21,9 и у 29,3% больных (+7,4%) соответственно, при отсутствии прогрессирования фиброза. Комбинированную терапию ХГС с включением циклоферона больные переносили лучше, чем стандартную: побочные эффекты регистрировались в 3,4 раза реже (составив 8,3%, против 28,6%, в пересчёте на 1 больного). Вероятность наступления стабильной ремиссии у пациентов, получавших в качестве дополнительного препарата к стандартной терапии циклоферон, была выше. Показатель риска (RR) составил 0,384, против 0,247 у пациентов, получавших стандартную терапию.
Оценка наступления стабильной ремиссии по показателю RR (благоприятный исход заболевания), рассчитанная у больных, получавших в качестве третьего препарата иммуномодуляторы (циклоферон, галавит, деринат), показала, что наступление благоприятного исхода заболевания (установление стабильной ремиссии) более вероятно у пациентов, получавших раствор циклоферона, в сравнении с галавитом (RR1—2=1,2) и деринатом (RR1—3=1,06), тогда как у больных контрольной группы величина относительного риска была максимальной (RR1—4=1,74).
Понятие «качество жизни» воспринимается пациентом в оценке его физического самочувствия, психического состояния и социальных функций, обеспечивая больному «глобальную» оценку его общего самочувствия. Учёт данной оценки в ходе медикаментозных и психотерапевтических воздействий позволяет оценить качество оказания медицинской помощи пациентам.
Циклоферон у наркопотребителей на фоне вирусного гепатита является препаратом выбора, однако его использование может вызвать серьёзные осложнения в случае употребления опиатов во временном интервале от 12 до 24 ч до или после введения препарата. Оценкой возможных осложнений применения индукторов интерферона (в частности циклоферона) у наркопотребителей на фоне вирусного гепатита служит определение чувствительности пациента к препарату.
Оценка клинико-биохимических показателей больных хроническим гепатитом указывает на эффективность ремаксола как метаболического гепатопротектора при хронических поражениях печени. Препарат снижает активность патологического процесса в печени, обеспечивает выраженный не только гепатопротекторный, но и антиоксидантный и антихолестатический эффекты. Быстрая нормализация ЛДГ (снижение в 14,7 раз) указывает на переключение анаэробных процессов на аэробные, улучшая энергетический баланс гепатоцитов. Показано улучшение синтетической функции печени, повышался коэффициент альбумины/глобулины, снижалась частота гипопротромбинемиии (до 8,1 против 19,4%) и гиперглюкоземии (до 6,8 против 11,9%). Препарат снижает риск неблагоприятных исходов терапии, оправдывая финансовые затраты на лечение. Учитывая ранее проведённые нами исследования, оценивающие эффективность ремаксола у больных с явлениями лекарственной (токсической) гепатотоксичности при длительном курсе антибактериальной полихимиотерапии больных туберкулёзом органов дыхания, ремаксол эффективно уменьшал проявления цитолиза, снижал активность гамма-глутамилтрансферазы, оказывая позитивное влияние на синдром холестаза. Высокая эффективность в сочетании с хорошей переносимостью (побочные эффекты, требующие отмены препарата, встречались только в 0,3% случаев) и минимальным риском отсутствия биохимической ремиссии позволяют расценивать ремаксол как высокоэффективный метаболический гепатопротектор для патогенетической терапии хронических гепатитов.
ЛИТЕРАТУРА
1. Кремень Н. В., Сологуб Т. В., Романцов М. Г. Индивидуальная чувствительность к препаратам интерферона для повышения эффективности терапии больных хроническим гепатитом С. Инфекции в практике клинициста. Антибактериальная и антивирусная терапия на догоспитальном и госпитальном этапах: мат науч конф. Харьков. 2007; 80—83.
2. Малеев В. В., Сологуб Т. В., Наровлянский А. Н. Хронический гепатит С: возможности и перспективы противовирусной терапии. Вест СПбГМА им. И. И. Мечникова 2008; 3: 28: 37—41.
3. Семеняко Н. А. Клинико-морфологическая и иммуносерологическая характеристика малосимптомных форм НСV-инфекции. Ав-тореф дисс. … к. м. н. СПб.: 2009; 22.
4. Mascolini M. HIV, HBV and HCV in Europe: border crossing and buried tombs. IAPA 2005; ll: 12: 386—403.
5. Ершов Ф. И. Пять десятилетий интерферона. Интерферону 50 лет: мат юбил конф. М.: 2007; 11—35.
6. Cornberg M., Deterding K., Manns M. Present and future therapy for hepatitis С virus. Expert Rev Anti Infect Ther 2006; 4: 5: 781—793.
7. Cjeruldsen S., Loge J. H., Myrvang В. Drug addiction in hepatitis С patient leads to a lower quality of life. Nord J Psychiatry 2006; 60: 2: 157—161.
8. Malyszczak K., Inglot M., Pawlowski X. Depressive symptoms during treatment with interferon for HCV infection. Psychiatr Poland 2006; 40: 4: 799—808.
9. Nacamura T. Retinopathy during interferon treatment in combination with ribavirin for chronic hepatitis С. Nippon Ganka Gakkai Zassshi 2005; 109: 748—752.
10. Ozkan M., Corapcioglu A., Bakioglu I. et al. Psychiatric morbidity and its effect on the quality of life in patients with chronic hepatitis С. Int J Psychiatry 2006; 36: 3: 283—297.
11. TalianiG., Ruccin P. Biliotti E. Therapy expectations and physical comorbidity affect on quality of life in chronic hepatitis С virus infection. J Viral Hepatology 2007; 14: 12: 875—879.
12. Bizolon T. Triple antiviral therapy with amantadin for IPN-ribavirin non-responders with recurrent posttransplantation hepatitis С. Transplantation 2005; 15: 325—329.
13. Brok J. Effects of adding ribavirin to interferon to treat chronic hepatitis С infection: a systematic review and meta-analysis of randomized trials. Arch Intern. Med 2005; 165: 2206—2212.
14. Laursen A., Vilstrup H. Treatment of chronic hepatitis C — ribavirin plus interferon. An analysis of a systematic Cochrane review. Ugeskr Laeger 2006; 168: 48: 4209—4212.
15. Balan V., Rosati M., Anderson M., Rakela J. Successful treatment with novel triple drug combination consisting of interferon-gamma, interfer-on alfacon-1, and ribavirin in a nonresponder HCV patient to pegylat-ed interferon therapy. Dig Dis Sci 2006; 51: 5: 956—959.
16. Katayama K., Kasahara A., Sasaki Y. Immunological response to interferon-gamma priming prior to interferon alpha treatment in refractory chronic hepatits С in relation to viral clearance. J Viral Hepat 2001; 8: 3: 180—185.
17. Milazzo L., Biazin M., Gatti N. Thalidomide in the treatment of chronic hepatitis С unresponsive to alpha-interferon and ribavirin. Am J Gastroenterol 2006; 101: 2: 399—402.
18. Musch E., Hogemann В., Gerritzen A. Phase II clinical trial of combined natural interferon-beta plus recombinant interferon-gamma treatment of chronic hepatitis В. Hepatogastroenterology 1998; 45: 24: 2282—2294.
19. Olveria A. Interferon, ribavirin and amantadin in prior nonresponders to interferon and ribavirin therapy with chronic hepatitis С (genotype 1). Gastroenterol Hepatol 2003; 26: 465—468.
20. Wang Т., Seiwert S. Immunomodulatory activities of IFN-gammalb in the treatment of chronic HCV infections. J Interferon Cytokine Res 2006; 26: 7: 473—483.
21. Hoofnagle J., Seeff L. Peginterferon and ribavirin for chronic hepatitis С. New Engl J Med 2006; 355: 23: 2444—2451.
22. Jacobson I. M., Gonzalez S. A., Ahmed F. A randomized trial of pegylat-ed interferon alpha-2b plus ribavirin in the retreatment of chronic hepatitis С. Am J Gastroenterol 2005; 100: 11: 2453—2462.
23. Shiffman M. L. Chronic hepatitis C: treatment of pegylated interfer-on/ribavirin nonresponders. Curr Gastroenterol Rep 2006; 8: 46—52.
24. Balfor L., Cooper С, Kowa J. Depression and cigarette smoking independently relate to reduced health-related quality of life among living hepatitis С. Gastroenterology 2006; 2: 2: 520—528.
25. Dan A. A., Martin I., Crone C. Depression, anemia and health-related quality of life in chronic hepatitic С. J Hepatol 2006; 44: 3: 491—498.
26. Dan A. A., Crone C., Wise T. N. Anger experiences among hepatitis С patient: relationship to depressive symptoms and health-related quality of life. Psychosomatics 2007; 48: 3: 223—229.
27. Danoff A., Khan O., Wan D. W. Sexual dysfunction is highly prevalent among men with chronic hepatitis С virus infection and negatively impacts health-related quality of life. Am J Gastroenterol 2006; 101: 6: 1235—1243.
28. Lang C. A., Caonrad S., Garett L. Symptom prevalence and clustering of symptoms in people living with cronic hepatitis С infection. J Pain Sympthom Manag 2006; 31: 4: 335—344.
29. Киселев О. И., Ершов Ф. И. Интерферон гамма:новый цитокин в клинической практике. М.: 2007; 15—46.
30. Наровлянский А. Н., Кремень Н. В., Романцов М. Г.,Мезенцева М. В. Иммунопатогенетические аспекты назначения иммунотропных препаратов при НСV-инфекции. Вест СПбГМА им. И. И. Мечникова. 2008; 3: 160—164.
31. Наследникова И. О. Иммунорегуляторные цитокины и хрониза-ция вирусного гепатита С: клинико-иммунологические параллели. Клин мед 2005; 9: 40—44.
32. Носик Н. Н. Интерфероны и противовирусный иммунитет. Интерферону 50 лет: мат юбил конф. М.: 2007; 72—81.
33. Романцов М. Г., Сологуб Т. В.,Кремень Н. В. Роль цитокинов в противовирусном иммунитете при хроническом вирусном гепатите С Вест СПбГМА им. И. И. Мечникова 2007; 4: 207—215.
34. Тихомирова И. В., Железникова Г. Ф., Горячева Л. Г. Цитокины Th1 и Th2 при вирусных гепатитах В и С у подростков. Цитокины и воспаление 2002; 2: 132—136.
35. Muller U., Steinhoff U., Reis L. F. et al. Functional role of type I and type II interferons in antiviral defense. Science 1994; 264: 1918—1921.
36. Радченко В. Г., Стельмах В. В., Коваленко А. Л. Терапия хронического вирусного гепатита С сочетанием рекомбинантного интерферона-α2b и индуктора интерферонов — циклоферона. Вест СПбГМА им. И. И. Мечникова 2002; 1—2: 123—128.
37. Романцов М. Г., Коваленко С. Н., Сологуб Т. В., Аникина О. В. Имму-номодуляторы в «золотом стандарте» терапии хронического вирусного гепатита С. Антибиотики и химиотер 2008; 5—6: 18—22.
38. Biron Ch., Gazzinelli R. Effects of IL-12 on immune responses to micro-bial infections: a key mediator in regulating disease outcome. Curr Opin Immunol 1995; 7: 485—496.
39. LarreyD., Couzigou P., Denis J. Chronic hepatitis C: management of side effects treatment. Gastro Clin Biol 2007; 31: 3: 420—428.
40. Manns M., Wedemeyer H., Cornberg M. Treating viral hepatitis C: efficacy, side effects, and complications. Gut 2006; 55: 9: 1350—1359.
41. Presti R. M., Popkin D. L., Connie M. Novel cell type-specific antiviral mechanism of interferon gamma action in macrophages. J Exp Med 2001; 123: 4: 483—496.
42. Samuel C. E. Antiviral actions of interferons. Clinical Microbiology Review 2001; 123: 1: 209—216
43. Milazzo L. Thalidomide in the treatment of chronic hepatitis С unresponsive to alpha-interferon and ribavirin. Am J Gastroenterol 2006; 101: 399—402.
44. Бондаренко А. Н. Этиотропная терапия вирусных гепатитов у лиц, употребляющих наркотик. Вест СПбГМА им. И. И. Мечникова. 2006; 4: 168—174.
45. Бондаренко А. Н. Влияние циклоферона на активность системы протеолиза у больных вирусными гепатитами, употребляющих наркотики. Там же 2005; 2: 37—42.
46. Bernstein D., Kleimann L., Barker C. Relationship of health-related quality of life to treatment adherence and sub-stained response chronic hepatitis С. Hepatology 2002; 35: 3: 704—708.
47. Rowan P. J., Al-Jurdi R., Tavakovli S. Physical and psychosocial contributions to quality of life in veterans with hepatitis С not on antiviral therapy. J Clin Gastroenterol 2005; 39: 8: 731—736.
48. Кремень Н. В., Агаева С. Г., Александрова Л. Н. Качество жизни и психологические особенности больных с хроническим поражением печени. Фармакотерапевтический альманах 2009; 3: 69—76.
49. Зарубина И. В., Шабанов П. Д. Биохимические механизмы гипо-ксического повреждения клетки. Молекулярная фармакология антигипоксантов. Из-во Н-Л. 2007; 17—82.
50. Суханов Д. С., Саватеева Т. Н., Коваленко А. Л. и др. Антиоксидант-ная активность ремаксола на модели лекарственного поражения печени. Вест СПбГМА им. И. И. Мечникова. 2008; 4: 127—132.
51. Кожока Т. Г. Субстраты энергетического обмена. Лекарственные средства в фармакотерапии патологии клетки. М.: 2007; 95—97.
52. Сологуб Т. В., Горячева Л. Г., Суханов Д. С.,Романцов М. Г. Изучение фармакотерапевтической эффективности, безопасности с оценкой риска неблагоприятных исходов, включения ремаксола в терапию хронических поражений печени. Вест СПбГМА им. И. И. Мечникова 2009; 2: 112—116.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru


