Влияние сукцинатсодержащих препаратов на процессы репаративной регенерации печени в эксперименте
Статьи
Опубликовано в журнале:
«ХИРУРГИЯ», 2011, №1, с. 56-60
К.м.н. Д.С. СУХАНОВ1, д.м.н., проф. Т.И. ВИНОГРАДОВА2, д.м.н. Н.В. ЗАБОЛОТНЫХ2, к.м.н. С.Н. ВАСИЛЬЕВА, д.б.н. А.Л. КОВАЛЕНКО, д.м.н., проф. М.Г. РОМАНЦОВ1
1Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова; 2Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии
Ключевые слова: печень, частичная гепатэктомия, репаративная регенерация, реамберин, ремаксол, адеметионин.
The effect of succinate-containing drugs on reparative and regenerative processes of a liver: the experimental results
D.S. SUKHANOV, T.I. VINOGRADOVA, N.V. ZABOLOTNYKH, S.N. VASILYEVA, A.L. KOVALENKO, M.G. ROMANTSOV
Key words: liver, reparative regeneration, reamberin, remaksol.
Введение
Фармакологическая коррекция в хирургической гепатологии имеет большое значение в практике, поскольку печень относится к наиболее метаболически активным органам, потребляющим значительное количество кислорода с общим уровнем энергозатрат 26,4% уровня энергетических потребностей организма в целом [6]. Часто отмечается нарушение функции печени и в послеоперационнм периоде, что проявляется транзиторной гиперферментемией или развитием печеночной недостаточности той или иной степени выраженности вследствие интраоперационной ишемии этого органа, нередких обильных кровопотерь в сочетании с высокой ксенобиотической нагрузкой, вызванной компонентами общей анестезии [1, 5]. Помимо обоснованности объема оперативного вмешательства с минимизацией времени ишемии, значение имеет и рациональное послеоперационное ведение пациентов, что в совокупности обеспечивает низкий уровень послеоперационной летальности (Оперативное вмешательство на печени, как и любой патологический процесс, стимулирует регенерацию этого органа, основными клеточными механизмами которой являются пролиферация, полиплоидизация и гипертрофия гепатоцитов [4, 7]. При этом перечисленные регенераторные процессы в печеночной паренхиме требуют адекватного пластического и энергетического обеспечения.
Изложенное выше обосновывает применение в послеоперационном периоде при резекции печени препаратов метаболического действия, к которым относятся препараты на основе янтарной кислоты. Янтарная кислота — универсальный энергообеспечивающий интермедиат цикла Кребса, при этом мощность системы энергопродуции, использующей сукцинат, в сотни раз превосходит мощность всех других систем энергообразования организма [2, 3]. К широко применяемым инфузионным препаратам на основе сукцината относят реамберин («НТФФ «ПОЛИСАН», Санкт-Петербург) — комплекс метилглюкаминовой соли янтарной кислоты с электролитами. Комбинация сукцината с ключевыми коферментами и метаболитами жизнедеятельности клетки потенцирует возможность действия антигипоксанта на разных уровнях метаболической цепи. Новый инфузионный гепатопротектор ремаксол («НТФФ «ПОЛИСАН») содержит активные метаболические компоненты — янтарную кислоту, рибоксин, никотинамид, метионин, а также электролиты — натрия хлорид, магния хлорид, калия хлорид и сольстабилизирующий агент N-метилглюкамин и является сбалансированным полиионным раствором.
Цель исследования — изучение действия реамберина, ремаксола и адеметионина на процессы репаративной регенерации печени крыс, подвергнутых частичной гепатэктомии.
Материал и методы
Эксперимент проведен на базе лаборатории патоморфологии и экспериментального туберкулеза Санкт-Петербургского научно-исследовательского института фтизиопульмонологии на 100 белых беспородных крысах-самцах с исходной массой 180— 200 г. Поставщик — питомник «Рапполово» РАМН (Санкт-Петербург).
Основные критерии включения животных в исследование: масса тела — не менее 180—200 г.; шерстяной покров — гладкий, блестящий; поведение и общее состояние — активная динамика движения и потребления кормов. Перед началом исследования крыс, отвечающих критериям включения, разделяли на группы с помощью метода рандомизации.
Методика моделирования частичной гепатэктомии
Частичную экстирпацию печени у крыс выполняли по методике А. Фишера [9]. Для обезболивания использовали комбинированный препарат золетил (S. Virbac, Франция), содержащий тилетамин — общий анестетик диссоциативного действия, дающий анальгетический эффект, и золазепам – транквилизатор бензодиазепинового ряда, оказывающий анксиолитическое и седативное действие и вызывающий мышечную релаксацию. Препарат разрешен для применения в ветеринарной практике на территории Российской Федерации. Золетил вводили внутримышечно в дозе 15 мг/кг. Крыс фиксировали в специальных станках в положении на спине, каудально от мечевидного отростка проводили медиальную лапаротомию длиной 2—3 см. Вынимали одним пальцем левую и медиальную доли печени, составляющие 68% вещества печени, и поворачивали вверх. Сосудистый ствол между двумя долями перевязывали, удаляли левую и медиальную доли печени, послойно сшивали брюшину и кожу.
В эксперименте сформировано 5 групп наблюдения:
1-я — интактные крысы — неоперированные и нелеченые (n=6); 2-я — контрольные крысы — оперированные, нелеченые (n=24); 3-я — крысы оперированные (n=24), получавшие реамберин в дозе 25 мл/кг внутрибрюшинно; 4-я — крысы оперированные (n=24), получавшие ремаксол в дозе 25 мл/кг внутрибрюшинно; 5-я — крысы оперированные (n=22), получавшие адеметионин в дозе 0,09 мл на 100 г массы тела внутрибрюшинно.
Введение реамберина, ремаксола и адеметионина начали в день операции. Контрольным животным вводили физиологический раствор в эквиобъемных количествах. Все исследуемые препараты применяли 1 раз в сутки, ежедневно, на протяжении 14 дней.
Крыс контрольной и опытных групп (n=6) выводили из опыта путем декапитации на 4, 10, 14 и 25-е сутки после операции. Извлекали печень, определяли массу органа, затем фиксировали в нейтральном формалине, осуществляли стандартную проводку, заливали в целлоидин — парафин — масло, срезы (4—6 мкм) окрашивали гематоксилином и эозином.
О скорости репаративных процессов судили по:
- нарастанию абсолютной массы печени;
- данным морфометрического исследования срезов печени, окрашенных гематоксилином и эозином, при сопоставлении с показателями у интактных животных (n=6). В ходе морфологических исследований подсчитывали количество двуядерных гепатоцитов, незрелых гепатоцитов, а также гепатоцитов, содержащих более одного ядрышка в ядре. В каждом микропрепарате печени учитывали не менее 4000 гепатоцитов с помощью стандартной окулярной сетки.
При статистической оценке полученных результатов использовали параметрический тест Стьюдента—Фишера [8].
Результаты и обсуждение
В эксперименте на крысах, которым выполнена частичная экстирпация печени, определяли ее динамику массы регенерирующего органа на разных сроках наблюдения.
У контрольных оперированных крыс масса регенерирующей печени достигла ее уровня у интактных животных к 25-м суткам после операции. Исследуемые препараты различались по степени влияния на темпы восстановления массы печени. Так, у крыс, получавших реамберин, накопление массы оставшейся части органа происходило менее интенсивно по сравнению с контрольными (оперированные, нелеченые) животными. К окончанию эксперимента (25-й день после операции) в этой группе масса печени составляла 88,89% по отношению к показателю у интактных крыс. Под влиянием ремаксола и адеметионина абсолютная масса печени после гепатэктомии возрастала более интенсивно. Через 14 сут средняя величина массы печени крыс, получавших ремаксол и адеметионин в послеоперационном периоде, была уже практически сопоставима с абсолютной массой печени интактных животных (9,17±0,3 и 9,34±0,7 г и 9,9±0,7 г соответственно). У контрольных (оперированные, нелеченые) крыс, а также у животных, получавших реамберин, масса печени к этому сроку регистрации составляла лишь 7,92±0,53 и 7,51±0,23 г, что достоверно ниже по отношению к показателю (в интактной группе — 9,9±0,7 г, рГистологическое исследование ткани печени контрольных оперированных нелеченых животных на 4-е сутки после частичной резекции показало нарушение архитектоники долек на фоне выраженного полнокровия в системе воротной вены (рис. 1). Балочная структура долек была нарушена, в некоторых дольках обнаружена фрагментация балок. Ядра гепатоцитов в этих фрагментах пикнотичны, некоторые из них окружены светлым ореолом, что можно расценивать как показатели некробиоза гепатоцитов. Зарегистрированы признаки «шоковой печени», т.е. стазы в капиллярах, отчетливая диффузная инфильтрация долек лейкоцитами, расширение синусоидов пространств Диссе и белковая дистрофия гепатоцитов. Встречались также участки распадающихся безъядерных гепатоцитов, местами замещенных мелкофокусными лимфогистиоцитарными инфильтратами.
Рис. 1. Печень контрольной оперированной нелеченой крысы через 4 сут после частичной экстирпации.
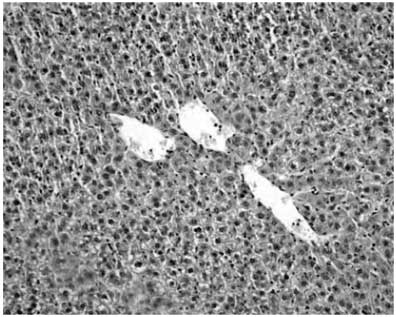
Балочная структура печени нарушена. Видны признаки «шоковой печени». Окраска гематоксилином и эозином. Ув. 300.
При лечении крыс исследуемыми препаратами отмечена несколько большая сохранность архитектоники органа и меньшая выраженность признаков «шоковой печени» у животных, получавших ремаксол (4-я группа) и адеметионин (5-я группа). Это проявилось сохранением балочной структуры долек и меньшей распространенностью белковой дистрофии в 2 из 6 случаев в каждой обсуждаемой группе. В качестве начального признака репарации органа в этих группах можно отметить выраженную портальную лимфогистиоцитарную инфильтрацию: в 4-й группе — в 3 из 6, в 5-й группе — в 2 из 6 случаев (рис. 2).
Рис. 2. Регенерирующая печень крысы, леченной ремаксолом.
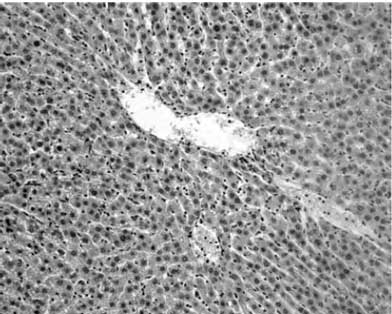
Архитектоника частично восстановлена. Прослеживается балочное строение органа. Признаки «шоковой печени» выражены меньше. Окраска гематоксилином и эозином. Ув. 300.
На 10-е сутки после резекции печени в контрольной группе в 2 из 6 случаев начало определяться восстановление архитектоники (печеночные балки прослеживались на большей площади срезов). При этом во всех случаях сохранялось полнокровие органа, часто регистрировалась фрагментация балок и группы балок с пикнотичными ядрами. В 5 из 6 случаев отмечены фокусы некротизированных гепатоцитов. В то же время наряду с наличием показателей «шоковой печени» в ее ткани появились признаки активации процессов регенерации. В 4 (66,7%) из 6 случаев вокруг некоторых, в основном крупных сосудов образовались участки компенсаторной гипертрофии печени (по Д.С. Саркисову) размером с небольшую дольку. Балки в этих участках были гипертрофированы, пространств Диссе не прослеживалось, цитоплазма гепатоцитов уплотнена. Кроме того, в междольковом пространстве у этих же крыс появились неширокие балки, состоящие из гепатоцитов с более интенсивной окраской цитоплазмы и ядер. При этом строение ядер прослеживалось, но было менее отчетливым, чем в основной массе гепатоцитов. Присутствие таких гепатоцитов расценивается как показатель внутриклеточной регенерации (по Д.С. Саркисову).
Как и на первом сроке наблюдения, у крыс, получавших ремаксол и адеметионин, отмечалась лучшая сохранность архитектоники долек (в 3 из 6 случаев в обеих группах), меньшая выраженность полнокровия печени и инфильтрации ткани лейкоцитами. Число фокусов некротизированных гепатоцитов в этих группах также уменьшилось: у крыс, получавших ремаксол, — только в 1 случае, при лечении адеметионином — в 3 из 6 случаев. Показатели стимуляции регенерации у животных всех опытных групп проявлялись отчетливее, чем в контроле операции. Участки компенсаторной гипертрофии увеличились до размеров 1—2 долек и уже не были связаны только с сосудами. Исключение составили лишь 2 из 6 случаев в 3-й группе (лечение реамберином), где эти участки были небольшими и находились периваскулярно. Участки с гепатоцитами, несущими признаки внутриклеточной регенерации, во всех 3 группах были более выражены и отмечены во всех случаях. Следует обратить особое внимание на то, что на этом сроке наблюдения только у крыс, получавших экзогенный адеметионин, альтеративные изменения печеночной ткани были наиболее выражены. У них чаще, чем в других опытных группах, отмечались очаговые скопления некротизированных гепатоцитов и, что самое важное, только в этой группе в 2 из 6 случаев обнаружены крупные участки некроза (рис. 3).
Рис. 3. Печень крысы, леченной адеметионином, через 10 сут после частичной гепатэктомии (соответствует 10-дневному курсу адеметионина).
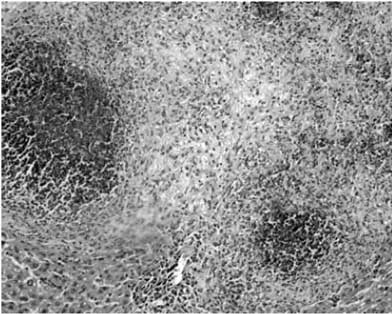
Крупные сливные очаги некроза. Окраска гематоксилином и эозином. Ув. 300.
Через 14 сут после частичной экстирпации в контрольной группе архитектоника печени частично восстановилась у 50% крыс. Из признаков «шоковой печени» местами определялись только слабо выраженные стаз капилляров и белковая дистрофия. Как и ранее, сохранялись полиморфизм гепатоцитов и в части долек — фрагментация долек с пикнозом ядер. Фокусы компенсаторной гипертрофии стали крупнее, располагались по всей поверхности среза печени, участки гепатоцитов с интенсивной окраской цитоплазмы и ядер встречались во всех случаях. В 3 из 6 случаев зарегистрирована резко выраженная портальная лимфогистиоцитарная инфильтрация.
У крыс, получавших исследуемые препараты, на 14-е сутки после операции принципиальных отличий от контрольной группы не наблюдалось. По показателям регенераторных процессов можно отметить только более частое наличие крупных лимфогистиоцитарных инфильтратов: при лечении ремаксолом — в 4 из 6, адеметионином — в 5 из 6 случаев. Кроме того, в 4-й группе (лечение ремаксолом) отмечена лучшая сохранность балочной структуры печени (нарушение ее в 1 из 6 случаев) и реже встречалась фрагментация балок (в 2 из 6 случаев против 4 из 6 в контроле). В 5-й группе (у крыс, получавших адеметионин), как и на предыдущем сроке наблюдения, продолжали обнаруживать признаки альтерации печени: мелкофокусная лимфогистиоцитарная инфильтрация долек и фокусы некротизированных гепатоцитов.
К последнему сроку наблюдения (на 25-е сутки после операции) балочная композиция ткани печени восстановилась у 100% контрольных оперированных нелеченых крыс. При этом в некоторых дольках (в 4 из 6 случаев) сохранялись показатели некробиоза — фрагменты балок с кариопикнозом гепатоцитов, а в одном микропрепарате — фокусы некротизированных гепатоцитов. У всех животных, получавших исследуемые препараты, на 25-е сутки после частичной гепатэктомии архитектоника печени также была восстановлена. В отличие от контроля операции у них не наблюдалось фрагментации балок как признака некробиоза. Как и на предыдущих сроках наблюдения, у крыс, получавших адеметионин, гораздо чаще, чем в других группах, отмечались признаки альтерации. В 3 из 5 случаев обнаружены мелкофокусная лимфогистиоцитарная инфильтрация долек и фокусы некротизированных гепатоцитов, а в 1 из 5 случаев — даже крупные очаги некроза.
При анализе морфометрической характеристики ткани печени установлено, что ее восстановление у контрольных (оперированных нелеченых) животных регистрируется уже на самом раннем сроке (4-е сутки), причем степень выраженности внутриклеточных регенераторных реакций меняется в течение всего периода наблюдения. Так, на первом сроке наблюдения отмечено достоверное увеличение числа незрелых гепатоцитов (в 1,78 раза, рОценивая влияние исследуемых препаратов, можно отметить, что динамика показателей внутриклеточных регенераторных процессов у крыс, получавших реамберин, существенно не отличалась от таковой в контрольной группе. Лишь на втором сроке (10 дней) наблюдения он привел к некоторому увеличению количества двуядерных гепатоцитов (по сравнению с контролем), но достоверными эти отличия не были.
В условиях применения ремаксола отмечены отчетливые различия в качестве течения компенсаторного процесса, о чем свидетельствовало достоверное увеличение процента клеток, указывающих на стимуляцию активности внутриклеточных регенераторных реакций уже через 4 дня после операции. На этом сроке наблюдения эффект ремаксола был максимальным: содержание двуядерных гепатоцитов по сравнению с нелеченым контролем увеличилось в 2,1 раза (рДействие экзогенного адеметионина на гепатоциты, участвующие в репарации, отмечено также уже на 4-й день после операции, но его выраженность была несколько меньше, чем у ремаксола, поскольку достоверно увеличились только два из трех показателей. Максимальный эффект препарата регистрировался через 10 дней после частичной экстирпации печени. Так, процент двуядерных гепатоцитов по сравнению с нелеченым контролем под действием адеметионина увеличился в 1,9 раза (рТаким образом, у крыс, леченных ремаксолом и адеметионином, быстрее восстанавливалась балочная структура органа и раньше появлялись признаки репаративной регенерации. Уже на 4-й день после частичной гепатэктомии практически у 50% крыс в обеих группах выявлена портальная лимфогистиоцитарная инфильтрация. На 10-й день отмечалась большая частота выявления (в 100% случаев в обеих группах против 66,7% в контроле операции) и гораздо большая распространенность (по размерам и независимости от портальной системы) участков компенсаторной гипертрофии печени. Параллельно зарегистрированной способности стимулировать процессы репаративной регенерации у крыс, леченных адеметионином, начиная с 10-го дня после резекции печени, что соответствовало 10-дневному курсу введения препарата, обнаружено отчетливое усиление альтеративных процессов в печени. Чаще, чем у других леченых животных, выявлялись фокусы некротизированных гепатоцитов, в единственной из всех опытных групп — крупные очаги некроза. Та же тенденция имела место и на последующем сроке наблюдения, и даже через 10 дней после отмены адеметионина (на 25-е сутки после операции), когда выявлены фокусы некротизированных гепатоцитов и крупные очаги некроза. У крыс, леченных ремаксолом, активации процессов альтерации не отмечено.
Морфометрический анализ показал, что ремаксол и адеметионин значимо повышают относительное содержание гепатоцитов, участвующих в репаративной регенерации печени, на 4-й и 10-й дни после частичной экстирпации органа. Уровень стимуляции гепатоцитов обоими препаратами практически не различается. Необходимо подчеркнуть, что в условиях применения ремаксола максимальная выраженность регенераторных реакций достигается раньше — на 4-й день после операции, при использовании адеметионина — на 10-й день. Стимуляция же внутриклеточных регенераторных реакций на 25-й день после частичной гепатэктомии у животных, получавших адеметионин, обусловлена репаративными процессами, индуцированными, вероятнее всего, альтеративным эффектом экзогенного адеметионина.
ЛИТЕРАТУРА
1. Вишневский В.А., Кубышкин В.А., Чжао А.В. и др. Операции на печени. М 2003.
2. Зарубина И.В., Шабанов П.Д. Молекулярная фармакология антигипоксантов. Н—Л 2004.
3. Коваленко А.Л. Фармакологическая активность оригинальных лекарственных препаратов на основе 1-дезокси-1(N-метиламино)-D-глюцитола: Автореф. дис. ... д-ра биол. наук. Ст-Петербург 2005.
4. Кудрявцев Б.Н., Кудрявцева М.В., Сакута Г.А. и др. Цитология 1993;35:70—83.
5. Мазина Н.К., Сухоруков В.П., Гоголев Н.В. и др. Вятский мед вестн 2010;1:34—42.
6. Оковитый С.В., Безбородкина Н.Н., Улейчик С.Г. и др. Гепатопротекторы. М 2010.
7. Сакута Г.А., Кудрявцев Б.Н. Цитология 1996;38:1158—1171.
8. Урбах В.Ю. Статистический анализ в биологических медицинских исследованиях. М 1975.
9. Фишер А. Физиология и экспериментальная патология печени. Пер. с нем. Будапешт 1961.
10. Eun-Sook Lee, Hontago Chen, Hardman Ch. et al. Life Sci 2008;19:83:25—26.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru



