Применение ремаксола в терапии метаболического синдрома у пациентов с неалкогольным стеатогепатитом и сахарным диабетом 2 типа
Статьи
Опубликовано в журнале:
« Экспериментальная и клиническая гастроэнтерология » выпуск 130, № 6, 2016
Дударенко С.В.1,Коваленко А.Л.2, Прокопенко С.М.3, Белогурова Е.В.1
1ФГБУ «Всероссийский центр экстренной и радиационной медицины им. А. М. Никифорова»
2 Институт токсикологии Федерального медико-биологического агентства
3Военно-медицинская академия имени С. М. Кирова
Резюме
Целью исследования стала оценка эффективности включения ремаксола в схемы терапии метаболического синдрома у пациентов с неалкогольным стеатогепатитом и сахарным диабетом 2 типа.
Материалы и методы: проведен анализ лечения 76 пациентов с метаболическим синдромом в виде неалкогольного стеатогепатита и сахарного диабета 2 типа. Пациенты были рандомизированы по полу и возрасту и разделены на 2 группы в зависимости от схемы проводимой терапии: больным I группы (основной - 38 человек) проведена базовая терапия в сочетании с ремаксолом: внутривенно капельно по 400 мл 1 раз в день в течение 10 дней, у пациентов II группы (сравнения - 38 человек) базовая терапия сочеталась с внутривенным введением адеметионина: 400 мг, разведенного в растворе NaCL 0,9% 400 мл 1 раз в день в течение 10 дней. Помимо стандартного клинико-лабораторного обследования было проведено исследование биохимических показателей печеночной активности, жирового и углеводного обмена, перекисного окисления липидов и антиоксидантной системы в динамике: перед началом терапии и после ее окончания.
Результаты: установлено, что включение в схемы терапии препаратов из группы сукцинатов (ремаксол) уменьшает выраженность метаболического синдрома за счет снижения проявлений холестаза и цитолиза и способствует улучшению липидного и углеводного обменов, активации антиоксидантной системы. В результате существенно снижается выраженность основных клинических синдромов: астеновегетативного и диспепсического - на 46% и 15% соответственно.
Ключевые слова: неалкогольная жировая болезнь печени, ремаксол, сахарный диабет 2 типа, метаболический синдром.
The use of remaxol in the treatment of metabolic syndrome in patients with nonalcoholic steatohepatitis and diabetes mellitus 2 type
Dudorenko S.V.1, Kovalenko A.L.2, Prokopenko S.M.3, Belogurova E.V.1
1 The Federal State Budaetary Institute «The Nikiforov Russian Center of Emergency and Radiation Medicine» The Ministry of Russian Federation for Civil Defense. Emergencies and Elimination of Consequences of Natural Disasters.
2 Federal Medical and Biological Agency. Institute of Toxicology.
3 The Kirov Military-medical Academy, Ministry of Defence of the Russian Federation
Summary
The aim of the study was to assess the effectiveness of the inclusion in the scheme remaxol treatment of metabolic syndrome in patients with nonalcoholic steatohepatitis and diabetes mellitus 2 type.
Materials and methods: Data of 76 patients with metabolic syndrome in a non-alcoholic steatohepatitis and type 2 diabetes were analyzed. Patients were randomized by gender and age, and are divided into 2 groups according to the scheme of therapy: patients in group I (major - 38) conducted a basic therapy in combination with remaxol: intravenous infusion of 400 ml of 1 times a day for 10 days, group II patients (comparison - 38) combined basic therapy with intravenous ademetionine: 400 mg. in a solution diluted NaCL 0,9% 400 ml 1 time per day for 10 days. In addition to standard clinical and laboratory tests were studied biochemical parameters of liver activity, lipid and carbohydrate metabolism in the dynamics: before therapy and after its completion.
Results: it was found that the inclusion in the scheme of drugs from the group of succinates (remaxol) reduces the severity of metabolic syndrome by reducing the manifestations of cholestasis and cytolysis, and improving lipid and glucose metabolism. As a result, significantly reduced the severity of the main clinical syndromes: asthenovegetative 46% and dyspeptic syndromes - 46% and 15%, respectively.
Keywords: nоn-alcoholic fatty liver disease, remaxol, diabetes mellitus 2 type, metabolic syndrome.
Введение Хронические психоэмоциональные перегрузки, напряжённая экологическая ситуация, связанная с загрязнением воды, почвы, воздуха стали «нормой» существования и обусловили изменение структуры и характера заболеваемости в большинстве развитых стран. На одно из первых мест в структуре заболеваемости оказались выдвинутыми болезни обмена веществ, такие как синдром хронического адаптивного перенапряжения (СХАП), а на его основе - метаболический синдром (МС). Несмотря на то, что МС не является самостоятельной нозологической формой, его роль в патогенезе атеросклеротического поражения сосудов с последующим развитием ишемической болезни сердца (ИБС), артериальной гипертензии и инфаркта миокарда, сахарного диабета 2 типа и других расстройств не вызывает сомнений [1,2]. В основе большинства физиологических и патофизиологических процессов в организме лежат процессы образования энергии и сопряженные с ними свободно-радикальное и перекисное окисление липидов. Нарушение равновесия между активностью окислительных и антиокислительных процессов, активация перекисного окисления липидов ведет к развитию так называемого окислительного стресса. Именно с последним в настоящее время связаны процессы эндотоксикоза и иммуносупрессии, нарушения клеточной дифференцировки и повреждения мембран клеток, атеросклероз и апоптоз, а также развитие поражений печени [2, 3, 4].
Понятие неалкогольной жировой болезни печени (НАЖБП) включает в себя ряд заболеваний: жировую дистрофию печени (стеатоз), жировую дистрофию печени с воспалением и повреждением гепатоцитов - неалкогольный стеатогепатит (НАСГ) и неалкогольный стеатогепатит с фиброзом (с возможностью прогрессии и переходом в цирроз) [5,6]. Распространенность неалкогольной жировой болезни печени в Западной Европе составляет 20-30%, в странах Азии - 15% [7]. В России из более 2 миллионов больных сахарным диабетом 2 типа и у 2/3 имеется неалкогольная жировая болезнь печени. Повышение индекса массы тела (ИМТ) более 30 кг/м2 в 95-100% случаев сопровождается развитием стеатоза печени и в 20-47% - неалкогольным стеатогепатитом. Сахарный диабет 2 типа или нарушение толерантности к глюкозе у 60% пациентов сочетаются со стеатозом печени, у 15% - с неалкогольным стеатогепатитом. Нарушение липидного обмена в виде дислипидемии в значительной части случаев (20-80%) сопровождается стеатозом печени [8, 9].
Проблема нарушений нескольких видов обмена при метаболическом синдроме у пациентов с НАСГ, превалирование проявлений оксидативного стресса как типового патологического процесса при поражении ключевого органа, участвующего во всех видах обменных процессов (печень) диктуют необходимость назначения патогенетических лекарственных средств из группы метаболических корректоров с гепатопротективной и антиоксидантной направленностью. В настоящее время строгих схем лечения пациентов с неалкогольным стеатогепатитом у больных сахарным диабетом не существует. Поиск новых препаратов, нормализующих обмен липидов и обладающих прямым цитопротекторным действием, является актуальной проблемой не только гепатологии, но и других разделов внутренних болезней [9,10].
Одним из перспективных препаратов в этой области является Ремаксол (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург) - сбалансированный инфузионный раствор, обладающий гепатопротекторным действием. Под действием Ремаксола ускоряется переход анаэробных процессов в аэробные, улучшается энергетическое обеспечение гепатоцитов, увеличивается синтез макроэргов, повышается устойчивость мембран клеток печени к повреждению продуктами перекисного окисления липидов, восстанавливается активность ферментов антиоксидантной защиты. Препарат уменьшает проявления цитолиза, что проявляется в снижении индикаторных ферментов и билирубина, улучшает экскрецию прямого билирубина в желчь. Ремаксол способствует уменьшению проявлений холестаза, о чем свидетельствуют снижение активности экскреторных ферментов гепатоцитов (щелочной фосфатазы и гаммаглюта-милтранспептидазы). К настоящему моменту проведены различные исследования эффективности и безопасности Ремаксола. На экспериментальной модели токсикоза, индуцированного введением токсической дозы цисдиамминдихлорплантина (цисплатин), доказано выраженное детоксицирующее действие препарата, что проявляется снижением летальности лабораторных животных [11]. На модели экспериментального повреждения печени противотуберкулёзными препаратами доказано влияние Ремаксола на восстановление структурных нарушений печени, гистоархитектоники, сокращение распространённости углеводной, белковой и жировой дистрофии, активацию процессов внутриклеточной регенерации [12]. Кроме того, на основании проведенных клинических исследований подтверждено успешное использование препарата при токсических, алкогольных поражениях печени и у больных с хроническим гепатитом В и С [13].
В связи с вышеперечисленным, перспективным является исследование эффективности применения препарата Ремакосол для коррекции метаболических нарушений у пациентов с НАСГ и сахарным диабетом 2 типа.
Цель исследования: оценить эффективность включения ремаксола в схемы терапии метаболического синдрома у пациентов с неалкогольным стеатогепатитом и сахарным диабетом 2 типа.
Методы и материалы
Путем сравнения результатов терапии 76 пациентов (73 мужчины и 3 женщины) с установленным диагнозом «неалкогольный стеатогепатит», сахарный диабет 2 типа, находившихся на лечении в отделении терапии и интегративной медицины ВЦЭРМ им. А. М. Никифорова МЧС РФ, проведен анализ эффективности Ремаксола в терапии указанных расстройств. У 51 (67,1%) пациента была диагностирована сопутствующая патология в виде артериальной гипертензии 1-2 ст., ишемической болезни сердца; у 48 (63%) больных - стенокардия 1-2 функционального класса; у 61 (80,2%) больных - хронический гастрит и хронический паренхиматозный панкреатит - у 59 (77,6%) пациентов.
Пациенты были рандомизированы по полу и возрасту и разделены на 2 группы в зависимости от схемы проводимой терапии. Больным I группы (основной - 38 человек) проведена базовая терапия основного заболевания в сочетании с ремаксолом (внутривенно капельно по 400 мл 1 раз в день в течение 10 дней), у пациентов II группы (сравнения - 38 человек) базовая терапия сочеталась с внутривенным введением адеметионина (400 мг внутривенно 1 раз в день в течение 10 дней).
Критериями включения в исследование помимо установления диагноза НАСГ и СД 2 типы были следующие лабораторные данные: изменение липидного спектра крови (снижение Л ПВП <1,0 у мужчин и <1,2 у женщин, увеличение ЛПНП >3,0, повышение уровня триглицеридов и/или холестерина в 1,5-5 раз выше верхней границы нормы), повышение активности АЛТ, ACT в сыворотке крови в 1,5-5 выше верхней границы нормы. Критериями исключения являлись недавние случаи (менее трех месяцев назад) острого инфаркта миокарда, аортокоронарного шунтирования, травмы головного и спинного мозга, соматические заболевания в стадии декомпенсации (сердечная, легочная, почечная, печеночная недостаточность), артериальная гипертензия 3 ст., наличие эндокринных заболеваний (кроме СД 2 типа), требующие заместительной или корригирующей терапии.
Помимо общепринятых клинико-лабораторных исследований пациентам проведено определение биохимических показателей: аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), общего билирубина и его фракций, гаммаглутамилтранспептидазы (ГГТП), лактатдегидрогеназы (ЛДГ), щелочной фосфатазы (ЩФ), липопротеины высокой, низкой и очень низкой плотности (ЛПВП, ЛПНП, ЛПОНП), триглицериды, общий холестерин, индекс атерогенности, показатели углеводного обмена: сахарная кривая (дневные колебания сахара крови) и лактат крови, показатели антиоксидантной системы (по содержанию в крови супероксиддисмутазы (СОД) и общего антиоксиданта). Исследование проведено в динамике: до начала исследования, 5-й день терапии и после окончания инфузионной терапии (через 10 дней после начала терапии).
Для обработки полученных данных были использованы пакеты программ Office Std. 2010 (Excel 2010) и Statistica 7.0. Перед началом анализа эмпирические распределения переменных были испытаны на согласие с законом нормального распределения по критерию Шапиро-Уилка (используется для выборок с 5<N<50).
Результаты
До начала лечения наиболее частыми (помимо основных проявлений заболевания) у обследованных были жалобы астеновегетативного характера (слабость, быстрая утомляемость): у 37 (97,3%) больных I группы и у 36 (94,7%) - II группы.
Признаки диспепсического синдрома (тошнота изжога, отрыжка) отмечены у 20 (52,6%) и 26 (68,4%) больных соответственно. После проведенного лечения отмечено уменьшение выраженности астеновегетативных проявлений на 46% (с 37 до 20 человек), получивших в схеме лечения ремаксол, и на 28% (с 36 до 26 человек) - получивших лечение адеметионином, в то же время, диспепсический синдром купировался у 3 (15%) пациентов из I группы и только у 1 (3,8%) больного из II группы.
Анализ данных функционального состояния печени до начала лечения выявил у подавляющего большинства пациентов повышение АЛТ и ACT на фоне умеренного повышения уровней билирубина, преимущественно за счет непрямой фракции, и активности процессов холестаза, о чем свидетельствовало повышение уровней ГГТП, ЛДГ и ЩФ (табл. 1).
Таблица 1. Динамика биохимических показателей в зависимости от инфузионной терапии (М±m)
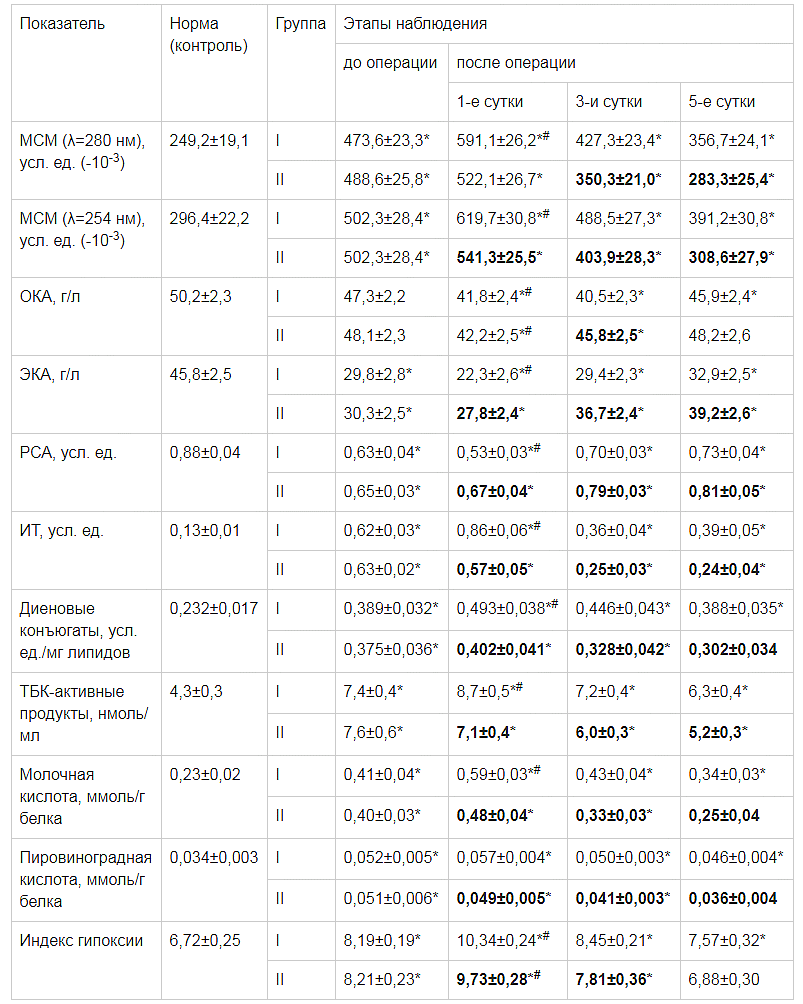 Примечание
Примечание: * - р<0,03, при сравнении с уровнем до начала лечения
Таблица 2. Динамика показателей липидного обмена в зависимости от схемы терапии (М±m)
| показатель
|
I группа
(n=38)
|
II группа
(n=38)
|
| до лечения
|
после лечения
|
до лечения
|
после лечения
|
| Общий холестерин, ммоль/л |
6,60±0,92 |
4,94±0,23* |
6,12±0,71 |
4,72±0,30 |
| ЛПНП, ммоль/л |
4,32±1,08 |
3,05±0,21 |
3,98±0,86 |
3,08±0,24 |
| ЛПОНП, ммоль/л |
1,16±0,77 |
0,74±0,08 |
1,11±0,39 |
0,72±0,07 |
| ЛПВП, ммоль/л |
1,14±0,36 |
0,85±0,05 |
1,21±0,75 |
0,92±0,05 |
| Триглицериды, ммоль/л |
2,57±1,59 |
1,42±0,17* |
2,53±0,88 |
1,56±0,16 |
| Индекс атерогенности |
5,07±1,04 |
3,74±0,31 |
4,85±1,38 |
4,15±0,20 |
Примечания: * - р<0,05 при сравнении с данными до начала терапии
После проведенного лечения нами было отмечено улучшение показателей печеночной активности, более выраженное у пациентов, получивших в схеме лечения ремаксол: снижение уровней АЛТ на 54,7% (с 82,26±19,66 до 37,22±6,57 ед/л), ACT на 39% (с 66,18±14,75 до 40,33±9,44 ед/л) и общего билирубина на 37,7% (с 18,30±5,22 до 11,40±1,16 мкмоль/л). В тоже время у пациентов II группы динамика данных показателей отмечена на 31%, 45,6% и 13,3% соответственно (р<0,03). Одновременно нами отмечено уменьшение холестатических проявлений, более выраженное у пациентов I группы: снижение уровней ГГТП на 45% (с 57,44±14,55 до 31,56±37,39 ед/л), ЩФ на 21,3% (с 80,51±36,65 до 63,33±8,35 ед/л) и ЛДГ на 22% (с 174,54±53,29 до 136,11±6,75 ед/л), в то время как у пациентов II группы снижение указанных показателей выявлено на 40%, 1,1% и 18,6% соответственно (р<0,05).
Признаки нарушения липидного обмена отмечены нами у всех пациентов двух групп (табл. 2). Последние заключались в дислипидемии при росте значений коэффициента атерогенности.
После проведенной терапии зарегистрировано улучшение показателей, более выраженное у пациентов 1 группы: снижение уровня общего холестерина на 25,1% (с 6,60±0,92 до 4,94±0,23 ммоль/л), и триглицеридов на 44,7% (с 2,57±1,59 до 1,42±0,17 ммоль/л), против 23,2% и 38,3% соответственно в группе сравнения (р<0,05), (табл. 2). При изучении динамики уровней фракций липопротеинов отмечена положительная реакция со стороны показателей у всех пациентов, несколько более выраженная у пациентов, получивших ремаксол: снижение ЛПНП на 29,8% (с 4,32±1,08 до 3,05±0,21 ммоль/л), ЛПОНП на 36,2% (с 1,16±0,77 до 0,74±0,08 ммоль/л) и ЛПВП на 25,4% (с 1,14±0,36 до 0,85±0,05 ммоль/л), в то время как в группе сравнения эти изменения составили 22,6%, 34,5% и 24% соответственно (р<0,05).
Исследование углеводного обмена до начала терапии выявило значительное повышение уровня глюкозы натощак и толерантность показателя в течении суток, а также значительно повышение лактата в крови у всех пациентов (табл. 3). После проведенной терапии у пациентов I группы уровень глюкозы снизился на 15,6% (с 7,41±0,21 до 6,25±0,06 ммоль/л), а лактата - на 18,5% (с 3,46±0,17 до 2,82±0,51 ммоль/л), в то время как в группе сравнения эти показатели составили 10% и 6,3% соответственно (р<0,01).
Исследование влияния инфузионной терапии в I и II группах на состояние антиоксидантной системы выявило следующее:
Как следует из данных табл. 4, применение ремаксола не приводит значительным изменениям уровня ферментного звена АОС (СОД), но при этом достоверно возрастает уровень общего антиоксиданта крови, определяющим совокупность всех звеньев АОС.
Результаты оценки аналогичных показателей крови в группе больных, получавших адеметионин, представлены в табл. 5.
Таблица 3. Динамика показателей углеводного обмена в зависимости от схемы терапии (М±m)
| показатель
|
I группа
(n=38)
|
II группа
(n=38)
|
| до лечения
|
после лечения
|
до лечения
|
после лечения
|
| Глюкоза натощак ммоль\л |
7,41±0,21 |
6,25±0,06* |
7,27±1,29 |
6,54±1,12* |
| Дневные колебания глюкозы (ммоль/л)
|
| через 2 часа после завтрака |
7,93±2,11 |
6,06±0,12 |
7,78±0,81 |
6,33±0,12 |
| через 2 часа после обеда |
6,60±0,15 |
5,86±0,82 |
6,33±0,12 |
6,01±1,16 |
| через 2 часа после ужина |
7,24±0,71 |
6,06±0,24 |
7,03±1,21 |
6,27±0,12 |
| Лактат, ммоль/л |
3,46±0,17 |
2,82±0,51* |
3,18±0,15 |
2,98±0,21* |
Примечания: * - р<0,01 при сравнении с данными до начала терапии
Таблица 4. Содержание показателей антиоксидантной защиты в крови больных 1 группы.
| Показатели
|
М
|
m
|
М
|
m
|
Р
|
| 0 день
|
10 день
|
| СОД ед. акт. /мг гемоглобина |
219,68 |
±49,67 |
216,07 |
±49,67 |
0.33 |
| Общий антиоксидант ммоль\л |
1,38 |
±0,15 |
1,45 |
±0,15 |
0.003 |
Таблица 5. Содержание показателей антиоксидантной защиты в крови больных II группы.
| Показатели
|
М
|
m
|
М
|
m
|
Р
|
| 0 день
|
10 день
|
| СОД ед. акт. /мг гемоглобина |
207,38 |
±22,90 |
214,52 |
±22,90 |
0.03 |
| Общий антиоксидант ммоль\л |
1,50 |
±0,22 |
1,58 |
±0,22 |
0.01 |
Таблица 6. Разница значений показателей активности антиоксидантной системы крови на 10 день лечения в I и II группах.
| Показатели
|
М
|
m
|
М
|
m
|
Р
|
I группа (n=38)
10 день
|
II группа (n=38)
10 день
|
| Дельта СОД |
3,52 |
±0,27 |
-7,14 |
±0,19 |
0,030 |
| Дельта общий антиоксидант |
-0,07 |
±0.01 |
-0,09 |
±0.01 |
0,037 |
Как следует из данных табл. 4 и 5 курсовое применение как ремаксола, так и адеметионина повышает активность антиоксидантной системы крови.
Так как группы больных могли быть неоднородны по активности антиоксидантной защиты, нами изучена разность показателей АОС крови на 10 день лечения в I и II группах больных (табл. 6).
Как следует из данных табл. 6 применение адеметионина более значимо повышает активность ферментного (СОД) звена АОС, а ремаксол более активно влияет на содержание общего антиоксиданта крови как за счет ферментного, так и неферментного звена АОС.
Таким образом, сравнительный анализ схем терапии, включающих гепатопротекторы, пациентов с НАСГ и сахарным диабетом 2 типа выявил высокую эффективность ремаксола, что проявлялось в улучшении функционального состояния печени (уменьшении признаков цитолиза и холестаза), липидного и углеводного обмена, повышении активности АОС и, как следствие, выраженной положительной динамике клинической симптоматики.
Результаты нашего исследования показали, что у всех пациентов, получавших терапию в полном объеме, нежелательных побочных явлений на введение ремаксола выявлено не было.
Выводы
- Включение в схемы терапии пациентов с неалкогольным стеатогепатитом и сахарным диабетом 2 типа ремаксола уменьшает выраженность метаболического синдрома за счет снижения проявлений холестаза и цитолиза, улучшения показателей липидного обмена и АОС.
- Выявлено положительное влияние ремаксола на углеводный обмен, проявляющееся в снижении уровня глюкозы на 15,6%, лактата на 18,5%, что является важным эффектом коррекции метаболических расстройств у больных СД 2 типа.
- Улучшение печеночной активности и обменных процессов, активация антиоксидантной системы, происходящее на фоне терапии ремаксолом, существенно уменьшает выраженность основных клинических синдромов (астеновегетативного на 46% и диспепсического - на 15%).
- Эффективность ремаксола, наряду с его безопасностью, позволяет рекомендовать включение препарата в схемы терапии пациентов с неалкогольной жировой болезнью печени и сахарным диабетом 2 типа для коррекции метаболических расстройств при данной патологии.
СПИСОК ЛИТЕРАТУРЫ
- Яковенко Э. П., Григорьев П. Я., Агафонова Н. А., Яковенко А. В. и соавт. Метаболические заболевания печени: проблемы терапии. Фарматека. - 2003. - № 10. - С. 20-23.
- Новицкий А. А., Алексанин С. С., Дударенко С. В. Механизмы развития патологии внутренних органов в условиях экологического и профессионального перенапряжения регуляторных систем организма человека. Медико-биологические и социально-психологические проблемы безопасности в чрезвычайных ситуациях. 2010. - № 1. - С. 5-9.
- Ивашкин В. Т., Шульпекова Ю. О. Неалкогольный стеатогепатит. Приложение РМЖ «Болезни органов пищеварения». 2000. - №2. - С. 41-45.
- Подымова С. Д. Жировой гепатоз, неалкогольный стеатогепатит. Клинико - морфологические особенности. Прогноз. Лечение. РМЖ. Болезни органов пищеварения. 2005. - Том VII, №2. - С. 61-67.
- Богомолов П. О., Павлова Т. В. Неалкогольный стеатогепатит патофизиология, патоморфология, клиника и подходы к лечению. Фарматека. 2003. - № 10. - С. 31-39.
- Звенигородская Л. А., Хомерики С. Г., Егорова Е. Г. Морфологические изменения печени при инсулинорезистентности. Русский медицинский журнал. 2008. - Т. XVI, №4. - С. 161-166.
- Bellentani S., Scaglioli F., Marino M., Bedogni G. Epidemiology of non-alcoholic fatty liver disease. Dig Dis. 2010.- №28.- P. 155-161.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 www.polysan.ru
www.polysan.ru
 Примечание: * - р<0,03, при сравнении с уровнем до начала лечения
Примечание: * - р<0,03, при сравнении с уровнем до начала лечения