-
Новые долгосрочные данные исследования фазы III препарата RINVOQ™ (упадацитиниб) для лечения ревматоидного артрита, представлены на ежегодном Европейском конгрессе ревматологов (EULAR) в 2020 году, который прошел в он-лайн формате
Новые долгосрочные данные исследования фазы III препарата RINVOQ™ (упадацитиниб) для лечения ревматоидного артрита, представлены на ежегодном Европейском конгрессе ревматологов (EULAR) в 2020 году, который прошел в он-лайн формате
СтатьиПредставлены новые долгосрочные результаты, согласно которым, ежедневный прием упадацитиниба оказывал выраженную положительную динамику признаков и симптомов ревматоидного артрита на 72 и 84 неделях в фазе III клинических исследований SELECT-COMPARE (упадацитиниб в дозе 15 мг в комбинации с метотрексатом (MT)) и SELECT-MONOTHERAPY (упадацитиниб в дозах 15 мг и 30 мг) соответственно1,2. Профиль безопасности упадацитиниба (15 мг и 30 мг) в монотерапии и упадацитиниба (15 мг) в комбинации с метотрексатом соответствовал ранее опубликованному комплексному анализу безопасности исследований фазы III при ревматоидном артрите, новых рисков безопасности не обнаружено1-5
Кроме того, результаты клинических исследований SELECT-EARLY (упадацитиниб в дозах 15 мг и 30 мг) и SELECT-COMPARE продемонстрировали эффективность упадацитиниба в предотвращении рентгенологического прогрессирования как в монотерапии, так и в комбинации с метотрексатом в течении 96 недель наблюдения3. Полные результаты были представлены на ежегодном Европейском конгрессе ревматологов (EULAR) 2020 года, который прошел в он-лайн формате.
Разработанный компанией AbbVie препарат RINVOQ™, являющийся селективным обратимым ингибитором JAK, одобрен для приема один раз в сутки, перорально, в дозе 15 мг у взрослых пациентов, страдающих ревматоидным артритом умеренной и высокой активности1-5.
«Эти новые долгосрочные данные демонстрируют эффективность применения препарата RINVOQTM для уменьшения признаков и симптомов ревматоидного артрита, как в монотерапии, так и в комбинации с метотрексатом», - сообщил Исидро Вильянуэва (Isidro Villanueva), вице-президент, отдел медицинской иммунологии компании AbbVie. «Мы рады поделиться с ревматологическим сообществом этими результатами, позволяющими рассматривать препарат РАНВЭК/RINVOQTM как значимый вариант лечения, который способен помочь большему количеству пациентов с ревматоидным артритом добиться целей терапии»
Результаты исследования SELECT-COMPARE, 72-недельный период наблюдения.
Долгосрочные результаты исследования SELECT-COMPARE демонстрируют, что препарат RINVOQTM в комбинации с метотрексатом достоверно способствовал достижению более высокого уровня ответа через 72 недели по основным индексам оценки активности ревматоидного артрита, включая ремиссию, по сравнению с адалимумабом в комбинации метотрексатом1.
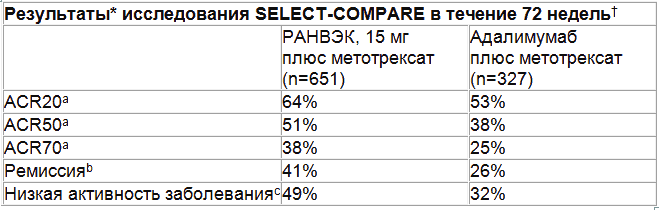
* Данные по эффективности получены на основании рандомизированного клинического исследования. У пациентов со сменой лечения, для определения бинарных конечных точек использовался подход замены недостающих пропущенных значений данными об отсутствии ответа на лечение (Non responder imputation(NRI)). Для препарата РАНВЭК/RINVOQTM в комбинации с метотрексатом все основные вторичные конечные точки через 72 недели достигли Р-значений ≤0,001 по сравнению с адалимумабом в комбинации с метотрексатом, за исключением ACR20 (для ACR20 значение p -≤0,01).
†При отсутствии улучшения состояния (уменьшения числа болезненных и припухших суставов по крайней мере на 20%) на 14-й, 18-й или 22-й неделях или если значение индекса клинической активности заболевания (CDAI) было больше 10 на 26-й неделе, пациенты, получавшие адалимумаб были переведены на прием препарата РАНВЭК/RINVOQTM в дозе 15 мг и наоборот. Метод NRI был использован для анализа смены лечения до 26-й недели, а метод замены пропущенных данных последним значением был использован для анализа смены лечения на 26-й неделе.
aACR20/50/70 определялся как по меньшей мере 20%/50%/70%-е снижение числа болезненных и припухших суставов (ЧПС) относительно исходного уровня и эквивалентное улучшение по трем (или более) из пяти других основных критериев Американской коллегии ревматологов: субъективная оценка боли пациентом, общая активность заболевания, функциональный статус, общая оценка активности заболевания врачом и острофазовые показатели
bРемиссия определялась по значению индекса DAS28-СРБ менее 2,6 (счет по 28 суставам)
cНизкая активность заболевания определялась по значению индекса DAS28-СРБ меньше или равной 3,2 (счет по 28 суставам)
Профиль безопасности препарата RINVOQTM (в дозе 15 мг один раз в сутки) в комбинации с метотрексатом в целом соответствовал ранее опубликованному комплексному анализу безопасности исследования фазы III при ревматоидном артрите, новых сигналов по безопасности обнаружено не было.1,[iv] Серьезные нежелательные явления (НЯ) возникали с частотой 12,7 случаев/100 ПЛ (на 100 пациенто-лет) при применении препарата РАНВЭК (в дозе 15 мг) в комбинации с метотрексатом, по сравнению с 15,9 случаев/100 ПЛ, при применении адалимумаба в комбинации с метотрексатом1. Частота серьезных инфекций составила 3,7 случаев/100ПЛ при применении препарата RINVOQTM (в дозе 15 мг) в комбинации с метотрексатом и 4,3 явления/100PY при применении адалимумаба в комбинации с метотрексатом. Было зарегистрировано восемь летальных исходов при применении препарата RINVOQTM (0,6/100ПЛ) и шесть летальных исходов при применении адалимумаба (1,2/100ПЛ), включая летальные исходы, которые не были связанны с проводимой терапией1. В течение всего периода исследования было зарегистрировано восемь крупных нежелательных сердечно-сосудистых явлений (MACE), в том числе пять на фоне приема препарата RINVOQTM (0,4/100ПЛ) и три на фоне терапии адалимумабом (0,6/100ПЛ). Также были зарегистрированы пациенты с венозными тромбозами и тромбоэмболиями (ВТЭ): четыре на фоне приема препарата RINVOQTM (0,3/100ПЛ), и пять на фоне приема адалимумаба (1,0/100 ПЛ)1.
Результаты исследования SELECT-MONOTHERAPY, 84-недельный период наблюдения.
В долгосрочном периоде наблюдения исследования SELECT-MONOTHERAPY пациенты, получавшие метотрексат в первой фазе исследования, на 14 неделе были переведены на заслепленный прием упадацитиниба (в дозах 15 или 30 мг) в соответствии с заранее определенным порядком на этапе включения2. Результаты этого исследования показывают, что монотерапия упадацитинибом приводила к улучшению признаков и симптомов ревматоидного артрита в течение 84 недель2.
*Полученные данные основаны на результатах клинического исследования SELECT-MONOTHERAPY
†Доза упадацитиниба 30 мг не одобрена к применению.
aACR20/50/70 определялся как по меньшей мере 20%/50%/70%-е снижение числа болезненных (ЧБС) и припухших суставов (ЧПС) относительно исходного уровня и эквивалентное улучшение по трем (или более) из пяти других основных критериев Американской коллегии ревматологов: субъективная оценка боли пациентом, общая активность заболевания, функциональный статус, общая оценка активности заболевания врачом и острофазовые показатели
bРемиссия определялась по значению индекса DAS28-СРБ менее 2,6 (счет по 28 суставам)
cНизкая активность заболевания (НАЗ) определялась по значению индекса DAS28-СРБ меньше или равной 3,2 (счет по 28 суставам)
Профиль безопасности препарата RINVOQTM (упадацитиниб 15 мг и 30 мг) в монотерапии на 84-й неделе в целом соответствовал ранее опубликованному комплексному анализу безопасности исследования фазы III при ревматоидном артрите, новых сигналов по безопасности не обнаружено2,4. Серьезные НЯ наблюдались на 84-й неделе с частотой 18,5 явлений/100ПЛ (на 100 пациенто-лет), при приеме упадацитиниба в дозе 15 мг и с частотой 16,9 явлений/100ПЛ, при приеме упадацитиниба в дозе 30 мг2. Наиболее распространенным серьезным НЯ являлась пневмония2. Частота возникновения опоясывающего лишая, нарушений функции печени и повышения уровня креатинфосфокиназы была выше у пациентов, получавших упадацитиниб в дозе 30 мг, в то время как частота появления серьезных инфекций и злокачественных новообразований между дозами упадацитиниба в 30 мг и 15 мг была сопоставима2. Было зарегистрировано семь случаев возникновения крупных нежелательных сердечно-сосудистых явлений (MACE) (0,5/100ПЛ при дозе 15 мг; 1,2/100ПЛ при дозе 30 мг) и пять случаев венозных тромбозов и тромбоэмболий (ВТЭ) (0,9/100ПЛ при дозе 15 мг; 0,2/100 ПЛ при дозе 30 мг)2. Все случаи возникновения крупных нежелательных сердечно-сосудистых явлений и венозных тромбоэмболических осложнений имели место у пациентов с основными факторами риска2. Было зарегистрировано три летальных исхода (0,7/100ПЛ) при приеме упадацитиниба в дозе 15 мг и 30 мг, включая летальные исходы, которые не были связанны с проводимой терапией.
Предотвращение рентгенологического прогрессирования в течении двух лет (96 недель): данные исследования SELECT-EARLY и SELECT-COMPARE
В исследования SELECT-EARLY и SELECT-COMPARE были включены пациенты с ревматоидным артритом и высоким риском развития прогрессирующих структурных повреждений суставов, имеющие начальные эрозивными изменения суставов и/или обладающие признаками серопозитивности3. Препарат RINVOQTM предотвращал рентгенологическое прогрессирование у пациентов, ранее не получавших метотрексат, в монотерапии и у пациентов с недостаточным ответом на метотрексат в комбинации с метотрексатом3.

d Отсутствие рентгенографического прогрессирования поражения суставов определялось с помощью модифицированного общего счета Шарпа (mTSS) с количеством баллов ≤0.* Доза упадацитиниба 30 мг не одобрена к применению. Применение препарата РАНВЭК/RINVOQTM для лечения ранее не получавших метотрексат пациентов не одобрено.
[1] Fleischmann R, et al. Long-Term Safety and Effectiveness of Upadacitinib or Adalimumab in Patients with Rheumatoid Arthritis: Results at 72 weeks from the SELECT-COMPARE Study. 2020 EULAR E-Congress; THU0201
[2] Smolen J, et al. Upadacitinib as Monotherapy in Patients with Rheumatoid Arthritis and Prior Inadequate Response to Methotrexate: Results at 84 Weeks From the SELECT-MONOTHERAPY Study. 2020 EULAR E-Congress; THU0213.
[3] Peterfy CG, et al. Radiographic Outcomes in Patients with Rheumatoid Arthritis Receiving Upadacitinib as Monotherapy or in Combination with Methotrexate: Results at 2 years from the SELECT-COMPARE and SELECT-EARLY Studies. 2020 EULAR E-Congress; THU0211.
[4] Cohen S, et al. Safety Profile of Upadacitinib Up to 3 Years of Exposure in Patients With Rheumatoid Arthritis. 2020 EULAR E-Congress; THU0197.
5 RINVOQ [Summary of Product Characteristics]. AbbVie Deutschland GmbH & Co. KG; March 2020. Available at: ema.europa.eu/en/documents/product-information/rin….
6 Pipeline – Our Science | AbbVie. AbbVie. 2020. Available at: abbvie.com/our-science/pipeline.html. Accessed on May 18, 2020.
7 A Study Comparing Upadacitinib (ABT-494) to Placebo and to Adalimumab in Participants With Psoriatic Arthritis Who Have an Inadequate Response to at Least One Non-Biologic Disease Modifying Anti-Rheumatic Drug (SELECT - PsA 1). ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT03104400. Accessed May 18, 2020.
8 A Multicenter, Randomized, Double-Blind, Placebo-Controlled Study of ABT-494 for the Induction of Symptomatic and Endoscopic Remission in Subjects With Moderately to Severely Active Crohn's Disease Who Have Inadequately Responded to or Are Intolerant to Immunomodulators or Anti-TNF Therapy. ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT02365649. Accessed on May 18, 2020.
9 Evaluation of Upadacitinib in Adolescent and Adult Patients With Moderate to Severe Atopic Dermatitis (Eczema)- Measure Up 1. ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT03569293. Accessed on May 18, 2020.
10 A Study to Evaluate the Safety and Efficacy of ABT-494 for Induction and Maintenance Therapy in Subjects With Moderately to Severely Active Ulcerative Colitis. ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT02819635. Accessed on May 18, 2020.
11 A Study Evaluating the Safety and Efficacy of Upadacitinib in Subjects With Active Ankylosing Spondylitis (SELECT Axis 1). ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/study/NCT03178487. Accessed on May 18, 2020.
12 A Study to Evaluate the Safety and Efficacy of Upadacitinib in Participants With Giant Cell Arteritis (SELECT-GCA). ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT03725202. Accessed on May 18, 2020.
13 A Study Comparing Upadacitinib (ABT-494) to Placebo in Participants With Active Psoriatic Arthritis Who Have a History of Inadequate Response to at Least One Biologic Disease Modifying Anti-Rheumatic Drug (SELECT - PsA 2). ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT03104374. Accessed on May 18, 2020.
14 A Study to Evaluate Efficacy and Safety of Upadacitinib in Adult Participants With Axial Spondyloarthritis (SELECT AXIS 2). ClinicalTrials.gov. 2020. Available at: clinicaltrials.gov/ct2/show/NCT04169373. Accessed on May 18, 2020.
15 HUMIRA [Summary of Product Characteristics]. AbbVie Deutschland GmbH & Co KG. Available at: ema.europa.eu/docs/en_GB/document_library/EPAR_-_P…. Accessed May 18, 2020.
17 июля 2020 г.Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)Если Вы медицинский специалист, войдите или зарегистрируйтесь
ПРАКТИКА ПЕДИАТРА
