Результаты лечения распространённого гнойного перитонита у детей
Статьи
B. А. Завьялкин1, М.А. Барская1, С.Н. Юхимец2
1 Самарский государственный медицинский университет, Самара, Россия;
2 Университет Святого Иосифа в Танзании, Дар-эс-Салам, Танзания
Аннотация
Обоснование. Несмотря на значительные достижения в области хирургического лечения и использование современных антибиотиков, тяжёлые гнойные осложнения хирургических заболеваний органов брюшной полости остаются актуальной проблемой. В связи со сложностью патогенеза распространённого гнойного перитонита, часто не уделяется достаточного внимания коррекции нарушений метаболизма, особенно у детей. Совершенствование комплексной терапии распространённого перитонита, позволяет добиться улучшения результатов лечения данной группы пациентов.
Цель. Анализ результатов лечения распространённого гнойного перитонита у детей с использованием оптимизированной патогенетической терапии, включающей дифференцированный подход к предоперационной подготовке, критерии санации брюшной полости на основании степени интраабдоминальной гипертензии и активную коррекцию дисметаболических расстройств в послеоперационном периоде.
Методы. В данном исследовании изучены результаты лечения 339 пациентов в возрасте от 1 г. до 14 лет с распространённым гнойным перитонитом различной этиологии, находившихся на стационарном лечении в детских хирургических отделениях г. Самара с 2006 по 2022 г. В основную группу (оптимизированного лечения) включили 237 детей, в контрольную (традиционного лечения) — 102 ребёнка. В основной группе лечебная тактика проводилась на основании разработанного нами лечебно-диагностического алгоритма. Комплексное обследование включало изучение динамики биохимических показателей крови.
Результаты. Изучив динамику трансаминаз, мы пришли к выводу, что у детей основной группы, несмотря на исходную тяжесть эндотоксикоза, наблюдалось более быстрое снижение уровня печёночных ферментов, свидетельствующее о более эффективном восстановлении клеточных мембран. Динамика концентрации общего белка и альбумина свидетельствовала о более быстром восстановлении белково-синтетической функции печени у детей основной группы, что находило отражение в улучшении общего состояния больных, стабилизации показателей гемостаза и снижении концентрации белков острой фазы воспаления в плазме крови.
Анализ результатов лечения выявил в основной группе статистически значимое уменьшение длительности инфузионной терапии в послеоперационном периоде, уменьшение сроков госпитализации и пребывания пациентов в отделении реанимации и интенсивной терапии.
Заключение. Таким образом, снижение длительности инфузионной терапии, госпитализации и нахождения больных в отделении реанимации свидетельствует о большей эффективности предложенного комплексного лечения детей с распространённым гнойным перитонитом.
Ключевые слова: распространённый перитонит; лечение перитонита; дети; антигипоксанты; Реамберин®; Ремаксол®.
Как цитировать:
Завьялкин В.А., Барская М.А., Юхимец С.Н. Результаты лечения распространённого гнойного перитонита у детей // Детская хирургия. 2024. Т. 28. № 1. C. 15-25.
Results of treatment of diffuse purulent peritonitis in children
Vladislav A. Zavyalkin1, Margarita A. Barskaya1, Sergey N. Yukhimets2
1 Samara State Medical University, Samara, Russia;
2 St. Joseph University In Tanzania, Dar es Salaam, Tanzania
Abstract
Background: Despite significant achievements in surgery and in antibiotic therapy, management of children with severe purulent complications of surgical diseases in the abdominal cavity remains an important issue. Due to the polyetiology of diffuse purulent peritonitis, sometimes not enough attention is paid to metabolism correction, especially in children. Optimization of comprehensive therapy in the diffuse purulent peritonitis promotes better outcomes in this group of patients.
Aim: To assess results of the treatment of children with diffuse purulent peritonitis applying the optimized pathogenetic therapy which includes a differentiated approach to the preoperative preparation, active correction of dysmetabolic disorders in the postoperative period as well as selection of the criteria for abdominal cavity sanation bearing in mind the degree of intraabdominal hypertension.
Methods: Outcomes of 339 patients, aged 1-14 years, with diffuse peritonitis of various etiology were analyzed. The patients were hospitalized to pediatric surgical departments in Samara in 2006-2022. The studied group included 237 children with diffuse purulent peritonitis who were prescribed the optimized comprehensive therapy. Control group included 102 children with diffuse purulent peritonitis who were prescribed traditional therapy according to the generally accepted standards. In the studied group, patients' therapeutic tactics included a therapeutic and diagnostic algorithm developed by the authors. Complex examination registered the dynamics of biochemical blood parameters: total protein, albumin, alanine transaminase, aspartate aminotransferase, as well as indicators of endotoxicosis (C-reactive protein and procalcitonin).
Results: After studying the dynamics of transaminases, we concluded that in children with widespread peritonitis in the main group, despite the initial severity of endotoxicosis, there was a faster decrease in the level of liver enzymes, indicating a more effective restoration of cell membranes. The dynamics of the level of total protein and albumin revealed a faster recovery of protein-synthetic liver function in children of the main group, including antitoxic, which was reflected in the improvement of the general condition of patients and stabilization of hemostasis indicators, a decrease in the levels of acute phase proteins. The analysis of the results of the complex treatment of children with advanced peritonitis revealed a statistically significant decrease in the main group: the duration of stay of patients in the intensive care unit after surgery, the timing of infusion therapy in the postoperative period, as well as the duration of hospitalization.
Conclusion: Thus, less stay in the intensive care unit in the postoperative period, less terms of infusion therapy as well as less length of stay in children with diffuse peritonitis demonstrate better effectiveness of the proposed comprehensive management of children with the discussed pathology.
Keywords: diffuse peritonitis; treatment of peritonitis; children; antihypoxants; Reamberin®; Remaxol®.
For citation: Zavyalkin VA, Barskay MA, Yukhimets SN. Results of treatment of diffuse purulent peritonitis in children. Russian Journal of Pediatric Surgery. 2024;28(1):15-25.
Обоснование
Несмотря на значительные достижения в области хирургического лечения и использования современных антибиотиков, лечение детей с тяжёлыми гнойными осложнениями хирургических заболеваний органов брюшной полости остаётся сложной задачей.
В связи с полиэтиологичностью распространённого гнойного перитонита (РГП) и сложностью его патогенеза, иногда не уделяется достаточного внимания коррекции нарушений внутреннего баланса организма, особенно у детей [1-3]. На данный момент нет чёткого алгоритма предоперационной подготовки. Часть литературных источников рекомендует ограничить её длительность до 3 ч [4, 5], некоторые авторы предлагают увеличить до 5-6 ч и более [6, 7].
До сих пор продолжаются дискуссии о методах хирургического лечения распространённого перитонита у детей. Большинство авторов поддерживают необходимость лапароскопической санации брюшной полости при распространённом перитоните, однако единого мнения о выборе оперативного доступа и способах санации брюшной полости не существует [8-11].
Лечение РГП должно сочетать: нутритивную поддержку; инфузионную терапию для восстановления водно-электролитного и кислотного щелочного равновесия организма; дезинтоксикацию с применением методов интракорпоральной и экстракорпоральной дезинтоксикации; посиндромную терапию, включающую различные методы восстановления перистальтики, вплоть до электростимуляции; антибактериальную терапию — от эмпирической и эскалационной до деэскалационной, в зависимости от тяжести РГП; обязательный контроль за очагом РГП и послеоперационными осложнениями [12-18].
В терапии тяжёлых хирургических инфекций, в том числе РГП, немаловажную роль играет эндогенный сукцинат. Являясь метаболическим переключателем, обеспечивающим адаптацию иммунных клеток к условиям дефицита энергетического субстрата и кислорода, он активирует макрофаги. Применение препаратов, содержащих экзогенные сукцинаты (антигипоксант Реамберин®), приводит к результативному уменьшению системной воспалительной реакции в связи с увеличением энергетического обеспечения иммунных клеток, восстановлением работы цепи переноса электронов, подавлением гликолиза и восстановлением регуляции стабильности фактора, индуцируемого гипоксией 1а [19].
Таким образом, совершенствование комплексной терапии распространённого перитонита, включающей тщательно проработанные программу предоперационной подготовки и критерии санации, а также оптимизация послеоперационной терапии, учитывающей дисметаболические нарушения при РГП, позволяют добиться улучшения непосредственных результатов лечения данной группы пациентов.
Цель
Цель нашего исследования — изучение результатов лечения РГП у детей с использованием оптимизированной патогенетической терапии, включающей дифференцированную предоперационную подготовку, критерии санации брюшной полости на основании степени интраабдоминальной гипертензии (ИАГ) и активную коррекцию дисметаболических расстройств в послеоперационном периоде.
Методы
Проведён анализ результатов лечения 339 детей от 1 г. до 14 лет с распространённым перитонитом (РП) различной этиологии, находившихся на стационарном лечении в детских хирургических отделениях лечебно-профилактических учреждений г. Самара с 2006 по 2022 г. Перед началом исследования было получено добровольное информированное согласие на исследование и использование медицинских данных в научных целях.
Критерии исключения из исследования были следующими: дети до 1 г. с РП различной этиологии, пациенты с РП при наличии нейрогенного мочевого пузыря, больные, причиной РП у которых явился панкреонекроз.
Для анализа динамики состояния проводилось клиническое исследование мочи и крови (концентрация гемоглобина в плазме крови, подсчёт числа лейкоцитов, лейкоцитарного индекса интоксикации, подсчёт числа тромбоцитов с помощью автоматического гематологического анализатора Mindray ВС-3600). У всех пациентов изучена динамика биохимических показателей крови с помощью автоматического биохимического анализатора Mindray ВС-800 при поступлении, на 3, 7 день и при выписке: концентрация С-реактивного белка (СРВ), Na+ и К+ в плазме крови, концентрация общего белка, альбумина и прокальцитонина в сыворотке крови, активность аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) в сыворотке крови.
В зависимости от вида лечения пациентов распределили на две группы. В основную группу (ОГ) вошли 237 пациентов — им выполняли оптимизированное комплексное лечение. В контрольную группу (КГ) вошли 102 пациента, которым проводили традиционную комплексную терапию согласно общепринятым подходам и «Национальным руководствам по детской хирургии» 2009 и 2021 гг. [4, 5].
В ОГ лечебная тактика проводилась на основании компьютерной программы «Программа для выбора алгоритма оперативной тактики при РП у детей в зависимости от внутрибрюшного давления» (свидетельство о государственной регистрации № RU 2023619650 от 27.04.2023). Лечебно-диагностический алгоритм представлен на рис. 1 [20].
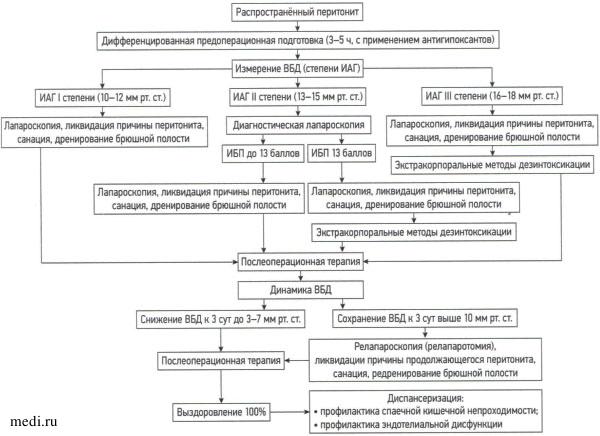 Рис. 1. Усовершенствованный алгоритм лечения распространённого гнойного перитонита у детей: ВБД — внутрибрюшное давление; И АГ — интраабдоминальная гипертензия; ИБП — индекс брюшной полости.
Рис. 1. Усовершенствованный алгоритм лечения распространённого гнойного перитонита у детей: ВБД — внутрибрюшное давление; И АГ — интраабдоминальная гипертензия; ИБП — индекс брюшной полости.
Fig. 1. The optimized algorithm of treating the diffuse purulent peritonitis in children: ВБД — intra-abdominal pressure; ИАГ — intraabdominal hypertension; ИБП — abdominal index.
Предоперационная подготовка у детей КГ проводилась согласно общепринятым подходам и «Национальным руководствам по детской хирургии» [4, 5]. У пациентов ОГ применялась дифференцированная предоперационная подготовка, которая зависела от возраста, степени тяжести состояния, степени эндотоксикоза, стадии РГП и синдрома кишечной недостаточности. Длилась дифференцированная подготовка не менее 4 ч. Кроме стандартной инфузионной терапии полиионными растворами, с целью улучшения интракорпоральной дезинтоксикации применялся препарат янтарной кислоты — антигипоксант Реамберин® в дозе 5 мл/кг в сут.
В ОГ у 175 детей с интраабдоминальной гипертензией (ИАГ) I степени (внутрибрюшное давление (ВБД) 10-12 мм рт. ст.) санация брюшной полости выполнялась при помощи видеолапароскопии. В 59 случаях с ИАГ II степени (ВБД 13-15 мм рт. ст.) выполнена диагностическая лапароскопия, изучен индекс брюшной полости (ИБП) по В.С. Савельеву [21]. В 49 случаях с ИБП выше 13 баллов проведена конверсия в срединную лапаротомию. Оперативное лечение 3 пациентов с ИАГ III степени сразу начинали со срединной лапаротомии. В КГ всем пациентам выполняли срединную лапаротомию.
После обеспечения доступа экссудат из брюшной полости эвакуировали видеолапароскопически или через срединную лапаротомию, проводили забор экссудата для посева на микрофлору и чувствительность к антибиотикам. Осуществляли первичную санацию брюшной полости для уменьшения всасывания токсинов, оценивали характер и распространённость перитонита. Выполняли ревизию органов брюшной полости и забрюшинного пространства для выявления первоисточника перитонита и возможной сопутствующей патологии, после чего принимали решение об объёме выполняемой операции. Выполняемый объем по устранению источника перитонита зависел от его этиологии.
У 301 больного причиной РП явился деструктивный аппендицит, который у 193 больных сопровождался гнойным оментитом. Этим пациентам кроме аппендэктомии проведена резекция сальника в пределах здоровых тканей. Клиновидная резекция подвздошной кишки выполнена у 17 пациентов с дивертикулитом Меккеля. При перфорациях кишечника инородными телами (магнитами у 6 пациентов) или при травматических перфорациях (у 5 пациентов) дефекты были ушиты, если отсутствовала инфильтрация вокруг перфоративного отверстия. Больным с некрозом кишки и реактивной стадией перитонита в 3 случаях инвагинации и в 1 случае странгуляционной непроходимости выполнена резекция поражённого участка тонкой кишки с наложением анастомоза конец в конец. При перфоративных язвах желудка выполняли иссечение краёв язвы с последующим ушиванием дефекта.
Всем пациентам КГ после завершения внутрибрюшных этапов оперативного лечения проводилась санация брюшной полости физиологическим раствором «до чистых вод». В 2012 году мы отказались от отмывания брюшной полости жидкостями, в том числе 0,9% раствором натрия хлорида. Пациентам ОГ выполнялась только тщательная эвакуация выпота электроотсосом под видеолапароскопическим контролем. Санация завершалась введением в брюшную полость 10 мл 1% раствора гидроксиметилхиноксалиндиоксида.
Послеоперационная терапия является важным компонентом лечения РП. Она складывается из продолжения этиотропной (антибактериальной) терапии, начатой в предоперационном периоде; патогенетической терапии, состоящей из базисной и посиндромной терапии; контроля за очагом хирургической инфекции — ухода за дренажами, перевязок и, при необходимости, повторных санаций брюшной полости.
Инфузионная терапия продолжалась в послеоперационном периоде с целью дальнейшей детоксикации, коррекции нарушения водно-электролитного баланса и борьбы с ацидозом. Инфузионная терапия корректировалась, исходя из физиологических потребностей организма ребёнка с учётом патологических потерь. Базовыми препаратами являлись растворы кристаллоидов. Коллоидные растворы применялись только при выраженных расстройствах гемодинамики, как правило, в 1 сут нахождения ребёнка в стационаре.
У детей ОГ кроме стандартной инфузионной терапии с целью совершенствования интракорпоральной детоксикации использовали антигипоксант, содержащий растворимую форму сукцината янтарной кислоты — Реамберин® в дозе 5 мл/кг в сут. С целью гепатопротекции, так как в патогенезе эндотоксикоза и последующего развития эндотелиальной дисфункции имеет большое значение повреждение гепатоцитов и ретикулоэндотелиальной системы печени, применялся Ремаксол® в дозе 5 мл/кг в сут. На применение гепатопротектора Ремаксол® получено разрешение биоэтического комитета (решение НОУ ВПО «Медицинский университет “Реавиз”» №7 от 15.04.2011 г.).
Эффективность послеоперационной инфузионной терапии контролировалась нормализацией водноэлектролитного состава крови и исчезновением симптомов интоксикации.
Статистический анализ
Статистическую обработку результатов выполняли в среде статистических вычислений R (R v.3.6.2-v.4.2.3, RStudio V. 1.1.463—v.2023.03.2, Jamovi v.2.3), первичный ввод данных производили с помощью электронных таблиц MS Excel. Использовали методы описательной статистики, тесты для сравнения пропорций, в том числе точный биноминальный для малых выборок и одновыборочный тест пропорций с коррекцией непрерывности для больших выборок.
Для проверки нулевой гипотезы относительно однородности пациентов в сравниваемых группах исследовали различия по t-критерию Стьюдента и 11-критерию Манна-Уитни для количественных признаков в зависимости от соблюдения условий их применения (нормальности распределения и равенства дисперсий для t критерия) и по критерию Хи-квадрат Пирсона (х2) для качественных, или номинальных признаков. При размерности таблицы сопряженности 2 на 2 использовали поправку Йейтса. В случаях, когда абсолютные частоты были меньше 5, применяли точный критерий Фишера. Статистически значимыми считали отличия при р <0,05.
Результаты
Проанализировав показатели периферической крови детей обеих групп при поступлении, мы обнаружили статистически значимое увеличение числа тромбоцитов и лейкоцитов, лейкоцитарного индекса интоксикации и гематокрита по сравнению с референсными значениями. При выписке значения всех показателей приближались к референсным у детей обеих групп (р=0,677).
Концентрация СРБ в плазме крови примерно в 20 раз превышала референсные значения: 69,5 [50,5; 122,0] мг/л у больных ОГ и 72,0 [52,0; 87,0] мг/л у больных КГ На 3 сут после начала лечения концентрация СРБ была ниже у детей ОГ по сравнению с детьми КГ, но статистически значимых отличий между ними во всех возрастных группах не выявлено: 1-3 г. (р=0,859), 4-6 лет (р=0,994), 7-11 лет (р=0,193), 12-14 лет (р=0,598).
На 7 сут мы обнаружили более выраженное снижение: в ОГ — до 22,0 [16,0; 29,0] мг/л, в КГ — 30,0 [24,0; 34,0] мг/л; статистически значимое в большинстве возрастных групп 1-3 г. (р=0,003), 4-6 лет (р=0,081), 7-11 лет (р <0,001), 12-14 лет (р-0,001). При выписке концентрация СРБ у всех детей приближались к референсным значениям: 1-3 г. (р=0,994); 4-6 лет (р=0,008), 7—11 лет (р=0,002), 12-14 лет (р <0,001) (рис. 2).
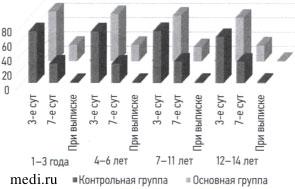 Рис. 2. Динамика концентрации С-реактивного белка в плазме крови детей с распространённым гнойным перитонитом после начала лечения.
Рис. 2. Динамика концентрации С-реактивного белка в плазме крови детей с распространённым гнойным перитонитом после начала лечения.
Fig. 2. C-reactive protein dynamics in children with diffuse purulent peritonitis after therapy beginning.
Таким образом, мы выявили снижение концентрации СРБ в обеих исследуемых группах более, чем 3 раза. При этом статистическая значимость была выше в ОГ по сравнению с КГ на 7 сут и при выписке.
Изучая динамику концентрации прокальцитонина после начала лечения, мы выявили выраженную разницу в сторону увеличения у детей КГ по сравнению с детьми ОГ во всех возрастных группах. На 3 сут разница составила в среднем (47,48±2,55)%; статистическая значимость в возрастных группах 1-2 г. (р=0,00**), 3-6 лет (p=0,010), 7-11 лет (р=0,010), 12-15 лет (р=0,00**). На 7 сут разница в среднем составила (68,35±3,68)% в сторону увеличения среди детей КГ по сравнению с детьми ОГ Различия были статистически значимыми во всех возрастных группах: 1-2 г. (р=0,010), 3-6 лет (р=0,010), 7-11 лет (р=0,00**), 12-15 лет (р=0,00**). При выписке концентрация прокальцитонина у всех больных приближались к показателям здоровых детей: 1-2 г. (р=0,010), 3-6 лет (р=0,022), 7-11 лет (p=0,010), 12-14 лет (р=0,00**) (рис. 3).
 Рис. 3. Динамика концентрации прокальцитонина в сыворотке крови детей с распространенным гнойным перитонитом после начала лечения.
Рис. 3. Динамика концентрации прокальцитонина в сыворотке крови детей с распространенным гнойным перитонитом после начала лечения.
Fig. 3. Procalcitonin dynamics in children with diffuse purulent peritonitis after therapy beginning.
У всех детей с РГП при поступлении активность трансаминаз в сыворотке крови была значительно выше по сравнению со здоровыми во всех возрастных группах, свидетельствуя о наличии токсической гепатопатии с выраженными морфологическими повреждениями гепатоцитов. С целью исследования эффективности предложенной совершенствованной стратегии лечения РГП нами выполнено изучение биохимических показателей цитолиза (АлАТ, АсАТ) в динамике на 3, 7 сут и при выписке.
Проанализировав динамику активности АлАТ на 3 сут мы обнаружили, что во всех возрастных группах активность была выше референсных значений здоровых детей. Статистически значимых различий между больными ОГ и КГ мы не выявили: 1-3 г. (р=0,104), 4-6 лет (р=0,832), 7-11 лет (р=0,179), 12-14 лет (р=0,794). На 7 сут мы обнаружили, что активность АлАТ среди детей ОГ приблизилась к референсному значению, однако среди детей КГ показатель был ещё существенно выше. Статистическая значимость различий между ОГ и КГ составила: 1-3 г. (р <0,001), 4-6 лет (р <0,001), 7-11 лет (р <0,001), 12-14 лет (р <0,001). При выписке активность АлАТ вернулась или приблизилась к норме как в ОГ, так и в КГ (рис. 4).
 Рис. 4. Динамика активности аланинаминотрансферазы в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Рис. 4. Динамика активности аланинаминотрансферазы в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Fig. 4. Alanine aminotransferase dynamics in children with diffuse purulent peritonitis after therapy beginning.
Изучение активности АсАТ в сыворотке крови на 3 сут показало, что среди детей ОГ активность снизилась по сравнению с детьми КГ. Статистическая значимость в возрастных группах 1-3 г. (р <0,001), 4-6 лет (р <0,001), 7-11 лет (р <0,001), 12-14 лет (р <0,001). Анализ динамики данного показателя на 7 сут выявил его приближение к референсным значениям, но более существенное снижение обнаружилось среди больных ОГ по сравнению с больными КГ Значимые статистические различия имелись в возрастных группах 7-11 лет (р <0,001), 12-14 лет (р=0,002). В возрастных группах 1-3 г. (р=0,076), 4-6 лет (р=0,051) статистически значимых различий не обнаружено. При выписке отмечалось достоверное возвращение или приближение к норме как в ОГ, так и в КГ во всех возрастных группах. Статистические отличия между ОГ и КГ обнаружены в возрастной группе 1-3 г. (р=0,042). В остальных возрастных группах значимых статистических различий не выявлено: 4-6 лет (р=0,804), 7-11 лет (р=0,575), 12-14 лет (р=0,862) (рис. 5).
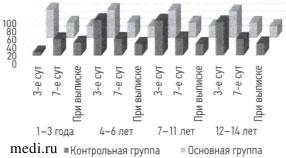 Рис. 5. Динамика активности аспартатаминотрансферазы в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Рис. 5. Динамика активности аспартатаминотрансферазы в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Fig. 5. Aspartate aminotransferase dynamics in children with diffuse purulent peritonitis after therapy beginning.
С целью оценки состояния белково-синтетической функции печени, нами изучена динамика концентраций общего белка и альбумина сыворотке крови.
Исследование динамики концентрации общего белка у больных с РГП после начала лечения, выявило снижение концентрации у всех детей на 3 сут. Более выраженное снижение произошло у детей КГ по сравнению с детьми ОГ Статистически значимая разница обнаружена в возрастной группе 4-6 лет (р=0,017). В остальных возрастных группах различия не были статистически значимыми: 1-3 г. (р=0,975), 7-11 лет (р=0,272), 12-14 лет (р=0,608). На 7 сут статистическая значимость различий между больными КГ и ОГ составила: 1-3 г. (р=0,051), 4-6 лет (р=0,938), 7-11 лет (р=0,003), 12-14 лет (р=0,568). При выписке показатель общего белка среди больных ОГ приблизился к референсным значениям здоровых. Среди больных КГ он был значительно ниже, чем среди больных ОГ, во всех возрастных группах. Статистические различия показателя составили: 1-3 г. (р <0,001), 4-6 лет (р <0,001), 7-11 лет (р <0,001), 12-14 лет (р <0,001) (рис. 6).
 Рис. 6. Динамика концентрации общего белка в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Рис. 6. Динамика концентрации общего белка в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Fig. 6. Total protein dynamics in children with diffuse purulent peritonitis after therapy beginning.
Анализируя динамику концентрации альбумина в сыворотке крови у пациентов с РГП после начала лечения, мы выявили его резкое уменьшение у всех детей как в ОГ, так и в КГ во всех возрастных группах по сравнению с референсным значениями, что свидетельствовало о тяжести гнойной хирургической инфекции и резком нарушении белково-синтетической функции гепатоцитов. На 3 сут между ОГ и КГ мы не выявили статистически значимых различий во всех возрастных группах: 1-3 г. (р=0,491), 4-6 лет (р=0,368), 7-11 лет (р=0,624), 12-14 лет (р=0,080). Изучая динамику показателя альбумина сыворотки крови на 7 сут мы обнаружили более значимое повышение и приближение к референсным значениям здоровых детей у пациентов ОГ по сравнению с пациентами КГ, во всех возрастных группах: 1—3 г. (р <0,001), 4-6 лет (р <0,001), 7-11 лет (р <0,001), 12-14 лет (р <0,001). При выписке показатель альбумина у больных с РГП в обеих группах приблизился к референсным значениям здоровых детей, но среди больных ОГ был значимо выше, чем среди больных КГ Во всех возрастных группах разница была статистически значимой: 1-3 г. (р <0,001), 4-6 лет (р <0,001), 7-11 лет (р <0,001), 12-14 лет (р <0,001) (рис. 7).
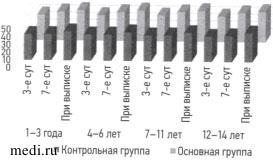 Рис. 7. Динамика концентрации альбумина в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Рис. 7. Динамика концентрации альбумина в сыворотке крови детей с распространённым гнойным перитонитом после начала лечения.
Fig. 7. Serum albumin dynamics in children with diffuse purulent peritonitis after therapy beginning.
У пациентов ОГ исчезновение симптомов интоксикации преимущественно наблюдалось в реактивной стадии на 3-4 сут, в токсической стадии и стадии полиморфных нарушений — после 5-7 сут заболевания. Динамика у пациентов КГ достоверно показала более позднее уменьшение интоксикации: к 5-7 сут у детей с реактивной стадией и к 9-12 сут у детей с токсической стадией (рис. 8).
 Рис. 8. Динамика объёма застойного содержимого желудка у детей с распространённым гнойным перитонитом после операции.
Рис. 8. Динамика объёма застойного содержимого желудка у детей с распространённым гнойным перитонитом после операции.
Fig. 8. Dynamics of the congested stomach content in children with diffuse purulent peritonitis after surgery.
Мы не выявили статистически значимой разницы между больными ОГ и КГ по количеству застойного отделяемого из желудка в 1 сут после оперативного лечения: средний объем отделяемого составил 12,2 мл/кг (р=0,783). Изучение данного показателя на 2 сут показало, что объем отделяемого в ОГ составил 6,17 мл/кг, в КГ — 8,64 мл/кг (р <0,001). На 3 сут объем отделяемого уменьшился у детей ОГ до 1,25 мл/кг, у детей КГ — до 6,26 мл/кг (р <0,001). С 4 сут мы обнаружили полное исчезновение застойного содержимого у детей ОГ У больных КГ на 4 сут объем снизился до 2,12 мл/кг и на 5 сут — до 1,19 мл/кг (р <0,001) (табл. 1).
Таблица 1.
Сроки появления самостоятельного стула у детей с распространённым гнойным перитонитом
Table 1. Terms of independent defecation in children with diffuse purulent peritonitis
| Срок появления самостоятельного стула, сут |
Все (n=339)
Me (Q1; Q3) |
КГ (n=102)
Me (Q1; Q3) |
ОГ (n=237)
Me (Q1; Q3) |
p |
| 2,41 [2,23; 3,11] |
3,72 [3,27; 4,09] |
2,28 [2,17; 2,44] |
<0,001 |
Примечание. КГ — контрольная группа; ОГ — основная группа; Me — медиана; Q1 — первый квартиль; Q3 — третий квартиль.
Note. КГ — control group; ОГ — main group; Me — median; Q1 — first quartile; Q3 — third quartile.
Исследуя сроки восстановления самостоятельного стула у детей после оперативного лечения по поводу РГП, мы обнаружили, что у пациентов ОГ стул появлялся в среднем через 2,28 сут, тогда как у пациентов в КГ — через 3,72 сут (р <0,001).
Анализируя результаты проведённого комплексного лечения, у детей ОГ мы выявили статистически значимое уменьшение медиан длительности инфузионной терапии, пребывания в стационаре и пребывания в отделении реанимации и интенсивной терапии (табл. 2). В обеих группах мы не наблюдали летальных исходов от основного заболевания и его осложнений.
Таблица 2.
Результаты лечения детей с распространённым гнойным перитонитом
Table 2. Outcomes after treating children with diffuse purulent peritonitis
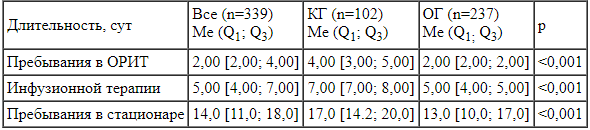 Примечание. 0РИТ — отделение реанимации и интенсивной терапии; КГ — контрольная группа; ОГ — основная группа; Me — медиана; Q1 — первый квартиль; Q3 — третий квартиль.
Примечание. 0РИТ — отделение реанимации и интенсивной терапии; КГ — контрольная группа; ОГ — основная группа; Me — медиана; Q1 — первый квартиль; Q3 — третий квартиль.
Note. КГ — control group; ОГ — main group; Me — median; Q1 — first quartile; Q3 — third quartile.
Обсуждение
РГП остаётся важной проблемой детской хирургии. Нами проведён анализ результатов лечения РГП у детей с использованием активной коррекции нарушений гомеостаза в послеоперационном периоде и совершенствованного лечебно-диагностического алгоритма, включающего дифференцированную предоперационную подготовку, выбор доступа, критерии санации брюшной полости на основе определения степени интраабдоминальной гипертензии.
Длительность и качество предоперационной подготовки зависели от степени тяжести состояния пациента, обусловленной выраженностью эндотоксикоза. Длительность предоперационной подготовки составляла 3-6 ч. При сравнении результатов нашего исследования с литературными источниками мы обнаружили, что в работах А.М. Шамсиева и соавт., Ю.С. Александровича и соавт. также подчёркивается важность устранения декомпенсированных расстройств гемодинамики, водно-электролитного баланса и кислотно-основного состояния. По данным авторов длительность предоперационной подготовки может достигать 6 ч и более [7, 22].
В литературе широко освещено преимущество лапароскопического доступа при РГП у детей [8, 9, 11]. В ряде работ отмечена важность значений интраабдоминальной гипертензии при РГП для определения исходов патологии [23, 24]. Нами выявлены величины ИАГ, позволяющие дифференцированно подходить к выбору доступа при РГП у детей: при ИАГ I степени (ВБД 10-12 мм рт. ст.) для санации брюшной полости использовали видеолапароскопию. При ИАГ II степени (ВБД 13-15 мм рт. ст.) проводили диагностическую лапароскопию с целью определения ИБП по В.С. Савельеву, при ИБП выше 13 баллов выполняли конверсию в срединную лапаротомию. Пациентам с ИАГ III степени (ВБД больше 15 мм рт. ст.) сразу выполняли срединную лапаротомию и осуществляли необходимый объем оперативного вмешательства.
С целью оптимизации интракорпоральной детоксикации в послеоперационном периоде, кроме стандартного лечения, терапия включала антигипоксант, содержащий растворимую форму сукцината янтарной кислоты — Реамберин®, а с целью гепатопротекции — Ремаксол®. Благоприятное воздействие этих препаратов на гомеостаз при воспалительных заболеваниях отражено в работе В.В. Лазарева и соавт. [19].
Сравнивая показатели больных ОГ и КГ — показатели периферической крови, динамику концентраций С-реактивного белка и прокальцитонина, активности трансаминаз, время исчезновения симптомов интоксикации, сроки восстановления функции желудочно-кишечного тракта, время лечения в отделении реанимации — мы отметили более выраженную положительную динамику перечисленных показателей в ОГ
Заключение
Использование предложенного лечебно-диагностического алгоритма, включающего оптимизацию каждого этапа, позволило улучшить результаты лечения детей с РГП и сделать следующие выводы:
1. Предоперационная подготовка при РГП должна быть дифференцированной, качество и длительность её должны зависеть от выраженности эндотоксикоза при поступлении пациента в стационар.
2. Для выбора оперативного доступа при РГП целесообразно определять уровни ИАГ и ИБП.
3. В послеоперационную терапию РГП целесообразно включать антигипоксант Реамберин® и гепатопротектор Ремаксол®.
Дополнительная информация
Вклад авторов. Все авторы подтверждают соответствие своего авторства международным критериям ICMJE. Наибольший вклад распределён следующим образом: В.А. Завьялкин — хирургическое лечение пациентов, обзор литературы, сбор и анализ литературных источников, написание текста; М.А. Барская — обзор литературы, сбор и анализ литературных источников, редактирование статьи подготовка и написание текста статьи; С.Н. Юхимец — статистическая обработка и анализ полученных результатов лечения, редактирование статьи.
Источник финансирования. Статья публикуется без спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов.
Этическая экспертиза. Протокол исследования был одобрен локальным этическим комитетом НОУ ВПО «Медицинский университет “Реавиз”» (№ 7 от 15.04.2011 г).
Additional information
Authors' contribution. All authors confirm compliance of their authorship with the international ICMJE criteria. The largest contribution is distributed as follows: V.A. Zavyalkin — surgical treatment of patients, literature review, collection, and analysis of literary sources, writing of the text; M.A. Barskaya — literature review, collection, and analysis of literary sources, editing of the article preparation, and writing of the text of the article; S.N. Yukhimets — statistical processing, and analysis of the results of treatment, and editing of the article.
Funding source. The publication had no sponsorship.
Competing interests. The authors claim that there is no conflict of interest in the article.
Ethics approval. The present study protocol was approved by the local Ethics Committee of the NEI HVE "Medical University" Reaviz" (No. 7 of 15.04.2011).
Об авторах
* Завьялкин Владислав Александрович, канд. мед. наук;
адрес: Россия, 443099, Самарская обл., Самара, ул. Чапаевская, д. 89;
Барская Маргарита Александровна, д-р мед. наук, профессор;
Юхимец Сергей Николаевич, канд. мед. наук;
Authors’ info
* Vladislav A. Zavyalkin, MD, Cand. Sci. (Medicine); address: 89 Chapaevskaya street, 443099 Samara, Samara region, Russia;
Margarita A. Barskaya, MD, Dr. Sci. (Medicine), Professor;
Sergey N. Yukhimets, MD, Cand. Sci. (Medicine);
Список литературы
1. Стец В.В., Половников С.Г., Журавлев А.Г., Шестопалов А.Е. Нутритивно-метаболическая коррекция в интенсивной терапии перитонита. Раны и раневые инфекции // Журнал имени профессора Б.М. Костюченка. 2016. Т. 3, № 1. С. 25-31. EDN: WMZLCH
2. Щеголев А.А., Товмасян Р.С., Чевокин А.Ю., и др. Третичный перитонит: состояние проблемы и возможные перспективы // Лечебное дело. 2018. № 4. С. 32-35. EDN: YYSJBB
3. Coral L.E., Ceron L.N., Delgado A.I. [Peritonitis treated by laparoscopy as an effective treatment. (In Spanish)] // Rev Gastroenterol Peru. 2018. Vol. 38, N3. P. 261-264.
4. Исаков Ю.Ф., Дронов А.Ф. Детская хирургия. Национальное руководство. Москва: ГЭОТАР-Медиа, 2009. 1168 с.
5. Разумовский А.Ю. Детская хирургия. Национальное руководство. 2-е изд., перераб. и доп. Москва: ГЭОТАР-Медиа, 2021. 1280 с.
6. Григорьев Е.Г., Совцов С.А., Кривцов Г.А. Острый перитонит. Клинические рекомендации. Москва, 2017. 91 с.
7. Шамсиев А.М., Юсупов Ш.А. Рязанцев В.А., и др. Особенности предоперационной подготовки детей с распространенными формами аппендикулярного перитонита // Российский вестник детской хирургии, анестезиологии и реаниматологии. 2013. Т. 3, № 1.С. 88-92. EDN: PZVTVD
8. Сатаев В.У., Миронов П.И., Мамлеев И.В., Гумеров А.А. Роль эндовидеохирургических плановых вмешательств в исходах абдоминального сепсиса у детей // Российский вестник детской хирургии, анестезиологии и реаниматологии. 2013. Т. 3, № 1. С. 22-27. EDN: PZVTQN
9. Соколов Ю.Ю., Коровин С.А., Недумов Ю.Н., и др. Эффективность лапароскопии у детей с острым аппендицитом и перитонитом // Детская больница. 2013. № 2. С. 29-33. EDN: SDYLRL
10. Соколов Ю.Ю., Коровин С.А., Дзядчик А.В. Лапароскопия у детей с острой ишемией органов брюшной полости // Ученые записки Орловского государственного университета. Серия: Естественные, технические и медицинские науки. 2014. Т. 2, № 7. С. 110-111. EDN: VEIQKF
11. Коровин С.А., Дзядчик А.В., Акопян М.К., Соколов Ю.Ю. Персонифицированные подходы хирургического лечения детей с гнойновоспалительными заболеваниями органов брюшной полости // Детская хирургия. 2020. Т. 24, № S1. С. 46. EDN: HBEREM
12. Багненко С.Ф., Байбарина Е.Н., Белобородов В.Б., и др. Сепсис: классификация, клинико-диагностическая концепция и лечение. 4-е изд., доп. и перераб. Москва: МИА-Мед, 2017. 408 с.
13. Gurlich R., Adamkova V., Ulrych J., et al. [Basic principles of diagnosis and treatment of secondary peritonitis-recommendations of experts with the support of SIS. (In Czech)] H Rozhl Chir. 2014. Vol. 93, N 6. P. 334-348.
14. Гельфанд Б.Р., Кириенко А.И., Хачатрян H.H. Абдоминальная хирургическая инфекция. Российские национальные рекомендации. Москва: Медицинское информационное агентство, 2018. 168 с.
15. Gurlich R. et al. Basic principles of diagnosis and treatment of secondary peritonitis-recommendations of experts with the support of SIS II Rozhledy v Chirurgii: Mesicnik Ceskoslovenske Chirurgicke Spolecnosti. 2014. Vol. 93, №. 6. P. 334-348.
16. Kim J., Kim Y.J., Ryoo S.M., et al. Risk factors for same pathogen sepsis readmission following hospitalization for septic shock // J Clin Med. 2019. Vol. 8, N 2. P. 181.
17. Петлах В.И., Липатов B.A., Елецкая E.C., Сергеев А.В. Морфология формирования послеоперационных брюшинных спаек // Детская хирургия. 2014. Т. 18, № 1. С. 42-46. EDN: RVNDWD
18. Магомедов М.М., Иманалиев М.Р., Магомедов М.А. Послеоперационные спайки брюшной полости: патофизиология и профилактика (обзор литературы) // Современная наука: актуальные проблемы теории и практики. Серия: Естественные и технические науки. 2020. № 8-2. С. 73-80. EDN: PZYFGL
19. Лазарев В.В., Анчутин П.Е. Влияние сукцинатов на воспалительную реакцию: обзор литературы // Вестник интенсивной терапии им. А.И. Салтанова. 2023. № 3. С. 155-165. EDN: IVCGIF
20. Завьялкин В.А., Барская М.А., Алкурди А.М., и др. Программа для выбора алгоритма оперативной тактики при распространенном перитоните у детей в зависимости от внутрибрюшного давления. Свидетельство о государственной регистрации № 2023619650 от 15.05.2023. Реестр свидетельств на программы для ЭВМ ФГБОУ ВО СамГМУ Минздрава России, 2023.
21. Савельев В.С., Гельфанд Б.Р., Филимонов М.И., и др. Оценка тяжести поражения органов брюшной полости при перитоните // Инфекции в хирургии. 2013. Т. 11, № 2. С. 5-9.
22. Александрович Ю.С., Пшениснов К.В. Предоперационная подготовка к анестезии у детей // Вестник анестезиологии и реаниматологии. 2020. Т. 17, № 3. С. 79-94. EDN: QZNFOB
23. Бабаев Б.Д., Соколов Ю.Ю., Смирнов Г.В., и др. Внутрибрюшная гипертензия у детей в периоперационном периоде при операциях на брюшной полости // РМЖ. 2022. № 5. С. 46-48. EDN: URWYKK
24. Морозов Д.А., Морозова О.Л., Клюев С.А., и др. Синдром интраабдоминальной гипертензии у детей // Новости хирургии. 2017. Т. 25, № 6. С. 621-631. EDN: ZSVXFR
References
1. Stets VV, Polovnikov SG, Zhuravlev AG, Shestopalov AE. Nutritional and metabolic correction in the intensive therapy of peritonitis. Wounds Wound Infections prof. B.M. Kostyuchenok J. 2016:3(1):25-31. EDN: WMZLCH
2. Schegolev AA, Tovmasyan S, Chevokin AY, et al. Tertiary peritonitis: State of the problem and possible perspectives. Lechebnoe delo. 2018:(4):32-35. EDN: YYSJBB
3. Coral LE, Ceron LN, Delgado Al. [Peritonitis treated by laparoscopy as an effective treatment. (In Spanish)]. Rev Gastroenterol Peru. 2018:38(3):261-264.
4. Isakov YF, Dronov AF. Paediatric surgery. National manual. Moscow: GEOTAR-Media; 2009.1168 p. (In Russ).
5. Razumovsky AY. Paediatric surgery. National guide. 2nd ed., revised and updated. Moscow: GEOTAR-Media; 2021. 1280 p. (In Russ).
6. Grigoriev G, Sovtsov SA, Krivtsov GA. Acute peritonitis. Clinical recommendations. Moscow; 2017. 91 p. (In Russ).
7. Shamsiev AM, Yusupov S, Ryazantsev VA, et al. The features of preoperational preparation of children with diffuse types of appendicular peritonitis. Russ J Pediatric Surg Anesthesia Intensive Care. 2013:3(1):88-92. EDN: PZVTVD
8. Sataev VU, Mironov PI, Mamleev IA, Gumerov AA. Role of planned interventions assisted surgery in the outcome of abdominal sepsis in children. Russ J Pediatric Surg Anesthesia Intensive Care. 2013:3(1):22-27. EDN: PZVTQN
9. Sokolov Yu, Korovin SA, Nedumov YN, et al. Laparoscopy efficacy in the children with acute appendicitis and peritonitis. Detskaya bolnitsa. 2013:(2):29-33. EDN: SDYLRL
10. Sokolov YY, Korovin SA, Dzyadchik AV. Laparoscopy in children with acute ischemia of abdominal organs. Scientific Notes Orel State University. 2014;2(7):110-111. EDN: VEIQKF
11. Korovin SA, Dziadchik AV, Akopyan MK, Sokolov YY. Personalised approaches to surgical treatment of children with purulent-inflammatory diseases of abdominal cavity organs. Detskaya khirurgiya (Russian Journal of Pediatric Surgery). 2020;24(S1):46. EDN:HBEREM
12. Bagnenko SF, Baibarina EN, Beloborodov VB, et al. Sepsis: Classification, clinical and diagnostic concept and treatment. 4th ed., revised and updated. Moscow: MIA-Med; 2017. 408 p. (In Russ).
13. Gurlich R, Adamkova V, Ulrych J, et al. [Basic principles of diagnosis and treatment of secondary peritonitis-recommendations of experts with the support of SIS. (In Czech)]. Rozhl Chir. 2014:93(6):334-348.
14. Gelfand BR, Kirienko Al, Khachatryan NN. Abdominal surgical infection. Russian notional recommendations. Moscow: Meditsinskoe informatsionnoe agentstvo; 2018. 168 p.
15. Gurlich R. et al. Basic principles of diagnosis and treatment of secondary peritonitis-recommendations of experts with the support of SIS. Rozhledy v Chirurgii: Mesicnik Ceskoslovenske Chirurgicke Spolecnosti. 2014;93(6):334-48.
16. Kim J, Kim YJ, Ryoo SM, et al. Risk factors for same pathogen sepsis readmission following hospitalization for septic shock. J Clin Med. 2019:8(2):181.
17. Petlakh VI, Lipatov VA, Eletskaya ES, Sergeev AV. Morphology of postoperative abdominal adhesions. Betskaya khirurgiya (Russian Journal of Pediatric Surgery). 2014:18(1):42-46. EDN: RVNDWD
18. Magomedov MM, Imanaliev MR, Magomedov MA. Postoperative abdominal adhesion: Pathophysiology and prevention (review). Modern Science: Actual Problems Theory Practice. 2020:(8-2):73-80. EDN: PZYFGL
19. Lazarev W, Anchutin PE. Effects of succinates on the inflammatory response: A review. Alexander Saltanov intensive care herald. 2023; (3):155-165. EDN: IVCGIF
20. Zavyalkin VA, Barskaya MA, Alkurdi AM, et al. A programme for selecting an algorithm of operative tactics in common peritonitis in children depending on intra-abdominal pressure. Certificate of state registration N 2023619650 from 15.05.2023. Register of certificates for computer programmes of Samara State Medical University; 2023. (In Russ).
21. Savelyev VS, Gelfand BR, Filimonov Ml, et al. Assessment of the severity of abdominal damage in peritonitis. Infections in surgery. 2013:11(2): 5-9.
22. Aleksandrovich YS, Pshenisnov KV. Pre-operative preparation to anesthesia in children. Messenger Anesthesiol Resuscitation. 2020:17(3):79-94. EDN: QZNFOB
23. Babaev BD, Sokolov YY, Smirnov GV, et al. Intraabdominal hypertension in the perioperative period during abdominal surgery in children. Russkii meditsinskii zhurnal. 2022;(5):46-48. EDN: URWYKK
24. Morozov DA, Morozova OL, Klyuev SA, et al. Intra-abdominal hypertension syndrome in children. Novosti hirurgii. 2017:25(6):621 -631. EDN: ZSVXFR
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)